文档内容
绝密★启用前
2025 年高考考前信息必刷卷 01(河南专用)
化 学
考情速递
高考·新动向:单选题由7个转变为14个,非选择题为4道大题,覆盖了工业流程、实验题、反应原理
的应用以及有机化学等知识
高考·新考法:通过对常规考点的新设问或知识融合,加强对探究性实验的考查等
高考·新情境:在试题的情境导入中,更多结合生活(非物质文化遗产、具有抗癌活性的分子等)、生
产、科技(离子液体、应用于新能源汽车的二次电池)等实际情境,考查学生在真是情境中应用化学
知识的能力等
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 Li-7 O-16 Fe-56
第I卷(选择题)
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.我国有很多非物质文化遗产,下列制作技艺的代表作的主要材料不属于有机物的是
A.傣族剪纸 B.云南斑铜
C.哈尼族牛角号 D.苗族芦笙
2.下列有关化学用语的表述正确的是
A.中子数为10的氧原子: B.氯离子的结构示意图:C. 为碳原子的一种激发态 D.四氟肼 的电子式:
3.一种名贵宝石的主要成分是由原子序数依次增大的短周期主族元素X、Y、Z、W组成,其中X、Z为
金属元素,X的质子数等于W的最外层电子数,Y、W的最外层电子数之和是X、Z最外层电子数之和
的2倍,Y单质是空气的主要成分之一,下列有关说法正确的是
A.X的氢氧化物易溶于水
B.X、Z位于同一主族
C.X、W的氯化物中各原子均为8电子稳定结构
D.Y、Z的第一电离能均小于同周期相邻两种元素
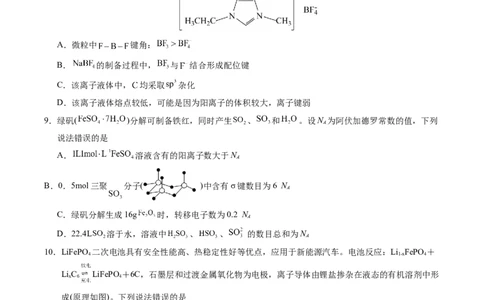
4.下列实验操作正确且能达到相应实验目的的是
A.收集 气体 B.量取8.00mL饱和食盐水 C.钠的燃烧 D.灼烧干燥海带
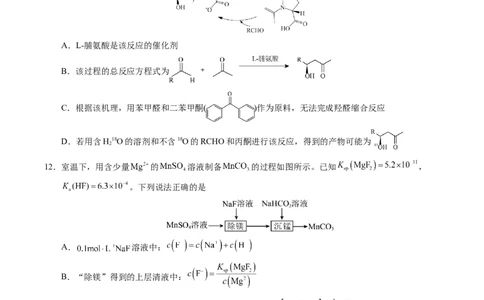
5.白藜芦醇具有强的抗癌活性,其分子结构如下图所示,下列说法不正确的是
A.和过量浓溴水反应,产物的分子式为
B.白藜芦醇存在顺反异构
C.白藜芦醇分子中不含手性碳原子
D.1mol白藜芦醇可以和3mol NaOH反应
6.取一定体积的两种试剂进行反应,改变两种试剂的滴加顺序(试剂浓度均为 ),反应现象没有
明显差别的是
选项 试剂① 试剂②
A 氨水 溶液
B 溶液 溶液
C 溶液 酸性 溶液
D 溶液 溶液
7.下列离子方程式书写正确的是A.向 溶液中通入少量 :
B.向草酸钠(Na C O)溶液中加入酸性高锰酸钾溶液:5C O +16H++2MnO =2Mn2++10CO ↑+8H O
2 2 4 2 2 2
C.过量 通入 溶液中:
D. 和 溶液反应至溶液恰好呈中性:
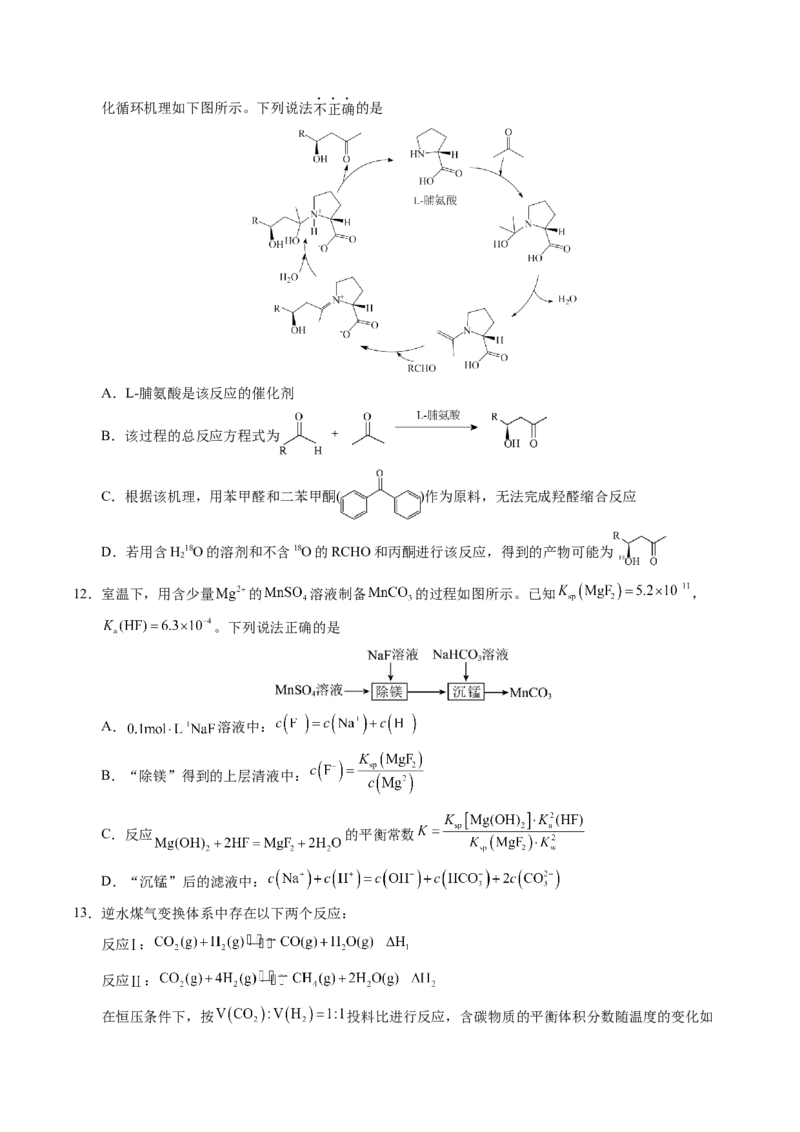
8.离子液体具有电导率高、化学稳定性好等优点,在电化学领域用途广泛。由 与 反应制得的
是制备某离子液体的原料,该离子液体的结构简式如下。下列说法不正确的是
A.微粒中 键角:
B. 的制备过程中, 与 结合形成配位键
C.该离子液体中, 均采取 杂化
D.该离子液体熔点较低,可能是因为阳离子的体积较大,离子键弱
9.绿矾( )分解可制备铁红,同时产生 、 和 。设N 为阿伏加德罗常数的值,下列
A
说法错误的是
A. 溶液含有的阳离子数大于N
A
B.0.5mol三聚 分子( )中含有σ键数目为6 N
A
C.绿矾分解生成16g 时,转移电子数为0.2 N
A
D.22.4L 溶于水,溶液中 、 、 的数目总和为N
A
10.LiFePO 二次电池具有安全性能高、热稳定性好等优点,应用于新能源汽车。电池反应:Li FePO +
4 1-x 4
LiC LiFePO +6C,石墨层和过渡金属氧化物为电极,离子导体由锂盐掺杂在液态的有机溶剂中形
x 6 4
成(原理如图)。下列说法错误的是
A.放电时,电流由石墨层经外电路流向过渡金属氧化物
B.放电时,正极电极反应式:Li FePO +xLi++xe-=LiFePO
1-x 4 4
C.充电时,阴极电极反应式:xLi++6C+xe-=Li C
x 6
D.充电时,Li+向石墨层电极移动,若电路中通过1 mol 电子,质量增加7 g
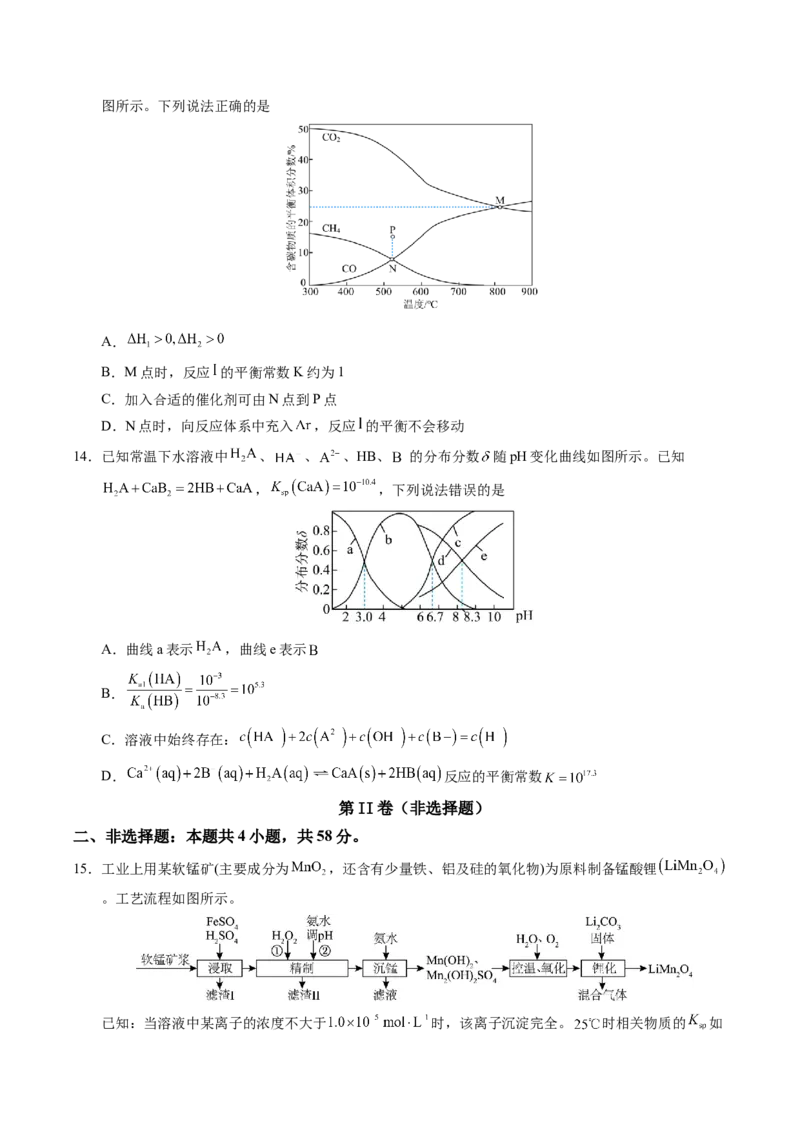
11.诺贝尔化学奖授予了对有机小分子不对称催化作出重大贡献的科学家,其研究成果羟醛缩合反应的催化循环机理如下图所示。下列说法不正确的是
A.L-脯氨酸是该反应的催化剂
B.该过程的总反应方程式为
C.根据该机理,用苯甲醛和二苯甲酮( )作为原料,无法完成羟醛缩合反应
D.若用含H18O的溶剂和不含18O的RCHO和丙酮进行该反应,得到的产物可能为
2
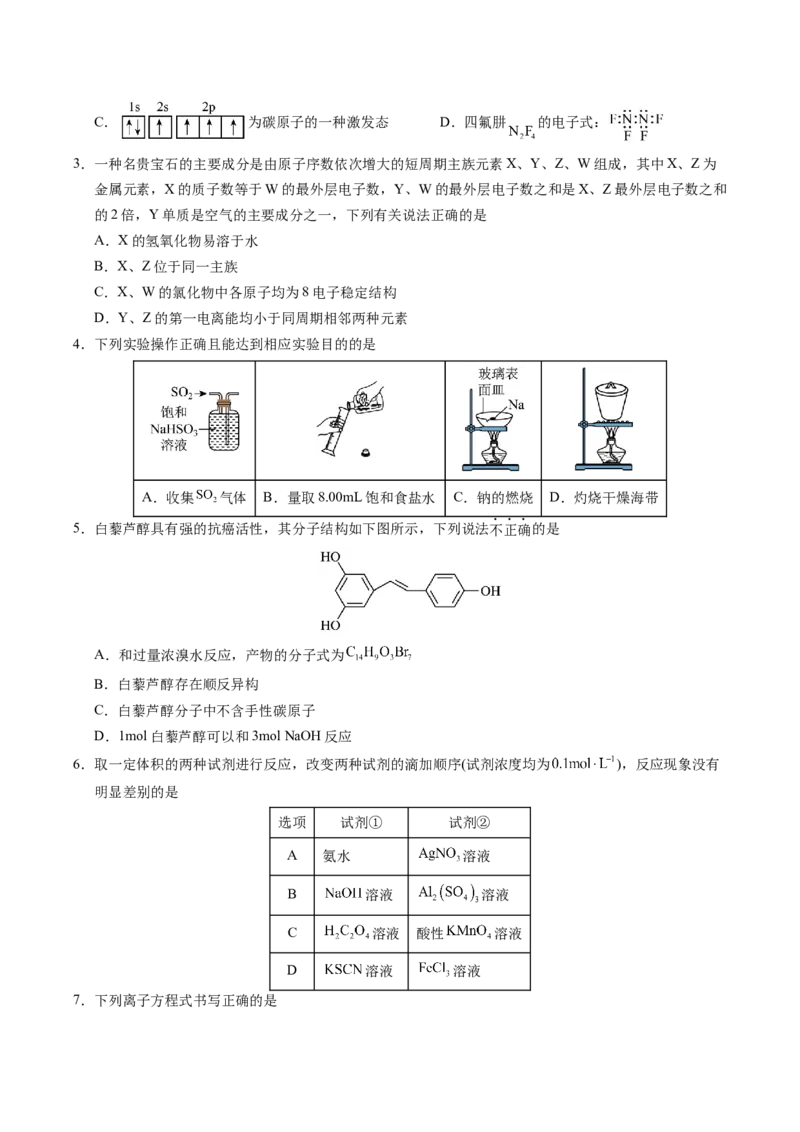
12.室温下,用含少量 的 溶液制备 的过程如图所示。已知 ,
。下列说法正确的是
A. 溶液中:
B.“除镁”得到的上层清液中:
C.反应 的平衡常数
D.“沉锰”后的滤液中:
13.逆水煤气变换体系中存在以下两个反应:
反应 :
反应 :
在恒压条件下,按 投料比进行反应,含碳物质的平衡体积分数随温度的变化如图所示。下列说法正确的是
A.
B.M点时,反应 的平衡常数K约为1
C.加入合适的催化剂可由N点到P点
D.N点时,向反应体系中充入 ,反应 的平衡不会移动
14.已知常温下水溶液中 、 、 、HB、 的分布分数 随pH变化曲线如图所示。已知
, ,下列说法错误的是
A.曲线a表示 ,曲线e表示
B.
C.溶液中始终存在:
D. 反应的平衡常数
第II卷(非选择题)
二、非选择题:本题共4小题,共58分。
15.工业上用某软锰矿(主要成分为 ,还含有少量铁、铝及硅的氧化物)为原料制备锰酸锂
。工艺流程如图所示。
已知:当溶液中某离子的浓度不大于 时,该离子沉淀完全。 时相关物质的 如表所示。
物质
回答下列问题:
(1)基态锰原子核外电子排布式为 。
(2)滤渣Ⅰ的主要成分是 ,其晶体类型为 。
(3)“浸取”时, 反应的离子方程式为 。
(4)“精制”时, 加入的量应大于理论值,原因是 。
(5)若“浸取”后溶液中 ,则“精制”时应调 的范围为 [计算时
只考虑生成 沉淀],滤渣Ⅱ的主要成分是 (写化学式)。
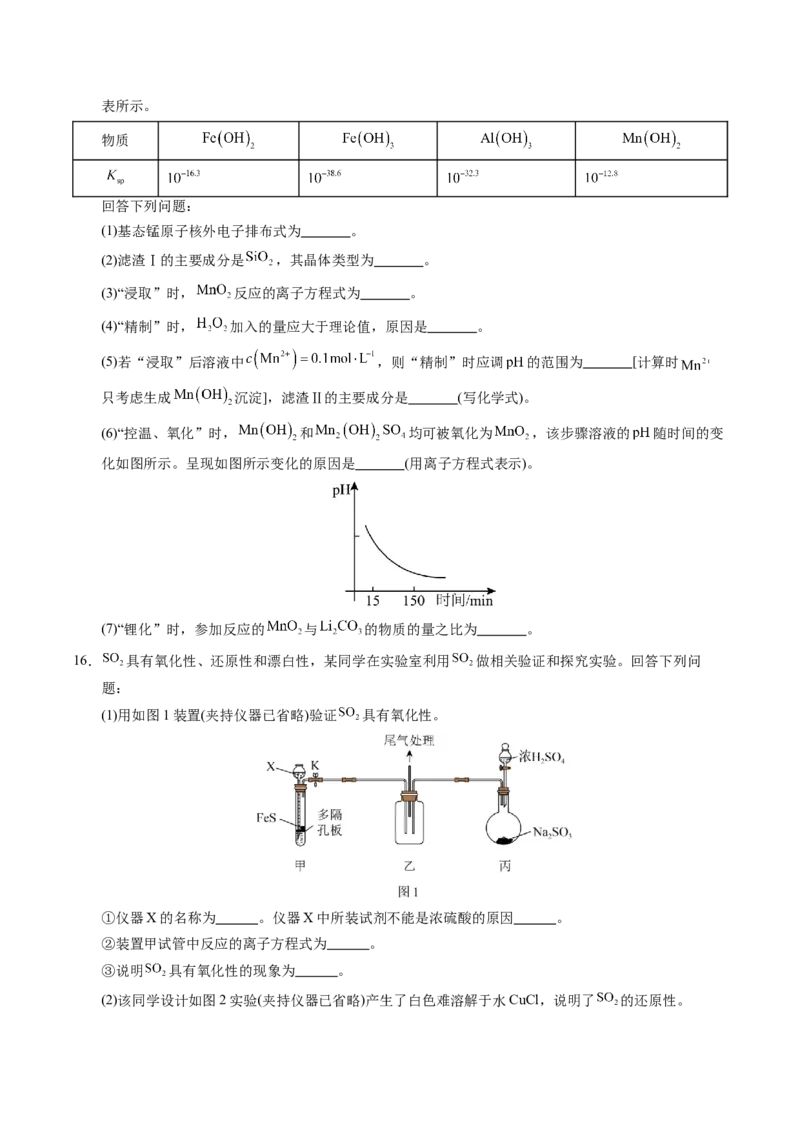
(6)“控温、氧化”时, 和 均可被氧化为 ,该步骤溶液的 随时间的变
化如图所示。呈现如图所示变化的原因是 (用离子方程式表示)。
(7)“锂化”时,参加反应的 与 的物质的量之比为 。
16. 具有氧化性、还原性和漂白性,某同学在实验室利用 做相关验证和探究实验。回答下列问
题:
(1)用如图1装置(夹持仪器已省略)验证 具有氧化性。
①仪器X的名称为 。仪器X中所装试剂不能是浓硫酸的原因 。
②装置甲试管中反应的离子方程式为 。
③说明 具有氧化性的现象为 。
(2)该同学设计如图2实验(夹持仪器已省略)产生了白色难溶解于水CuCl,说明了 的还原性。①仪器a的作用是 。
②三颈烧瓶中反应的化学方程式为 。
③从元素化合价变化的角度说明该反应 有还原性的原因 。
(3)实验表明,将纯净的 缓缓地通入到1.00mol/L 溶液中,得到 沉淀。为了探究该
反应中的氧化剂,该同学提出以下假设:
假设Ⅰ:溶液中的 ;
假设Ⅱ:溶解在水中的氧气。
①验证假设Ⅰ(配制溶液前已将蒸馏水煮沸并密封冷却)。
实验步骤 实验操作 实验现象 结论
实验ⅰ 向______溶液中缓慢通入纯净的 气体 无白色沉淀
假设Ⅰ成立
实验ⅱ 向1.00mol/L 溶液的烧杯中缓慢通入纯净的 气体
实验ⅰ的溶液 ,实验Ⅱ的现象为 。
②验证假设Ⅱ.请完成下列表格:
实验步骤 实验现象 实验目的
实验ⅲ 同实验ⅰ步骤 同实验ⅰ的相关现象 作对照实验
实验ⅳ 产生白色沉淀
实验ⅳ的步骤为 ,实验目的是 。
17.氨是重要化工原料,其工业合成原理为 。回答下列问题:
(1)已知:ⅰ. ;
ⅱ. (a、b都大于0)。
则反应 的 (用含a、b的代数式表示),利于该反应正向
进行的条件为 (填“低温”“高温”或“任意温度”)。
(2)向恒温恒容密闭容器中充入体积比 的 和 ,发生反应 。下列情
况表明该反应一定达到平衡状态的是___________(填字母,下同)。
A.气体密度不随时间变化 B.气体平均摩尔质量不随时间变化C.气体总压强不随时间变化 D. 体积分数不随时间变化
(3)下列关于 的叙述正确的是 。
A. 生成速率等于 消耗速率的2倍
B.若加入高效催化剂,平衡常数和反应热都会增大
C.若起始按体积比 投入 和 ,则 和 的转化率相等
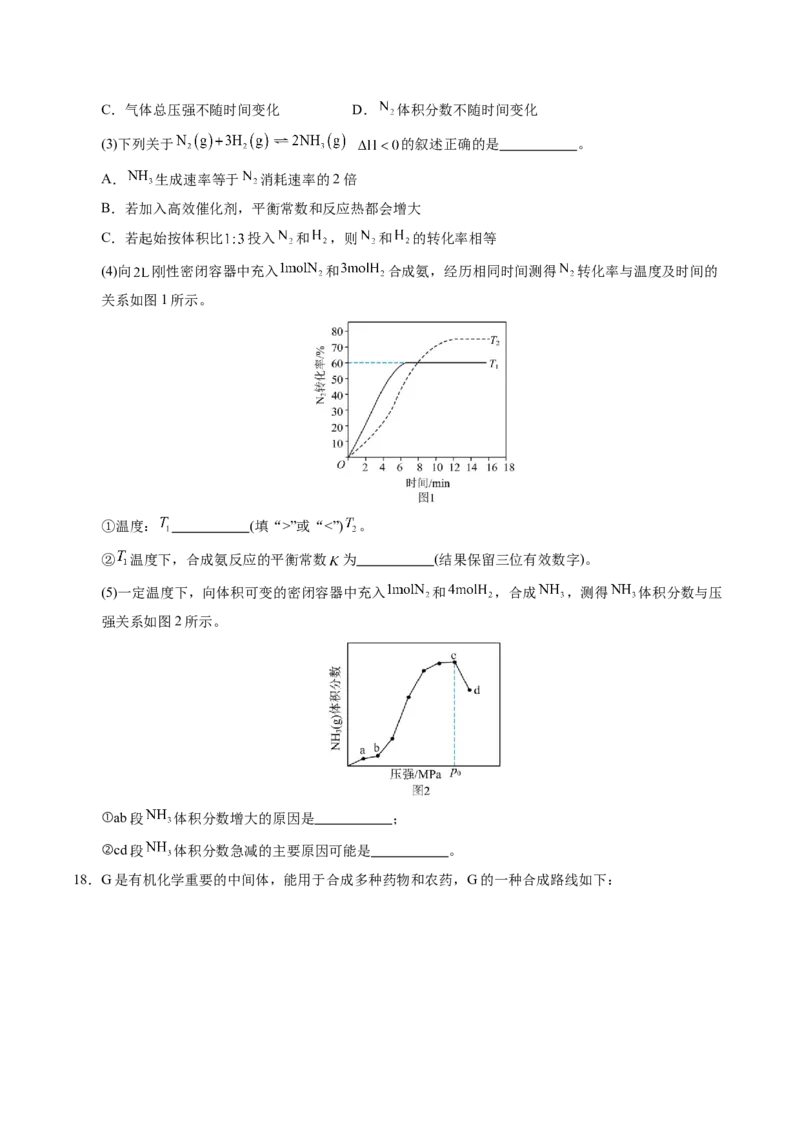
(4)向 刚性密闭容器中充入 和 合成氨,经历相同时间测得 转化率与温度及时间的
关系如图1所示。
①温度: (填“>”或“<”) 。
② 温度下,合成氨反应的平衡常数 为 (结果保留三位有效数字)。
(5)一定温度下,向体积可变的密闭容器中充入 和 ,合成 ,测得 体积分数与压
强关系如图2所示。
①ab段 体积分数增大的原因是 ;
②cd段 体积分数急减的主要原因可能是 。
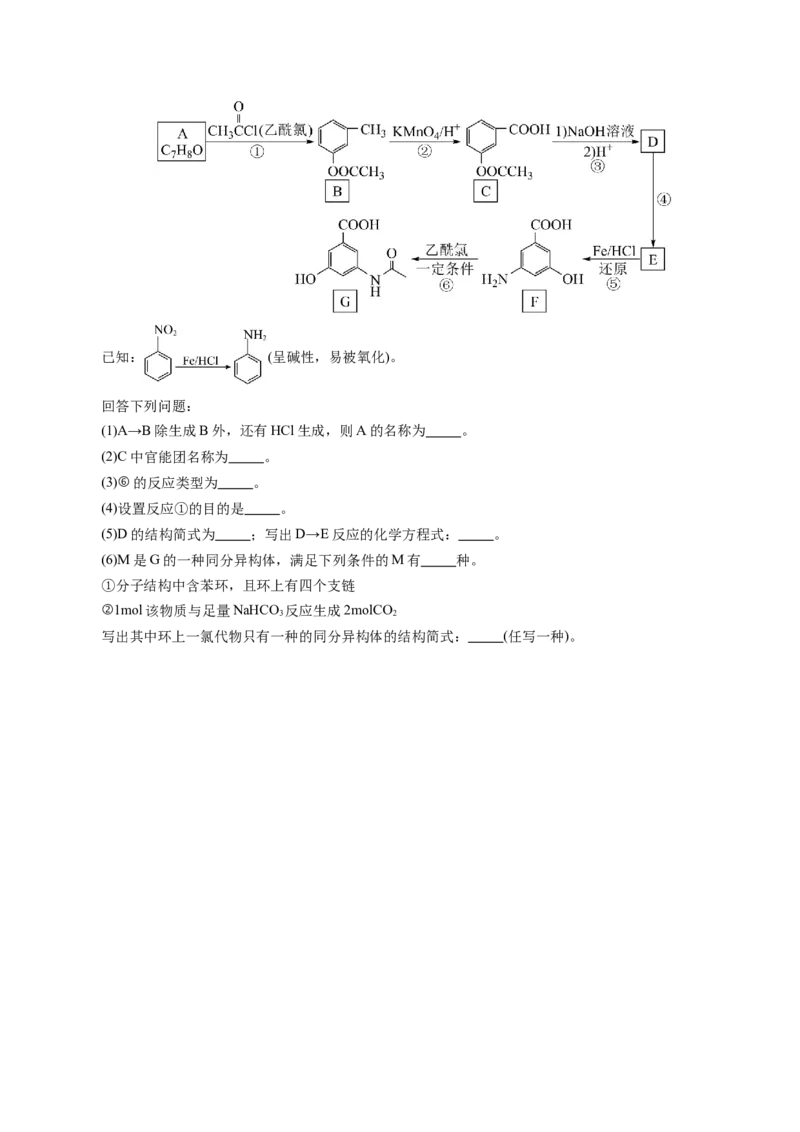
18.G是有机化学重要的中间体,能用于合成多种药物和农药,G的一种合成路线如下:已知: (呈碱性,易被氧化)。
回答下列问题:
(1)A→B除生成B外,还有HCl生成,则A的名称为 。
(2)C中官能团名称为 。
(3)⑥的反应类型为 。
(4)设置反应①的目的是 。
(5)D的结构简式为 ;写出D→E反应的化学方程式: 。
(6)M是G的一种同分异构体,满足下列条件的M有 种。
①分子结构中含苯环,且环上有四个支链
②1mol该物质与足量NaHCO 反应生成2molCO
3 2
写出其中环上一氯代物只有一种的同分异构体的结构简式: (任写一种)。