文档内容
绝密★启用前
2025 年高考考前信息必刷卷 01(黑吉辽蒙专用)
化 学
考情速递
高考·新动向:2024年高考辽宁省自主命题,黑吉辽使用相同试卷;2025年吉林省将接手高考命题工作,
黑吉辽蒙使用相同试卷。2025年1月长春市东北师范大学附属中学(五校联考)化学科目考试能够体
现吉林省自主命题的模式,单项选择题本大题有15小题,每小题3分,共45分;非选择题本大题有4
小题,每小题13或14分,共55分。
高考·新考法:2025年高考化学题型考点覆盖更加全面,知识更加综合,学科融合体现更多,注重考察
各种物质在生产生活中的应用,对于考生能力的要求更高,更注重考察学生的学科素养。
高考·新情境:在试题的情境导入中,更加注重与风土人情的结合,基于身边熟悉的事物发现问题,提
出问题。学生需要对知识进行综合运用,而不仅仅是对化学知识的死记硬背,要求学生学以致用。
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 P 31 Ti 48
一、选择题:本题共15小题,每小题3分,共45分。每小题只有一个选项符合题目要求。
1.历史文物见证了中华民族共同体在发展中的交流交往交融,下列吉林省博物馆陈列的文物主要由天然
高分子化合物构成的是
A.《文姬归汉图》绢本设色画 B.北宋官窑贯耳瓶 C.契丹文八角铜镜 D.长白山出土的石叶石核
【答案】A
【详解】A.绢本设色画是画在绢丝上的彩色作品,原料蚕丝是天然高分子化合物,A正确;
B、北宋官窑贯耳瓶是瓷器,主要成分为硅酸盐,B错误;
C.契丹文八角铜镜是青铜器,青铜属于合金,C错误;D、石叶石核是一种黑曜岩石制品,富含二氧化硅(大约为35~80%),D错误;
答案选A。
2.下列有关化学用语表述正确的是
A.HO 电子式: B.顺式聚异戊二烯结构简式:
2 2
C.HCl中 共价键的电子云图: D.SO 的VSEPR模型:
3
【答案】C
【详解】A.过氧化氢是含有极性键和非极性键的共价化合物,电子式为 ,A错误;
B.顺式聚异戊二烯中亚甲基位于碳碳双键的同侧,结构简式为: ,B错误;
C.H 的 1s 电子和 Cl 原子的 3p 电子通过“头碰头”形成 H-Cl 键,H-Cl 键属于单键,为 σ 键,即
,C正确;
D.SO 的中心原子的价层电子对数为:3+ =3,VSEPR模型为平面三角形,SO 的VSEPR模型为:
3 3
,D错误;
故答案为:C。
3.“劳动最光荣,勤奋出智慧”。下列劳动项目与所述化学知识没有关联的是
选
劳动项目 化学知识
项
A 试剂运输:常用铁罐车运输浓硫酸 常温下,铁遇浓硫酸钝化
B 医学手术:医生用聚乳酸作手术缝合线 聚乳酸在人体内可水解、吸收
C 泳池消毒:用漂粉精作游泳池的消毒剂 漂粉精有漂白性
D 消防宣传:消防员使用泡沫灭火器灭火 碳酸氢钠与硫酸铝发生双水解
【答案】C
【详解】A.常温下,铁遇浓硫酸钝化,可防止内部的铁继续反应,因此可用铁罐车运输浓硫酸,故A正
确;
B.聚乳酸在人体内可水解,最终被吸收,因此常用聚乳酸作手术缝合线,故B正确;
C.漂粉精作游泳池的消毒剂是因其有强氧化性,能杀菌消毒,故C错误;D.泡沫灭火器原理是利用碳酸氢钠与硫酸铝发生完全双水解反应生成氢氧化铝和二氧化碳,故D正确;
故选:C。
4.下列化学用语对事实的表述正确的是
A.用碳酸钠溶液处理锅炉水垢:
B.用电子式表示氯化钠的形成过程:
C.氯化铁溶液腐蚀铜的电路板:
D.电解饱和食盐水阳极的电极反应:
【答案】B
【详解】A.用碳酸钠溶液处理锅炉水垢即将CaSO 微溶物转化为CaCO 沉淀,然后加入酸进行酸溶,反
4 3
应原理为: ,A错误;
B.NaCl为离子化合物,Na原子失电子、Cl原子得电子形成氯化钠,用电子式表示形成过程为
,B正确;
C.用FeCl 溶液腐蚀铜线路板的离子反应为Cu+2Fe3+=Cu2++2Fe2+,C错误;
3
D.碳棒作电极电解饱和食盐水,阳极发生氧化反应,氯离子被氧化生成氯气,阳极的电极反应式为
2Cl--2e- ═ Cl ↑,D错误;
2
故选B。
5.设 为阿伏加德罗常数的值。下列说法错误的是
A.6.2g白磷中含 键数目为0.3
B.常温下,pH=13的 溶液中,由水电离出的 数目为
C.标准状况下,2.24L 中含原子数目为0.5
D.已知葡萄糖可发生银镜反应,0.1mol葡萄糖完全反应可生成银原子的数目为0.2
【答案】B
【详解】A.白磷分子式为P,为正四面体结构,1个分子中含有6个 键,6.2g白磷中含 键数目为
4
,故A正确;
B.常温下,pH=13的 溶液中,c(H+)=10-13mol/L、c(OH-)=10-1mol/L,抑制水电离,所以由水电离
出的c(OH-)=10-13mol/L。但此题没有明确溶液体积,不能计算 的数目,故B错误;
C.标准状况下,2.24L 的物质的量为0.1mol,含原子数目为0.5 ,故C正确;
D.葡萄糖的结构简式为 ,1mol葡萄糖中含有1mol醛基,发生银镜反应产生2mol
银,0.1mol葡萄糖能生成银原子数目为0.2 ,故D正确;
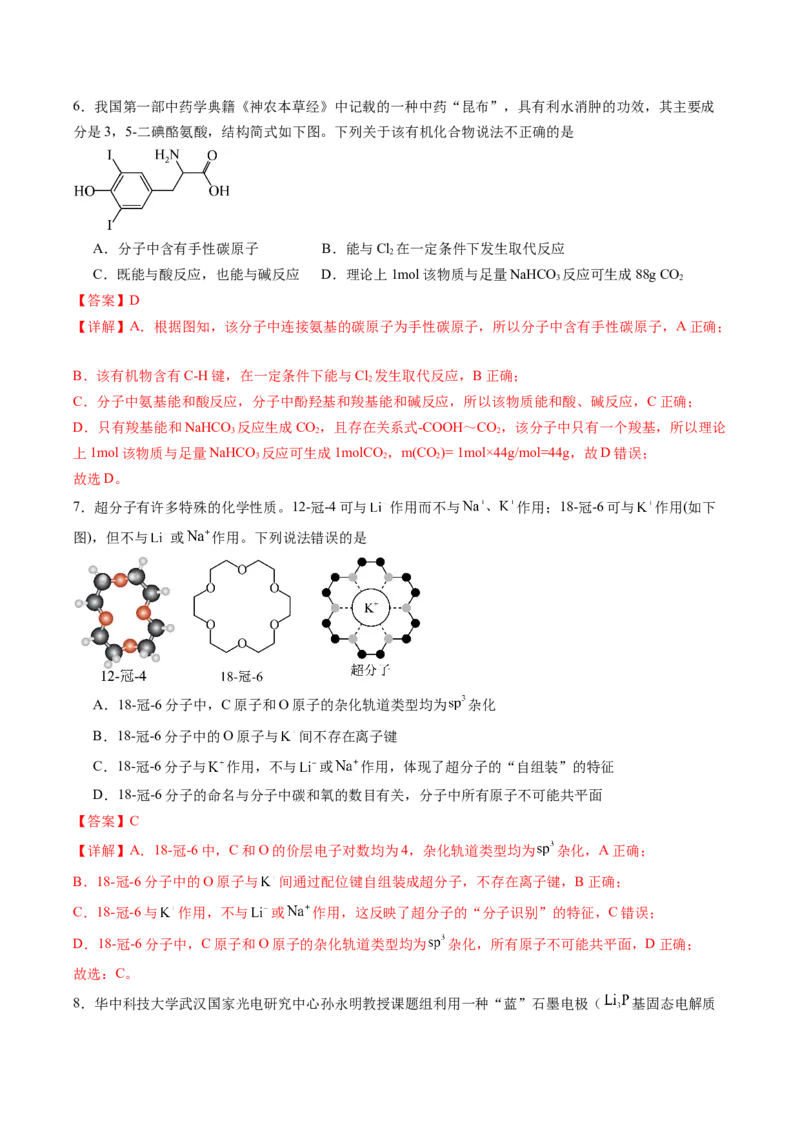
故选B。6.我国第一部中药学典籍《神农本草经》中记载的一种中药“昆布”,具有利水消肿的功效,其主要成
分是3,5-二碘酪氨酸,结构简式如下图。下列关于该有机化合物说法不正确的是
A.分子中含有手性碳原子 B.能与Cl 在一定条件下发生取代反应
2
C.既能与酸反应,也能与碱反应 D.理论上1mol该物质与足量NaHCO 反应可生成88g CO
3 2
【答案】D
【详解】A.根据图知,该分子中连接氨基的碳原子为手性碳原子,所以分子中含有手性碳原子,A正确;
B.该有机物含有C-H键,在一定条件下能与Cl 发生取代反应,B正确;
2
C.分子中氨基能和酸反应,分子中酚羟基和羧基能和碱反应,所以该物质能和酸、碱反应,C正确;
D.只有羧基能和NaHCO 反应生成CO,且存在关系式-COOH~CO,该分子中只有一个羧基,所以理论
3 2 2
上1mol该物质与足量NaHCO 反应可生成1molCO ,m(CO )= 1mol×44g/mol=44g,故D错误;
3 2 2
故选D。
7.超分子有许多特殊的化学性质。12-冠-4可与 作用而不与 作用;18-冠-6可与 作用(如下
图),但不与 或 作用。下列说法错误的是
A.18-冠-6分子中,C原子和O原子的杂化轨道类型均为 杂化
B.18-冠-6分子中的O原子与 间不存在离子键
C.18-冠-6分子与 作用,不与 或 作用,体现了超分子的“自组装”的特征
D.18-冠-6分子的命名与分子中碳和氧的数目有关,分子中所有原子不可能共平面
【答案】C
【详解】A.18-冠-6中,C和O的价层电子对数均为4,杂化轨道类型均为 杂化,A正确;
B.18-冠-6分子中的O原子与 间通过配位键自组装成超分子,不存在离子键,B正确;
C.18-冠-6与 作用,不与 或 作用,这反映了超分子的“分子识别”的特征,C错误;
D.18-冠-6分子中,C原子和O原子的杂化轨道类型均为 杂化,所有原子不可能共平面,D正确;
故选:C。
8.华中科技大学武汉国家光电研究中心孙永明教授课题组利用一种“蓝”石墨电极( 基固态电解质界面膜),实现了锂离子电池的极速充电和长循环寿命,工作原理如下图所示。下列说法正确的是
A.充电时, 通过固态电解质向N极移动
B.放电时,M极的电极电势比N极高
C.充电时,M极发生的电极反应为
D.当电路中通过 电子时,理论上两电极的质量变化差为
【答案】C
【分析】由图可知,N充电由LiNi Co Mn O→Li Ni Co Mn O,Li+数减少,失电子,发生氧化反应
0.6 0.2 0.2 2 1-x 0.6 0.2 0.2 2
为阳极,放电为正极,M为负极或阴极。
【详解】A.充电时,Li+向阴极(M极)移动,A错误;
B.放电时,正极电极电势高,M极的电极电势比N极低,B错误;
C.充电时,阴极电极反应式为 ,C正确;
D.当电路中通过1 mol电子时,发生反应的Li+为1mol,理论上两电极的质量变化差为14 g(正负两极质量
一增一减),D错误;
答案选C。
9.海洋植物如海带、海藻中含有丰富的碘元素。从海带中提取碘单质的工艺流程如下,下列说法不正确
的是
干海带 海带灰 悬浊液 滤液 碘水 I 的有机溶液―→粗碘
2
A.过程①需要用到蒸发皿 B.过程②中发生氧化还原反应
C.过程③的操作为萃取分液 D.粗碘可通过升华进行纯化
【答案】A
【详解】A.过程①为灼烧干海带,应在坩埚中进行,A错误;
B.过程②是将I-转化为I,发生氧化还原反应,B正确;
2
C.过程③是利用碘单质在有机溶剂中溶解度大于在水中的溶解度,从碘水中提取碘,为萃取分液,C正
确;
D.碘易升华,粗碘可通过升华进行纯化,D正确;
故选A。
10.一种由短周期主族元素组成的化合物(结构如图)是有机工业中良好的溶剂,其中W、X、Y、Z、M的
原子序数依次增大,五种元素的核外电子总数为33.下列叙述正确的是A.W与Z能形成非极性分子 B.第一电离能:
C.M与Z形成的化合物中只含离子键 D.该化合物既能溶于水又能溶于有机溶剂
【答案】D
【分析】W、X、Y、Z、M均为短周期主族元素,且原子序数依次增大,由化合物的结构图可知,W形成
一个键,且原子序数最小,W为H元素,X形成4个共价键,为C元素,Y形成3个共价键,则为N元素,
Z得到1个电子后形成1个键,Z为O元素,M形成+1价的M+离子,则为Na元素,将五种元素的核外电
子总数相加等于33,推断正确。
【详解】A.W与Z能形成 ,均为极性分子,A项错误;
B.同周期元素,从左到右第一电离能呈增大趋势,N原子2p轨道半充满稳定,第一电离能大于O,则第
一电离能: ,B项错误;
C.M与Z形成的化合物可以是NaO, 中含有非极性键,C项错误;
2 2
D.该化合物是含有钠离子的化合物,可以溶于水,同时又是有机工业中良好的溶剂,又能溶于有机溶剂,
D项正确;
答案选D。
11.室温下,根据下列实验过程及现象,能验证相应实验结论的是
选项 实验过程及现象 实验结论
将等浓度等体积的 溶液与 溶液混合有 二者水解相互促进生成氢氧化铝
A
沉淀
白色沉淀生成
将 固体加入饱和 溶液中,充分搅拌后过滤,在
B
滤渣中加稀盐酸,有气泡产生
取少量 样品溶于水,加入 溶液,再加入足
C 无法判断原样品是否变质
量盐酸,产生白色沉淀
将新制饱和氯水慢慢滴入含酚酞的稀NaOH溶液中,溶液红色
D HClO具有漂白性
褪去
【答案】C
【详解】A.将等浓度等体积的 溶液与 溶液混合发生反应
,不是水解反应,故A错误;
B.将 固体加入饱和 溶液中,增大碳酸根离子浓度, 硫酸钡转化为碳酸钡,不能证明 ,故B错误;
C.取少量 样品溶于水,加入 溶液,再加入足量盐酸,酸性条件下硝酸根离子能把
氧化为 ,产生白色沉淀硫酸钡,不能判断原样品是否变质,故C正确;
D.新制氯水中含有盐酸和次氯酸,盐酸、次氯酸能中和氢氧化钠,将新制饱和氯水慢慢滴入含酚酞的稀
NaOH溶液中,溶液红色褪去,可能是盐酸、次氯酸和氢氧化钠发生中和反应,不能证明HClO具有漂白
性,故D错误;
故选C。
12.温度为 时,在容积为 的恒容密闭容器充入一定量的 和 ,发生反应
。反应过程中的部分数据如表,下列说法正确的是
0 5 10
6.0 4.0
3.0 1.0
A. 内,用M表示的平均反应速率为
B.该反应在第 时
C.当P、Q的物质的量之比保持不变时,可判断该反应达到平衡状态
D.若 时该反应的化学平衡常数为1.0,则
【答案】D
【分析】根据表格信息,可列三段式:
再结合10min时的数据可知温度为T 时,反应在5min时已达到平衡,在该温度下的平衡常数为:
1
,由此解答。
【详解】A.根据三段式可知,0-5 min内,用M表示的平均反应速率为
,A错误;
B.根据分析可知,反应在5min时达到平衡状态,故在第8 min时v逆=v正,B错误;
C.初始P、Q为0,变化量等于化学计量数之比,故根据反应方程式P、Q的化学计量数之比可知,二者
的物质的量之比始终保持不变,是个定值,不能判断该反应达到平衡状态,C错误;
D.该反应为吸热反应,升高温度,平衡正向进行,平衡常数增大,已知T 时该反应的化学平衡常数为
1
0.8,T 时该反应的化学平衡常数为1.0,故T>T,D正确;
2 2 1答案选D。
13.邻二氮菲能与Fe2+发生显色反应,生成橙红色螯合物,用于Fe2+检验,化学反应如下。下列说法正确
的是
A.邻二氮菲的核磁共振氢谱有6组吸收峰 B.元素的电负性:C>N> Fe
C.每个螯合物离子中含有2个配位键 D.用邻二氮菲检验Fe2+时,需要调节合适的酸碱性环境
【答案】D
【详解】A.邻二氮菲分子中含有4种不同位置的H原子,故核磁共振氢谱有4组吸收峰,A错误;
B.电负性越大,对键合电子的吸引力越大,同一周期从左至右,元素电负性逐渐增大,故元素的电负性
顺序:N> C > Fe,B错误;
C.根据题中结构可以看出每个螯合物离子中含有6个配位键,C错误;
D.溶液酸性太强时,邻二氮菲中的N优先与H+形成配位键而减弱与Fe2+的配位能力;溶液碱性太强时,
会生成Fe(OH) ,所以用邻二氮菲检验Fe2+时,需要调节合适的酸碱性环境,D正确;
2
答案选D。
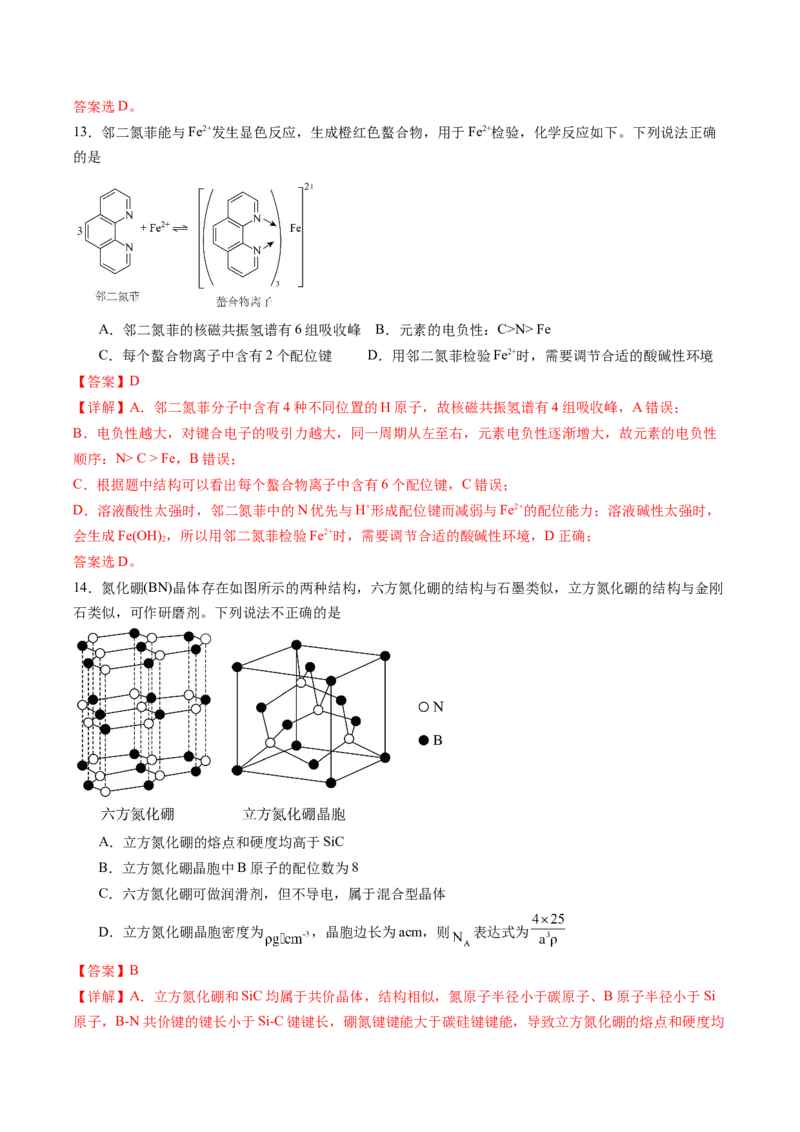
14.氮化硼(BN)晶体存在如图所示的两种结构,六方氮化硼的结构与石墨类似,立方氮化硼的结构与金刚
石类似,可作研磨剂。下列说法不正确的是
A.立方氮化硼的熔点和硬度均高于SiC
B.立方氮化硼晶胞中B原子的配位数为8
C.六方氮化硼可做润滑剂,但不导电,属于混合型晶体
D.立方氮化硼晶胞密度为 ,晶胞边长为acm,则 表达式为
【答案】B
【详解】A.立方氮化硼和SiC均属于共价晶体,结构相似,氮原子半径小于碳原子、B原子半径小于Si
原子,B-N共价键的键长小于Si-C键键长,硼氮键键能大于碳硅键键能,导致立方氮化硼的熔点和硬度均高于SiC,A正确;
B.立方氮化硼晶胞中N原子处于B构成的四面体中,N的配位数为4,由化学式BN可知,B的配位数为
4,B错误;
C.六方氮化硼的结构与石墨类似,可做润滑剂,不存在大π键电子,不导电,层内B和N以共价键结合,
具有共价晶体的特征,层间存在分子间作用力,属于混合型晶体,C正确;
D.据“均摊法”,晶胞中含 个B、4个N,则晶体密度为
,则 表达式为 ,D正确;
故选B。
15.常温下,pH均为2、体积均为 的 、 、 溶液,分别加水稀释至体积为V,溶液pH随
的变化关系如下图所示,下列叙述正确的是
A.当 时,水的电离程度:a点>c点
B.HB为强酸,且
C.当 时,升高溶液的温度,b点的 增大
D.中和体积、浓度均相同的NaOH溶液,三种酸中HA用量最少,生成的盐溶液碱性最弱
【答案】C
【详解】A.酸溶液对水的电离起抑制作用,a点酸性强,对水的电离抑制作用大,则水的电离程度:a点
点,故A错误;
B.稀释100倍时,pH由2变为4的酸为强酸,pH由2变为小于4的酸为弱酸,根据图知,HA为强酸,
、 为弱酸,pH变化越小的酸酸性越弱,则酸性: ,B错误。
C.HC为弱酸,升高温度,促进弱酸电离, 增大,故C正确;
D.pH均为2、体积均为 的三种酸的浓度: ,中和相同体积、相同浓度的NaOH
溶液消耗酸体积与酸浓度成反比,所以HA消耗体积大;HA为强酸,NaA溶液呈中性,故D错误;
故选C。二、非选择题:本题共4小题,共55分。
16.(13分)以钛铁矿(主要成分为钛酸亚铁下 )为主要原料制备钛白粉 常用硫酸法,工艺流
程如下:
(1)Ti的价电子轨道表示式为
(2)为提高“酸解”效率,可采取的措施有 (写一条即可);
(3)加入铁屑的目的是 。浸出还原后所得溶液中含有 和少量 等阳离子。已知常温下
为 ,若所得溶液中 的物质的量浓度为 ,当溶液的 时,
开始沉淀。
(4) 水解得到 ,则其水解方程式为 。
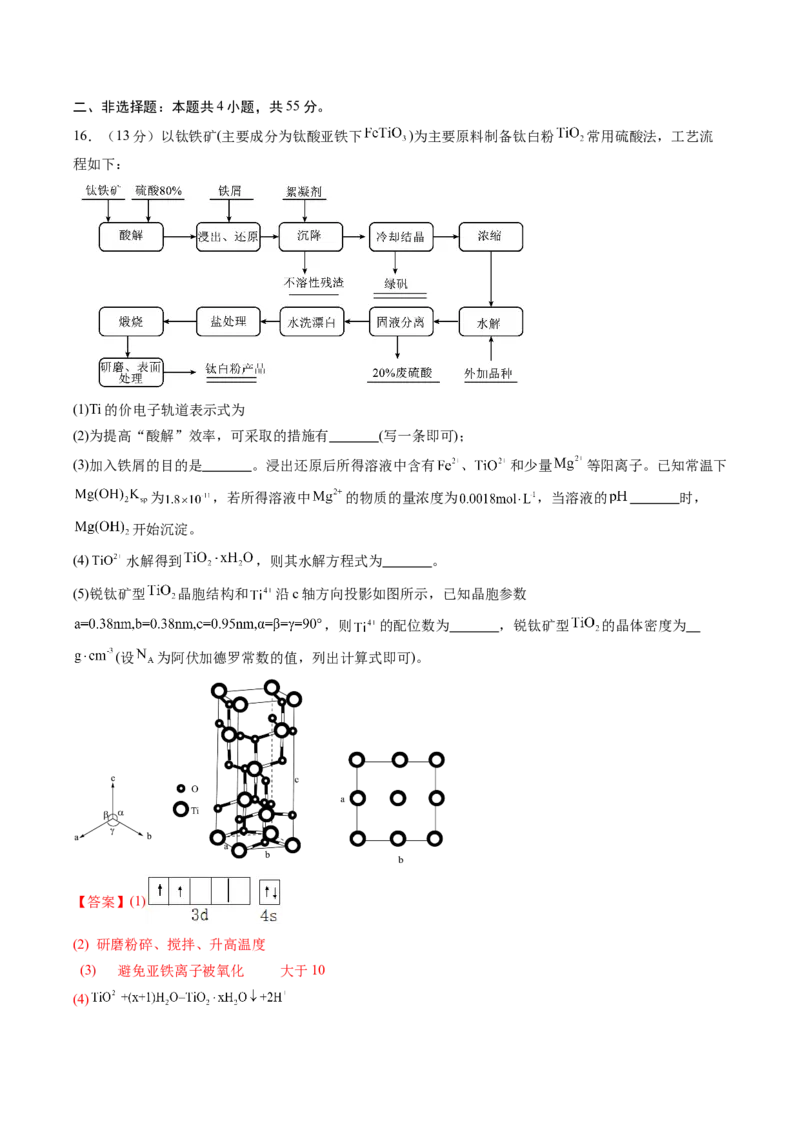
(5)锐钛矿型 晶胞结构和 沿c轴方向投影如图所示,已知晶胞参数
,则 的配位数为 ,锐钛矿型 的晶体密度为
(设 为阿伏加德罗常数的值,列出计算式即可)。
【答案】(1)
(2) 研磨粉碎、搅拌、升高温度
(3) 避免亚铁离子被氧化 大于10
(4)(5) 6
【详解】(1)钛的价电子轨道表示式,即电子排布图为
(2)为提高“酸解”效率,可采取的措施有研磨粉碎、搅拌、升高温度等;
(3)亚铁离子容易被空气中氧气氧化为铁离子,铁单质能将铁离子还原为亚铁离子,故加入铁屑的目的
是避免亚铁离子被氧化;所得溶液中 的物质的量浓度为 ,
,pOH=4,则pH=10时, 开始沉淀。
(4) 水解得到 沉淀,结合质量守恒,还生成氢离子,则其水解离子方程式为
;
(5)由图,中心 周围有6个最近的氧, 的配位数为6;根据“均摊法”,晶胞中含
个Ti,则结合化学式可判断含8个O(其中8个在楞上,8个在面上,内部2个),则晶
体密度为 。
17.(14分)三苯甲醇 是一种重要的有机合成中间体,实验室可通过苯甲酸乙酯和苯基溴
化镁的反应制备三苯甲醇,反应原理如下:
已知:苯基溴化镁( )易与空气发生反应。
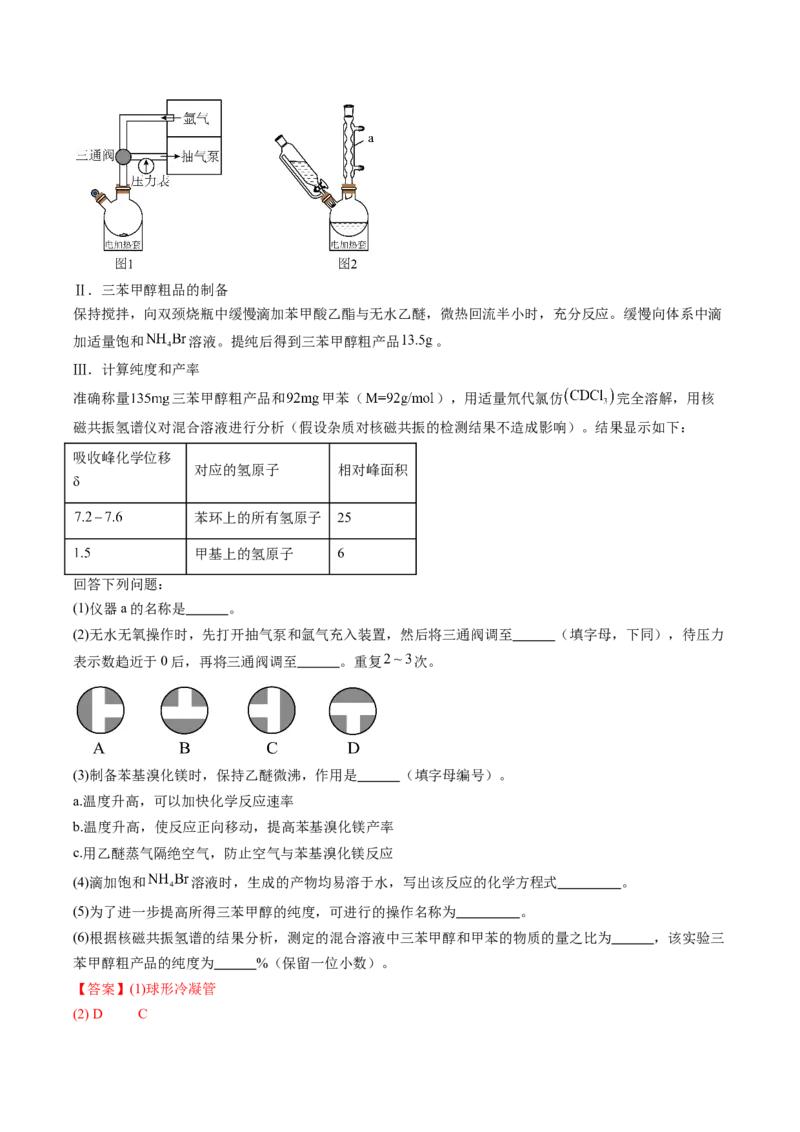
Ⅰ.苯基溴化镁的制备
向双颈烧瓶中加入 镁屑、一小粒碘和磁力搅拌子,按图1装置对双颈烧瓶进行无水无氧操作。之后按
照图2装置,向烧瓶中滴加无水乙醚 和 新蒸溴苯的混合液,开始搅拌,控制温度为 保持
乙醚微沸,回流半小时至镁屑完全反应。Ⅱ.三苯甲醇粗品的制备
保持搅拌,向双颈烧瓶中缓慢滴加苯甲酸乙酯与无水乙醚,微热回流半小时,充分反应。缓慢向体系中滴
加适量饱和 溶液。提纯后得到三苯甲醇粗产品 。
Ⅲ.计算纯度和产率
准确称量 三苯甲醇粗产品和 甲苯( ),用适量氘代氯仿 完全溶解,用核
磁共振氢谱仪对混合溶液进行分析(假设杂质对核磁共振的检测结果不造成影响)。结果显示如下:
吸收峰化学位移
对应的氢原子 相对峰面积
δ
苯环上的所有氢原子 25
甲基上的氢原子 6
回答下列问题:
(1)仪器a的名称是 。
(2)无水无氧操作时,先打开抽气泵和氩气充入装置,然后将三通阀调至 (填字母,下同),待压力
表示数趋近于0后,再将三通阀调至 。重复 次。
(3)制备苯基溴化镁时,保持乙醚微沸,作用是 (填字母编号)。
a.温度升高,可以加快化学反应速率
b.温度升高,使反应正向移动,提高苯基溴化镁产率
c.用乙醚蒸气隔绝空气,防止空气与苯基溴化镁反应
(4)滴加饱和 溶液时,生成的产物均易溶于水,写出该反应的化学方程式 。
(5)为了进一步提高所得三苯甲醇的纯度,可进行的操作名称为 。
(6)根据核磁共振氢谱的结果分析,测定的混合溶液中三苯甲醇和甲苯的物质的量之比为 ,该实验三
苯甲醇粗产品的纯度为 %(保留一位小数)。
【答案】(1)球形冷凝管
(2) D C(3)ac
(4)
(5)重结晶
(6)
【详解】(1)仪器a的名称是球形冷凝管,该空填球形冷凝管;
(2)无水无氧操作时,应先抽尽装置中的空气,待压力表趋近0后,在通入氩气,因此三通阀应先调至D
状态,完成抽气后在将三通阀调至C状态,充入氩气,重复2-3次,以达到无水无氧状态,该空分别填
D、C;
(3)a.温度升高有助于加快反应速率,a正确;
b.镁与溴苯反应生成苯基溴化镁反应为放热反应,温度升高不利于平衡正向移动,b错误;
c.苯基溴化镁易与空气反应,通过控制温度保持乙醚微沸,可保证反应在乙醚蒸气环境下进行,起到隔
绝空气的作用,c正确;
本题选ac;
(4)滴加饱和溴化铵溶液可促进 水解,根据物料守恒且产物均易溶于水,可得化学方
程式为
(5)为了进一步提高所得三苯甲醇的纯度,可通过重结晶方法提高纯度,故该空填重结晶;
(6)设混合溶液中三苯甲醇与甲苯的物质的量之比为x:y,根据结构特点,1个三苯甲醇中含有15个苯环
上的H原子,无甲基上的H原子,1个甲苯中含有5个苯环上的H原子,3个甲基上H原子,故存在
15x+5y=25,3y=6,解得y=2,x=1,故混合溶液中三苯甲醇和甲苯的物质的量之比为1:2,根据已知得,
n(甲苯)= ,故n(三苯甲醇)= ,其纯度为
,该空分别填1:2,96.3。
18.(14分)c氨是最基本的化工原料之一,工业合成氨是人类科学技术的一项重大突破,目前已有三位
科学家因其获得诺贝尔奖,其反应原理为 。回答下列问题:
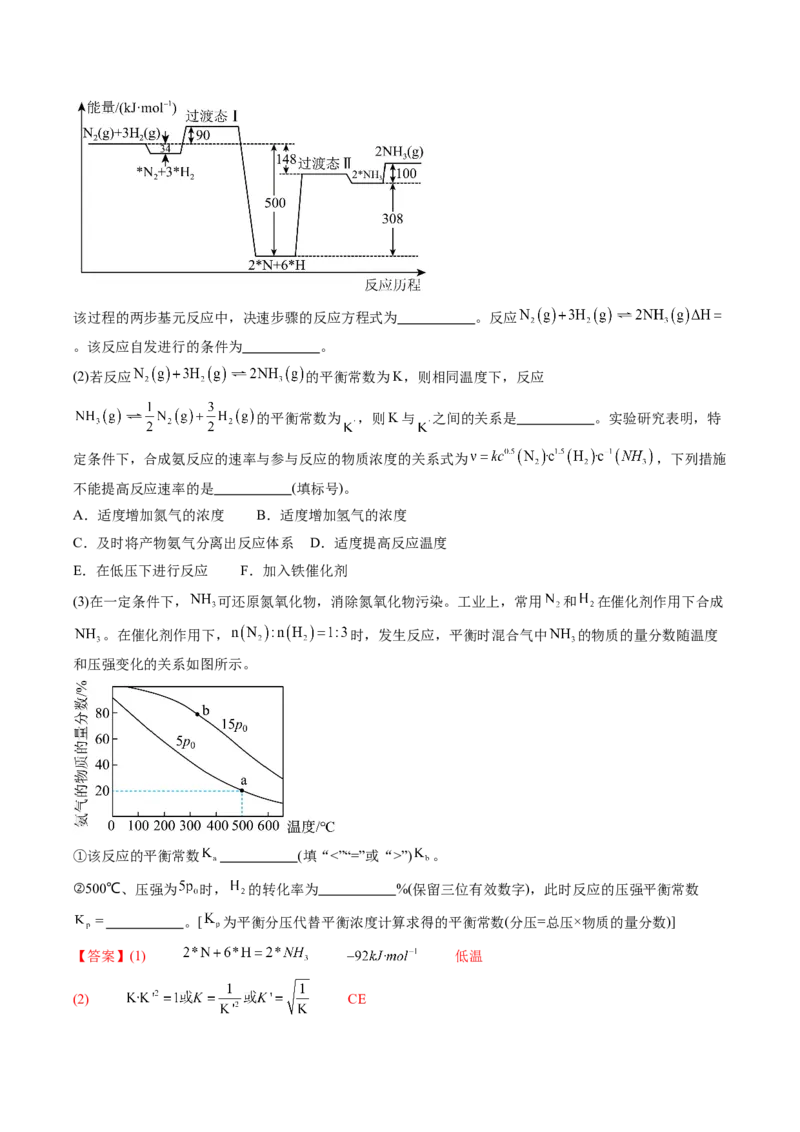
(1)在某种催化剂存在下,合成氨反应历程和能量变化如图所示(*R表示微粒处于吸附状态)。该过程的两步基元反应中,决速步骤的反应方程式为 。反应
。该反应自发进行的条件为 。
(2)若反应 的平衡常数为K,则相同温度下,反应
的平衡常数为 ,则K与 之间的关系是 。实验研究表明,特
定条件下,合成氨反应的速率与参与反应的物质浓度的关系式为 ,下列措施
不能提高反应速率的是 (填标号)。
A.适度增加氮气的浓度 B.适度增加氢气的浓度
C.及时将产物氨气分离出反应体系 D.适度提高反应温度
E.在低压下进行反应 F.加入铁催化剂
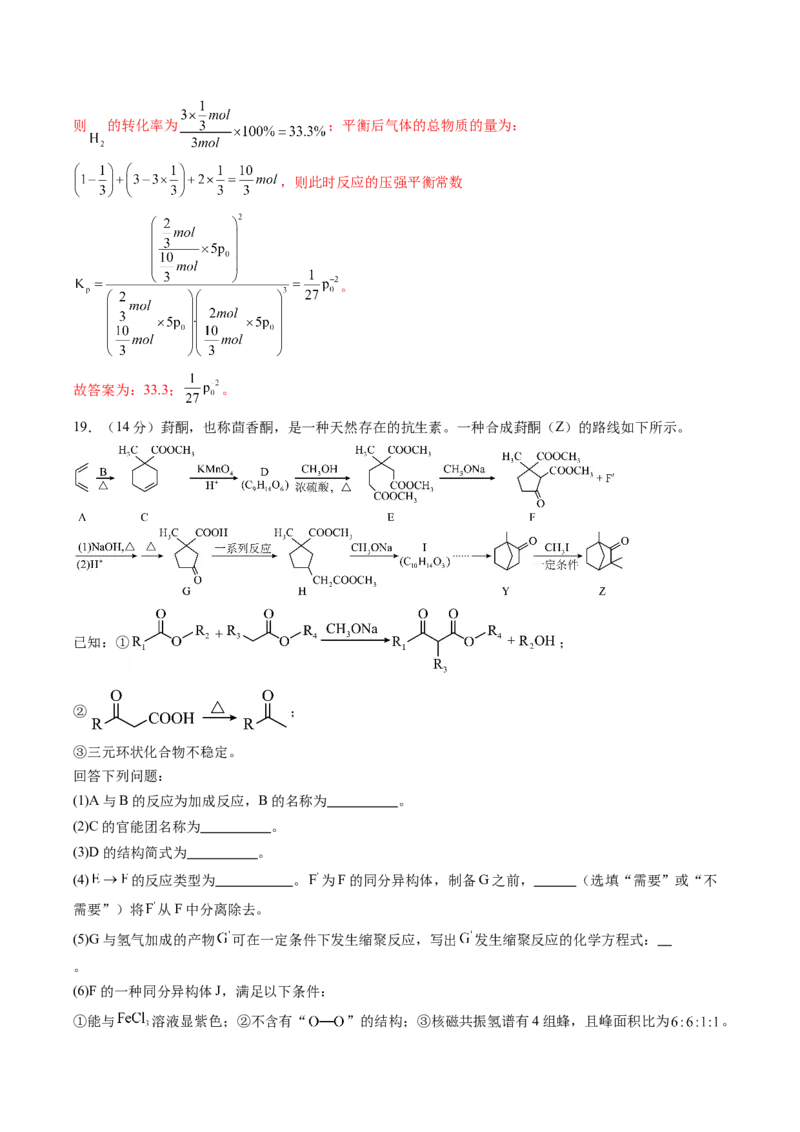
(3)在一定条件下, 可还原氮氧化物,消除氮氧化物污染。工业上,常用 和 在催化剂作用下合成
。在催化剂作用下, 时,发生反应,平衡时混合气中 的物质的量分数随温度
和压强变化的关系如图所示。
①该反应的平衡常数 (填“<”“=”或“>”) 。
②500℃、压强为 时, 的转化率为 %(保留三位有效数字),此时反应的压强平衡常数
。[ 为平衡分压代替平衡浓度计算求得的平衡常数(分压=总压×物质的量分数)]
【答案】(1) 低温
(2) CE(3) < 33.3
【详解】(1)在多步的基元反应中,基元反应活化能越大,反应速率越慢,为反应的决速步,根据反应
机理图,过渡态II的活化能最大,反应的方程式为: 。根据图形和过渡态I和II,反
应物的活化能为: ,生成物的活化能为: ,则反应
。反应 , ,根据
能自发,则T为低温才能使 ,即低温下自发。
故答案为: ; ;低温。
(2)在相同温度下,反应 的平衡常数为 ,反应
的平衡常数为 ,则K与 之间的关系为
;在特定条件下,合成氨反应的速率与参与反应的物质浓度的关系式为
,即 ,下列措施不能提高反应速率的为:
A.适度增加氮气的浓度:增大气体的浓度, 增大,A不符合题意;
B.适度增加氢气的浓度:增大气体的浓度, 增大,B不符合题意;
C.及时将产物氨气分离出反应体系:减小气体的浓度, 减慢,C符合题意;
D.适度提高反应温度:升高温度, 加快,D不符合题意;
E.在低压下进行反应:降低压强, 减慢,E符合题意;
F.加入铁催化剂:使用催化剂, 加快,D不符合题意;
故答案为: ;CE。
(3)①根据反应 ,平衡常数只受到温度的影响,a点温度比
b点高,平衡左移,则平衡常数减小,所以得到 ;
②500℃,压强为 时,将 进行反应,达到平衡时氨气的物质的量分数为20%,设
、 、消耗的 为 ,列三段式:
,由 计算出 ,则 的转化率为 ;平衡后气体的总物质的量为:
,则此时反应的压强平衡常数
。
故答案为:33.3; 。
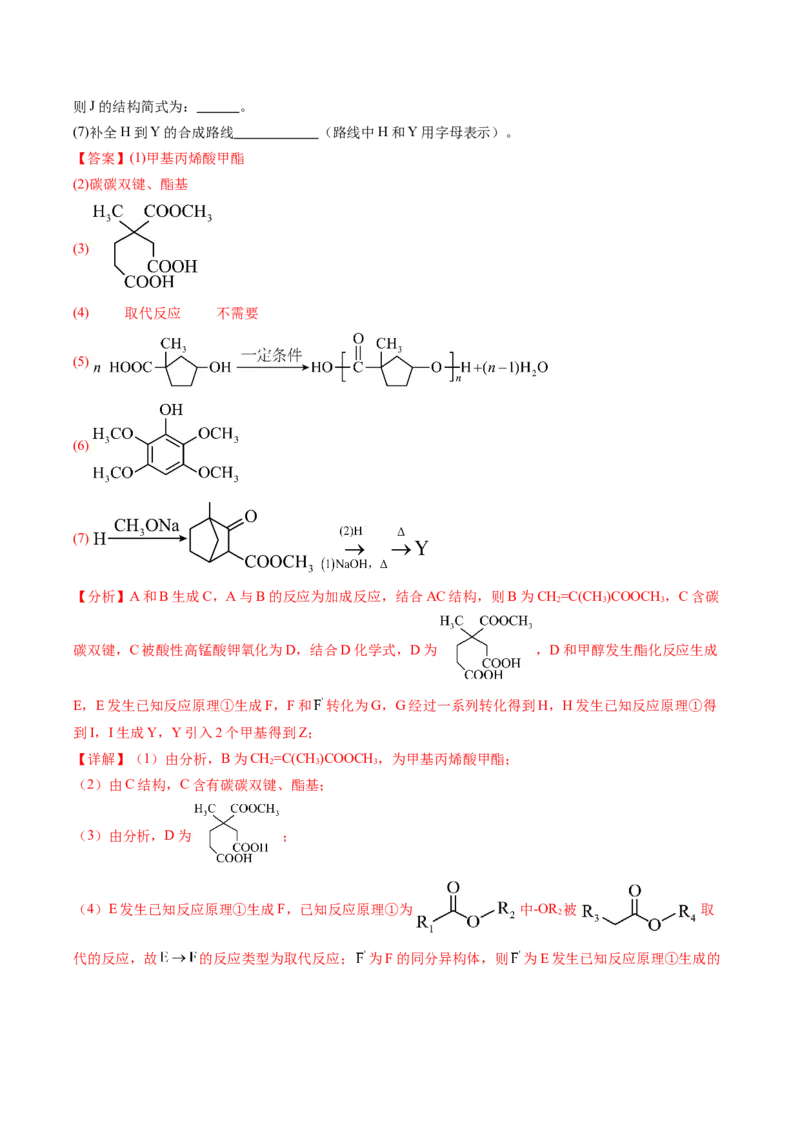
19.(14分)葑酮,也称茴香酮,是一种天然存在的抗生素。一种合成葑酮(Z)的路线如下所示。
已知:① ;
② ;
③三元环状化合物不稳定。
回答下列问题:
(1)A与B的反应为加成反应,B的名称为 。
(2)C的官能团名称为 。
(3)D的结构简式为 。
(4) 的反应类型为 。 为F的同分异构体,制备G之前, (选填“需要”或“不
需要”)将 从F中分离除去。
(5)G与氢气加成的产物 可在一定条件下发生缩聚反应,写出 发生缩聚反应的化学方程式:
。
(6)F的一种同分异构体J,满足以下条件:
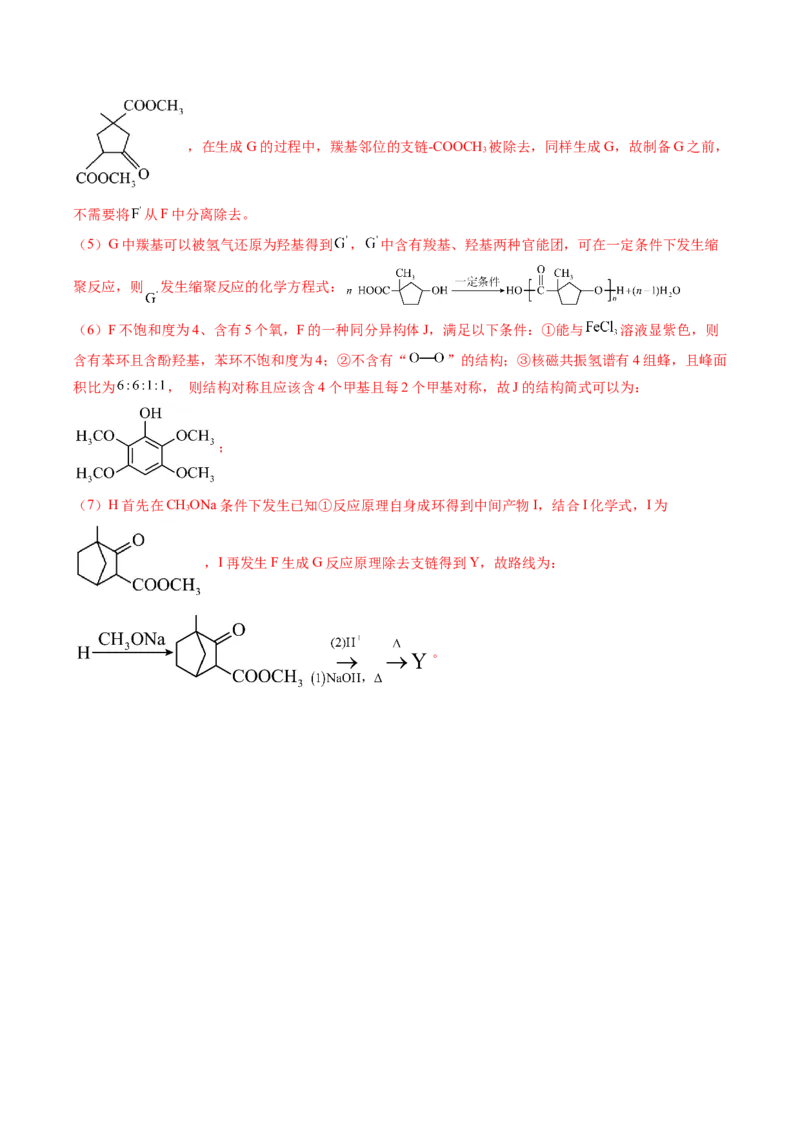
①能与 溶液显紫色;②不含有“ ”的结构;③核磁共振氢谱有4组蜂,且峰面积比为 。则J的结构简式为: 。
(7)补全H到Y的合成路线 (路线中H和Y用字母表示)。
【答案】(1)甲基丙烯酸甲酯
(2)碳碳双键、酯基
(3)
(4) 取代反应 不需要
(5)
(6)
(7)
【分析】A和B生成C,A与B的反应为加成反应,结合AC结构,则B为CH=C(CH )COOCH ,C含碳
2 3 3
碳双键,C被酸性高锰酸钾氧化为D,结合D化学式,D为 ,D和甲醇发生酯化反应生成
E,E发生已知反应原理①生成F,F和 转化为G,G经过一系列转化得到H,H发生已知反应原理①得
到I,I生成Y,Y引入2个甲基得到Z;
【详解】(1)由分析,B为CH=C(CH )COOCH ,为甲基丙烯酸甲酯;
2 3 3
(2)由C结构,C含有碳碳双键、酯基;
(3)由分析,D为 ;
(4)E发生已知反应原理①生成F,已知反应原理①为 中-OR 被 取
2
代的反应,故 的反应类型为取代反应; 为F的同分异构体,则 为E发生已知反应原理①生成的,在生成G的过程中,羰基邻位的支链-COOCH 被除去,同样生成G,故制备G之前,
3
不需要将 从F中分离除去。
(5)G中羰基可以被氢气还原为羟基得到 , 中含有羧基、羟基两种官能团,可在一定条件下发生缩
聚反应,则 发生缩聚反应的化学方程式:
(6)F不饱和度为4、含有5个氧,F的一种同分异构体J,满足以下条件:①能与 溶液显紫色,则
含有苯环且含酚羟基,苯环不饱和度为4;②不含有“ ”的结构;③核磁共振氢谱有4组蜂,且峰面
积比为 , 则结构对称且应该含4个甲基且每2个甲基对称,故J的结构简式可以为:
;
(7)H首先在CHONa条件下发生已知①反应原理自身成环得到中间产物I,结合I化学式,I为
3
,I再发生F生成G反应原理除去支链得到Y,故路线为:
。