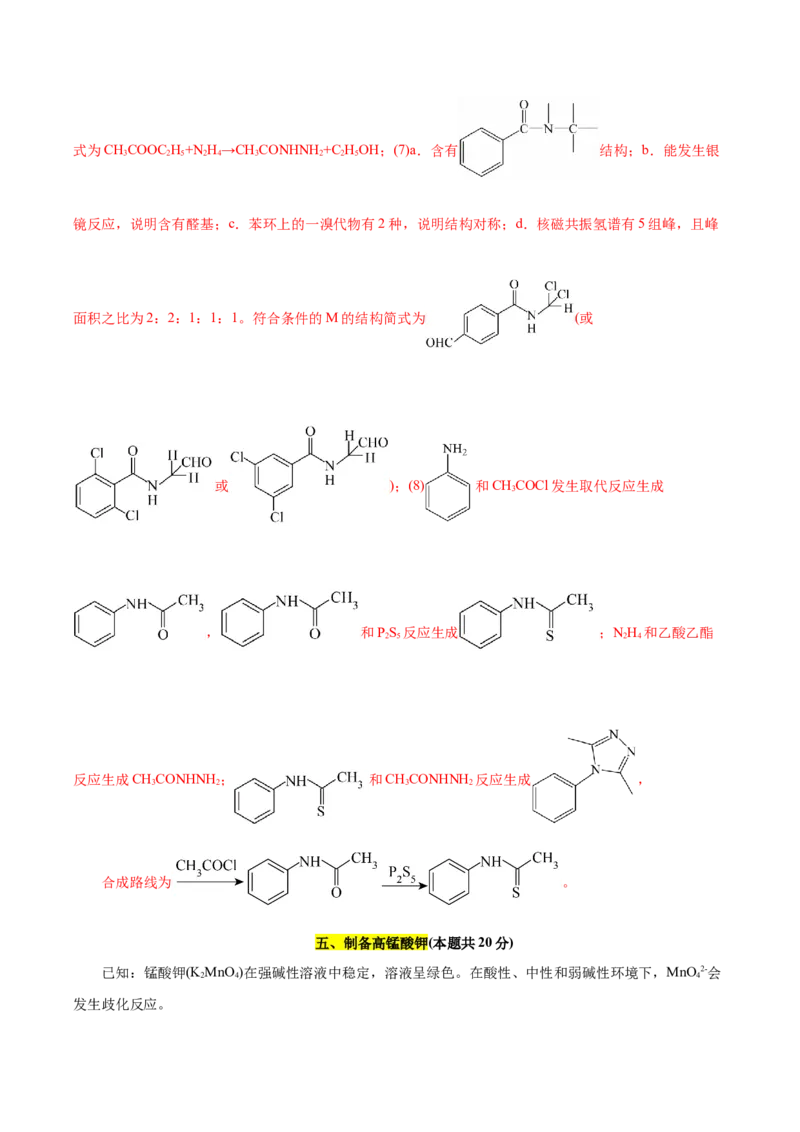
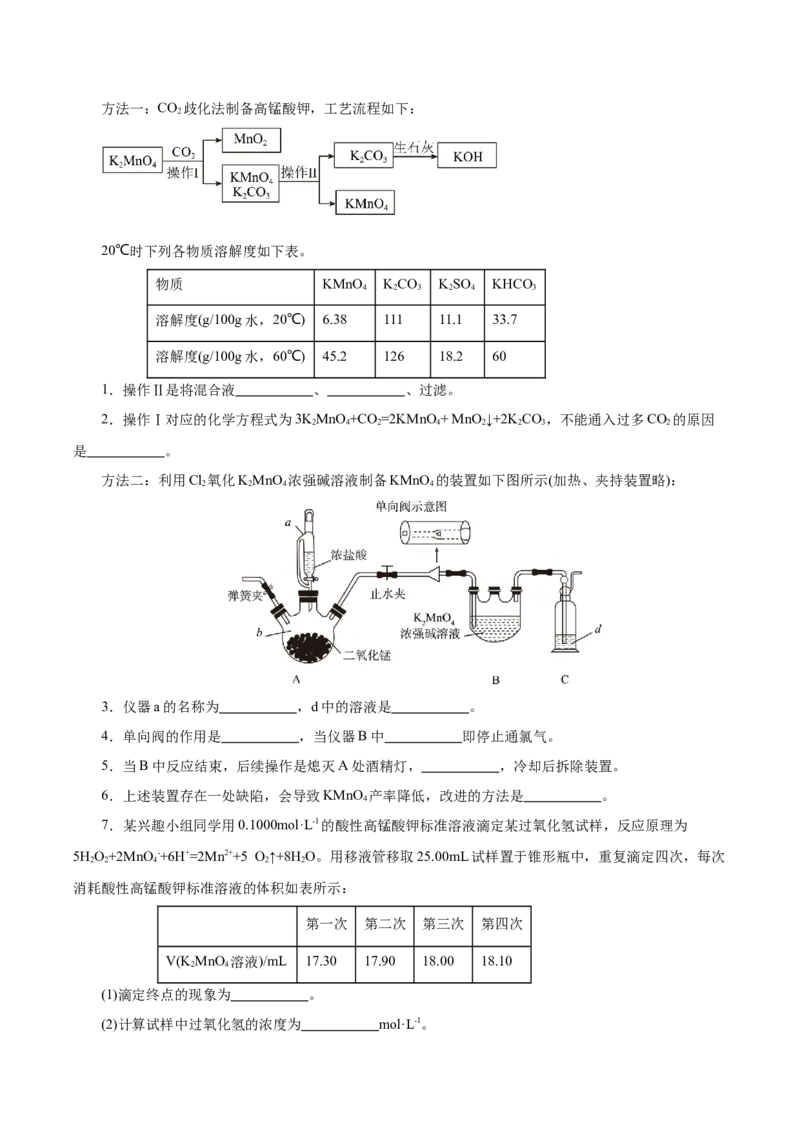
文档内容
绝密★启用前
2025 年高考考前信息必刷卷 04(上海专用)
化 学
考情速递
高考·新动向:上海高考化学试题独树一帜,题目以课题形式出现,有助于引导高中化学教学方式的转
变。上海高考化学中设置一些与实际教学内容相联系但形式为课题研究的题目,促使教师在教学中更
加注重将知识与实际的课题研究相融合,培养学生解决复杂问题的能力,也让学生适应这种在课题情
境下运用知识的考查方式。
高考·新考法:上海高考化学试卷设置了五道主题式综合题,这可以看作是一种课题形式的体现。每道
大题依据其内在的逻辑关联分设选择、填空、简答、计算等题型,形式新颖。这些主题式综合题多角
度、多层次考查学生化学学科核心素养发展水平。
高考·新情景:创设真实情境是上海高考化学命题的一大特点,这与课题形式出题相契合。比如以医药
健康中的降血糖药物瑞格列奈的合成情境出题,这类似于一个药物合成课题。学生要在这个情境下分
析合成过程中的化学物质转化、反应条件、反应类型等化学知识,从原料出发,经过多步反应得到目
标产物,如同在研究一个具体的化学课题。这种情境化的课题形式命题有助于考查学生将化学知识应
用于实际情境的能力,以及在复杂情境下分析和解决问题的能力。
命题·大预测:预测在2025年的高考试题中仍会继续延续课题出题方式,更贴近工业生产。以课题形式
出现的题目要求考生具备综合运用化学知识的能力。例如在一道关于环境污染治理的课题形式题目中,
考生可能需要运用化学平衡、氧化还原反应、离子反应等多方面知识来提出治理方案。这需要考生将
所学的各个知识点串联起来,从整体上分析和解决问题,而不是孤立地看待每个知识点,这是应对课
题形式题目的关键能力之一。
(试卷满分100分,考试时间60分钟)
1.本考试分设试卷和答题纸。答题前,务必在答题纸上填写学校、姓名、座位号,并将核对后的条
形码贴在指定位置上。作答必须涂或写在答题纸上,在试卷上作答一律不得分。
2.选择类试题中,标注“不定项”的试题,每小题有1~2个符合条件的选项;标注“双选”的试题,
每小题有两个符合条件的选项;标注“单选”的试题,每小题只有一个符合条件的选项。
3.可能用到的相对原子质量:H-1 C-12 N-14 O-16 F-19 Na-23 Mg-24 Al-27 P-31
Cl-35.5 Ca-40 Mn-55 Cr-52 Fe-56 Cu-64 I-127 Pb-207
一、亚硝酰氯(本题共20分)
1.关于N与O两种元素的比较正确的是 。
A.第一电离能:O>N B.电负性:N>O
C.原子半径:O>N D.基态原子核外未成对电子数:N>O2.NOCl 分子中各原子均满足8电子稳定结构,则NOCl的电子式为 ,该分子的空间构型
。
3.NOCl水解生成两种酸,写出相应的化学方程式: 。
4.NOCl 在一定频率(v)光的照射下会发生光解,其反应机理为:
第一步:NOCl(g) + hv=NOCl*(g);
第二步:NOCl(g) + NOCl*(g)=2NO(g) + Cl (g)
2
其中 hv 表示一个光子能量,NOCl*表示 NOCl 的激发态。
(1)以下均从选项中选择:第一步的焓变 ΔH 0;第二步的熵变 ΔS 0。
A.大于 B. 小于 C.等于
(2)分解1molNOCl 需要吸收 mol 光子。
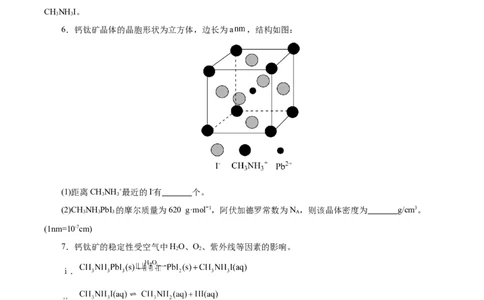
5.实验室可用NO与Cl 在通常条件下制备NOCl,(已知NO 与Cl 反应可得到NO Cl),装置如下图
2 2 2 2
所示。
实验时,先通入一种气体,待E中U形管内充满该气体时,再缓缓通入另一种气体。
(1)装置F的作用是 。
(2)实验中应先通Cl 还是NO? 。请举出一条理由 。
2
【答案】1.D(2分)
2. (2分) V形(2分)
3.NOCl+HO=HNO +HCl (2分)
2 2
4.(1) A(2分) A(2分) (2)0.5(2分)
5.(1)防止G中水蒸气进入U形管,避免引起NOCl水解(2分)
(2)Cl (2分) 先通Cl 可以排除装置中的空气,避免O 与NO生成NO ,进而产生杂质NO Cl(2
2 2. 2 2 2
分)
【解析】1.A项,由于N的价层电子排布式为2s22p3,为半充满状态,能量较低,难失电子,因此第一电离能高于O,故第一电离能::N>O,A错误;B项,非金属性越强则电负性越大,非金属性:N<
O,电负性:N<O,B错误;C项,同周期从左往右原子半径在减小,因此原子半径:N>O,C错误;D
项,N的价层电子排布式为2s22p3,未成对电子数为3,氧的价层电子排布式为2s22p4,未成对电子数为
2,基态原子核外未成对电子数:N>O,D正确;故选D。
2.NOCl分子中各原子均满足8电子稳定结构,其中N原子化合价为+3价,O原子化合价为−2价,
Cl原子化合价为-1价,则氮原子与氧原子形成两对共用电子对,与氯原子形成一对共用电子对,则NOCl
分子的电子式为: ;NOCl分子的中心原子N原子存在一对孤电子,利用价层电子对互斥
理论得到NOCl的VSEPR模型为平面三角形,则NOCl分子的空间构为V形。
3.亚硝酰氯(NOCl)中氮元素的化合价为+3价,氯元素的化合价为-1价,氧原子的化合价为−2价,其
水解生成两种酸,则化合价未发生变化,则水解分别得到亚硝酸和盐酸,水解方程式为:
NOCl+HO=HNO +HCl。
2 2
4.(1)第一步: NOCl+hv→NOCl*为基态到激发态,即需要吸热,所以第一步的焓变 H>0;第二步反
应气体分子数增多,混乱度增大,是熵增的过程,其熵变 S>0,故选A、A;(2)由反应机△理可知,反应总
反应方程式为:2NOCl+ hv→2NO+Cl ,故分解1molNOCl△需要吸收0.5mol光子。
2
5.(1)NOCl会发生水解,因此装置F的作用是防止G中水蒸气进入U形管,避免引起NOCl水解;
(2)本实验是用Cl 和NO制备NOCl,但NO 与Cl 反应可得到NO Cl,因此要先通入Cl,用Cl 排除装置
2 2 2 2 2 2
中的空气,避免空气与O 生成NO ,进而产生杂质NO Cl。
2 2 2
二、新型半导体材料(本题共20分)
某钙钛矿CHNH PbI 是一种新型半导体材料,用于制造太阳能电池。
3 3 3
1.Pb位于元素周期表第6周期ⅣA族,写出基态 原子价电子轨道表示式 。
2.NH 分子的空间构型是 。
3
3.NH 的N-H键是由N的 轨道与H的1s轨道重叠形成 键。
3
4.钛的某配合物可用于催化环烯烃聚合,其结构如下图所示:(1)钛的配位数为 ,碳原子的杂化类型有 种。
(2)该配合物中存在的化学键有_______(双选)。
A.氢键 B.配位键 C.金属键 D.共价键
5.可用CHOH、NH 、I、PbI ,制备钙钛矿CHNH PbI ,过程如下所示:
3 3 2 2 3 3 3
(1)Ⅰ中,CHOH的沸点高于CHI的沸点,原因是 。
3 3
(2)Ⅱ中,由于NH 分子中的 原子(填元素符号)具有孤电子对,容易与CHI反应生成盐
3 3
CHNH I。
3 3
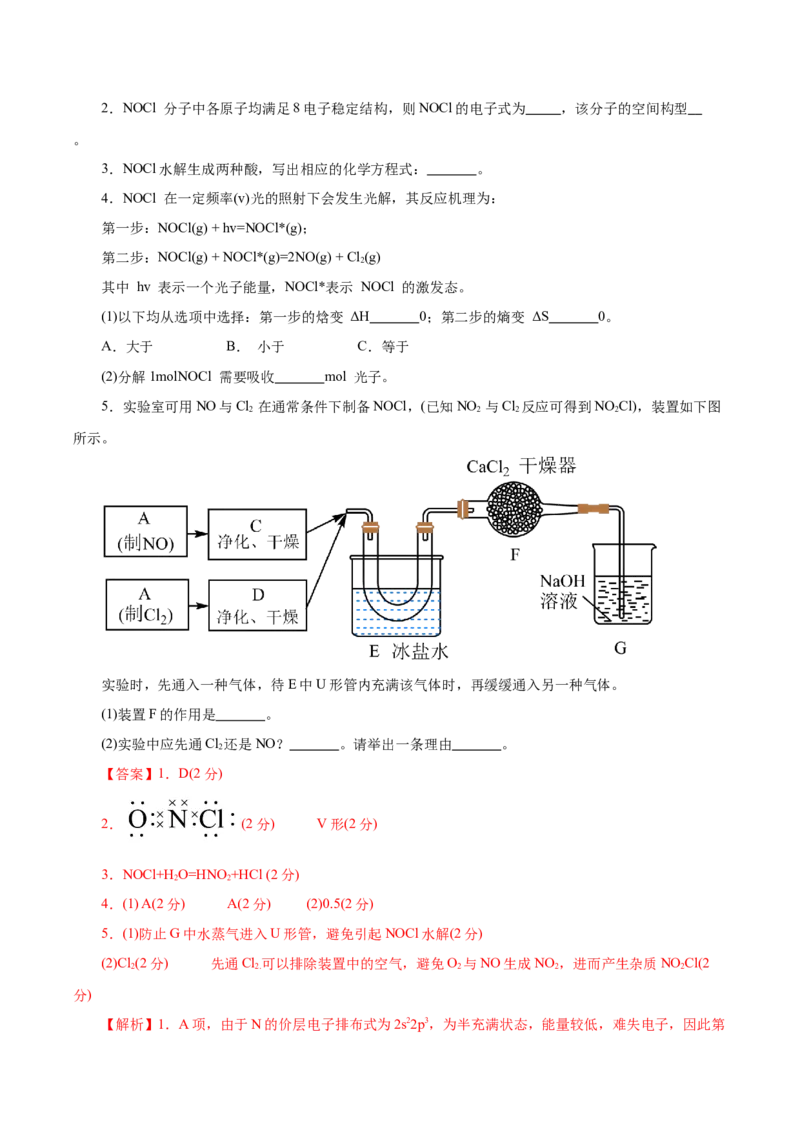
6.钙钛矿晶体的晶胞形状为立方体,边长为a ,结构如图:
(1)距离CHNH +最近的I-有 个。
3 3
(2)CH NH PbI 的摩尔质量为620 g·molˉ1,阿伏加德罗常数为N ,则该晶体密度为 g/cm3。
3 3 3 A
(1nm=10-7cm)
7.钙钛矿的稳定性受空气中HO、O、紫外线等因素的影响。
2 2
ⅰ.
ⅱ.
研究发现,一旦生成 ,钙钛矿的分解程度就会增大,请结合化学平衡移动原理解释: ,我
国研究人员利用聚乙二醇有效地解决了该问题。
【答案】1. (2分)
2.三角锥形(2分)
3.sp3杂化(2分)4.(1)6(2分) 2(2分) (2)BD(2分)
5.(1)CH OH能形成分子间氢键,CHI不能形成分子间氢键(2分)
3 3
(2)N(2分)
6.(1)12(2分) (2) (2分)
7.发生反应4HI+O=2H O+2I (或2HI=H+I ),HI浓度减小,反应ⅱ正向移动,CHNH I的浓度减小,
2 2 2 2 2 3 3
使反应ⅰ平衡正向移动(2分)
【解析】1.由铅元素位于元素周期表第6周期ⅣA族可知,基态原子的电子排布式为6s26p2,轨道表
示式为 ;
2.氨分子中氮原子的价层电子对数为4,则原子的杂化方式为sp3杂化,分子的VSEPR模型为四面体
形,因为有一对孤对电子,NH 分子的空间构型是三角锥形;
3
3.分子中的氮氢键是氮原子的sp3杂化轨道与氢原子的1s轨道道重叠形成σ键。
4.(1)据图分析得,Ti与4个O和2个Cl形成配位键,配位数为6;甲基碳的杂化类型为sp3,双键碳
的杂化类型为sp2,共2种;(2)Ti和氯原子、O原子之间存在配位键,C-H和C-C及C-O原子之间存在共
价键,所以含有的化学键为配位键和共价键,氢键不是化学键,故答案为BD。
5.(1)甲醇分子能形成分子间氢键,一碘甲烷不能形成分子间氢键,所以甲醇的分子间作用力大于一
碘甲烷,沸点高于一碘甲烷;(2)Ⅱ中,由于氨分子中氮原子具有孤电子对,能与一碘甲烷的CH+中具有
3
空轨道的碳原子形成配位键生成CHNH I。
3 3
6.(1)由晶胞结构可知,晶胞中位于顶点的CHNH +与位于面心的碘离子距离最近,则距离
3 3
CHNH +最近的碘离子的个数为12;(2)由晶胞结构可知,晶胞中位于顶点的CHNH +个数为8× =1,位于
3 3 3 3
面心的碘离子个数为6× =3,位于体内的铅离子个数为1,设晶体的密度为dg/cm3,由晶胞的质量公式可
得: =(10-7a)3d,解得d= ;
7.一旦生成HI,则发生4HI+O=2H O+2I 或2HI=H+I ,HI浓度减小,使反应ⅱ平衡正向移动,
2 2 2 2 2
CHNH I的浓度减小,使反应ⅰ平衡正向移动,钙钛矿的分解程度增大。
3 3三、氨的合成与应用(本题共22分)
I.20世纪初,哈伯和博施开发了以N 和H 为原料合成氨工艺,目前该工艺仍在广泛使用。
2 2
1.基态氮原子中电子占据最高能级的电子云轮廓图为 形,基态N原子的轨道表示式为
。
2.关于哈伯和博施法工业合成氨的说法错误的是__________。
A.反应温度为500℃主要因为该温度是催化剂的活性温度
B.合成氨工业中利用了热交换器,实现绿色低碳化
C.理论上通过该反应ΔS>0、ΔH<0可以判断该反应可以自发进行
D.将气态氨变成液氨后及时从平衡混合物中分离出去,可以提高平衡转化率
3.关于NH 说法正确的是__________。
3
A.NH 遇到HCl产生白烟 B.可用NH Cl受热分解可制得NH
3 4 3
C.NH 可用湿润的蓝色石蕊试纸检验 D.NH 是氮元素唯一的氢化物
3 3
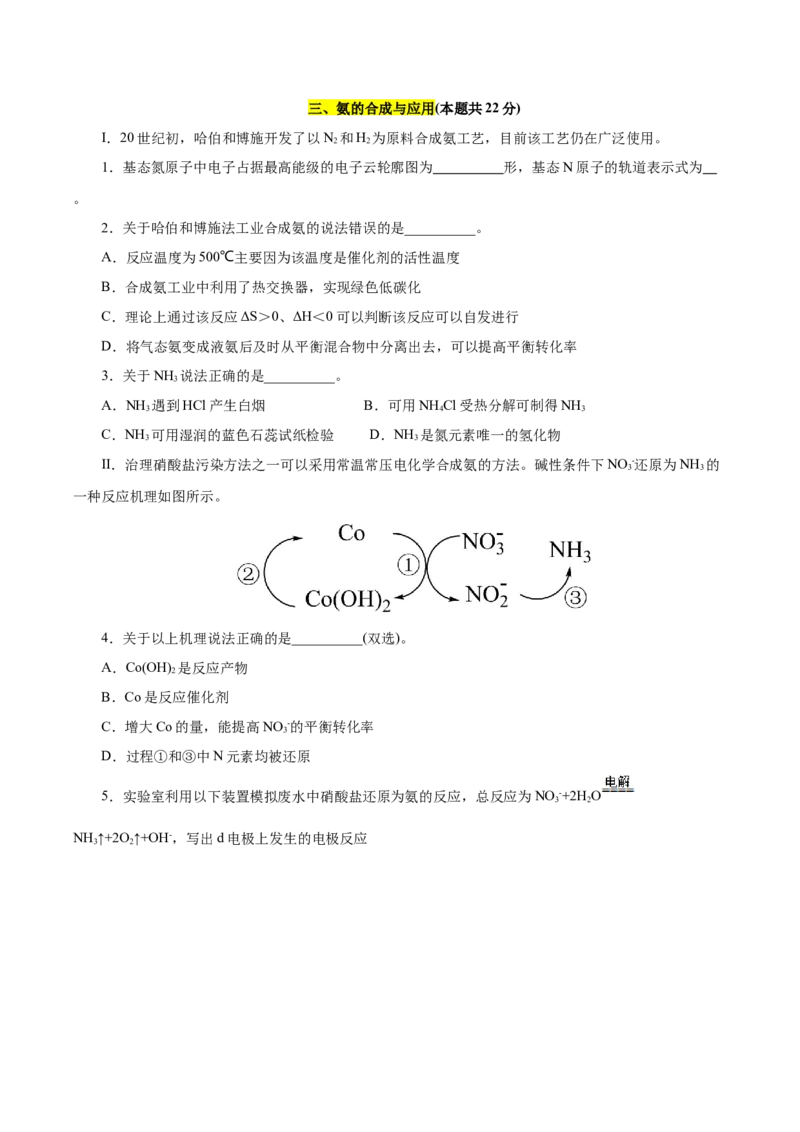
II.治理硝酸盐污染方法之一可以采用常温常压电化学合成氨的方法。碱性条件下NO -还原为NH 的
3 3
一种反应机理如图所示。
4.关于以上机理说法正确的是__________(双选)。
A.Co(OH) 是反应产物
2
B.Co是反应催化剂
C.增大Co的量,能提高NO -的平衡转化率
3
D.过程①和③中N元素均被还原
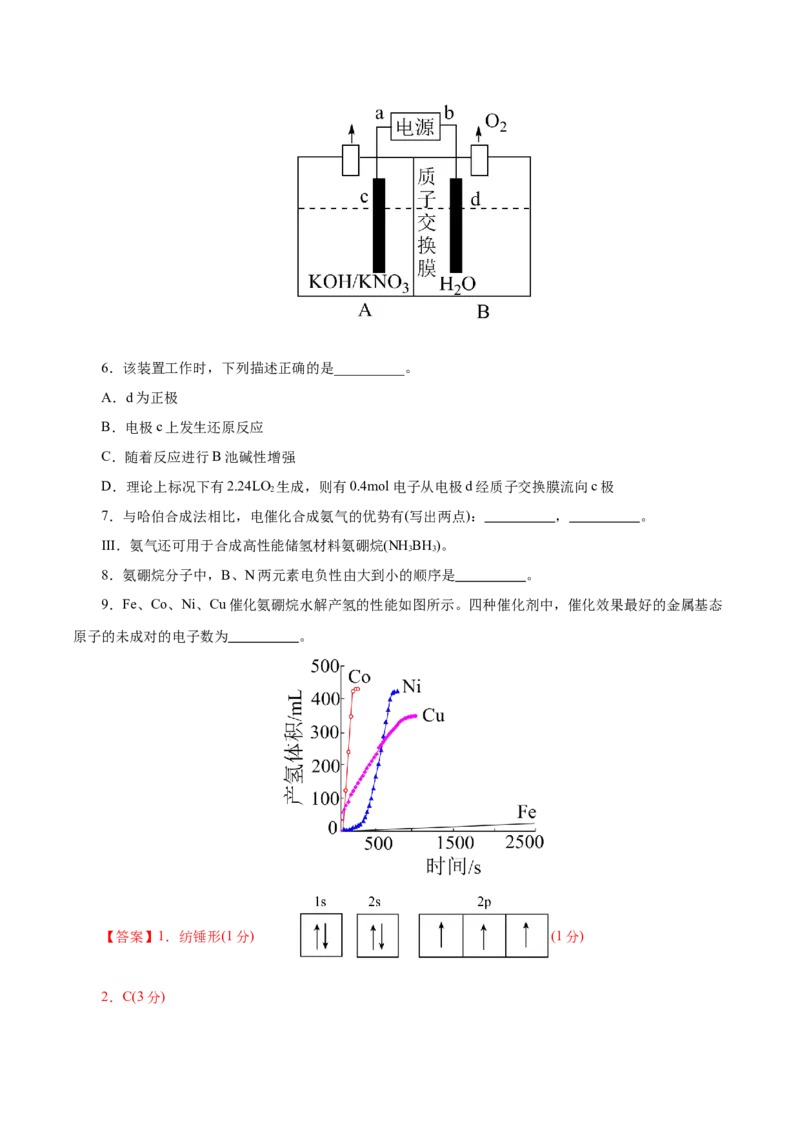
5.实验室利用以下装置模拟废水中硝酸盐还原为氨的反应,总反应为NO -+2H O
3 2
NH ↑+2O ↑+OH-,写出d电极上发生的电极反应
3 26.该装置工作时,下列描述正确的是__________。
A.d为正极
B.电极c上发生还原反应
C.随着反应进行B池碱性增强
D.理论上标况下有2.24LO 生成,则有0.4mol电子从电极d经质子交换膜流向c极
2
7.与哈伯合成法相比,电催化合成氨气的优势有(写出两点): , 。
III.氨气还可用于合成高性能储氢材料氨硼烷(NH BH)。
3 3
8.氨硼烷分子中,B、N两元素电负性由大到小的顺序是 。
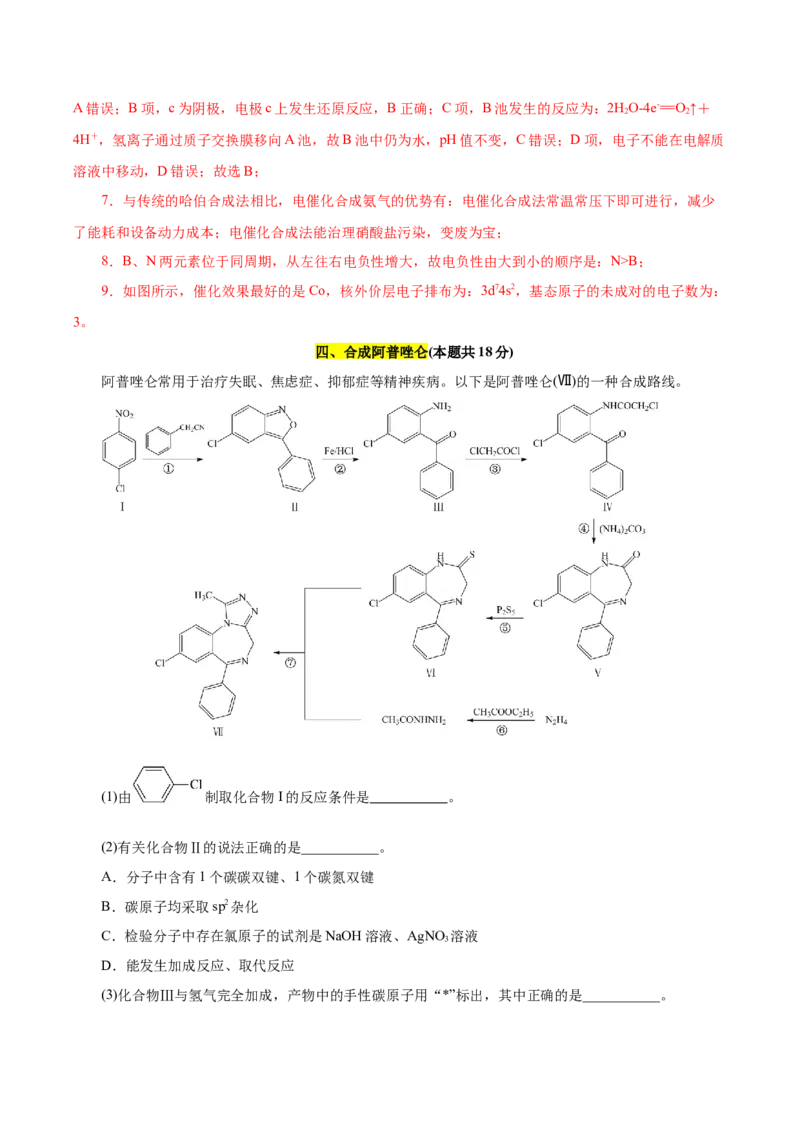
9.Fe、Co、Ni、Cu催化氨硼烷水解产氢的性能如图所示。四种催化剂中,催化效果最好的金属基态
原子的未成对的电子数为 。
【答案】1.纺锤形(1分) (1分)
2.C(3分)3.A(2分)
4.BD(2分)
5.2HO-4e-=O↑+4H+(2分)
2 2
6.B(3分)
7.电催化合成法常温常压下即可进行,减少了能耗和设备动力成本(2分) 电催化合成法能治理
硝酸盐污染,变废为宝(2分)
8.N>B(2分)
9.3(2分)
【解析】1.基态氮原子的核外电子排布式为:1s22s22p3,电子占据最高能级的电子云轮廓图为纺锤形,
基态N原子的轨道表示式为: ;
2.A项,以氮气和氢气为原料合成氨的反应为放热反应,低温有利于反应正向进行,采用温度为
500℃是因为催化剂在500℃左右活性最高,A正确;B项,合成氨工业中利用了热交换器,可以充分利用
能源,实现绿色低碳化,B正确;C项,ΔG=ΔH-TΔS<0时反应能自发,该反应ΔS<0、ΔH<0,所以理
论上该反应常温下有可能自发进行,C错误;D项,将气态氨变成液氨后及时从平衡混合物中分离出去,
平衡正向移动,可以提高平衡转化率,D正确;故选C;
3.A项,NH 遇到HCl反应生成的氯化铵为固态,即产生的是白烟,A正确;B项,不能利用NH Cl
3 4
受热分解可制得NH ,因为氯化铵分解生成的氨气和氯化氢遇冷重新结合成氯化铵,B错误;C项,NH
3 3
为碱性气体,可使湿润的红色石蕊试纸变蓝,所以应该用湿润的红色石蕊试纸检验NH ,C错误;D项,
3
N元素的氢化物有NH 还有NH,D错误;故选A;
3 2 4
4.过程①为Co+NO-→Co(OH) + NO -,过程②为Co(OH) →Co,过程③为NO -→NH 。A项,由图示
3 2 2 2 2 3
和分析可知,过程中Co(OH) 先生成后消耗,是反应历程中的中间产物,A错误;B项,由图示和分析可
2
知,过程中Co先消耗后生成,所以Co是催化剂,B正确;C项,由以上分析可知,Co是催化剂,所以增
大Co的量,不能改变平衡,即不能提高的平衡转化率,C错误;D项,过程①为Co+ NO -→Co(OH) +
3 2
NO -,过程③为NO -→NH ,N元素化合价均降低,均被还原,D正确;故选BD;
2 2 3
5.该装置为电解池,d电极产生氧气,为阳极,故b为正极,a为负极,c为阴极。d电极上发生的电
极反应:2HO-4e-=O↑+4H+;
2 2
6.该装置为电解池,d电极产生氧气,为阳极,故b为正极,a为负极,c为阴极。A项,d为阳极,A错误;B项,c为阴极,电极c上发生还原反应,B正确;C项,B池发生的反应为:2HO-4e-=O↑+
2 2
4H+,氢离子通过质子交换膜移向A池,故B池中仍为水,pH值不变,C错误;D项,电子不能在电解质
溶液中移动,D错误;故选B;
7.与传统的哈伯合成法相比,电催化合成氨气的优势有:电催化合成法常温常压下即可进行,减少
了能耗和设备动力成本;电催化合成法能治理硝酸盐污染,变废为宝;
8.B、N两元素位于同周期,从左往右电负性增大,故电负性由大到小的顺序是:N>B;
9.如图所示,催化效果最好的是Co,核外价层电子排布为:3d74s2,基态原子的未成对的电子数为:
3。
四、合成阿普唑仑(本题共18分)
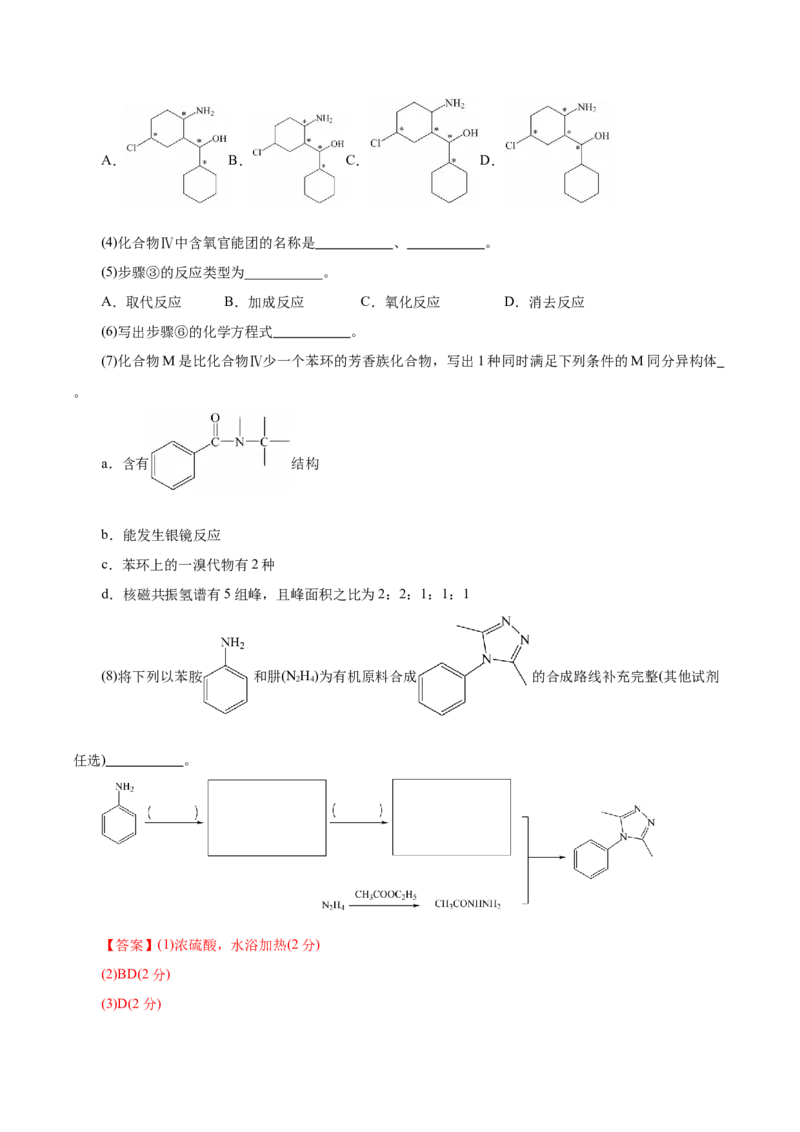
阿普唑仑常用于治疗失眠、焦虑症、抑郁症等精神疾病。以下是阿普唑仑(Ⅶ)的一种合成路线。
(1)由 制取化合物I的反应条件是 。
(2)有关化合物Ⅱ的说法正确的是___________。
A.分子中含有1个碳碳双键、1个碳氮双键
B.碳原子均采取sp2杂化
C.检验分子中存在氯原子的试剂是NaOH溶液、AgNO 溶液
3
D.能发生加成反应、取代反应
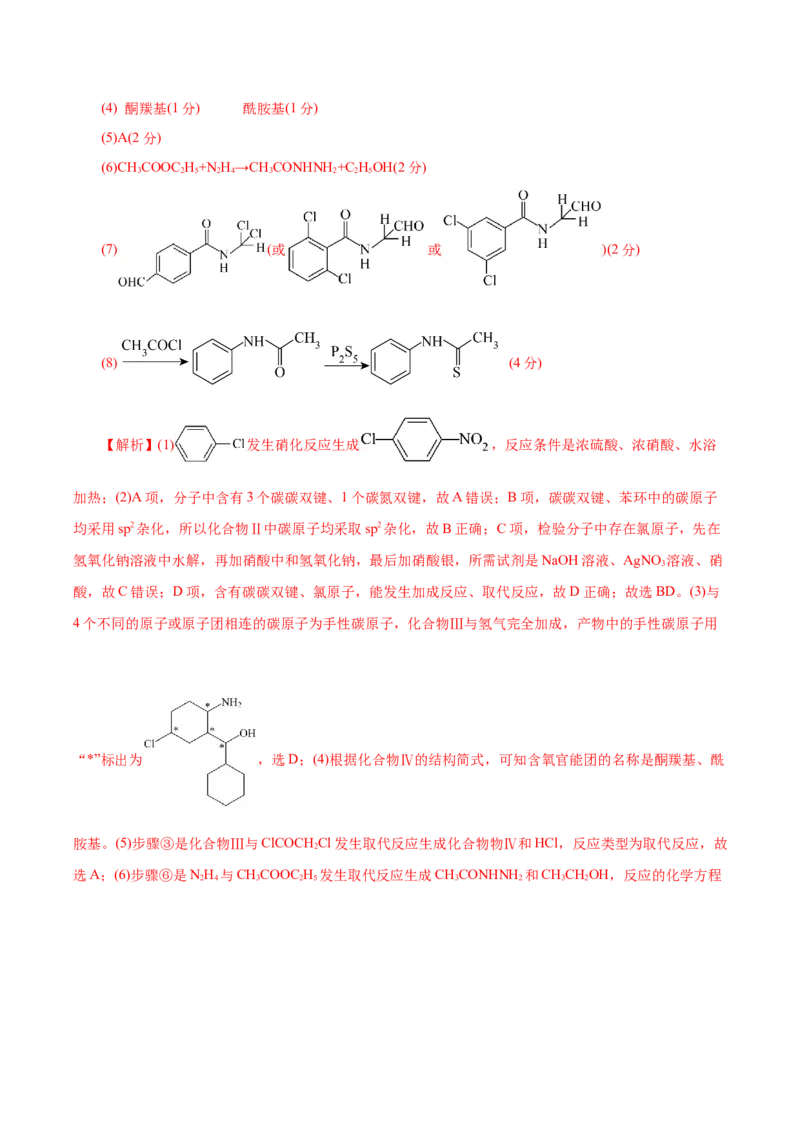
(3)化合物Ⅲ与氢气完全加成,产物中的手性碳原子用“*”标出,其中正确的是___________。A. B. C. D.
(4)化合物Ⅳ中含氧官能团的名称是 、 。
(5)步骤③的反应类型为___________。
A.取代反应 B.加成反应 C.氧化反应 D.消去反应
(6)写出步骤⑥的化学方程式 。
(7)化合物M是比化合物Ⅳ少一个苯环的芳香族化合物,写出1种同时满足下列条件的M同分异构体
。
a.含有 结构
b.能发生银镜反应
c.苯环上的一溴代物有2种
d.核磁共振氢谱有5组峰,且峰面积之比为2:2:1:1:1
(8)将下列以苯胺 和肼(N H)为有机原料合成 的合成路线补充完整(其他试剂
2 4
任选) 。
【答案】(1)浓硫酸,水浴加热(2分)
(2)BD(2分)
(3)D(2分)(4) 酮羰基(1分) 酰胺基(1分)
(5)A(2分)
(6)CH COOC H+N H→CHCONHNH +C HOH(2分)
3 2 5 2 4 3 2 2 5
(7) (或 或 )(2分)
(8) (4分)
【解析】(1) 发生硝化反应生成 ,反应条件是浓硫酸、浓硝酸、水浴
加热;(2)A项,分子中含有3个碳碳双键、1个碳氮双键,故A错误;B项,碳碳双键、苯环中的碳原子
均采用sp2杂化,所以化合物Ⅱ中碳原子均采取sp2杂化,故B正确;C项,检验分子中存在氯原子,先在
氢氧化钠溶液中水解,再加硝酸中和氢氧化钠,最后加硝酸银,所需试剂是NaOH溶液、AgNO 溶液、硝
3
酸,故C错误;D项,含有碳碳双键、氯原子,能发生加成反应、取代反应,故D正确;故选BD。(3)与
4个不同的原子或原子团相连的碳原子为手性碳原子,化合物Ⅲ与氢气完全加成,产物中的手性碳原子用
“*”标出为 ,选D;(4)根据化合物Ⅳ的结构简式,可知含氧官能团的名称是酮羰基、酰
胺基。(5)步骤③是化合物Ⅲ与ClCOCH Cl发生取代反应生成化合物物Ⅳ和HCl,反应类型为取代反应,故
2
选A;(6)步骤⑥是NH 与CHCOOC H 发生取代反应生成CHCONHNH 和CHCHOH,反应的化学方程
2 4 3 2 5 3 2 3 2式为CHCOOC H+N H→CHCONHNH +C HOH;(7)a.含有 结构;b.能发生银
3 2 5 2 4 3 2 2 5
镜反应,说明含有醛基;c.苯环上的一溴代物有2种,说明结构对称;d.核磁共振氢谱有5组峰,且峰
面积之比为2:2:1:1:1。符合条件的M的结构简式为 (或
或 );(8) 和CHCOCl发生取代反应生成
3
, 和PS 反应生成 ;NH 和乙酸乙酯
2 5 2 4
反应生成CHCONHNH ; 和CHCONHNH 反应生成 ,
3 2 3 2
合成路线为 。
五、制备高锰酸钾(本题共20分)
已知:锰酸钾(KMnO )在强碱性溶液中稳定,溶液呈绿色。在酸性、中性和弱碱性环境下,MnO 2-会
2 4 4
发生歧化反应。方法一:CO 歧化法制备高锰酸钾,工艺流程如下:
2
20℃时下列各物质溶解度如下表。
物质 KMnO KCO KSO KHCO
4 2 3 2 4 3
溶解度(g/100g水,20℃) 6.38 111 11.1 33.7
溶解度(g/100g水,60℃) 45.2 126 18.2 60
1.操作Ⅱ是将混合液 、 、过滤。
2.操作Ⅰ对应的化学方程式为3KMnO +CO =2KMnO + MnO ↓+2K CO,不能通入过多CO 的原因
2 4 2 4 2 2 3 2
是 。
方法二:利用Cl 氧化KMnO 浓强碱溶液制备KMnO 的装置如下图所示(加热、夹持装置略):
2 2 4 4
3.仪器a的名称为 ,d中的溶液是 。
4.单向阀的作用是 ,当仪器B中 即停止通氯气。
5.当B中反应结束,后续操作是熄灭A处酒精灯, ,冷却后拆除装置。
6.上述装置存在一处缺陷,会导致KMnO 产率降低,改进的方法是 。
4
7.某兴趣小组同学用0.1000mol·L-1的酸性高锰酸钾标准溶液滴定某过氧化氢试样,反应原理为
5HO+2MnO-+6H+=2Mn2++5 O↑+8H O。用移液管移取25.00mL试样置于锥形瓶中,重复滴定四次,每次
2 2 4 2 2
消耗酸性高锰酸钾标准溶液的体积如表所示:
第一次 第二次 第三次 第四次
V(KMnO 溶液)/mL 17.30 17.90 18.00 18.10
2 4
(1)滴定终点的现象为 。
(2)计算试样中过氧化氢的浓度为 mol·L-1。【答案】1.蒸发浓缩(1分) 冷却结晶(1分)
2.CO 通入过多,生成KHCO ,KHCO 与KMnO 溶解度相差较少,部分与KMnO 一起析出,造成
2 3 3 4 4
产物纯度较低(2分)
3.恒压滴液漏斗(2分) NaOH溶液(2分)
4.防止倒吸(2分) 溶液由绿色完全转变为紫红色(2分)
5.打开弹簧夹,通入空气(或N) (2分)
2
6.在A、B之间增加盛有饱和食盐水的洗气瓶(2分)
7.(1)滴入最后半滴KMnO 标准溶液,溶液由无色变为浅紫红色且半分钟内不褪色(2分)
2 4
(2)0.1800(2分)
【解析】方法一:CO 歧化法制备高锰酸钾,反应原理为3KMnO +CO =2KMnO + MnO ↓+2K CO,
2 2 4 2 4 2 2 3
操作Ⅰ为过滤,得到高锰酸钾和碳酸钾的混合溶液,高锰酸钾溶解度受温度影响较大,则可通过降温结晶
的方法提纯高锰酸钾;
方法二:装置A中浓盐酸和二氧化锰共热制取氯气,生成的氯气通入装置B中与KMnO 浓强碱溶液
2 4
反应制备KMnO ,反应原理为Cl+2K MnO =2KCl+2KMnO ,氯气有毒,不能排放到空气中,装置C用于
4 2 2 4 4
尾气处理。
1.操作Ⅱ是提纯高锰酸钾,由表中数据可知,高锰酸钾溶解度受温度影响较大,碳酸钾溶解度受温
度影响不大,因此可通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥的方法提纯高锰酸钾;
2.CO 歧化法制备高锰酸钾生成的产物含有碳酸钾,若通入过多CO 则会生成KHCO ,KHCO 与
2 2 3 3
KMnO 溶解度相差较少,部分与KMnO 一起析出,造成产物纯度较低;
4 4
3.仪器a的名称为恒压滴液漏斗;d中溶液用于吸收氯气,则为NaOH溶液;
4.单向阀只允许气体从左流向右,能起到防倒吸的作用;KMnO 浓强碱溶液为绿色,高锰酸钾溶液
2 4
为紫色,当溶液由绿色完全转变为紫红色时,反应完全,停止通氯气;
5.装置中还有残留的氯气,为防止拆装置时装置中残留的氯气污染空气,熄灭酒精灯后,要打开弹
簧夹,通入空气(或N),将装置中残留的氯气赶入装置C中,待冷却后拆除装置;
2
6.装置A中产生的氯气中混有氯化氢,氯化氢会与装置B中的强碱发生反应,使得溶液碱性减弱,
会导致KMnO 产率降低,因此改进方法为:在A、B之间增加盛有饱和食盐水的洗气瓶,以除去氯气中的
4
氯化氢。
7.(1)该实验是酸性高锰酸钾标准溶液滴定试样中的过氧化氢,发生反应:2 MnO -
4
+5H O+6H+=2Mn2++8H O+5O↑,若达到滴定终点,高锰酸钾恰好完全反应,故滴定达到终点的现象是滴
2 2 2 2
入最后半滴KMnO 标准溶液,溶液由无色变为浅紫红色且半分钟内不褪色;(2)由于第一次数据误差过大,
2 4
故舍去;其他三组数据的平均值18.00mL,根据反应2 MnO -+5H O+6H+=2Mn2++8H O+5O↑,
4 2 2 2 2n(H O)=2.5×n(MnO -)=2.5×0.1000mol∙L-1×0.018L,c(HO)= mol∙L-1=0.1800mol∙L-1。
2 2 4 2 2