文档内容
2023 年邵阳市高三第二次联考试题卷
化 学
本试卷共 页, 个小题。 满分 分。 考试用时 分钟。
8 18 100 75
注意事项:
. 答卷前,考生务必将自己的姓名、班级、考号填写在答题卡上。 将条形码
1
横贴在答题卡上“条形码粘贴区”。
. 作答选择题时,选出每小题答案后,用 B 铅笔在答题卡上对应题目选项
2 2
的答案信息点涂黑;如需改动,用橡皮擦干净后,再选涂其他答案。 答案
不能答在试卷上。
. 非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卡各
3
题目指定区域内相应位置上;如需改动,先划掉原来的答案,然后再写上
新答案;不准使用铅笔和涂改液。 不按以上要求作答无效。
. 保持答题卡的整洁。 考试结束后,只交答题卡,试题卷自行保存。
4
可能用到的相对原子质量:H— O— Al— S— Cl— . Ti—
1 16 27 32 35 5 48
Ni— Ba—
59 137
一、选择题:本题共 小题,每小题 分,共 分。 在每小题给出的四个选项
14 3 42
中,只有一项是符合题目要求的。
. 化学与生活 生产及环境密切相关 下列说法错误的是
1 、 。
A. “北溪”管道输送的天然气主要成分是烷烃,其中己烷占绝大多数
B. 用 CO 人工合成淀粉,有利于减少农药、化肥污染和促进“碳中和”
2
C. “自古书契多编以竹简,其用缣帛者(丝织品)谓之为纸”,文中“纸”的主要
成分是蛋白质
D. 我国气象探测气球可飞入 万米以上高空,气球内充有氦气,含 个中子的
3 2
氦原子可表示为 He
4
2
. 下列化学用语或图示表达错误的是
2
··
A. NaOH 的电子式为 Na+[ O H]- B. HClO 的结构式为 H O Cl
∶··∶
C. 乙醇的分子式为 C H OH D. 氯离子的结构示意图为
2 5
. 实验室制取少量 NH 下列方法不能达到目的的是
3 3,
A. 加热分解氯化铵固体
B. 加热分解浓氨水
C. 将浓氨水滴入到碱石灰上
D. 加热氯化铵和氢氧化钙的固体混合物
年邵阳市高三第二次联考试题卷(化学) 第 页(共 页)
2023 1 8. 下列有关说法正确的是
4
A. SO 中 S 原子价层电子对数为
2 2
B. 基态 Mn 2+ 的核外电子排布式为[Ar] d 5
3
C. 丁烯的结构简式为 CH CH—CH CH
2- 2 2
D. 基态氧原子核外电子轨道表达式为
. 短周期主族元素 R X Y M 原子序数依次增大 Y 为地壳中含量最高的元素
5 、 、 、 , ,
M 与 Y 元素不同周期且 M 原子的核外未成对电子数为 由 R X Y M 组成
1, 、 、 、
的物质结构式如图所示 下列说法错误的是
。
A. XY 2- 的空间结构为平面三角形
3
B. M 的最高价氧化物对应的水化物为强酸
C. 该化合物中 X 原子最外层均满足 e- 结构
8
D. Y 元素所在周期中,第一电离能大于 Y 的元素有 种
2
. 下列方程式与所给事实相符的一项是
6
A. Na O 吸收 SO 气体: Na O SO Na SO O
2 2 2 2 2 2 +2 2 2 2 3 + 2
B. 明矾水溶液中加 Ba(OH) 溶液至沉淀的质量最大时:
2
2
Al 3+
+6
OH-
+3
Ba 2+
+3
SO 2
4
-
2
Al(OH)
3↓+3
BaSO
4↓
C. H S 溶液中通入 Cl ,生成黄色沉淀:H S Cl S HCl
2 2 2 + 2 ↓+2
D. 在稀硝酸中加入过量铁粉:Fe H+ NO- Fe 3+ NO H O
+4 + 3 + ↑+2 2
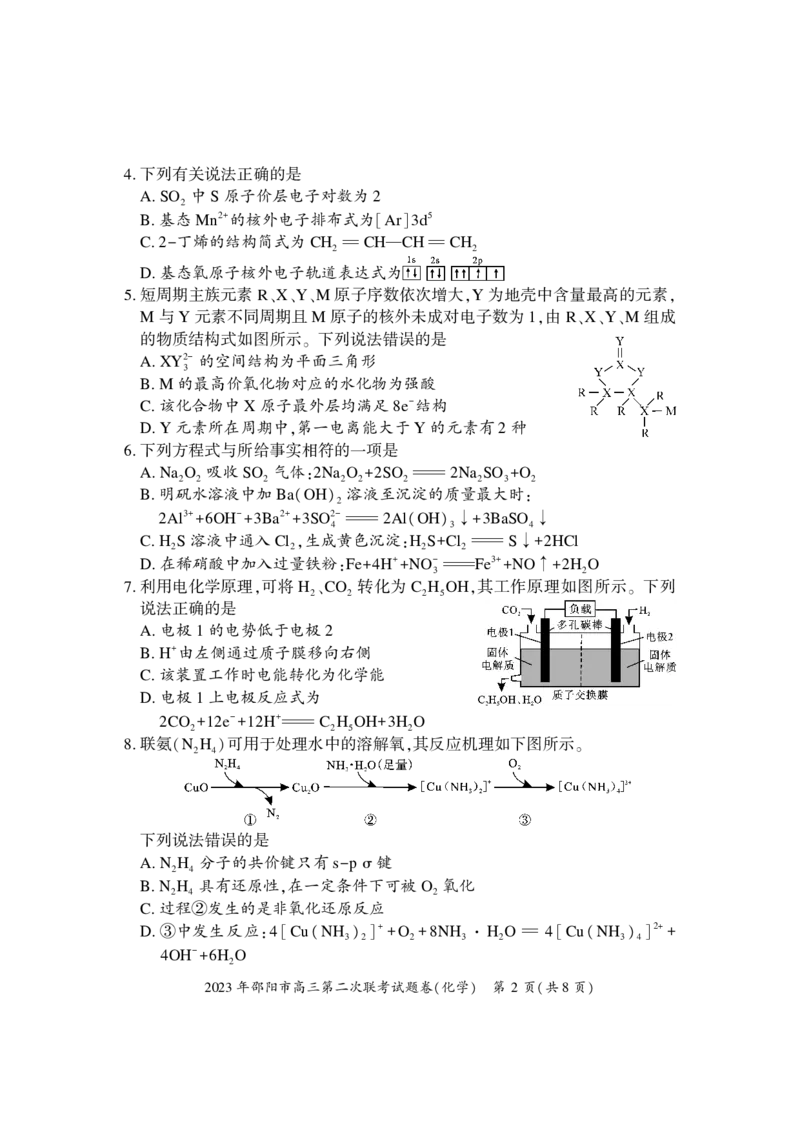
. 利用电化学原理 可将 H CO 转化为 C H OH 其工作原理如图所示 下列
7 , 2、 2 2 5 , 。
说法正确的是
A. 电极 的电势低于电极
1 2
B. H+ 由左侧通过质子膜移向右侧
C. 该装置工作时电能转化为化学能
D. 电极 上电极反应式为
1
CO e- H+ C H OH H O
2 2 +12 +12 2 5 +3 2
. 联氨 N H 可用于处理水中的溶解氧 其反应机理如下图所示
8 ( 2 4) , 。
下列说法错误的是
A. N H 分子的共价键只有 s p 键
2 4 - σ
B. N H 具有还原性,在一定条件下可被 O 氧化
2 4 2
C. 过程 发生的是非氧化还原反应
②
D. 中发生反应: [Cu(NH ) ]+ O NH ·H O [Cu(NH ) ]2+
③ 4 3 2 + 2 +8 3 2 4 3 4 +
OH- H O
4 +6 2
年邵阳市高三第二次联考试题卷(化学) 第 页(共 页)
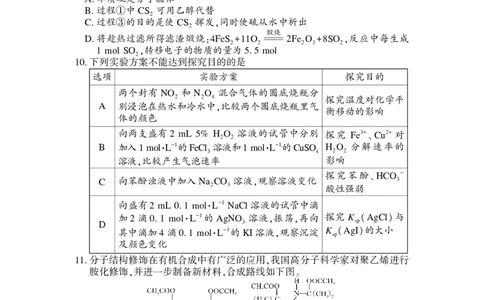
2023 2 8. 某化学兴趣小组设计一种从硫矿石 主要成分为硫黄及少量 FeS 中提取硫
9 ( 2)
黄的方法如下
:
查阅资料 S 的熔点为 . ℃ CS 的沸点为 . ℃
: 115 2 ; 2 46 2 。
下列说法错误的是
A. 单质硫是分子晶体
B. 过程 中 CS 可用乙醇代替
C. 过程 ① 的目的2是使 CS 挥发,同时使硫从水中析出
③ 2 煅烧
D. 将趁热过滤所得滤渣煅烧: FeS O Fe O SO ,反应中每生成
mol SO ,转移电子的物质 4 的量2为 +11 . 2 m o l 2 2 3 +8 2
. 下 1 列实验方2案不能达到探究目的的是 5 5
10
选项 实验方案 探究目的
两个封有 NO 和 N O 混合气体的圆底烧瓶分
探究温度对化学平
2 2 4
A 别浸泡在热水和冷水中,比较两个圆底烧瓶里气
衡移动的影响
体的颜色
向两支盛有 mL % H O 溶液的试管中分别 探究 Fe 3+、Cu 2+ 对
2 5 2 2
B 加入 mol·L-1 的FeCl 溶液和 mol·L-1 的CuSO H O 分解速率的
1 3 1 4 2 2
溶液,比较产生气泡速率 影响
探究苯酚、HCO
-
C 向苯酚浊液中加入 Na CO 溶液,观察溶液变化
3
2 3 酸性强弱
向盛有 mL . mol·L-1 NaCl 溶液的试管中滴
2 0 1
D 加 其中 2 滴 滴加 0 . 1 滴 mol· . L - m 1 的 ol· A L g -1 N 的 O 3 K 溶 I 溶 液 液 ,振 ,观 荡 察 ,再 沉 向 淀 探 K sp 究 (A K g s I p ) ( 的 Ag 大 C 小 l)与
4 0 1
及颜色变化
.分子结构修饰在有机合成中有广泛的应用 我国高分子科学家对聚乙烯进行
11 ,
胺化修饰 并进一步制备新材料 合成路线如下图
, , 。
下列说法正确的是
A. a 分子的核磁共振氢谱有 组峰
4
B. 生成高分子 b 的反应为加聚反应
C. a 分子中含有 个手性碳原子
2
D. 高分子 c 的水溶性比聚乙烯的水溶性好
年邵阳市高三第二次联考试题卷(化学) 第 页(共 页)
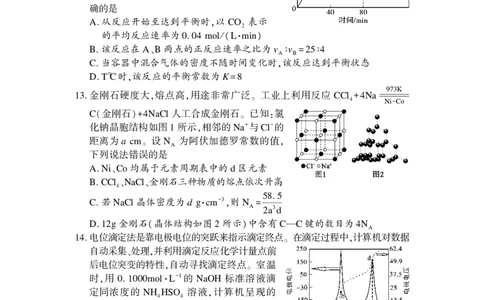
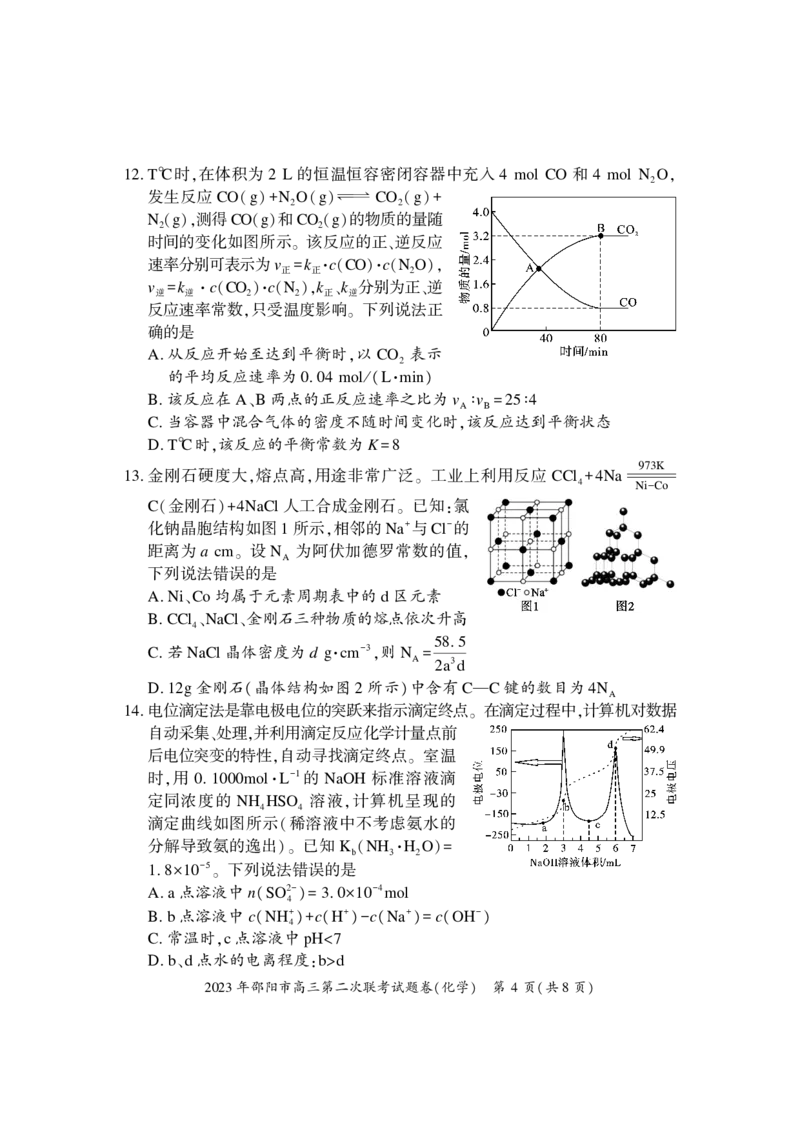
2023 3 8. T℃时 在体积为 L 的恒温恒容密闭容器中充入 mol CO 和 mol N O
12 , 2 4 4 2 ,
发生反应 CO g N O g CO g
( )+ 2 ( ) 2( )+
N g 测得CO g 和CO g 的物质的量随
2( ), ( ) 2( )
时间的变化如图所示 该反应的正 逆反应
。 、
速率分别可表示为v k c CO c N O
正= 正·( )·( 2 ),
v k c CO c N k k 分别为正 逆
逆= 逆· ( 2)·( 2), 正、 逆 、
反应速率常数 只受温度影响 下列说法正
, 。
确的是
A. 从反应开始至达到平衡时,以 CO 表示
2
的平均反应速率为 . mol/(L·min)
0 04
B. 该反应在 A、B 两点的正反应速率之比为 v v
A ∶ B=25∶4
C. 当容器中混合气体的密度不随时间变化时,该反应达到平衡状态
D. T℃时,该反应的平衡常数为 K
=8
K
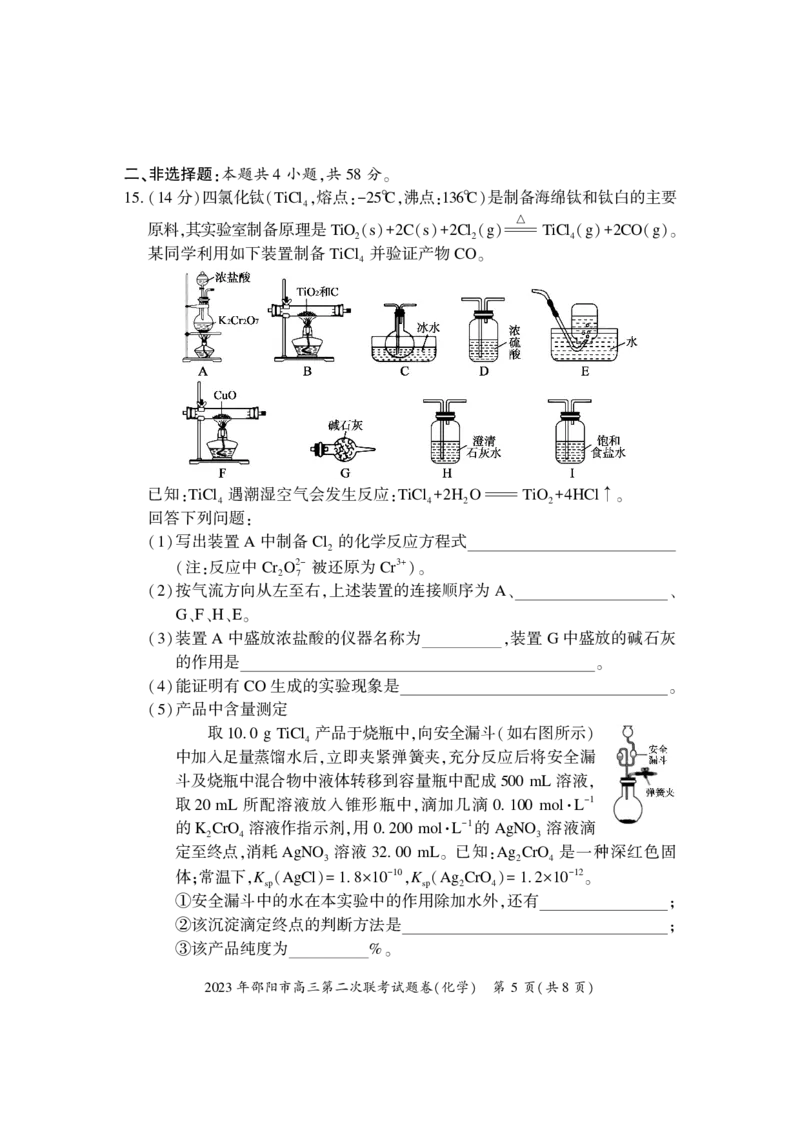
. 金刚石硬度大 熔点高 用途非常广泛 工业上利用反应 CCl Na 973
13 , , 。 4 +4 Ni Co
-
C 金刚石 NaCl 人工合成金刚石 已知 氯
( )+4 。 :
化钠晶胞结构如图 所示 相邻的Na+与Cl-的
1 ,
距离为 a cm 设 N 为阿伏加德罗常数的值
。 A ,
下列说法错误的是
A. Ni、Co 均属于元素周期表中的 d 区元素
B. CCl 、NaCl、金刚石三种物质的熔点依次升高
4
.
C. 若 NaCl 晶体密度为 d g·cm-3,则 N 58 5
A=
a d
3
2
D. g 金刚石(晶体结构如图 所示)中含有 C—C 键的数目为 N
12 2 4 A
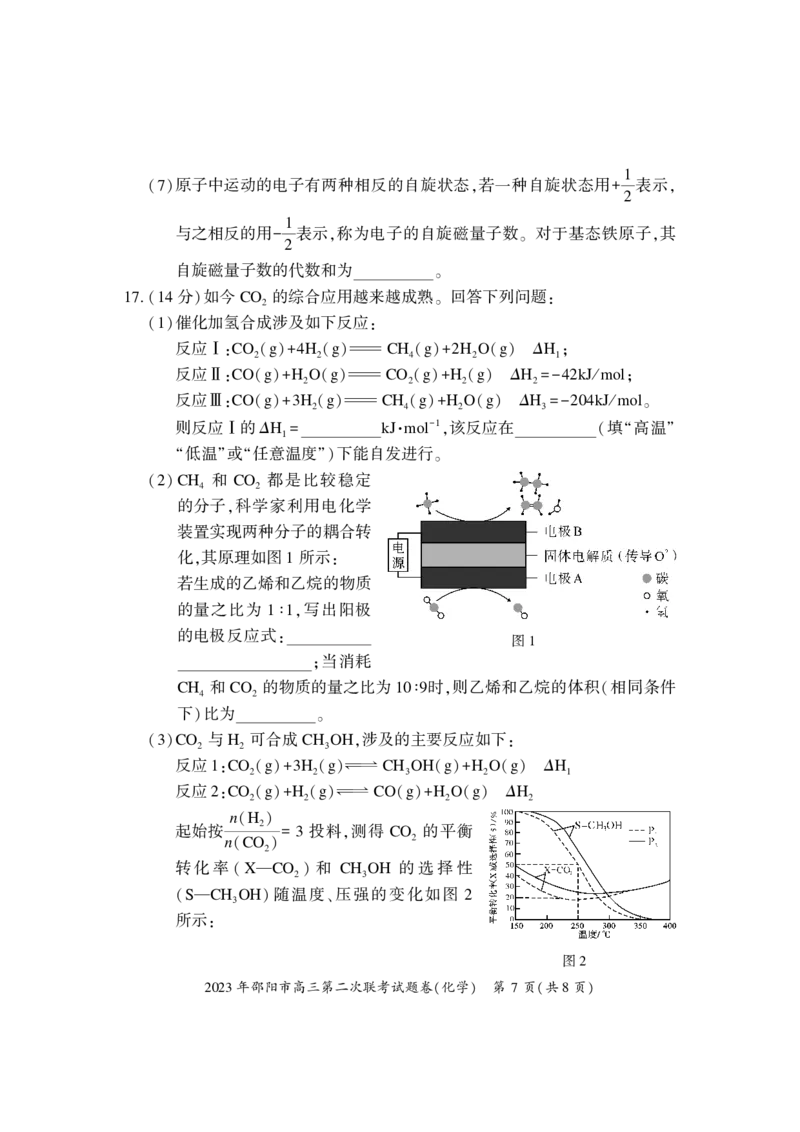
. 电位滴定法是靠电极电位的突跃来指示滴定终点 在滴定过程中 计算机对数据
14 。 ,
自动采集 处理 并利用滴定反应化学计量点前
、 ,
后电位突变的特性 自动寻找滴定终点 室温
, 。
时 用 . mol L-1 的 NaOH 标准溶液滴
, 0 1000 ·
定同浓度的 NH HSO 溶液 计算机呈现的
4 4 ,
滴定曲线如图所示 稀溶液中不考虑氨水的
(
分解导致氨的逸出 已知 K NH H O
)。 b( 3· 2 )=
. -5 下列说法错误的是
1 8×10 。
A. a 点溶液中 n(SO 2-) . -4 mol
4 = 3 0×10
B. b 点溶液中 c(NH+) c(H+) c(Na+) c(OH-)
+ - =
4
C. 常温时,c 点溶液中 pH
<7
D. b、d 点水的电离程度:b d
>
年邵阳市高三第二次联考试题卷(化学) 第 页(共 页)
2023 4 8二、非选择题:本题共 小题,共 分。
4 58
. 分 四氯化钛 TiCl 熔点 ℃ 沸点 ℃ 是制备海绵钛和钛白的主要
15 (14 ) ( 4, :-25 , :136 )
原料 其实验室制备原理是 TiO s C s Cl g △ TiCl g CO g
, 2( )+2 ( )+2 2( ) 4( )+2 ( )。
某同学利用如下装置制备 TiCl 并验证产物 CO
4 。
已知 TiCl 遇潮湿空气会发生反应 TiCl H O TiO HCl
: 4 : 4 +2 2 2 +4 ↑。
回答下列问题
:
写出装置 A 中制备 Cl 的化学反应方程式
(1) 2
注 反应中 Cr O 2- 被还原为 Cr 3+
( : 2 7 )。
按气流方向从左至右 上述装置的连接顺序为 A
(2) , 、 、
G F H E
、 、 、 。
装置 A 中盛放浓盐酸的仪器名称为 装置 G 中盛放的碱石灰
(3) ,
的作用是
。
能证明有 CO 生成的实验现象是
(4) 。
产品中含量测定
(5)
取 . g TiCl 产品于烧瓶中 向安全漏斗 如右图所示
10 0 4 , ( )
中加入足量蒸馏水后 立即夹紧弹簧夹 充分反应后将安全漏
, ,
斗及烧瓶中混合物中液体转移到容量瓶中配成 mL 溶液
500 ,
取 mL 所配溶液放入锥形瓶中 滴加几滴 . mol L-1
20 , 0 100 ·
的K CrO 溶液作指示剂 用 . mol L-1 的 AgNO 溶液滴
2 4 , 0 200 · 3
定至终点 消耗 AgNO 溶液 . mL 已知 Ag CrO 是一种深红色固
, 3 32 00 。 : 2 4
体 常温下 K AgCl . -10 K Ag CrO . -12
; , sp( )= 1 8×10 , sp( 2 4)= 1 2×10 。
安全漏斗中的水在本实验中的作用除加水外 还有
① , ;
该沉淀滴定终点的判断方法是
② ;
该产品纯度为 %
③ 。
年邵阳市高三第二次联考试题卷(化学) 第 页(共 页)
2023 5 8. 分 某废镍催化剂的主要成分是 Ni Al 合金 还含有少量 Cr Fe 及不溶
16 (15 ) — , 、
于酸碱的有机物 采用如下工艺流程回收其中的镍 制备镍的氧化物
。 ,
Ni O
( x y)。
回答下列问题
:
碱浸 时发生的主要反应离子方程式为
(1)“ ” 。
溶解 后的溶液中 所含金属离子有 Cr 3+ Fe 2+ Na+ Ni 2+
(2)“ ” , 、 、 、 、 。
在空气中煅烧 NiCO 其热重曲线如图
(3) 3, 1
所示 ℃时 NiCO 转化为 Ni O
,300~400 3 2 3,
反应的化学方程式为
;
℃ 生成的固体产物的化学式
400~ 450
为
。
工业上可用电解法制取 Ni O 用 NaOH
(4) 2 3。
溶液调节 NiCl 溶液 pH 至 . 加入适量硫酸钠后采用惰性电极进行电
2 7 5,
解 电解过程中产生的 Cl 有 %在弱碱性条件下生成 ClO- 再把二价
。 2 80 ,
镍氧化为三价镍 写出 ClO-氧化 Ni OH 生成 Ni O 的离子方程式
。 ( )2 2 3
a mol 二价镍全部转化为三价镍时
, ,
外电路中通过的电子的物质的量为 mol 假设电解时阳极只考
(
虑 Cl-放电
)。
金属镍的配合物 Ni CO 的中心原子的价电子数与配体提供的成键电
(5) ( )n
子总数之和为 则 n CO 与 N 结构相似 CO 分子内 键
18, = ; 2 , σ
与 键个数之比为
π 。
NiO 的晶胞结构如图 所示 其中离子坐标参
(6) 2 ,
数 A 为 C 为 1 1 则 B 的离子
(0,0,0), (1, , ),
2 2
坐标参数为
。
年邵阳市高三第二次联考试题卷(化学) 第 页(共 页)
2023 6 8原子中运动的电子有两种相反的自旋状态 若一种自旋状态用 1表示
(7) , + ,
2
与之相反的用 1表示 称为电子的自旋磁量子数 对于基态铁原子 其
- , 。 ,
2
自旋磁量子数的代数和为
。
. 分 如今 CO 的综合应用越来越成熟 回答下列问题
17 (14 ) 2 。 :
催化加氢合成涉及如下反应
(1) :
反应 CO g H g CH g H O g ΔH
Ⅰ: 2( )+4 2( ) 4( )+2 2 ( ) 1;
反应 CO g H O g CO g H g ΔH kJ/mol
Ⅱ: ( )+ 2 ( ) 2( )+ 2( ) 2 =-42 ;
反应 CO g H g CH g H O g ΔH kJ/mol
Ⅲ: ( )+3 2( ) 4( )+ 2 ( ) 3 =-204 。
则反应 的 ΔH kJ mol-1 该反应在 填 高温
Ⅰ 1 = · , ( “ ”
低温 或 任意温度 下能自发进行
“ ” “ ”) 。
CH 和 CO 都是比较稳定
(2) 4 2
的分子 科学家利用电化学
,
装置实现两种分子的耦合转
化 其原理如图 所示
, 1 :
若生成的乙烯和乙烷的物质
的量之比为 写出阳极
1 ∶1,
的电极反应式
图
:
1
当消耗
;
CH 和 CO 的物质的量之比为 时 则乙烯和乙烷的体积 相同条件
4 2 10∶9 , (
下 比为
) 。
CO 与 H 可合成 CH OH 涉及的主要反应如下
(3) 2 2 3 , :
反应 CO g H g CH OH g H O g ΔH
1: 2( )+3 2( ) 3 ( )+ 2 ( ) 1
反应 CO g H g CO g H O g ΔH
2: 2( )+ 2( ) ( )+ 2 ( ) 2
n H
起始按 ( 2) 投料 测得 CO 的平衡
n CO = 3 , 2
( 2)
转化率 X CO 和 CH OH 的选择性
( — 2) 3
S CH OH 随温度 压强的变化如图
( — 3 ) 、 2
所示
:
图
2
年邵阳市高三第二次联考试题卷(化学) 第 页(共 页)
2023 7 8n 转化为 CH OH 的 CO
已知 S CH OH ( 3 2) %
[ — 3 = n 转化的 CO ×100 ]
( 2)
p p 填 或
① 1 2( “>” “<”);
温度高于 ℃后 压强 p 和 p 下 CO 的平衡转化率几乎交于一点
② 350 , 1 2 , 2
的原因是
;
℃ 压强 p 下 用各物质的平衡分压代替物质的量浓度表示反应
③250 、 1 , 2
的平衡常数 K 结果保留 位有效数字
p= ( 2 )。
. 分 一种治疗糖尿病药物的合成路线如下 部分反应条件已省略
18 (15 ) ( )。
回答下列问题
:
有机物 I 中含氧官能团的名称为
(1) 、 。
反应 反应 的反应类型分别是
(2) ③、 ⑤ 、 。
反应 的化学方程式为
(3) ② 。
H 是一种氨基酸 其结构简式为 其本身发生聚
(4) , ,
合反应 所得高分子化合物的结构简式为
, 。
符合下列条件的 E 的同分异构体有 种 其中核磁共振氢谱有
(5) ,
组峰 且峰面积之比为 的结构简式为
5 , 6∶2∶2∶1∶1 。
属于芳香族化合物且苯环上有 个取代基
① 3 ;
既可发生银镜反应 又可发生水解反应
② , 。
设计以甲醛 甲苯为起始原料制备 COOCH CH
(6) 、 2 3
的合成路线 无机试剂任用
: ( )。
年邵阳市高三第二次联考试题卷(化学) 第 页(共 页)
2023 8 8