文档内容
巴蜀中学 2023 届高考适应性月考卷(二)
化学参考答案
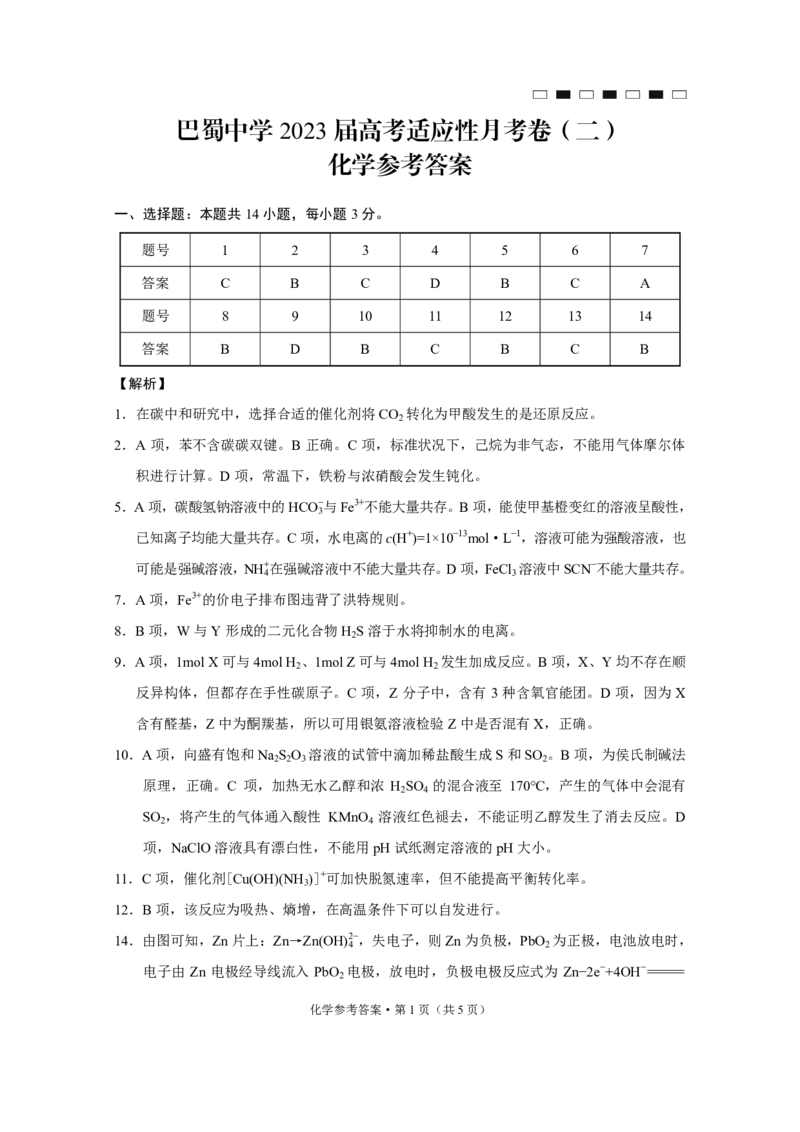
一、选择题:本题共14小题,每小题3分。
题号 1 2 3 4 5 6 7
答案 C B C D B C A
题号 8 9 10 11 12 13 14
答案 B D B C B C B
【解析】
1.在碳中和研究中,选择合适的催化剂将CO 转化为甲酸发生的是还原反应。
2
2.A 项,苯不含碳碳双键。B 正确。C 项,标准状况下,己烷为非气态,不能用气体摩尔体
积进行计算。D项,常温下,铁粉与浓硝酸会发生钝化。
5.A项,碳酸氢钠溶液中的HCO−与Fe3+不能大量共存。B项,能使甲基橙变红的溶液呈酸性,
3
已知离子均能大量共存。C项,水电离的c(H+)=1×10−13mol·L−1,溶液可能为强酸溶液,也
可能是强碱溶液,NH+在强碱溶液中不能大量共存。D项,FeCl 溶液中SCN−不能大量共存。
4 3
7.A项,Fe3+的价电子排布图违背了洪特规则。
8.B项,W与Y形成的二元化合物H S溶于水将抑制水的电离。
2
9.A项,1mol X可与4mol H 、1mol Z可与4mol H 发生加成反应。B项,X、Y均不存在顺
2 2
反异构体,但都存在手性碳原子。C 项,Z 分子中,含有 3 种含氧官能团。D 项,因为 X
含有醛基,Z中为酮羰基,所以可用银氨溶液检验Z中是否混有X,正确。
10.A项,向盛有饱和Na S O 溶液的试管中滴加稀盐酸生成S和SO 。B项,为侯氏制碱法
2 2 3 2
原理,正确。C 项,加热无水乙醇和浓 H SO 的混合液至 170℃,产生的气体中会混有
2 4
SO ,将产生的气体通入酸性 KMnO 溶液红色褪去,不能证明乙醇发生了消去反应。D
2 4
项,NaClO溶液具有漂白性,不能用pH试纸测定溶液的pH大小。
11.C项,催化剂[Cu(OH)(NH )]+可加快脱氮速率,但不能提高平衡转化率。
3
12.B项,该反应为吸热、熵增,在高温条件下可以自发进行。
14.由图可知,Zn片上:Zn→Zn(OH)2−,失电子,则Zn为负极,PbO 为正极,电池放电时,
4 2
电子由 Zn 电极经导线流入 PbO 电极,放电时,负极电极反应式为 Zn−2e−+4OH−=
2
化学参考答案·第1页(共5页)Zn(OH)2−。正极电极反应式为 PbO +SO2−+2e−+4H+=PbSO +2H O,充电逆向进行。
4 2 4 4 2
结合题给条件,放电后R区域电解质溶液浓度增加,负极消耗OH−,正极消耗H+,所以
M 区域为KOH,N区域为H SO ,R 区域为K SO 。综上,放电时,钾离子通过a向正
2 4 2 4
极移动,SO2−通过 b 向负极移动,所以 A 错误。B 正确。为放电时电极反应,C 错误。
4
消耗13g Zn,电子转移0.4mol,N区消耗0.8mol H+,0.2mol SO2−,同时有0.2mol SO2−移
4 4
向 R 区,则相当于减少 0.4mol H SO ,同时生成 0.4mol H O,则 R 区实际减少质量为
2 4 2
0.4mol×98g/mol−0.4mol×18g/mol=32g,D不正确。
二、非选择题:本题共4小题,共58分。
15.(除特殊标注外,每空1分,共14分)
(1)第四周期第Ⅷ族 4d2
(2)Mo、S(2分) 6mol
(3)MoO +2H+=MoO2++H O
3 2 2
(4)分液漏斗、烧杯(2分)
(5)H+、Al3+(2分) 硫酸 (c−10−5)2+0.8
△
(6)3CoC O +2O =====Co O +6CO (2分)
2 4 2 3 4 2
焙烧
【解析】(2)MoS 在高温条件下焙烧生成MoO 、SO ,反应的化学方程式为2MoS +7O =====
2 3 2 2 2
2MoO +4SO ,发生氧化反应的元素即化合价升高的是Mo、S。根据转移电子守恒,反应
3 2
中失电子总数等于1.5mol O 得电子总数,即6mol。
2
(4)操作Ⅰ是分液,所以用到的玻璃仪器为分液漏斗和烧杯。
(5)分析流程前后元素走向,Al3+存在于水相2中,H SO 过量,还存在H+。加入试剂X
2 4
的目的是反萃取Co2+,加入硫酸使平衡Co2++H R CoR+2H+逆移,便于反萃取Co2+。
2
依据 Co2++C O2− CoC O 计算溶液 NH+浓度可转化为先求得溶液中的 C O2−浓度,
2 4 2 4 4 2 4
分为沉淀中所需浓度及平衡中所需浓度进行计算。当 Co2+沉淀完全时,溶液中 c(Co2+)
=10−5mol/L,根据K =c(Co2+)·c(C O2−)=4×10−6,溶液中c(C O2−)至少为0.4mol/L,而沉
sp 2 4 2 4
淀消耗C O2−为(c−10−5)mol/L,则c(NH+)的浓度至少为(c−10−5)2+0.8mol/L。
2 4 4
147
(6)CoC O ·2H O 失去全部结晶水的质量为10.98 g8.82g,即加热到 210℃时,
2 4 2
183
8.82
固体物质是 CoC O 。根据元素守恒,n(CO ) 2mol0.12mol,质量为 0.12mol×
2 4 2
147
化学参考答案·第2页(共5页)44g·mol−15.28g,而固体质量减少为(8.824.82)g4.00g,说明有气体参加反应,即
1.28
氧气参加,氧气的质量为(5.284.00)g1.28g ,其物质的量为 mol0.04mol ,
32
8.82
n(CoC O )∶n(O )∶n(CO ) ∶0.04∶0.12 3∶2∶6,依据原子守恒,3CoC O +
2 4 2 2 2 4
147
△
2O =====Co O +6CO 。
2 3 4 2
16.(除特殊标注外,每空2分,共15分)
高温
(1)3Fe+4H O=====Fe O +4H 蒸发皿(1分)
2 3 4 2
(2)2Fe2++4OH−+H O =2FeOOH↓+2H O
2 2 2
(3)除去多余的H O ,防止其在后续步骤中继续氧化+2价铁元素 1.75(1分)
2 2
11∶7
(4)浓度较大时会超过标准曲线,误差较大
(5)FeO(1分) 94.16%
【解析】(3)由A转化为B时,为了将Fe(Ⅱ)全部氧化成Fe(Ⅲ),需要加入过量的H O ,
2 2
混合前需要加热除去 H O ,以免在混合 A和 B时将溶液中的 Fe(Ⅱ)氧化。根据图丙,
2 2
3
n(Fe) 7
R1.75时,Fe O 产率最高,此时R ,设滤液A中铁元素的物质的量为a mol,
3 4 2 4
n(Fe)
b 7 a 11
浊液B中铁元素的物质的量为b mol,则有 ,则n(A)∶n(B) 。
ab 4 b 7
(4)分光光度计是用来做微量或痕量测试的。当仪器的测定误差一定时,不同的透光率
位置对应的浓度误差是不同的。透光率在15%到65%之间,即吸光度在0.2到0.8之间测
定误差符合要求。如果浓度过大,测出来相对误差太大,是不符合要求的。
(5)依据反应 Cr O2−+6Fe2++14H+=2Cr3++6Fe3++7H O 可知,溶液中 n(Fe2+)=4mol/L
2 7 2
0.05L6=1.2mol,将步骤 2 得到的溶液配制成 1000mL 溶液,取该溶液 1.00mL,稀释
至25.6L,测得溶液的吸光度为0.7618,对应的Fe3+的含量为7mg/L,则25.6L稀释后的
溶液中 Fe3+的含量为 25.6L7mg/L=179.2mg=0.1792g,即 1mL 配制后的溶液中含 Fe3+
0.1792g,则 1000mL 配制后的溶液中含 Fe3+ 179.2g,经过步骤 2 之后所得溶液中铁离子
179.2g
Fe3+的物质的量为 3.2mol,若样品只有Fe O (FeO·Fe O ),根据Fe元素守恒,
3 4 2 3
56g/mol
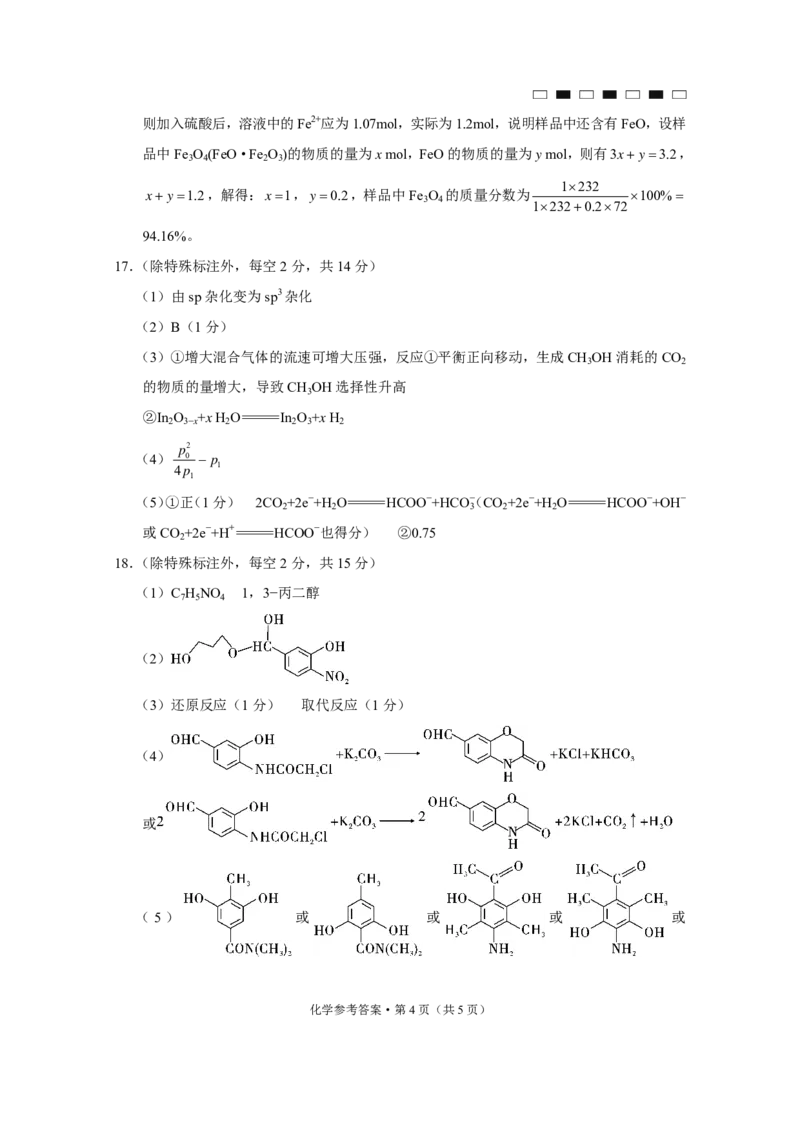
化学参考答案·第3页(共5页)则加入硫酸后,溶液中的Fe2+应为1.07mol,实际为1.2mol,说明样品中还含有FeO,设样
品中Fe O (FeO·Fe O )的物质的量为x mol,FeO的物质的量为y mol,则有3x y3.2,
3 4 2 3
1232
x y1.2,解得:x1,y0.2,样品中Fe O 的质量分数为 100%
3 4
12320.272
94.16%。
17.(除特殊标注外,每空2分,共14分)
(1)由sp杂化变为sp3杂化
(2)B(1分)
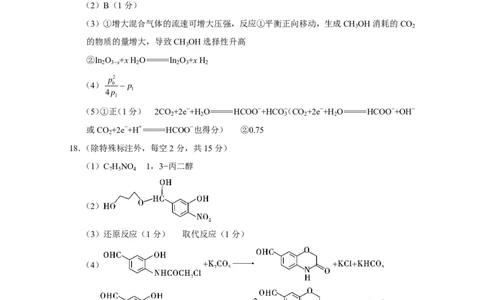
(3)①增大混合气体的流速可增大压强,反应①平衡正向移动,生成CH OH消耗的CO
3 2
的物质的量增大,导致CH OH选择性升高
3
②In O +x H O=In O +x H
2 3−x 2 2 3 2
p2
(4) 0 p
4p 1
1
(5)①正(1分) 2CO +2e−+H O=HCOO−+HCO(− CO +2e−+H O=HCOO−+OH−
2 2 3 2 2
或CO +2e−+H+=HCOO−也得分) ②0.75
2
18.(除特殊标注外,每空2分,共15分)
(1)C H NO 1,3−丙二醇
7 5 4
(2)
(3)还原反应(1分) 取代反应(1分)
(4)
或
( 5 ) 或 或 或 或
化学参考答案·第4页(共5页)或 或 或
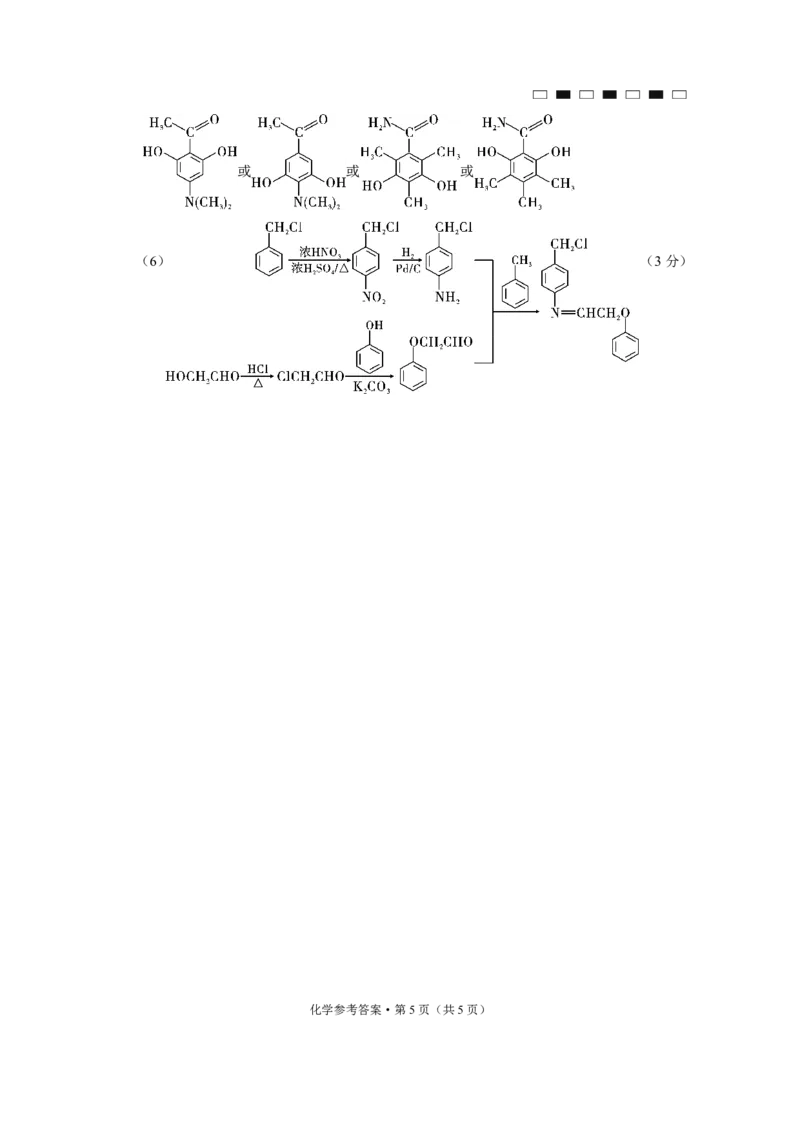
(6) (3分)
化学参考答案·第5页(共5页)