文档内容
微专题40 氧化还原滴定与沉淀滴定的相关计算
1.(2023·浙江·统考高考真题)某研究小组用铝土矿为原料制备絮凝剂聚合氯化铝( )
按如下流程开展实验。
已知:①铝土矿主要成分为 ,含少量 和 。用 溶液溶解铝土矿过程中 转变为难
溶性的铝硅酸盐。
② 的絮凝效果可用盐基度衡量,盐基度
当盐基度为0.60~0.85时,絮凝效果较好。
请回答:
(1)步骤Ⅰ所得滤液中主要溶质的化学式是 。
(2)下列说法不正确的是___________。
A.步骤I,反应须在密闭耐高压容器中进行,以实现所需反应温度
B.步骤Ⅱ,滤液浓度较大时通入过量 有利于减少 沉淀中的杂质C.步骤Ⅲ,为减少 吸附的杂质,洗涤时需对漏斗中的沉淀充分搅拌
D.步骤Ⅳ中控制 和 的投料比可控制产品盐基度
(3)步骤V采用如图所示的蒸汽浴加热,仪器A的名称是 ;步骤V不宜用酒精灯直接加热的原
因是 。
(4)测定产品的盐基度。
的定量测定:称取一定量样品,配成溶液,移取 溶液于锥形瓶中,调 ,滴加指示
剂 溶液。在不断摇动下,用 标准溶液滴定至浅红色(有 沉淀),30秒
内不褪色。平行测试3次,平均消耗 标准溶液 。另测得上述样品溶液中
。
①产品的盐基度为 。
②测定 过程中溶液 过低或过高均会影响测定结果,原因是 。
2.(2023·湖北·统考高考真题)学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
(1)铜与浓硝酸反应的装置如下图,仪器A的名称为 ,装置B的作用为 。
(2)铜与过量 反应的探究如下:实验②中Cu溶解的离子方程式为 ;产生的气体为 。比较实验①和②,从氧化还原角度说
明 的作用是 。
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰
性氛围下加热,mgX完全分解为ng黑色氧化物Y, 。X的化学式为 。
(4)取含X粗品0.0500g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示剂,
用 标准溶液滴定,滴定终点时消耗 标准溶液15.00mL。(已知:
, )标志滴定终点的现象是 ,粗品中X的相对含量
为 。
指示剂选择:
氧化还原滴定法的指示剂有三类。①氧化还原指示剂;②专用指示剂,如在碘量法滴定中,可溶性淀粉溶
液遇碘标准溶液变蓝;③自身指示剂,如高锰酸钾标准溶液滴定草酸时,滴定终点为溶液由无色变为浅粉
红色。
滴定操作不仅适用于酸碱中和反应,也可迁移应用于氧化还原反应,NaOH、NaCO 混合溶液与盐酸的反
2 3
应及沉淀反应。
1.氧化还原滴定法
(1)原理:以氧化剂或还原剂为滴定剂,直接滴定一些具有还原性或氧化性的物质,或者间接滴定一些本身并没
有还原性或氧化性、但能与某些还原剂或氧化剂反应的物质。
(2)试剂:常用于滴定的氧化剂有KMnO 、KCr O 等;常用于滴定的还原剂有亚铁盐、草酸、维生素C等。
4 2 2 7(3)实例
①酸性KMnO 溶液滴定HC O 溶液
4 2 2 4
原理:2MnO+6H++5HC O===10CO ↑+2Mn2++8HO。
2 2 4 2 2
指示剂:酸性KMnO 溶液本身呈紫色,不用另外选择指示剂,当滴入最后一滴酸性KMnO 溶液后,溶液
4 4
由无色变浅红色,且半分钟内不褪色,说明达到滴定终点。
②NaSO 溶液滴定碘液
2 2 3
原理:2NaSO+I===Na SO+2NaI。
2 2 3 2 2 4 6
指示剂:用淀粉溶液做指示剂,当滴入最后一滴NaSO 溶液后,溶液的蓝色褪去,且半分钟内不恢复原
2 2 3
色,说明达到滴定终点。
2.沉淀滴定法
(1)概念:沉淀滴定是利用沉淀反应进行滴定、测量分析的方法。生成沉淀的反应很多,但符合条件的却很
少,实际上应用最多的是银量法,即利用Ag+与卤素离子的反应来测定Cl-、Br-、I-浓度。
(2)原理:沉淀滴定所用的指示剂本身就是一种沉淀剂,滴定剂与被滴定物反应的生成物的溶解度要比滴定
剂与指示剂反应的生成物的溶解度小,否则不能用这种指示剂。如用AgNO 溶液测定溶液中Cl-的含量时
3
常以CrO为指示剂,这是因为AgCl比Ag CrO 更难溶的缘故。
2 4
1.(2023·浙江·统考高考真题)草酸( )是二元弱酸。某小组做如下两组实验:
实验I:往 溶液中滴加 溶液。
实验Ⅱ:往 溶液中滴加 溶液。
[已知: 的电离常数 ,溶液混合后体积变化忽略不
计],下列说法正确的是
A.实验I可选用甲基橙作指示剂,指示反应终点
B.实验I中 时,存在
C.实验Ⅱ中发生反应
D.实验Ⅱ中 时,溶液中2.(2023·山东·统考高考真题)一定条件下,乙酸酐 醇解反应
可进行完全,利用此反应定量测定有机醇 中的羟
基含量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入 样品,充分反应后,加适量水使剩余乙酸酐完
全水解: 。
③加指示剂并用 甲醇标准溶液滴定至终点,消耗标准溶液 。
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用
甲醇标准溶液滴定至终点,消耗标准溶液 。对于上述实验,下列做法正确的是
A.进行容量瓶检漏时,倒置一次即可
B.滴入半滴标准溶液,锥形瓶中溶液变色,即可判定达滴定终点
C.滴定读数时,应单手持滴定管上端并保持其自然垂直
D.滴定读数时,应双手一上一下持滴定管
3.(2023·浙江·高考真题)某研究小组制备纳米 ,再与金属有机框架 )材料复合制备荧光材料
,流程如下:
已知:①含
锌组分间的转化关系:
② 是 的一种晶型, 以下稳定。
请回答:
(1)步骤Ⅰ,初始滴入 溶液时,体系中主要含锌组分的化学式是 。
(2)下列有关说法不正确的是___________。
A.步骤Ⅰ,搅拌的作用是避免反应物浓度局部过高,使反应充分B.步骤Ⅰ,若将过量 溶液滴入 溶液制备 ,可提高 的利用率
C.步骤Ⅱ,为了更好地除去杂质,可用 的热水洗涤
D.步骤Ⅲ,控温煅烧的目的是为了控制 的颗粒大小
(3)步骤Ⅲ,盛放样品的容器名称是 。
(4)用 和过量 反应,得到的沉淀可直接控温煅烧得纳米 ,沉淀无需洗涤的原
因是 。
(5)为测定纳米 产品的纯度,可用已知浓度的 标准溶液滴定 。从下列选项中选择合理的仪
器和操作,补全如下步骤[“___________”上填写一件最关键仪器,“(___________)”内填写一种操作,均用
字母表示]。
用___________(称量 样品 )→用烧杯(___________)→用___________(___________)→用移液管
(___________)→用滴定管(盛装 标准溶液,滴定 )
仪器:a、烧杯;b、托盘天平;c、容量瓶;d、分析天平;e、试剂瓶
操作:f、配制一定体积的Zn2+溶液;g、酸溶样品;h、量取一定体积的 溶液;i、装瓶贴标签
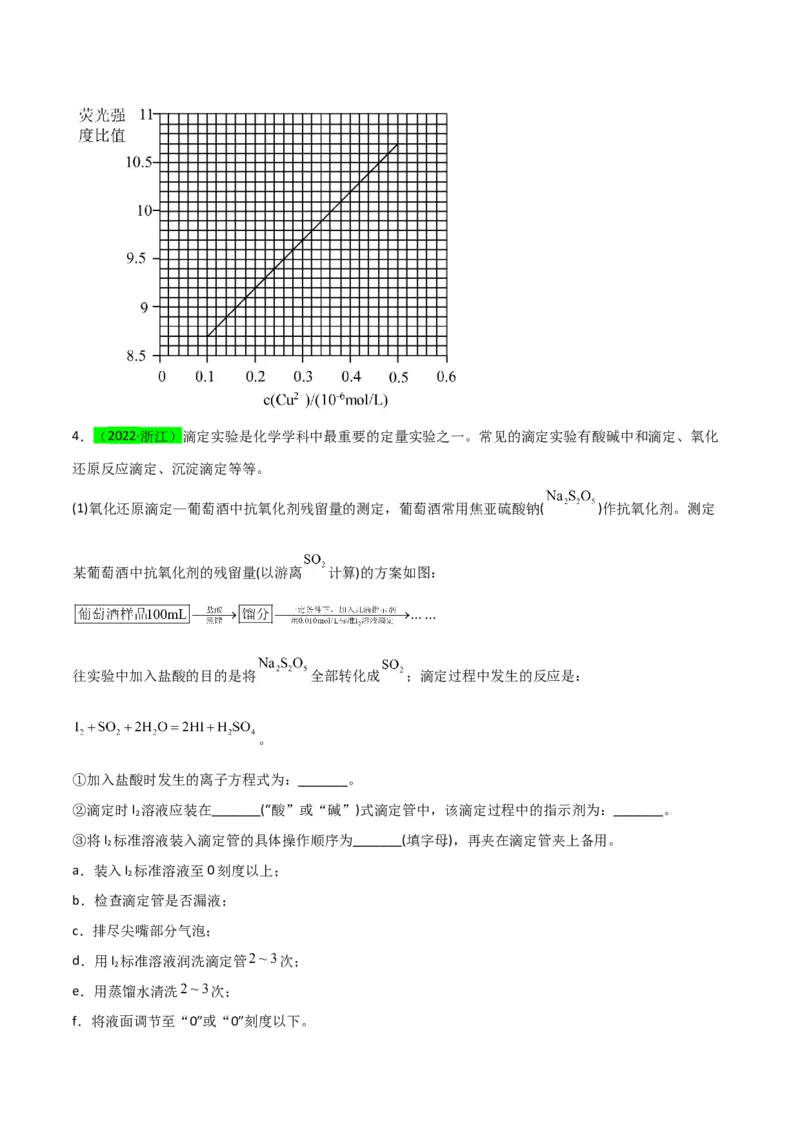
(6)制备的 荧光材料可测 浓度。已知 的荧光强度比值与 在一定浓度范围
内的关系如图。
某研究小组取 人血浆铜蓝蛋白(相对分子质量 ),经预处理,将其中 元素全部转化为
并定容至 。取样测得荧光强度比值为10.2,则1个血浆铜蓝蛋白分子中含 个铜原子。4.(2022·浙江)滴定实验是化学学科中最重要的定量实验之一。常见的滴定实验有酸碱中和滴定、氧化
还原反应滴定、沉淀滴定等等。
(1)氧化还原滴定—葡萄酒中抗氧化剂残留量的测定,葡萄酒常用焦亚硫酸钠( )作抗氧化剂。测定
某葡萄酒中抗氧化剂的残留量(以游离 计算)的方案如图:
往实验中加入盐酸的目的是将 全部转化成 ;滴定过程中发生的反应是:
。
①加入盐酸时发生的离子方程式为:_______。
②滴定时I 溶液应装在_______(“酸”或“碱”)式滴定管中,该滴定过程中的指示剂为:_______。
2
③将I 标准溶液装入滴定管的具体操作顺序为_______(填字母),再夹在滴定管夹上备用。
2
a.装入I 标准溶液至0刻度以上;
2
b.检查滴定管是否漏液;
c.排尽尖嘴部分气泡;
d.用I 标准溶液润洗滴定管 次;
2
e.用蒸馏水清洗 次;
f.将液面调节至“0”或“0”刻度以下。④实验消耗I 溶液 ,所测样品中抗氧化剂的残留量(以游离 计算)为_______ 。下列情形会
2
造成测定结果偏高的是:_______。
A.滴定持续时间稍长,溶液中部分 被空气氧化
B.滴定前平视,滴定后俯视
C.滴定前滴定管尖有气泡,滴定后气泡消失
D.盛装标准溶液的滴定管用蒸馆水洗净后,未润洗
(2)沉淀滴定——滴定剂与被滴定物生成的沉淀比滴定剂与指示剂生成的沉淀更难溶;且二者之间,有明显
的颜色差别。参考表中的数据,若用 滴定 溶液,可选用的指示剂是:_______(填选项字母)
A. B. C. D.
难溶物
颜色 白 浅黄 白 砖红 白
1.(2023·湖南娄底·统考模拟预测)某小组设计实验测定胆矾( )纯度(杂质不参与反应):称取
胆矾样品溶于蒸馏水,加入足量KI溶液,充分反应后,过滤。把滤液配制成250mL溶液,准确量取配
制溶液25.00mL于锥形瓶中,滴加2滴溶液X,用 溶液滴定至终点,消耗滴定液Vml。涉
及有关反应如下: , 。下列叙述正确的是A.X为甲基橙溶液
B.滴加 溶液时选择滴定管如图所示
C.滴定管装液之前最后一步操作是水洗
D.胆矾纯度为
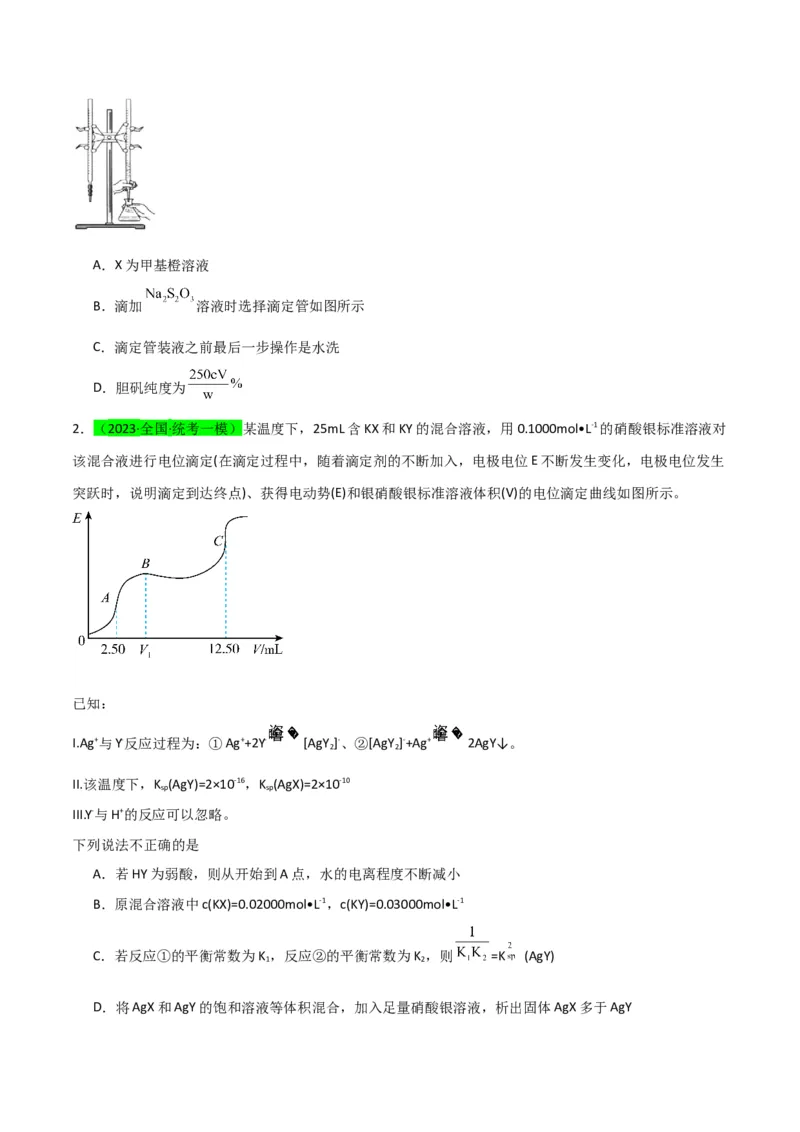
2.(2023·全国·统考一模)某温度下,25mL含KX和KY的混合溶液,用0.1000mol•L-1的硝酸银标准溶液对
该混合液进行电位滴定(在滴定过程中,随着滴定剂的不断加入,电极电位E不断发生变化,电极电位发生
突跃时,说明滴定到达终点)、获得电动势(E)和银硝酸银标准溶液体积(V)的电位滴定曲线如图所示。
已知:
I.Ag+与Y-反应过程为:①Ag++2Y- [AgY ]-、②[AgY ]-+Ag+ 2AgY↓。
2 2
II.该温度下,K (AgY)=2×10-16,K (AgX)=2×10-10
sp sp
III.Y-与H+的反应可以忽略。
下列说法不正确的是
A.若HY为弱酸,则从开始到A点,水的电离程度不断减小
B.原混合溶液中c(KX)=0.02000mol•L-1,c(KY)=0.03000mol•L-1
C.若反应①的平衡常数为K ,反应②的平衡常数为K ,则 =K (AgY)
1 2
D.将AgX和AgY的饱和溶液等体积混合,加入足量硝酸银溶液,析出固体AgX多于AgY3.(2023·山东·高三统考专题练习)实验室常用基准物质Na C O 标定KMnO 溶液的浓度。将Na C O 溶液
2 2 4 4 2 2 4
置于锥形瓶中,并加入稀硫酸,反应时温度不宜过高。为提高初始速率,常滴加几滴MnSO 溶液。下列说
4
法错误的是
A.应选用碱式滴定管量取Na C O 溶液
2 2 4
B.加MnSO 溶液的作用是做催化剂
4
C.若溶液温度过高、酸性过强,生成的草酸易分解,将导致结果偏高
D.已知 ,若初期滴加过快、温度过高,发生该反应,将导致结
果偏高
4.(2023·山东·高三统考专题练习)实验室测定反应 的平衡常数K的过程为:
①一定温度下,将 溶液与 溶液 等体积混合,产生灰黑色
沉淀;
②待步骤①中反应达到平衡时,取v mL上层清液,用 标准溶液滴定 ,至出现稳定的浅
红色时消耗KSCN标准溶液 。
资料: (白色) , (红色)
下列说法正确的是
A. 溶液可替换为 溶液
B.过程①中产生的灰黑色沉淀为Fe或Ag元素的氧化物
C.可用KCl标准溶液代替KSCN的标准溶液滴定
D.步骤②中不待溶液澄清,直接用浊液做滴定实验测定 ,则所测K值偏小
5.(2023·山东聊城·校联考三模)高纯三氯氧磷 是集成电路、太阳能电池生产的掺杂剂。实验室
可通过以下实验步骤测定三氯氧磷产品中氯元素的含量,并计算产品的纯度[已知:常温下,, , 呈白色]。
①取 产品置于盛 蒸馏水的水解瓶中,摇动至完全水解,将水解液配成 溶液并预处理
排除含磷粒子的影响。
②取 溶液于锥形瓶中,向其中加入 的 标准溶液 ,使 完全沉淀,再加入
硝基苯,振荡,使沉淀表面被有机物覆盖;然后加入几滴 溶液作指示剂,用
标准溶液滴定过量 至终点,所用体积为 。
假设杂质不参加反应,则下列说法正确的是
A.配制好的 标准溶液可盛放在棕色广口试剂瓶中
B.实验过程中可用甲苯代替硝基苯进行实验
C.滴定终点时锥形瓶中有血红色沉淀生成
D.实验过程中若忘记加入硝基苯,会导致所测 的含量偏低
6.(2023春·山东·高三校联考阶段练习)用c 酸性 溶液滴定 mL未知浓度的草酸溶液,
达到滴定终点时消耗滴定液xmL。下列说法正确的是
A.滴定终点时溶液由粉红色变为无色
B.需要锥形瓶、碱式滴定管
C.若用草酸溶液润洗锥形瓶,使测得结果偏低
D.测得草酸浓度
1.(2023·江西·校联考二模)硫脲[CS(NH ) ]在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制
2 2
备Ca(HS) ,再与CaCN 合成CS(NH ) ,实验装置(夹持及加热装置略)如图所示。
2 2 2 2已知:CS(NH ) 易溶于水,易被氧化,受热(150℃左右)时发生异构化生成NH SCN。
2 2 4
回答下列问题:
(1)仪器M名称 。
(2)实验前先检查装置气密性。检查气密性后加入药品,打开K ,装置B中盛装的试剂为 。反应结束
2
后关闭K ,打开K 通N 一段时间,目的是 。
2 2
(3)撤走搅拌器,打₁开K ,水浴加热D中三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温
度在80℃的原因是 ₃ ,D处合成硫脲的化学方程式为 。判断制备Ca(HS) 反应中H S已过量的
2 2
方法是
(4)将装置D中液体过滤后,结晶得到粗产品。
称取mg产品,加水溶解配成250mL溶液,量取50mL于锥形瓶中,滴加一定量的稀硫酸使溶液显酸性,用
c mol·L-1KMnO 标准溶液滴定,滴定至终点时消耗KMnO 标准溶液V mL。滴定时,硫脲发生反应的离子方
4 4
程式为: 5[CS(NH ) ] +14 +32H+= 14Mn2++5CO +5N +5 + 26H O 。则样品中硫脲的质量分数为
2 2 2 2 2
(用含“m、c、V”的最简式表示)。
已知:NH SCN、KSCN都易溶于乙醇、水,温度高时容易分解和氧化;常温下KSCN的溶解度为217g。利用
4
硫脲制备KSCN的方法是:取一定量硫脲在隔绝空气的条件下加热至150℃充分反应,将加热后的产物溶于
一定比例的无水乙醇和水中形成溶液, (填写操作过程),得到KSCN晶体。(实验中可选用试剂:
K CO 、无水乙醇。)
2 3
2.(2023·山东济宁·统考三模)亚硝酰氯(NOCl)是有机物合成中的重要试剂,熔点为-64.5℃、沸点
为-5.5℃,气态呈黄色,液态时呈红褐色,遇水易反应生成一种氢化物和两种氮的常见氧化物。NOCl可由
NO与Cl 在通常条件下反应得到,相关实验装置如图所示。
2回答下列问题:
(1)装置的连接顺序为a→ →h,实验时先打开分液漏斗活塞滴入稀硝酸,当观察到F中 时,
开始向装置中通入Cl 。
2
(2)装置D的作用有:根据气泡快慢调节气体流速、 、 。
(3)尾气处理装置中若用NaOH溶液只能吸收氯气和NOCl,不能吸收NO,经过查阅资料发现用高锰酸钾溶
液可以吸收NO气体,因此在氢氧化钠溶液中加入高锰酸钾,反应产生黑色沉淀,写出该反应的离子方程
式: 。
(4)制得的NOCl中可能含有少量N O 杂质,为测定产品纯度进行如下实验:
2 4
a.将所得亚硝酰氯(NOCl)产品7.0g溶于水,配制成250 mL溶液;取出25.00 mL,加入足量的30.00 mL0.5
mol/LAgNO 溶液,充分反应;
3
b.向其中加入少量硝基苯,使沉淀表面被有机物覆盖;
c.加入指示剂,用NH SCN标准溶液滴定过量的AgNO 溶液;
4 3
d.重复实验操作三次,消耗0.5 mol/LNH SCN溶液的体积平均为10.00 mL。
4
已知 ,
①加入硝基苯的作用是 。
②滴定选用的指示剂是 。
A.FeCl B.FeCl C.NH Fe(SO ) D.(NH ) Fe(SO )
3 2 4 4 2 4 2 4 2
③NOCl的纯度为 。
3.(2023·河北衡水·河北衡水中学校考模拟预测)硫代硫酸钠 是最重要的硫代硫酸盐,
易溶于水,不溶于乙醇, 熔化, 分解,具有较强的还原性和配位能力,是定量分析中的还原
剂和冲洗照相底片的定影剂。
I.制备硫代硫酸钠的一种方法: 。(1)请选择制备 的合适装置: (填序号),对应的制备原理的化学方程式为 。
(2)将制得的硫代硫酸钠晶体粗品纯化后,再干燥得到纯净的硫代硫酸钠晶体。干燥时温度不能超过 的
原因: 。
Ⅱ.硫代硫酸钠性质探究:
(3) 溶液 溶液迅速变为紫黑色 溶液颜色逐渐变浅最终呈浅绿色。
查资料知:
① (紫黑色) 快
② 慢
③ 慢
试结合已知条件从动力学角度解释溶液颜色变化的可能原因: 。
Ⅲ.硫代硫酸钠应用:
是实验室定量分析中的重要还原剂。为测定咸菜中亚硝酸根离子的含量(忽略硝酸根离子的干扰,
取 咸菜榨汁,收集榨出的液体,加入提取剂,过滤得到无色滤液,将该滤液稀释至体积为 ,取
稀释后的滤液与过量的稀硫酸和碘化钾溶液的混合液反应,再滴加几滴淀粉溶液,用 的
溶液进行滴定,共消耗 溶液的体积为 。
(4)若配制 的 溶液,需要称量 晶体。(5)①在碱式滴定管中装入 溶液后,要先排放滴定管尖嘴处的气泡,其正确的图示为 (填字
母)。
②该咸菜榨汁中亚硝酸根离子的含量为 (已知: ,
)。下列操作引起测量结果偏高的是 (填字母)。
A.配制 溶液时俯视容量瓶刻线
B.称取 固体时药品和砝码位置放反
C.滴定终点时俯视读数
D.碱式滴定管未润洗
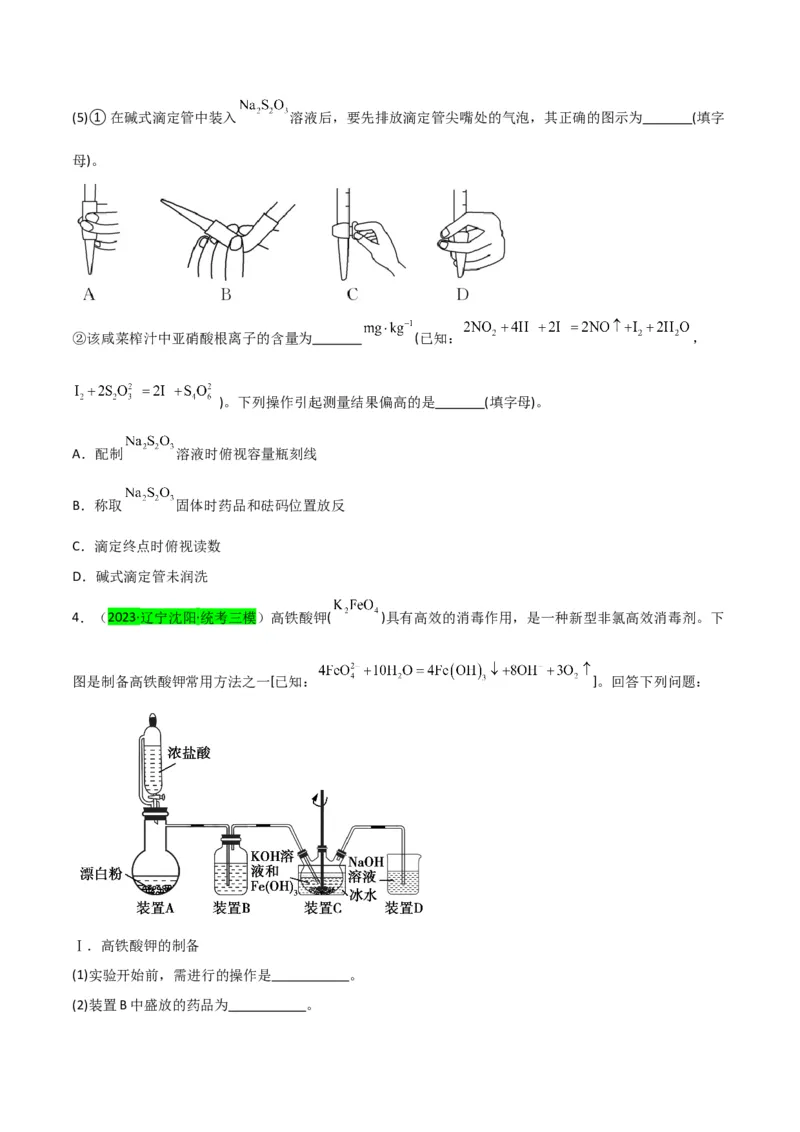
4.(2023·辽宁沈阳·统考三模)高铁酸钾( )具有高效的消毒作用,是一种新型非氯高效消毒剂。下
图是制备高铁酸钾常用方法之一[已知: ]。回答下列问题:
Ⅰ.高铁酸钾的制备
(1)实验开始前,需进行的操作是 。
(2)装置B中盛放的药品为 。(3)装置C中发生反应的离子方程式为 。
Ⅱ.高铁酸钾的分离与提纯
(4)高铁酸钾减压过滤时采用如图装置。打开水龙头,抽气,用倾析法先后将溶液和沉淀转移至布氏漏斗中。
抽滤完毕,接下来的操作为 。
(5)用3mol/L KOH溶液溶解,若选用KOH浓度过低,高铁酸钾产率会下降,原因是 。所得固体用
正戊烷、甲醇、乙醚依次洗涤,真空干燥箱中60℃烘干。
(6)工业上常用“滴定法”测定高铁酸钾样品的纯度,其方法是:称取2.0g 样品溶于3
KOH溶液中,加入足量 ,充分反应后过滤,滤液在250mL容量瓶中定容。定容后取25.00mL加入稀
硫酸酸化,用0.1000 标准溶液滴定至终点,重复操作3次,平均消耗
溶液的体积为24.00mL。
已知:a.
b.
c.
①该过程中下列仪器不需要的是 (填写仪器名称)②该 样品的纯度为 (保留三位有效数字)。
5.(2023·山东东营·东营市第一中学校考二模)三草酸合铁酸钾 为翠绿
色晶体,可溶于水,难溶于乙醇。实验室进行制备并对其阴离子电荷和晶体组成进行测定,方法如下并回
答有关问题:
Ⅰ.晶体制备
ⅰ.称取一定量 加水溶解,向其中滴加稍过量的 氨水和6% 溶液,于
40℃水浴中加热搅拌;静置,弃去上层清液,洗涤后得到 沉淀。
ⅱ.向 沉淀中加入 溶液,于80℃水浴中不断搅拌至溶液呈翠绿色;将溶液加热浓缩、冷却、
结晶;结晶完全后减压抽滤,得到产品。
(1)步骤ⅰ中,向静置后的上层清液中滴加 (填化学式),观察现象可确定反应是否进行完全。
(2)步骤ⅱ中为促进结晶,冷却后可加入 (填试剂名称)。
(3)减压抽滤采用如图装置。抽滤完毕,接下来的操作为 (填选项字母)。
A.先关闭水龙头,后拔掉橡胶管 B.先拔掉橡胶管,后关闭水龙头
Ⅱ.阴离子电荷的测定准确称取 三草酸合铁酸钾加水溶解,控制流速,使其全部通过装有阴离子交换树脂(用 表示)
的交换柱,发生阴离子(用 表示)交换: 。结束后,用去离子水
洗涤交换柱,合并流出液,并将其配成 溶液。取 该溶液,以 溶液为指示剂,用
标准液滴定至终点,消耗标准液 。
(4)阴离子电荷数为 (用含字母的代数式表示);若交换时样品液的流速过快,则会导致测定结果
(填“偏高”“偏低”或“无影响”)。
(5)阴离子交换树脂复原回收:实验完毕,用饱和 溶液淋洗交换柱内树脂,取最后一次淋洗液进行检
验,合格后可回收。该检验操作为 。
Ⅲ.晶体部分组成的测定
ⅰ. 含量测定:称取一定量三草酸合铁酸钾,加硫酸酸化后配成溶液置于锥形瓶中,用 标准
液滴定至终点。
ⅱ.Fe3+含量测定:向ⅰ中滴定后的溶液中加入 粉和适量稀 ,加热至沸腾,过滤除去过量 粉得
滤液,冷却后用 标准液滴定至终点。
(6)若省略步骤ⅰ,直接利用步骤ⅱ不能测定 含量,解释其原因为 。