文档内容
(新高考)小题必练4:氧化还原反应
对氧化还原的考查,主要包括:以生产、生活、社会中的实际问题为载体,考查氧化还原的
基本概念;比较无知氧化性、还原性的强弱及其规律应用;以元素化合物为载体,考查氧化还
原反应中电子转移的方向和数目。
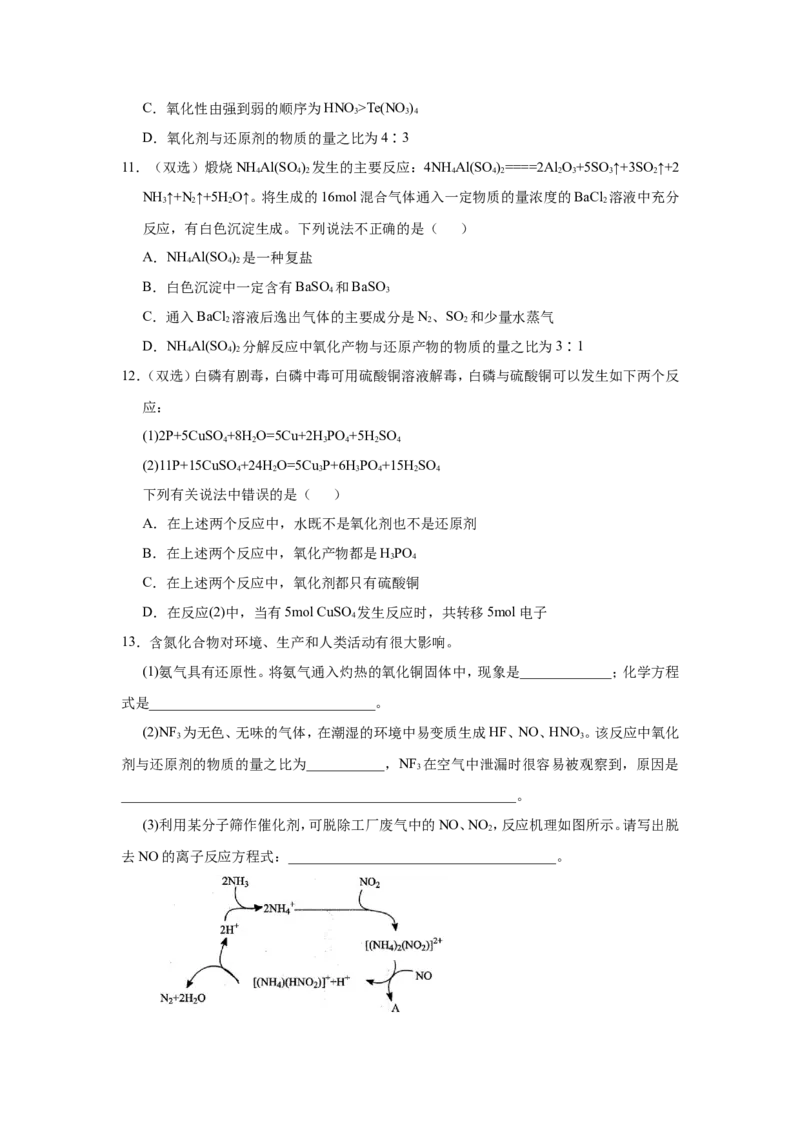
1.【2020年北京卷】实验室分离Fe3+和Al3+的流程如下:
知Fe3+在浓盐酸中生成黄色配离子[FeCl ]−,该配离子在乙醚(Et O,沸点34.6℃)中生成缔
4 2
合物 。下列说法错误的是( )
A.萃取振荡时,分液漏斗下口应倾斜向下
B.分液时,应先将下层液体由分液漏斗下口放出
C.分液后水相为无色,说明已达到分离目的
D.蒸馏时选用直形冷凝管
2.【2020年北京卷】下列物质的应用中,利用了氧化还原反应的是( )
A.用石灰乳脱除烟气中的SO
2
B.用明矾[KAl(SO)·12HO]处理污水
4 2 2
C.用盐酸去除铁锈(主要成分Fe O·xHO)
2 3 2
D.用84消毒液(有效成分NaClO)杀灭细菌
3.【2020年浙江选考】水与下列物质反应时,水表现出氧化性的是( )
A.Na B.Cl C.NO D.NaO
2 2 2
4.【2020年北京卷】反应MnO +4HCl(浓)====MnCl +Cl↑+2HO中,氧化产物是( )
2 2 2 2
A.MnO B.HCl C.MnCl D.Cl
2 2 2
5.【2020年浙江选考】硫酸盐(含SO、HSO)气溶胶是PM 的成分之一。近期科研人员提出了
2.5雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如图:
下列说法不正确的是( )
A.该过程有HO参与 B.NO 是生成硫酸盐的氧化剂
2 2
C.硫酸盐气溶胶呈酸性 D.该过程没有生成硫氧键
1.反应MnO +4HCl====MnCl +Cl+2HO中,氧化产物与还原产物的物质的量之比是( )
2 2 2 2
A.1∶2 B.1∶1 C.2∶1 D.4∶1
2.丙烷还原氧化铁的反应为C H+Fe O→CO+Fe+ ,下列叙述错误的是( )
3 8 2 3 2
A.配平方程后方框内的化学式为HO且系数为12
2
B.该反应中氧化剂与氧化产物的物质的量之比为10∶9
C.还原性:C H>Fe
3 8
D.25℃、101kPa条件下,消耗11.2L C H 转移的电子数为10N
3 8 A
3.NaFeO 是一种高效多功能水处理剂。制备方法之一为:2FeSO +6NaO=2NaFeO+
2 4 4 2 2 2 4
2NaO+2NaSO +O↑,下列说法正确的是( )
2 2 4 2
A.NaO 只作氧化剂
2 2
B.1mol FeSO 可还原2.5mol Na O
4 2 2
C.转移0.8 mol电子时生成33.2g Na FeO
2 4
D.还原剂与氧化剂的物质的量之比为1∶3
4.工业上用发烟HClO 把潮湿的CrCl 氧化为棕色的烟[CrO (ClO )]来除去Cr(III),HClO 中
4 3 2 4 2 4
部分氯元素转化为最低价态。下列说法错误的( )
A.HClO 属于强酸,该反应也生成了另一种强酸
4
B.CrO(ClO ) 中Cr元素显+6价
2 4 2
C.该反应每生成1mol氧化产物,便有0.375mol HClO 被还原
4
D.该反应的离子方程式为19ClO+8Cr3+=8CrO(ClO )+3Cl−
2 4 2
5.现有由 0.2mol CuS 和0.1mol Cu O组成的混合物,与足量稀 HNO 充分反应,生成
2 3Cu(NO )、HSO 、NO和HO,则被还原的HNO 的物质的量是( )
3 2 2 4 2 3
A.0.4mol B.0.6mol C.0.8mol D.1.0mol
6.下列我国古代的技术应用中,不涉及氧化还原反应的是( )
A.粮食酿醋 B.古法炼铁 C.淮南王发明豆浆制豆腐 D.火药爆炸
7.已知:①在发烟硫酸(H SO ·SO )中,I 和IO 生成I(SO ) 。②I(SO ) 溶于水生成I 和
2 4 3 2 2 5 2 4 3 2 4 3 2
IO。下列说法不正确的是( )
2 4
A.发烟硫酸的摩尔质量为178
B.反应①中氧化剂与还原剂的物质的量之比为3∶2
C.反应②中氧化产物与还原产物的物质的量之比为3∶1
D.若反应②中消耗2mol I (SO ),则电子转移3mol
2 4 3
8.稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很
快反应并产生气体。已知:铈常见的化合价为+3和+4,且Ce4++Fe2+=Ce3++Fe3+。下列说法
正确的是( )
A.用Pt作阴极,Fe作阳极,电解熔融CeO,可在阳极获得铈
2
B.将少量的碘化亚铁溶液滴加到Ce(SO) 溶液中,其离子方程式为:Ce4++Fe2+=Ce3++Fe3+
4 2
C.金属铈着火,可采用普通的泡沫灭火器灭火
D.金属铈可浸于煤油中保存,储存在阴凉、通风的地方,要远离火种和热源
9.氰化物是剧毒物质,传统生产工艺的电镀废水中含一定浓度的CN−,无害化排放时必须对
这种废水进行处理。可采用碱性条件下的Cl 氧化法处理这种废水,涉及两个反应:
2
反应i,CN−+OH−+Cl OCN−+Cl−+H O(未配平);
2 2
反应ii,OCN−+OH−+Cl X+Y+Cl−+H O(未配平)。
2 2
其中反应i中N元素的化合价没有变化,X、Y是两种无毒的气体。下列判断正确的是(
)
A.反应i中氧化剂与还原剂的化学计量数之比为1∶2
B.X、Y是CO、N,且均为反应ii的氧化产物
2 2
C.该废水处理工艺过程中须采取措施,防止Cl 逸出到空气中
2
D.处理c(CN−)=0.0001mol·L−1的废水106L,消耗标况下的Cl 4.48×103L
2
10.工业上提取碲(Te)的反应之一为3Te+16HNO =3Te(NO )+4NO↑+8HO,下列说法不正确
3 3 4 2
的是( )
A.生成标准状况下11.2L NO,转移的电子数为2N
A
B.Te(NO ) 是氧化产物,NO是还原产物
3 4C.氧化性由强到弱的顺序为HNO>Te(NO )
3 3 4
D.氧化剂与还原剂的物质的量之比为4∶3
11.(双选)煅烧NH Al(SO ) 发生的主要反应:4NH Al(SO )====2Al O+5SO↑+3SO↑+2
4 4 2 4 4 2 2 3 3 2
NH ↑+N ↑+5H O↑。将生成的16mol混合气体通入一定物质的量浓度的BaCl 溶液中充分
3 2 2 2
反应,有白色沉淀生成。下列说法不正确的是( )
A.NH Al(SO ) 是一种复盐
4 4 2
B.白色沉淀中一定含有BaSO 和BaSO
4 3
C.通入BaCl 溶液后逸出气体的主要成分是N、SO 和少量水蒸气
2 2 2
D.NH Al(SO ) 分解反应中氧化产物与还原产物的物质的量之比为3∶1
4 4 2
12.(双选)白磷有剧毒,白磷中毒可用硫酸铜溶液解毒,白磷与硫酸铜可以发生如下两个反
应:
(1)2P+5CuSO +8H O=5Cu+2H PO +5H SO
4 2 3 4 2 4
(2)11P+15CuSO+24H O=5Cu P+6HPO +15H SO
4 2 3 3 4 2 4
下列有关说法中错误的是( )
A.在上述两个反应中,水既不是氧化剂也不是还原剂
B.在上述两个反应中,氧化产物都是HPO
3 4
C.在上述两个反应中,氧化剂都只有硫酸铜
D.在反应(2)中,当有5mol CuSO 发生反应时,共转移5mol电子
4
13.含氮化合物对环境、生产和人类活动有很大影响。
(1)氨气具有还原性。将氨气通入灼热的氧化铜固体中,现象是_____________;化学方程
式是________________________________。
(2)NF 为无色、无味的气体,在潮湿的环境中易变质生成HF、NO、HNO。该反应中氧化
3 3
剂与还原剂的物质的量之比为___________,NF 在空气中泄漏时很容易被观察到,原因是
3
________________________________________________________。
(3)利用某分子筛作催化剂,可脱除工厂废气中的NO、NO ,反应机理如图所示。请写出脱
2
去NO的离子反应方程式:______________________________________。(4)火箭燃料偏二甲肼C HN 与NO 反应放出大量的热,生成无毒、无污染的气体和水。
2 8 2 2 4
1mol C HN 完全反应转移的电子数是___________。
2 8 2
14.一种利用电解锰阳极泥(主要成分MnO 、MnO)制备MnO 的工艺流程如下:
2 2
(1)“煅烧氧化”时,1mol MnO完全转化为NaMnO 失去电子的物质的量为____mol;
2 4
MnO 煅烧反应的化学方程式为______________。
2
(2)“调pH”是将溶液pH调至约为10,防止pH较低时NaMnO 自身发生氧化还原反应生
2 4
成MnO 和____________。
2
(3)“还原”时有无机含氧酸盐生成,反应的化学方程式为___________。
(4)测定产品中MnO 质量分数的步骤如下:
2
步骤1:准确称取mg产品,加入c mol/L NaC O 溶液VmL(过量)及适量的稀硫酸,水
1 2 2 4 1
浴加热煮沸一段时间。(已知:NaC O+2H SO +MnO=MnSO +2CO ↑+2H O+Na SO )
2 2 4 2 4 2 4 2 2 2 4
步骤2:用c mol/L KMnO 标准溶液滴定剩余的NaC O,滴定至终点时消耗KMnO 标
2 4 2 2 4 4
准溶液VmL。(已知:5HC O+2KMnO +3H SO =2MnSO +l0CO ↑+K SO +8H O)
2 2 4 4 2 4 4 2 2 4 2
步骤 2 达滴定终点时的判断依据是___________,产品中 MnO 的质量分数为
2
w(MnO)=______(列出计算表达式即可)。
2
15.碳酸铈[Ce (CO)]为白色粉末,难溶于水,主要用作生产铈的中间化合物。它可由氟碳酸
2 3 3
铈精矿经如图流程制得:
回答下列问题:
(1)若NaCO 溶液改为NaOH溶液,则反应生成难溶物一氢氧化铈(M),其暴露于空气中
2 3
时变成紫色,最终变成黄色的氢氧化高铈(IV)。氢氧化铈在空气中被氧化成氢氧化高铈的化
学方程式为 。
(2)取(1)中得到的Ce(OH) 产品1.00g,加硫酸溶解后,用0.1000mol/L的FeSO 标准溶
4 4
液滴定至终点(铈被还原成Ce3+),消耗标准溶液45.00mL,则所得产品中Ce(OH) 的质量分数
4为 。
参考答案
考点透视
1.【答案】A
【解析】A.萃取振荡时,分液漏斗下口应倾斜向上,A错误;B.分液时,密度大的液体在下
层,密度小的液体在上层,下层液体由分液漏斗下口放出,下层液体放完后,密度小的上层液
体从分液漏斗上口倒出,B正确;C.Fe3+在浓盐酸中生成黄色配离子,该离子在乙醚中生成缔
合物,乙醚与水不互溶,故分液后水相为无色,则水相中不再含有Fe3+,说明已经达到分离目的,C正确;D.蒸馏时选用直形冷凝管,能使馏分全部转移到锥形瓶中,而不会残留在冷凝管
中,D正确;答案选A。
【点睛】萃取分液操作的考查,熟练掌握实验操作流程。
2.【答案】D
【解析】A.SO 是酸性氧化物,可与碱反应,用石灰乳脱除烟气中的SO 时,SO 与氢氧化
2 2 2
钙反应生成亚硫酸钙或亚硫酸氢钙,反应过程中无元素的化合价变化,没有利用氧化还原反
应,故A不符合题意;B.用明矾[KAl(SO)·12HO]溶于水中,电离出的铝离子发生水解生成
4 2 2
氢氧化铝胶体,利用胶体的吸附性可吸附污水中的固体颗粒物,该过程利用胶体的吸附性,
发生的反应没有发生化合价变化,没有利用氧化还原反应,故B不符合题意;C.用盐酸去除
铁锈(主要成分Fe O·xHO),发生的主要反应为:6HCl+Fe O=2FeCl +3H O,反应中没有元
2 3 2 2 3 3 2
素化合价的变化,没有利用氧化还原反应,故 C不符合题意;D.用84消毒液有效成分
NaClO,具有强氧化性,能使蛋白质发生变性从而杀死细菌病毒,杀菌消毒的过程利用了氧
化还原反应,故D符合题意;答案选D。
【点睛】判断氧化还原反应的依据是有元素化合价的升降。
3.【答案】A
【解析】A.2Na+2HO=2NaOH+H ↑,HO中H元素化合价由+1降为0价,得电子被还原,
2 2 2
做氧化剂,在反应中表现出氧化性,故A符合题意;B.Cl+H O HCl+HClO,HO中的元
2 2 2
素没有发生化合价的变化,水在反应中既不是氧化剂也不是还原剂,既不表现氧化性也不表
现还原性,故B不符合题意;C.3NO +H O=2HNO +NO,HO中的元素没有发生化合价的变
2 2 3 2
化,水在反应中既不是氧化剂也不是还原剂,既不表现氧化性也不表现还原性,故C不符合
题意;D.NaO+HO=2NaOH,该反应没有元素化合价变化,不是氧化还原反应,水在反应中
2 2
既不表现氧化性也不表现还原性,故D不符合题意;答案选A。
【点睛】氧化剂是化合价降低,发生还原反应的物质。
4.【答案】D
【解析】反应中,HCl的Cl元素化合价升高变为0价,作还原剂,而氯气为氧化产物,MnO
2
中的Mn化合价降低,作氧化剂,MnCl 为还原产物,综上所述,答案为D。
2
【点睛】掌握氧化还原反应中常见的几个概念,例如还原剂是化合价升高的发生氧化反应,
得到氧化产物的物质。
5.【答案】D
【解析】根据图示中各微粒的构造可知,该过程有HO参与,故A正确;B.根据图示的转
2化过程,NO 转化为HNO,N元素的化合价由+4价变为+3价,化合价降低,得电子被还原,
2 2
做氧化剂,则NO 的是生成硫酸盐的氧化剂,故B正确;C.硫酸盐(含SO、HSO)气溶胶中含
2
有HSO,转化过程有水参与,则HSO在水中可电离生成H+和SO,则硫酸盐气溶胶呈酸性,
故C正确;D.根据图示转化过程中,由SO转化为HSO,根据图示对照,有硫氧键生成,故D
错误;答案选D。
【点睛】将一个氧化还原反应拆分成几步,以图像的形式表达出来,考查学生细致的观察
能力与分析能力。
考点突破
1.【答案】B
【解析】由反应方程式可知,反应物MnO 中的Mn元素的化合价为+4价,生成物MnCl 中
2 2
Mn元素的化合价为+2价,反应物HCl中Cl元素的化合价为-1价,生成物Cl 中Cl元素的化
2
合价为0价,故MnCl 是还原产物,Cl 是氧化产物,由氧化还原反应中得失电子守恒可知,
2 2
n(Cl )∶n(MnCl )=1∶1,B符合题意;答案选B。
2 2
2.【答案】D
【解析】烷还原氧化铁的反应为C H+Fe O→CO+Fe+ ,反应中C元素的化合价由-
3 8 2 3 2
变为+4价,化合价升高,失电子,发生氧化反应,C H 作还原剂;Fe元素的化合价由+3价变
3 8
为0价,化合价降低,得电子,发生还原反应,Fe O 作氧化剂,根据氧化还原反应得失电子守
2 3
恒和原子守恒,则配平该反应方程式为:3C H+10Fe O=9CO +20Fe+12H O。根据上述分析
3 8 2 3 2 2
可知,A正确;该反应中氧化剂为Fe O,氧化产物为CO,则二者物质的量之比为10∶9,故
2 3 2
B正确;根据氧化还原反应规律,还原剂的还原性大于还原产物的还原性,则还原性:C H>
3 8
Fe,故C正确;11.2L C H 的状态条件不是标准状况,不能用标况下气体的摩尔体积计算消
3 8
耗C H 物质的量,则反应中转移电子的数目不能确定,故D错误;答案选D。
3 8
【点睛】注意气体求算物质的量时是否是在标况下,能否直接使用22.4L/mol。
3.【答案】B
【解析】该反应中Fe元素化合价由+2价变为+6价、O元素化合价由-1价变为0价、-2价,
所以硫酸亚铁是还原剂、过氧化钠既是氧化剂又是还原剂,氧化剂对应的产物是还原产物,
还原剂对应的产物是氧化产物。A.根据分析,NaO 既是氧化剂又是还原剂,故A错误;B.
2 2
反应2FeSO +6NaO=2NaFeO+2NaO+2NaSO +O↑中,化合价升高的元素有Fe,由+2价
4 2 2 2 4 2 2 4 2→+6价,化合价升高的元素还有O元素,由-1价→0价,2mol FeSO 发生反应时,共有
4
2mol×4+1mol×2=10mol电子转移,6mol NaO 有5mol作氧化剂、1mol NaO 作还原剂,其中
2 2 2 2
2mol FeSO 还原5mol Na O,即1mol FeSO 还原2.5mol Na O,故B正确;C.由方程式转移
4 2 2 4 2 2
10mol 电子生成 2mol NaFeO ,转移 0.8mo1 电子时生成 ×2×166g·mol−1=26.56g
2 4
NaFeO,故C错误;D.根据B项分析,6mol NaO 有5mol作氧化剂、1mol NaO 作还原剂,
2 4 2 2 2 2
2mol FeSO 作还原剂,则还原剂与氧化剂的物质的量之比为3∶5,故D错误;答案选B。
4
4.【答案】D
【解析】A.Cl元素非金属性较强,HClO 属于强酸,生成盐酸,也属于强酸,故A正确;B.
4
CrO(ClO ) 中0为-2价、Cl为+7价,则Cr元素显+6价,故B正确;C.该反应每生成1mol氧
2 4 2
化产物,则转移3mol电子,HClO 被还原的物质的量为 ,故C正确;D.该反
4
应的离子方程式为19ClO+8Cr3++4H O=8CrO(ClO )+3Cl−+8H+,故D错误;故选D。
2 2 4 2
【点睛】离子方程式的书写注意等式两边的电荷守恒。
5.【答案】B
【解析】CuS中硫元素化合价从-2升高到+6,则1mol CuS被氧化失去8mol电子、Cu O中
2
铜元素化合价从+1升高到+2,则1mol Cu O被氧化失去2mol电子,稀HNO 作氧化剂时氮
2 3
元素化合价从+5降低到+2,每1mol硝酸被还原得电子物质的量为3mol,0.2mol CuS和
0.1mol Cu O被氧化失去电子的物质的量为0.2mol×8+0.1mol×2=1.8mol,按得失电子数守恒,
2
被还原的HNO 的物质的量是 ,B正确;答案选B。
3
【点睛】解题关键在于抓住氧化还原反应中得失电子数相等。
6.【答案】C
【解析】A.粮食酿醋的过程中有元素化合价变化,属于氧化还原反应,故A不符合题意;
B.古法炼铁过程中有元素化合价变化,属于氧化还原反应,故B不符合题意;C.淮南王发明
豆浆制豆腐没有元素化合价变化,不属于氧化还原反应,故C符合题意;D.火药爆炸有元素
化合价变化,属于氧化还原反应,故D不符合题意;故选C。
7.【答案】A
【解析】A.发烟硫酸(H SO ·SO )的摩尔质量是178g·mol−1,故A错误;B.I 中碘为0价,
2 4 3 2
IO 中碘为+5价,得到+3价的碘化合物I(SO ),则化学方程式为:4I+6I O+15H SO ·
2 5 2 4 3 2 2 5 2 4SO =10I(SO )+15H O,氧化剂IO 与还原剂I 的物质的量之比为3∶2,故B错误;C.I(SO )
3 2 4 3 2 2 5 2 2 4 3
溶于水生成I 和IO,另外还应生成HSO ,根据反应物与产物中I元素的化合价可推知I 与
2 2 4 2 4 2
IO 的物质的量之比为1∶3,则化学方程式:4I(SO )+12H O=I+3I O+12H SO ,氧化产物
2 4 2 4 3 2 2 2 4 2 4
IO 与还原产物 I 的物质的量之比为 3∶1,故 C 错误;D.根据 C 中②的反应
2 4 2
4I(SO )+12H O=I+3I O+12H SO ,4I(SO )~I~6e−,所以消耗2mol I(SO ),则电子转移
2 4 3 2 2 2 4 2 4 2 4 3 2 2 4 3
3mol,故D正确;故选A。
8.【答案】D
【解析】A.电解时活性电极做阳极,阳极本身失电子发生氧化反应,得到Fe2+,与Ce4+反应,
最终使得熔融的CeO 中的四价铈离子不放电,A错误;B.将少量的碘化亚铁溶液滴加到
2
Ce(SO) 溶液中,由于I−和Fe2+都有还原性,故两者均可以与Ce4+反应,反应为3Ce4++Fe2+
4 2
+2I−=3Ce3++I+Fe3+,B错误;C.普通的泡沫灭火器中有二氧化碳和氢氧化铝的糊状物,由于
2
铈是活泼金属,会与糊状物中的水反应,所以不能用泡沫灭火器灭火,C错误;D.金属铈是活
泼金属,易与水、氧气反应,所以保存时放在煤油中隔离空气,储存在阴凉、通风的地方,要远
离火种和热源,D正确;故选D。
9.【答案】C
【解析】A.反应i中N元素的化合价没有变化,碳化合价从+2升高到+4,氯元素化合价降
低,所以氯气是氧化剂,CN−是还原剂,二者比例为1∶1,故A错误;B.X、Y是两种无毒的气
体,从元素分析,应含有碳元素和氮元素,其中一种为二氧化碳,另一种为氮气,其中碳元素
化合价不变,氮元素化合价升高,氮气为氧化产物,二氧化碳不是氧化产物,故B错误;C.氯
气是有毒气体,应采取措施,防止氯气逸出到空气中,故C正确;D.CN−+2OH−+Cl=OCN−
2
+2Cl−+H O,2OCN−+4OH−+3Cl=2CO +N +6Cl−+2H O,总反应方程式为,2CN−+8OH−
2 2 2 2 2
+5Cl=2CO +N +10Cl−+4H O,处理 c(CN−)=0.0001mol·L−1的废水 106L,则的物质的量为
2 2 2 2
100mol,消耗的氯气为250mol,标况下的Cl 250mol×22.4L/mol=5.6×103L,故D错误。故选
2
C。
10.【答案】A
【解析】A.由化学方程式可知,生成4mol NO,反应转移12mol电子,标准状况下11.2L
NO的物质的量为0.5mol,则转移1.5mol电子,电子数为1.5N ,故A错误;B.由化学方程式
A
可知,反应中Te元素化合价升高被氧化,N元素化合价部分降低被还原,则Te(NO ) 是氧化
3 4
产物,NO是还原产物,故B正确;C.由氧化还原反应规律可知,氧化剂的氧化性强于氧化产
物,由元素化合价变化可知,HNO 起酸和氧化剂的作用,Te(NO ) 是氧化产物,则氧化性由
3 3 4强到弱的顺序为HNO>Te(NO ),故C正确;D.由化学方程式可知,反应中Te元素化合价升
3 3 4
高被氧化,N元素化合价部分降低被还原,Te为还原剂,HNO 起酸和氧化剂的作用,则氧化
3
剂与还原剂的物质的量之比为4∶3,故D正确;故选A。
11.【答案】BD
【解析】A.NH Al(SO ) 是由两种不同的金属阳离子(铵根离子性质类似金属阳离子)和一
4 4 2
种酸根离子组成的盐,因此属于复盐,A正确;B.根据物质分解反应方程式可知反应产生的
气体中,SO 、SO 、NH 物质的量的比是5∶3∶2,反应后溶液显酸性,SO 与水反应产生
3 2 3 3
HSO ,HSO 与BaCl 反应产生BaSO 沉淀,由于BaSO 能够溶于酸,故在酸性环境中不存
2 4 2 4 2 4 3
在,则白色沉淀中一定含有BaSO,但不含BaSO,B错误;C.4mol NH Al(SO ) 完全分解产
4 3 4 4 2
生16mol气体,其中5mol SO 与水反应产生5mol的HSO ,2mol NH 与1mol HSO 反应产
3 2 4 3 2 4
生(NH )SO ,(NH )SO 及未反应的4mol HSO 与BaCl 反应产生BaSO 沉淀,在酸性环境
4 2 4 4 2 4 2 4 2 4
中SO 不能溶解,N 也不能溶解,故逸出气体的主要成分是N、SO 和少量水蒸气,C正确;
2 2 2 2
D.在该反应中,N元素化合价由反应前NH Al(SO ) 中的-3价变为反应后N 中的0价,化合
4 4 2 2
价升高,失去电子被氧化,N 是氧化产物;S元素化合价由反应前NH Al(SO ) 中的+6价变为
2 4 4 2
反应后SO 中的+4价,化合价降低,得到电子被还原,SO 是还原产物,故分解反应中氧化产
2 2
物与还原产物的物质的量之比为1∶3,D错误;故合理选项是BD。
12.【答案】CD
【解析】在(1)2P+5CuSO +8H O=5Cu+2H PO +5H SO 反应中P元素化合价由0价变为5
4 2 3 4 2 4
价,Cu元素化合价由+2价变为0价;在(2)11P+15CuSO+24H O=5Cu P+6HPO +15H SO 反
4 2 3 3 4 2 4
应中P元素化合价由0价变为-3价、+5价,Cu元素化合价由+2价变为+1价,如果有11mol P
参加氧化还原反应,则有6/11的P被氧化,其余的P被还原,A、两个反应中只有P、Cu元素
化合价变化,水既不是氧化剂也不是还原剂,故A正确;B、两个反应中P元素化合价由0价
变为+5价,化合价升高被氧化,所以氧化产物都是HPO ,故B正确;C.在反应(2)中,P元
3 4
素化合价由0价变为-3价、+5价,所以P既是氧化剂又是还原剂,故C错误;D、在反应(2)中,
15mol CuSO 转移30mol电子,则当有5mol CuSO 发生反应时,共转移10mol电子,故D错
4 4
误;故选CD。
【点睛】本题考查氧化还原反应,掌握元素化合价变化和氧化剂、还原剂的概念是解本题
关键,注意该反应中P元素化合价变化,在反应(2)中既升高又降低,为易错点,侧重于考查
学生对基础知识的应用能力。
13.【答案】(1)黑色氧化铜变为红色 2NH +3CuO====3Cu+N +3H O
3 2 2(2)2∶1 NO与氧气反应生成红棕色的二氧化氮
(3)[(NH )(NO )]2++NO=[(NH )(HNO)]++H++N +H O
4 2 2 4 2 2 2
(4)16N
A
【解析】(1)氨气具有还原性,能使黑色的氧化铜变为红色的单质铜,反应的方程式为
2NH +3CuO====3Cu+N +3H O;(2)NF 在潮湿的环境中与水反应,易变质生成HF、NO、
3 2 2 3
HNO,则方程式为3NF +5H O=9HF+2NO+HNO ,当有3mol NF 反应时,生成2mol NO和
3 3 2 3 3
1mol HNO ,则反应中氧化剂与还原剂的物质的量之比为2∶1;NF 易变质,生成NO,NO与
3 3
氧气反应生成红棕色的二氧化氮,而硝酸易于空气中的水蒸气结合形成白雾;(3)根据图像可
知,反应的方程式为NO+NO +2NH=2N +3H O,A为氮气和水,则脱去NO的离子反应方程
2 3 2 2
式为[(NH )(NO )]2++NO=[(NH )(HNO)]++H++N +H O;(4)已知C HN 与NO 反应放出大量
4 2 2 4 2 2 2 2 8 2 2 4
的热,生成无毒、无污染的气体和水,C HN+2N O=2CO +4H O+3N,1mol C HN 完全反应
2 8 2 2 4 2 2 2 2 8 2
转移的电子为16mol。
14.【答案】(1)4 2MnO +4NaOH+O=====2NaMnO +2H O
2 2 2 4 2
(2)MnO[(或NaMnO )
4
(3)2NaMnO +HCHO=2MnO ↓+Na CO+2NaOH
2 4 2 2 3
(4)滴 入 最 后 一 滴 KMnO 溶 液 时 , 溶 液 呈 浅 红 色 且 30s 内 不 褪 去
4
×100%
【解析】锰阳极泥“煅烧氧化”使MnO完全转化为NaMnO ;“浸取”得到NaMnO 的
2 4 2 4
浸取液;“调pH”是将溶液pH调至约为10,加入甲醛发生氧化还原反应制备二氧化锰。
(1)“煅烧氧化”时MnO Na MnO 锰由+2价变成+6价,失去电子为4e−,1mol MnO煅烧
2 4
完全失去电子的物质的量为4mol;MnO 煅烧反应的化学方程式为2MnO +4NaOH+O=====
2 2 2
2NaMnO +2H O;(2)Na MnO 中Mn的化合价为+6,MnO 中Mn的化合价为+4,NaMnO 自
2 4 2 2 4 2 2 4
身发生氧化还原反应,Mn的化合价部分变为+4价,部分要升高为+7价,所以能生成MnO ,
2
NaMnO ;(3)根据流程可知,“还原指NaMnO 与甲醛反应生成二氧化锰和碳酸钠,反应的
4 2 4
化学方程式为2NaMnO +HCHO=2MnO ↓+Na CO+2NaOH;(4)用KMnO 标准溶液滴定草酸,
2 4 2 2 3 4
滴定终点时高锰酸钾过量,则判断依据是:滴入最后一滴KMnO 溶液时,溶液呈浅红色且
4
30s内不褪去;由5HC O+2KMnO +3H SO =2MnSO +10CO ↑+K SO +8H O,得2n
2 2 4 4 2 4 4 2 2 4 2
(H C O)=5n(KMnO ),n(H C O)= ;NaC O+2H SO +MnO=MnSO +2CO
2 2 4 4 2 2 4 2 2 4 2 4 2 4 2↑+2H O+Na SO , n(Na C O)=n(MnO) , n(Na C O)=c mol/L×V mL- ,
2 2 4 2 2 4 2 2 2 4 1 1
m(MnO)=(c V- )×87g/mol÷1000 , 产 品 中 MnO 的 质 量 分 数 为 ω(MnO )=
2 1 1 2 2
×100%。
15.【答案】(1)4Ce(OH) +O +2H O=4Ce(OH)
3 2 2 4
(2)93.6%
【解析】氟碳酸铈精矿在空气中氧化焙烧生成二氧化铈(CeO)、二氧化碳和HF;二氧化铈
2
与稀硫酸、过氧化氢反应生成铈(III)溶液、氧气;分离出不溶物后,加入碳酸钠溶液制备
Ce (CO)。(3)若试剂NaCO 改为氢氧化钠溶液,则发生反应Cs(SO )+6NaOH=2Ce(OH)
2 3 3 2 3 2 4 3 3
↓+3Na SO ,将氢氧化铈(Ⅲ)暴露于空气中时会被空气中的氧气氧化变成紫色,最终变成黄色
2 4
的氢氧化高铈(Ⅳ)。根据元素守恒和得失电子守恒,化学方程式为4Ce(OH) +O +2H O=4
3 2 2
Ce(OH) ;(4)用0.1000mol/L的FeSO 标准溶液滴定时,发生Ce(OH) +Fe2++4H+=Ce3++Fe3++4
4 4 4
HO,则n[Ce(OH) ]=0.1000mol/L×45.00mL=0.0045mol,m[Ce(OH) ]=0.0045mol×208g/mol=
2 4 4
0.936g,Ce(OH) 的质量分数= ×100%=93.6%。
4