文档内容
(新高考)小题必练5:铁及其重要化合物
铁是过渡元素的代表,铁及其化合物相关知识是历年高考命题的热点,常常通过离子方
程式正误考查氧化还原知识的应用,离子共存(铁盐的性质)、以铁的氢氧化物沉淀平衡为载
体考查识图能力,以铁及其化合物为信息源考查计算能力,通过实验分析考查其基础知识的
应用,通过物质制备考查实验分析能力等。
1.【2020江苏卷】下列有关化学反应的叙述正确的是( )
A.室温下,Na在空气中反应生成NaO
2 2
B.室温下,Al与4.0mol·L−1 NaOH溶液反应生成NaAlO
2
C.室温下,Cu与浓HNO 反应放出NO气体
3
D.室温下,Fe与浓HSO 反应生成FeSO
2 4 4
【答案】B
【解析】A.室温下,钠与空气中氧气反应生成氧化钠,故A错误;B.室温下,铝与NaOH
溶液反应生成偏铝酸钠和氢气,故B正确;C.室温下,铜与浓硝酸反应生成二氧化氮气体,
故C错误;D.室温下,铁在浓硫酸中发生钝化,故D错误。综上所述,答案为B 。
【点睛】常见的金属与酸,碱的反应,熟记反应方程式即可。
2.【2019江苏】下列有关化学反应的叙述正确的是( )
A.Fe在稀硝酸中发生钝化 B.MnO 和稀盐酸反应制取Cl
2 2
C.SO 与过量氨水反应生成(NH )SO D.室温下Na与空气中O反应制取NaO
2 4 2 3 2 2 2
【答案】C
【解析】A.常温下,Fe在与浓硝酸发生钝化反应,故A错误;B.二氧化锰与浓盐酸在加热
条件下反应制取氯气,故B错误;C.二氧化硫与过量氨水反应生成硫酸铵,故C正确;D.常
温下,Na与空气中的氧气反应生成NaO;加热条件下,钠与氧气反应生成NaO,故D错误;
2 2 2
综上所述,本题应选C。
【点睛】常见物质的制取的考查,制氯气常用的试剂是二氧化锰和浓盐酸、过氧化钠是将
金属钠在空气中加热反应得到。3.【2020浙江7月选考】黄色固体X,可能含有漂白粉、FeSO 、Fe (SO )、CuCl 、KI之中的几
4 2 4 3 2
种或全部。将X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论
合理的是( )
A.X中含KI,可能含有CuCl
2
B.X中含有漂白粉和FeSO
4
C.X中含有CuCl ,Y中含有Fe(OH)
2 3
D.用HSO 酸化溶液Z,若有黄绿色气体放出,说明X中含有CuCl
2 4 2
【答案】C
【解析】固体X为黄色,则含有Fe (SO ),溶于水后,要使溶液Z为无色碱性,则一定含有
2 4 3
漂白粉,且漂白粉过量,得到深棕色固体混合物Y,则固体Y是Fe(OH) 和Cu(OH) 的混合物,
3 2
X中一定含有CuCl ,FeSO 和Fe (SO ) 中含有其中一种或两种都含,据此解答。A.若X含有
2 4 2 4 3
KI,则会与漂白粉反应生成I,溶液不为无色,A不正确;B.由分析可知,不一定含有FeSO ,
2 4
B不正确;C.由分析可知,X含有CuCl ,Y含有Fe(OH) ,C正确;D.酸化后,产生黄绿色气体,
2 3
为氯气,则发生的发生反应的离子反应方程式为:Cl−+ClO−+2H+=
Cl↑+H O,此时的Cl−有可能来自于漂白粉氧化FeSO 产生的Cl−,也有可能是漂白粉自身含
2 2 4
有的,不能推导出含有CuCl ,D不正确;故选C。
2
【点睛】根据实验现象进行推断可能发生的反应和得到的产物。
1.《淮南子·说山训》云:慈石能引铁(慈,旧作磁)。“慈石”的主要成分是( )
A.四氧化三铁 B.氧化铜 C.三氧化二铁 D.硅酸盐
【答案】A
【解析】四氧化三铁,化学式Fe O。俗称氧化铁黑、吸铁石、黑氧化铁,为具有磁性的黑色
3 4
晶体,故又称为磁性氧化铁。“慈石”的主要成分是四氧化三铁,A项正确。
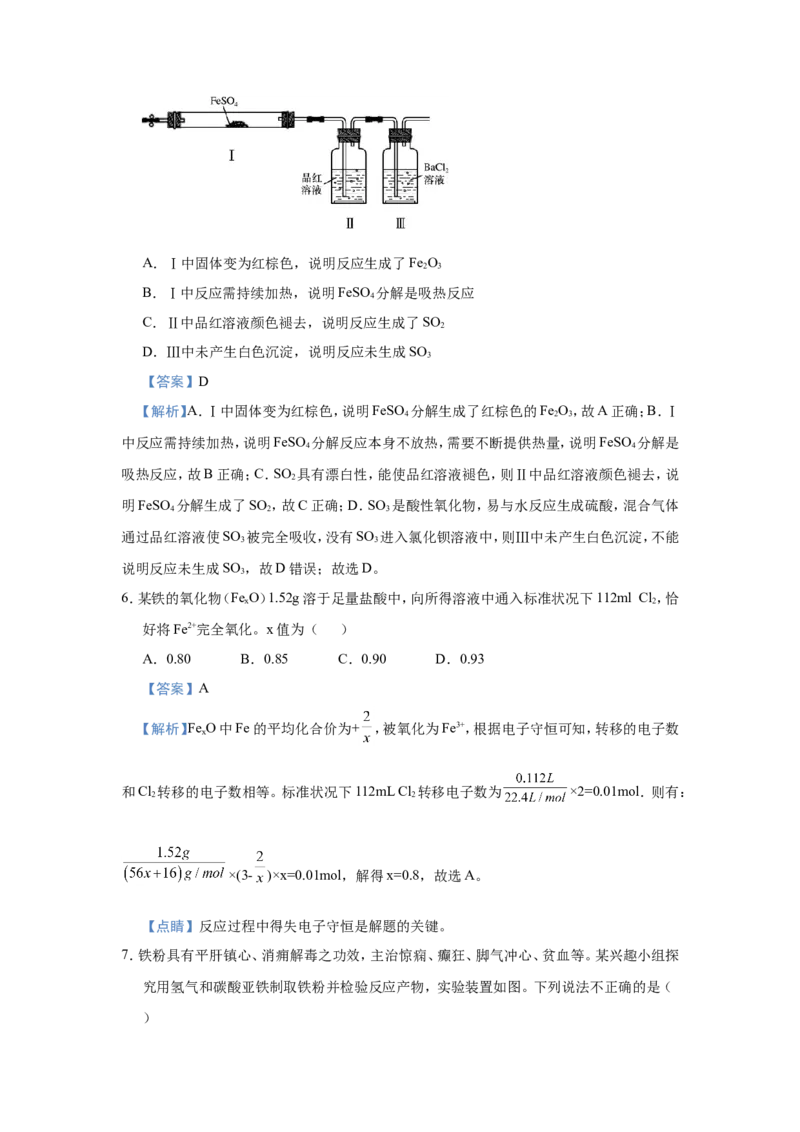
2.下列有关实验的叙述正确的是( )
A.用图1装置将氯化铁溶液直接蒸干得到氯化铁固体B.利用图2装置可制备Fe(OH)
2
C.图3微热稀HNO 片刻,溶液中有气泡产生,广口瓶内始终保持无色
3
D.利用图4可收集氯化氢并进行尾气吸收
【答案】B
【解析】A项,在FeCl 溶液中,Fe3+发生水解:FeCl +3H O Fe(OH) +3HCl,由于加热
3 3 2 3
蒸发,使HCl挥发,使平衡不断向右移动,结果生成Fe(OH) ,又由于灼热使Fe(OH) 分解生
3 3
成Fe O,故A错误;B项,如图2装置制备Fe(OH) ,稀硫酸与铁粉反应生成氢气,可排出试
2 3 2
管中的空气,盛NaOH溶液的胶头滴管伸入FeSO 溶液中,右侧导管插入水中隔绝了空气,
4
所以制得的Fe(OH) 可以较长时间稳定存在,故B正确;C项,稀硝酸与Cu反应生成NO气
2
体,无色NO气体进入广口瓶,被空气中的氧气氧化为红棕色NO 气体,故C错误;D项,氯
2
化氢的密度比空气的大,如图所示收集应该长导管进气,空气从短导管排出,故D错误;答案
选B。
3.下列有关铁及其化合物的说法中不正确的是( )
A.工业上在高温下用CO还原含Fe O 的铁矿石炼铁
2 3
B.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe O
3 4
C.工业上可用铁制容器储存、运输浓硝酸和浓硫酸
D.氯化铁溶液有较强氧化性,故可用作净水剂
【答案】D
【解析】FeCl 溶液用作净水剂的原因是Fe3+水解产生Fe(OH) 胶体,其可吸附水中悬浮物
3 3
和杂质等并形成沉淀沉降下来,从而起到净水作用,与氧化性无关。
4.铁屑溶于过量稀硫酸,过滤后向滤液中加入过量氨水,有白色沉淀生成,过滤,在空气中加
热沉淀至质量不再发生变化为止,得到红棕色残渣,上述沉淀和残渣分别是( )
A.Fe(OH) Fe O B.Fe(OH) Fe O
3 2 3 2 2 3
C.Fe(OH) Fe(OH) D.Fe(OH) Fe O
2 3 2 3 4
【答案】B
【解析】铁与稀硫酸反应生成FeSO ,再与过量氨水反应生成白色沉淀Fe(OH) ,在空气中
4 2
加热Fe(OH) ,铁元素被氧化为+3价,最后所得红棕色残渣为Fe O。
2 2 3
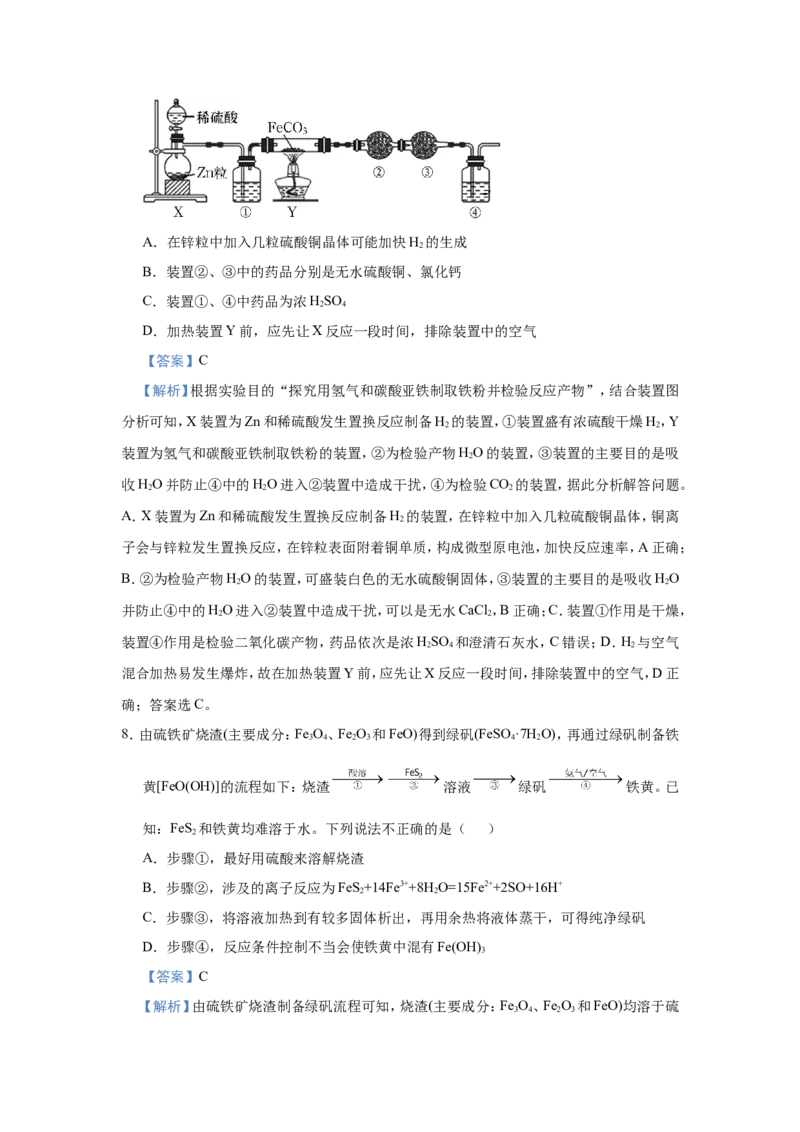
5.实验小组同学探究FeSO 分解反应并检验反应产物(加热及加持装置略)。下列有关FeSO
4 4
分解的说法不正确的是( )A.Ⅰ中固体变为红棕色,说明反应生成了Fe O
2 3
B.Ⅰ中反应需持续加热,说明FeSO 分解是吸热反应
4
C.Ⅱ中品红溶液颜色褪去,说明反应生成了SO
2
D.Ⅲ中未产生白色沉淀,说明反应未生成SO
3
【答案】D
【解析】A.Ⅰ中固体变为红棕色,说明FeSO 分解生成了红棕色的Fe O,故A正确;B.Ⅰ
4 2 3
中反应需持续加热,说明FeSO 分解反应本身不放热,需要不断提供热量,说明FeSO 分解是
4 4
吸热反应,故B正确;C.SO 具有漂白性,能使品红溶液褪色,则Ⅱ中品红溶液颜色褪去,说
2
明FeSO 分解生成了SO ,故C正确;D.SO 是酸性氧化物,易与水反应生成硫酸,混合气体
4 2 3
通过品红溶液使SO 被完全吸收,没有SO 进入氯化钡溶液中,则Ⅲ中未产生白色沉淀,不能
3 3
说明反应未生成SO ,故D错误;故选D。
3
6.某铁的氧化物(Fe O)1.52g溶于足量盐酸中,向所得溶液中通入标准状况下112ml Cl,恰
x 2
好将Fe2+完全氧化。x值为( )
A.0.80 B.0.85 C.0.90 D.0.93
【答案】A
【解析】Fe O中Fe的平均化合价为+ ,被氧化为Fe3+,根据电子守恒可知,转移的电子数
x
和Cl 转移的电子数相等。标准状况下112mL Cl 转移电子数为 ×2=0.01mol.则有:
2 2
×(3- )×x=0.01mol,解得x=0.8,故选A。
【点睛】反应过程中得失电子守恒是解题的关键。
7.铁粉具有平肝镇心、消痈解毒之功效,主治惊痫、癫狂、脚气冲心、贫血等。某兴趣小组探
究用氢气和碳酸亚铁制取铁粉并检验反应产物,实验装置如图。下列说法不正确的是(
)A.在锌粒中加入几粒硫酸铜晶体可能加快H 的生成
2
B.装置②、③中的药品分别是无水硫酸铜、氯化钙
C.装置①、④中药品为浓HSO
2 4
D.加热装置Y前,应先让X反应一段时间,排除装置中的空气
【答案】C
【解析】根据实验目的“探究用氢气和碳酸亚铁制取铁粉并检验反应产物”,结合装置图
分析可知,X装置为Zn和稀硫酸发生置换反应制备H 的装置,①装置盛有浓硫酸干燥H,Y
2 2
装置为氢气和碳酸亚铁制取铁粉的装置,②为检验产物HO的装置,③装置的主要目的是吸
2
收HO并防止④中的HO进入②装置中造成干扰,④为检验CO 的装置,据此分析解答问题。
2 2 2
A.X装置为Zn和稀硫酸发生置换反应制备H 的装置,在锌粒中加入几粒硫酸铜晶体,铜离
2
子会与锌粒发生置换反应,在锌粒表面附着铜单质,构成微型原电池,加快反应速率,A正确;
B.②为检验产物HO的装置,可盛装白色的无水硫酸铜固体,③装置的主要目的是吸收HO
2 2
并防止④中的HO进入②装置中造成干扰,可以是无水CaCl ,B正确;C.装置①作用是干燥,
2 2
装置④作用是检验二氧化碳产物,药品依次是浓HSO 和澄清石灰水,C错误;D.H 与空气
2 4 2
混合加热易发生爆炸,故在加热装置Y前,应先让X反应一段时间,排除装置中的空气,D正
确;答案选C。
8.由硫铁矿烧渣(主要成分:Fe O、Fe O 和FeO)得到绿矾(FeSO ·7H O),再通过绿矾制备铁
3 4 2 3 4 2
黄[FeO(OH)]的流程如下:烧渣 溶液 绿矾 铁黄。已
知:FeS 和铁黄均难溶于水。下列说法不正确的是( )
2
A.步骤①,最好用硫酸来溶解烧渣
B.步骤②,涉及的离子反应为FeS+14Fe3++8H O=15Fe2++2SO+16H+
2 2
C.步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
D.步骤④,反应条件控制不当会使铁黄中混有Fe(OH)
3
【答案】C
【解析】由硫铁矿烧渣制备绿矾流程可知,烧渣(主要成分:Fe O、Fe O 和FeO)均溶于硫
3 4 2 3酸,溶液含Fe2+、Fe3+,步骤②发生FeS+7Fe (SO )+8H O=15FeSO +8H SO ,步骤③为蒸发浓
2 2 4 3 2 4 2 4
缩、冷却结晶析出绿矾,绿矾与氨水、空气可发生反应生成铁黄。A.因中间产品为绿矾,其酸
根离子为硫酸根离子,则步骤①最好用硫酸来溶解烧渣,故A说法正确;B.结合分析,步骤
②中加入FeS 可以将Fe3+还原为Fe2+,该反应的化学方程式为FeS+7Fe (SO )
2 2 2 4 3
+8H O=15FeSO +8H SO ,离子反应为FeS+14Fe3++8H O=15Fe2++2SO+16H+,故B说法正确;
2 4 2 4 2 2
C.步骤③为蒸发浓缩、冷却结晶析出绿矾,若蒸干液体,绿矾受热会失去结晶水,则得不到
绿矾,故C说法错误;D.步骤④,反应条件应控制适当,若氨水的用量过大会使溶液的pH过
大,容易生成Fe(OH) ,这样制得的铁黄会含有氢氧化铁杂质,故D说法正确;答案选C。
3
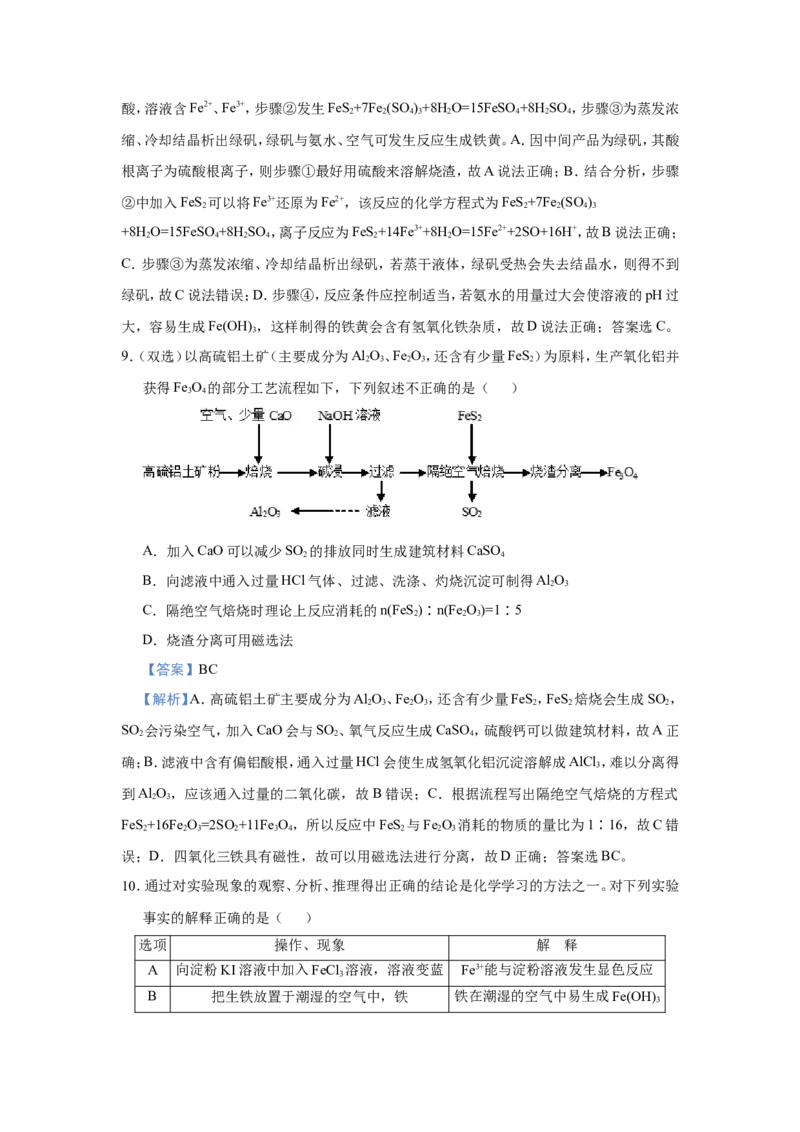
9.(双选)以高硫铝土矿(主要成分为Al O、Fe O,还含有少量FeS)为原料,生产氧化铝并
2 3 2 3 2
获得Fe O 的部分工艺流程如下,下列叙述不正确的是( )
3 4
A.加入CaO可以减少SO 的排放同时生成建筑材料CaSO
2 4
B.向滤液中通入过量HCl气体、过滤、洗涤、灼烧沉淀可制得Al O
2 3
C.隔绝空气焙烧时理论上反应消耗的n(FeS )∶n(Fe O)=1∶5
2 2 3
D.烧渣分离可用磁选法
【答案】BC
【解析】A.高硫铝土矿主要成分为Al O、Fe O,还含有少量FeS,FeS 焙烧会生成SO ,
2 3 2 3 2 2 2
SO 会污染空气,加入CaO会与SO 、氧气反应生成CaSO,硫酸钙可以做建筑材料,故A正
2 2 4
确;B.滤液中含有偏铝酸根,通入过量HCl会使生成氢氧化铝沉淀溶解成AlCl ,难以分离得
3
到Al O ,应该通入过量的二氧化碳,故B错误;C.根据流程写出隔绝空气焙烧的方程式
2 3
FeS+16Fe O=2SO+11Fe O,所以反应中FeS 与Fe O 消耗的物质的量比为1∶16,故C错
2 2 3 2 3 4 2 2 3
误;D.四氧化三铁具有磁性,故可以用磁选法进行分离,故D正确;答案选BC。
10.通过对实验现象的观察、分析、推理得出正确的结论是化学学习的方法之一。对下列实验
事实的解释正确的是( )
选项 操作、现象 解 释
A 向淀粉KI溶液中加入FeCl 溶液,溶液变蓝 Fe3+能与淀粉溶液发生显色反应
3
B 把生铁放置于潮湿的空气中,铁 铁在潮湿的空气中易生成Fe(OH)
3表面有一层红棕色的斑点
说明Fe置换出溶液中的
C 向稀硝酸中加入少量铁粉,有气泡产生
氢,生成了氢气
新制Fe(OH) 露置于空气中一段时 说明Fe(OH) 易被O
2 2 2
D
间,白色物质变成了红褐色 氧化成Fe(OH)
3
【答案】D
【解析】Fe3+与I−发生反应:2Fe3++2I−=I+2Fe2+,生成的碘单质使淀粉溶液变蓝,A错误;铁
2
在潮湿的空气中易生锈,铁锈的主要成分是Fe O·xHO,B错误;铁与稀硝酸反应生成的气
2 3 2
体为NO,不能得到氢气,C错误;Fe(OH) 露置于空气中,易被O 氧化成Fe(OH) ,由白色变
2 2 3
为红褐色,反应的化学方程式为4Fe(OH) +O +2H O=4Fe(OH) ,D正确。
2 2 2 3
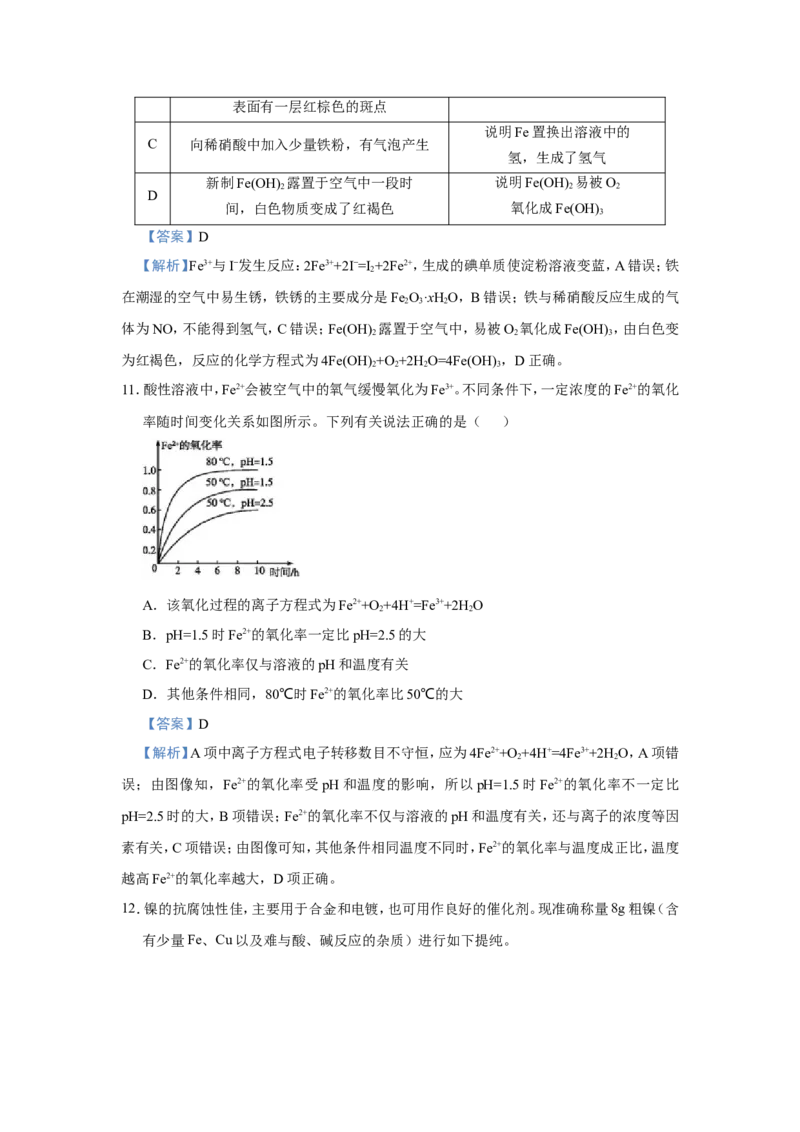
11.酸性溶液中,Fe2+会被空气中的氧气缓慢氧化为Fe3+。不同条件下,一定浓度的Fe2+的氧化
率随时间变化关系如图所示。下列有关说法正确的是( )
A.该氧化过程的离子方程式为Fe2++O +4H+=Fe3++2H O
2 2
B.pH=1.5时Fe2+的氧化率一定比pH=2.5的大
C.Fe2+的氧化率仅与溶液的pH和温度有关
D.其他条件相同,80℃时Fe2+的氧化率比50℃的大
【答案】D
【解析】A项中离子方程式电子转移数目不守恒,应为4Fe2++O +4H+=4Fe3++2H O,A项错
2 2
误;由图像知,Fe2+的氧化率受pH和温度的影响,所以pH=1.5时Fe2+的氧化率不一定比
pH=2.5时的大,B项错误;Fe2+的氧化率不仅与溶液的pH和温度有关,还与离子的浓度等因
素有关,C项错误;由图像可知,其他条件相同温度不同时,Fe2+的氧化率与温度成正比,温度
越高Fe2+的氧化率越大,D项正确。
12.镍的抗腐蚀性佳,主要用于合金和电镀,也可用作良好的催化剂。现准确称量8g粗镍(含
有少量Fe、Cu以及难与酸、碱反应的杂质)进行如下提纯。请回答下列问题:
(1)写出稀硝酸溶解镍的离子方程式 。
(2)在溶液A的净化除杂中,首先将溶液A煮沸,调节pH=5.5,继续加热煮沸5min,加热
过程中补充适量的水保持溶液的体积不变,静止一段时间后,过滤出Fe O、FeO(OH)。
2 3
①写出煮沸过程中生成FeO(OH)的离子方程式 。
②控制溶液的pH,可利用 。
a.pH试纸 b.石蕊指示剂 c.pH计
③为了得到纯净的溶液B,还需要加入以下物质___(填字母)进行除杂。(已知:K(CuS)
sp
=8.8×10−36;K (NiS)=3.2×10−19;K [Cu(OH) ]=2.2×10−20;K [Ni(OH) ]=5.4×10−16)
sp sp 2 sp 2
a.NaOH b.NaS c.HS d.NH ·H O
2 2 3 2
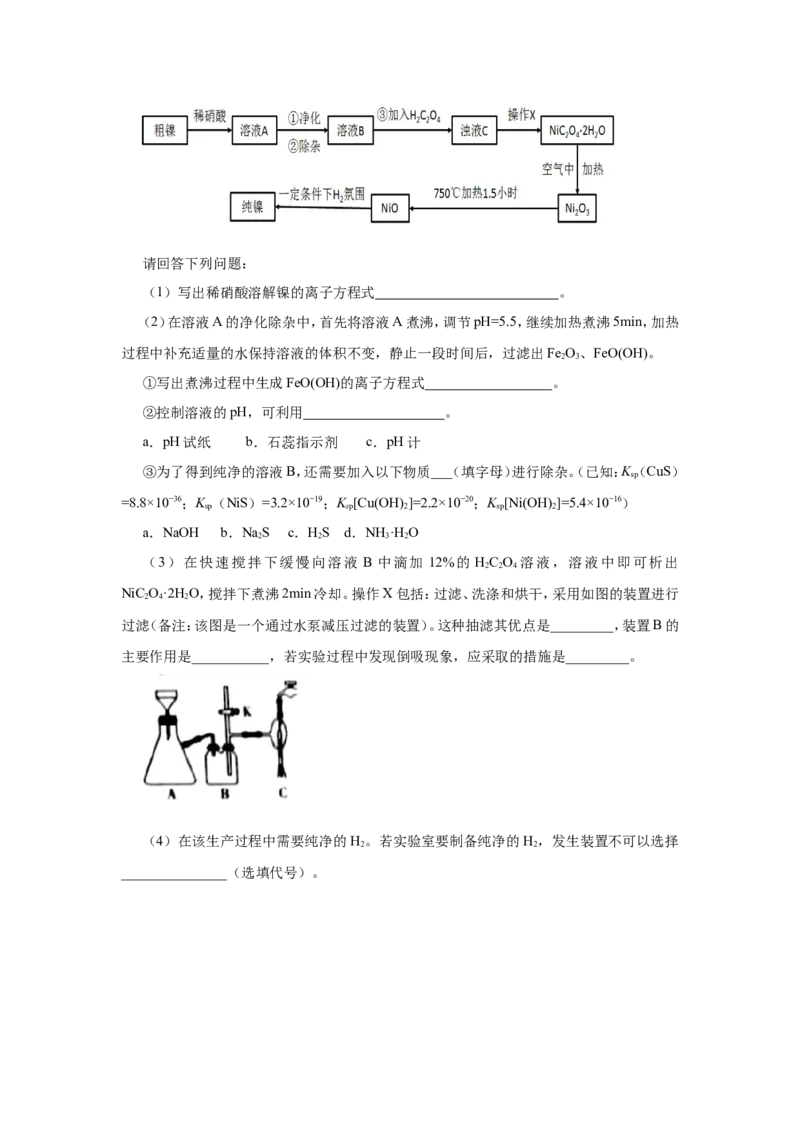
(3)在快速搅拌下缓慢向溶液 B 中滴加 12%的 HC O 溶液,溶液中即可析出
2 2 4
NiC O·2H O,搅拌下煮沸2min冷却。操作X包括:过滤、洗涤和烘干,采用如图的装置进行
2 4 2
过滤(备注:该图是一个通过水泵减压过滤的装置)。这种抽滤其优点是_________,装置B的
主要作用是___________,若实验过程中发现倒吸现象,应采取的措施是_________。
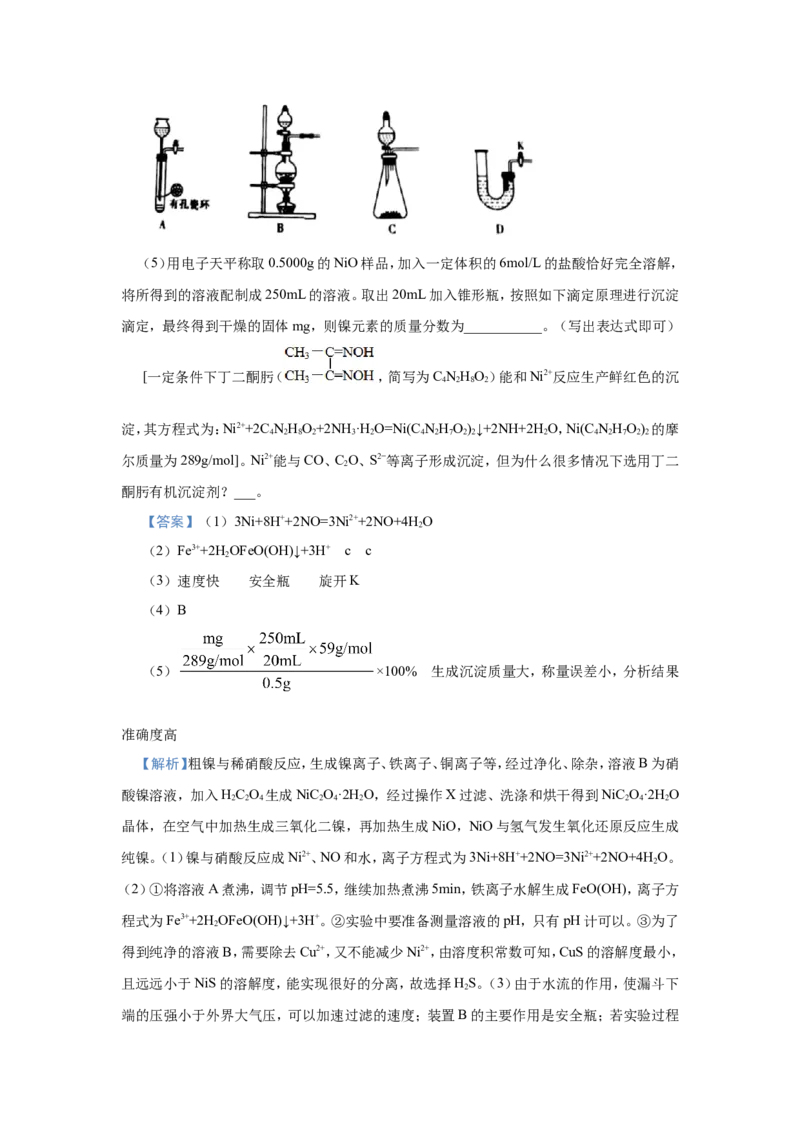
(4)在该生产过程中需要纯净的H。若实验室要制备纯净的H,发生装置不可以选择
2 2
_______________(选填代号)。(5)用电子天平称取0.5000g的NiO样品,加入一定体积的6mol/L的盐酸恰好完全溶解,
将所得到的溶液配制成250mL的溶液。取出20mL加入锥形瓶,按照如下滴定原理进行沉淀
滴定,最终得到干燥的固体mg,则镍元素的质量分数为___________。(写出表达式即可)
[一定条件下丁二酮肟( ,简写为C NHO)能和Ni2+反应生产鲜红色的沉
4 2 8 2
淀,其方程式为:Ni2++2C NHO+2NH·H O=Ni(C NHO)↓+2NH+2HO,Ni(C NHO) 的摩
4 2 8 2 3 2 4 2 7 2 2 2 4 2 7 2 2
尔质量为289g/mol]。Ni2+能与CO、C O、S2−等离子形成沉淀,但为什么很多情况下选用丁二
2
酮肟有机沉淀剂?___。
【答案】(1)3Ni+8H++2NO=3Ni2++2NO+4HO
2
(2)Fe3++2H OFeO(OH)↓+3H+ c c
2
(3)速度快 安全瓶 旋开K
(4)B
(5) ×100% 生成沉淀质量大,称量误差小,分析结果
准确度高
【解析】粗镍与稀硝酸反应,生成镍离子、铁离子、铜离子等,经过净化、除杂,溶液B为硝
酸镍溶液,加入HC O 生成NiC O·2H O,经过操作X过滤、洗涤和烘干得到NiC O·2H O
2 2 4 2 4 2 2 4 2
晶体,在空气中加热生成三氧化二镍,再加热生成NiO,NiO与氢气发生氧化还原反应生成
纯镍。(1)镍与硝酸反应成Ni2+、NO和水,离子方程式为3Ni+8H++2NO=3Ni2++2NO+4HO。
2
(2)①将溶液A煮沸,调节pH=5.5,继续加热煮沸5min,铁离子水解生成FeO(OH),离子方
程式为Fe3++2H OFeO(OH)↓+3H+。②实验中要准备测量溶液的pH,只有pH计可以。③为了
2
得到纯净的溶液B,需要除去Cu2+,又不能减少Ni2+,由溶度积常数可知,CuS的溶解度最小,
且远远小于NiS的溶解度,能实现很好的分离,故选择HS。(3)由于水流的作用,使漏斗下
2
端的压强小于外界大气压,可以加速过滤的速度;装置B的主要作用是安全瓶;若实验过程中发生倒吸现象,先旋开旋塞K,恢复常压后关闭抽水泵。(4)实验室制氢气采用锌与稀硫酸
反应,不需要加热,装置B为加热制气装置,不符合题意,答案选B。(5)NiO与盐酸反应生成
Ni2+ , 取 250mL 中 的 20mL 溶 液 用 丁 二 酮 肟 滴 定 Ni2+ 发 生 反 Ni2+
+2C NHO+2NH·H O=Ni(C NHO)↓+2NH+2HO,得到干燥的固体mg,则Ni(C NHO)
4 2 8 2 3 2 4 2 7 2 2 2 4 2 7 2 2
的质量为 mg,其中镍元素的质量为 ;则 0.5g 样品中镍元素的质量为
,镍元素的质量分数为 ×100%。