文档内容
选择题突破二
(选择题每小题3分)
题组一 阿伏加德罗常数的正误判断
1.(2024·七省适应性测试贵州化学,3)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.标准状况下,2.24 L 18O 含有的中子数为2N
2 A
B.常温下,1.7 g HS中含有的孤电子对数为0.2N
2 A
C.1.0 L 0.1 mol·L-1 CuSO 溶液中含有的Cu2+数为0.1N
4 A
D.0.2 mol SO 与足量O 充分反应转移的电子数为0.4N
2 2 A
2.(2024·七省适应性测试江西化学,4改编)火箭表面耐高温涂层的制备反应为4Al+3TiO+3C
2
2Al O+3TiC。设阿伏加德罗常数的值为N ,下列说法正确的是( )
2 3 A
A.1 mol C中共价键的数目为4N
A
48
B.6 g TiC中含有的中子数为3N
22 A
C.1 mol Al O 与足量稀硫酸反应后溶液中Al3+的数目为2N
2 3 A
D.消耗1 mol TiO 时,该反应中转移的电子数为4N
2 A
3.(2024·湖南益阳4月联考)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.24 g T 18 O的中子数为14N
2 A
B.标准状况下,22.4 L HF所含的原子数为2N
A
C.2 g H 与足量的碘蒸气充分反应,生成HI的数目为2N
2 A
D.56 g Fe与足量的水蒸气完全反应,转移的电子数为8N
A
4.(2024·广东汕头一模)微观探析是认识物质的一种途径。设N 为阿伏加德罗常数的值,下列有关说
A
法正确的是( )
A.1.8 g D O中含有的中子数目为N
2 A
B.1 mol·L-1 CuCl 溶液中含有Cu2+的数目小于N
2 A
C.46 g NO 与NO 的混合物中含有的分子数为N
2 2 4 A
D.25 ℃、101 kPa时的气体摩尔体积是24.5 L·mol-1,该条件下2.45 L Cl 与NaOH溶液完全反应时转
2
移电子数目为0.1N
A
5.(2024·东北三省四市联考)常温常压下,电化学合成氨总反应方程式为2N+6H O 4NH +3O ,
2 2 3 2
设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.28 g氮气含有的共用电子对数为0.3N
A
B.每产生34 g NH ,N 失去电子数为6N
3 2 A
C.1 mol·L-1氨水中,含NH ·H O分子数小于N
3 2 A
D.标准状况下,11.2 L N 参加反应时,产生O 分子数为0.75N
2 2 A6.(2024·安徽淮北一模)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.常温下,46 g NO 中分子的数目为N
2 A
B.100 mL 0.1 mol·L-1 H PO
溶液中PO3-
的数目为0.01N
3 4 4 A
C.30 g CH COOH中含有σ键的数目为3.5N
3 A
D.100 mL 18.4 mol·L-1的浓硫酸中H+的数目为3.68N
A
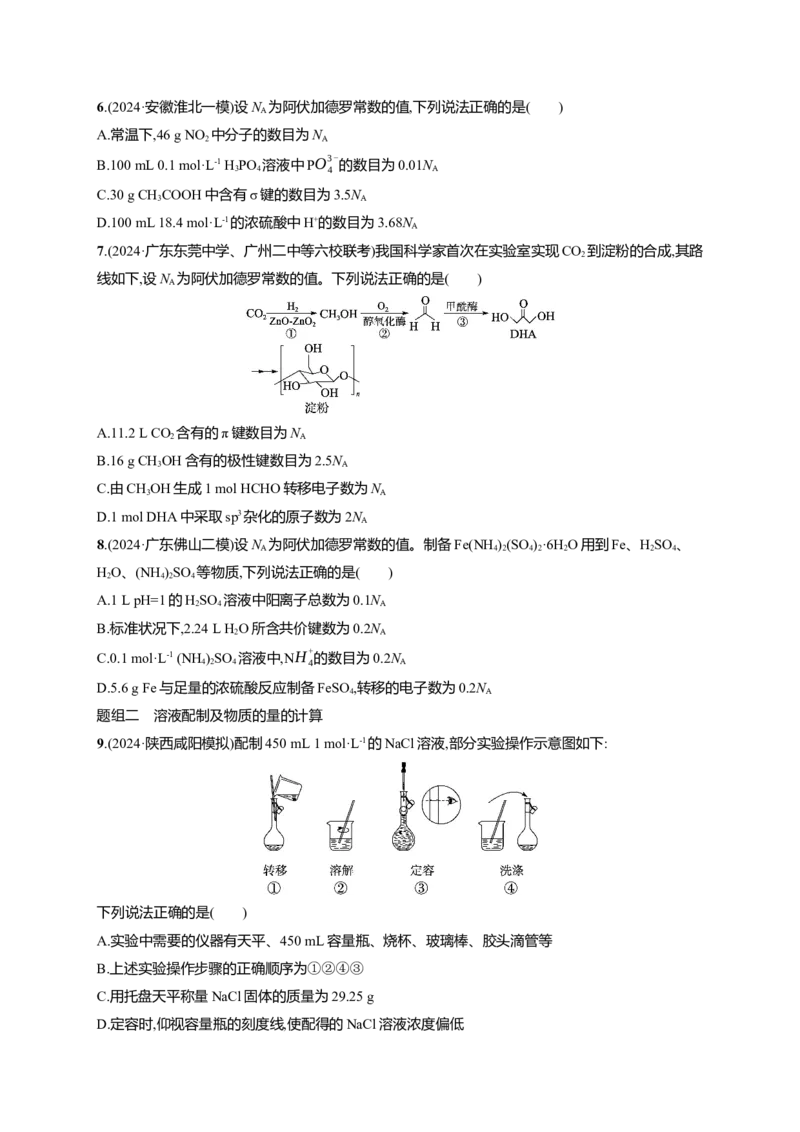
7.(2024·广东东莞中学、广州二中等六校联考)我国科学家首次在实验室实现CO 到淀粉的合成,其路
2
线如下,设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.11.2 L CO 含有的π键数目为N
2 A
B.16 g CH OH含有的极性键数目为2.5N
3 A
C.由CHOH生成1 mol HCHO转移电子数为N
3 A
D.1 mol DHA中采取sp3杂化的原子数为2N
A
8.(2024·广东佛山二模)设N 为阿伏加德罗常数的值。制备Fe(NH )(SO )·6H O用到Fe、HSO 、
A 4 2 4 2 2 2 4
HO、(NH )SO 等物质,下列说法正确的是( )
2 4 2 4
A.1 L pH=1的HSO 溶液中阳离子总数为0.1N
2 4 A
B.标准状况下,2.24 L HO所含共价键数为0.2N
2 A
C.0.1 mol·L-1 (NH)SO
溶液中,NH+
的数目为0.2N
4 2 4 4 A
D.5.6 g Fe与足量的浓硫酸反应制备FeSO ,转移的电子数为0.2N
4 A
题组二 溶液配制及物质的量的计算
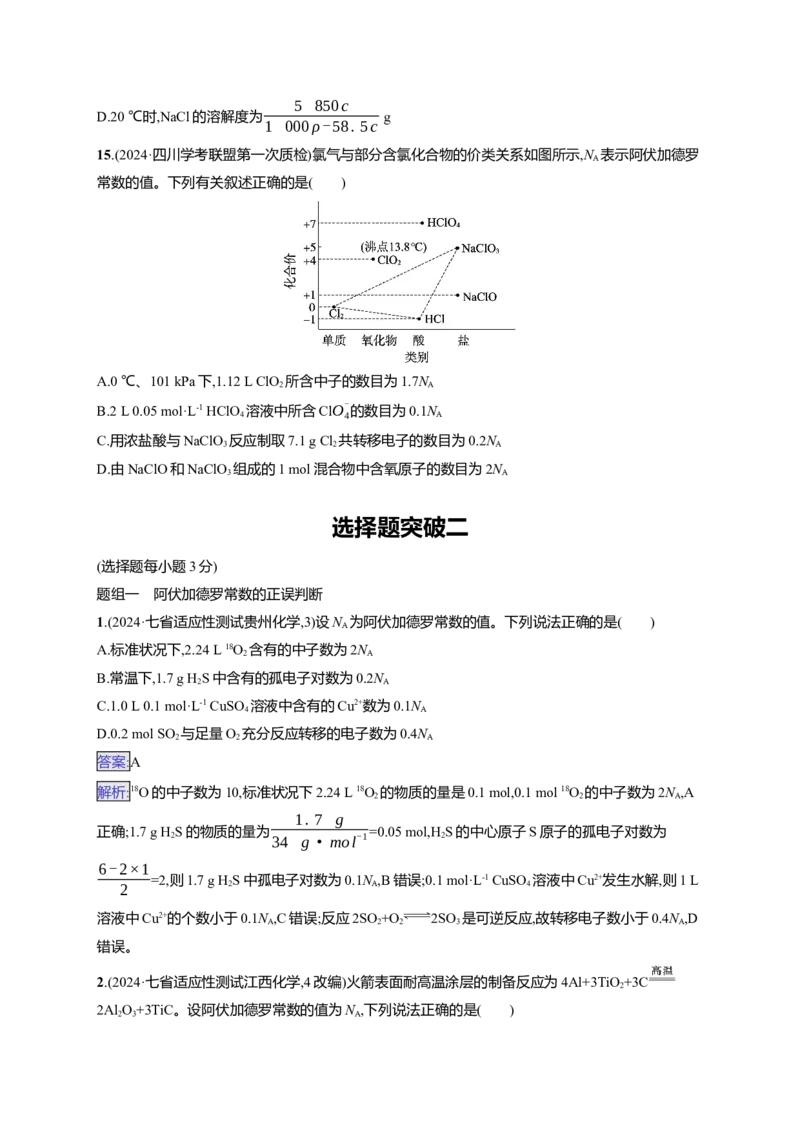
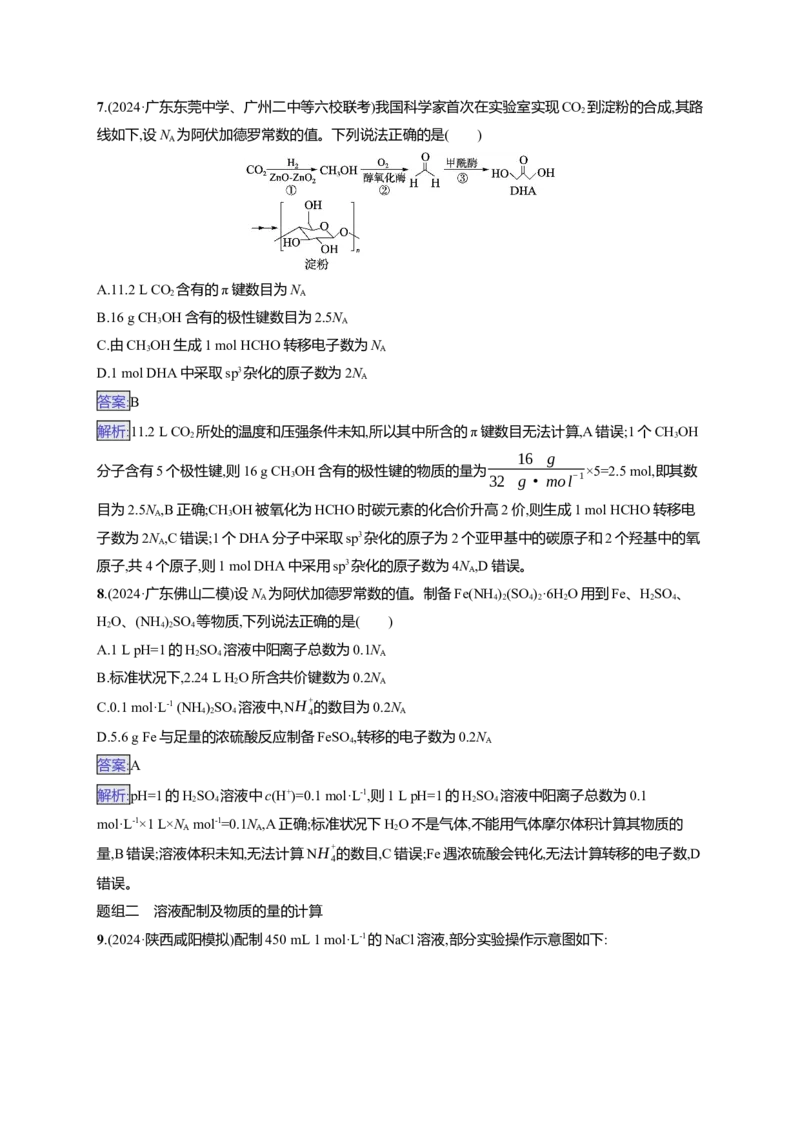
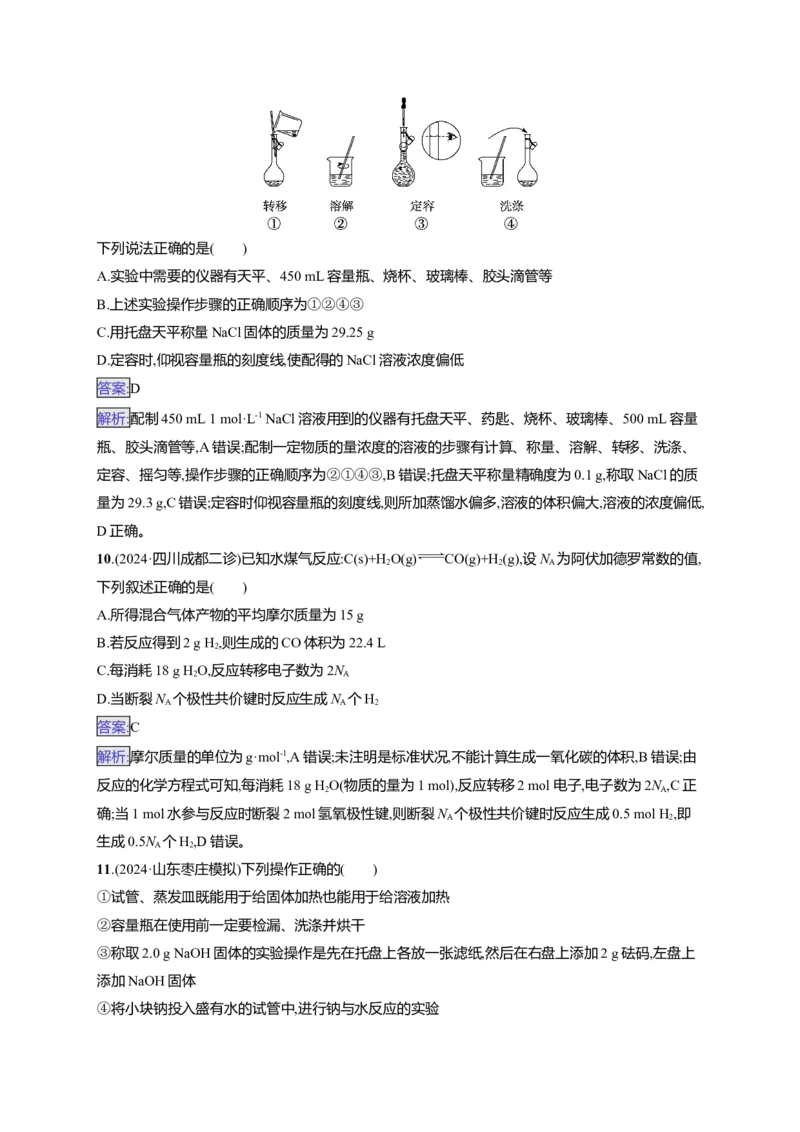
9.(2024·陕西咸阳模拟)配制450 mL 1 mol·L-1的NaCl溶液,部分实验操作示意图如下:
下列说法正确的是( )
A.实验中需要的仪器有天平、450 mL容量瓶、烧杯、玻璃棒、胶头滴管等
B.上述实验操作步骤的正确顺序为①②④③
C.用托盘天平称量NaCl固体的质量为29.25 g
D.定容时,仰视容量瓶的刻度线,使配得的NaCl溶液浓度偏低10.(2024·四川成都二诊)已知水煤气反应:C(s)+H O(g) CO(g)+H(g),设N 为阿伏加德罗常数的值,
2 2 A
下列叙述正确的是( )
A.所得混合气体产物的平均摩尔质量为15 g
B.若反应得到2 g H,则生成的CO体积为22.4 L
2
C.每消耗18 g HO,反应转移电子数为2N
2 A
D.当断裂N 个极性共价键时反应生成N 个H
A A 2
11.(2024·山东枣庄模拟)下列操作正确的( )
①试管、蒸发皿既能用于给固体加热也能用于给溶液加热
②容量瓶在使用前一定要检漏、洗涤并烘干
③称取2.0 g NaOH固体的实验操作是先在托盘上各放一张滤纸,然后在右盘上添加2 g砝码,左盘上
添加NaOH固体
④将小块钠投入盛有水的试管中,进行钠与水反应的实验
⑤配制一定浓度的NaCO 溶液时,将称得的碳酸钠小心转移至250 mL容量瓶中,加入蒸馏水至刻度
2 3
线
A.3个 B.2个 C.1个 D.0个
12.(2024·河南驻马店模拟)下列有关叙述正确的是( )
A.标准状况下,等体积的SO 和CHCl所含分子数相等
3 3
B.等物质的量的HO、DO、TO所含中子数相等
2 2 2
C.11.2 g Fe和13 g Zn分别与足量稀硫酸反应失去的电子数相等
D.1 mol H 分别与足量I(g)、F(g)完全反应生成的HX(X为I或F)分子数相等
2 2 2
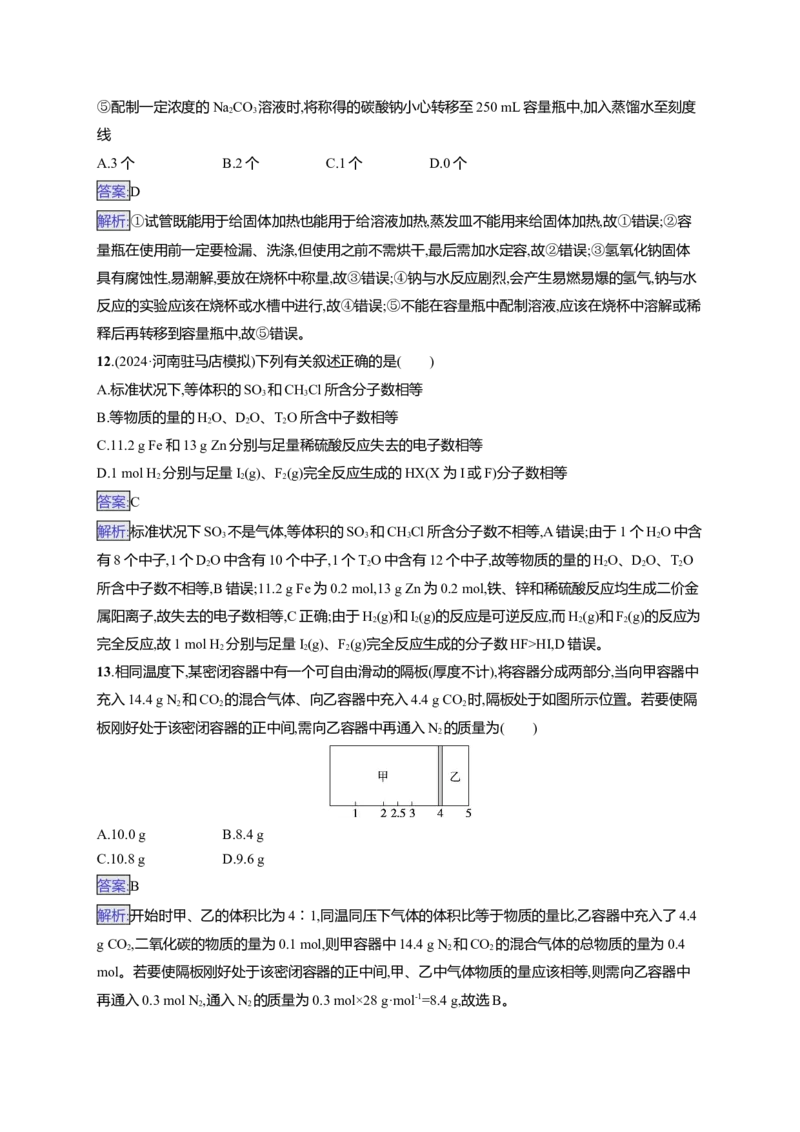
13.相同温度下,某密闭容器中有一个可自由滑动的隔板(厚度不计),将容器分成两部分,当向甲容器中
充入14.4 g N 和CO 的混合气体、向乙容器中充入4.4 g CO 时,隔板处于如图所示位置。若要使隔
2 2 2
板刚好处于该密闭容器的正中间,需向乙容器中再通入N 的质量为( )
2
A.10.0 g B.8.4 g
C.10.8 g D.9.6 g
14.(2024·陕西宝鸡检测)20 ℃时,饱和NaCl溶液的密度为ρ g·cm-3,物质的量浓度为c mol·L-1,则下列
说法错误的是( )
A.温度低于20 ℃时,饱和NaCl溶液的浓度小于c mol·L-1
58.5c
B.20 ℃时,饱和NaCl溶液中NaCl的质量分数为 ×100%
1 000ρ
C.20 ℃时,将58.5 g NaCl溶解在1 L水中,所得溶液的浓度为1 mol·L-15 850c
D.20 ℃时,NaCl的溶解度为 g
1 000ρ-58.5c
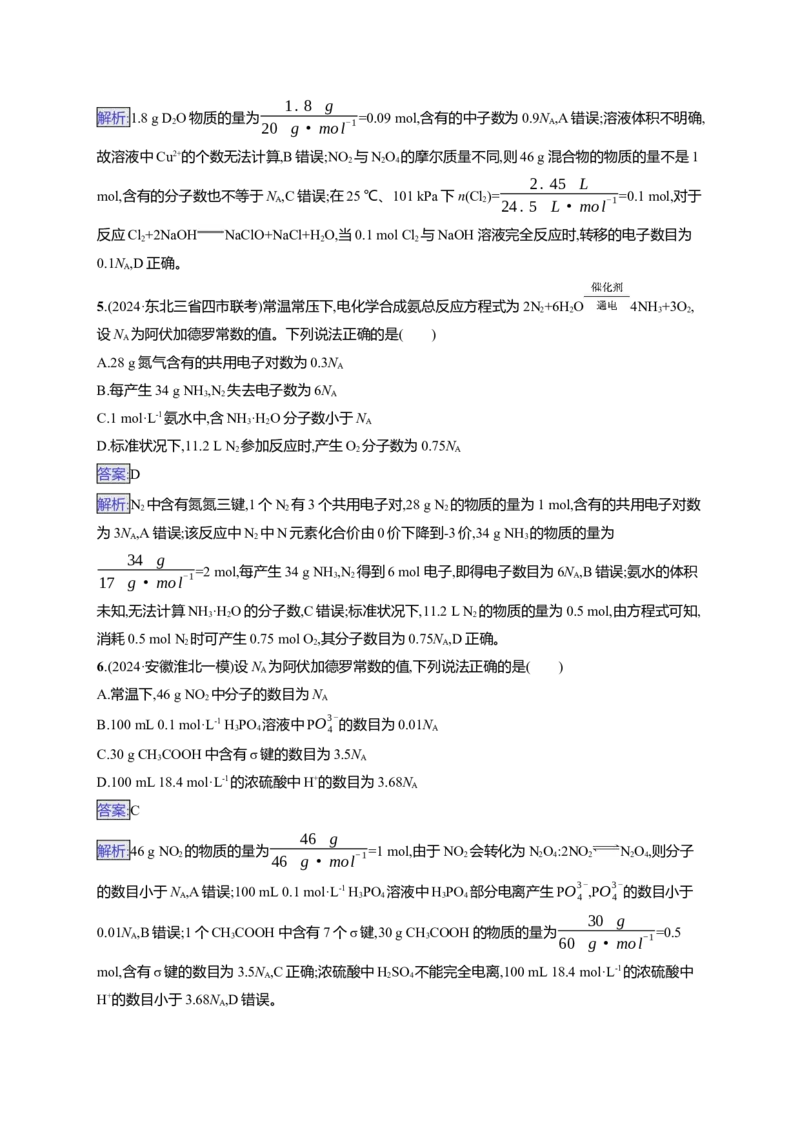
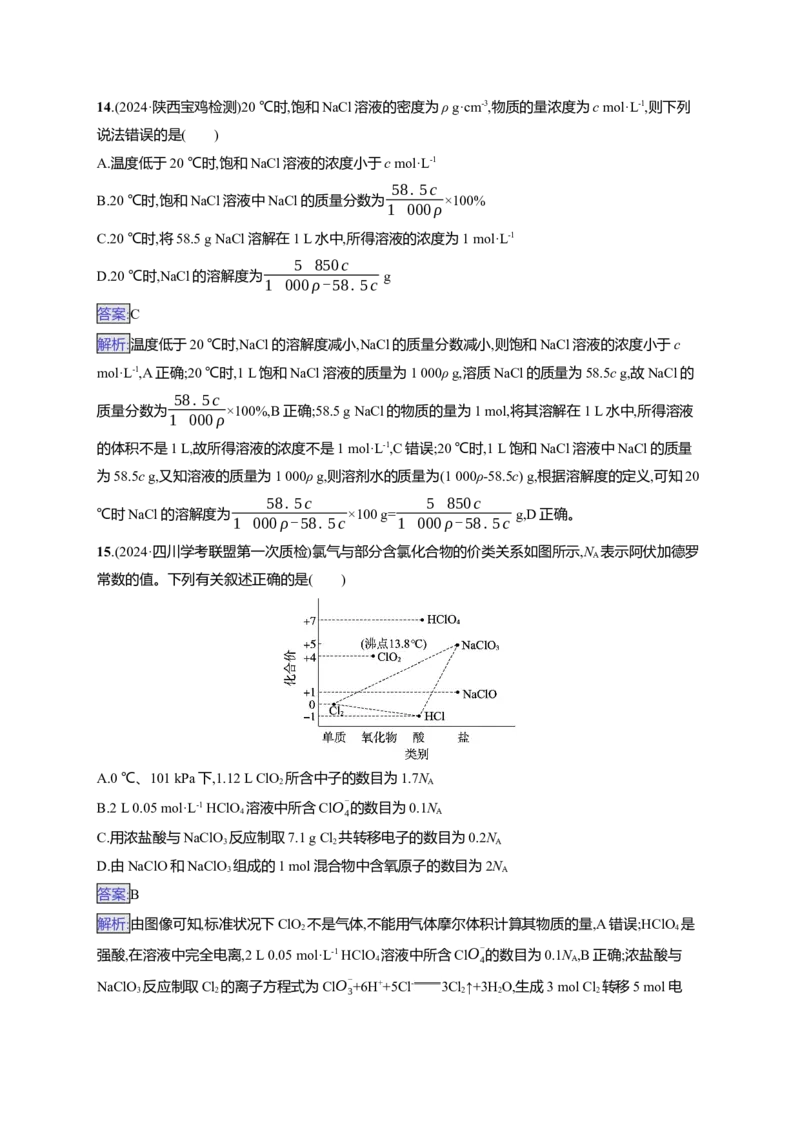
15.(2024·四川学考联盟第一次质检)氯气与部分含氯化合物的价类关系如图所示,N 表示阿伏加德罗
A
常数的值。下列有关叙述正确的是( )
A.0 ℃、101 kPa下,1.12 L ClO 所含中子的数目为1.7N
2 A
B.2 L 0.05 mol·L-1 HClO
溶液中所含ClO-
的数目为0.1N
4 4 A
C.用浓盐酸与NaClO 反应制取7.1 g Cl 共转移电子的数目为0.2N
3 2 A
D.由NaClO和NaClO 组成的1 mol混合物中含氧原子的数目为2N
3 A
选择题突破二
(选择题每小题3分)
题组一 阿伏加德罗常数的正误判断
1.(2024·七省适应性测试贵州化学,3)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.标准状况下,2.24 L 18O 含有的中子数为2N
2 A
B.常温下,1.7 g HS中含有的孤电子对数为0.2N
2 A
C.1.0 L 0.1 mol·L-1 CuSO 溶液中含有的Cu2+数为0.1N
4 A
D.0.2 mol SO 与足量O 充分反应转移的电子数为0.4N
2 2 A
答案:A
解析:18O的中子数为10,标准状况下2.24 L 18O 的物质的量是0.1 mol,0.1 mol 18O 的中子数为2N ,A
2 2 A
1.7 g
正确;1.7 g H S的物质的量为 =0.05 mol,H S的中心原子S原子的孤电子对数为
2 34 g·mol-1 2
6-2×1
=2,则1.7 g H S中孤电子对数为0.1N ,B错误;0.1 mol·L-1 CuSO 溶液中Cu2+发生水解,则1 L
2 2 A 4
溶液中Cu2+的个数小于0.1N ,C错误;反应2SO +O 2SO 是可逆反应,故转移电子数小于0.4N ,D
A 2 2 3 A
错误。
2.(2024·七省适应性测试江西化学,4改编)火箭表面耐高温涂层的制备反应为4Al+3TiO+3C
2
2Al O+3TiC。设阿伏加德罗常数的值为N ,下列说法正确的是( )
2 3 AA.1 mol C中共价键的数目为4N
A
48
B.6 g TiC中含有的中子数为3N
22 A
C.1 mol Al O 与足量稀硫酸反应后溶液中Al3+的数目为2N
2 3 A
D.消耗1 mol TiO 时,该反应中转移的电子数为4N
2 A
答案:D
48
解析:由于碳单质的结构不确定,因此无法确定共价键的数目,A错误;6 g TiC的物质的量为
22
6 g
=0.1
mol,48
TiC中含有的中子数为48-22+6=32,故6 g
48
TiC中含有的中子数为
60 g·mol-1 22 22
3.2N ,B错误;Al O 与HSO 反应生成Al (SO ) 和HO,由于Al3+会发生水解,则溶液中Al3+的数目小
A 2 3 2 4 2 4 3 2
于2N ,C错误;由4Al+3TiO+3C 2Al O+3TiC可知,消耗3 mol TiO,转移的电子数为12N ,则消耗
A 2 2 3 2 A
1 mol TiO 时该反应中转移的电子数为4N ,D正确。
2 A
3.(2024·湖南益阳4月联考)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.24 g T 18 O的中子数为14N
2 A
B.标准状况下,22.4 L HF所含的原子数为2N
A
C.2 g H 与足量的碘蒸气充分反应,生成HI的数目为2N
2 A
D.56 g Fe与足量的水蒸气完全反应,转移的电子数为8N
A
答案:A
24 g
解析:24 g T 18 O的中子数为 ×14×N mol-1=14N ,A正确;标准状况下,HF为液体,不能
2 24 g·mol-1 A A
用气体摩尔体积计算其物质的量,B错误;I 与H 的反应为可逆反应,反应物不能完全转化为生成物,则
2 2
生成HI的分子数小于2N ,C错误;56 g Fe与足量的水蒸气完全反应生成Fe O 和氢气,转移的电子数
A 3 4
56 g 8 8
为 × ×N mol-1= N ,D错误。
56 g·mol-1 3 A 3 A
4.(2024·广东汕头一模)微观探析是认识物质的一种途径。设N 为阿伏加德罗常数的值,下列有关说
A
法正确的是( )
A.1.8 g D O中含有的中子数目为N
2 A
B.1 mol·L-1 CuCl 溶液中含有Cu2+的数目小于N
2 A
C.46 g NO 与NO 的混合物中含有的分子数为N
2 2 4 A
D.25 ℃、101 kPa时的气体摩尔体积是24.5 L·mol-1,该条件下2.45 L Cl 与NaOH溶液完全反应时转
2
移电子数目为0.1N
A
答案:D1.8 g
解析:1.8 g D O物质的量为 =0.09 mol,含有的中子数为0.9N ,A错误;溶液体积不明确,
2 20 g·mol-1 A
故溶液中Cu2+的个数无法计算,B错误;NO 与NO 的摩尔质量不同,则46 g混合物的物质的量不是1
2 2 4
2.45 L
mol,含有的分子数也不等于N ,C错误;在25 ℃、101 kPa下n(Cl )= =0.1 mol,对于
A 2 24.5 L·mol-1
反应Cl+2NaOH NaClO+NaCl+H O,当0.1 mol Cl 与NaOH溶液完全反应时,转移的电子数目为
2 2 2
0.1N ,D正确。
A
5.(2024·东北三省四市联考)常温常压下,电化学合成氨总反应方程式为2N+6H O 4NH +3O ,
2 2 3 2
设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.28 g氮气含有的共用电子对数为0.3N
A
B.每产生34 g NH ,N 失去电子数为6N
3 2 A
C.1 mol·L-1氨水中,含NH ·H O分子数小于N
3 2 A
D.标准状况下,11.2 L N 参加反应时,产生O 分子数为0.75N
2 2 A
答案:D
解析:N 中含有氮氮三键,1个N 有3个共用电子对,28 g N 的物质的量为1 mol,含有的共用电子对数
2 2 2
为3N ,A错误;该反应中N 中N元素化合价由0价下降到-3价,34 g NH 的物质的量为
A 2 3
34 g
=2 mol,每产生34 g NH ,N 得到6 mol 电子,即得电子数目为6N ,B错误;氨水的体积
17 g·mol-1 3 2 A
未知,无法计算NH ·H O的分子数,C错误;标准状况下,11.2 L N 的物质的量为0.5 mol,由方程式可知,
3 2 2
消耗0.5 mol N 时可产生0.75 mol O,其分子数目为0.75N ,D正确。
2 2 A
6.(2024·安徽淮北一模)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.常温下,46 g NO 中分子的数目为N
2 A
B.100 mL 0.1 mol·L-1 H PO
溶液中PO3-
的数目为0.01N
3 4 4 A
C.30 g CH COOH中含有σ键的数目为3.5N
3 A
D.100 mL 18.4 mol·L-1的浓硫酸中H+的数目为3.68N
A
答案:C
46 g
解析:46 g NO 的物质的量为 =1 mol,由于NO 会转化为NO:2NO NO,则分子
2 46 g·mol-1 2 2 4 2 2 4
的数目小于N ,A错误;100 mL 0.1 mol·L-1 H PO 溶液中HPO
部分电离产生PO3- ,PO3-
的数目小于
A 3 4 3 4 4 4
30 g
0.01N ,B错误;1个CHCOOH中含有7个σ键,30 g CH COOH的物质的量为 =0.5
A 3 3 60 g·mol-1
mol,含有σ键的数目为3.5N ,C正确;浓硫酸中HSO 不能完全电离,100 mL 18.4 mol·L-1的浓硫酸中
A 2 4
H+的数目小于3.68N ,D错误。
A7.(2024·广东东莞中学、广州二中等六校联考)我国科学家首次在实验室实现CO 到淀粉的合成,其路
2
线如下,设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.11.2 L CO 含有的π键数目为N
2 A
B.16 g CH OH含有的极性键数目为2.5N
3 A
C.由CHOH生成1 mol HCHO转移电子数为N
3 A
D.1 mol DHA中采取sp3杂化的原子数为2N
A
答案:B
解析:11.2 L CO 所处的温度和压强条件未知,所以其中所含的π键数目无法计算,A错误;1个CHOH
2 3
16 g
分子含有5个极性键,则16 g CHOH含有的极性键的物质的量为 ×5=2.5 mol,即其数
3 32 g·mol-1
目为2.5N ,B正确;CH OH被氧化为HCHO时碳元素的化合价升高2价,则生成1 mol HCHO转移电
A 3
子数为2N ,C错误;1个DHA分子中采取sp3杂化的原子为2个亚甲基中的碳原子和2个羟基中的氧
A
原子,共4个原子,则1 mol DHA中采用sp3杂化的原子数为4N ,D错误。
A
8.(2024·广东佛山二模)设N 为阿伏加德罗常数的值。制备Fe(NH )(SO )·6H O用到Fe、HSO 、
A 4 2 4 2 2 2 4
HO、(NH )SO 等物质,下列说法正确的是( )
2 4 2 4
A.1 L pH=1的HSO 溶液中阳离子总数为0.1N
2 4 A
B.标准状况下,2.24 L HO所含共价键数为0.2N
2 A
C.0.1 mol·L-1 (NH)SO
溶液中,NH+
的数目为0.2N
4 2 4 4 A
D.5.6 g Fe与足量的浓硫酸反应制备FeSO ,转移的电子数为0.2N
4 A
答案:A
解析:pH=1的HSO 溶液中c(H+)=0.1 mol·L-1,则1 L pH=1的HSO 溶液中阳离子总数为0.1
2 4 2 4
mol·L-1×1 L×N mol-1=0.1N ,A正确;标准状况下HO不是气体,不能用气体摩尔体积计算其物质的
A A 2
量,B错误;溶液体积未知,无法计算NH+
的数目,C错误;Fe遇浓硫酸会钝化,无法计算转移的电子数,D
4
错误。
题组二 溶液配制及物质的量的计算
9.(2024·陕西咸阳模拟)配制450 mL 1 mol·L-1的NaCl溶液,部分实验操作示意图如下:下列说法正确的是( )
A.实验中需要的仪器有天平、450 mL容量瓶、烧杯、玻璃棒、胶头滴管等
B.上述实验操作步骤的正确顺序为①②④③
C.用托盘天平称量NaCl固体的质量为29.25 g
D.定容时,仰视容量瓶的刻度线,使配得的NaCl溶液浓度偏低
答案:D
解析:配制450 mL 1 mol·L-1 NaCl溶液用到的仪器有托盘天平、药匙、烧杯、玻璃棒、500 mL容量
瓶、胶头滴管等,A错误;配制一定物质的量浓度的溶液的步骤有计算、称量、溶解、转移、洗涤、
定容、摇匀等,操作步骤的正确顺序为②①④③,B错误;托盘天平称量精确度为0.1 g,称取NaCl的质
量为29.3 g,C错误;定容时仰视容量瓶的刻度线,则所加蒸馏水偏多,溶液的体积偏大,溶液的浓度偏低,
D正确。
10.(2024·四川成都二诊)已知水煤气反应:C(s)+H O(g) CO(g)+H(g),设N 为阿伏加德罗常数的值,
2 2 A
下列叙述正确的是( )
A.所得混合气体产物的平均摩尔质量为15 g
B.若反应得到2 g H,则生成的CO体积为22.4 L
2
C.每消耗18 g HO,反应转移电子数为2N
2 A
D.当断裂N 个极性共价键时反应生成N 个H
A A 2
答案:C
解析:摩尔质量的单位为g·mol-1,A错误;未注明是标准状况,不能计算生成一氧化碳的体积,B错误;由
反应的化学方程式可知,每消耗18 g HO(物质的量为1 mol),反应转移2 mol 电子,电子数为2N ,C正
2 A
确;当1 mol水参与反应时断裂2 mol氢氧极性键,则断裂N 个极性共价键时反应生成0.5 mol H,即
A 2
生成0.5N 个H,D错误。
A 2
11.(2024·山东枣庄模拟)下列操作正确的( )
①试管、蒸发皿既能用于给固体加热也能用于给溶液加热
②容量瓶在使用前一定要检漏、洗涤并烘干
③称取2.0 g NaOH固体的实验操作是先在托盘上各放一张滤纸,然后在右盘上添加2 g砝码,左盘上
添加NaOH固体
④将小块钠投入盛有水的试管中,进行钠与水反应的实验⑤配制一定浓度的NaCO 溶液时,将称得的碳酸钠小心转移至250 mL容量瓶中,加入蒸馏水至刻度
2 3
线
A.3个 B.2个 C.1个 D.0个
答案:D
解析:①试管既能用于给固体加热也能用于给溶液加热,蒸发皿不能用来给固体加热,故①错误;②容
量瓶在使用前一定要检漏、洗涤,但使用之前不需烘干,最后需加水定容,故②错误;③氢氧化钠固体
具有腐蚀性,易潮解,要放在烧杯中称量,故③错误;④钠与水反应剧烈,会产生易燃易爆的氢气,钠与水
反应的实验应该在烧杯或水槽中进行,故④错误;⑤不能在容量瓶中配制溶液,应该在烧杯中溶解或稀
释后再转移到容量瓶中,故⑤错误。
12.(2024·河南驻马店模拟)下列有关叙述正确的是( )
A.标准状况下,等体积的SO 和CHCl所含分子数相等
3 3
B.等物质的量的HO、DO、TO所含中子数相等
2 2 2
C.11.2 g Fe和13 g Zn分别与足量稀硫酸反应失去的电子数相等
D.1 mol H 分别与足量I(g)、F(g)完全反应生成的HX(X为I或F)分子数相等
2 2 2
答案:C
解析:标准状况下SO 不是气体,等体积的SO 和CHCl所含分子数不相等,A错误;由于1个HO中含
3 3 3 2
有8个中子,1个DO中含有10个中子,1个TO中含有12个中子,故等物质的量的HO、DO、TO
2 2 2 2 2
所含中子数不相等,B错误;11.2 g Fe为0.2 mol,13 g Zn为0.2 mol,铁、锌和稀硫酸反应均生成二价金
属阳离子,故失去的电子数相等,C正确;由于H(g)和I(g)的反应是可逆反应,而H(g)和F(g)的反应为
2 2 2 2
完全反应,故1 mol H 分别与足量I(g)、F(g)完全反应生成的分子数HF>HI,D错误。
2 2 2
13.相同温度下,某密闭容器中有一个可自由滑动的隔板(厚度不计),将容器分成两部分,当向甲容器中
充入14.4 g N 和CO 的混合气体、向乙容器中充入4.4 g CO 时,隔板处于如图所示位置。若要使隔
2 2 2
板刚好处于该密闭容器的正中间,需向乙容器中再通入N 的质量为( )
2
A.10.0 g B.8.4 g
C.10.8 g D.9.6 g
答案:B
解析:开始时甲、乙的体积比为4∶1,同温同压下气体的体积比等于物质的量比,乙容器中充入了4.4
g CO ,二氧化碳的物质的量为0.1 mol,则甲容器中14.4 g N 和CO 的混合气体的总物质的量为0.4
2 2 2
mol。若要使隔板刚好处于该密闭容器的正中间,甲、乙中气体物质的量应该相等,则需向乙容器中
再通入0.3 mol N,通入N 的质量为0.3 mol×28 g·mol-1=8.4 g,故选B。
2 214.(2024·陕西宝鸡检测)20 ℃时,饱和NaCl溶液的密度为ρ g·cm-3,物质的量浓度为c mol·L-1,则下列
说法错误的是( )
A.温度低于20 ℃时,饱和NaCl溶液的浓度小于c mol·L-1
58.5c
B.20 ℃时,饱和NaCl溶液中NaCl的质量分数为 ×100%
1 000ρ
C.20 ℃时,将58.5 g NaCl溶解在1 L水中,所得溶液的浓度为1 mol·L-1
5 850c
D.20 ℃时,NaCl的溶解度为 g
1 000ρ-58.5c
答案:C
解析:温度低于20 ℃时,NaCl的溶解度减小,NaCl的质量分数减小,则饱和NaCl溶液的浓度小于c
mol·L-1,A正确;20 ℃时,1 L饱和NaCl溶液的质量为1 000ρ g,溶质NaCl的质量为58.5c g,故NaCl的
58.5c
质量分数为 ×100%,B正确;58.5 g NaCl的物质的量为1 mol,将其溶解在1 L水中,所得溶液
1 000ρ
的体积不是1 L,故所得溶液的浓度不是1 mol·L-1,C错误;20 ℃时,1 L饱和NaCl溶液中NaCl的质量
为58.5c g,又知溶液的质量为1 000ρ g,则溶剂水的质量为(1 000ρ-58.5c) g,根据溶解度的定义,可知20
58.5c 5 850c
℃时NaCl的溶解度为 ×100 g= g,D正确。
1 000ρ-58.5c 1 000ρ-58.5c
15.(2024·四川学考联盟第一次质检)氯气与部分含氯化合物的价类关系如图所示,N 表示阿伏加德罗
A
常数的值。下列有关叙述正确的是( )
A.0 ℃、101 kPa下,1.12 L ClO 所含中子的数目为1.7N
2 A
B.2 L 0.05 mol·L-1 HClO
溶液中所含ClO-
的数目为0.1N
4 4 A
C.用浓盐酸与NaClO 反应制取7.1 g Cl 共转移电子的数目为0.2N
3 2 A
D.由NaClO和NaClO 组成的1 mol混合物中含氧原子的数目为2N
3 A
答案:B
解析:由图像可知,标准状况下ClO 不是气体,不能用气体摩尔体积计算其物质的量,A错误;HClO 是
2 4
强酸,在溶液中完全电离,2 L 0.05 mol·L-1 HClO
溶液中所含ClO-
的数目为0.1N ,B正确;浓盐酸与
4 4 A
NaClO 反应制取Cl
的离子方程式为ClO-
+6H++5Cl- 3Cl↑+3H O,生成3 mol Cl 转移5 mol电
3 2 3 2 2 25 1
子,7.1 g Cl 的物质的量为0.1 mol,生成7.1 g Cl 转移电子的物质的量为 mol= mol,C错误;不知道
2 2 30 6
NaClO和NaClO 的组成比例,无法计算氧原子的数目,D错误。
3