文档内容
第 5 讲 物质的量 气体摩尔体积
[复习目标] 1.掌握物质的量、阿伏加德罗常数、摩尔质量、气体摩尔体积的含义并能进行
简单的计算。2.理解阿伏加德罗定律并能进行有关气体体积、压强与物质的量关系的判断。
考点一 物质的量 摩尔质量
1.物质的量
2.摩尔质量
1.1 mol NaCl和1 mol HCl含有相同的分子数目( )
2.12 g 12C中所含碳原子的数目约为6.02×1023( )3.2 mol H O的摩尔质量是1 mol H O的摩尔质量的2倍( )
2 2
4.1 mol O 的质量与它的相对分子质量相等( )
2
5.1 mol OH-的质量为17 g·mol-1( )
答案 1.× 2.√ 3.× 4.× 5.×
质量、物质的量与微粒数目之间的换算
1.“可燃冰”是由水和甲烷在一定条件下形成的类冰结晶化合物。1.6 g “可燃
冰”(CH·xHO)的物质的量与6.02×1021个水分子的物质的量相等,则该“可燃冰”的摩尔
4 2
质量为________________,x的值为________________。
答案 160 g·mol-1 8
2.最近材料科学家研究发现了首例带结晶水的晶体在5 K下呈现超导性。据报道,该晶体
的化学式为Na CoO·1.3H O。若用N 表示阿伏加德罗常数的值,试计算12.2 g该晶体中
0.35 2 2 A
含氧原子数为________,氢原子的物质的量为________mol(结果保留2位小数)。
答案 0.33N 0.26
A
计算判断物质中所含指定微粒数目的技巧
弄清楚微粒与所给物质的关系:原子(或电子)的物质的量=分子(或特定组合)的物质的量×1
个分子(或特定组合)中所含这种原子(或电子)的个数。如:第2题中,Na CoO·1.3H O是
0.35 2 2
一个整体,计算对象氧原子、氢原子为部分,它们的关系为 Na CoO·1.3H O~3.3O~
0.35 2 2
2.6H。
考点二 气体摩尔体积 阿伏加德罗定律
1.气体摩尔体积
2.阿伏加德罗定律
(1)阿伏加德罗定律:同温、同压下,同体积的任何气体具有相同的分子数或物质的量。(2)阿伏加德罗定律的推论
气体的体积之比等于分子数之比:V∶V=N ∶ N
1 2 1 2
同温、同压下
气体的摩尔质量之比等于密度之比:M∶M=ρ ∶ ρ
1 2 1 2
同温、同体积下 气体的压强之比等于物质的量之比:p∶p=n ∶ n
1 2 1 2
1.22 g CO 气体的体积为11.2 L( )
2
2.标准状况下,11.2 L SO 中含有的原子数为2N ( )
3 A
3.标准状况下,11.2 L O 和H 的混合气体所含分子数约为3.01×1023( )
2 2
4.同温、同体积的条件下,等质量的SO 和O 的压强之比为2∶1( )
2 2
5.同温同压下,ρ(H )<ρ(O )( )
2 2
答案 1.× 2.× 3.√ 4.× 5.√
一、n===关系的应用
1.(1)标准状况下,4.8 g甲烷(CH)所占的体积为________L,它与标准状况下________L硫
4
化氢(H S)含有相同数目的氢原子。
2
(2)标准状况下,16 g O 与14 g N 的混合气体所占的体积是________。
2 2
(3)9.03×1023个 NH 含______mol 氢原子,______mol 质子,在标准状况下的体积约为
3
________L。
(4)标准状况下,若6.72 L O 含有m个氧原子,则阿伏加德罗常数的值可表示为________(用
3
含m的式子表示)。
答案 (1)6.72 13.44 (2)22.4 L (3)4.5 15 33.6 (4)
以物质的量为中心计算的思维流程
二、相对分子质量的计算
2.按要求解答下列问题。
(1)已知标准状况下,气体A的密度为2.857 g·L-1,则气体A的相对分子质量为________,
可能是______(填化学式)气体。
(2)CO和CO 的混合气体18 g,完全燃烧后测得CO 的体积为11.2 L(标准状况),则
2 2
①混合气体在标准状况下的密度是__________________________________________g·L-1(结果保留小数点后2位)。
②混合气体的平均摩尔质量是________g·mol-1。
答案 (1)64 SO (2)①1.61 ②36
2
解析 (1)M=ρ×22.4 L·mol-1≈64 g·mol-1。
(2)2CO+O=====2CO ,CO的体积与生成CO 的体积相等,故18 g CO和CO 的混合气体
2 2 2 2
的总体积为11.2 L,在标准状况下,该混合气体的物质的量为0.5 mol,设CO的物质的量为
x mol,CO 的物质的量为y mol,
2
则,解得x=0.25,y=0.25。
①混合气体的密度为≈1.61 g·L-1。
②解法一:=ρ×22.4 L·mol-1≈36 g·mol-1;
解法二:==36 g·mol-1;
解法三:=28 g·mol-1×50%+44 g·mol-1×50%=36 g·mol-1。
3.(2023·哈尔滨六中高三模拟)同温同压下,m g NH HCO (s)完全分解生成 NH (g)、
4 3 3
CO(g)、HO(g)。按要求填空。
2 2
(1)若所得混合气体的密度是H 的d倍,则混合气体的物质的量为______,NH HCO 的摩尔
2 4 3
质量为________(用含m、d的代数式表示)。
(2)若所得混合气体的密度折合成标准状况为 ρ g·L-1,则混合气体的平均摩尔质量为
________。
(3)在该条件下,所得NH (g)、CO(g)、HO(g)的体积分数分别为a%、b%、c%,则混合气
3 2 2
体的平均相对分子质量为________________。
答案 (1) mol 6d g·mol-1
(2)22.4ρ g·mol-1 (3)17a%+44b%+18c%
解析 (1)NH HCO =====NH ↑+HO↑+CO↑,假设NH HCO 的摩尔质量为M,混合气
4 3 3 2 2 4 3
体的平均摩尔质量(混)==。同温同压下,==d,则(混)=2d g·mol-1=,所以M=6d
g·mol-1。混合气体的物质的量n(混)== mol。
(2)(混)=ρ·V =22.4ρ g·mol-1。
m
(3)(混)=M(NH )·φ(NH )+M(CO)·φ(CO)+M(H O)·φ(H O)=17a%+44b%+18c%。
r r 3 3 r 2 2 r 2 2
求气体摩尔质量(M)的常用方法
(1)根据物质的质量(m)和物质的量(n):M=。
(2)根据一定质量(m)的物质中微粒数目(N)和阿伏加德罗常数(N ):M=。
A
(3)根据标准状况下气体的密度ρ:M=ρ×22.4 L·mol-1。
(4)根据气体的相对密度(D=):=D。
(5)对于混合气体,求其平均摩尔质量,上述计算式仍然成立;还可以用下式计算:=M×a%+M×b%+M×c%……,a%、b%、c%……指混合气体中各成分的物质的量分数
1 2 3
(或体积分数)。
三、阿伏加德罗定律应用
4.三种气体X、Y、Z的相对分子质量关系为M(X)ρ(Ne)>ρ(H ) (2)p(H )>p(Ne)>p(O ) (3)V(H )>V(Ne)>V(O )
2 2 2 2 2 2
(4)m(O )>m(Ne)>m(H )
2 2
解析 (1)根据阿伏加德罗定律的推论,同温、同压时,气体的密度与摩尔质量成正比,所
以 ρ(O )>ρ(Ne)>ρ(H )。(2)温度、密度相同时,气体的压强与摩尔质量成反比,所以
2 2
p(H )>p(Ne)>p(O )。(3)温度、压强均相同时,气体的体积与物质的量成正比;质量相同时,
2 2
气体的物质的量与摩尔质量成反比,所以V(H )>V(Ne)>V(O )。(4)温度、压强、体积均相同
2 2
时,气体的物质的量相同,则气体的质量与摩尔质量成正比,所以m(O )>m(Ne)>m(H )。
2 2
应用阿伏加德罗定律解题的一般思路第一步,分析“条件”:分析题干中的条件,找出相同与不同。
第二步,明确“要求”:分析题目要求,明确所要求的比例关系。
第三步,利用“规律”:利用阿伏加德罗定律及其推论,根据条件和要求进行判断。
1.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.4.4 g C HO中含有σ键数目最多为0.7N (2023·浙江6月选考,7A)
2 4 A
B.1.7 g H O 中含有氧原子数为0.2N (2023·浙江6月选考,7B)
2 2 A
C.1 mol重水比1 mol水多N 个质子(2020·全国卷Ⅲ,9B)
A
D.标准状况下,11.2 L Cl 通入水中,溶液中氯离子数为0.5N (2023·浙江6月选考,7D)
2 A
答案 A
解析 1个C HO中含有6个σ键和1个π键(乙醛)或7个σ键(环氧乙烷),4.4 g C HO的物
2 4 2 4
质的量为0.1 mol,则含有σ键数目最多为0.7N ,A正确;1.7 g H O 的物质的量为0.05
A 2 2
mol,则含有氧原子数为0.1N ,B不正确;标准状况下,11.2 L Cl 的物质的量为0.5 mol,
A 2
通入水中后只有一部分 Cl 与水反应生成 H+、Cl-和HClO,所以溶液中氯离子数小于
2
0.5N ,D不正确。
A
2.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.11.2 L CO 含π键数目为N (2023·辽宁,5A)
2 A
B.1 mol Si含Si—Si的数目约为4N (2023·湖北,3B改编)
A
C.0.1 mol KNO 晶体中含离子数目为0.2N (2023·辽宁,5C)
3 A
D.0.1 mol CH COOH 与足量 CHCHOH 充分反应生成的 CHCOOCH CH 分子数目为
3 3 2 3 2 3
0.1N (2021·浙江1月选考,18D)
A
答案 C
解析 1个CO 分子含有2个π键,题中没有说是标况条件下,气体摩尔体积未知,无法计
2
算π键个数,A错误;在晶体硅中,每个Si与其周围的4个Si形成共价键并形成空间网状
结构,因此,平均每个Si形成2个共价键, 1 mol Si含Si—Si的数目约为2N ,B错误。
A
3.填空
(1)(2022·辽宁,3A改编)1.8 g 18O中含有的中子数为___________。
(2)(2022·辽宁,3B改编)28 g C H 分子中含有的σ键数目为___________。
2 4
(3)(2022·广东,9C改编)1 mol CO中含有________个电子。
(4)(2022·海南,7C改编)2.8 g 56Fe含有的中子数为________。
(5)(2022·浙江6月选考,12A改编)12 g NaHSO 中含有__________个阳离子。
4
(6)(2022·浙江6月选考,12C改编)8 g CH 含有的中子数为___________。
4答案 (1)N (2)5N (3)14N (4)1.5N (5)0.1N (6)3N
A A A A A A
解析 (1)1个18O原子中含有10个中子,1.8 g 18O的物质的量为0.1 mol,故1.8 g 18O中含
有中子的物质的量为1 mol,中子数为N 。(2)1个乙烯分子中含有5个σ键, 28 g C H 的
A 2 4
物质的量为1 mol,其中含有的σ键数目为5N 。(3)1个CO分子中有14个电子,1 mol CO
A
含有的电子数为14N 。(4)56Fe的质子数为26、中子数为56-26=30,2.8 g 56Fe的物质的量
A
为0.05 mol,所含中子为0.05 mol×30=1.5 mol,即1.5N 。(5)NaHSO 由钠离子和硫酸氢根
A 4
离子构成,其中的阳离子只有钠离子,12 g NaHSO 的物质的量为0.1 mol,因此,其中只含
4
有0.1N 个阳离子。(6)1个CH 分子中有6个中子,8 g CH 的物质的量为0.5 mol,因此,8
A 4 4
g CH 含有的中子数为3N 。
4 A
4.下列叙述正确的是( )
A.22.4 L(标准状况)氩气含有的质子数为18N (2018·全国卷Ⅰ,10B)
A
B.同温同压下,O 和CO 的密度相同(2020·北京,5A)
2 2
C.标准状况下,2.24 L乙醇中碳氢键的数目为0.5N (2017·浙江4月选考,22A)
A
D.22.4 L(标准状况)氮气中含7N 个中子(2020·全国卷Ⅲ,9A)
A
答案 A
解析 氩气( Ar)是单原子分子,标况下22.4 L氩气是1 mol,其中含有的质子数是18N ,A
18 A
正确;同温同压下,=,所以=,不相同,B错误;标况下,乙醇为非气体,C错误;标况
下,22.4 L(即1 mol) N 分子中含中子数为(14-7)×2N =14N ,D错误。
2 A A
课时精练
1.下列物质中,与0.3 mol HO含有相同氢原子数的物质是( )
2
A.18.9 g HNO
3
B.0.1 mol NH HSO
4 4
C.3.612×1023个HCl分子
D.4.48 L CH(标准状况)
4
答案 C
2.某硫原子的质量是a g,12C原子的质量是b g,若N 表示阿伏加德罗常数的值,则下列说
A
法正确的是( )
①该硫原子的相对原子质量为 ②m g该硫原子的物质的量为 mol ③该硫原子的摩尔质
量是aN g ④a g该硫原子所含的电子数为16N
A A
A.①③ B.②④ C.①② D.②③
答案 C
解析 该硫原子的相对原子质量为=,①对;该硫原子的摩尔质量M(S)=a g×N mol-1=
AaN g·mol-1,③错;m g该硫原子的物质的量n(S)== mol,②对;a g硫原子即1个硫原
A
子,其所含电子数为16个,④错。
3.设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.CO 的摩尔质量为44 g
2
B.1 L 0.5 mol·L-1 KSO 溶液中含有K+的质量为78 g
2 4
C.常温常压下,22.4 L O 含分子数为N
2 A
D.16 g CH 中含有氢原子的总数为4N
4 A
答案 D
4.(2023·郑州高三模拟)一定温度和压强下,30 L某种气态纯净物中含有6.02×1023个分子,
这些分子由1.204×1024个原子组成,下列有关说法不正确的是( )
A.该温度和压强可能是标准状况
B.标准状况下该纯净物若为气态,其体积约是22.4 L
C.该气体中每个分子含有2个原子
D.若O 在该条件下为气态,则1 mol O 在该条件下的体积也为30 L
2 2
答案 A
解析 据n=可知,该气体的物质的量为1 mol。该温度和压强下,1 mol该气体的体积为30
L,若是标准状况,其体积约是22.4 L,故A不正确、B正确;1 mol该气体含有1.204×1024
个原子,则1个该气体分子中含有原子个数为=2,故C正确;因1 mol该气体在该条件下
为30 L,由此可知该条件下气体摩尔体积为30 L·mol-1,故若O 在该条件下为气态,则1
2
mol O 在该条件下的体积也为30 L,故D正确。
2
5.(2023·菏泽模拟)下列说法正确的是( )
A.标准状况下,22.4 L H 和O 的混合物所含分子数为N
2 2 A
B.标准状况下,18 g HO的体积是22.4 L
2
C.在常温常压下,11.2 L N 含有的分子数为0.5N
2 A
D.标准状况下,11.2 L CCl 含有的原子数为2.5N
4 A
答案 A
解析 标准状况下,22.4 L H 和O 的混合气体的物质的量为1 mol,所含分子数为N ,A项
2 2 A
正确;标准状况下,HO为液体,18 g H O的体积不是22.4 L,B项错误;常温常压下,
2 2
11.2 L N 含有的分子数不是0.5N ,C项错误;标准状况下,CCl 为液体,不能用V =22.4
2 A 4 m
L·mol-1计算,D项错误。
6.设N 为阿伏加德罗常数的值,如果a g某气态双原子分子的分子数为p,则b g该气体
A
在标准状况下的体积V(L)是( )
A. B.
C. D.
答案 D解析 a g该气态双原子分子的物质的量为 mol,摩尔质量为= g·mol-1,所以b g该气体
在标准状况下的体积为×22.4 L·mol-1= L。
7.(2023·济南模拟)配位化合物广泛应用于物质分离、定量测定、医药、催化等方面。利用
氧化法可制备某些配位化合物,如 2CoCl +2NH Cl+8NH +HO===2[Co(NH )Cl]Cl +
2 4 3 2 2 3 5 2
2HO。设N 是阿伏加德罗常数的值,下列叙述正确的是( )
2 A
A.1 mol [Co(NH)Cl]Cl 中σ键的数目为21N
3 5 2 A
B.0.1 mol·L-1 CoCl 溶液中Co2+数目为0.1N
2 A
C.0.1 mol N 与足量H 在催化剂作用下合成氨,生成的NH 分子数为0.2N
2 2 3 A
D.100 g质量分数为17%的HO 溶液中,氧原子总数为N
2 2 A
答案 A
解析 溶液体积未知,不能计算Co2+的数目,B错误;合成氨是可逆反应,0.1 mol N 不能
2
完全反应,故生成的NH 分子数小于0.2N ,C错误;水中也含有氧原子,则n(O)=×2+
3 A
≈5.6 mol,D错误。
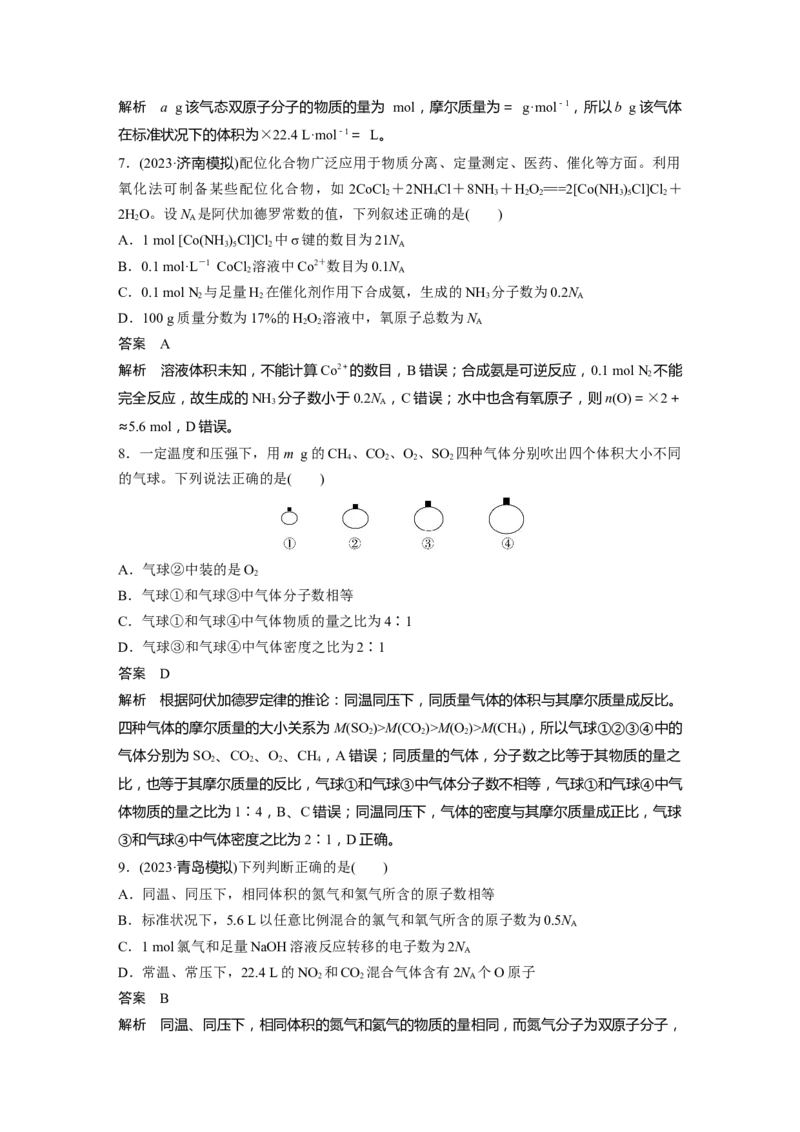
8.一定温度和压强下,用m g的CH、CO、O、SO 四种气体分别吹出四个体积大小不同
4 2 2 2
的气球。下列说法正确的是( )
A.气球②中装的是O
2
B.气球①和气球③中气体分子数相等
C.气球①和气球④中气体物质的量之比为4∶1
D.气球③和气球④中气体密度之比为2∶1
答案 D
解析 根据阿伏加德罗定律的推论:同温同压下,同质量气体的体积与其摩尔质量成反比。
四种气体的摩尔质量的大小关系为M(SO )>M(CO)>M(O )>M(CH),所以气球①②③④中的
2 2 2 4
气体分别为SO 、CO 、O 、CH ,A错误;同质量的气体,分子数之比等于其物质的量之
2 2 2 4
比,也等于其摩尔质量的反比,气球①和气球③中气体分子数不相等,气球①和气球④中气
体物质的量之比为1∶4,B、C错误;同温同压下,气体的密度与其摩尔质量成正比,气球
③和气球④中气体密度之比为2∶1,D正确。
9.(2023·青岛模拟)下列判断正确的是( )
A.同温、同压下,相同体积的氮气和氦气所含的原子数相等
B.标准状况下,5.6 L以任意比例混合的氯气和氧气所含的原子数为0.5N
A
C.1 mol氯气和足量NaOH溶液反应转移的电子数为2N
A
D.常温、常压下,22.4 L的NO 和CO 混合气体含有2N 个O原子
2 2 A
答案 B
解析 同温、同压下,相同体积的氮气和氦气的物质的量相同,而氮气分子为双原子分子,氦气分子为单原子分子,所以二者含有的原子数不相等,A错误;标准状况下5.6 L任意气
体的物质的量为=0.25 mol,氯气分子和氧气分子都是双原子分子,所以以任意比例混合的
氯气和氧气所含的原子数为0.5N ,B正确;1 mol氯气与足量氢氧化钠溶液反应会生成1
A
mol氯化钠和1 mol次氯酸钠,转移1 mol电子,转移的电子数为N ,C错误;不是标准状
A
况,不能使用22.4 L·mol-1计算混合气体的物质的量,D错误。
10.(2023·石家庄模拟)已知标准状况下:①6.72 L NH ;②1.204×1023个HS分子;③5.6
3 2
g CH ;④0.5 mol HCl。下列关系正确的是( )
4
A.体积大小:④>③>①>②
B.原子数目:③>①>②>④
C.密度大小:④>②>③>①
D.质量大小:④>③>②>①
答案 A
11.现有14.4 g CO和CO 的混合气体,在标准状况下所占的体积约为8.96 L。将混合气体
2
依次通过如图装置,最后收集在气球中。下列结论错误的是( )
A.原混合气体所含碳原子总数为0.8N (N 表示阿伏加德罗常数的值)
A A
B.标准状况下,气球中收集到的气体体积为4.48 L
C.NaOH溶液增重8.8 g
D.原混合气体中CO和CO 的体积比为1∶1
2
答案 A
解析 由题意知,n(CO)×28 g·mol-1+n(CO)×44 g·mol-1=14.4 g、n(CO)+n(CO)==0.4
2 2
mol,联立两式解得:n(CO)=n(CO)=0.2 mol。A错,混合气体的总物质的量为0.4 mol,
2
则所含碳原子总数为0.4N ;B对,混合气体通过NaOH溶液时,CO 被吸收,气球中收集
A 2
到的气体是CO,其物质的量为0.2 mol,故在标准状况下的体积为4.48 L;C对,NaOH溶
液吸收 CO 生成 NaCO 和 HO,则 NaOH 溶液增加的质量即为 CO 的质量,应为 0.2
2 2 3 2 2
mol×44 g·mol-1=8.8 g;D对,相同温度和压强下,气体的体积之比等于其物质的量之比,
则CO和CO 的体积之比等于0.2 mol∶0.2 mol=1∶1。
2
12.(2023·福建上杭一中模拟)室温下如图所示,关闭活塞,向左右两室(容积相同)各充入一
定量H 和Cl ,且恰好使两容器内气体密度相同,打开活塞,放电使H 与Cl 充分反应生成
2 2 2 2
氯化氢气体:H+Cl=====2HCl,恢复至原温度后,下列判断正确的是( )
2 2A.开始时左右两室分子数相同
B.最终容器内无H 存在
2
C.反应后H 室压强减小
2
D.最终容器内气体密度比原来大
答案 C
解析 左右两室体积相同,气体密度相同,则气体质量相同,根据 N=n·N =N ,相同质量
A A
时,分子数与摩尔质量成反比,则开始时氢气室分子数多,故 A错误;两种气体质量相同
时,氢气的物质的量多,氢气和氯气以1∶1反应,则氢气过量,所以最终容器内有氢气剩
余,故B错误;反应中氢气有剩余,且气体总的物质的量不变,反应后两室气体物质的量
相同,氢气室气体的物质的量减小,即压强减小,故C正确;反应前后气体总质量不变,
容器体积不变,根据ρ=知,最终容器内气体密度与原来相同,故D错误。
13.填写下列空白。
(1)将等物质的量的NH 和CH 混合,混合气体中NH 与CH 的质量比为________。
3 4 3 4
(2)标准状况下,密度为 0.75 g·L-1的NH 与CH 组成的混合气体中,NH 的体积分数为
3 4 3
________。
(3)已知 a g A 和 b g B 恰好完全反应生成 0.2 mol C 和 d g D,则 C 的摩尔质量为
_____________。
(4)现有下列三种气体:①32 g CH ;②约含有6.02×1023个HCl分子的氯化氢气体;③标准
4
状况下33.6 L O 。请按物理量由小到大的顺序排列:
2
a . 质 量 :
_____________________________________________________________________(填序号,下
同);
b.分子数目:_________________________________________________________________;
c.相同状况下气体的体积:______________________________________________________。
答案 (1)17∶16 (2)80% (3)5(a+b-d)g·mol-1 (4)a.①<②<③ b.②<③<① c.
②<③<①
解析 (2)标准状况下,混合气体的平均摩尔质量为 0.75 g·L-1×22.4 L·mol-1=16.8 g·mol-
1,设NH 的体积分数为x,则17x+16(1-x)=16.8,解得x=0.8,即80%。(3)根据元素质
3
量守恒,C的质量为(a+b-d)g,则C的摩尔质量为=5(a+b-d) g·mol-1。(4)①32 g CH 的
4
物质的量为2 mol;②约含有6.02×1023个HCl分子的氯化氢气体的物质的量为1 mol,其质
量为36.5 g;③标准状况下33.6 L O 的物质的量为1.5 mol,其质量为32 g·mol-1×1.5 mol=
2
48 g。a.根据上述分析可知,三种物质的质量大小为①<②<③。b.根据N=n·N 可知,气体
A
分子数与其物质的量成正比,气体的物质的量大小为②<③<①,则三种气体含有分子数目
大小为②<③<①。c.根据V=n·V 可知,相同条件下气体的体积与其物质的量成正比,气体
m
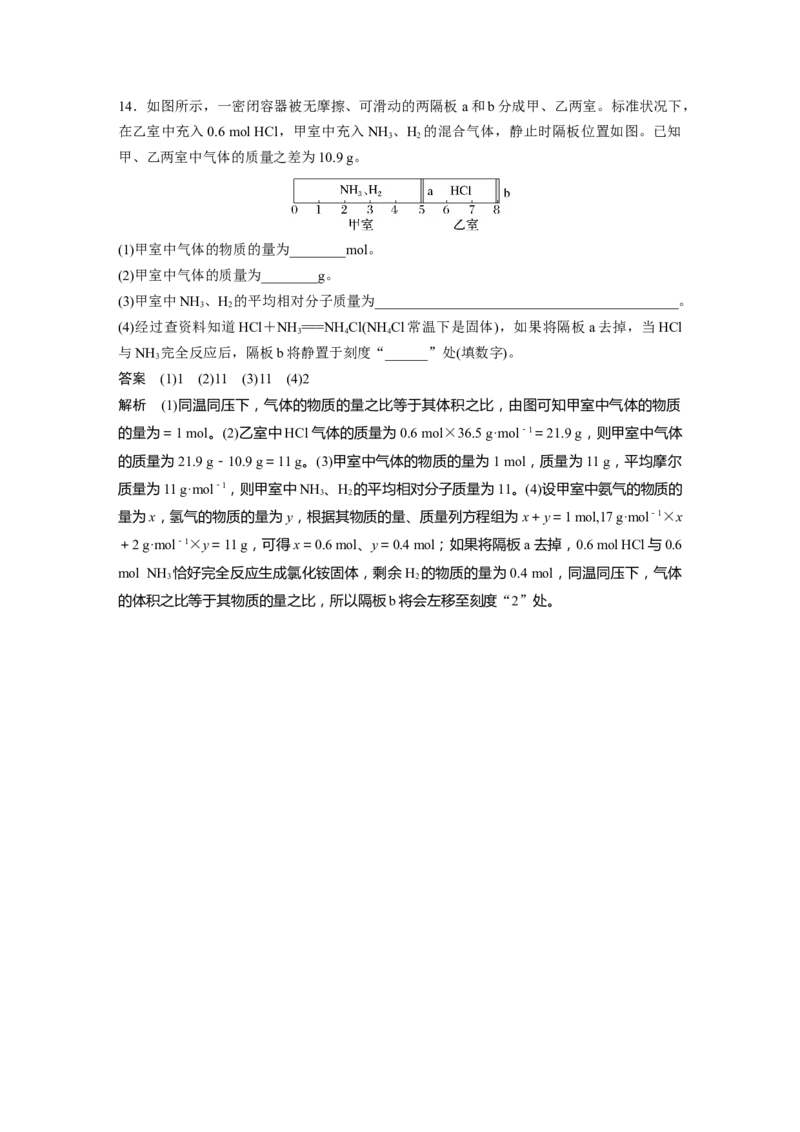
的物质的量大小为②<③<①,则三种气体的体积大小为②<③<①。14.如图所示,一密闭容器被无摩擦、可滑动的两隔板a和b分成甲、乙两室。标准状况下,
在乙室中充入0.6 mol HCl,甲室中充入NH 、H 的混合气体,静止时隔板位置如图。已知
3 2
甲、乙两室中气体的质量之差为10.9 g。
(1)甲室中气体的物质的量为________mol。
(2)甲室中气体的质量为________g。
(3)甲室中NH 、H 的平均相对分子质量为___________________________________________。
3 2
(4)经过查资料知道HCl+NH ===NH Cl(NHCl常温下是固体),如果将隔板a去掉,当HCl
3 4 4
与NH 完全反应后,隔板b将静置于刻度“______”处(填数字)。
3
答案 (1)1 (2)11 (3)11 (4)2
解析 (1)同温同压下,气体的物质的量之比等于其体积之比,由图可知甲室中气体的物质
的量为=1 mol。(2)乙室中HCl气体的质量为0.6 mol×36.5 g·mol-1=21.9 g,则甲室中气体
的质量为21.9 g-10.9 g=11 g。(3)甲室中气体的物质的量为1 mol,质量为11 g,平均摩尔
质量为11 g·mol-1,则甲室中NH 、H 的平均相对分子质量为11。(4)设甲室中氨气的物质的
3 2
量为x,氢气的物质的量为y,根据其物质的量、质量列方程组为x+y=1 mol,17 g·mol-1×x
+2 g·mol-1×y=11 g,可得x=0.6 mol、y=0.4 mol;如果将隔板a去掉,0.6 mol HCl与0.6
mol NH 恰好完全反应生成氯化铵固体,剩余H 的物质的量为0.4 mol,同温同压下,气体
3 2
的体积之比等于其物质的量之比,所以隔板b将会左移至刻度“2”处。