文档内容
第 16 讲 氯及其重要化合物
[复习目标] 1.掌握氯气的性质和实验室制法。2.了解次氯酸及其盐的性质和用途。3.了解氯
及其重要化合物对环境的影响。
考点一 氯气、次氯酸及其盐
1.氯气
(1)氯气的物理性质
氯气是一种________色、有________气味的气体,密度比空气的____,沸点:-34.6 ℃,
____液化。
(2)氯气的化学性质
①氧化性
②从化合价的角度认识Cl 的化学性质——歧化反应
2
氯气与水或碱反应时,氯元素的化合价既有升高又有降低,因而氯气既表现________性又表
现________性。用化学方程式表示上述两类反应。_______________________________________________________________________________
_______________________________________________________________________________
(3)氯水
①从平衡的角度理解氯水的成分
在25 ℃时,1体积的水可溶解约____体积的氯气,氯气的水溶液称为氯水,溶于水中的部
分氯气与水反应。
三种平衡 存在微粒
Cl+HOHCl+HClO
2 2
HClOH++ClO-
HOH++OH-
2
②从成分的角度理解氯水的性质
新制氯水的多种成分决定了它具有多重性质,在不同的化学反应中,氯水中参与反应的微粒
可能不同。
2.次氯酸及其盐
(1)次氯酸
(2)漂白液
(3)漂白粉
1.闻氯气气味时,应用手在瓶口轻轻扇动,使极少量气体飘进鼻孔( )
2.常温下液态氯与铁不反应,故可用钢瓶储运液氯( )3.若贮氯罐意外发生泄露,人们应用浸有一定浓度 NaHCO 溶液的毛巾捂住鼻子,在低洼
3
处等待救援( )
4.过量的铁粉在少量氯气中加热,充分反应后产物为FeCl ( )
2
5.Cl 具有很强的氧化性,在化学反应中只能作氧化剂( )
2
6.可以用pH试纸测定氯水的pH( )
7.“84”消毒液的消毒原理和HO 的相同,都是利用强氧化性( )
2 2
8.漂白粉与盐酸可混合使用以提高消毒效果(2022·全国甲卷,7A)( )
9.向Ca(ClO) 溶液中通入SO ,生成白色沉淀CaSO( )
2 2 3
一、氯气、氯水的性质
1.(2023·无锡高三检测)向下列溶液中通入氯气,现象和结论描述正确的是( )
A.品红溶液:红色褪去,加热该褪色溶液,溶液又恢复红色;次氯酸具有漂白性
B.紫色石蕊溶液:先变红,后褪色;氯气与水反应生成盐酸和次氯酸
C.含酚酞的氢氧化钠溶液:红色褪去;氯气只作氧化剂
D.硫化钠溶液:溶液变浑浊;氯气作还原剂
2.下列实验事实,分别说明氯水中含有哪些粒子?完成下列表格:
序号 实验事实 粒子化学式
① 新制氯水显黄绿色且有刺激性气味
② 向氯水中加入AgNO 溶液生成白色沉淀
3
③ 向氯水中加入NaCO 粉末,有气泡产生
2 3
④ 向氯水中滴加石蕊溶液,先变红后褪色
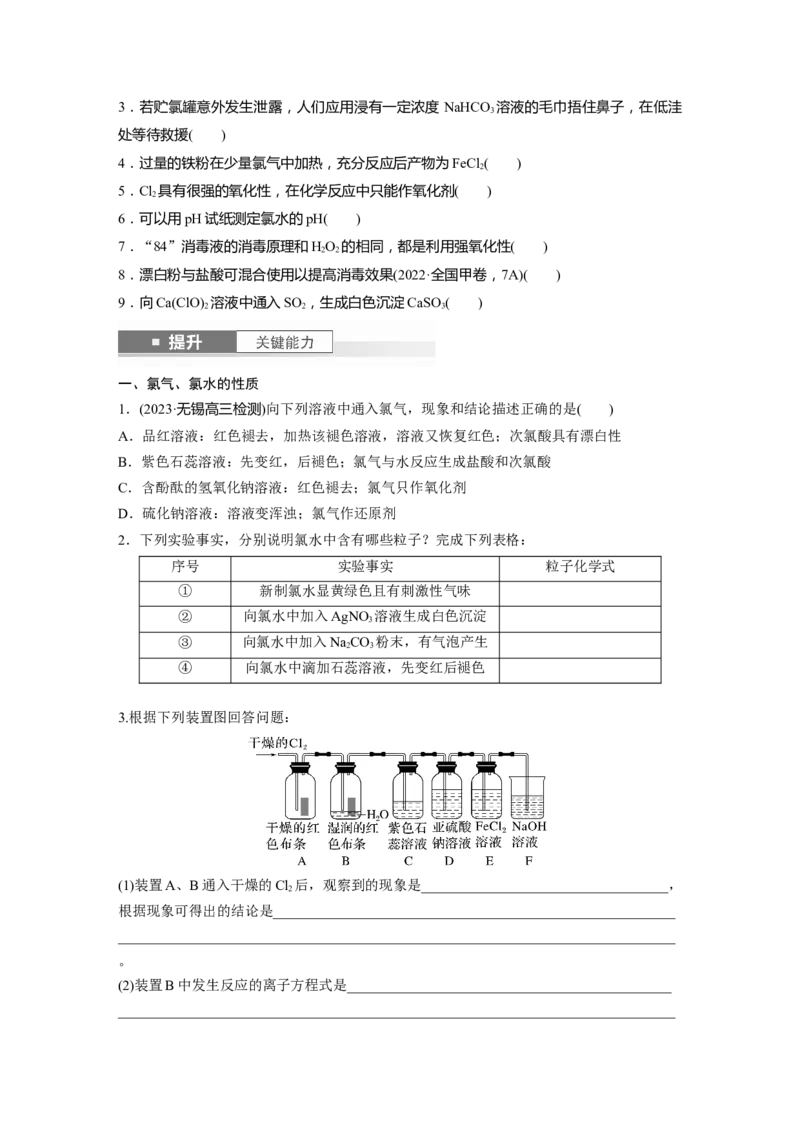
3.根据下列装置图回答问题:
(1)装置A、B通入干燥的Cl 后,观察到的现象是___________________________________,
2
根据现象可得出的结论是_________________________________________________________
_______________________________________________________________________________
。
(2)装置B中发生反应的离子方程式是______________________________________________
_______________________________________________________________________________。
(3)实验开始后,观察装置C中的现象是____________________________________________
_______________________________________________________________________________
。
(4)通入Cl 时装置D中发生反应的离子方程式是_____________________________________。
2
(5)装置E中发生反应的离子方程式是______________________________________________
_______________________________________________________________________________
。
(6)装置F的作用是_______________________________________________________________
_______________________________________________________________________________
。
二、次氯酸及其盐的性质
4.某项目化学学习小组开展了对84消毒液使用安全性的研究。查找资料可知:
①常温下电离常数K(HClO)=4.0×10-8,K (H CO)=4.5×10-7,K (H CO)=4.7×10-11;
a a1 2 3 a2 2 3
②HClO的消毒效果远高于ClO-,而ClO-的稳定性要高于HClO。
(1)在84消毒液中滴加几滴酚酞溶液,可观察到的现象是______________________________。
(2)通常购买的84消毒液pH在12左右,目的是增强消毒液的稳定性,结合方程式与必要的
文字说明,试从化学平衡的角度分析原因:_________________________________________
_______________________________________________________________________________
。
(3)84消毒液必须避光密封保存,目的是防止与空气中的二氧化碳反应而变质,试写出该反
应 的 离 子 方 程 式 :
_________________________________________________________________。
(4)将漂粉精加入到稀盐酸中,发现漂白性不仅没有增强,反而减弱,结合离子方程式解释
其原因:________________________________________________________________________
_______________________________________________________________________________
。
三、含氯消毒剂有效氯的计算
5.有效氯是指每克含氯消毒剂的氧化能力相当于多少克 Cl 的氧化能力,试分别计算
2
NaClO、ClO 、NaClO 的有效氯。
2 2
_______________________________________________________________________________
_______________________________________________________________________________
6.ClO 和NaFeO 在水处理过程中分别被还原为Cl-和Fe3+。如果以单位质量的氧化剂所
2 2 4
得到的电子数来表示消毒效率,那么ClO 、NaFeO、Cl 三种消毒杀菌剂的消毒效率由大到
2 2 4 2
小的顺序是______>______>______(填化学式)。考点二 氯气的实验室制法
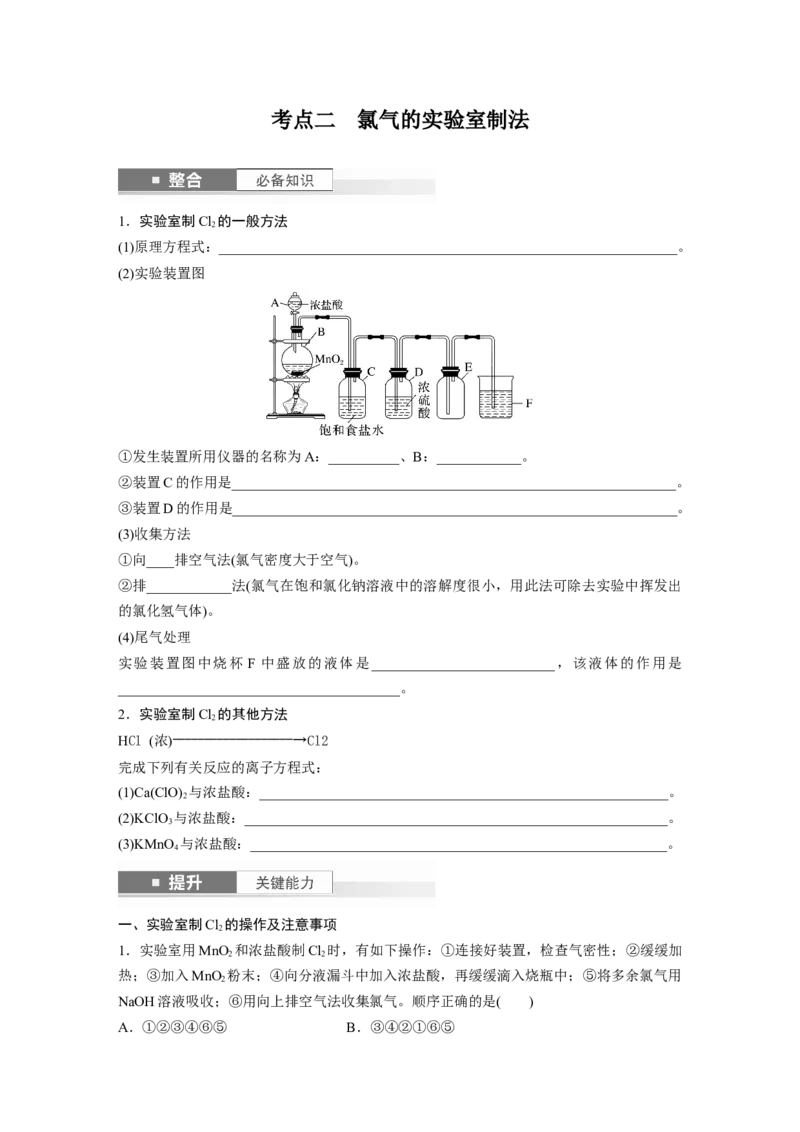
1.实验室制Cl 的一般方法
2
(1)原理方程式:_________________________________________________________________。
(2)实验装置图
①发生装置所用仪器的名称为A:__________、B:____________。
②装置C的作用是_______________________________________________________________。
③装置D的作用是_______________________________________________________________。
(3)收集方法
①向____排空气法(氯气密度大于空气)。
②排____________法(氯气在饱和氯化钠溶液中的溶解度很小,用此法可除去实验中挥发出
的氯化氢气体)。
(4)尾气处理
实验装置图中烧杯 F 中盛放的液体是__________________________,该液体的作用是
________________________________________。
2.实验室制Cl 的其他方法
2
HCl (浓)―――――――――――――――――――→Cl2
完成下列有关反应的离子方程式:
(1)Ca(ClO) 与浓盐酸:__________________________________________________________。
2
(2)KClO 与浓盐酸:____________________________________________________________。
3
(3)KMnO 与浓盐酸:___________________________________________________________。
4
一、实验室制Cl 的操作及注意事项
2
1.实验室用MnO 和浓盐酸制Cl 时,有如下操作:①连接好装置,检查气密性;②缓缓加
2 2
热;③加入MnO 粉末;④向分液漏斗中加入浓盐酸,再缓缓滴入烧瓶中;⑤将多余氯气用
2
NaOH溶液吸收;⑥用向上排空气法收集氯气。顺序正确的是( )
A.①②③④⑥⑤ B.③④②①⑥⑤C.①④③②⑥⑤ D.①③④②⑥⑤
2.(1)如何用最简单的方法判断氯气已收集满?
______________________________________________________________________________
______________________________________________________________________________
(2)实验室常用排饱和食盐水法收集氯气,请解释用此方法收集氯气的原因。
______________________________________________________________________________
______________________________________________________________________________
二、实验室制Cl 原理探究
2
3.某兴趣小组用50 mL 12 mol·L-1浓盐酸与足量MnO 共热制取Cl,结果收集到的Cl 远小
2 2 2
于0.15 mol,经检查实验装置没有问题。
(1)请帮助分析,制取的气体远小于理论值的可能原因:_______________________________
_______________________________________________________________________________
。
(2)经检验可知,反应后容器中仍存在MnO 和盐酸,该小组对不再产生Cl 的原因进行以下
2 2
实验探究。
[提出猜想]
猜想一:在此反应中,随H+浓度降低,______(填氧化剂化学式)氧化性减弱。
猜想二:在此反应中,随__________(填“Cl-”或“Mn2+”)浓度降低,还原剂还原性减弱。
猜想三:在此反应中,随Mn2+浓度升高,氧化剂氧化性减弱。
[设计实验、验证猜想]
向反应后的固液混合物中加入试剂,观察并记录有无氯气生成。
已知:Na+、SO对各物质的氧化性与还原性均无影响。限选试剂:浓HSO 、NaCl固体、
2 4
MnO 固体、MnSO 固体、蒸馏水。
2 4
序号 操作 现象与结论
1 滴加浓硫酸,继续加热 有黄绿色气体产生,猜想____成立
2 加入适量______固体,继续加热 有黄绿色气体产生,猜想二成立
3 无气体产生,猜想三成立
[数据分析、得出结论] 猜想一、二、三均正确。
1.正误判断,正确的打“√”,错误的打“×”。
(1)氯气与强碱反应时既是氧化剂又是还原剂,符合“事物的双方既相互对立又相互统一”
的哲学观点(2023·湖北,2B)( )
(2)“洁厕灵”(主要成分为盐酸)和“84消毒液”(主要成分为次氯酸钠)不能混用(2022·浙江
6月选考,9D)( )(3)Cl 中含有的HCl杂质通过饱和食盐水除去(2020·全国卷Ⅰ,9B改编)( )
2
(4)用同一针筒先后抽取 80 mL氯气、20 mL水,振荡,气体完全溶解,溶液变为黄绿色
(2019·浙江4月选考,11A)( )
2.[2020·江苏,18(1)]NaClO溶液可由低温下将Cl 缓慢通入NaOH溶液中而制得。制备
2
NaClO的离子方程式为______________________________________________;用于环境杀
菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间过长且见光,将会导致消毒
作用减弱,其原因是__________________________________________________________。
3.[2021·广东,17(1)(2)(3)]含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰
矿(主要成分是MnO )的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,
2
戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。
(1)实验室沿用舍勒的方法制取Cl 的化学方程式为___________________________________
2
_______________________________________________________________________________
。
(2) 实 验 室 制 取 干 燥 Cl 时 , 净 化 与 收 集 Cl 所 需 装 置 的 接 口 连 接 顺 序 为
2 2
_______________________________________________________________________________。
(3)某氯水久置后不能使品红溶液褪色,可推测氯水中________已分解。检验此久置氯水中
Cl-存在的操作及现象是__________________________________________________________
_______________________________________________________________________________
。