文档内容
第 24 讲 氮及其化合物的转化关系
[复习目标] 1.能从物质类别、氮的化合价变化理解氮及其化合物的转化关系。2.能从含氮
物质的性质和转化的视角解释生产、生活中的相关现象。
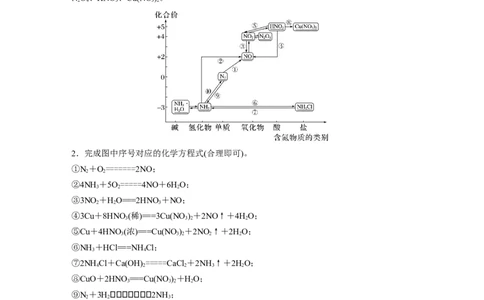
1.在氮及其化合物的“价—类”二维图中填充N 、NH 、NH ·H O、NH Cl、NO、NO 、
2 3 3 2 4 2
NO、HNO、Cu(NO )。
2 4 3 3 2
2.完成图中序号对应的化学方程式(合理即可)。
①N+O=======2NO;
2 2
②4NH +5O=====4NO+6HO;
3 2 2
③3NO +HO===2HNO+NO;
2 2 3
④3Cu+8HNO(稀)===3Cu(NO )+2NO↑+4HO;
3 3 2 2
⑤Cu+4HNO(浓)===Cu(NO )+2NO ↑+2HO;
3 3 2 2 2
⑥NH +HCl===NH Cl;
3 4
⑦2NH Cl+Ca(OH) =====CaCl +2NH ↑+2HO;
4 2 2 3 2
⑧CuO+2HNO===Cu(NO )+HO;
3 3 2 2
⑨N+3H2NH ;
2 2 3
⑩8NH +3Cl===6NH Cl+N。
3 2 4 2
3.常见无机物A、B、C、D存在如图转化关系:
(1)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的
化学方程式为____________________________________________________________________。
(2)若A为常见挥发性强酸,D是生产生活中用量最大、用途最广的金属单质,则B的化学
式是__________________。(3)若A、C、D都是常见气体,C是形成酸雨的主要气体,则A的电子式是_____________。
(4)若A、B、C的水溶液均显碱性,焰色试验均为黄色,D为CO ,举出C的一种用途:
2
_________
_______________________________________________________________________________
。
答案 (1)4NH +5O=====4NO+6HO
3 2 2
(2)Fe(NO ) (3) (4)治疗胃酸过多、作发酵粉、用于泡沫灭火器等(任答其中一
3 3
种即可)
解析 (1)由题意知,A为氨气,B是NO,D是氧气,C是二氧化氮,反应①的化学方程式
为4NH +5O=====4NO+6HO。(2)由题意知,A是硝酸,B是硝酸铁,C是硝酸亚铁,则
3 2 2
B的化学式为Fe(NO ) 。(3)由题意知,C是二氧化硫,A是硫化氢,D是氧气,B是S,A
3 3
的电子式是 。(4)若A、B、C的水溶液均显碱性,焰色试验均为黄色,说明都含
有Na元素,D为CO,A为NaOH,B是碳酸钠,C为碳酸氢钠。
2
1.空气中的氮气可通过人工固氮获得氨气,氨气是重要的化工原料,通过氨氧化法可制得
硝酸,反应过程如下:
N――――――――――→NH ――――――→NO――→NO ―――→HNO
2 3 2 3
硝酸是一种强氧化性酸,制硝酸工业产生的尾气中含有氮氧化物,应处理后才能排放。下列
说法不正确的是( )
A.常温下,浓硝酸可盛放在铝制或铁制容器中
B.BaSO 固体能溶于稀硝酸,生成Ba(NO ),放出SO 气体
3 3 2 2
C.工业上,当转化①的反应达到平衡时,需不断地从混合气体中分离出NH ,将未反应的
3
原料气送回合成塔以提高原料的利用率
D.转化④中,当V(NO )∶V(O )=4∶1时,理论上NO 可全部转化为HNO
2 2 2 3
答案 B
解析 硝酸是强氧化性酸,BaSO 固体能溶于稀硝酸,被氧化生成硫酸钡,硝酸被还原生成
3
NO,B错误。
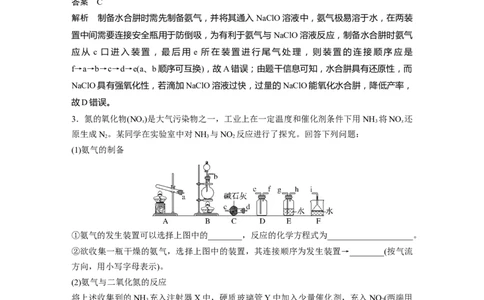
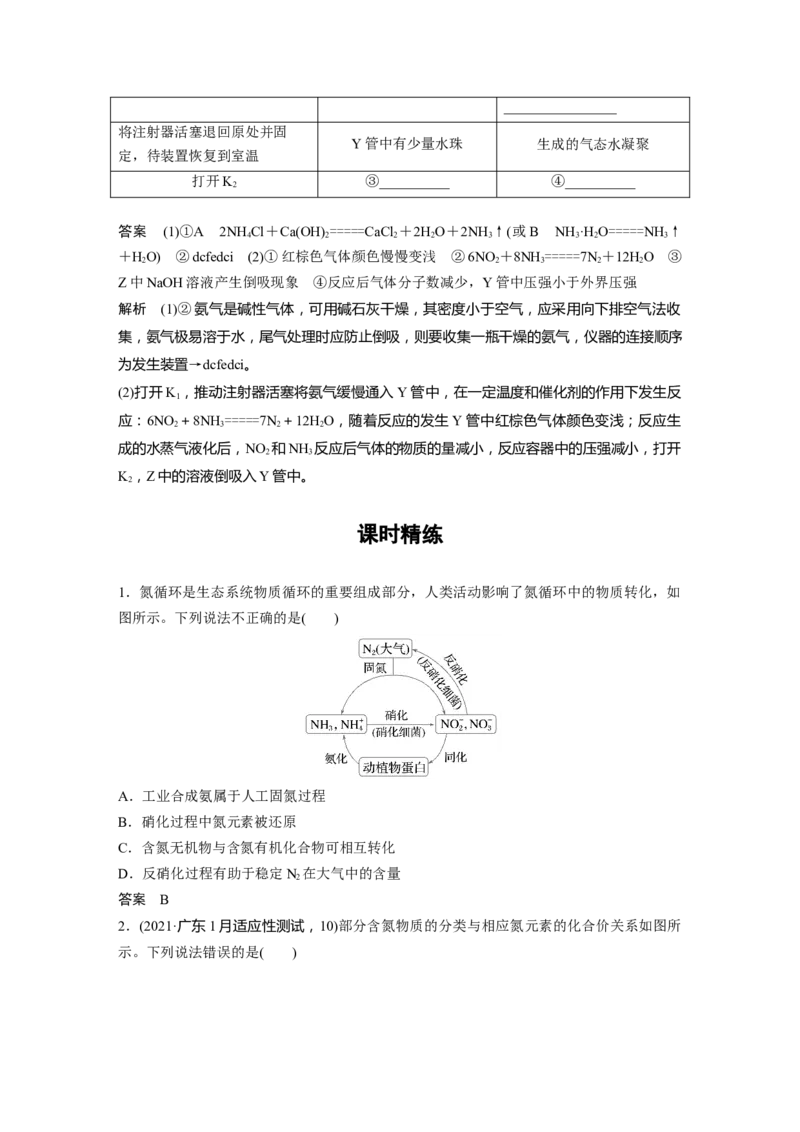
2.(2023·河北衡水中学一模)水合肼又称水合联氨,广泛用作还原剂、抗氧化剂、发泡剂等。
其制备原理为NaClO+2NH ===NH·H O+NaCl。用如图装置制取水合肼的有关分析正确
3 2 4 2
的是( )A.装置的连接顺序是f→a→b→d→c→e
B.e所在装置的漏斗可以没入水面以下
C.f所在装置可以快速制备氨气
D.操作过程中要快速滴加NaClO溶液
答案 C
解析 制备水合肼时需先制备氨气,并将其通入NaClO溶液中,氨气极易溶于水,在两装
置中间需要连接安全瓶用于防倒吸,为有利于氨气与 NaClO溶液反应,制备水合肼时氨气
应从 c 口进入装置,最后用 e 所在装置进行尾气处理,则装置的连接顺序应是
f→a→b→c→d→e(a、b顺序可互换),故A错误;由题干信息可知,水合肼具有还原性,而
NaClO具有强氧化性,若滴加NaClO溶液过快,过量的NaClO能氧化水合肼,降低产率,
故D错误。
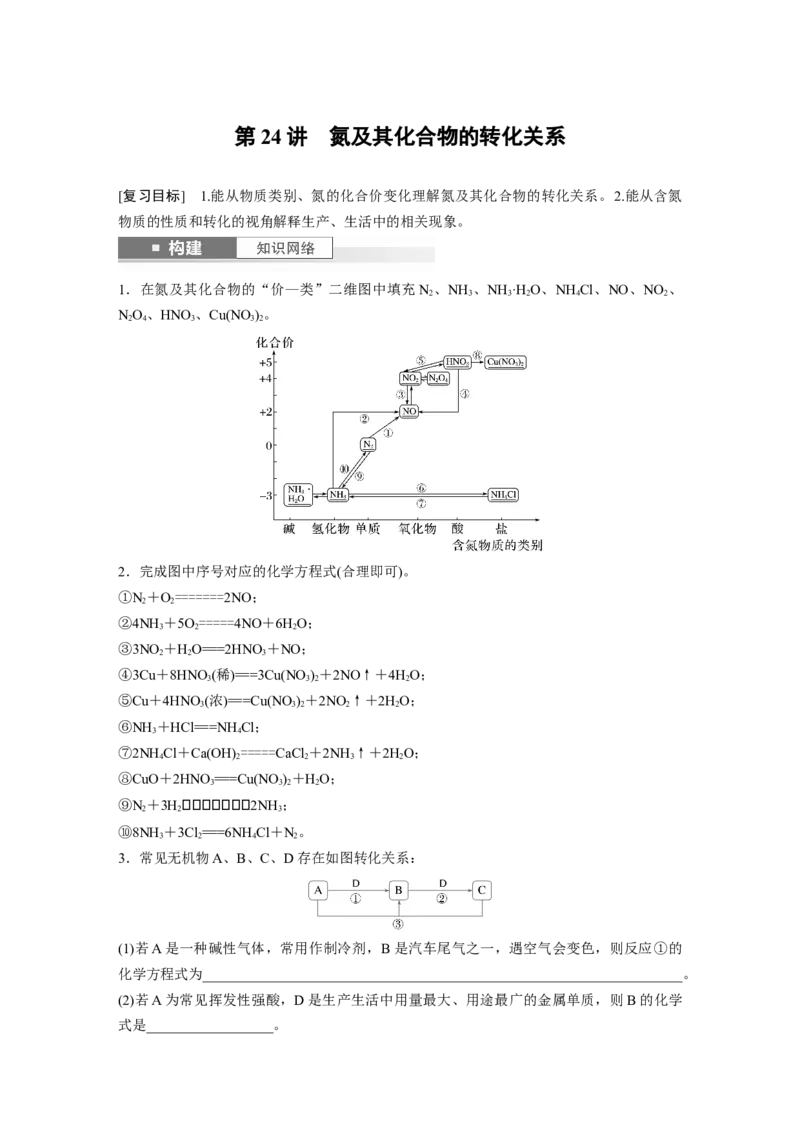
3.氮的氧化物(NO)是大气污染物之一,工业上在一定温度和催化剂条件下用NH 将NO 还
x 3 x
原生成N。某同学在实验室中对NH 与NO 反应进行了探究。回答下列问题:
2 3 2
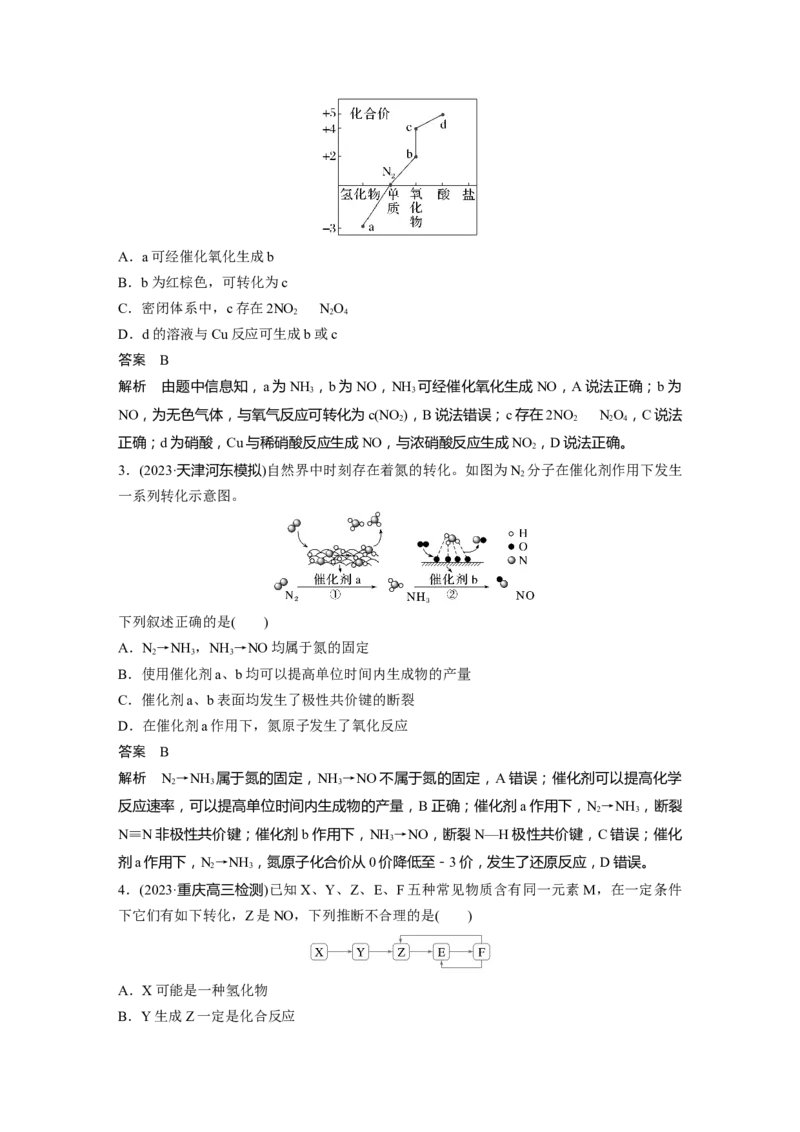
(1)氨气的制备
①氨气的发生装置可以选择上图中的________,反应的化学方程式为____________________。
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为发生装置→________(按气流
方向,用小写字母表示)。
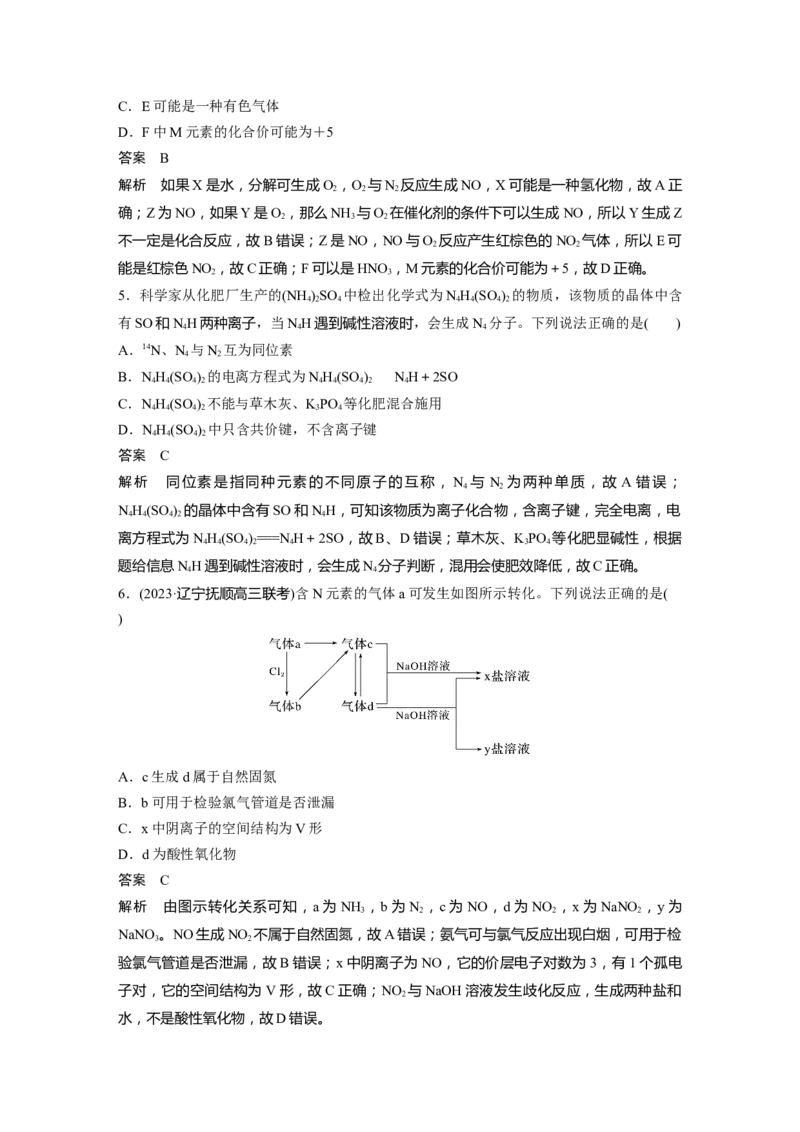
(2)氨气与二氧化氮的反应
将上述收集到的NH 充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO (两端用
3 2
夹子K、K 夹好)。在一定温度下按图示装置进行实验。
1 2
操作步骤 实验现象 解释原因
打开K,推动注射器活塞,使
1 ①Y管中______________
②反应的化学方程式:
X中的气体缓慢通入Y管中________________
将注射器活塞退回原处并固
Y管中有少量水珠 生成的气态水凝聚
定,待装置恢复到室温
打开K ③__________ ④__________
2
答案 (1)①A 2NH Cl+Ca(OH) =====CaCl +2HO+2NH ↑(或B NH ·H O=====NH ↑
4 2 2 2 3 3 2 3
+HO) ②dcfedci (2)①红棕色气体颜色慢慢变浅 ②6NO +8NH =====7N+12HO ③
2 2 3 2 2
Z中NaOH溶液产生倒吸现象 ④反应后气体分子数减少,Y管中压强小于外界压强
解析 (1)②氨气是碱性气体,可用碱石灰干燥,其密度小于空气,应采用向下排空气法收
集,氨气极易溶于水,尾气处理时应防止倒吸,则要收集一瓶干燥的氨气,仪器的连接顺序
为发生装置→dcfedci。
(2)打开K ,推动注射器活塞将氨气缓慢通入Y管中,在一定温度和催化剂的作用下发生反
1
应:6NO +8NH =====7N +12HO,随着反应的发生Y管中红棕色气体颜色变浅;反应生
2 3 2 2
成的水蒸气液化后,NO 和NH 反应后气体的物质的量减小,反应容器中的压强减小,打开
2 3
K,Z中的溶液倒吸入Y管中。
2
课时精练
1.氮循环是生态系统物质循环的重要组成部分,人类活动影响了氮循环中的物质转化,如
图所示。下列说法不正确的是( )
A.工业合成氨属于人工固氮过程
B.硝化过程中氮元素被还原
C.含氮无机物与含氮有机化合物可相互转化
D.反硝化过程有助于稳定N 在大气中的含量
2
答案 B
2.(2021·广东1月适应性测试,10)部分含氮物质的分类与相应氮元素的化合价关系如图所
示。下列说法错误的是( )A.a可经催化氧化生成b
B.b为红棕色,可转化为c
C.密闭体系中,c存在2NO NO
2 2 4
D.d的溶液与Cu反应可生成b或c
答案 B
解析 由题中信息知,a为NH ,b为NO,NH 可经催化氧化生成NO,A说法正确;b为
3 3
NO,为无色气体,与氧气反应可转化为c(NO ),B说法错误;c存在2NO NO ,C说法
2 2 2 4
正确;d为硝酸,Cu与稀硝酸反应生成NO,与浓硝酸反应生成NO ,D说法正确。
2
3.(2023·天津河东模拟)自然界中时刻存在着氮的转化。如图为N 分子在催化剂作用下发生
2
一系列转化示意图。
下列叙述正确的是( )
A.N→NH ,NH →NO均属于氮的固定
2 3 3
B.使用催化剂a、b均可以提高单位时间内生成物的产量
C.催化剂a、b表面均发生了极性共价键的断裂
D.在催化剂a作用下,氮原子发生了氧化反应
答案 B
解析 N→NH 属于氮的固定,NH →NO不属于氮的固定,A错误;催化剂可以提高化学
2 3 3
反应速率,可以提高单位时间内生成物的产量,B正确;催化剂a作用下,N→NH ,断裂
2 3
N≡N非极性共价键;催化剂b作用下,NH →NO,断裂N—H极性共价键,C错误;催化
3
剂a作用下,N→NH ,氮原子化合价从0价降低至-3价,发生了还原反应,D错误。
2 3
4.(2023·重庆高三检测)已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件
下它们有如下转化,Z是NO,下列推断不合理的是( )
A.X可能是一种氢化物
B.Y生成Z一定是化合反应C.E可能是一种有色气体
D.F中M元素的化合价可能为+5
答案 B
解析 如果X是水,分解可生成O ,O 与N 反应生成NO,X可能是一种氢化物,故A正
2 2 2
确;Z为NO,如果Y是O ,那么NH 与O 在催化剂的条件下可以生成NO,所以Y生成Z
2 3 2
不一定是化合反应,故B错误;Z是NO,NO与O 反应产生红棕色的NO 气体,所以E可
2 2
能是红棕色NO ,故C正确;F可以是HNO,M元素的化合价可能为+5,故D正确。
2 3
5.科学家从化肥厂生产的(NH )SO 中检出化学式为NH(SO ) 的物质,该物质的晶体中含
4 2 4 4 4 4 2
有SO和NH两种离子,当NH遇到碱性溶液时,会生成N 分子。下列说法正确的是( )
4 4 4
A.14N、N 与N 互为同位素
4 2
B.NH(SO ) 的电离方程式为NH(SO )NH+2SO
4 4 4 2 4 4 4 2 4
C.NH(SO ) 不能与草木灰、KPO 等化肥混合施用
4 4 4 2 3 4
D.NH(SO ) 中只含共价键,不含离子键
4 4 4 2
答案 C
解析 同位素是指同种元素的不同原子的互称,N 与 N 为两种单质,故 A 错误;
4 2
NH(SO ) 的晶体中含有SO和NH,可知该物质为离子化合物,含离子键,完全电离,电
4 4 4 2 4
离方程式为NH(SO )===NH+2SO,故B、D错误;草木灰、KPO 等化肥显碱性,根据
4 4 4 2 4 3 4
题给信息NH遇到碱性溶液时,会生成N 分子判断,混用会使肥效降低,故C正确。
4 4
6.(2023·辽宁抚顺高三联考)含N元素的气体a可发生如图所示转化。下列说法正确的是(
)
A.c生成d属于自然固氮
B.b可用于检验氯气管道是否泄漏
C.x中阴离子的空间结构为V形
D.d为酸性氧化物
答案 C
解析 由图示转化关系可知,a为NH ,b为N ,c为NO,d为NO ,x为NaNO ,y为
3 2 2 2
NaNO 。NO生成NO 不属于自然固氮,故A错误;氨气可与氯气反应出现白烟,可用于检
3 2
验氯气管道是否泄漏,故B错误;x中阴离子为NO,它的价层电子对数为3,有1个孤电
子对,它的空间结构为V形,故C正确;NO 与NaOH溶液发生歧化反应,生成两种盐和
2
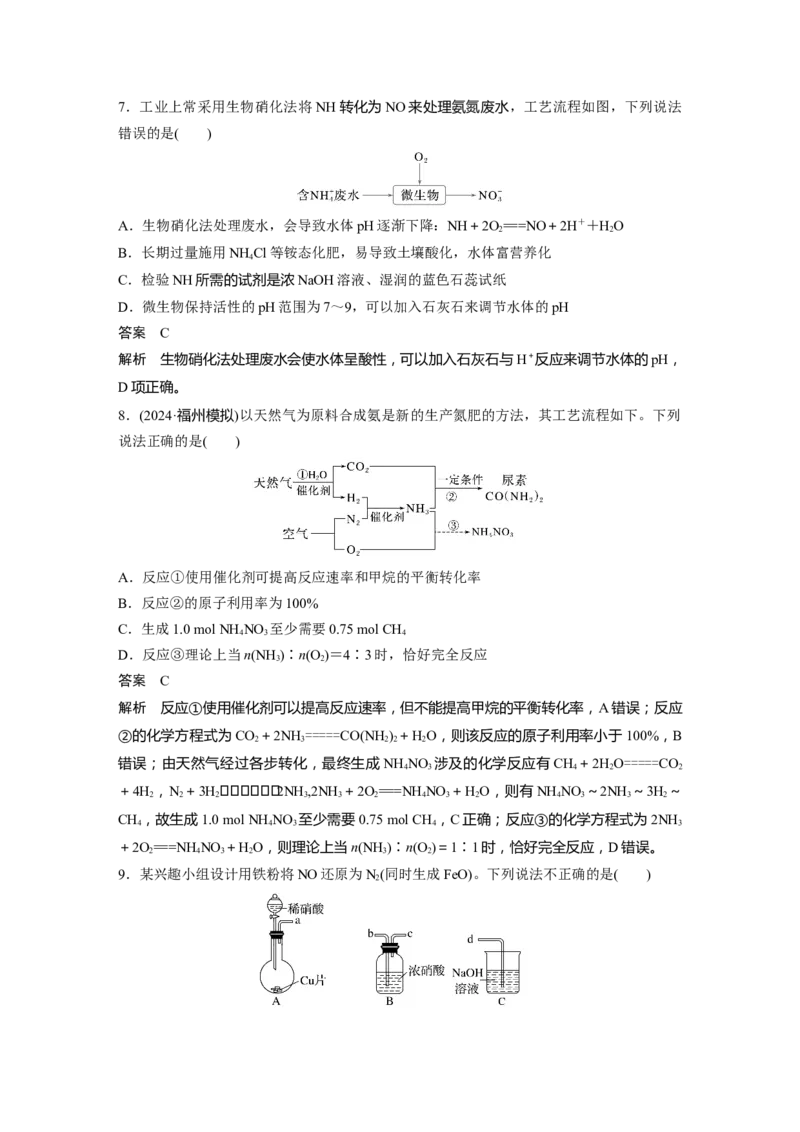
水,不是酸性氧化物,故D错误。7.工业上常采用生物硝化法将NH转化为NO来处理氨氮废水,工艺流程如图,下列说法
错误的是( )
A.生物硝化法处理废水,会导致水体pH逐渐下降:NH+2O===NO+2H++HO
2 2
B.长期过量施用NH Cl等铵态化肥,易导致土壤酸化,水体富营养化
4
C.检验NH所需的试剂是浓NaOH溶液、湿润的蓝色石蕊试纸
D.微生物保持活性的pH范围为7~9,可以加入石灰石来调节水体的pH
答案 C
解析 生物硝化法处理废水会使水体呈酸性,可以加入石灰石与H+反应来调节水体的pH,
D项正确。
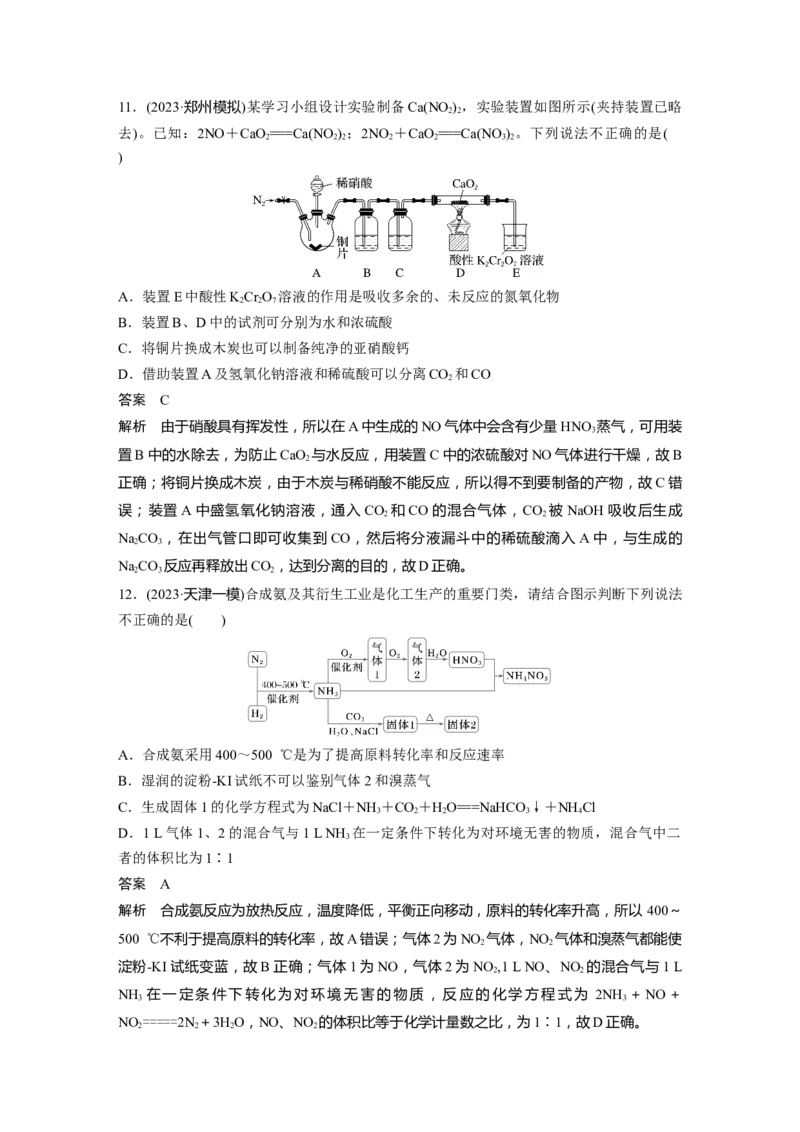
8.(2024·福州模拟)以天然气为原料合成氨是新的生产氮肥的方法,其工艺流程如下。下列
说法正确的是( )
A.反应①使用催化剂可提高反应速率和甲烷的平衡转化率
B.反应②的原子利用率为100%
C.生成1.0 mol NH NO 至少需要0.75 mol CH
4 3 4
D.反应③理论上当n(NH )∶n(O )=4∶3时,恰好完全反应
3 2
答案 C
解析 反应①使用催化剂可以提高反应速率,但不能提高甲烷的平衡转化率,A错误;反应
②的化学方程式为CO +2NH =====CO(NH) +HO,则该反应的原子利用率小于100%,B
2 3 2 2 2
错误;由天然气经过各步转化,最终生成NH NO 涉及的化学反应有CH +2HO=====CO
4 3 4 2 2
+4H ,N +3H2NH ,2NH +2O===NH NO +HO,则有NH NO ~2NH ~3H ~
2 2 2 3 3 2 4 3 2 4 3 3 2
CH ,故生成1.0 mol NH NO 至少需要0.75 mol CH ,C正确;反应③的化学方程式为2NH
4 4 3 4 3
+2O===NH NO +HO,则理论上当n(NH )∶n(O )=1∶1时,恰好完全反应,D错误。
2 4 3 2 3 2
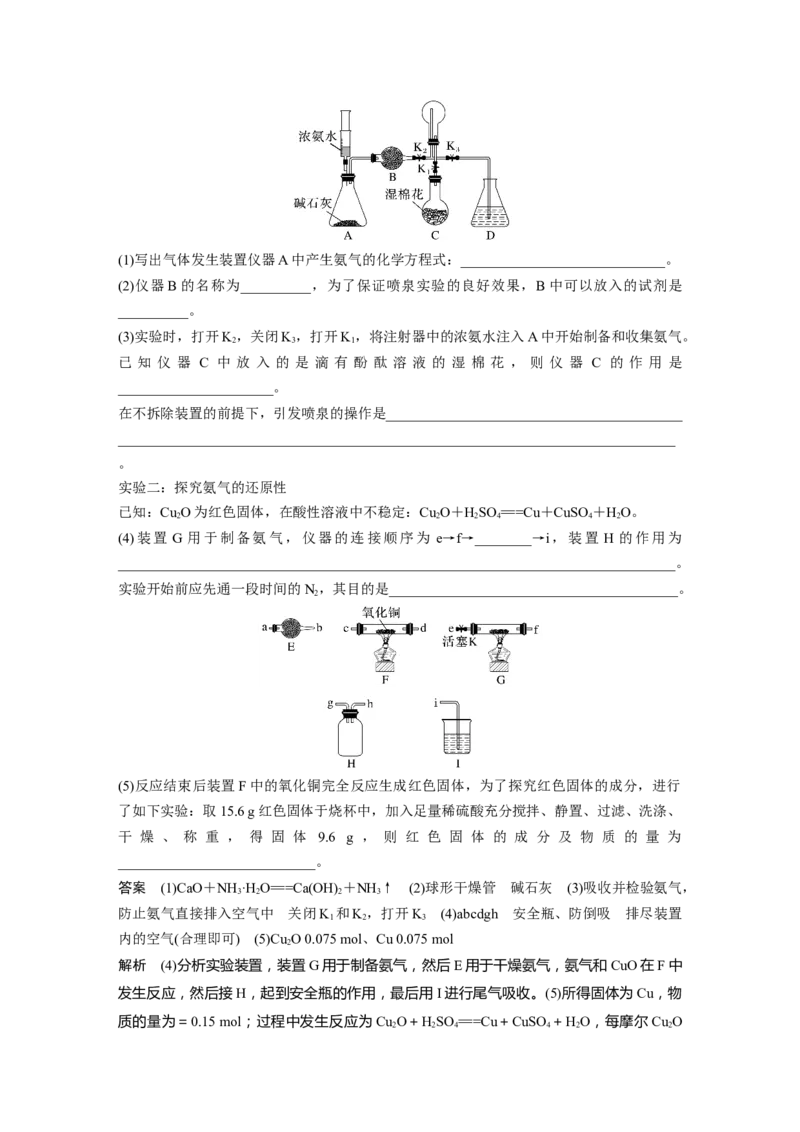
9.某兴趣小组设计用铁粉将NO还原为N(同时生成FeO)。下列说法不正确的是( )
2已知:①浓硝酸可氧化NO;②NaOH溶液能吸收NO ,不吸收NO。
2
A.装置的连接顺序为a→f→e→j→i→h→g(或g→h)→b→c→d
B.装置E中发生反应的化学方程式为2NO+2Fe=====2FeO+N
2
C.装置D的作用是吸收挥发出来的硝酸和产生的NO
2
D.装置B的作用是干燥,防止水蒸气进入装置E中干扰反应
答案 D
解析 根据实验原理“NO被灼热的铁粉还原为N ,同时生成FeO”,所以首先利用铜与稀
2
硝酸反应生成NO,由于硝酸具有挥发性,所以制得的NO中会混有硝酸蒸气和产生的
NO ,故先通过装置D除去挥发出的HNO 和产生的NO ,再通过装置F干燥,得到纯净干
2 3 2
燥的NO,然后进入装置E中与铁粉反应,最后处理多余的NO,由于NaOH溶液不与NO
反应,而浓硝酸可氧化NO生成NO ,所以先通过装置B氧化NO,再通过装置C吸收尾气,
2
故上述装置的连接顺序为a→f→e→j→i→h→g(或g→h)→b→c→d,A正确。
10.某学习小组设计实验探究NO与铜粉的反应并检验NO,实验装置如图所示(夹持装置
略)。实验开始前,向装置中通入一段时间的N,排尽装置内的空气。
2
已知:在溶液中FeSO +NO [Fe(NO)]SO (棕色),该反应可用于检验NO。
4 4
下列说法不正确的是( )
A.装置F、I中的试剂依次为水、硫酸亚铁溶液
B.若观察到装置H中红色粉末变黑色,则NO与Cu发生了反应
C.实验结束后,先熄灭酒精灯,再关闭分液漏斗的活塞
D.装置J收集的气体中一定不含NO
答案 D
解析 稀硝酸与铜反应生成一氧化氮,一氧化氮能够被氧气氧化,因此实验前需要通入氮气,
排尽装置中的空气,硝酸具有挥发性,生成的一氧化氮中混有少量硝酸蒸气,可以通过水吸
收后再干燥,干燥的一氧化氮在装置H中与铜粉发生反应,未反应的NO可以利用硫酸亚铁
溶液检验。装置F、I中的试剂依次为水、硫酸亚铁溶液,A项正确;实验结束后,为了防
止倒吸,需要先熄灭酒精灯,再关闭分液漏斗的活塞,C 项正确;由于 FeSO +
4
NO[Fe(NO)]SO (棕色)为可逆反应,装置J收集的气体中可能含有NO,D项错误。
411.(2023·郑州模拟)某学习小组设计实验制备Ca(NO ) ,实验装置如图所示(夹持装置已略
2 2
去)。已知:2NO+CaO===Ca(NO ) ;2NO +CaO===Ca(NO ) 。下列说法不正确的是(
2 2 2 2 2 3 2
)
A.装置E中酸性KCr O 溶液的作用是吸收多余的、未反应的氮氧化物
2 2 7
B.装置B、D中的试剂可分别为水和浓硫酸
C.将铜片换成木炭也可以制备纯净的亚硝酸钙
D.借助装置A及氢氧化钠溶液和稀硫酸可以分离CO 和CO
2
答案 C
解析 由于硝酸具有挥发性,所以在A中生成的NO气体中会含有少量HNO 蒸气,可用装
3
置B中的水除去,为防止CaO 与水反应,用装置C中的浓硫酸对NO气体进行干燥,故B
2
正确;将铜片换成木炭,由于木炭与稀硝酸不能反应,所以得不到要制备的产物,故C错
误;装置A中盛氢氧化钠溶液,通入 CO 和CO的混合气体,CO 被NaOH吸收后生成
2 2
NaCO ,在出气管口即可收集到 CO,然后将分液漏斗中的稀硫酸滴入 A中,与生成的
2 3
NaCO 反应再释放出CO,达到分离的目的,故D正确。
2 3 2
12.(2023·天津一模)合成氨及其衍生工业是化工生产的重要门类,请结合图示判断下列说法
不正确的是( )
A.合成氨采用400~500 ℃是为了提高原料转化率和反应速率
B.湿润的淀粉-KI试纸不可以鉴别气体2和溴蒸气
C.生成固体1的化学方程式为NaCl+NH +CO+HO===NaHCO ↓+NH Cl
3 2 2 3 4
D.1 L气体1、2的混合气与1 L NH 在一定条件下转化为对环境无害的物质,混合气中二
3
者的体积比为1∶1
答案 A
解析 合成氨反应为放热反应,温度降低,平衡正向移动,原料的转化率升高,所以 400~
500 ℃不利于提高原料的转化率,故A错误;气体2为NO 气体,NO 气体和溴蒸气都能使
2 2
淀粉-KI试纸变蓝,故B正确;气体1为NO,气体2为NO ,1 L NO、NO 的混合气与1 L
2 2
NH 在一定条件下转化为对环境无害的物质,反应的化学方程式为 2NH +NO+
3 3
NO =====2N+3HO,NO、NO 的体积比等于化学计量数之比,为1∶1,故D正确。
2 2 2 213.氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答问题:
(1)下列有关NH 的说法不正确的是________(填字母)。
3
A.工业合成NH 需要在高温、高压、催化剂下进行
3
B.NH 可用来生产碳铵和尿素等化肥
3
C.NH 可用浓硫酸或无水氯化钙干燥
3
D.NH 受热易分解,须置于冷暗处保存
3
(2)NH 易溶于水,标准状况下,用充满NH 的烧瓶做喷泉实验,水充满整个烧瓶后所形成
3 3
溶液的物质的量浓度为______ mol·L-1。
(3)氨气燃烧的化学方程式为____________________________________________________。
(4)HNO 是一种重要的化工原料,工厂生产出的浓硝酸可用铝槽车或铁槽车来运输。在常温
3
下能使铝、铁钝化,说明浓硝酸具有很强的________性。
(5)“吸收塔” 尾部会有含NO、NO 等氮氧化物的尾气排出,为消除它们对环境的污染,
2
通常用以下两种方法处理:
①纯碱溶液吸收法。纯碱溶液与NO 的反应原理为NaCO +2NO ===NaNO +__________
2 2 3 2 3
+CO(完成化学方程式)。
2
②氨转化法。已知7 mol氨恰好能将含NO和NO 共6 mol的混合气体完全转化为N ,则混
2 2
合气体中NO和NO 的物质的量之比为________,若用通式NO 表示氮氧化物,则每摩尔氨
2 x
可将________ mol的NO 转化为N。
x 2
答案 (1)CD (2)(或 0.045) (3)4NH +3O=====2N +6HO (4)氧化 (5)①NaNO
3 2 2 2 2
②1∶3
解析 (5)②7 mol 氨失去 21 mol 电子,根据题意和得失电子守恒可得 n(NO)+n(NO )=6
2
mol,2n(NO)+4n(NO )=21 mol,解得n(NO)=1.5 mol,n(NO )=4.5 mol,则混合气体中NO
2 2
和NO 的物质的量之比为1∶3,若用通式NO 表示氮氧化物,反应过程中NO 分子得到2x
2 x x
e-,则每摩尔氨可将 mol的NO 转化为N。
x 2
14.(2023·安徽淮南一模)某化学实验小组为了探究氨气的性质设计了如下实验方案。
实验一:探究氨气的溶解性
氨气具有强刺激性气味,会污染空气。实验小组经过多次尝试,最终将氨气的制备、收集、
检验和喷泉实验组装在一起,设计出如图装置。(1)写出气体发生装置仪器A中产生氨气的化学方程式:_____________________________。
(2)仪器B的名称为__________,为了保证喷泉实验的良好效果,B中可以放入的试剂是
__________。
(3)实验时,打开K,关闭K,打开K,将注射器中的浓氨水注入A中开始制备和收集氨气。
2 3 1
已 知 仪 器 C 中 放 入 的 是 滴 有 酚 酞 溶 液 的 湿 棉 花 , 则 仪 器 C 的 作 用 是
______________________。
在不拆除装置的前提下,引发喷泉的操作是__________________________________________
_______________________________________________________________________________
。
实验二:探究氨气的还原性
已知:Cu O为红色固体,在酸性溶液中不稳定:Cu O+HSO ===Cu+CuSO +HO。
2 2 2 4 4 2
(4)装置 G 用于制备氨气,仪器的连接顺序为 e→f→________→i,装置 H 的作用为
_______________________________________________________________________________。
实验开始前应先通一段时间的N,其目的是_________________________________________。
2
(5)反应结束后装置F中的氧化铜完全反应生成红色固体,为了探究红色固体的成分,进行
了如下实验:取15.6 g红色固体于烧杯中,加入足量稀硫酸充分搅拌、静置、过滤、洗涤、
干 燥 、 称 重 , 得 固 体 9.6 g , 则 红 色 固 体 的 成 分 及 物 质 的 量 为
____________________________。
答案 (1)CaO+NH ·H O===Ca(OH) +NH ↑ (2)球形干燥管 碱石灰 (3)吸收并检验氨气,
3 2 2 3
防止氨气直接排入空气中 关闭K 和K ,打开K (4)abcdgh 安全瓶、防倒吸 排尽装置
1 2 3
内的空气(合理即可) (5)Cu O 0.075 mol、Cu 0.075 mol
2
解析 (4)分析实验装置,装置G用于制备氨气,然后E用于干燥氨气,氨气和CuO在F中
发生反应,然后接H,起到安全瓶的作用,最后用I进行尾气吸收。(5)所得固体为Cu,物
质的量为=0.15 mol;过程中发生反应为Cu O+HSO ===Cu+CuSO +HO,每摩尔Cu O
2 2 4 4 2 2与酸反应前后质量损失为80 g,根据反应前后质量损失为15.6 g-9.6 g=6 g,则参加反应的
Cu O为=0.075 mol,则生成Cu的物质的量为0.075 mol,所以原固体中Cu O的物质的量为
2 2
0.075 mol,Cu物质的量为=0.075 mol,故红色固体的成分及物质的量为Cu O 0.075 mol、
2
Cu 0.075 mol。