文档内容
第 65 讲 羧酸 羧酸衍生物
[复习目标] 1.掌握羧酸的结构与性质。2.熟悉酯、油脂、酰胺的结构特点及相关性质。3.掌
握乙酸乙酯的实验室制法。
考点一 羧酸
1.羧酸的组成和结构
(1)羧酸:由烃基(或氢原子)与羧基( )相连而构成的有机化合物。
(2)通式
一元羧酸的通式为R—COOH,饱和链状一元羧酸的分子通式:C H O(n≥1,n为整数)或
n 2n 2
C H COOH(n≥0,n为整数)。
n 2n+1
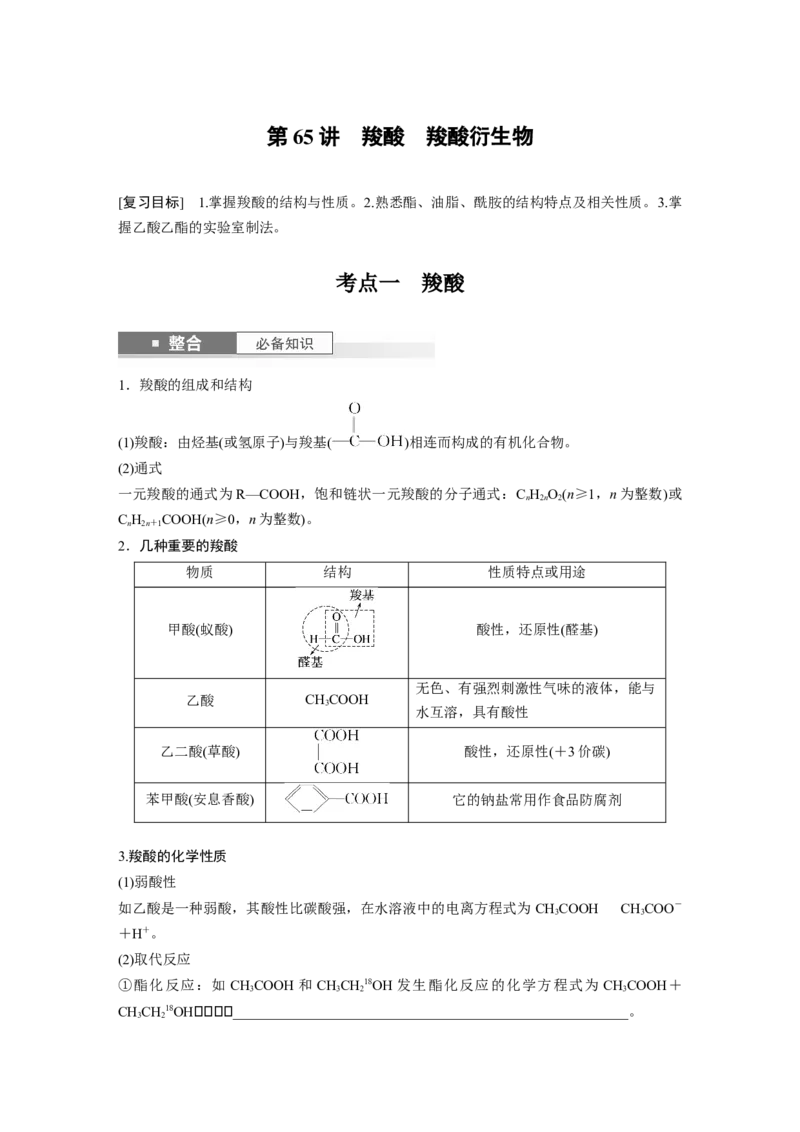
2.几种重要的羧酸
物质 结构 性质特点或用途
甲酸(蚁酸) 酸性,还原性(醛基)
无色、有强烈刺激性气味的液体,能与
乙酸 CHCOOH
3
水互溶,具有酸性
乙二酸(草酸) 酸性,还原性(+3价碳)
苯甲酸(安息香酸) 它的钠盐常用作食品防腐剂
3.羧酸的化学性质
(1)弱酸性
如乙酸是一种弱酸,其酸性比碳酸强,在水溶液中的电离方程式为 CHCOOHCHCOO-
3 3
+H+。
(2)取代反应
①酯化反应:如 CHCOOH 和 CHCH18OH 发生酯化反应的化学方程式为 CHCOOH+
3 3 2 3
CHCH18OH________________________________________________________。
3 2注意 酯化反应的机理是“酸脱羟基醇脱氢”。
②与NH 反应生成酰胺
3
如CHCOOH+NH ――→ +HO。
3 3 2
③α-H取代
如CHCHCOOH+Cl――→CHCHClCOOH+HCl。
3 2 2 3
注 意 在 强 还 原 剂 LiAlH 作 用 下 , 羧 酸 也 可 以 发 生 还 原 反 应 , 如
4
CHCHCOOH――→CHCHCHOH。
3 2 3 2 2
1.乙酸、硬脂酸、油酸互为同系物( )
2.乙醇能发生氧化反应,而乙酸不能发生氧化反应( )
3.能与NaHCO 溶液反应产生CO 的有机物应含有羧基( )
3 2
4.甲酸能发生银镜反应,能与新制的氢氧化铜反应生成砖红色沉淀( )
5.甲酸、乙酸和石炭酸都属于羧酸( )
一、羧酸的酸性
1.分子式为C H O 并能与饱和NaHCO 溶液反应放出气体的有机物有(不含立体异构)(
5 10 2 3
)
A.3种 B.4种 C.5种 D.6种
2.有机物A的结构简式是 ,下列有关A的性质的叙述错误的是(
)
A.A与金属钠完全反应时,两者物质的量之比是1∶3
B.A与氢氧化钠完全反应时,两者物质的量之比是1∶3
C.A能与碳酸钠溶液反应
D.A既能与羧酸反应,又能与醇反应
醇、酚、羧酸中羟基活泼性比较
羟基类型
醇羟基 酚羟基 羧羟基
比较项目
氢原子活泼性 ―――→电离 极难电离 微弱电离 部分电离
酸碱性 中性 很弱的酸性 弱酸性
与Na反应 反应放出H 反应放出H 反应放出H
2 2 2
与NaOH反应 不反应 反应 反应
与NaHCO 反应 不反应
3
不反应 反应放出CO
2
与NaCO 反应 反应,生成酚钠和NaHCO
2 3 3
二、羧酸的酯化反应
3.按要求书写酯化反应的化学方程式。
(1)一元羧酸与多元醇之间的酯化反应,如乙酸与乙二醇以物质的量之比为1∶1酯化:
_____________________________________________________________________________。
(2)多元羧酸与一元醇之间的酯化反应,如乙二酸与乙醇以物质的量之比为1∶2酯化:
_____________________________________________________________________________。
(3)多元羧酸与多元醇之间的酯化反应,如乙二酸与乙二醇酯化
①生成环酯:
_____________________________________________________________________________。
②生成高聚酯:
nHOOC—COOH+nHOCH CHOH_________________________________________。
2 2
(4)羟基酸自身的酯化反应,如 自身酯化
①生成环酯:
________________________________________________________________________。
②生成高聚酯:
________________________________________________________________________。
考点二 酯和油脂
1.酯
(1)定义:羧酸分子羧基中的________被—OR′取代后的产物,可简写为________。
(2)官能团:____________。
(3)物理性质:低级酯的物理性质(4)化学性质——水解反应(取代反应)
酯在酸性或碱性环境下,均可以发生水解反应。如乙酸乙酯的水解:
①酸性条件下水解:____________________________________________________________
________________________________________________________________________(可逆)。
②碱性条件下水解:____________________________________________________________
________________________________________________________________________(进行彻
底)。
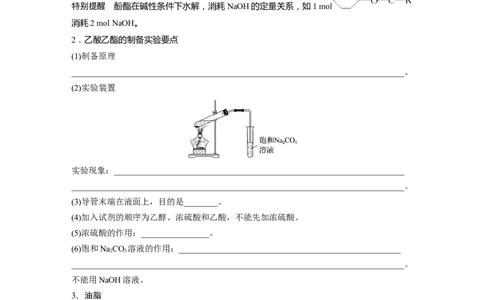
特别提醒 酚酯在碱性条件下水解,消耗NaOH的定量关系,如1 mol
消耗2 mol NaOH。
2.乙酸乙酯的制备实验要点
(1)制备原理
______________________________________________________________________________。
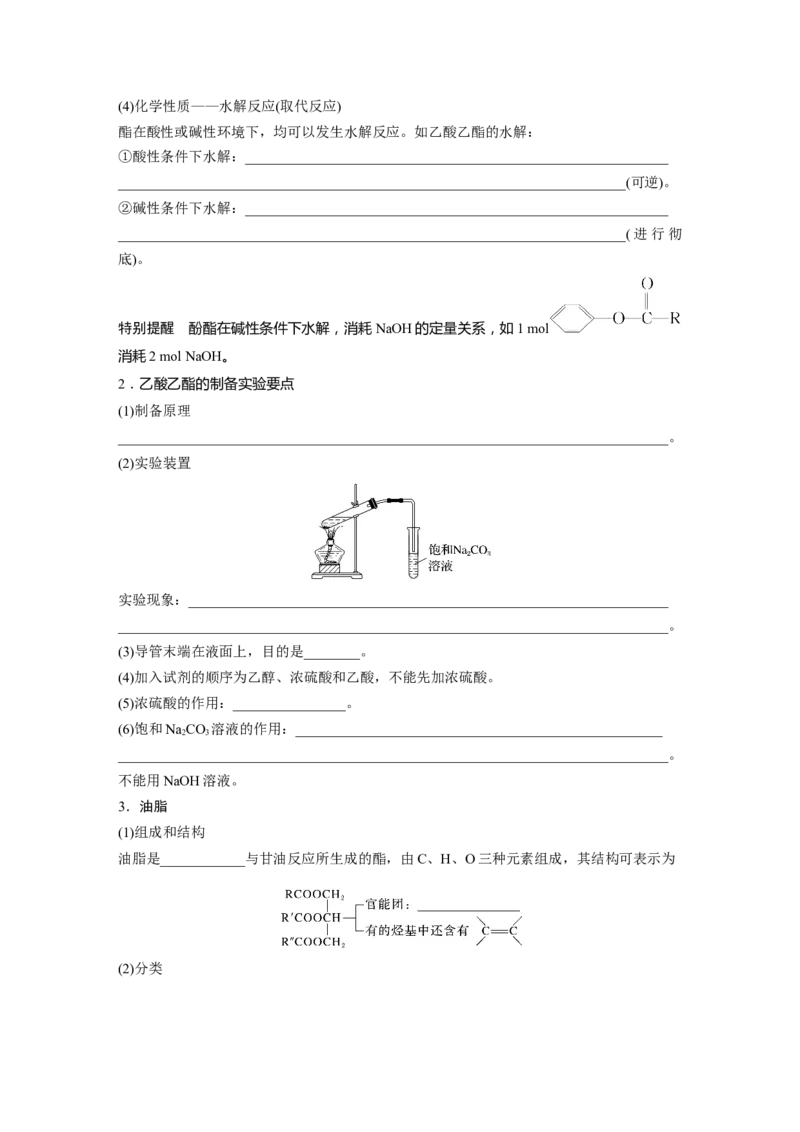
(2)实验装置
实验现象:____________________________________________________________________
______________________________________________________________________________。
(3)导管末端在液面上,目的是________。
(4)加入试剂的顺序为乙醇、浓硫酸和乙酸,不能先加浓硫酸。
(5)浓硫酸的作用:________________。
(6)饱和NaCO 溶液的作用:____________________________________________________
2 3
______________________________________________________________________________。
不能用NaOH溶液。
3.油脂
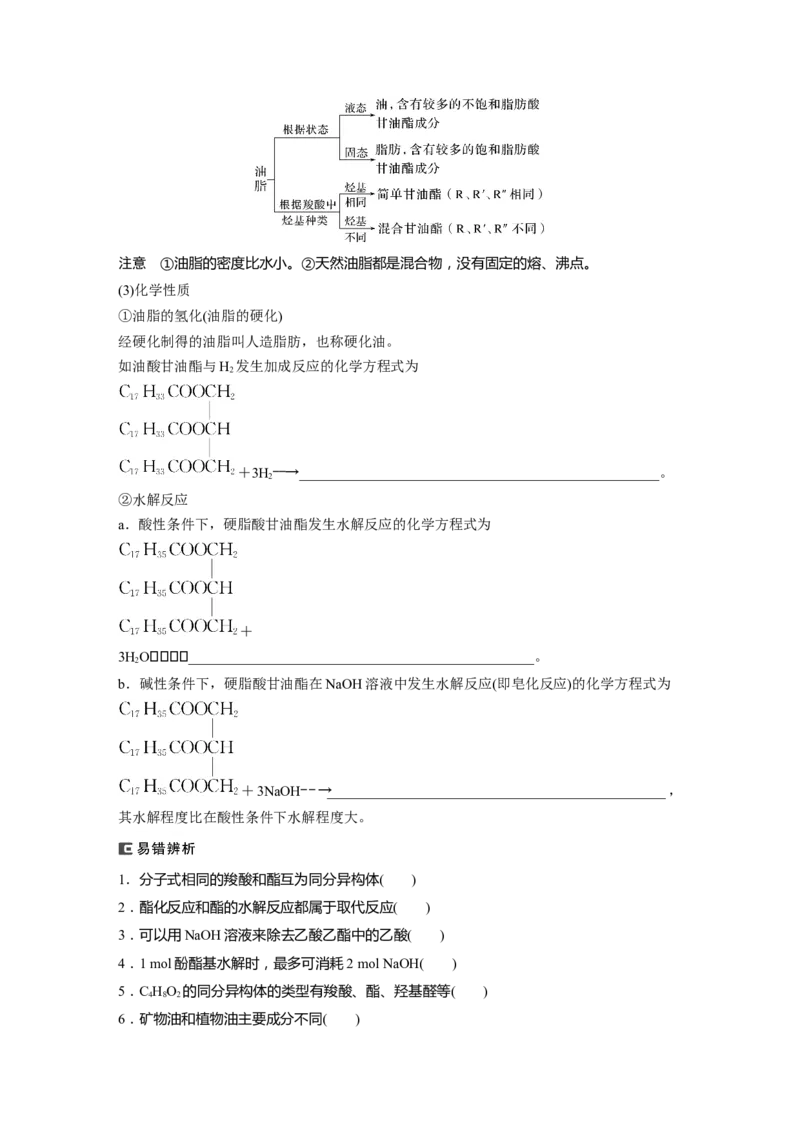
(1)组成和结构
油脂是____________与甘油反应所生成的酯,由C、H、O三种元素组成,其结构可表示为
(2)分类注意 ①油脂的密度比水小。②天然油脂都是混合物,没有固定的熔、沸点。
(3)化学性质
①油脂的氢化(油脂的硬化)
经硬化制得的油脂叫人造脂肪,也称硬化油。
如油酸甘油酯与H 发生加成反应的化学方程式为
2
+3H――→___________________________________________________。
2
②水解反应
a.酸性条件下,硬脂酸甘油酯发生水解反应的化学方程式为
+
3HO_________________________________________________。
2
b.碱性条件下,硬脂酸甘油酯在NaOH溶液中发生水解反应(即皂化反应)的化学方程式为
+3NaOH――→________________________________________________,
其水解程度比在酸性条件下水解程度大。
1.分子式相同的羧酸和酯互为同分异构体( )
2.酯化反应和酯的水解反应都属于取代反应( )
3.可以用NaOH溶液来除去乙酸乙酯中的乙酸( )
4.1 mol酚酯基水解时,最多可消耗2 mol NaOH( )
5.C HO 的同分异构体的类型有羧酸、酯、羟基醛等( )
4 8 2
6.矿物油和植物油主要成分不同( )7.“酯”和“脂”意义不同,不能混用( )
8.油脂的皂化反应属于加成反应( )
9.天然植物油常温下一般呈液态,难溶于水,有恒定的熔、沸点( )
一、羧酸和酯的同分异构体的书写
1.某芳香族化合物的分子式为C HO,分别写出所有羧酸和酯的结构简式。
8 8 2
_______________________________________________________________________________
_______________________________________________________________________________
二、酯化反应实验
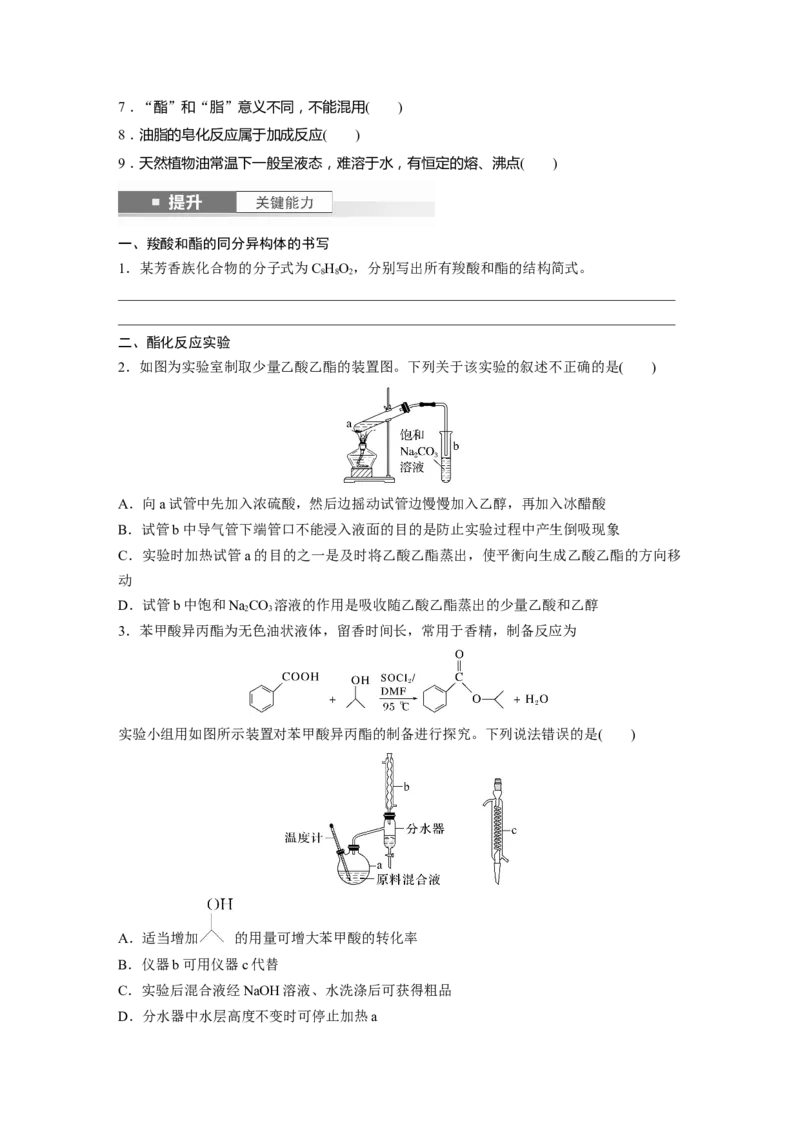
2.如图为实验室制取少量乙酸乙酯的装置图。下列关于该实验的叙述不正确的是( )
A.向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加入冰醋酸
B.试管b中导气管下端管口不能浸入液面的目的是防止实验过程中产生倒吸现象
C.实验时加热试管a的目的之一是及时将乙酸乙酯蒸出,使平衡向生成乙酸乙酯的方向移
动
D.试管b中饱和NaCO 溶液的作用是吸收随乙酸乙酯蒸出的少量乙酸和乙醇
2 3
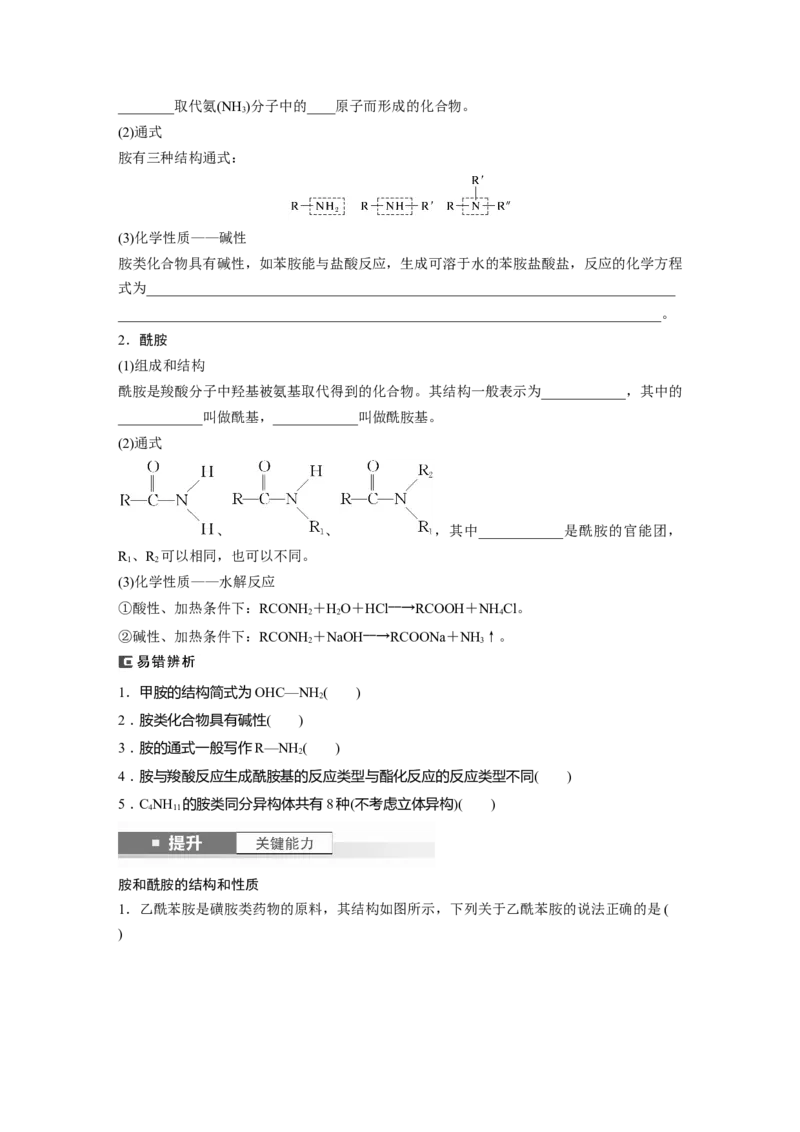
3.苯甲酸异丙酯为无色油状液体,留香时间长,常用于香精,制备反应为
实验小组用如图所示装置对苯甲酸异丙酯的制备进行探究。下列说法错误的是( )
A.适当增加 的用量可增大苯甲酸的转化率
B.仪器b可用仪器c代替
C.实验后混合液经NaOH溶液、水洗涤后可获得粗品
D.分水器中水层高度不变时可停止加热a三、油脂的组成、性质和应用
4.“油”在生活生产中应用广泛,下列有关“油”的说法正确的是( )
A.食用油的主要成分是不饱和高级脂肪酸甘油酯,属于天然有机高分子
B.汽油、煤油、生物柴油等均来源于石油,主要成分都是烃类
C.甘油是丙三醇的俗称,既可以做护肤品,又可以制作炸药
D.天然奶油、黄油等是从牛奶或羊奶中提取出来的半固态物质,属于蛋白质
5.某物质的结构为 ,下列关于该物质的叙述正确的是( )
A.一定条件下与氢气反应可以生成硬脂酸甘油酯
B.1 mol该物质一定条件下可与3 mol H 发生加成反应
2
C.与氢氧化钠溶液混合加热能得到肥皂的主要成分
D.与其互为同分异构体且完全水解后产物相同的油脂有三种
脂肪、油、矿物油三者的比较
油脂
物质 矿物油
脂肪 油
多种高级脂肪酸的甘油酯
组成 多种烃(石油及其分馏产品)
含饱和烃基多 含不饱和烃基多
固态或半固态 液态
性质 具有酯的性质,能水解,有的油脂兼有烯烃 具有烃的性质,不能水解
的性质
加含酚酞的NaOH溶液,加热,红色变浅, 加含酚酞的NaOH溶液,加
鉴别
液体不再分层 热,无变化
人类重要的营养物质和食物之一;化工原料
用途 燃料、化工原料
如制肥皂、甘油
考点三 胺和酰胺
1.胺
(1)概念________取代氨(NH )分子中的____原子而形成的化合物。
3
(2)通式
胺有三种结构通式:
(3)化学性质——碱性
胺类化合物具有碱性,如苯胺能与盐酸反应,生成可溶于水的苯胺盐酸盐,反应的化学方程
式为___________________________________________________________________________
_____________________________________________________________________________。
2.酰胺
(1)组成和结构
酰胺是羧酸分子中羟基被氨基取代得到的化合物。其结构一般表示为____________,其中的
____________叫做酰基,____________叫做酰胺基。
(2)通式
、 、 ,其中____________是酰胺的官能团,
R 、R 可以相同,也可以不同。
1 2
(3)化学性质——水解反应
①酸性、加热条件下:RCONH +HO+HCl――→RCOOH+NH Cl。
2 2 4
②碱性、加热条件下:RCONH +NaOH――→RCOONa+NH ↑。
2 3
1.甲胺的结构简式为OHC—NH( )
2
2.胺类化合物具有碱性( )
3.胺的通式一般写作R—NH ( )
2
4.胺与羧酸反应生成酰胺基的反应类型与酯化反应的反应类型不同( )
5.C NH 的胺类同分异构体共有8种(不考虑立体异构)( )
4 11
胺和酰胺的结构和性质
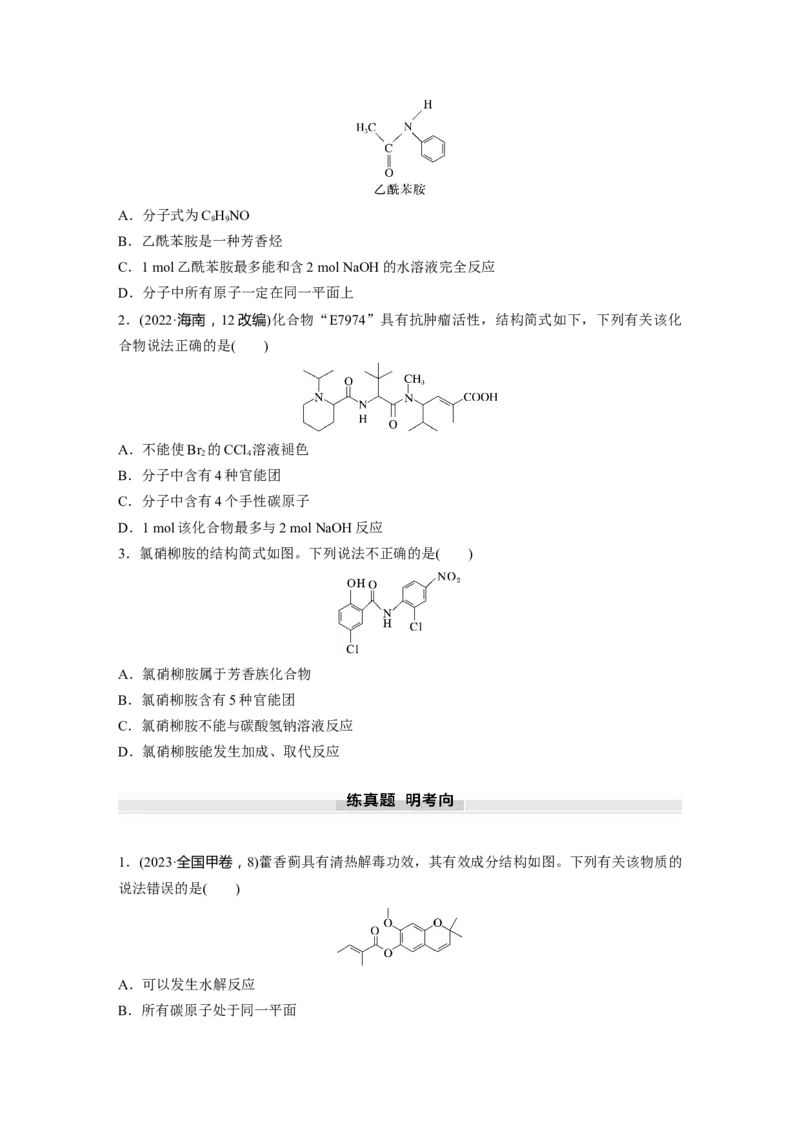
1.乙酰苯胺是磺胺类药物的原料,其结构如图所示,下列关于乙酰苯胺的说法正确的是(
)A.分子式为C HNO
8 9
B.乙酰苯胺是一种芳香烃
C.1 mol乙酰苯胺最多能和含2 mol NaOH的水溶液完全反应
D.分子中所有原子一定在同一平面上
2.(2022·海南,12改编)化合物“E7974”具有抗肿瘤活性,结构简式如下,下列有关该化
合物说法正确的是( )
A.不能使Br 的CCl 溶液褪色
2 4
B.分子中含有4种官能团
C.分子中含有4个手性碳原子
D.1 mol该化合物最多与2 mol NaOH反应
3.氯硝柳胺的结构简式如图。下列说法不正确的是( )
A.氯硝柳胺属于芳香族化合物
B.氯硝柳胺含有5种官能团
C.氯硝柳胺不能与碳酸氢钠溶液反应
D.氯硝柳胺能发生加成、取代反应
1.(2023·全国甲卷,8)藿香蓟具有清热解毒功效,其有效成分结构如图。下列有关该物质的
说法错误的是( )
A.可以发生水解反应
B.所有碳原子处于同一平面C.含有2种含氧官能团
D.能与溴水发生加成反应
2.(2023·北京,11)化合物K与L反应可合成药物中间体M,转化关系如下。
已知L能发生银镜反应,下列说法正确的是( )
A.K的核磁共振氢谱有两组峰
B.L是乙醛
C.M完全水解可得到K和L
D.反应物K与L的化学计量比是1∶1
3.(2023·新课标卷,8)光学性能优良的高分子材料聚碳酸异山梨醇酯可由如下反应制备。
下列说法错误的是( )
A.该高分子材料可降解
B.异山梨醇分子中有3个手性碳
C.反应式中化合物X为甲醇
D.该聚合反应为缩聚反应
4.(2022·河北,2)茯苓新酸DM是从中药茯苓中提取的一种化学物质,具有一定生理活性,
其结构简式如图。关于该化合物,下列说法错误的是( )
A.可使酸性KMnO 溶液褪色
4
B.可发生取代反应和加成反应
C.可与金属钠反应放出H
2
D.分子中含有3种官能团
5.(2022·湖南,3)聚乳酸是一种新型的生物可降解高分子材料,其合成路线如下:
下列说法错误的是( )A.m=n-1
B.聚乳酸分子中含有两种官能团
C.1 mol乳酸与足量的Na反应生成1 mol H
2
D.两分子乳酸反应能够生成含六元环的分子