文档内容
第 56 讲 溶液中的粒子平衡曲线分类突破
[复习目标] 1.能正确识别图像,能从图像中找到曲线指代、趋势、关键点。2.利用溶液中
的平衡关系,学会分析不同类型图像中各粒子浓度之间的关系。
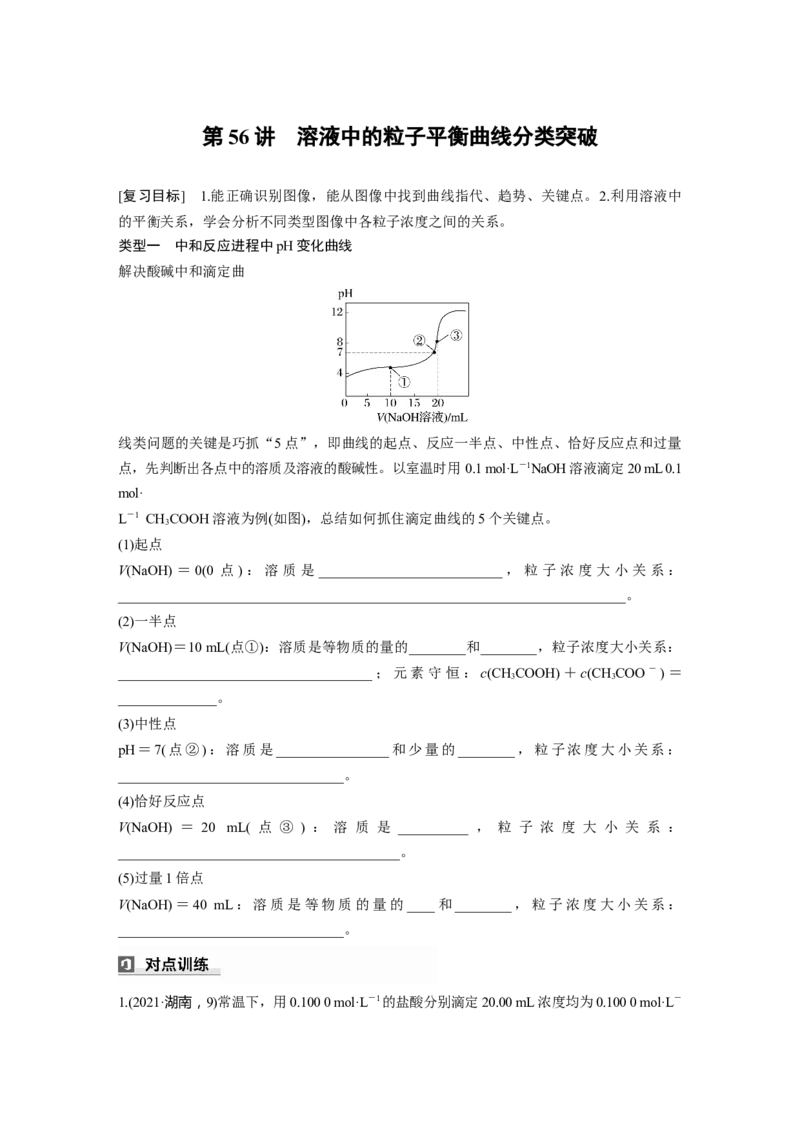
类型一 中和反应进程中pH变化曲线
解决酸碱中和滴定曲
线类问题的关键是巧抓“5点”,即曲线的起点、反应一半点、中性点、恰好反应点和过量
点,先判断出各点中的溶质及溶液的酸碱性。以室温时用 0.1 mol·L-1NaOH溶液滴定20 mL 0.1
mol·
L-1 CHCOOH溶液为例(如图),总结如何抓住滴定曲线的5个关键点。
3
(1)起点
V(NaOH)=0(0 点):溶质是__________________________,粒子浓度大小关系:
________________________________________________________________________。
(2)一半点
V(NaOH)=10 mL(点①):溶质是等物质的量的________和________,粒子浓度大小关系:
____________________________________;元素守恒:c(CHCOOH)+c(CHCOO-)=
3 3
______________。
(3)中性点
pH=7(点②):溶质是________________和少量的________,粒子浓度大小关系:
________________________________。
(4)恰好反应点
V(NaOH) = 20 mL( 点 ③ ) : 溶 质 是 __________ , 粒 子 浓 度 大 小 关 系 :
________________________________________。
(5)过量1倍点
V(NaOH)=40 mL:溶质是等物质的量的____和________,粒子浓度大小关系:
________________________________。
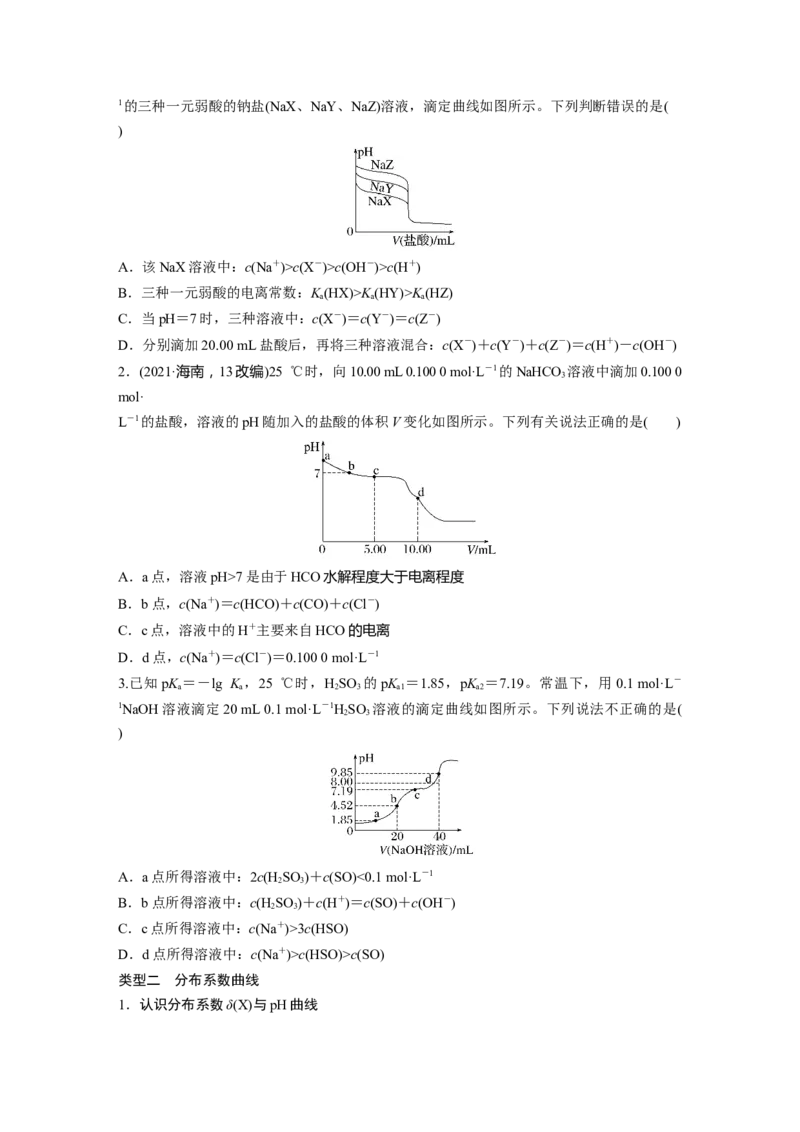
1.(2021·湖南,9)常温下,用0.100 0 mol·L-1的盐酸分别滴定20.00 mL浓度均为0.100 0 mol·L-1的三种一元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是(
)
A.该NaX溶液中:c(Na+)>c(X-)>c(OH-)>c(H+)
B.三种一元弱酸的电离常数:K(HX)>K(HY)>K(HZ)
a a a
C.当pH=7时,三种溶液中:c(X-)=c(Y-)=c(Z-)
D.分别滴加20.00 mL盐酸后,再将三种溶液混合:c(X-)+c(Y-)+c(Z-)=c(H+)-c(OH-)
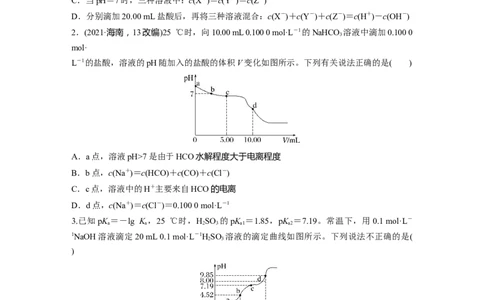
2.(2021·海南,13改编)25 ℃时,向10.00 mL 0.100 0 mol·L-1的NaHCO 溶液中滴加0.100 0
3
mol·
L-1的盐酸,溶液的pH随加入的盐酸的体积V变化如图所示。下列有关说法正确的是( )
A.a点,溶液pH>7是由于HCO水解程度大于电离程度
B.b点,c(Na+)=c(HCO)+c(CO)+c(Cl-)
C.c点,溶液中的H+主要来自HCO的电离
D.d点,c(Na+)=c(Cl-)=0.100 0 mol·L-1
3.已知pK =-lg K ,25 ℃时,HSO 的pK =1.85,pK =7.19。常温下,用0.1 mol·L-
a a 2 3 a1 a2
1NaOH溶液滴定20 mL 0.1 mol·L-1HSO 溶液的滴定曲线如图所示。下列说法不正确的是(
2 3
)
A.a点所得溶液中:2c(H SO )+c(SO)<0.1 mol·L-1
2 3
B.b点所得溶液中:c(H SO )+c(H+)=c(SO)+c(OH-)
2 3
C.c点所得溶液中:c(Na+)>3c(HSO)
D.d点所得溶液中:c(Na+)>c(HSO)>c(SO)
类型二 分布系数曲线
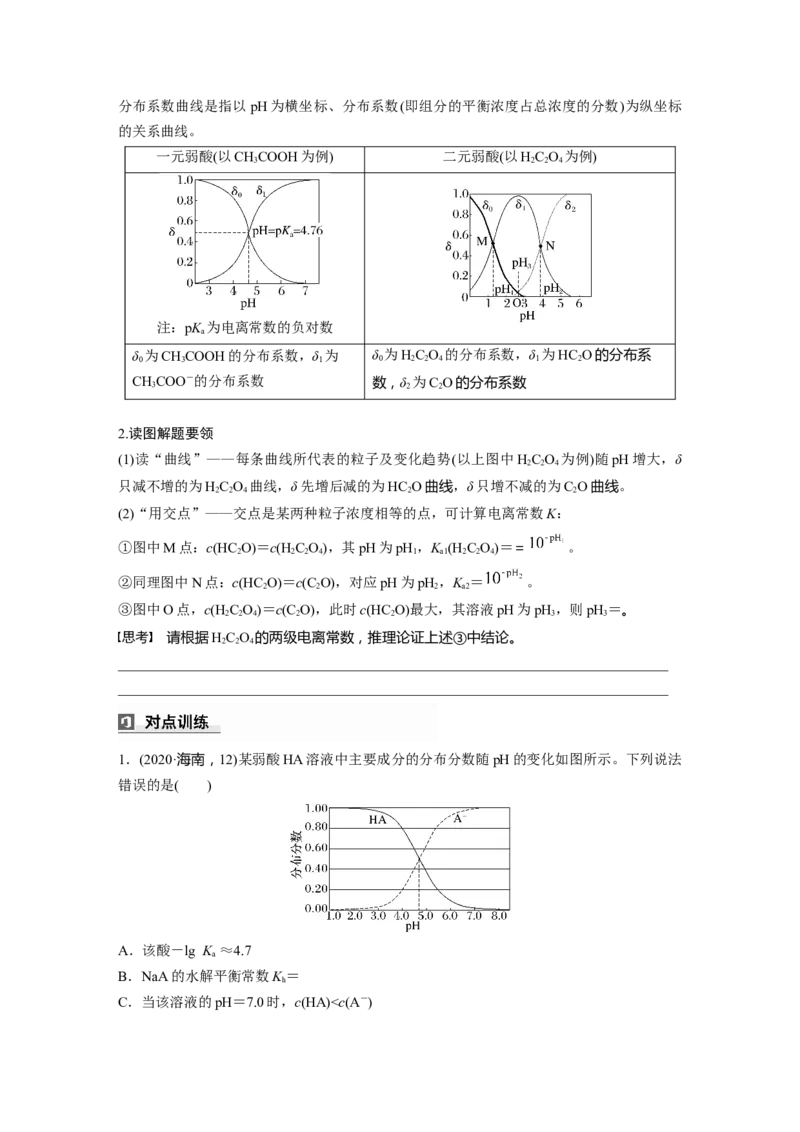
1.认识分布系数δ(X)与pH曲线分布系数曲线是指以pH为横坐标、分布系数(即组分的平衡浓度占总浓度的分数)为纵坐标
的关系曲线。
一元弱酸(以CHCOOH为例) 二元弱酸(以HC O 为例)
3 2 2 4
注:pK 为电离常数的负对数
a
δ 为CHCOOH的分布系数,δ 为 δ 为HC O 的分布系数,δ 为HC O的分布系
0 3 1 0 2 2 4 1 2
CH
3
COO-的分布系数 数,δ
2
为C
2
O的分布系数
2.读图解题要领
(1)读“曲线”——每条曲线所代表的粒子及变化趋势(以上图中HC O 为例)随pH增大,δ
2 2 4
只减不增的为HC O 曲线,δ先增后减的为HC O曲线,δ只增不减的为C O曲线。
2 2 4 2 2
(2)“用交点”——交点是某两种粒子浓度相等的点,可计算电离常数K:
①图中M点:c(HC O)=c(H C O),其pH为pH,K (H C O)== 。
2 2 2 4 1 a1 2 2 4
②同理图中N点:c(HC O)=c(C O),对应pH为pH,K = 。
2 2 2 a2
③图中O点,c(H C O)=c(C O),此时c(HC O)最大,其溶液pH为pH,则pH=。
2 2 4 2 2 3 3
思考 请根据HC O 的两级电离常数,推理论证上述③中结论。
2 2 4
______________________________________________________________________________
______________________________________________________________________________
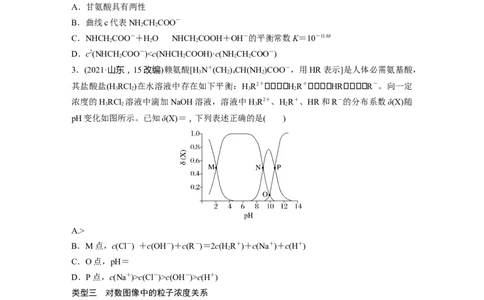
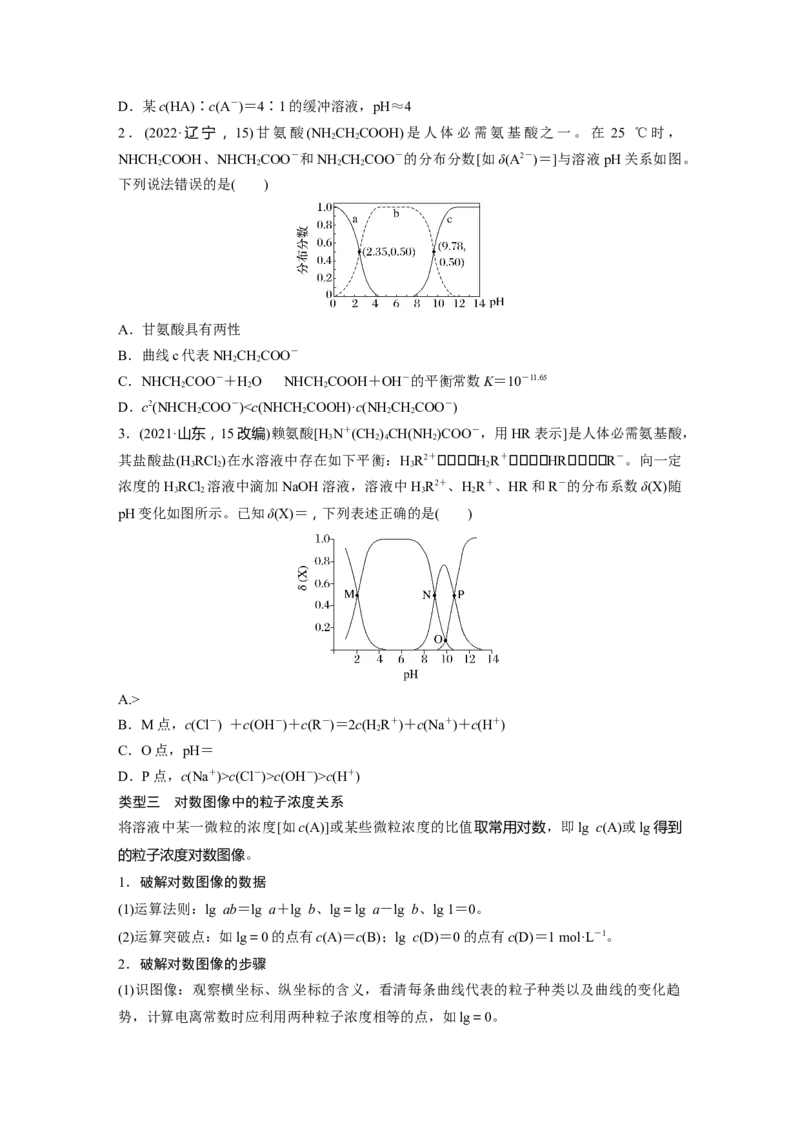
1.(2020·海南,12)某弱酸HA溶液中主要成分的分布分数随pH的变化如图所示。下列说法
错误的是( )
A.该酸-lg K ≈4.7
a
B.NaA的水解平衡常数K =
h
C.当该溶液的pH=7.0时,c(HA)
B.M点,c(Cl-) +c(OH-)+c(R-)=2c(H R+)+c(Na+)+c(H+)
2
C.O点,pH=
D.P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)
类型三 对数图像中的粒子浓度关系
将溶液中某一微粒的浓度[如c(A)]或某些微粒浓度的比值取常用对数,即lg c(A)或lg得到
的粒子浓度对数图像。
1.破解对数图像的数据
(1)运算法则:lg ab=lg a+lg b、lg=lg a-lg b、lg 1=0。
(2)运算突破点:如lg=0的点有c(A)=c(B);lg c(D)=0的点有c(D)=1 mol·L-1。
2.破解对数图像的步骤
(1)识图像:观察横坐标、纵坐标的含义,看清每条曲线代表的粒子种类以及曲线的变化趋
势,计算电离常数时应利用两种粒子浓度相等的点,如lg=0。(2)找联系:根据图像中的坐标含义和曲线的交点,分析所给电解质的电离平衡常数或pH与
纵、横坐标之间的联系。
(3)想原理:涉及电离平衡常数,写出平衡常数表达式,在识图像、想原理的基础上,将图
像与原理结合起来思考。
(4)用公式:运用对数计算公式分析。
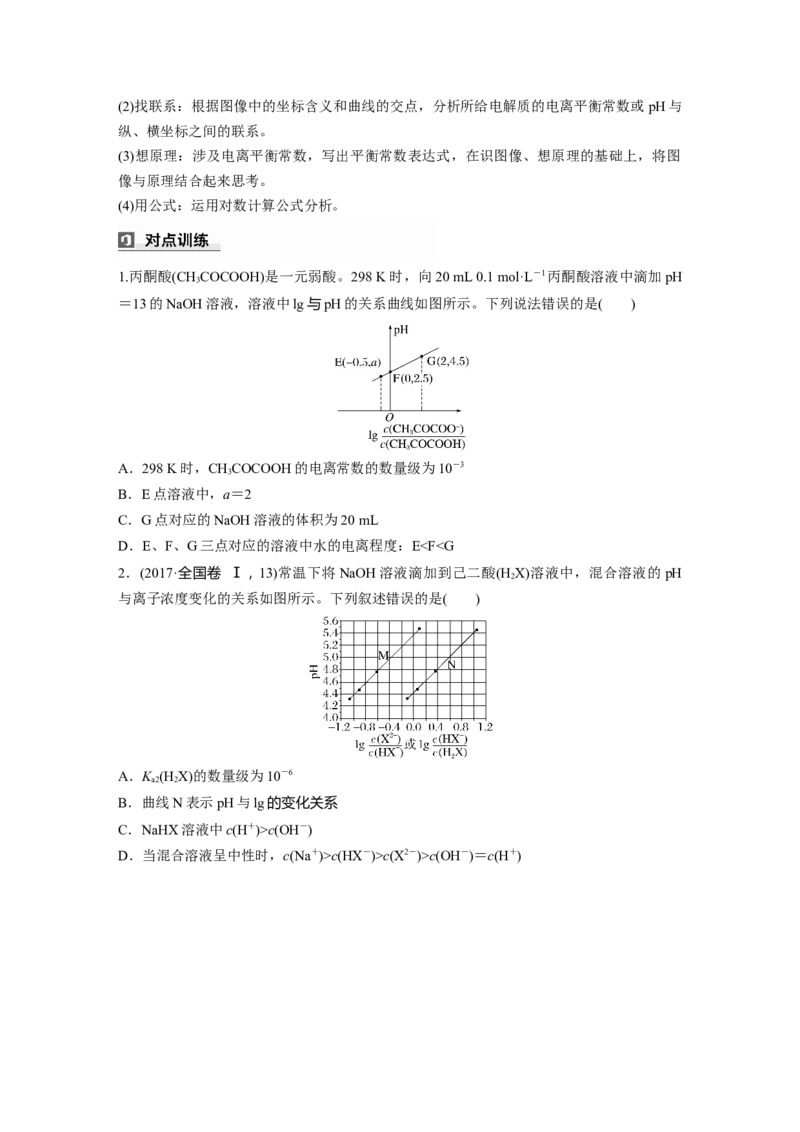
1.丙酮酸(CHCOCOOH)是一元弱酸。298 K时,向20 mL 0.1 mol·L-1丙酮酸溶液中滴加pH
3
=13的NaOH溶液,溶液中lg与pH的关系曲线如图所示。下列说法错误的是( )
A.298 K时,CHCOCOOH的电离常数的数量级为10-3
3
B.E点溶液中,a=2
C.G点对应的NaOH溶液的体积为20 mL
D.E、F、G三点对应的溶液中水的电离程度:Ec(OH-)
D.当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(OH-)=c(H+)