文档内容
第 38 讲 反应热 热化学方程式
[复习目标] 1.知道常见的吸热反应和放热反应,理解反应热、焓变及相关概念。2.了解中
和反应反应热的测定方法。3.能正确书写热化学方程式。4.会分析化学反应过程中能量变化
图像。5.了解燃烧热的含义和能源及其利用的意义。
考点一 反应热 焓变
1.反应热和焓变及相关概念
(1)反应热
(2)焓和焓变
2.识记常见的吸热反应和放热反应
有下列常见的化学反应:
①Ba(OH) ·8H O与NH Cl的反应 ②大多数的分解反应 ③大多数的化合反应 ④大多数
2 2 4
的盐类水解 ⑤C和HO(g)、C和CO 的反应 ⑥中和反应 ⑦可燃物的燃烧
2 2
⑧金属与酸的置换反应 ⑨铝热反应其中属于放热反应的是______________(填序号,下同),属于吸热反应的是__________。
3.反应过程中能量变化的原因
(1)从化学键变化分析
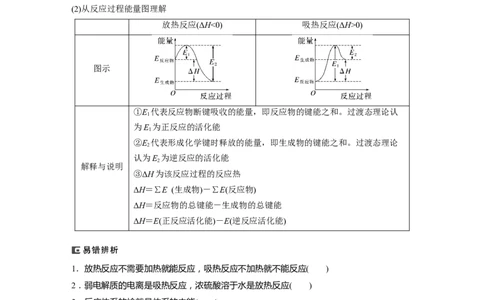
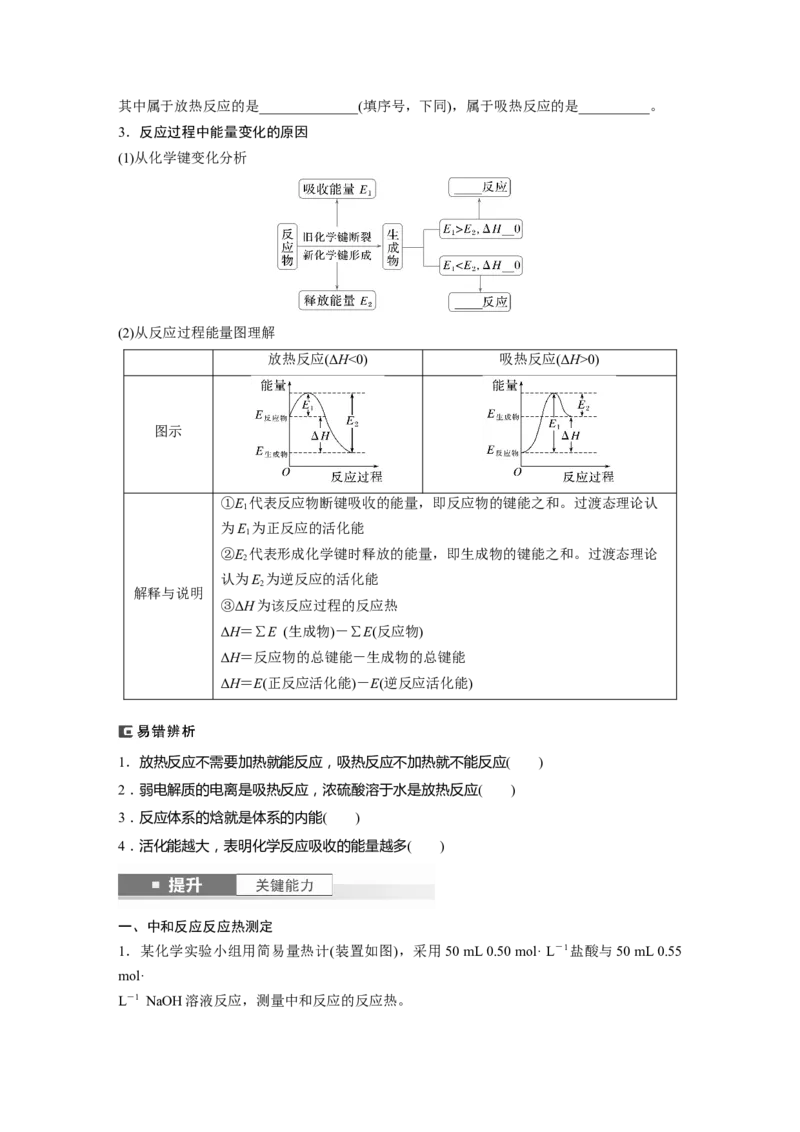
(2)从反应过程能量图理解
放热反应(ΔH<0) 吸热反应(ΔH>0)
图示
①E 代表反应物断键吸收的能量,即反应物的键能之和。过渡态理论认
1
为E 为正反应的活化能
1
②E 代表形成化学键时释放的能量,即生成物的键能之和。过渡态理论
2
认为E 为逆反应的活化能
2
解释与说明
③ΔH为该反应过程的反应热
ΔH=∑E (生成物)-∑E(反应物)
ΔH=反应物的总键能-生成物的总键能
ΔH=E(正反应活化能)-E(逆反应活化能)
1.放热反应不需要加热就能反应,吸热反应不加热就不能反应( )
2.弱电解质的电离是吸热反应,浓硫酸溶于水是放热反应( )
3.反应体系的焓就是体系的内能( )
4.活化能越大,表明化学反应吸收的能量越多( )
一、中和反应反应热测定
1.某化学实验小组用简易量热计(装置如图),采用50 mL 0.50 mol· L-1盐酸与50 mL 0.55
mol·
L-1 NaOH溶液反应,测量中和反应的反应热。测定操作
Ⅰ.用量筒量取50 mL 0.50 mol·L-1盐酸倒入量热计内筒中,测出盐酸的温度;
Ⅱ.用另一量筒量取50 mL 0.55 mol·L-1 NaOH溶液,并用同一温度计测出其温度;
Ⅲ.将NaOH溶液倒入量热计内筒中,使之混合均匀,测得混合液最高温度。
重复上述步骤,记录数据。
回答下列问题:
(1)NaOH溶液与盐酸混合均匀的正确操作是________(填字母)。
a.把NaOH溶液分多次倒入量热计内筒小烧杯中与盐酸反应
b.用温度计小心搅拌
c.揭开杯盖用玻璃棒搅拌
d.用套在温度计上的玻璃搅拌器上下轻轻地搅动
e.实验时可用铜质搅拌器代替玻璃搅拌器
(2)NaOH溶液稍过量的原因:______________________________________________。
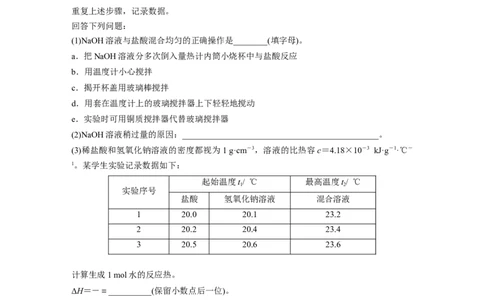
(3)稀盐酸和氢氧化钠溶液的密度都视为1 g·cm-3,溶液的比热容c=4.18×10-3 kJ·g-1·℃-
1。某学生实验记录数据如下:
起始温度t/ ℃ 最高温度t/ ℃
1 2
实验序号
盐酸 氢氧化钠溶液 混合溶液
1 20.0 20.1 23.2
2 20.2 20.4 23.4
3 20.5 20.6 23.6
计算生成1 mol水的反应热。
ΔH=-=__________(保留小数点后一位)。
(4)问题讨论
①在中和反应反应热的测定实验中,使用弱酸或弱碱会使测得的中和反应反应热数值
____( 填 “ 偏 高 ” “ 不 变 ” 或 “ 偏 低 ” ) , 其 原 因 是
_________________________________________
______________________________________________________________________________。
②有两组实验:ⅰ.50 mL 0.50 mol·L-1盐酸和50 mL 0.55 mol·L-1 NaOH溶液,ⅱ.60 mL 0.50
mol·
L-1盐酸和50 mL 0.55 mol·L-1 NaOH溶液。实验ⅰ、ⅱ反应放出的热量______(填“相等”
或“不相等”,下同),测得的中和反应反应热________,原因是___________________________________________________________________________________________________。
二、反应过程中物质能量变化图像
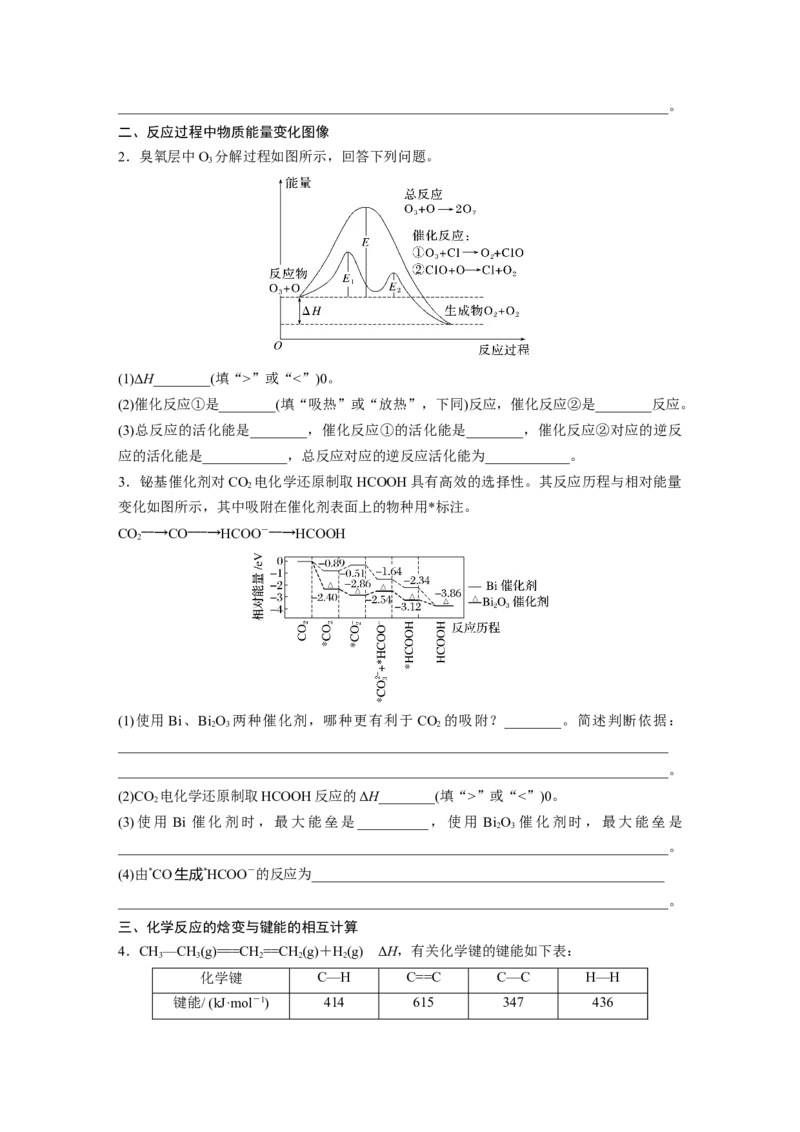
2.臭氧层中O 分解过程如图所示,回答下列问题。
3
(1)ΔH________(填“>”或“<”)0。
(2)催化反应①是________(填“吸热”或“放热”,下同)反应,催化反应②是________反应。
(3)总反应的活化能是________,催化反应①的活化能是________,催化反应②对应的逆反
应的活化能是____________,总反应对应的逆反应活化能为____________。
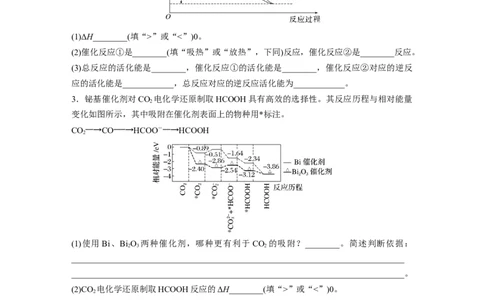
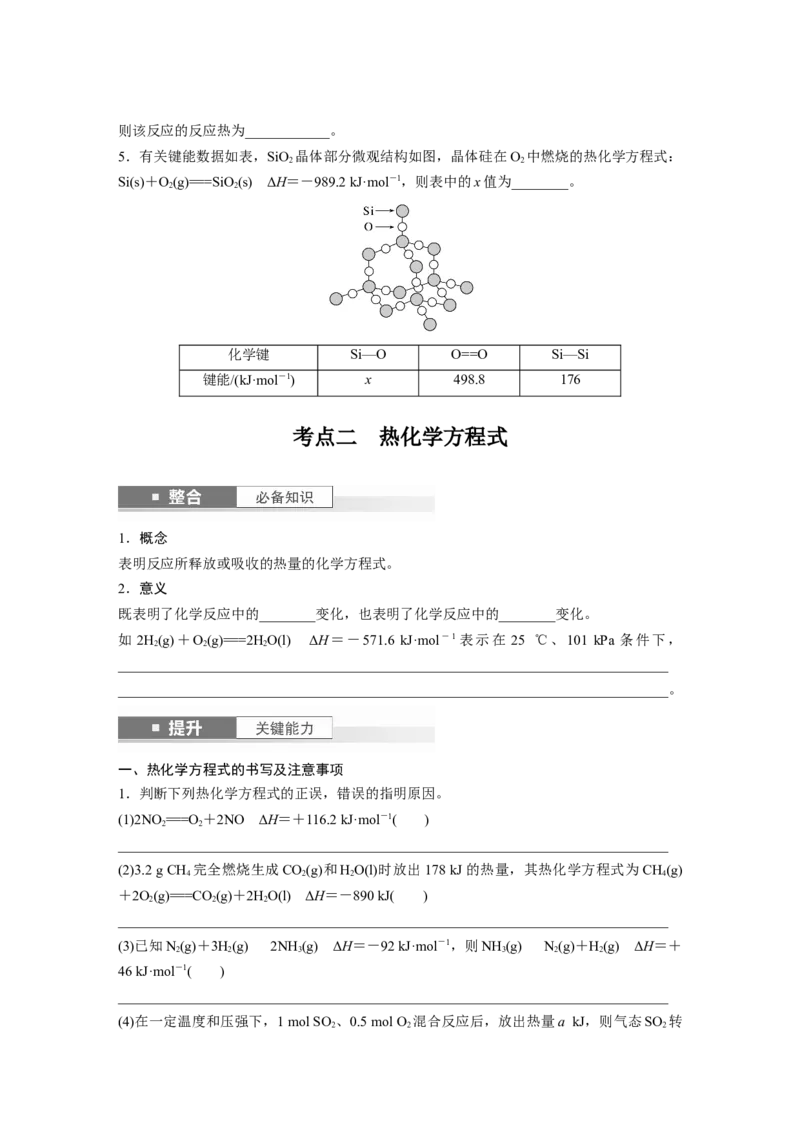
3.铋基催化剂对CO 电化学还原制取HCOOH具有高效的选择性。其反应历程与相对能量
2
变化如图所示,其中吸附在催化剂表面上的物种用*标注。
CO――→CO―――→HCOO-――→HCOOH
2
(1)使用Bi、BiO 两种催化剂,哪种更有利于 CO 的吸附?________。简述判断依据:
2 3 2
______________________________________________________________________________
______________________________________________________________________________。
(2)CO 电化学还原制取HCOOH反应的ΔH________(填“>”或“<”)0。
2
(3)使用 Bi 催化剂时,最大能垒是__________,使用 BiO 催化剂时,最大能垒是
2 3
______________________________________________________________________________。
(4)由*CO生成*HCOO-的反应为__________________________________________________
______________________________________________________________________________。
三、化学反应的焓变与键能的相互计算
4.CH—CH(g)===CH==CH(g)+H(g) ΔH,有关化学键的键能如下表:
3 3 2 2 2
化学键 C—H C==C C—C H—H
键能/ (kJ·mol-1) 414 615 347 436则该反应的反应热为____________。
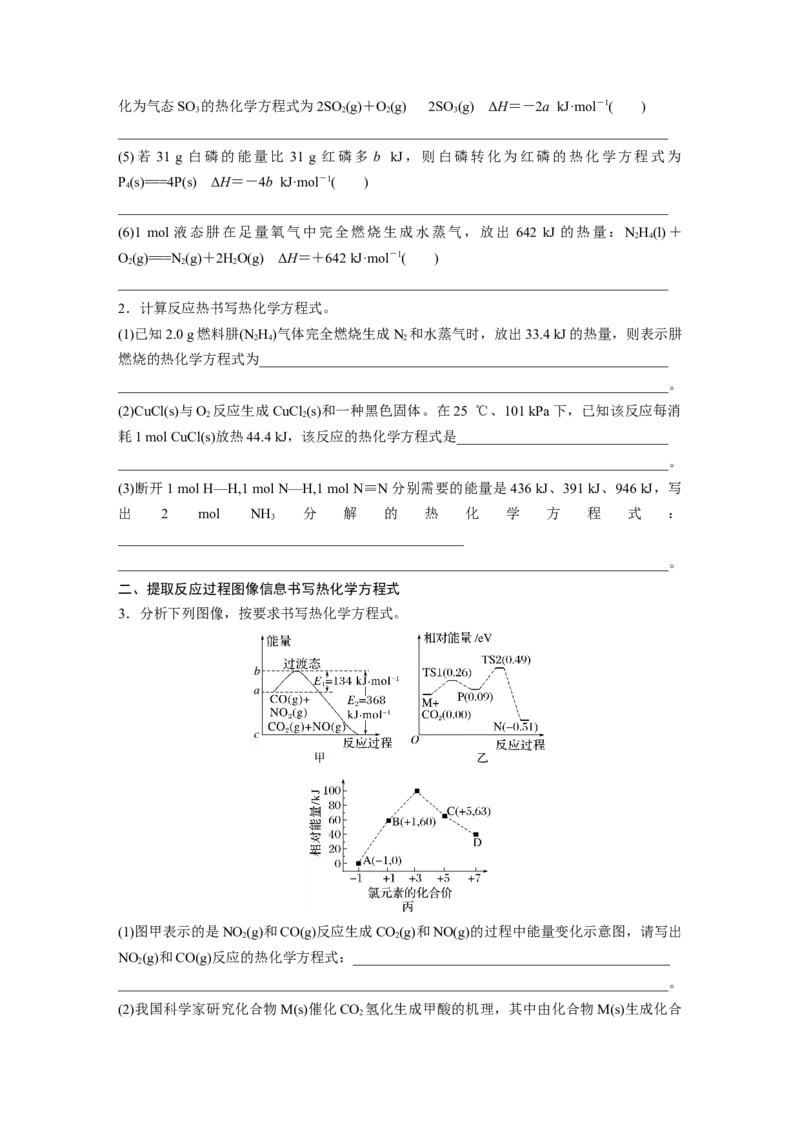
5.有关键能数据如表,SiO 晶体部分微观结构如图,晶体硅在O 中燃烧的热化学方程式:
2 2
Si(s)+O(g)===SiO(s) ΔH=-989.2 kJ·mol-1,则表中的x值为________。
2 2
化学键 Si—O O==O Si—Si
键能/(kJ·mol-1) x 498.8 176
考点二 热化学方程式
1.概念
表明反应所释放或吸收的热量的化学方程式。
2.意义
既表明了化学反应中的________变化,也表明了化学反应中的________变化。
如 2H(g)+O(g)===2HO(l) ΔH=-571.6 kJ·mol-1表示在 25 ℃、101 kPa 条件下,
2 2 2
______________________________________________________________________________
______________________________________________________________________________。
一、热化学方程式的书写及注意事项
1.判断下列热化学方程式的正误,错误的指明原因。
(1)2NO ===O+2NO ΔH=+116.2 kJ·mol-1( )
2 2
______________________________________________________________________________
(2)3.2 g CH 完全燃烧生成CO(g)和HO(l)时放出178 kJ的热量,其热化学方程式为CH(g)
4 2 2 4
+2O(g)===CO(g)+2HO(l) ΔH=-890 kJ( )
2 2 2
______________________________________________________________________________
(3)已知N(g)+3H(g)2NH (g) ΔH=-92 kJ·mol-1,则NH (g)N(g)+H(g) ΔH=+
2 2 3 3 2 2
46 kJ·mol-1( )
______________________________________________________________________________
(4)在一定温度和压强下,1 mol SO 、0.5 mol O 混合反应后,放出热量a kJ,则气态SO 转
2 2 2化为气态SO 的热化学方程式为2SO (g)+O(g)2SO (g) ΔH=-2a kJ·mol-1( )
3 2 2 3
______________________________________________________________________________
(5)若 31 g 白磷的能量比 31 g 红磷多 b kJ,则白磷转化为红磷的热化学方程式为
P(s)===4P(s) ΔH=-4b kJ·mol-1( )
4
______________________________________________________________________________
(6)1 mol 液态肼在足量氧气中完全燃烧生成水蒸气,放出 642 kJ 的热量:NH(l)+
2 4
O(g)===N(g)+2HO(g) ΔH=+642 kJ·mol-1( )
2 2 2
______________________________________________________________________________
2.计算反应热书写热化学方程式。
(1)已知2.0 g燃料肼(N H)气体完全燃烧生成N 和水蒸气时,放出33.4 kJ的热量,则表示肼
2 4 2
燃烧的热化学方程式为__________________________________________________________
______________________________________________________________________________。
(2)CuCl(s)与O 反应生成CuCl (s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消
2 2
耗1 mol CuCl(s)放热44.4 kJ,该反应的热化学方程式是______________________________
______________________________________________________________________________。
(3)断开1 mol H—H,1 mol N—H,1 mol N≡N分别需要的能量是436 kJ、391 kJ、946 kJ,写
出 2 mol NH 分 解 的 热 化 学 方 程 式 :
3
_________________________________________________
______________________________________________________________________________。
二、提取反应过程图像信息书写热化学方程式
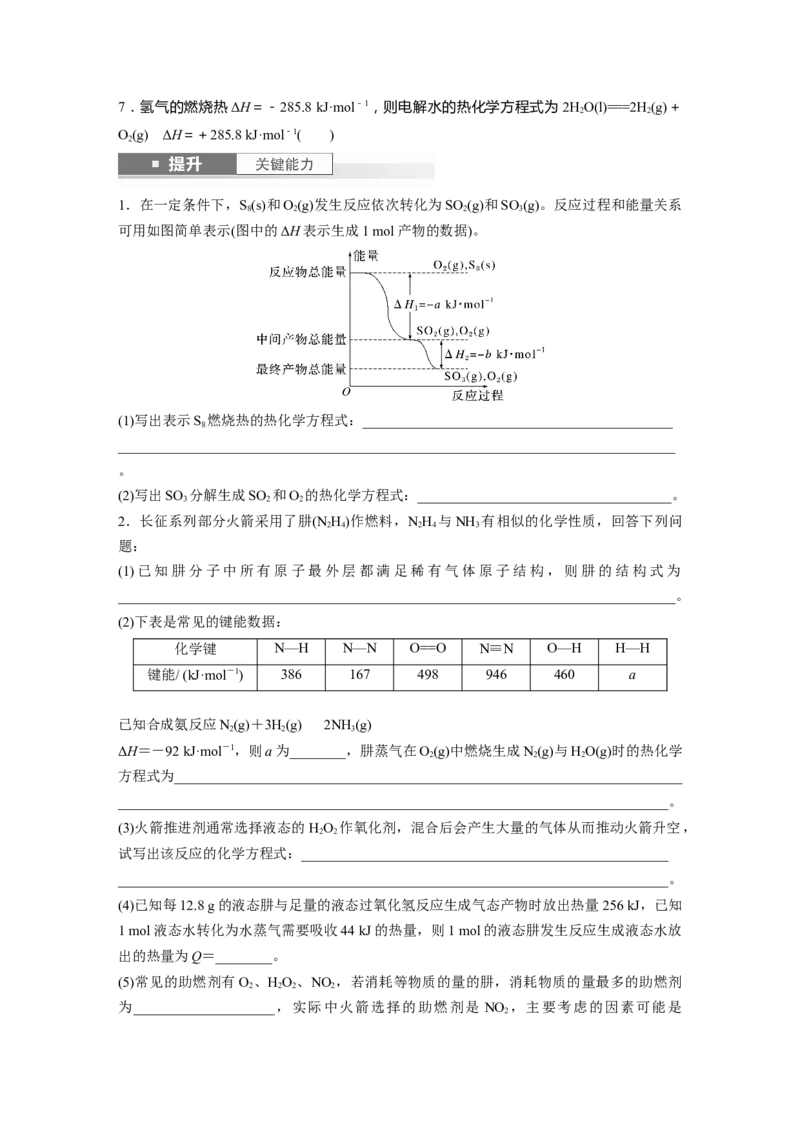
3.分析下列图像,按要求书写热化学方程式。
(1)图甲表示的是NO (g)和CO(g)反应生成CO(g)和NO(g)的过程中能量变化示意图,请写出
2 2
NO (g)和CO(g)反应的热化学方程式:_____________________________________________
2
______________________________________________________________________________。
(2)我国科学家研究化合物M(s)催化CO 氢化生成甲酸的机理,其中由化合物M(s)生成化合
2物N(s)的反应过程和相对能量曲线如图乙所示,TS1、TS2均为过渡态(已知:1 eV=96 kJ·mol
-1)。写出该反应的热化学方程式:_________________________________________________。
(3)图丙表示一定条件下,在水溶液中1 mol Cl-、ClO(x=1、2、3、4)的能量相对大小,
①D是____________(填离子符号)。
②B→A+C反应的热化学方程式为_______________________________________________
________________________________________________________________________(用离子
符号表示)。
考点三 燃烧热 能源
1.燃烧热
(1)概念:在101 kPa时,____ mol纯物质____________生成指定产物时所放出的热量。
(2)意义:衡量燃料燃烧时放出热量的多少。
(3)熟记常见元素完全燃烧生成的指定物质
元素 C H S N
指定产物及状态 CO(g) HO(l) SO (g) N(g)
2 2 2 2
2.燃料的选择、能源
(1)燃料选择的原则要综合考虑
①环境保护;②热值大小;③其他因素,如来源、价格、运输、稳定性等。
(2)能源分类及利用
1.开发利用各种新能源,减少对化石燃料的依赖,可以降低空气中PM 的含量( )
2.5
2.使用氢气作燃料有助于控制温室效应( )
3.101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热( )
4.煤、石油、天然气等燃料的最初来源都可追溯到太阳能( )
5.燃料燃烧阶段,可通过改进锅炉的炉型、燃料空气比等提高燃料的燃烧效率( )
6.空气燃料比越大,燃料燃烧越充分,则燃烧效率一定越高( )7.氢气的燃烧热ΔH=-285.8 kJ·mol-1,则电解水的热化学方程式为2HO(l)===2H(g)+
2 2
O(g) ΔH=+285.8 kJ·mol-1( )
2
1.在一定条件下,S(s)和O(g)发生反应依次转化为SO (g)和SO (g)。反应过程和能量关系
8 2 2 3
可用如图简单表示(图中的ΔH表示生成1 mol产物的数据)。
(1)写出表示S 燃烧热的热化学方程式:____________________________________________
8
_______________________________________________________________________________
。
(2)写出SO 分解生成SO 和O 的热化学方程式:____________________________________。
3 2 2
2.长征系列部分火箭采用了肼(N H)作燃料,NH 与NH 有相似的化学性质,回答下列问
2 4 2 4 3
题:
(1)已知肼分子中所有原子最外层都满足稀有气体原子结构,则肼的结构式为
_______________________________________________________________________________。
(2)下表是常见的键能数据:
化学键 N—H N—N O==O N≡N O—H H—H
键能/ (kJ·mol-1) 386 167 498 946 460 a
已知合成氨反应N(g)+3H(g)2NH (g)
2 2 3
ΔH=-92 kJ·mol-1,则a为________,肼蒸气在O(g)中燃烧生成N(g)与HO(g)时的热化学
2 2 2
方程式为________________________________________________________________________
______________________________________________________________________________。
(3)火箭推进剂通常选择液态的HO 作氧化剂,混合后会产生大量的气体从而推动火箭升空,
2 2
试写出该反应的化学方程式:____________________________________________________
______________________________________________________________________________。
(4)已知每12.8 g的液态肼与足量的液态过氧化氢反应生成气态产物时放出热量256 kJ,已知
1 mol液态水转化为水蒸气需要吸收44 kJ的热量,则1 mol的液态肼发生反应生成液态水放
出的热量为Q=________。
(5)常见的助燃剂有O 、HO 、NO ,若消耗等物质的量的肼,消耗物质的量最多的助燃剂
2 2 2 2
为____________________,实际中火箭选择的助燃剂是 NO ,主要考虑的因素可能是
2________________________________________________________________________。
1.(2023·湖北,1)2023年5月10日,天舟六号货运飞船成功发射,标志着我国航天事业进
入到高质量发展新阶段。下列不能作为火箭推进剂的是( )
A.液氮-液氢 B.液氧-液氢
C.液态NO -肼 D.液氧-煤油
2
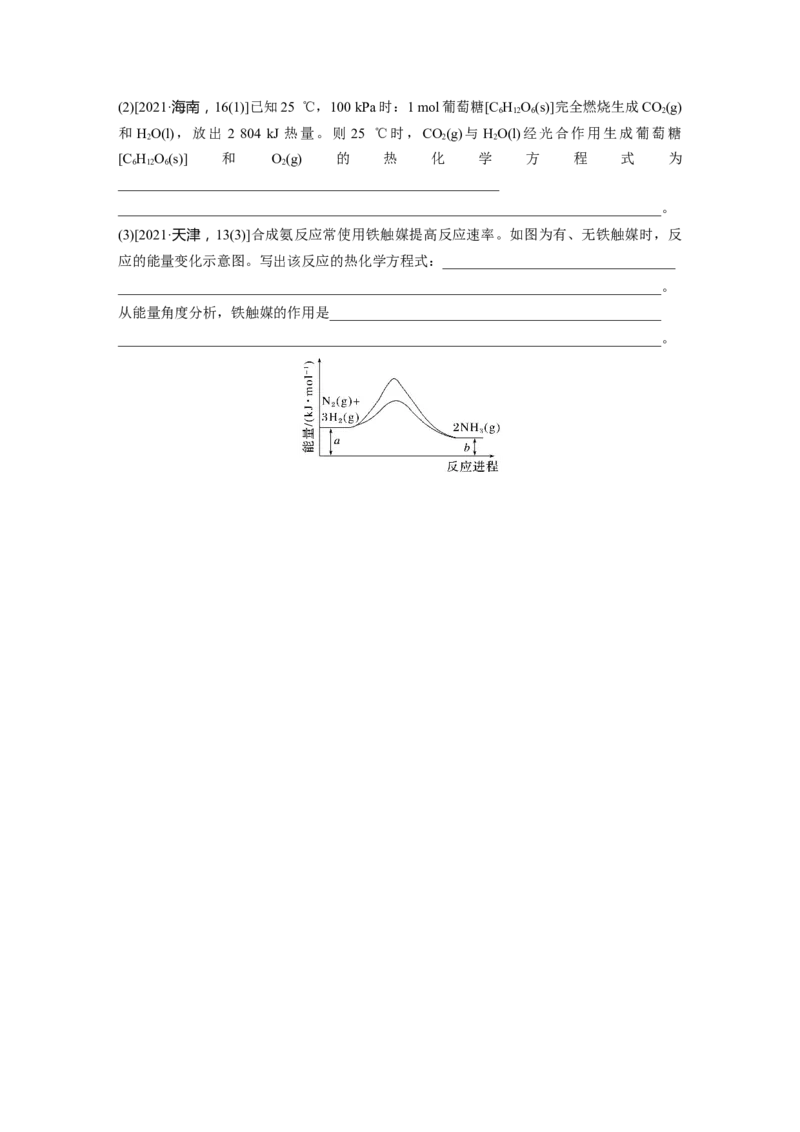
2.[2023·北京,16(2)]二十世纪初,工业上以CO 和NH 为原料在一定温度和压强下合成尿
2 3
素。反应分两步:
ⅰ.CO 和NH 生成NH COONH;
2 3 2 4
ⅱ.NHCOONH 分解生成尿素。
2 4
结合反应过程中能量变化示意图,下列说法正确的是____________(填序号)。
a.活化能:反应ⅰ<反应ⅱ
b.ⅰ为放热反应,ⅱ为吸热反应
c.CO(l)+2NH (l)===CO(NH)(l)+HO(l) ΔH=E-E
2 3 2 2 2 1 4
3.(2022·浙江6月选考,18)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H O HO HO
2 2 2 2 2
能量/ (kJ·mol-1) 249 218 39 10 0 0 -136 -242
可根据HO(g)+HO(g)===HO(g)计算出HO 中氧氧单键的键能为214 kJ·mol-1。下列说法
2 2 2 2
不正确的是( )
A.H 的键能为436 kJ·mol-1
2
B.O 的键能大于HO 中氧氧单键的键能的两倍
2 2 2
C.解离氧氧单键所需能量:HOO