文档内容
“学情空间”区域教研共同体高三入学检测
化学试题
可能用到的相对原子质量:
一、选择题:本题共10个小题,每小题2分,每个小题只有一个选项符合题目要求。
1. 化学与生产、生活、社会密切相关。下列有关说法中正确的是( )
A. 服用铬含量超标的药用胶囊会对人体健康造成危害
B. 酒精可以使蛋白质变性,酒精纯度越高杀菌消毒效果越好
C. 食品袋中放置的CaO可直接防止食品氧化变质
D. “酸雨”是由大气中的碳、氮、硫的氧化物溶于雨水造成的
【答案】A
【解析】
【详解】A、铬为重金属元素,摄入过多导致重金属中毒,A正确;
B、酒精可以使蛋白质变性,杀菌消毒效果最佳的浓度为75%,并不是越高越好,B错误;
C、CaO作为干燥剂,不能防止食品氧化变质,C错误;
D、“酸雨”是由大气中的氮、硫的氧化物溶于雨水造成的,D错误;
故选A。
2. 下图是某84消毒液(有效成分为次氯酸钠)标签的部分内容。下列说法正确的是
84消毒液
[性状]本品为无色透明液体
[规格]250 mL、252.50 g
[含量]氯含量为5.00%
[贮藏]密封保存
A. 密封保存的目的是防止 分解
B. 该84消毒液中含 的质量为
C. 该84消毒液的密度为
D. 该84消毒液中含氯微粒的物质的量浓度约为
下载最新免费模拟卷,到公众号:一枚试卷君【答案】D
【解析】
【分析】
【详解】A.密封保存的目的是防止NaClO水解生成的HClO分解,故A错误;
B.该84消毒液中含NaClO的质量=252.50g×次氯酸钠的质量分数,252.50g是次氯酸钠溶液的质量,故B
错误;
C.该84消毒液的密度= =1.01gcm−3,故C错误;
⋅
D.该84消毒液中含氯的物质的量浓度= =1.42molL−1,故D正确;
⋅
故选:D。
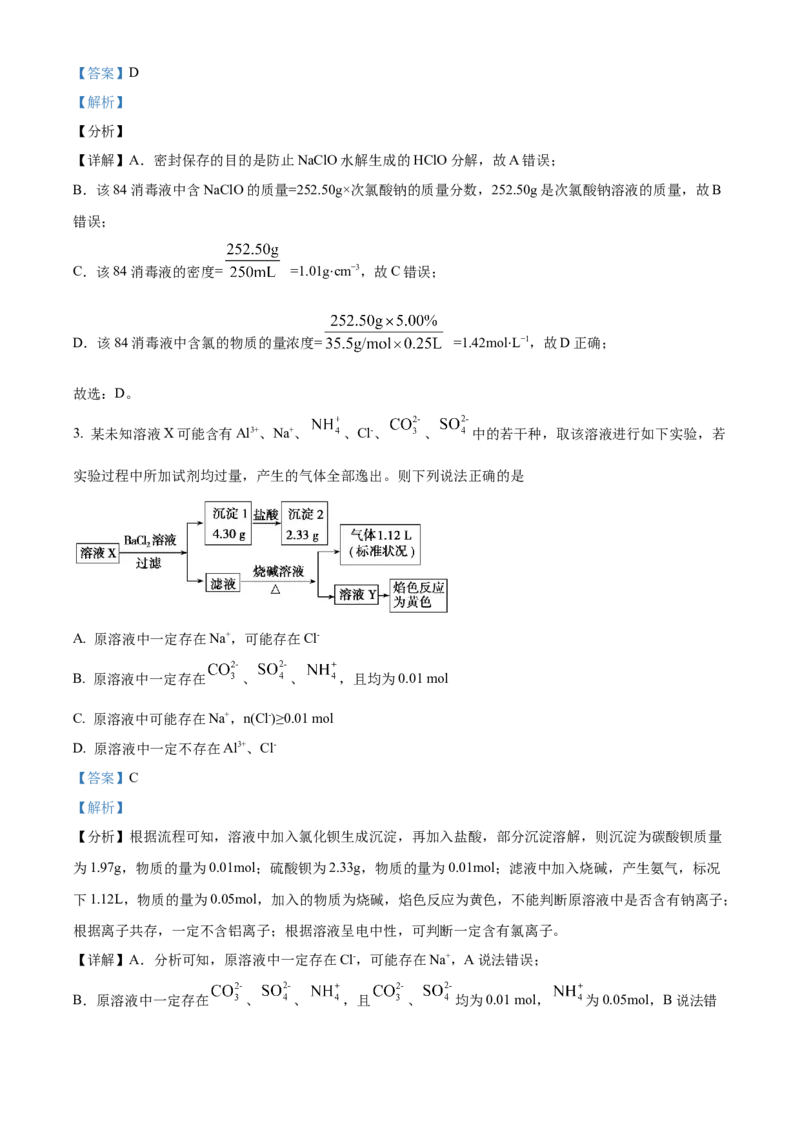
3. 某未知溶液X可能含有Al3+、Na+、 、Cl-、 、 中的若干种,取该溶液进行如下实验,若
实验过程中所加试剂均过量,产生的气体全部逸出。则下列说法正确的是
A. 原溶液中一定存在Na+,可能存在Cl-
B. 原溶液中一定存在 、 、 ,且均为0.01 mol
C. 原溶液中可能存在Na+,n(Cl-)≥0.01 mol
D. 原溶液中一定不存在Al3+、Cl-
【答案】C
【解析】
【分析】根据流程可知,溶液中加入氯化钡生成沉淀,再加入盐酸,部分沉淀溶解,则沉淀为碳酸钡质量
为1.97g,物质的量为0.01mol;硫酸钡为2.33g,物质的量为0.01mol;滤液中加入烧碱,产生氨气,标况
下1.12L,物质的量为0.05mol,加入的物质为烧碱,焰色反应为黄色,不能判断原溶液中是否含有钠离子;
根据离子共存,一定不含铝离子;根据溶液呈电中性,可判断一定含有氯离子。
【详解】A.分析可知,原溶液中一定存在Cl-,可能存在Na+,A说法错误;
B.原溶液中一定存在 、 、 ,且 、 均为0.01 mol, 为0.05mol,B说法错误;
C.根据溶液呈电中性,不含Na+时,n(Cl-)=0.01mol,若存在Na+,n(Cl-)≥0.01 mol,C说法正确;
D.原溶液中一定不存在Al3+,存在Cl-,D说法错误;
答案为C。
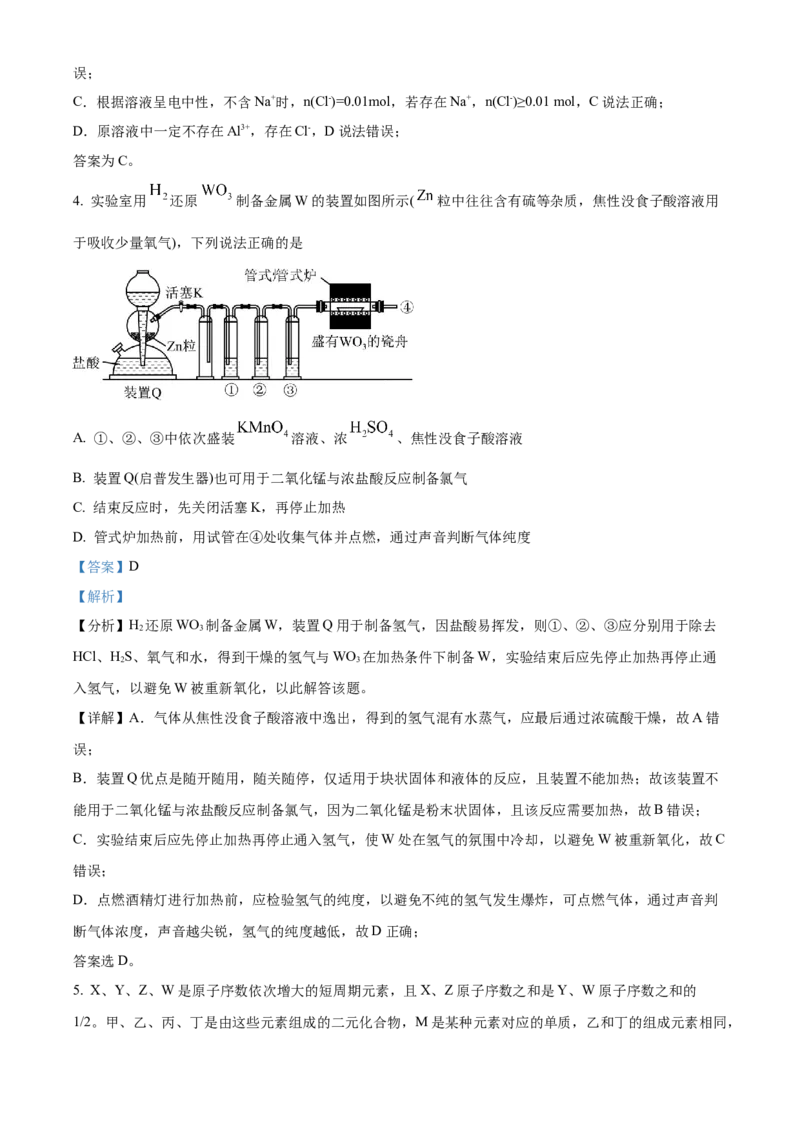
4. 实验室用 还原 制备金属W的装置如图所示( 粒中往往含有硫等杂质,焦性没食子酸溶液用
于吸收少量氧气),下列说法正确的是
A. ①、②、③中依次盛装 溶液、浓 、焦性没食子酸溶液
B. 装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
C. 结束反应时,先关闭活塞K,再停止加热
D. 管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度
【答案】D
【解析】
【分析】H 还原WO 制备金属W,装置Q用于制备氢气,因盐酸易挥发,则①、②、③应分别用于除去
2 3
HCl、HS、氧气和水,得到干燥的氢气与WO 在加热条件下制备W,实验结束后应先停止加热再停止通
2 3
入氢气,以避免W被重新氧化,以此解答该题。
【详解】A.气体从焦性没食子酸溶液中逸出,得到的氢气混有水蒸气,应最后通过浓硫酸干燥,故A错
误;
B.装置Q优点是随开随用,随关随停,仅适用于块状固体和液体的反应,且装置不能加热;故该装置不
能用于二氧化锰与浓盐酸反应制备氯气,因为二氧化锰是粉末状固体,且该反应需要加热,故B错误;
C.实验结束后应先停止加热再停止通入氢气,使W处在氢气的氛围中冷却,以避免W被重新氧化,故C
错误;
D.点燃酒精灯进行加热前,应检验氢气的纯度,以避免不纯的氢气发生爆炸,可点燃气体,通过声音判
断气体浓度,声音越尖锐,氢气的纯度越低,故D正确;
答案选D。
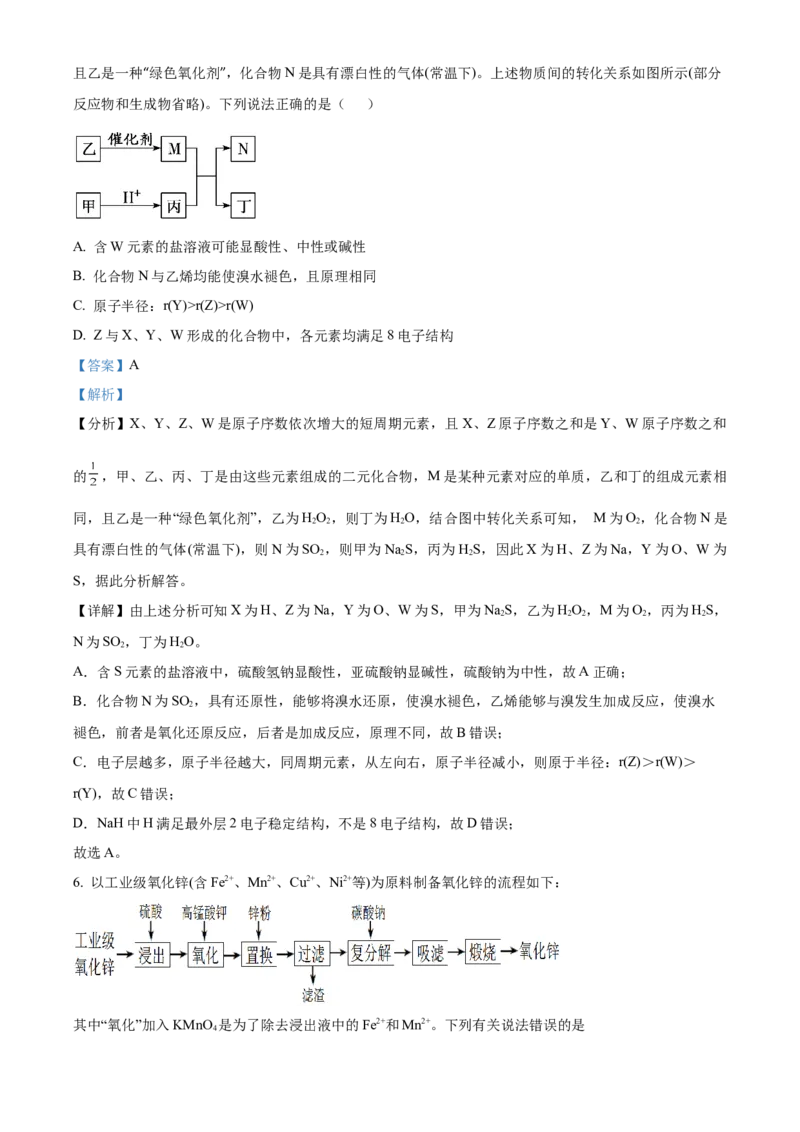
5. X、Y、Z、W是原子序数依次增大的短周期元素,且X、Z原子序数之和是Y、W原子序数之和的
1/2。甲、乙、丙、丁是由这些元素组成的二元化合物,M是某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下)。上述物质间的转化关系如图所示(部分
反应物和生成物省略)。下列说法正确的是( )
A. 含W元素的盐溶液可能显酸性、中性或碱性
B. 化合物N与乙烯均能使溴水褪色,且原理相同
C. 原子半径:r(Y)>r(Z)>r(W)
D. Z与X、Y、W形成的化合物中,各元素均满足8电子结构
【答案】A
【解析】
【分析】X、Y、Z、W是原子序数依次增大的短周期元素,且X、Z原子序数之和是Y、W原子序数之和
的 ,甲、乙、丙、丁是由这些元素组成的二元化合物,M是某种元素对应的单质,乙和丁的组成元素相
同,且乙是一种“绿色氧化剂”,乙为HO ,则丁为HO,结合图中转化关系可知, M为O ,化合物N是
2 2 2 2
具有漂白性的气体(常温下),则N为SO ,则甲为NaS,丙为HS,因此X为H、Z为Na,Y为O、W为
2 2 2
S,据此分析解答。
【详解】由上述分析可知X为H、Z为Na,Y为O、W为S,甲为NaS,乙为HO,M为O,丙为HS,
2 2 2 2 2
N为SO ,丁为HO。
2 2
A.含S元素的盐溶液中,硫酸氢钠显酸性,亚硫酸钠显碱性,硫酸钠为中性,故A正确;
B.化合物N为SO ,具有还原性,能够将溴水还原,使溴水褪色,乙烯能够与溴发生加成反应,使溴水
2
褪色,前者是氧化还原反应,后者是加成反应,原理不同,故B错误;
C.电子层越多,原子半径越大,同周期元素,从左向右,原子半径减小,则原于半径:r(Z)>r(W)>
r(Y),故C错误;
D.NaH中H满足最外层2电子稳定结构,不是8电子结构,故D错误;
故选A。
6. 以工业级氧化锌(含Fe2+、Mn2+、Cu2+、Ni2+等)为原料制备氧化锌的流程如下:
其中“氧化”加入KMnO 是为了除去浸出液中的Fe2+和Mn2+。下列有关说法错误的是
4A. 浸出时通过粉碎氧化锌提高了浸出率
B. “氧化”生成的固体是MnO 和Fe(OH)
2 3
C. “置换”加入锌粉是为了除去溶液中的Cu2+、Ni2+等
D. “煅烧”操作用到的仪器:玻璃棒、蒸发皿、泥三角
【答案】D
【解析】
【详解】A.浸出时通过粉碎固体氧化锌,使物质颗粒变小,扩大了与硫酸的接触面积,反应速率加快,因
而也可以提高了浸出率,A正确;
B.向硫酸浸取工业级ZnO后的溶液中存在Fe2+、Mn2+、Zn2+和Ni2+,加入KMnO 溶液,Ni2+不能被氧化,
4
Fe2+、Mn2+被氧化而形成MnO 和Fe(OH) 除去,KMnO 被还原形成MnO ,B正确;
2 3 4 2
C.由于金属活动性Zn>Ni>Cu,所以“置换”加入锌粉可以与溶液中的是为了与溶液中Ni2+、Cu2+发生主反应,
除去溶液中的Cu2+、Ni2+等,C正确;
D. “煅烧”操作用到的仪器:玻璃棒、坩埚、泥三角,D错误;
故合理选项是D。
的
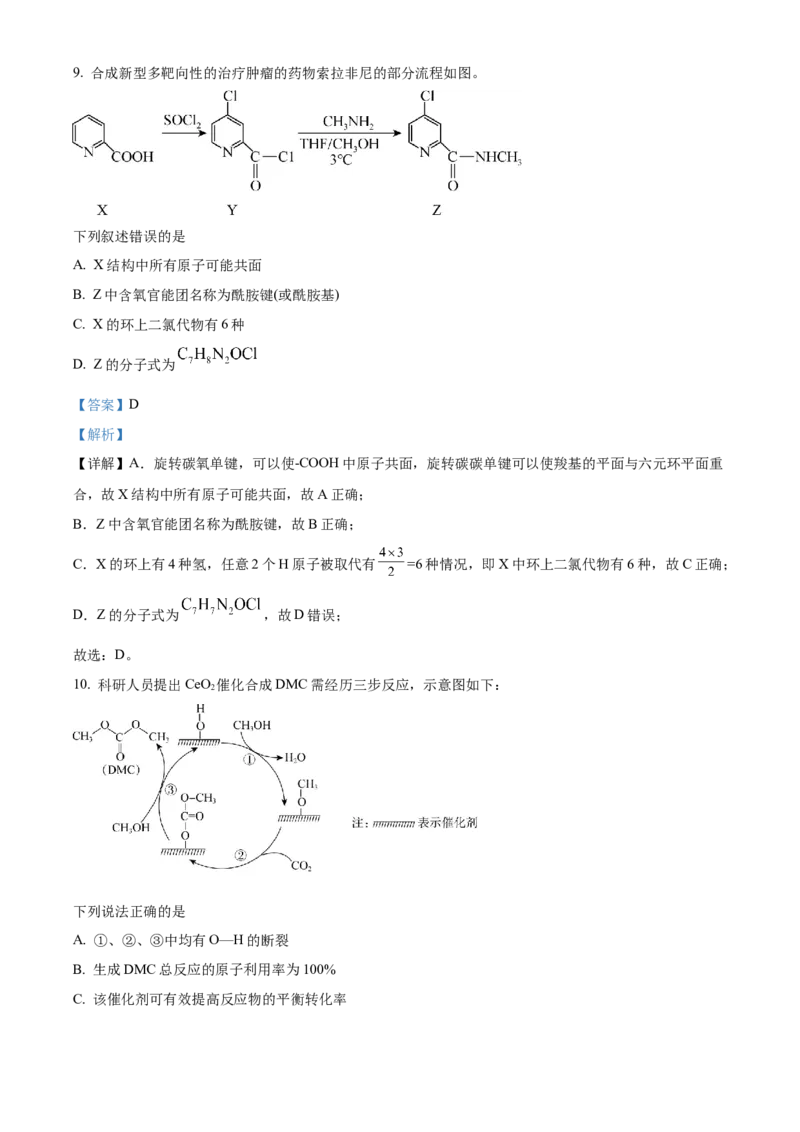
7. 探究 与水 反应,实验如图:(已知: 、 ),下列分析正
确的是
A. ①④中均发生了氧化还原反应和复分解反应
B. ①⑤中 均发生化学变化
C. ②⑤中 与 的作用不同,产生气体的量相同
D. 通过③能比较酸性:
【答案】A【解析】
【详解】A.①中发生反应 ,④中发生反应
、 ,均发生了氧化还原反应和复分解反应,故A
正确;
B.⑤发生反应 ,⑤中HO没发生化学变化,故B错误;
2
C.②中 是反应物,做氧化剂,HO 只做还原剂,1mol双氧水生成1mol氧气;⑤中 做催
2 2
化剂,HO 既做氧化剂又做还原剂,1mol双氧水生成0.5mol氧气,故C错误;
2 2
D.③发生反应 ,不能证明酸性 ,故D错误;
选A。
8. 取x g铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生8960mL的 气体和672mL的
气体(都已折算到标准状况),在反应后的溶液中加入足量的氢氧化钠溶液,生成沉淀的质量为
17.02g。则x等于
A. 8.64 B. 9.00 C. 9.20 D. 9.44
【答案】C
【解析】
【分析】铜和镁失去 的电子的物质的量,等于硝酸被还原为二氧化氮、四氧化二氮获得的电子的物质的量,
等于它们的离子反应生成氢氧化物沉淀结合的氢氧根的物质的量,根据氮的氧化物计算氢氧根的物质的量,
沉淀的总质量减去氢氧根的质量即为金属的质量,据此分析计算。
【详解】8.960L的NO 气体的物质的量为 =0.4mol,0.672L的NO 气体的物质的量
2 2 4
为 =0.03mol,所以金属提供的电子的物质的量为0.4mol×(5-4)+0.03mol×2×(5-
4)=0.46mol,所以沉淀中含有氢氧根的物质的量为0.46mol,氢氧根的质量为0.46mol×17g/mol=7.82g,所
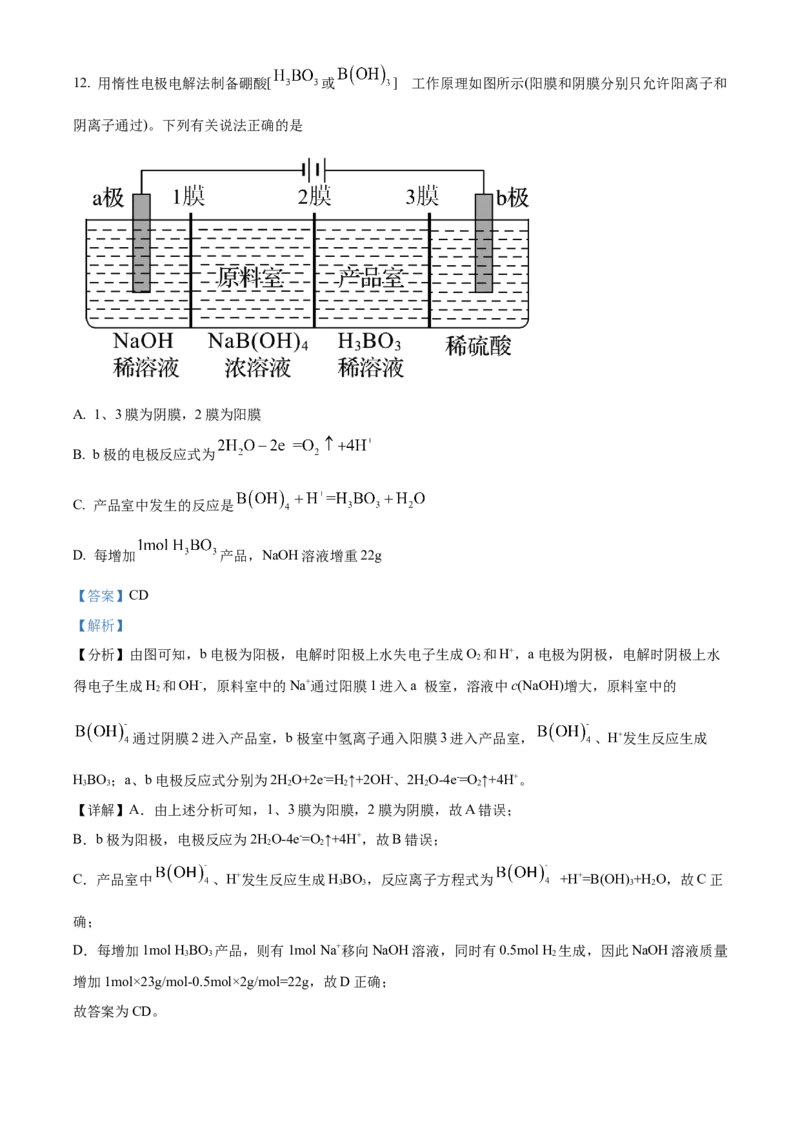
以金属的质量为17.02g-7.82g=9.2g,故选C。9. 合成新型多靶向性的治疗肿瘤的药物索拉非尼的部分流程如图。
下列叙述错误的是
A. X结构中所有原子可能共面
B. Z中含氧官能团名称为酰胺键(或酰胺基)
C. X的环上二氯代物有6种
D. Z的分子式为
【答案】D
【解析】
【详解】A.旋转碳氧单键,可以使-COOH中原子共面,旋转碳碳单键可以使羧基的平面与六元环平面重
合,故X结构中所有原子可能共面,故A正确;
B.Z中含氧官能团名称为酰胺键,故B正确;
C.X的环上有4种氢,任意2个H原子被取代有 =6种情况,即X中环上二氯代物有6种,故C正确;
D.Z的分子式为 ,故D错误;
故选:D。
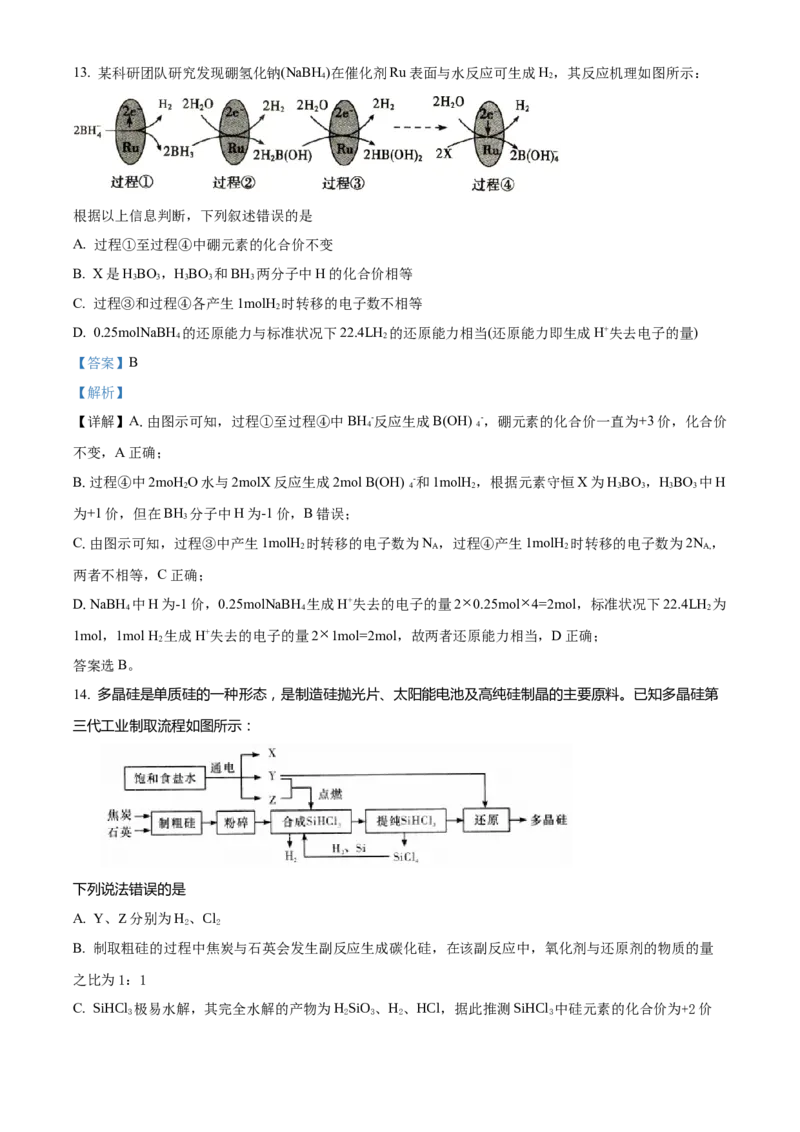
10. 科研人员提出CeO 催化合成DMC需经历三步反应,示意图如下:
2
下列说法正确的是
A. ①、②、③中均有O—H的断裂
B. 生成DMC总反应的原子利用率为100%
C. 该催化剂可有效提高反应物的平衡转化率D. DMC与过量NaOH溶液反应生成 和甲醇
【答案】D
【解析】
【详解】A.根据示意图可知①、②、③中①、③有O—H的断裂,A错误;
B.①中有水分子生成,生成DMC总反应的原子利用率小于100%,B错误;
C.催化剂的使用不影响化学反应平衡,不能提高反应物的平衡转化率,C错误;
D. DMC的结构中有酯基,能与过量NaOH溶液发生水解反应生成 和甲醇,D正确;
答案选D。
二、选择题:本题共5个小题,每小题4分,共20分。每个小题只有一个或两个选项符合题
目要求,全部选对得4分,选对但不全的得2分,有选错的得0分。
11. 在同一温度下,在3个容积均为1.0 L的恒容密闭容器中发生反应:PCl (g) PCl (g)+Cl (g)。下列说
5 3 2
法错误的是
物质的起始浓度/(mol/L) 物质的平衡浓度/(mol/L)
容器编号
c(PCl ) c(PCl ) c(Cl ) c(Cl )
5 3 2 2
I 0.4 0 0 0.2
II 0.6 0 0.2
III 0.8 0 0
A. 反应达到平衡时,容器I中 比容器II中的大
B. 反应达到平衡时,容器I与容器II中的总压强之比为3∶4
C. 反应达到平衡时,容器III中Cl 的体积分数小于
2
D. 反应达到平衡时,容器III中0.4 mol/L<c(PCl )<0.8 mol/L
5
【答案】AB
【解析】
【详解】A.容器编号I中发生反应PCl (g) PCl (g)+Cl (g),起始浓度c(PCl )=0.4 mol/L,
5 3 2 5c(PCl )=c(Cl )=0,当反应达到平衡时c(Cl )=0.2 mol/L,根据物质反应转化关系可知平衡时c(PCl )=0.2
3 2 2 3
mol/L,c(PCl )=0.4 mol/L-0.2 mol/L=0.2 mol/L,此时 =1,该温度下化学平衡常数K=
5
;
对于容器II,反应正向进行,假设反应达到平衡时消耗c(PCl )=x mol/L,根据物质反应转化关系可知平衡
5
时c(PCl )=(0.6-x) mol/L,c(PCl )=x mol/L,c(Cl )=(0.2+x)mol/L,由于温度不变,化学平衡常数不变可知
5 3 2
K= ,解得x=0.2 mol/L,则平衡时c(PCl )=0.4 mol/L,c(Cl )=0.4
5 2
mol/L,此时 =1,可见反应达到平衡时,容器I中 比容器II的 小,A
错误;
B.根据选项A分析可知平衡时:对于容器I,c(PCl )=c(Cl )=c(PCl )=0.2 mol/L,由于容器的容积是1.0 L,
3 2 5
气体的物质的量与浓度数值相等;此时容器内气体的物质的量为n(总)=(0.2 mol/L+0.2 mol/L +0.2
mol/L)×1.0 L=0.6 mol;对于容器II平衡时c(PCl )=c(Cl )=0.4 mol/L,c(PCl )=0.2 mol/L,容器的容积是1.0
5 2 3
L,气体总物质的量n(总)=(0.4 mol/L+0.4 mol/L+0.2 mol/L)×1.0 L=1.0 mol,在恒温恒容时,气体的物质的
量与压强呈正比,则反应达到平衡时,容器I与容器II中的总压强之比为0.6 mol:1.0 mol=3:5,B错误;
C.根据选项A分析可知平衡时:对于容器I,c(PCl )=c(Cl )=c(PCl )=0.2 mol/L,平衡时Cl 的体积分数为:
3 2 5 2
;对于容器III,相当于对容器I反应增大压强,化学平衡向气体体
积减小的逆反应方向移动,Cl 的量减小,所以达平衡时,器III中Cl 的体积分数小于 ,C正确;
2 2
D.III中起始量为I中2倍,若平衡不移动,II中平衡时c(PCl )=0.4 mol/L,压强增大使化学平衡逆向移动,
5
生成物不可能完全转化为反应物,则平衡时,容器IIII中0.4 mol/L<c(PCl )<0.8 moI/L,D正确;
5
故合理选项是AB。12. 用惰性电极电解法制备硼酸[ 或 ] 工的作原理如图所示(阳膜和阴膜分别只允许阳离子和
阴离子通过)。下列有关说法正确的是
A. 1、3膜为阴膜,2膜为阳膜
B. b极的电极反应式为
C. 产品室中发生的反应是
D. 每增加 产品,NaOH溶液增重22g
【答案】CD
【解析】
【分析】由图可知,b电极为阳极,电解时阳极上水失电子生成O 和H+,a电极为阴极,电解时阴极上水
2
得电子生成H 和OH-,原料室中的Na+通过阳膜1进入a 极室,溶液中c(NaOH)增大,原料室中的
2
通过阴膜2进入产品室,b极室中氢离子通入阳膜3进入产品室, 、H+发生反应生成
HBO;a、b电极反应式分别为2HO+2e-=H ↑+2OH-、2HO-4e-=O ↑+4H+。
3 3 2 2 2 2
【详解】A.由上述分析可知,1、3膜为阳膜,2膜为阴膜,故A错误;
B.b极为阳极,电极反应为2HO-4e-=O ↑+4H+,故B错误;
2 2
C.产品室中 、H+发生反应生成HBO,反应离子方程式为 +H+=B(OH) +H O,故C正
3 3 3 2
确;
D.每增加1mol HBO 产品,则有1mol Na+移向NaOH溶液,同时有0.5mol H 生成,因此NaOH溶液质量
3 3 2
增加1mol×23g/mol-0.5mol×2g/mol=22g,故D正确;
故答案为CD。13. 某科研团队研究发现硼氢化钠(NaBH )在催化剂Ru表面与水反应可生成H,其反应机理如图所示:
4 2
根据以上信息判断,下列叙述错误的是
A. 过程①至过程④中硼元素的化合价不变
B. X是HBO,HBO 和BH 两分子中H的化合价相等
3 3 3 3 3
C. 过程③和过程④各产生1molH 时转移的电子数不相等
2
D. 0.25molNaBH 的还原能力与标准状况下22.4LH 的还原能力相当(还原能力即生成H+失去电子的量)
4 2
【答案】B
【解析】
【详解】A.由图示可知,过程①至过程④中BH-反应生成B(OH) -,硼元素的化合价一直为+3价,化合价
4 4
不变,A正确;
B.过程④中2moH O水与2molX反应生成2mol B(OH) -和1molH ,根据元素守恒X为HBO,HBO 中H
2 4 2 3 3 3 3
为+1价,但在BH 分子中H为-1价,B错误;
3
C.由图示可知,过程③中产生1molH 时转移的电子数为N ,过程④产生1molH 时转移的电子数为2N ,
2 A 2 A,
两者不相等,C正确;
D.NaBH 中H为-1价,0.25molNaBH 生成H+失去的电子的量2 0.25mol 4=2mol,标准状况下22.4LH 为
4 4 2
1mol,1mol H 生成H+失去的电子的量2 1mol=2mol,故两者还原能力相当,D正确;
2
答案选B。
14. 多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电池及高纯硅制晶的主要原料。已知多晶硅第
三代工业制取流程如图所示:
下列说法错误的是
A. Y、Z分别为H、Cl
2 2
B. 制取粗硅的过程中焦炭与石英会发生副反应生成碳化硅,在该副反应中,氧化剂与还原剂的物质的量
之比为1:1
C. SiHCl 极易水解,其完全水解的产物为HSiO、H、HCl,据此推测SiHCl 中硅元素的化合价为+2价
3 2 3 2 3D. Y与SiHCl 制备多晶硅的反应属于置换反应
3
【答案】B
【解析】
【详解】A. 电解饱和食盐水生成氢氧化钠、氢气和氯气,Y和Z点燃化合,其中Y还能与将硅从其化合物
中还原出来,这说明Y、Z分别为H、Cl,A正确;B. 制取粗硅的过程中焦炭与石英会发生副反应生成碳
2 2
化硅:3C+SiO SiC+2CO↑,在该副反应中碳既是氧化剂,也是还原剂,氧化剂与还原剂的物质的
2
量之比为1:2,B错误;C. SiHCl 中H是+1价,Cl是-1价,则硅元素的化合价为+2价,C正确;D. 氢
3
气与SiHCl 制备多晶硅的反应:SiHCl +H =Si+3HCl,属于置换反应,D正确,答案选B。
3 3 2
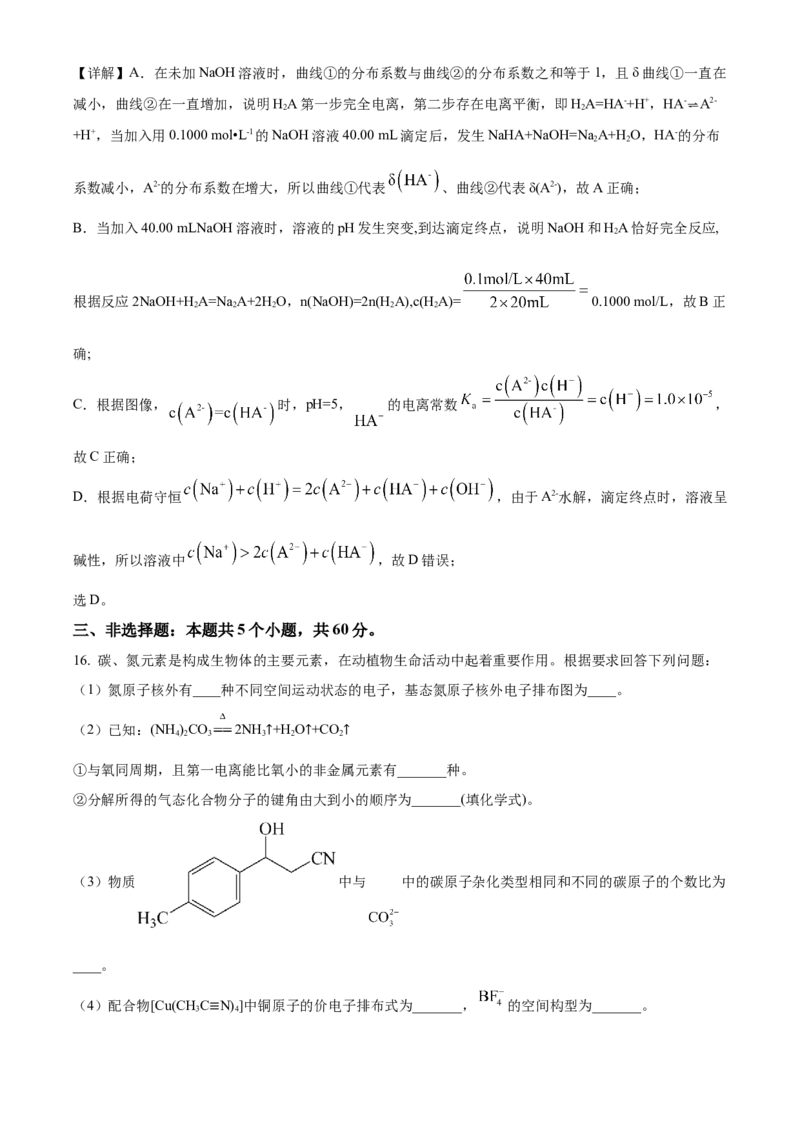
15. 以酚酞为指示剂,用 的NaOH溶液滴定20.00mL未知浓度的二元酸 溶液。溶液中,
pH、分布系数δ随滴加NaOH溶液体积 的变化关系如图所示。[比如 的分布系数:
]。下列叙述不正确的是
A. 曲线①代表 ,曲线②代表
B. 溶液的浓度为
C. 的电离常数
D. 滴定终点时,溶液中
【答案】D
【解析】【详解】A.在未加NaOH溶液时,曲线①的分布系数与曲线②的分布系数之和等于1,且δ曲线①一直在
减小,曲线②在一直增加,说明H
2
A第一步完全电离,第二步存在电离平衡,即H
2
A=HA-+H+,HA- ⇌A2-
+H+,当加入用0.1000 mol•L-1的NaOH溶液40.00 mL滴定后,发生NaHA+NaOH=Na A+HO,HA-的分布
2 2
系数减小,A2-的分布系数在增大,所以曲线①代表 、曲线②代表δ(A2-),故A正确;
B.当加入40.00 mLNaOH溶液时,溶液的pH发生突变,到达滴定终点,说明NaOH和HA恰好完全反应,
2
根据反应2NaOH+H A=Na A+2HO,n(NaOH)=2n(H A),c(HA)= 0.1000 mol/L,故B正
2 2 2 2 2
确;
C.根据图像, 时,pH=5, 的电离常数 ,
故C正确;
D.根据电荷守恒 ,由于A2-水解,滴定终点时,溶液呈
碱性,所以溶液中 ,故D错误;
选D。
三、非选择题:本题共5个小题,共60分。
16. 碳、氮元素是构成生物体的主要元素,在动植物生命活动中起着重要作用。根据要求回答下列问题:
(1)氮原子核外有____种不同空间运动状态的电子,基态氮原子核外电子排布图为____。
(2)已知:(NH )CO 2NH +H O +CO
4 2 3 3 2 2
↑ ↑ ↑
①与氧同周期,且第一电离能比氧小的非金属元素有_______种。
②分解所得的气态化合物分子的键角由大到小的顺序为_______(填化学式)。
(3)物质 中与 中的碳原子杂化类型相同和不同的碳原子的个数比为
____。
(4)配合物[Cu(CHC N) ]中铜原子的价电子排布式为_______, 的空间构型为_______。
3 4
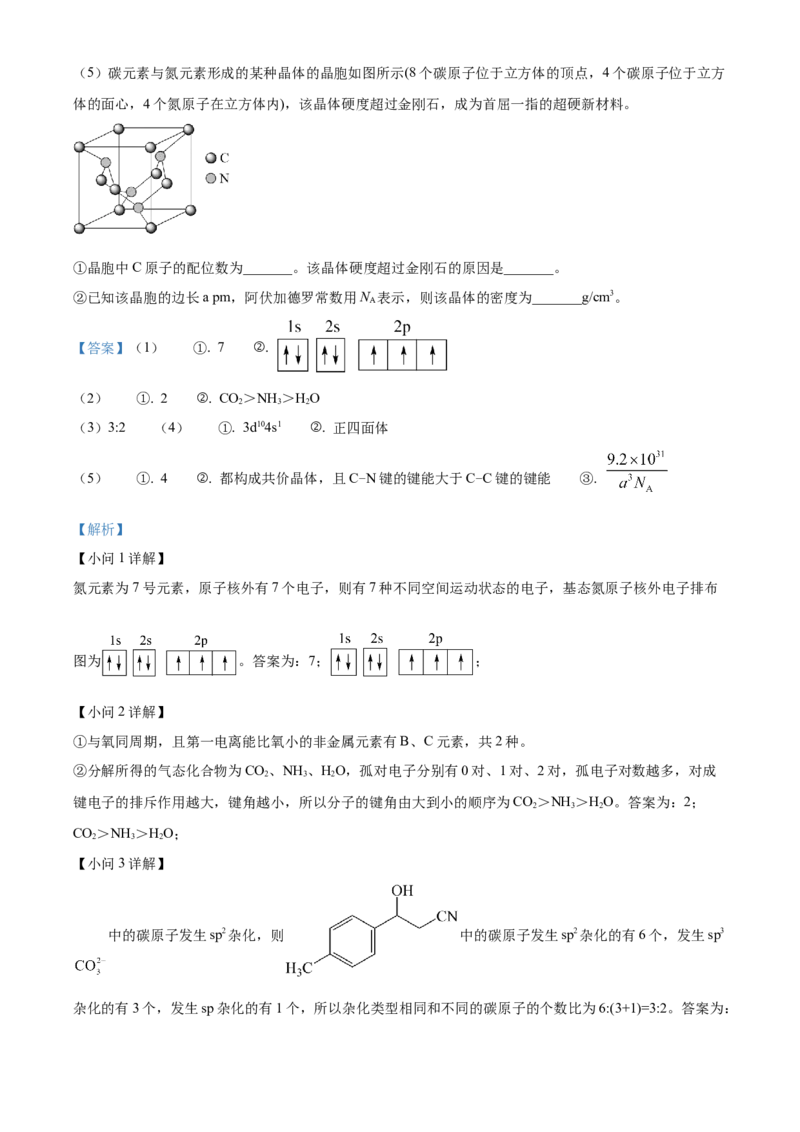
≡(5)碳元素与氮元素形成的某种晶体的晶胞如图所示(8个碳原子位于立方体的顶点,4个碳原子位于立方
体的面心,4个氮原子在立方体内),该晶体硬度超过金刚石,成为首屈一指的超硬新材料。
①晶胞中C原子的配位数为_______。该晶体硬度超过金刚石的原因是_______。
②已知该晶胞的边长a pm,阿伏加德罗常数用N 表示,则该晶体的密度为_______g/cm3。
A
【答案】(1) ①. 7 ②.
(2) ①. 2 ②. CO>NH >HO
2 3 2
(3)3:2 (4) ①. 3d104s1 ②. 正四面体
(5) ①. 4 ②. 都构成共价晶体,且C-N键的键能大于C-C键的键能 ③.
【解析】
【小问1详解】
氮元素为7号元素,原子核外有7个电子,则有7种不同空间运动状态的电子,基态氮原子核外电子排布
图为 。答案为:7; ;
【小问2详解】
①与氧同周期,且第一电离能比氧小的非金属元素有B、C元素,共2种。
②分解所得的气态化合物为CO、NH 、HO,孤对电子分别有0对、1对、2对,孤电子对数越多,对成
2 3 2
键电子的排斥作用越大,键角越小,所以分子的键角由大到小的顺序为CO>NH >HO。答案为:2;
2 3 2
CO>NH >HO;
2 3 2
【小问3详解】
中的碳原子发生sp2杂化,则 中的碳原子发生sp2杂化的有6个,发生sp3
杂化的有3个,发生sp杂化的有1个,所以杂化类型相同和不同的碳原子的个数比为6:(3+1)=3:2。答案为:3:2;
【小问4详解】
配合物[Cu(CHC≡N) ]中的铜原子,没有得失电子,原子核外电子数仍为29个,所以价电子排布式为
3 4
3d104s1, 中,B原子的价层电子对数为4,空间构型为正四面体。答案为:3d104s1;正四面体;
【小问5详解】
①设定晶胞中右上角的碳原子为中心碳原子,它被8个晶胞共用,有4个晶胞中的N原子与该碳原子形成
共价键,所以晶胞中C原子的配位数为4。该晶体中,C-N键的键长比C-C键的键长短,所以硬度超过金
刚石,原因是:都构成共价晶体,且C-N键的键能大于C-C键的键能。
②在晶胞中,含有的C原子数为 =3,N原子数为4,则化学式为C N,边长a pm,阿伏加德
3 4
罗常数用N 表示,则该晶体的密度为 = g/cm3。答案为:4;都构成共价
A
晶体,且C-N键的键能大于C-C键的键能; 。
【点睛】计算晶胞中所含原子的数目时,可使用均摊法。
17. 亚氯酸钠 常用于纺织、造纸业漂白,也用于食品消毒、水处理等。
已知:①亚氯酸钠 受热易分解;
②纯 易分解爆炸,一般用稀有气体或空气稀释到10%以下。
I:制取 晶体(1)实验过程中需要持续通入空气,目的是_______。
(2)装置A中产生 的化学方程式为_______。
(3)装置B中还原剂和氧化剂的物质的量之比为_______,还原产物为_______;反应结束后,为从溶液
中得到 固体,采取减压蒸发而不用常压蒸发,原因是_______。
(4)装置C的作用是_______。
II:测定亚氯酸钠的含量
实验步骤:①准确称取所得亚氯酸钠样品m g于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入
适量的稀硫酸,充分反应,将所得混合液配成250mL待测溶液。②移取25.00mL待测溶液于锥形瓶中,加
几滴淀粉溶液,用 标准溶液滴定至终点,重复2次,测得消耗 标准溶液体积
的平均值为V mL。(已知: 、 )
(5)达到滴定终点时的现象为_______。
(6)该样品中 的质量分数为_______%(用含m、c、V的代数式表示)。在滴定操作正确的情况下,
此实验测得结果偏高,可能原因为_______(用离子方程式表示)。
【答案】(1)稀释ClO 以防爆炸
2
(2)2NaClO+NaSO +HSO =2ClO ↑+2NaSO +HO
3 2 3 2 4 2 2 4 2
(3) ①. 2∶1 ②. O ③. 常压蒸发温度过高,亚氯酸钠容易分解
2
(4)吸收ClO ,防止污染空气
2
(5)当滴入最后一滴标准溶液时,溶液由蓝色变成无色,且30 s内颜色不恢复
(6) ①. ②. 4I-+O+4H+=2I +2H O
2 2 2【解析】
【分析】A中75%硫酸与亚硫酸钠固体反应生成二氧化硫,二氧化硫与氯酸钠反应生成ClO ,B中ClO 在
2 2
碱性条件下与过氧化氢反应生成NaClO,C为尾气吸收装置,且可防止倒吸;
2
【小问1详解】
根据题给信息“纯ClO 易分解爆炸,一般用稀有气体或空气稀释到10%以下”,可知实验过程中持续通入空
2
气的目的是稀释ClO ,以防止发生爆炸;
2
【小问2详解】
装置A中NaClO 被还原为ClO ,NaSO 被氧化为NaSO ;根据得失电子守恒和元素守恒,可知装置A中
3 2 2 3 2 4
产生ClO 的化学方程式为2NaClO+NaSO +HSO ===2ClO ↑+2NaSO +HO;
2 3 2 3 2 4 2 2 4 2
【小问3详解】
装置B中ClO 参加反应生成NaClO,Cl元素的化合价降低,作氧化剂,HO 作还原剂,有氧气生成,根
2 2 2 2
据得失电子守恒可得关系式:2ClO ~HO,故装置B中氧化剂和还原剂的物质的量之比为2∶1,氧化产
2 2 2
物为O。根据题给信息“亚氯酸钠(NaClO)受热易分解”,可知反应结束后为从溶液中得到NaClO 固体,应
2 2 2
采取减压蒸发而不用常压蒸发,原因是常压蒸发温度过高,亚氯酸钠容易分解;
【小问4详解】
装置C的作用是吸收ClO ,防止污染空气;
2
【小问5详解】
用NaSO 标准溶液滴定待测溶液,发生反应:I+2 =2I-+ ,指示剂淀粉溶液遇I 变为蓝色,
2 2 3 2 2
故滴定终点的现象为滴入最后一滴标准溶液时,溶液由蓝色变成无色,且30 s内颜色不恢复;
【小问6详解】
①由反应中的I元素守恒可知: ~2I~4 ,故25.00 mL待测溶液中n(NaClO)= ×cV×10-
2 2
3mol,m(NaClO )= ×90.5cV×10-3g;样品m g配成250 mL待测溶液,故样品中NaClO 的质量分数为
2 2
;
②实验测得结果偏高,说明滴定消耗的NaSO 标准溶液体积偏大,则溶液中碘单质的含量偏高,可能原
2 2 3
因为过量的碘离子被空气中的氧气氧化为碘单质,反应的离子方程式为4I-+O+4H+===2I +2HO。
2 2 218. 草酸钴可用于指示剂和催化剂的制备。用含钴废料(主要成分为Co,含有一定量的NiO、 、
Fe、 等),制备草酸钴晶体 的流程如下:
已知:①草酸钴晶体难溶于水;②RH为有机物(难电离)。回答下列问题:
(1)酸浸时钴溶解反应的化学方程式为_______,浸出液中加入 后发生反应的离子方程式为_______。
(2)加入氧化钴的目的是_______,滤渣II高温灼烧的产物主要有_______。
(3)操作①为_______(填操作名称)。
(4)已知: ;
;
。
该流程中所用 溶液的pH_______7(填“>”“<”或“=”)。
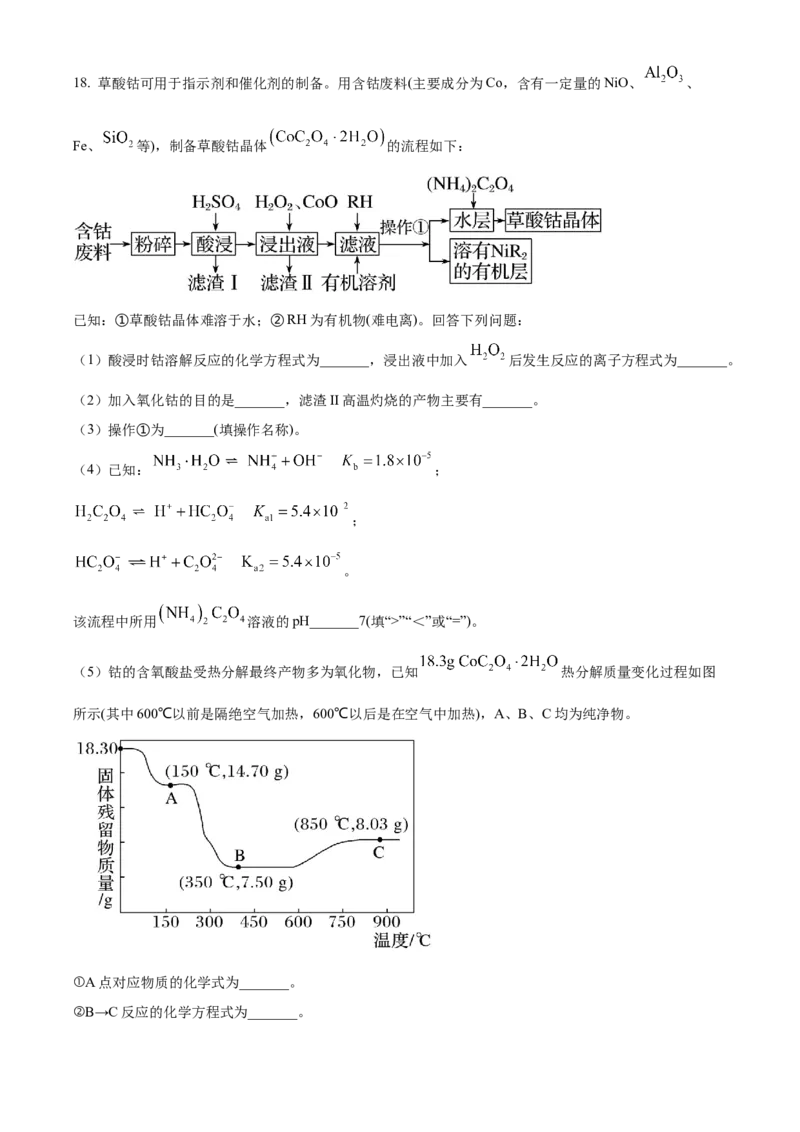
(5)钴的含氧酸盐受热分解最终产物多为氧化物,已知 热分解质量变化过程如图
所示(其中600℃以前是隔绝空气加热,600℃以后是在空气中加热),A、B、C均为纯净物。
①A点对应物质的化学式为_______。
②B→C反应的化学方程式为_______。【答案】(1) ①. Co+H OS =CoSO+H ↑ ②. 2Fe2++2H++H O=2Fe3++2H O
2 4 4 2 2 2 2
(2) ①. 调节溶液的pH,使Fe3+、Al3+分别转化为沉淀 ②. Al O、Fe O
2 3 2 3
(3)萃取分液 (4)<
(5) ①. CoC O ②.
2 4
【解析】
【分析】废料粉碎后加入稀硫酸酸浸,Co、NiO、Al O、Fe都和稀硫酸反应生成相应的盐,SiO 不溶于稀
2 3 2
硫酸,滤渣I为SiO,浸出液中加入双氧水和CoO,双氧水氧化Fe2+生成Fe3+,CoO和稀硫酸反应生成
2
CoSO 而增大溶液pH值,使Fe3+、Al3+分别转化为Fe(OH)、Al(OH) 沉淀,则滤渣II为Fe(OH)
4 3 3
,向滤液中加入RH,萃取后得到的水层中含有CoSO ,有机层中含有NiR ,向水层中加入草酸铵得到草
3 4 2
酸钴晶体;
【
小问1详解】
酸浸时Co和稀硫酸反应生成硫酸钴和氢气,反应方程式为Co+H OS =CoSO+H ↑;浸出液中加入HO,
2 4 4 2 2 2
双氧水具有氧化性,能氧化具有还原性的亚铁离子生成铁离子,离子方程式为2Fe2++2H++H O=2Fe3+
2 2
+2H O;
2
故答案为:Co+H OS =CoSO+H ↑;2Fe2++2H++H O=2Fe3++2H O;
2 4 4 2 2 2 2
【小问2详解】
CuO能和稀硫酸反应生成水而调节溶液的pH值,使Fe3+、Al3+分别转化为沉淀而除去杂质离子;滤渣的II
主要成分是Fe(OH)、Al(OH),高温灼烧Fe(OH)、Al(OH) 的产物为Al O、Fe O;
3 3 3 3 2 3 2 3
故答案为:调节溶液的pH,使Fe3+、Al3+分别转化为沉淀;Al O、Fe O;
2 3 2 3
【小问3详解】
分离互不相溶的液体采用分液方法,所以操作①为萃取分液;
故答案为:萃取分液;
【小问4详解】
; NH +水解程度大
4
于 -,NH +水解导致溶液呈酸性、 水解导致溶液呈碱性,所以该溶液呈酸性,溶液的pH<7;
4
故答案为:<;
【小问5详解】18.3gCoC O•2HO中n(CoC O•2HO) ,CoC O•2HO受热时如果完全失去HO
2 4 2 2 4 2 2 4 2 2
生成CoC O,m(CoC O)=0.1mol×147g/mol=14.7g,如果CoC O 分解生成CoO,根据Co原子守恒得n
2 4 2 4 2 4
(CoO)=n(CoC O)=0.1mol×75g/mol=7.5g,C点得到的固体中m(Co)=0.1mol×59g/mol=5.9g,m
2 4
(O)=(8.03-5.9)g=2.13g,n(Co):n(O)= ,所以其化学式为Co O;
3 4
①通过以上分析知,A点对应物质为CoC O;
2 4
②B点溶质为CoO、C点溶质为Co O,B→C反应的化学方程式为 ;
3 4
故答案为:CoC O; 。
2 4
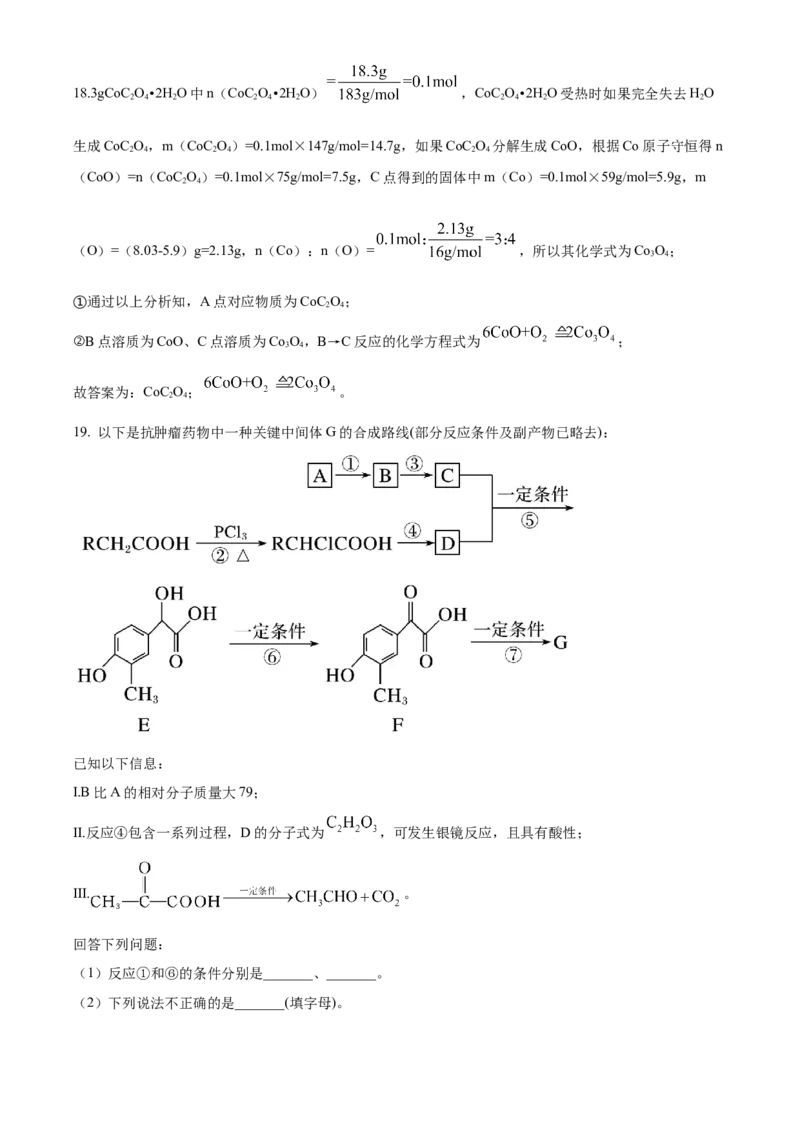
19. 以下是抗肿瘤药物中一种关键中间体G的合成路线(部分反应条件及副产物已略去):
已知以下信息:
I.B比A的相对分子质量大79;
II.反应④包含一系列过程,D的分子式为 ,可发生银镜反应,且具有酸性;
III. 。
回答下列问题:
(1)反应①和⑥的条件分别是_______、_______。
(2)下列说法不正确的是_______(填字母)。a.C物质能使三氯化铁溶液显紫色
b.D分子中含有的官能团有醛基、羧基和羟基
c.E能发生氧化、加成、取代、缩聚反应
d.1mol F最多可与 发生加成反应
(3)反应⑤的反应类型是_______。由C和D生成E的化学反应方程式:_______。
(4)G的结构简式为_____。既能发生银镜反应,又含苯环的G的同分异构体有_______种。
的
(5)由2分子E生成 含有3个六元环化合物中不同化学环境的氢原子共有_______种。
【答案】(1) ①. Br 、铁粉 ②. 铜、氧气、加热
2
(2)bd (3) ①. 加成反应 ②.
+
(4) ①. ②. 24
(5)6
【解析】
【分析】反应④包含一系列过程,D的分子式为C HO,可发生银镜反应,且具有酸性,则D为
2 2 3
OHCCOOH,根据D、E结构简式知,CD发生加成反应生成E,则C为 ,B比A的相对分
子质量大79,则B为 、A为 ,A需要和液溴在溴化铁作催化剂条件下发生取代反
应生成B,B发生水解反应生成C;E发生催化氧化生成F,F发生信息[3]的反应生成G为,结合题目分析解答。
【小问1详解】
反应①为甲苯和溴的取代反应,条件是Br 、铁粉,⑥为醇的催化氧化反应,条件是铜、氧气、加热,故
2
答案为:Br 、铁粉;铜、氧气、加热;
2
【小问2详解】
a.C为 ,属于酚类物质,属于C物质能使三氯化铁溶液显紫色,故正确;
b.D为OHCCOOH,D分子中含有羧基和醛基,故错误;
c.E中含有醇羟基、酚羟基、羧基,醇羟基和酚羟基能发生氧化反应,苯环能发生加成反应,羟基、羧基
能发生取代反应,羧基和醇羟基能发生缩聚反应,故正确;
d.F中苯环和羰基都能和氢气发生加成反应,但羧基不能和氢气发生加成反应,则1molF最多可与
4molH 发生加成反应,故错误;
2
故选bd;
【小问3详解】
反应⑤的类型是加成反应,由C 和D生成E的化学反应方程式:
+
;
【小问4详解】
根据上述推断G的结构简式为 ;其同分异构体中既能发生银镜反应,又含苯环的一共有24种。即①含有—CHO、—OH、—CH 三个取代基,两个在对位,另一个有2种位置;两个在间位,
3
另一个有4种位置;两个在邻位,另一个有4种位置;②含有—OH和—CH—CHO两个取代基的共4种;
2
含有—CHO和—CHOH两个取代基的共3种;含有—CHO和—OCH 两个取代基的共3种;含有—CH 和
2 3 3
—OOCH两个取代基的共3种;③含有—CHOOCH一个取代基的有1种,共计24种;
2
【小问5详解】
由于E分子中既有—OH又有—COOH,则2个E分子之间发生酯化反应生成六元环酯,再加上两个六元苯
环,即为含有3个六元环的化合物,其结构简式为 ,这是一个对称
结构的有机物,含有不同化学环境的氢原子一共为6种,分别是苯环上3种,—OH上1种,—CH 上1种,
3
CH原子团上1种。
20. 水煤气变换 是重要的化工过程,主要用于合成氨、制氢以
及合成气加工等工业领域中。回答下列问题:
(1)Shibata曾做过下列实验:
①使纯 缓慢地通过处于721℃下的过量氧化钴CoO(s),氧化钴部分被还原为金属钴Co(s),平衡后气体
中 的物质的量分数为0.0250。
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.0192。
根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是 _______CO(填“大于”或“小于”)。
(2)721℃时,在密闭容器中将等物质的量的CO(g)和 混合,采用适当的催化剂进行反应,则平
衡时体系中 的物质的量分数为_______(填标号)。
A.<0.25 B.0.25~0.50 C.>0.50
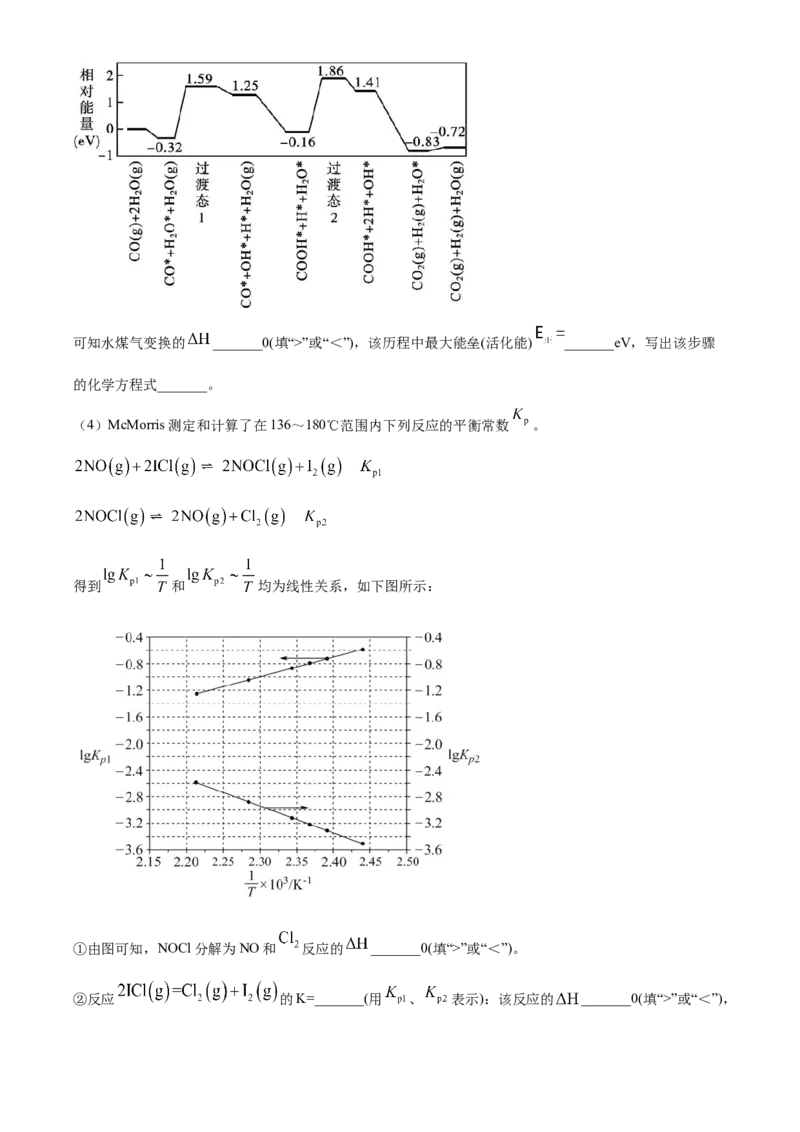
(3)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,
其中吸附在金催化剂表面上的物种用*标注。可知水煤气变换的 _______0(填“>”或“<”),该历程中最大能垒(活化能) _______eV,写出该步骤
的化学方程式_______。
(4)McMorris测定和计算了在136~180℃范围内下列反应的平衡常数 。
得到 和 均为线性关系,如下图所示:
①由图可知,NOCl分解为NO和 反应的 _______0(填“>”或“<”)。
②反应 的K=_______(用 、 表示):该反应的 _______0(填“>”或“<”),写出推理过程。
【答案】(1)小于 (2)B
(3) ①. 小于 ②. 2.02 ③. COOH+H+H O=COOH+2H+OH或HO=H+OH
2 2
(4) ①. 大于 ②. K p1 •K p2 ③. 大于⋅ ⋅ ⋅ ⋅ ⋅ ⋅ ⋅ ⋅ ⋅
【解析】
【小问1详解】
H 还原氧化钴的方程式为: ;CO还原氧化钴的方程式为:
2
,平衡时H 还原体系中H 的物质的量分数( )高
2 2
于CO还原体系中CO的物质的量分数( ),故还原CoO(s)为Co(s)的倾向是CO大于H;
2
【小问2详解】
721℃时,在密闭容器中将等物质的量的CO(g)和HO(g)混合,可设其物质的量为1mol,则
2
,则平衡时体系中H 的物质的量分数=
2
,因该反应为可逆反应,故x<1,可假设二者的还原倾向相等,则
x=0.5,由(1)可知CO的还原倾向大于H,所以CO更易转化为H,故x>0.5,由此可判断最终平衡时体系
2 2
中H 的物质的量分数介于0.25~0.50,故答案为B;
2
【小问3详解】
根据水煤气变换[ ]并结合水煤气变换的反应历程相对能量可知,
CO(g)+HO(g)的能量(-0.32eV)高于CO(g)+H(g)的能量(-0.83eV),故水煤气变换的ΔH小于0;活化能即反
2 2 2
应物状态达到活化状态所需能量,根据变换历程的相对能量可知,最大差值为:其最大能垒(活
化能)E =1.86-(-0.16)eV=2.02eV;该步骤的反应物为COOH +H +H O =COOH +2H +OH ;因反应前后
正 2
COOH 和1个H 未发生改变,也可以表述成HO =H +OH ;
2
【小问4详解】
①由图可知,lgKp 随着温度的升高而增大,说明升高温度,平衡正向移动,则NOCl分解为NO和Cl 反
2 2
应为吸热反应,ΔH大于0,故答案为:大于;
②Ⅰ2NO(g)+2ICl(g) 2NOCl(g)+I(g),Ⅱ2NOCl(g) 2NO(g)+Cl (g)根据盖斯定律Ⅰ+Ⅱ得2ICl(g)=Cl (g)
2 2 2
+I (g),则反应2ICl(⇌g)=Cl (g)+I (g)的K=K •K ;令⇌T>T,则lgK(T )-lgK(T )=lgK (T )•K (T )-
2 2 2 P1 P2 1 2 1 2 P1 1 P2 1
lgK (T )•K (T )=lgK (T )+lgK (T )-lgK (T )-lgK (T )=lgK (T )-lgK (T )-[lgK (T )-lgK (T )],由图中信息
P1 2 P2 2 P1 1 P2 1 P1 2 P2 2 P2 1 P2 2 P1 2 P1 1
可知,lgKp 随着温度的升高而增大,则lgK (T )-lgK (T )>0,lgKp 随着温度的升高而减小,则lgK (T )-
2 P2 1 P2 2 1 P1 2
lgK (T )>0,lgK ~ 和lgK ~ 均为线性关系,且代表lgK ~ 曲线更陡,则lgK (T )-lgK (T )>
P1 1 P1 P2 P2 P2 1 P2 2
lgK (T )-lgK (T ),说明lgK(T )-lgK(T )>0,则升高温度,K值变大,该反应为吸热反应,ΔH大于0。
P1 2 P1 1 1 2、、
下载最新免费模拟卷,到公众号:一枚试卷君