文档内容
2020 级高三模拟考试
化学试题
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Al 27 Cl 35.5 Ti 48 Ag 108
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1. 2022年卡塔尔世界杯中国元素随处可见,下列说法错误的是
A. 中国打造的卢塞尔体育场的主体钢结构材料属于合金
B. 中国承建的阿尔卡萨光伏电站使用的电池材料主要为二氧化硅
C. 中国新能源客车的引入有助于实现卡塔尔世界杯绿色低碳的目标
D. 中国制造的足球球面材料Speed Shell(纹理聚氨酯),属于有机高分子材料
2. 下列叙述正确的是
A. 容量瓶、滴定管、分液漏斗使用前均需要检验是否漏水
B. 可用氢氟酸清洗做过硅酸分解实验的瓷坩埚
C. 金属镁着火时,可用泡沫灭火器灭火
D. 可将硝酸银固体保存在棕色细口瓶中
3. 铁铝铅榴石主要成分为 ,其组成也可写成的氧化物形式:
。下列说法正确的是
A. 组成元素均位于元素周期表的p区
B. 晶体硅的熔点比二氧化硅晶体高
C. 基态铝原子核外电子有7种不同的空间运动状态
D. 中Fe(II)与Fe(III)的个数比为2:1
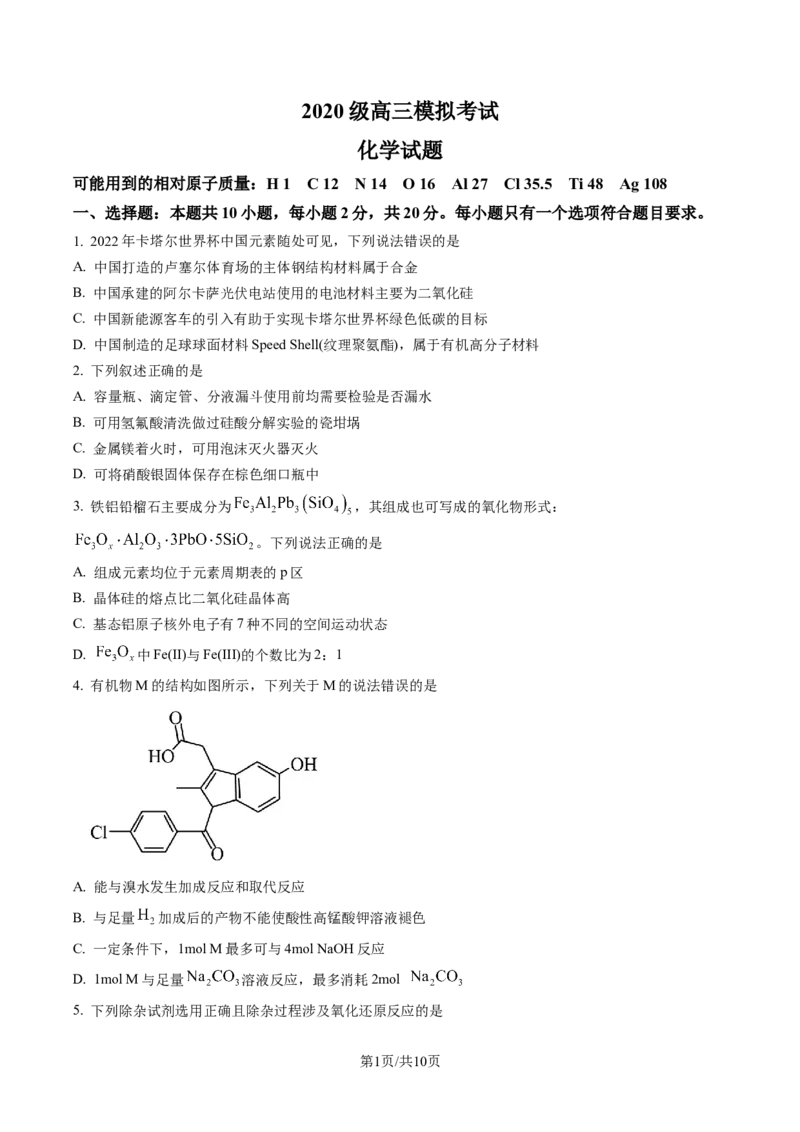
4. 有机物M的结构如图所示,下列关于M的说法错误的是
A. 能与溴水发生加成反应和取代反应
B. 与足量 加成后的产物不能使酸性高锰酸钾溶液褪色
C. 一定条件下,1mol M最多可与4mol NaOH反应
D. 1mol M与足量 溶液反应,最多消耗2mol
5. 下列除杂试剂选用正确且除杂过程涉及氧化还原反应的是
第1页/共10页
学科网(北京)股份有限公司选项 物质(括号内为杂质) 除杂试剂
A ( ) 饱和 溶液
B ( ) 盐酸、NaOH溶液、
C ( ) 无水
D 溴苯( ) NaOH溶液
A. A B. B C. C D. D
6. 铬与铝性质相似,但活泼性比铝弱、熔点比铝高。下列说法错误的是
A. 可用铝热反应制备铬
B. 常温下铬在浓硝酸中发生钝化
C. 可直接蒸发 溶液制备无水
D. 已知碱性条件下,Cr(Ⅲ)可被氧化为Cr(Ⅵ),则其氧化产物为
7. 前四周期元素W、X、Y、Z的原子序数依次增大且分属不同周期。X的最高能级的电子数比电子层数
多1,Y的最高价含氧酸为具有吸水性的弱酸,Z与W中均存在单电子,且两者单电子数和最外层电子数
均相同。下列说法正确的是
A. 四种元素中电负性最大的为Y
B. X元素的第一电离能高于其同周期相邻元素
C. Z元素在同周期中金属性最强
D. W与X两种元素形成的化合物中只含有极性键
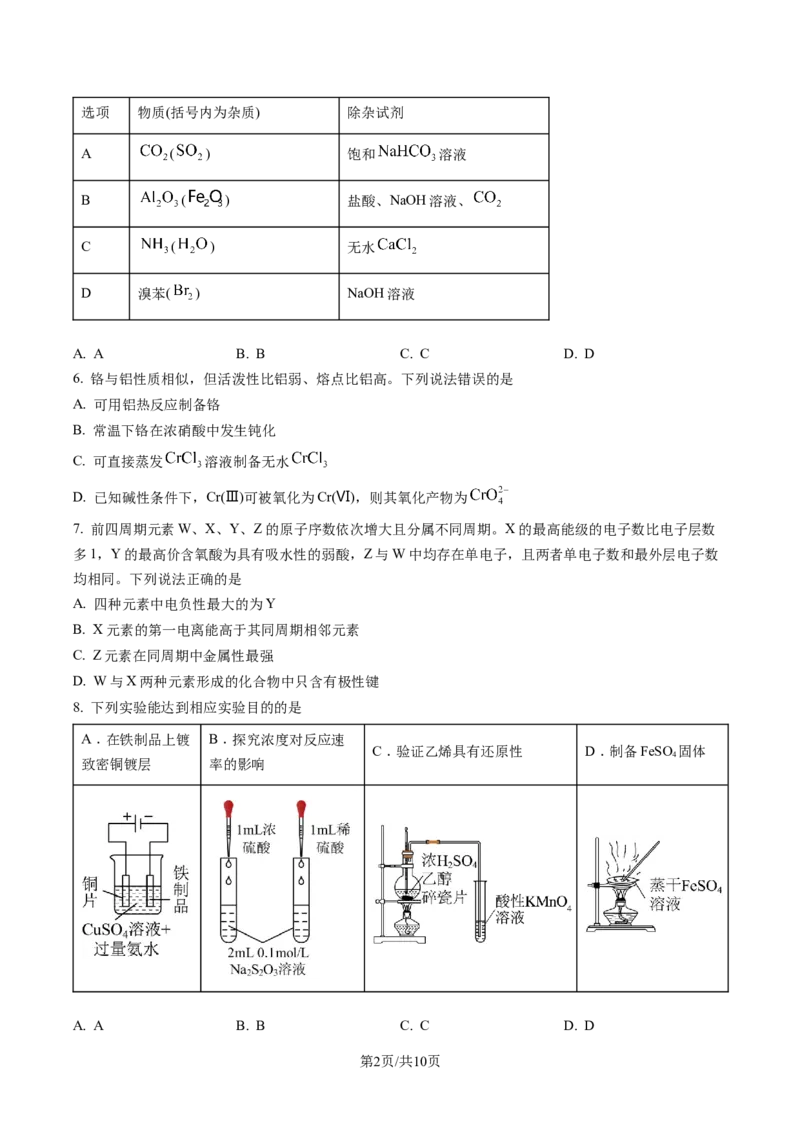
8. 下列实验能达到相应实验目的的是
A.在铁制品上镀 B.探究浓度对反应速
C.验证乙烯具有还原性 D.制备FeSO 固体
4
致密铜镀层 率的影响
A. A B. B C. C D. D
第2页/共10页
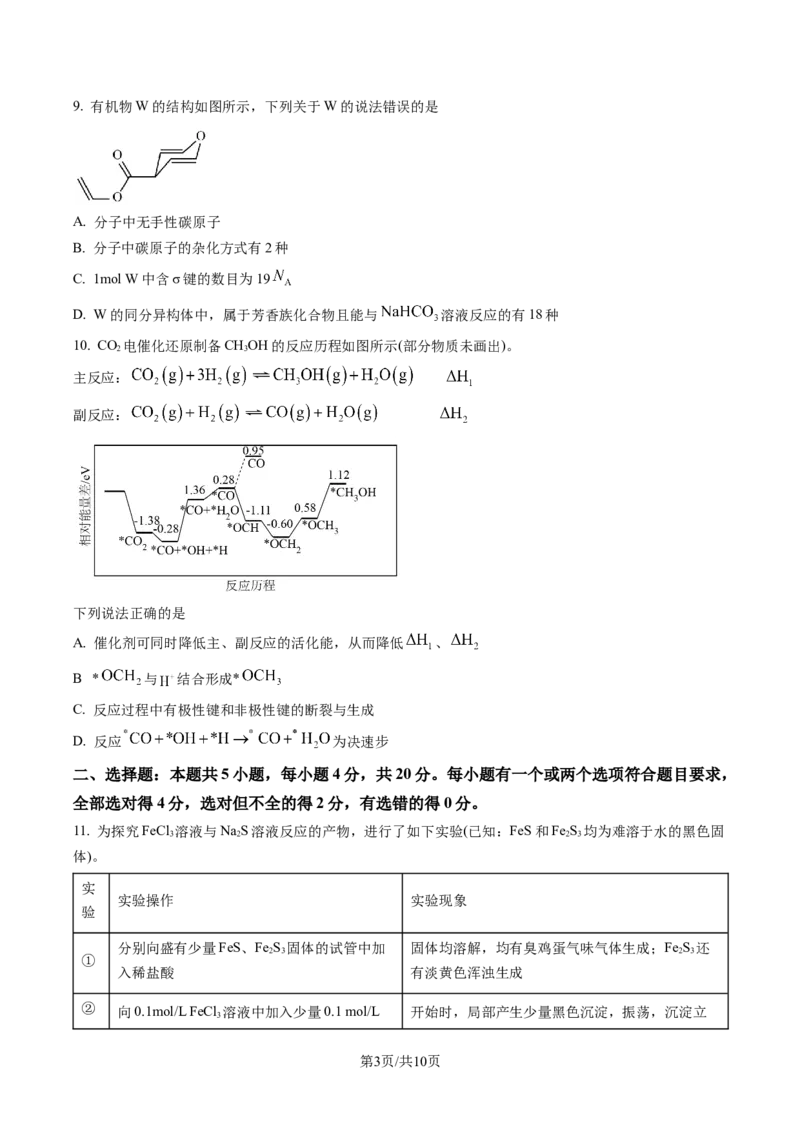
学科网(北京)股份有限公司9. 有机物W的结构如图所示,下列关于W的说法错误的是
A. 分子中无手性碳原子
B. 分子中碳原子的杂化方式有2种
C. 1mol W中含σ键的数目为19
D. W的同分异构体中,属于芳香族化合物且能与 溶液反应的有18种
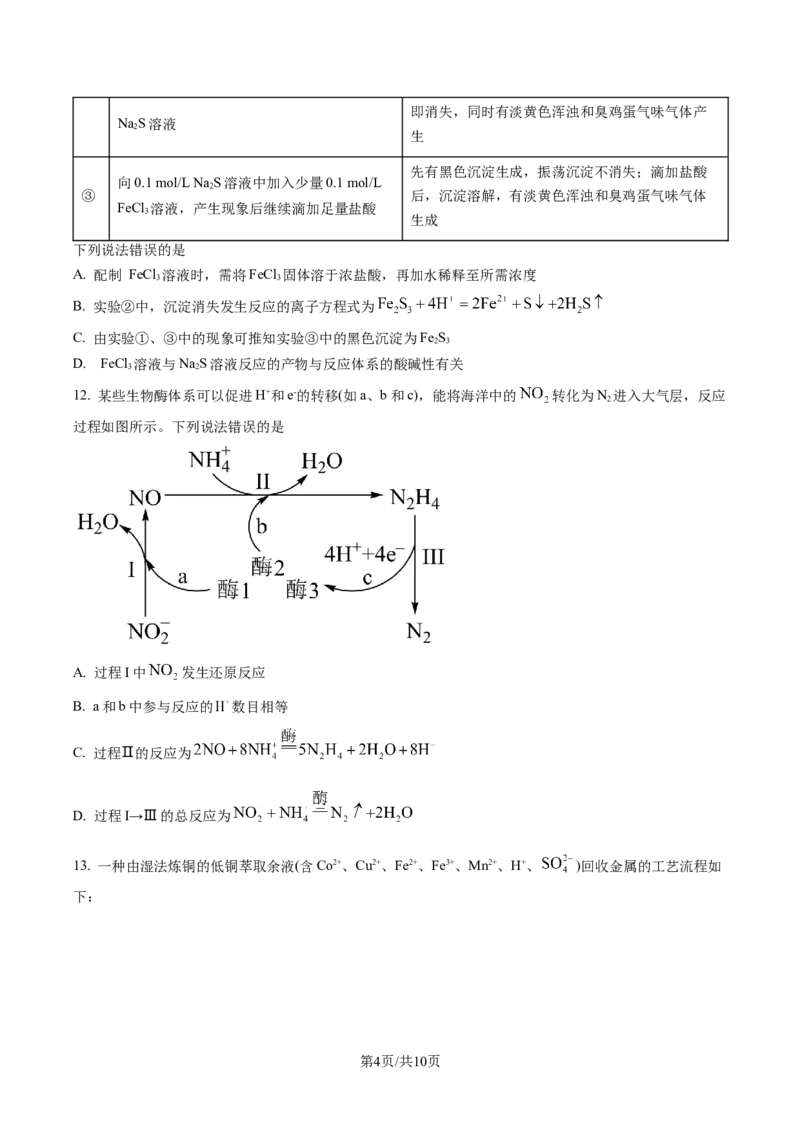
10. CO 电催化还原制备CHOH的反应历程如图所示(部分物质未画出)。
2 3
主反应:
副反应:
下列说法正确的是
A. 催化剂可同时降低主、副反应的活化能,从而降低 、
.
B * 与 结合形成*
C. 反应过程中有极性键和非极性键的断裂与生成
D. 反应 为决速步
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,
全部选对得4分,选对但不全的得2分,有选错的得0分。
11. 为探究FeCl 溶液与NaS溶液反应的产物,进行了如下实验(已知:FeS和Fe S 均为难溶于水的黑色固
3 2 2 3
体)。
实
实验操作 实验现象
验
分别向盛有少量FeS、Fe S 固体的试管中加 固体均溶解,均有臭鸡蛋气味气体生成;Fe S 还
2 3 2 3
①
入稀盐酸 有淡黄色浑浊生成
② 向0.1mol/L FeCl 溶液中加入少量0.1 mol/L 开始时,局部产生少量黑色沉淀,振荡,沉淀立
3
第3页/共10页
学科网(北京)股份有限公司即消失,同时有淡黄色浑浊和臭鸡蛋气味气体产
NaS溶液
2
生
先有黑色沉淀生成,振荡沉淀不消失;滴加盐酸
向0.1 mol/L Na S溶液中加入少量0.1 mol/L
2
③ 后,沉淀溶解,有淡黄色浑浊和臭鸡蛋气味气体
FeCl 溶液,产生现象后继续滴加足量盐酸
3
生成
下列说法错误的是
A. 配制 FeCl 溶液时,需将FeCl 固体溶于浓盐酸,再加水稀释至所需浓度
3 3
B. 实验②中,沉淀消失发生反应的离子方程式为
C. 由实验①、③中的现象可推知实验③中的黑色沉淀为Fe S
2 3
D. FeCl 溶液与NaS溶液反应的产物与反应体系的酸碱性有关
3 2
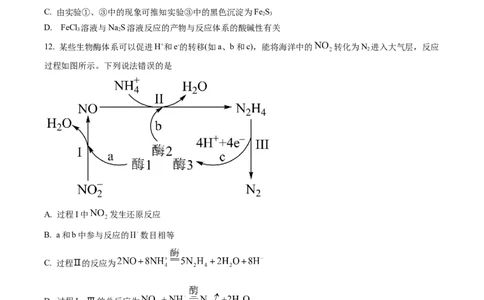
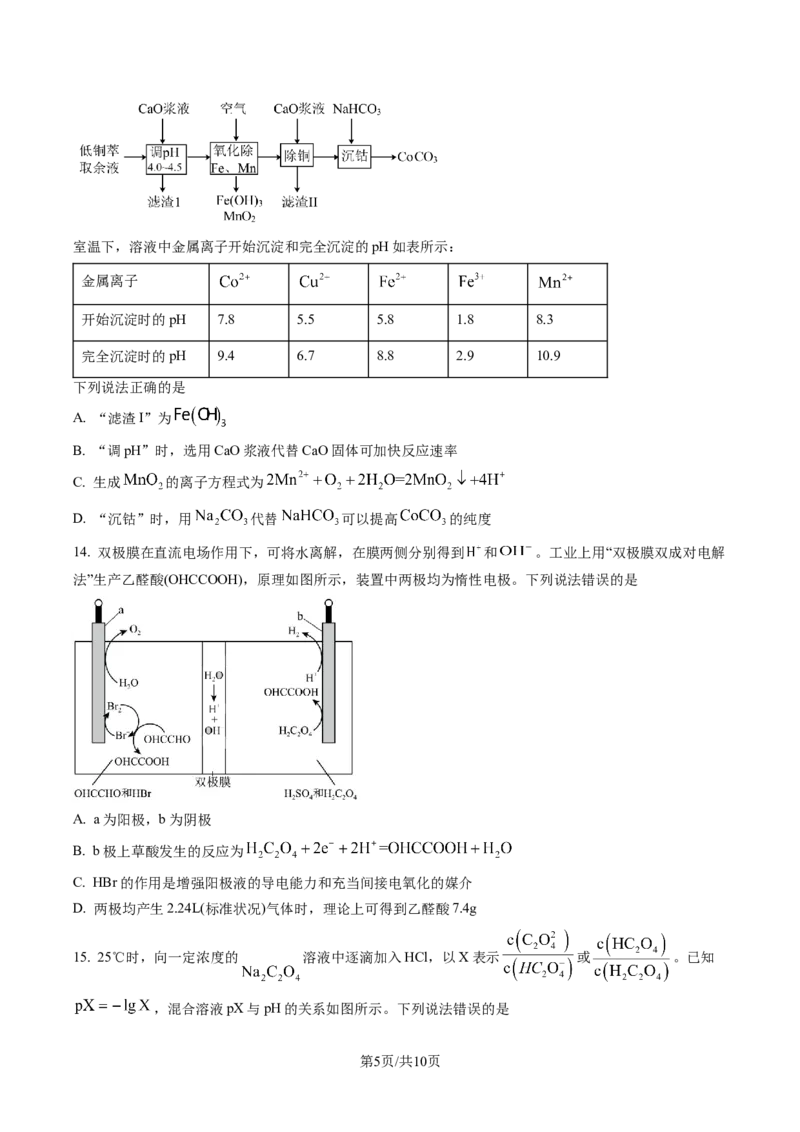
12. 某些生物酶体系可以促进H+和e-的转移(如a、b和c),能将海洋中的 转化为N 进入大气层,反应
2
过程如图所示。下列说法错误的是
A. 过程I中 发生还原反应
B. a和b中参与反应的 数目相等
C. 过程Ⅱ的反应为
D. 过程I→Ⅲ的总反应为
13. 一种由湿法炼铜的低铜萃取余液(含Co2+、Cu2+、Fe2+、Fe3+、Mn2+、H+、 )回收金属的工艺流程如
下:
第4页/共10页
学科网(北京)股份有限公司室温下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
金属离子
开始沉淀时的pH 7.8 5.5 5.8 1.8 8.3
完全沉淀时的pH 9.4 6.7 8.8 2.9 10.9
下列说法正确的是
A. “滤渣I”为
B. “调pH”时,选用CaO浆液代替CaO固体可加快反应速率
C. 生成 的离子方程式为
D. “沉钴”时,用 代替 可以提高 的纯度
14. 双极膜在直流电场作用下,可将水离解,在膜两侧分别得到 和 。工业上用“双极膜双成对电解
法”生产乙醛酸(OHCCOOH),原理如图所示,装置中两极均为惰性电极。下列说法错误的是
A. a为阳极,b为阴极
B. b极上草酸发生的反应为
C. HBr的作用是增强阳极液的导电能力和充当间接电氧化的媒介
D. 两极均产生2.24L(标准状况)气体时,理论上可得到乙醛酸7.4g
15. 25℃时,向一定浓度的 溶液中逐滴加入HCl,以X表示 或 。已知
,混合溶液pX与pH的关系如图所示。下列说法错误的是
第5页/共10页
学科网(北京)股份有限公司A. 曲线I表示 与pH的关系
B. 第一步电离常数 的数量级为
C. 时,
D. 时,
三、非选择题:本题共5小题,共60分。
16. VA族元素原子核外电子排布有着特殊性,能与其他元素组成结构、性质各异的化合物。回答下列问题:
(1)氮原子可以提供孤电子对与氧原子形成配位键,基态氧原子 的价层电子发生重排提供一个空轨道,
则重排后的氧原子价电子排布图为_______,基态氧原子的价层电子不是重排结构,原因是不符合
_______(填“泡利不相容原理”或“洪特规则”)。
(2)沸点: _______ (填“>”或“<”,下同),键角: _______ 。
(3)As、Ge、Se三种元素 第的一电离能由大到小的顺序是_______。
(4)基态As原子的最高能级组的电子排布式为_______,与 互为等电子体的分子为_______(写出
一种)。
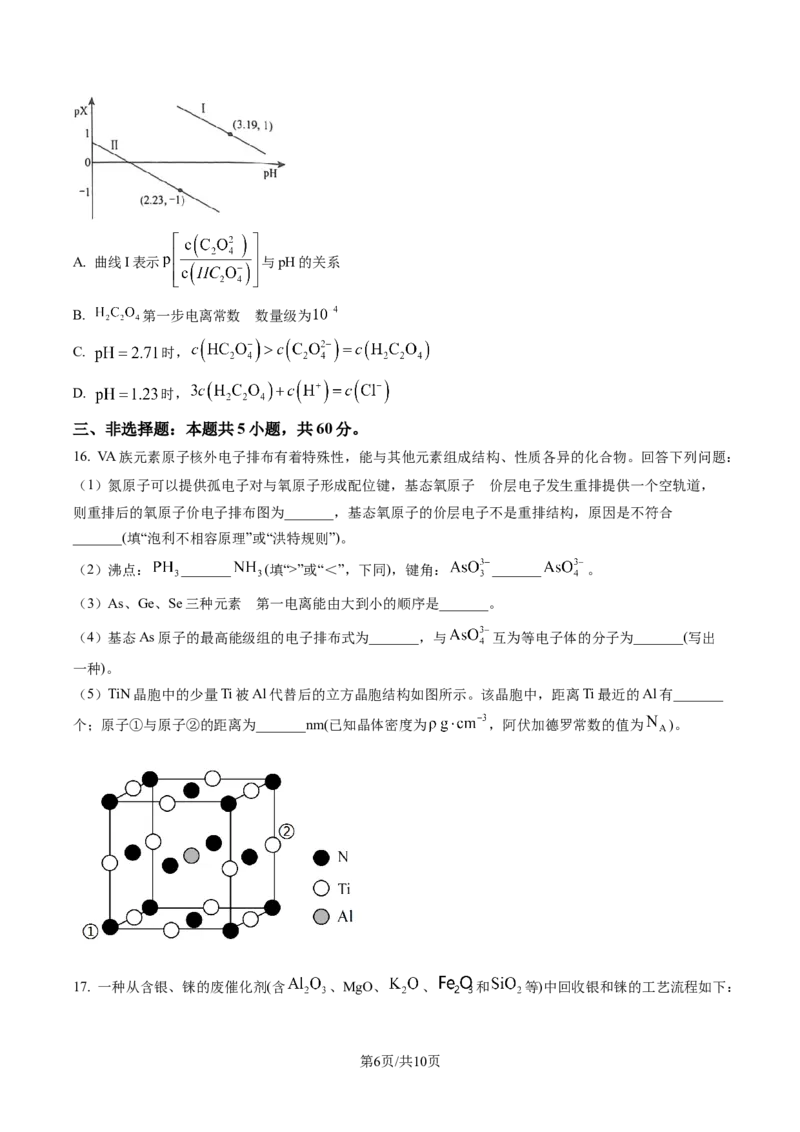
(5)TiN晶胞中的少量Ti被Al代替后的立方晶胞结构如图所示。该晶胞中,距离Ti最近的Al有_______
个;原子①与原子②的距离为_______nm(已知晶体密度为 ,阿伏加德罗常数的值为 )。
17. 一种从含银、铼的废催化剂(含 、MgO、 、 和 等)中回收银和铼的工艺流程如下:
第6页/共10页
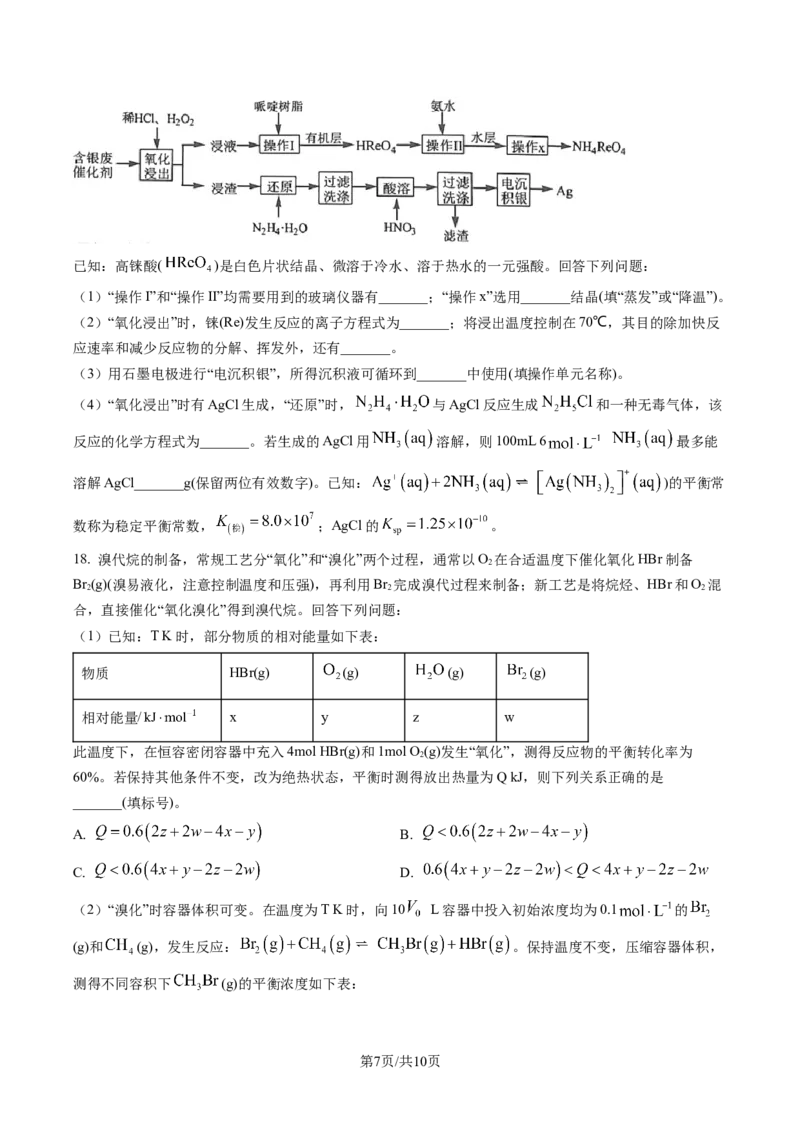
学科网(北京)股份有限公司已知:高铼酸( )是白色片状结晶、微溶于冷水、溶于热水的一元强酸。回答下列问题:
(1)“操作I”和“操作II”均需要用到的玻璃仪器有_______;“操作x”选用_______结晶(填“蒸发”或“降温”)。
(2)“氧化浸出”时,铼(Re)发生反应的离子方程式为_______;将浸出温度控制在70℃,其目的除加快反
应速率和减少反应物的分解、挥发外,还有_______。
(3)用石墨电极进行“电沉积银”,所得沉积液可循环到_______中使用(填操作单元名称)。
(4)“氧化浸出”时有AgCl生成,“还原”时, 与AgCl反应生成 和一种无毒气体,该
反应的化学方程式为_______。若生成的AgCl用 溶解,则100mL 6 最多能
溶解AgCl_______g(保留两位有效数字)。已知: )的平衡常
数称为稳定平衡常数, ;AgCl的 。
18. 溴代烷的制备,常规工艺分“氧化”和“溴化”两个过程,通常以O 在合适温度下催化氧化HBr制备
2
Br (g)(溴易液化,注意控制温度和压强),再利用Br 完成溴代过程来制备;新工艺是将烷烃、HBr和O 混
2 2 2
合,直接催化“氧化溴化”得到溴代烷。回答下列问题:
(1)已知:T K时,部分物质的相对能量如下表:
物质 HBr(g) (g) (g) (g)
相对能量/ x y z w
此温度下,在恒容密闭容器中充入4mol HBr(g)和1mol O(g)发生“氧化”,测得反应物的平衡转化率为
2
60%。若保持其他条件不变,改为绝热状态,平衡时测得放出热量为Q kJ,则下列关系正确的是
_______(填标号)。
A. B.
C. D.
(2)“溴化”时容器体积可变。在温度为T K时,向10 L容器中投入初始浓度均为0.1 的
(g)和 (g),发生反应: 。保持温度不变,压缩容器体积,
测得不同容积下 (g)的平衡浓度如下表:
第7页/共10页
学科网(北京)股份有限公司容器体积V/L 10 3
m 0.09 0.25
当容器体积从10 L缩小到3 L时,测得此时容器内仅有四种气态组分,平衡_______移动(填“正向”
“逆向”或“不”),m=_______;容器体积缩小到 L时,平衡_______移动(填“正向”“逆向”或“不”)。T K时,
此反应在容积为10 L和 L时化学平衡常数分别为 、 ,则 _______ (填“大于”“小于”或“等
于”)。
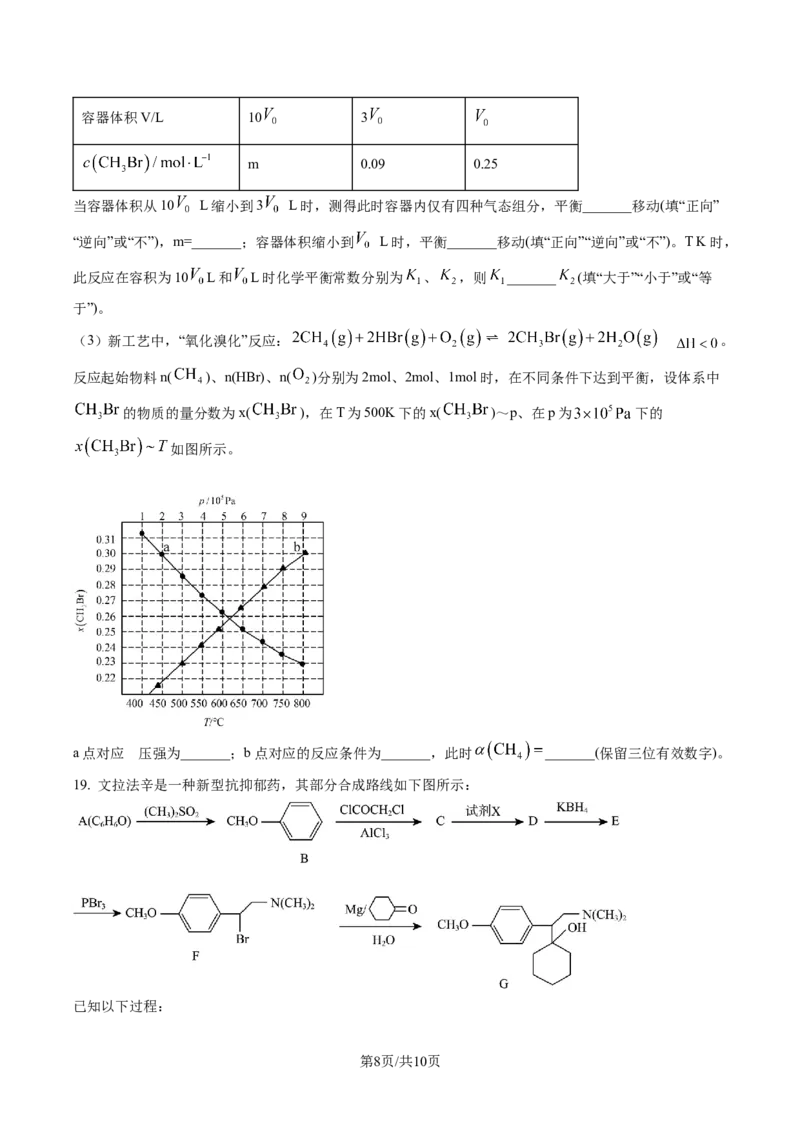
(3)新工艺中,“氧化溴化”反应: 。
反应起始物料n( )、n(HBr)、n( )分别为2mol、2mol、1mol时,在不同条件下达到平衡,设体系中
的物质的量分数为x( ),在T为500K下的x( )~p、在p为 下的
如图所示。
a点对应 的压强为_______;b点对应的反应条件为_______,此时 _______(保留三位有效数字)。
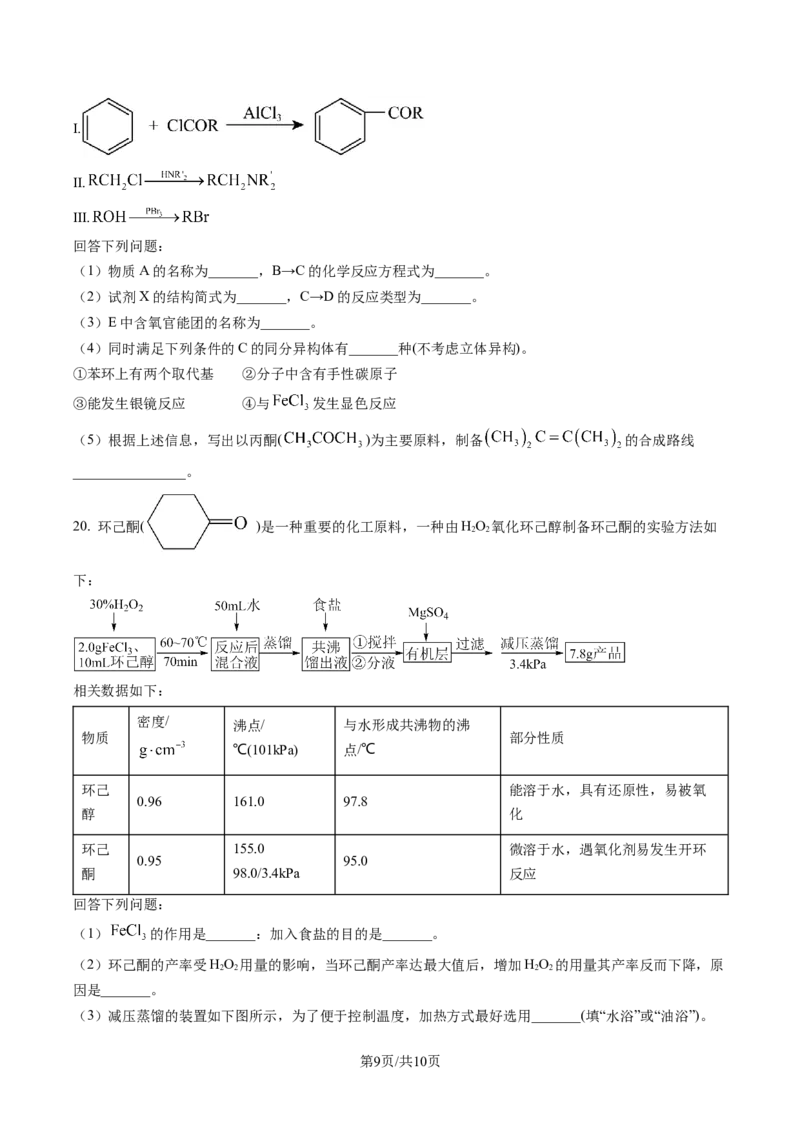
19. 文拉法辛是一种新型抗抑郁药,其部分合成路线如下图所示:
已知以下过程:
第8页/共10页
学科网(北京)股份有限公司I.
II.
III.
回答下列问题:
(1)物质A的名称为_______,B→C的化学反应方程式为_______。
(2)试剂X的结构简式为_______,C→D的反应类型为_______。
(3)E中含氧官能团的名称为_______。
(4)同时满足下列条件的C的同分异构体有_______种(不考虑立体异构)。
①苯环上有两个取代基 ②分子中含有手性碳原子
③能发生银镜反应 ④与 发生显色反应
(5)根据上述信息,写出以丙酮( )为主要原料,制备 的合成路线
________________。
20. 环己酮( )是一种重要的化工原料,一种由HO 氧化环己醇制备环己酮的实验方法如
2 2
下:
相关数据如下:
密度/ 沸点/ 与水形成共沸物的沸
物质 部分性质
℃(101kPa) 点/℃
环己 能溶于水,具有还原性,易被氧
0.96 161.0 97.8
醇 化
环己 155.0 微溶于水,遇氧化剂易发生开环
0.95 95.0
酮 98.0/3.4kPa 反应
回答下列问题:
(1) 的作用是_______:加入食盐的目的是_______。
(2)环己酮的产率受HO 用量的影响,当环己酮产率达最大值后,增加HO 的用量其产率反而下降,原
2 2 2 2
因是_______。
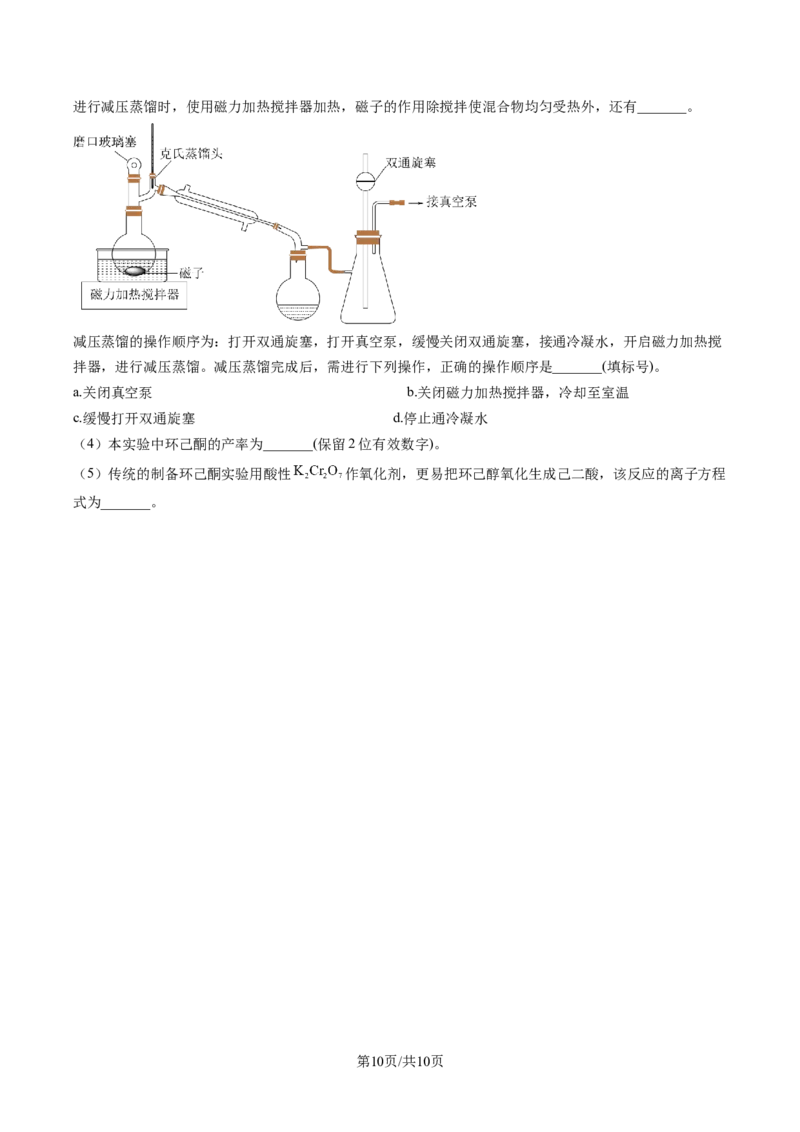
(3)减压蒸馏的装置如下图所示,为了便于控制温度,加热方式最好选用_______(填“水浴”或“油浴”)。
第9页/共10页
学科网(北京)股份有限公司进行减压蒸馏时,使用磁力加热搅拌器加热,磁子的作用除搅拌使混合物均匀受热外,还有_______。
减压蒸馏的操作顺序为:打开双通旋塞,打开真空泵,缓慢关闭双通旋塞,接通冷凝水,开启磁力加热搅
拌器,进行减压蒸馏。减压蒸馏完成后,需进行下列操作,正确的操作顺序是_______(填标号)。
a.关闭真空泵 b.关闭磁力加热搅拌器,冷却至室温
c.缓慢打开双通旋塞 d.停止通冷凝水
(4)本实验中环己酮的产率为_______(保留2位有效数字)。
(5)传统的制备环己酮实验用酸性 作氧化剂,更易把环己醇氧化生成己二酸,该反应的离子方程
式为_______。
第10页/共10页
学科网(北京)股份有限公司