文档内容
2024 届新高三开学摸底考试卷
化 学
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Cu 64 Zn 65
第Ⅰ卷(选择题 共42分)
一、选择题:本题共14个小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.我国力争2030年前实现碳达峰,2060年前实现碳中和,事关中华民族永续发展和构建人类命运共同
体。下列措施中不能减少污染并降碳排放的是
A.完善充电桩、自行车道等相应的配套设施建设,引导公众优先绿色出行
B.大规模开采可燃冰作为新能源和通过清洁煤技术减少煤燃烧污染
C.支持风力发电、光伏发电、潮汐发电等行业健康有序发展
D.加大农村房屋建筑节能改造力度,降低冬季取暖燃料的使用
【答案】B
【详解】A.完善充电桩、自行车道等相应的配套设施建设,提倡电动车、自行车出行,可减少石油燃料
的使用,实现减污降碳,故A正确;
B.可燃冰主要成分为甲烷,燃烧产物会产生二氧化碳,大规模开采使用不能实现降碳,故B错误;
C.风力发电、光伏发电、潮汐发电没有污染,没有二氧化碳排放,可以达到降碳的目的,故C正确;
D.加大农村房屋门窗气密性改造力度,减少跑风漏气,可减少化石燃料的使用,实现减污降碳,故D正
确;
答案选B。
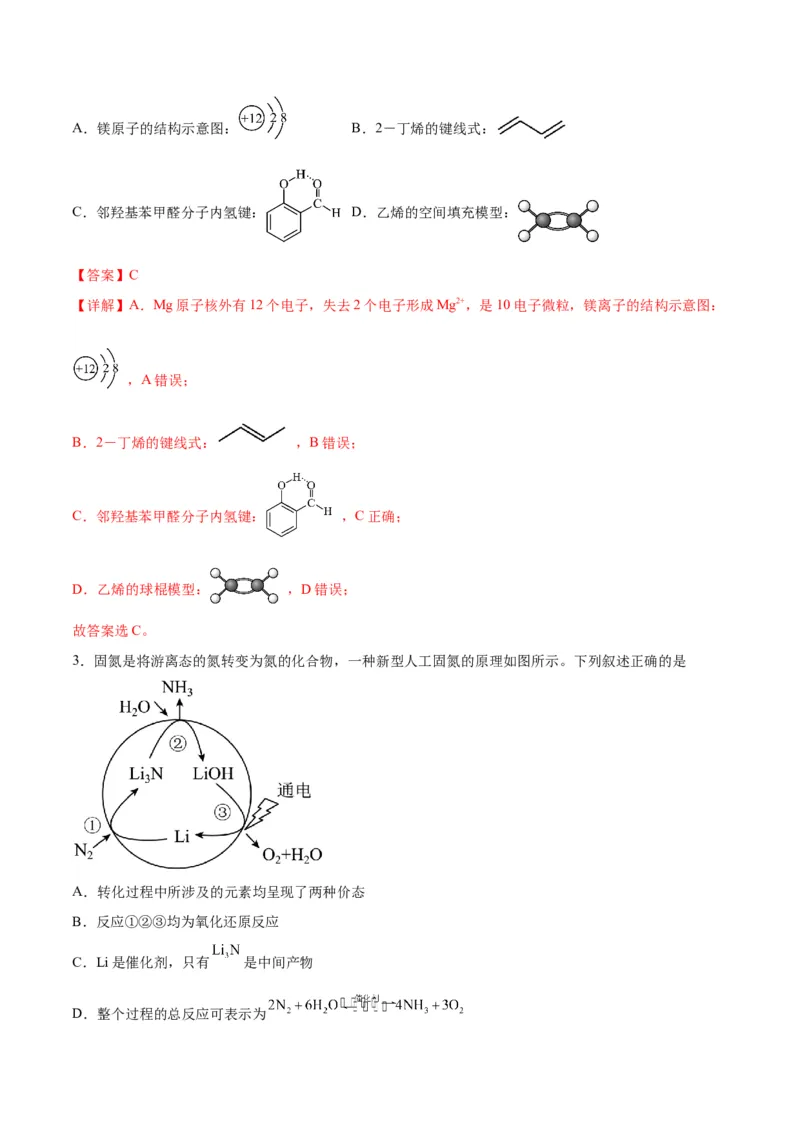
2.下列化学用语表示正确的是A.镁原子的结构示意图: B.2-丁烯的键线式:
C.邻羟基苯甲醛分子内氢键: D.乙烯的空间填充模型:
【答案】C
【详解】A.Mg原子核外有12个电子,失去2个电子形成Mg2+,是10电子微粒,镁离子的结构示意图:
,A错误;
B.2-丁烯的键线式: ,B错误;
C.邻羟基苯甲醛分子内氢键: ,C正确;
D.乙烯的球棍模型: ,D错误;
故答案选C。
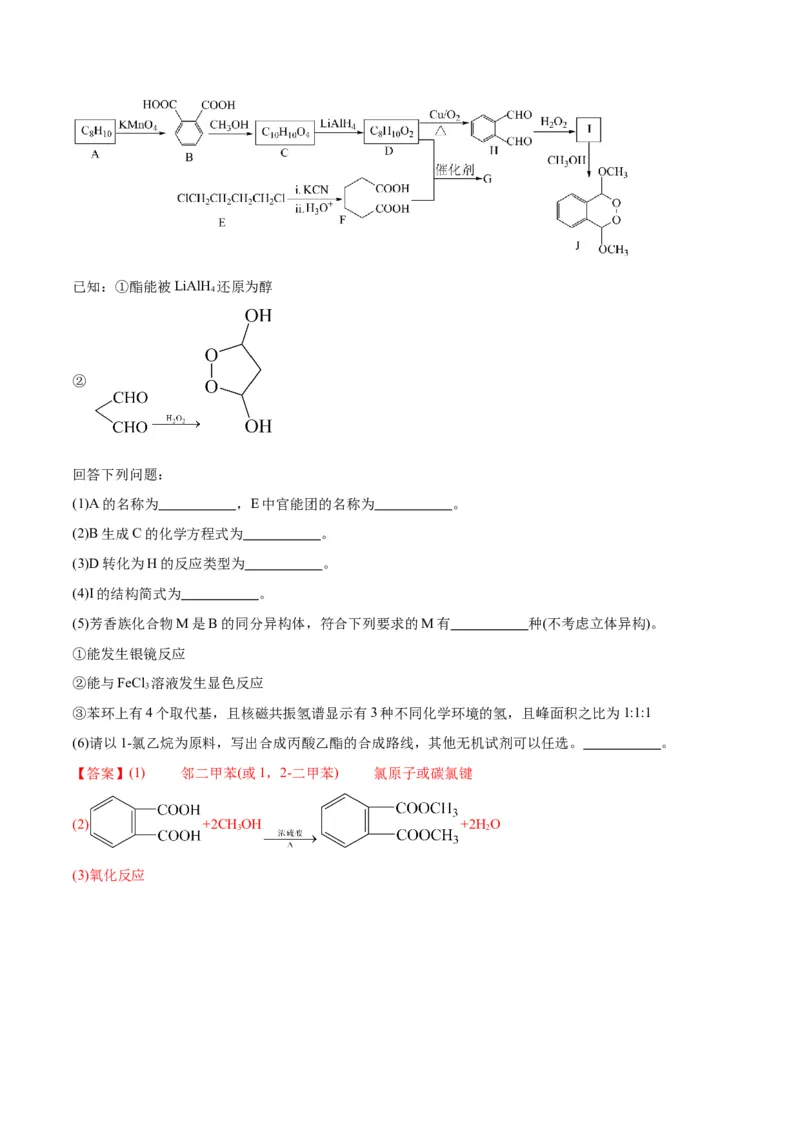
3.固氮是将游离态的氮转变为氮的化合物,一种新型人工固氮的原理如图所示。下列叙述正确的是
A.转化过程中所涉及的元素均呈现了两种价态
B.反应①②③均为氧化还原反应
C.Li是催化剂,只有 是中间产物
D.整个过程的总反应可表示为【答案】D
【详解】A.根据转化关系可知:在转化过程中H始终呈+1价,A错误;
B.反应②为 ,该反应过程中元素化合价不变,因此反应属于非氧化还原反
应,B错误;
C.Li是催化剂, 和LiOH均是中间产物,C错误;
D.根据分析,整个过程的总反应为氮气和水生成氨气和氧气,可表示为
,D正确;
故选D。
4.有机物M是制备螺虫乙酯的重要中间体,结构如图所示。下列关于M的说法不正确的是
A.能发生取代反应和加成反应
B.分子中所有碳原子可能共平面
C.有三种含氧官能团
D.分子式C H NO
19 27 4
【答案】B
【详解】A.含酯基可发生取代反应,含苯环,羰基可发生加成反应,A项正确;
B. 左侧六元环中6个C原子均为 杂化,所有碳原子不能共面,B项错误;
C. 分子中含酯基,醚键,羰基,则有三种含氧官能团,C项正确;
D. 由结构可知,1个分子中含有19个C原子,27个H原子,1个N原子,4个O原子,分子式
,D项正确;
答案选B。
5.关注“实验室化学”并加以实践能有效提高学生的实验素养,用如图所示装置(夹持装置均已省略)进行
实验,能达到实验目的的是A.甲装置可用于验证NaO 与水反应的能量变化
2 2
B.乙装置可用于观察氯化钠的焰色试验
C.丙装置可用于制取并收集干燥、纯净的NO
D.丁装置可用于准确量取一定体积的KCr O 溶液
2 2 7
【答案】A
【详解】A.2NaO+2H O=4NaOH+O ↑,虽然反应生成气体,但是气体不进入集气瓶中,可以用液面变化
2 2 2 2
来说明反应能量变化,A符合题意;
B.Cu的焰色反应为绿色,不能用铜丝代替铂丝,B不符合题意;
C.NO与氧气反应,不能选排空气法收集NO,C不符合题意;
D.重铬酸钾溶液属于氧化性滴定液,因此应装在酸性滴定管中,丁装置为碱性滴定管,D不符合题意;
故选A。
6.能正确表示下列反应的离子方程式的是
A.浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H ↑
2
B.钠与硫酸铜溶液反应:2Na+Cu2+=Cu+2Na+
C.过量铁与稀硝酸反应:Fe+4H++ =3Fe3++2H O+NO↑
2
D.等物质的量的Ba(OH) 与NaHSO 在溶液中反应:Ba2++OH−+H++ =BaSO ↓+H O
2 4 4 2
【答案】D
【详解】A.浓盐酸与铁屑反应生成亚铁离子和氢气,离子方程式为: Fe+2H+=Fe2++H ↑,故A错误;
2
B.钠与硫酸铜溶液反应先和水反应生成氢氧化钠溶液再和硫酸铜反应生成氢氧化铜沉淀,反应的离子方
程式:2Na+2HO+Cu2+=Cu(OH) ↓+H ↑+2Na+,故B错误;
2 2 2
C.过量铁与稀硝酸反应生成亚铁离子,反应的离子方程式为:3Fe+8H++2 ═3Fe2++4H O+2NO↑,故C
2
错误;
D.等物质的量的Ba(OH) 与NaHSO 在溶液中反应,氢氧根离子过量,硫酸氢根离子应该拆开,正确的离
2 4子方程式为:Ba2++OH-+H++ ═BaSO ↓+H O,故D正确;
4 2
故选D。
7.设 为阿伏加德罗常数的值,下列叙述正确的是
A.常温常压下,48gO 的价层电子中所含的孤电子对数为
3
B.1mol液态水完全转化为固态冰,则最多新形成的氢键数为
C.40g的金刚砂(SiC)中,所含的碳硅键个数为
D.标准状况下22.4L的乙炔与氢气完全加成,共有 的共价键发生断裂
【答案】A
【详解】A.48g臭氧的物质的量为 =1mol,臭氧的电子式为 ,故其单个分子中,孤
电子对数为5,A正确;
B.含1molH O的冰中,最多形成2mol的氢键,但是液体水中本就存在氢键,B错误;
2
C.经计算40gSiC的物质的量为 =1mol,根据SiC的结构分析可得其中含有的碳硅键个数为
;
D.1mol乙炔与氢气完全加成,断裂的为乙炔中2mol的π键及氢气中2mol的 键,D错误;
故答案为:A。
8.X、Y、Z、J、Q是原子序数依次增大,且分布在三个短周期的主族元素,Y元素原子的核外未成对电
子数在同周期中最多,Y、Z同周期,Z、J同主族.下列说法错误的是
A.电负性:Q>J;第一电离能:Y>Z B.最高价含氧酸的酸性:Q>J
C. 、 的中心原子杂化方式相同 D.简单离子半径:Y>Z、J>Q
【答案】C
【分析】由X、Y、Z、J、Q是原子序数依次增大,分布在三个短周期的主族元素,可知X为第一周期元
素,为H,由Z、J同主族可知,Y、Z为第二周期元素,J、Q为第三周期元素,Y元素原子的核外未成对
电子数在同周期中最多,则可知为N,可推出,Z为O,J为S,Q为Cl。【详解】A.同周期原子从左到右电负性逐渐增大,则电负性Q>J(Cl>S),N最外层电子为半充满状态,第
一电离能Y>Z(N>O),A正确;
B.非金属性越强,最高价含氧酸的酸性越强,酸性 ,B正确;
C. 中N原子价层电子对数 ,为 杂化, 中Cl原子价层电子对数
,为 杂化,C错误;
D.简单离子半径 , ,D正确。
故选C。
9.某溶液仅由 、Cl-、 、 、 、Fe3+、Al3+和K+中的若干种离子组成,且各离子浓度相
等,取适量溶液进行如下实验:
①取该溶液加入过量NaOH溶液,加热,产生无色气体;
②将①过滤、洗涤、灼烧,得到固体a;
③向上述滤液中加足量BaCl 溶液,产生白色沉淀:
2
根据以上实验,下列推断错误的是
A.根据操作①,推断一定存在
B.②中固体a为氧化铁
C.原溶液中一定不存在 、Al3+,可能含有K+
D.说明原溶液中一定存在 、Cl-、 、 、Fe3+、
【答案】C
【分析】加入过量的碱产生气体为NH ,溶液有 。信息②知加入过量的碱产生了沉淀Fe(OH) ,溶液
3 3
中有Fe3+, 与Fe3+会发生双水解不能共存,则溶液中不存在 。信息③知加溶液中有 。
【详解】A.由上分析溶液中一定有 ,A项正确;
B.Fe(OH) 受热分解为氧化铁Fe O,B项正确;
3 2 3C.由上分析溶液中一定有 和Fe3+而阴离子有 ,又溶液中各离子浓度相同,溶液中电荷不守恒,
所以一定还有Cl-和 。溶液中这五种离子刚好电荷守恒,所以一定不存在 和Al3+、K+,C项错误;
D.由C项分析溶液中一定存在 、Fe3+、 、Cl-和 ,D项正确;
故选C。
10.一种利用废旧镀锌铁皮制备磁性Fe O 纳米粒子的工艺流程如图。
3 4
下列有关说法不正确的是
A.“碱洗”是为了去除废旧镀锌铁皮表面的油污
B.“氧化”时发生反应的离子方程式为2Fe2++ClO-+2H+=2Fe3++Cl-+H O
2
C.“氧化”后的溶液中金属阳离子主要有Fe2+、Fe3+、Na+
D.用激光笔照射“加热沉铁”后所得分散系,产生丁达尔效应
【答案】A
【分析】向废旧镀锌铁皮中加入氢氧化钠溶液除去锌,过滤向固体中加入稀硫酸,铁与稀硫酸反应生成硫
酸亚铁,向硫酸亚铁溶液中加入次氯酸钠溶液,将一部分亚铁离子氧化为铁离子,发生反应:2Fe2++ClO-
+2H+=2Fe3++Cl-+H O,先通入氮气排尽空气(防止后续生成的氢氧化亚铁被氧化),加入氢氧化钠溶液产生氢
2
氧化亚铁、氢氧化铁胶体,分离得到氢氧化亚铁和氢氧化铁,灼烧得到四氧化三铁。
【详解】A.由分析可知,“碱洗”是为了除去锌,生成NaZnO,过滤得到铁单质,A错误;
2 2
B.“氧化”时,亚铁离子与次氯酸根离子发生氧化还原反应,反应的离子方程式为:2Fe2++ClO-
+2H+=2Fe3++Cl-+H O,B正确;
2
C.“氧化”时,部分亚铁离子与次氯酸根离子发生反应:2Fe2++ClO-+2H+=2Fe3++Cl-+H O,故溶液中金属
2
阳离子主要有Fe2+、Fe3+、Na+,C正确;
D.“加热沉铁”后所得分散系为胶体,胶体可产生丁达尔效应,D正确;
答案选A。
11.将amolX、Y混合气体(物质的量之比为1∶1)加入某容积可变的密闭容器中,发生反应:,保持一定温度,改变压强分别达到平衡时,测得不同压强下气体X的物质的量浓度如表所示:
压强p/Pa 2×105 5×105 1×106 3×106
0.08 0.20 0.40 0.80
下列说法正确的是
A.保持一定温度,增大压强,平衡正向移动
B.当压强为3×106Pa时,此反应的平衡常数表达式为
C.2×105Pa时X的平衡转化率大于5×105Pa时X的平衡转化率
D.当压强为2×105Pa时,若再向体系中加入bmolY,重新达到平衡时,体系中气体总物质的量为
【答案】D
【分析】保持一定温度、X(g)和Y(g)起始量相同,容积可变,结合表格中数据可知,在1×106Pa之前,增
大压强为原来的x倍,X的平衡浓度等于原来X平衡浓度的x倍,则1×106Pa之前增大压强,平衡不移
动,m+n=p,且Z一定为气体;3×106Pa是1×106Pa的3倍,但X的平衡浓度的值比0.40的3倍小,说明此
时Z为非气态。
【详解】A.根据分析,1×106Pa之前增大压强,平衡不移动,3×106Pa之后增大压强,平衡正向移动,A
错误;
B.当压强为3×106Pa时,Z为非气态,故此反应的平衡常数表达式为 ,B错误;
C.由上述分析可得,2×105Pa时X的平衡转化率与5×105Pa时X的平衡转化率相等,C错误;
D.当压强为2×105Pa时,反应前后气体分子数不变,达到平衡时,体系共有amol气体,再向体系中加入
bmolY,重新达到平衡时,体系中气体总物质的量为 ,D正确;
故选D。
12.下列实验操作及现象、实验结论均正确的是
选
实验操作及现象 实验结论
项
NO 一定为碳还原浓硝酸的产
A 将炽热的木炭加入浓硝酸中,产生红棕色气体 2
物B 用pH计测量NaHCO 溶液呈碱性,NaHSO 溶液呈酸性 碳酸、亚硫酸均为弱酸
3 3
向装有溴水的分液漏斗中加入苯,振荡静置,溶液分层,上层为橙
C 苯萃取了溴水中的溴
红色
D 向HO 溶液中滴入几滴酸性高锰酸钾溶液,高锰酸钾紫色褪去 HO 有氧化性
2 2 2 2
A.A B.B C.C D.D
【答案】C
【详解】A.浓硝酸受热易分解为NO ,无法证明NO 是被C还原来的,A项错误;
2 2
B.NaHCO 为呈碱性说明其为弱酸强碱盐,所以碳酸为弱酸。而NaHSO 呈酸性为电离无法证明亚硫酸为
3 3
弱酸,B项错误;
C.溴易溶于苯,苯加入溴水中分层上层为橙色,C项正确;
D.HO 将酸性高锰酸钾还原为无色的Mn2+,HO 呈现还原性,D项错误;
2 2 2 2
故选C。
13.据2022年1月统计,我国光伏发电并网装机容量突破3亿千瓦,连续七年稳居全球首位。已知四甲基
氢氧化铵[(CH )NOH]常用作电子工业清洗剂,以四甲基氯化铵[(CH )NCl]为原料,采用电渗析法合成
3 4 3 4
[(CH )NOH],工作原理如图。下列说法错误的是
3 4
A.光伏并网发电装置中P型半导体为正极
B.c为阳离子交换膜,d、e均为阴离子交换膜
C.阳极的电极反应为4OH--4e-=2H O+O↑
2 2
D.制备182g四甲基氢氧化铵,两极共产生33.6L气体(标准状况)
【答案】B
【详解】从图中可以看出,光伏并网发电装置中, a电极连接N型半导体,则其为负极,b电极连接P型半
导体,则其为正极;电解装置中,a极为阴极,b极为阳极。从电解池a极区溶液中四甲基氢氧化铵[ ( CH )
3
NOH]浓度增大,也可推出( CH ) N+透过c膜向a电极移动,则a电极为阴极,c膜为阳膜;Cl-透过d膜向
4 3 4
右侧移动,则d膜为阴膜;Na+透过e膜向左侧移动,则e膜为阳膜。
A.由分析可知,光伏并网发电装置中,N型半导体为负极,P型半导体为正极,A正确;B.由分析可知,c、e为阳离子交换膜,d为阴离子交换膜,B错误;
C.b为阳极,溶液中的氢氧根离子失去电子生成氧气,电极反应为4OH--4e-=2H O+O↑,C正确;
2 2
D.182克四甲基氢氧化铵的物质的量为 ,则a极生成1mol氢气,b极生成0.5mol氧气,两
极共产生1.5mol气体,在标况下体积为33.6L,D正确;
故选B。
14.某温度下,25mL含KX和KY的混合溶液,用0.1000mol•L-1的硝酸银标准溶液对该混合液进行电位滴
定(在滴定过程中,随着滴定剂的不断加入,电极电位E不断发生变化,电极电位发生突跃时,说明滴定到
达终点)、获得电动势(E)和银硝酸银标准溶液体积(V)的电位滴定曲线如图所示。
已知:
I.Ag+与Y-反应过程为:①Ag++2Y- [AgY ]-、②[AgY ]-+Ag+ 2AgY↓。
2 2
II.该温度下,K (AgY)=2×10-16,K (AgX)=2×10-10
sp sp
III.Y-与H+的反应可以忽略。
下列说法不正确的是
A.若HY为弱酸,则从开始到A点,水的电离程度不断减小
B.原混合溶液中c(KX)=0.02000mol•L-1,c(KY)=0.03000mol•L-1
C.若反应①的平衡常数为K,反应②的平衡常数为K,则 =K (AgY)
1 2
D.将AgX和AgY的饱和溶液等体积混合,加入足量硝酸银溶液,析出固体AgX多于AgY
【答案】B
【详解】A.对于结构相似的物质,溶度积小的先生成沉淀,根据反应的方程式可知,A点生成[AgY ]-,B
2
点生成AgY,若HY为弱酸,则KY溶液中由于水解促进水的电离,滴加AgNO 溶液时,Y-浓度逐渐减
3
小,水的电离程度逐渐减小,故A正确;B.OA段发生的反应为Ag++2Y- [AgY ]-,AB段发生的反应为[AgY ]-+Ag+ 2AgY↓,所以
2 2
V=5.0,原溶液中n(Y-)=2 0.1000 mol/L 2.50 10-3 L=5 10-4mol,c(KY)=5 10-4mol÷0.025 L=0.02000
1
mol/L,BC段发生的反应为Ag++X-=AgX↓,BC段消耗的标准AgNO3溶液的体积为12.50mL-5.00ml=7.50
mL,则原溶液中n(X- )=0. 1000 mol/L 7.5 10-3 L=7.5 10-4mol,c(KX)= =0.03mol/L,故B
错误;
C.①的平衡常数为K= ,反应②的平衡常数为K= ,K K=
1 2 1 2
,Ag++Y-=AgY↓,K (AgY)=c(Ag+)c(Y-)= ,则 =K (AgY),故C正确;
sp
D.因为K (AgY)”“<”或“=”)。
②在210~270℃间, 的选择性随温度的升高而下降,请写出一条可能原因 。
(3)一定条件下,向刚性容器中充入物质的量之比为1:3的 和 发生上述反应。
①有利于提高甲醇平衡产率的条件是 (填标号)。
A.高温高压 B.低温高压 C.高温低压 D.低温低压
②达到平衡时 的转化率为20%, 的选择性为75%,则 的转化率为 ;反应b的压
强平衡常数 。(压强平衡常数为用分压表示的化学平衡常数,分压=总压×物质的量分数)
【答案】(1) -58 低温
(2) > 温度升高,催化剂的活性降低(或温度升高,更有利于反应b速率增大等)
(3) B 16.7%
【详解】(1)根据盖斯定律可知,反应 可由反应a-b得到,故 H =△H
3 1
△
-△H=−99 kJ•mol−1,故 H=△H +△H=-99kJ•mol−1+41 kJ•mol−1=-58 kJ•mol−1;反应a为放热的熵减反应,
2 1 3 2
则在低温下易自发进行;△
(2)①由上图可知,催化剂1的CO 的转化率和CHOH的选择性均优于催化剂2,故催化效果Cat.1>
2 3
Cat.2,故答案为:>;
②催化剂的活性强弱与温度有关,每一种催化剂均有最适宜的温度,在210~270℃间,CHOH的选择性随
3温度的升高而下降,可能原因温度升高,催化剂的活性降低,故答案为:温度升高,催化剂的活性降低;
(3)①由(1)分析可知,该反应为 H=-58 kJ•mol−1,正反应
1
△
是一个放热的气体体积减小的方向,降低温度、增大压强平衡正向移动,甲醇的产率增大,故低温高压有
利于提高甲醇平衡产率,故答案为:B。
②假设加入的CO 的物质的量为amol,则H 为3amol,反应a中CO 转化了xmol,反应b中CO 转化了
2 2 2 2
(0.2a-x)mol,根据三段式: ,
则
甲醇的选择性= ×100%= ,x=0.15amol,则 (H )=
2
;故平衡时CO 为0.8amol,H 为
2 2
3a-0.5a=2.5amol,CHOH为0.15amol,CO为0.05a,HO为0.2amol,则体系中,各物质的平衡分压为:P
3 2
(CO)= ,P (H )= ,P(CO)= ,P (H O)=
2 2 2
,故反应b的压强平衡常数Kp= 5×10-3,故答案为:16.7%;5×10-3。
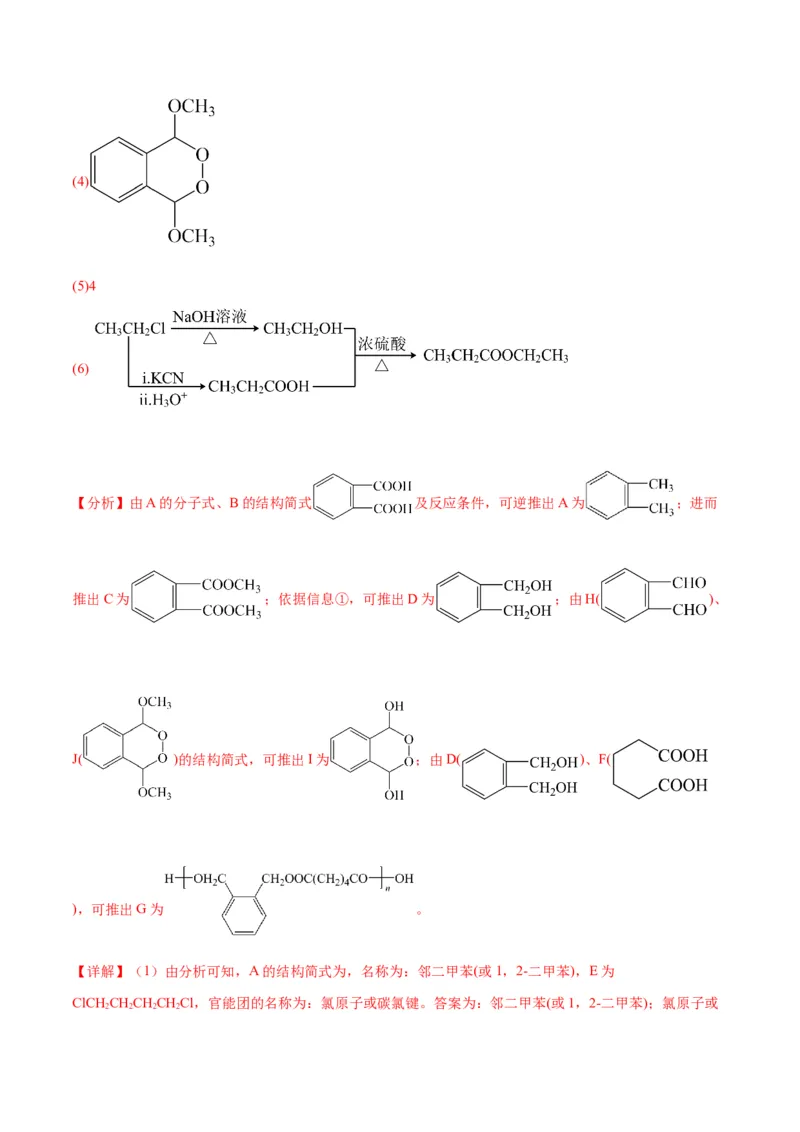
18.(15分)高聚物G是一种广泛用在生产生活中的合成纤维,由A与E为原料制备J和G的合成路线如
下:已知:①酯能被LiAlH 还原为醇
4
②
回答下列问题:
(1)A的名称为 ,E中官能团的名称为 。
(2)B生成C的化学方程式为 。
(3)D转化为H的反应类型为 。
(4)I的结构简式为 。
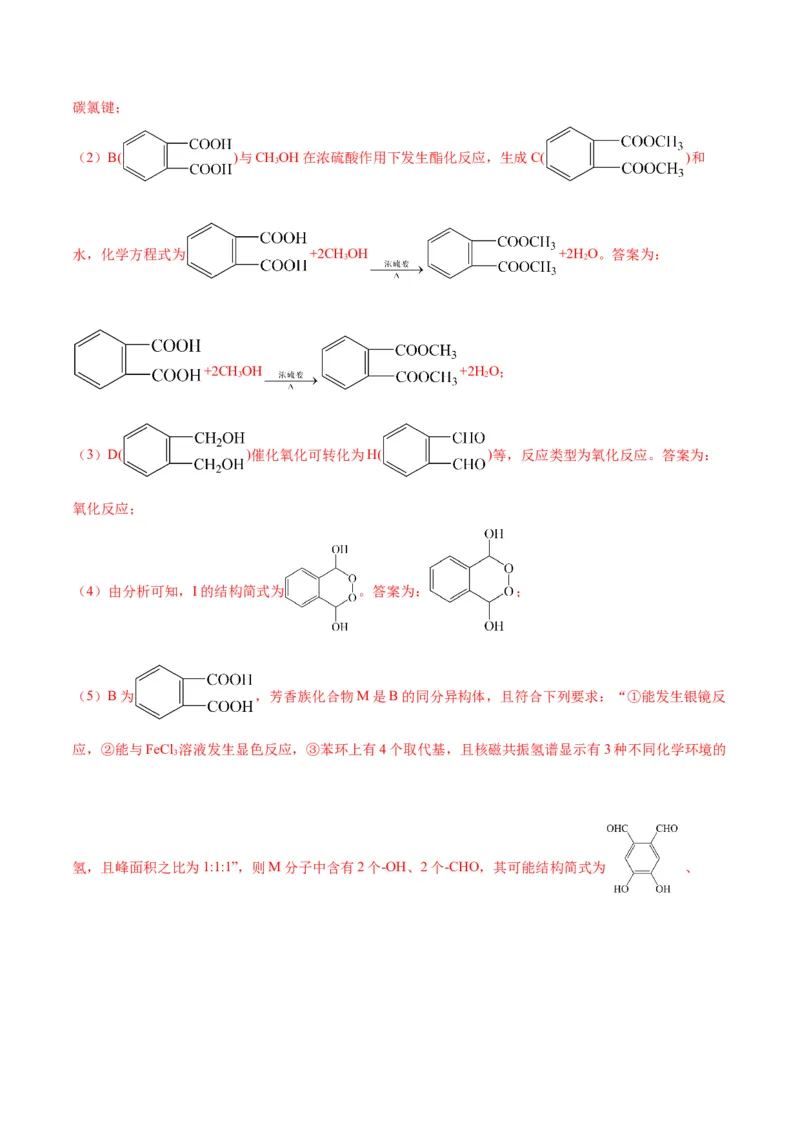
(5)芳香族化合物M是B的同分异构体,符合下列要求的M有 种(不考虑立体异构)。
①能发生银镜反应
②能与FeCl 溶液发生显色反应
3
③苯环上有4个取代基,且核磁共振氢谱显示有3种不同化学环境的氢,且峰面积之比为1:1:1
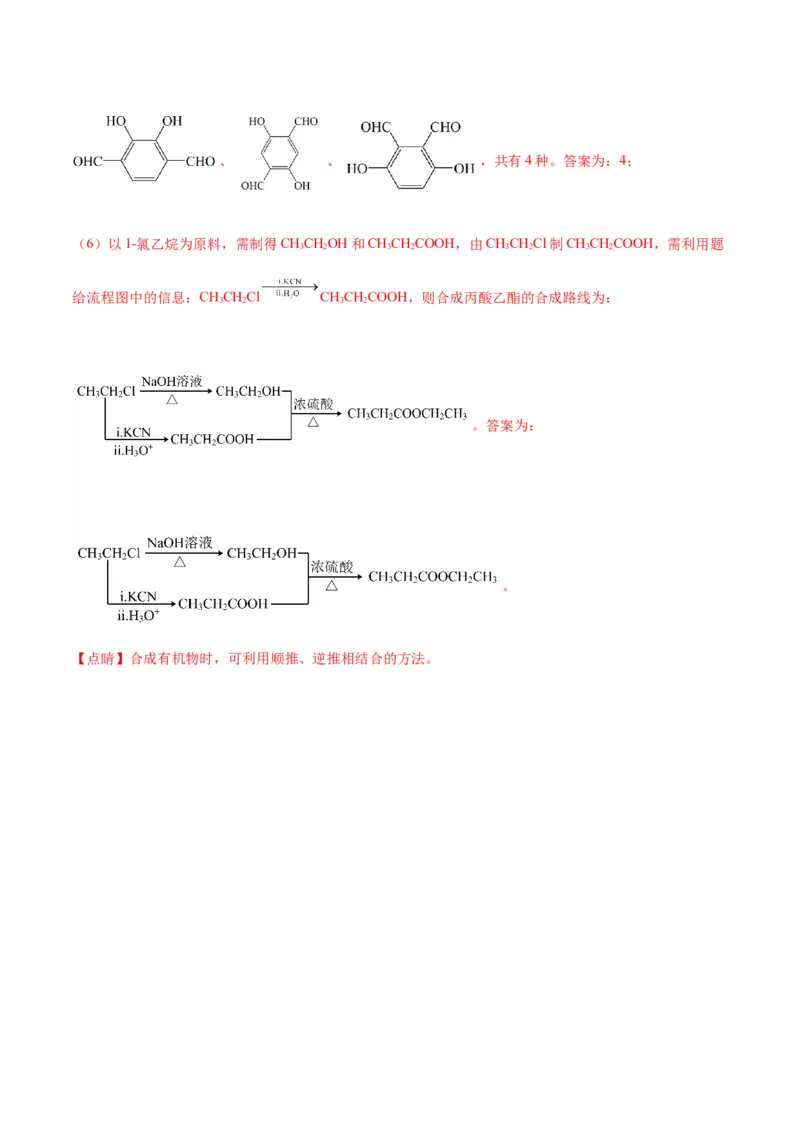
(6)请以1-氯乙烷为原料,写出合成丙酸乙酯的合成路线,其他无机试剂可以任选。 。
【答案】(1) 邻二甲苯(或1,2-二甲苯) 氯原子或碳氯键
(2) +2CH OH +2H O
3 2
(3)氧化反应(4)
(5)4
(6)
【分析】由A的分子式、B的结构简式 及反应条件,可逆推出A为 ;进而
推出C为 ;依据信息①,可推出D为 ;由H( )、
J( )的结构简式,可推出I为 ;由D( )、F(
),可推出G为 。
【详解】(1)由分析可知,A的结构简式为,名称为:邻二甲苯(或1,2-二甲苯),E为
ClCH CHCHCHCl,官能团的名称为:氯原子或碳氯键。答案为:邻二甲苯(或1,2-二甲苯);氯原子或
2 2 2 2碳氯键;
(2)B( )与CHOH在浓硫酸作用下发生酯化反应,生成C( )和
3
水,化学方程式为 +2CH OH +2H O。答案为:
3 2
+2CH OH +2H O;
3 2
(3)D( )催化氧化可转化为H( )等,反应类型为氧化反应。答案为:
氧化反应;
(4)由分析可知,I的结构简式为 。答案为: ;
(5)B为 ,芳香族化合物M是B的同分异构体,且符合下列要求:“①能发生银镜反
应,②能与FeCl 溶液发生显色反应,③苯环上有4个取代基,且核磁共振氢谱显示有3种不同化学环境的
3
氢,且峰面积之比为1:1:1”,则M分子中含有2个-OH、2个-CHO,其可能结构简式为 、、 、 ,共有4种。答案为:4;
(6)以1-氯乙烷为原料,需制得CHCHOH和CHCHCOOH,由CHCHCl制CHCHCOOH,需利用题
3 2 3 2 3 2 3 2
给流程图中的信息:CHCHCl CHCHCOOH,则合成丙酸乙酯的合成路线为:
3 2 3 2
。答案为:
。
【点睛】合成有机物时,可利用顺推、逆推相结合的方法。