文档内容
微专题 14 氢氧化亚铁、高铁酸盐的制备实验探究
近几年高考对以铁及其化合物为载体的知识考查较多,其中有关铁及其化合物
的实验的考查尤甚,有关铁及其化合物的实验涉及面甚广,物质类别方面有单
质,氧化物,氢氧化物和盐,性质方面有制备,检验,分离,提纯,性质验证
和实验探究等,其中氢氧化亚铁、高铁酸盐的制备实验探究是高考的重点。下面对氢
氧化亚铁、高铁酸盐的制备实验探究进行整理总结:
一、制备Fe(OH) 常用的三种方法
2
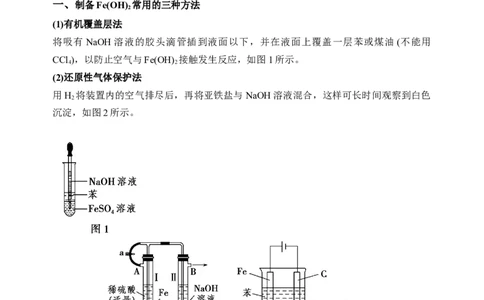
(1)有机覆盖层法
将吸有NaOH溶液的胶头滴管插到液面以下,并在液面上覆盖一层苯或煤油(不能用
CCl ),以防止空气与Fe(OH) 接触发生反应,如图1所示。
4 2
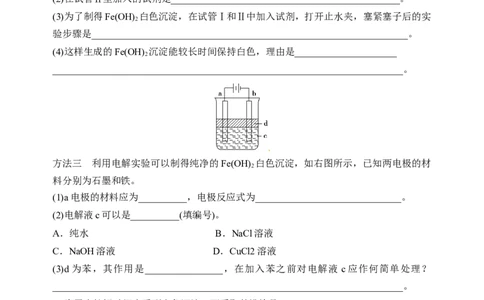
(2)还原性气体保护法
用H 将装置内的空气排尽后,再将亚铁盐与NaOH溶液混合,这样可长时间观察到白色
2
沉淀,如图2所示。
(3)电解法
用铁做阳极,电解NaCl(或NaOH)溶液,并在液面上覆盖苯(或煤油),如图3所示。
二、高铁酸盐的制备
工业制法工业上先制得高铁酸钠,然后在低温下向高铁酸钠溶液中加入一定量的KOH就可制得高
铁酸钾。制备高铁酸钠的两种方法的主要反应原理如下:
1.湿法制备:
2Fe(OH) +3NaClO-+4NaOH-=2Na FeO+3NaCl-+5H O;
3 2 4 2
2Fe(OH) +3ClO-+4OH-=2FeO 2-+3Cl-+5H O;
3 4 2
2.干法制备:
2FeSO +6Na O=2Na FeO+2Na O+2Na SO +O ↑
4 2 2 2 4 2 2 4 2
注意:干法制备的反应有时会写成以下形式
FeSO +2Na O=Na FeO++Na SO
4 2 2 2 4 2 4
这是反应条件不同而形成不同反应过程导致的。
3.其他制法:
Fe O+3Na O=2Na FeO+Na O
2 3 2 2 2 4 2
2Fe(NO ) + 16NaOH + 3Cl = 2Na FeO + 6NaCl + 6NaNO + 8H O
3 3 2 2 4 3 2
10NaOH+3Cl +2Fe(OH) ═2Na FeO+6NaCl+8HO;
2 3 2 4 2
电解时阳极发生氧化反应,电极反应方程式为Fe+8OH--6e-═FeO 2-+4H O;
4 2
【专题精练】
一、氢氧化亚铁的制备
1.用下面三种方法均可制得Fe(OH) 白色沉淀。
2
方法一 用不含Fe3+的FeSO 溶液与不含O 的蒸馏水配制的NaOH溶液反应制备。
4 2
(1)用硫酸亚铁晶体配制上述FeSO 溶液时还需要加入__________。
4
(2)除去蒸馏水中溶解的O 常采用________的方法。
2
(3)生成Fe(OH) 白色沉淀的操作是用长滴管吸取不含 O 的NaOH溶液,插入FeSO 溶液
2 2 4
液面下,再挤出NaOH溶液,这样操作的理由是_______________________________
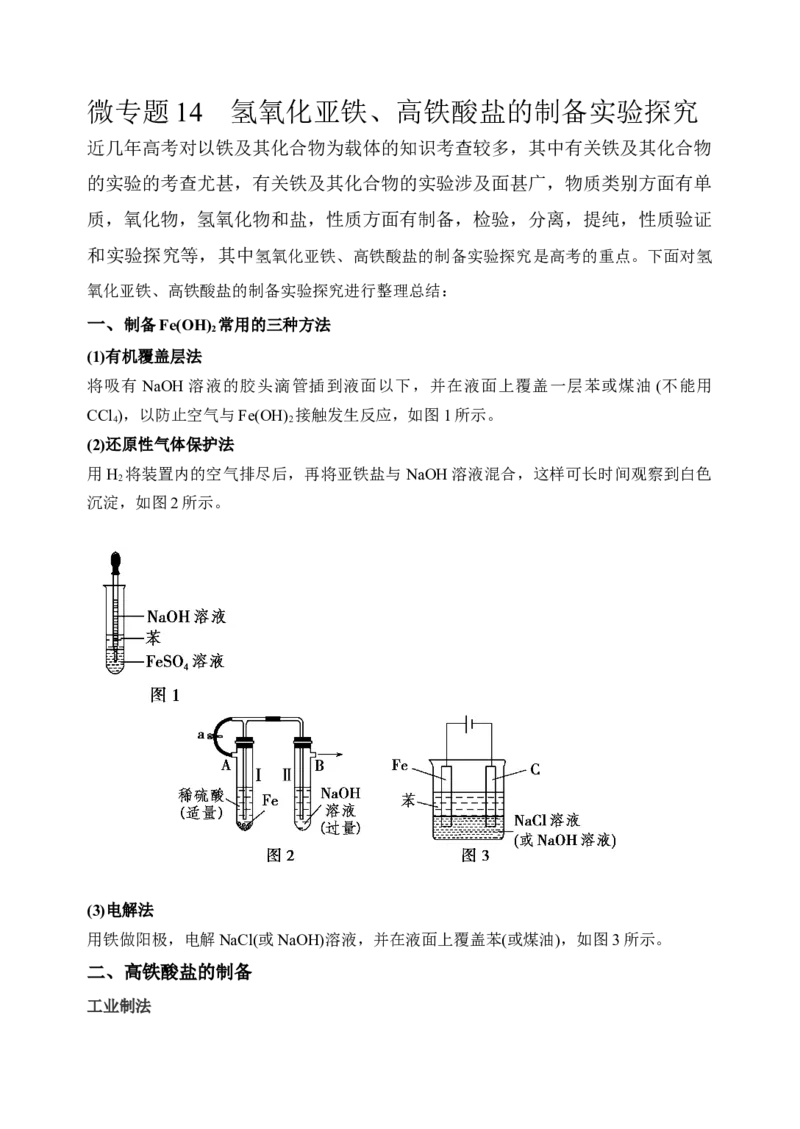
________________________________________________________________________。方法二 在如图所示的装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。
(1)在试管Ⅰ里加入的试剂是_____________________________________________。
(2)在试管Ⅱ里加入的试剂是_______________________________________________。
(3)为了制得Fe(OH) 白色沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实
2
验步骤是_________________________________________________________________。
(4)这样生成的Fe(OH) 沉淀能较长时间保持白色,理由是_____________________
2
________________________________________________________________________。
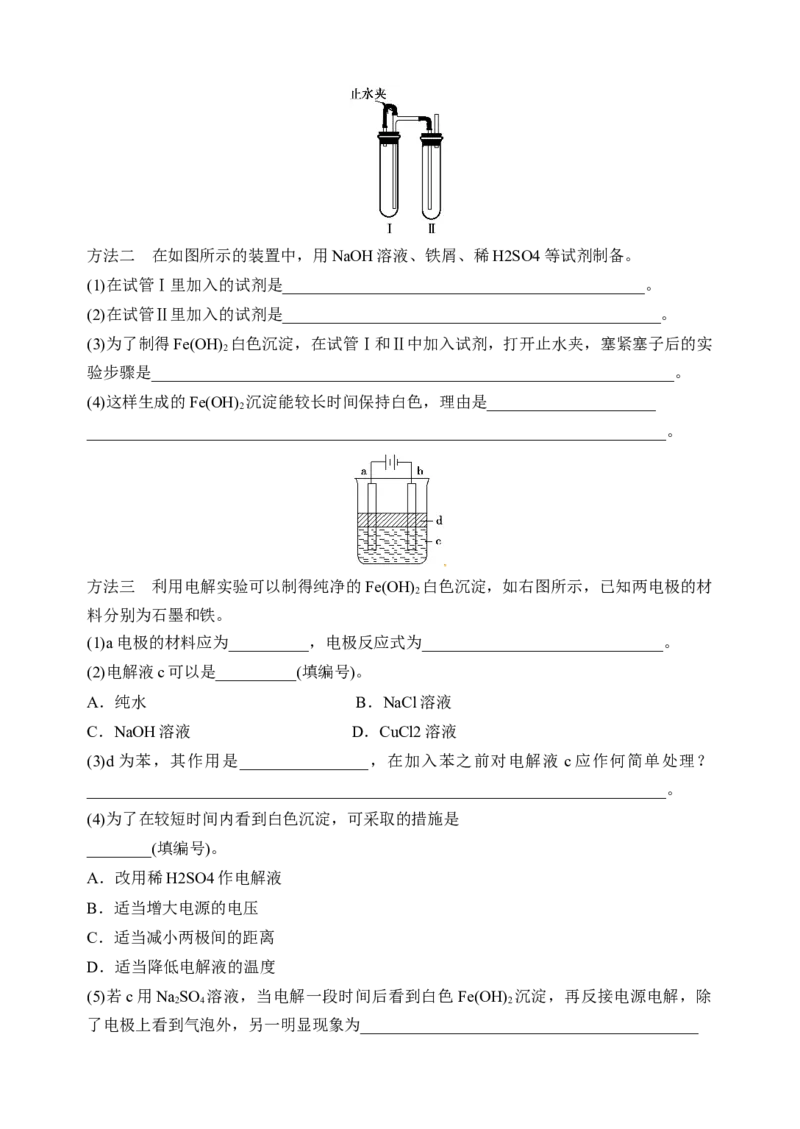
方法三 利用电解实验可以制得纯净的Fe(OH) 白色沉淀,如右图所示,已知两电极的材
2
料分别为石墨和铁。
(1)a电极的材料应为__________,电极反应式为______________________________。
(2)电解液c可以是__________(填编号)。
A.纯水 B.NaCl溶液
C.NaOH溶液 D.CuCl2溶液
(3)d为苯,其作用是________________,在加入苯之前对电解液 c应作何简单处理?
________________________________________________________________________。
(4)为了在较短时间内看到白色沉淀,可采取的措施是
________(填编号)。
A.改用稀H2SO4作电解液
B.适当增大电源的电压
C.适当减小两极间的距离
D.适当降低电解液的温度
(5)若c用NaSO 溶液,当电解一段时间后看到白色Fe(OH) 沉淀,再反接电源电解,除
2 4 2
了电极上看到气泡外,另一明显现象为__________________________________________________________________________________________________________________。
【答案】
方法一 (1)稀HSO 、铁屑 (2)煮沸 (3)避免生成的Fe(OH) 沉淀接触O 而被氧化
2 4 2 2
方法二 (1)稀HSO 和铁屑 (2)NaOH溶液 (3)检验试管Ⅱ出口处排出的H 的纯度,当
2 4 2
排出的H 已经纯净时再夹紧止水夹 (4)试管Ⅰ中反应生成的H 充满了试管Ⅰ和试管Ⅱ,
2 2
故外界O 不易进入
2
方法三 (1)Fe Fe-2e-===Fe2+ (2)BC
(3)隔绝空气,防止生成的Fe(OH) 被氧化
2
加热煮沸,排出溶解的O (4)BC (5)白色沉淀迅速变为灰绿色,最后变成红褐色
2
【解析】
方法一 Fe2+易水解,要加入稀HSO 防止其水解;Fe2+易被空气中的O 氧化,要加铁
2 4 2
粉,将被氧化生成的Fe3+还原成Fe2+。气体的溶解度是随温度升高而降低的,所以煮沸
后的蒸馏水中溶解的O 变少。
2
方法二 两支试管,试管Ⅱ是开口式,无法用产生的气体将试液压入试管Ⅰ中,所以制
取FeSO 应在试管Ⅰ中,而在试管Ⅱ中盛不含O 的NaOH溶液。当Fe与稀HSO 放入试
4 2 2 4
管Ⅰ后,产生的H 可以从试管Ⅰ内短管处排出,从而排尽试管Ⅰ内空气。再经过止水夹
2
通入试管Ⅱ中,排尽试管Ⅱ内空气。然后关闭止水夹,试管Ⅰ内产生的H 无法逸出,造
2
成管内压强增大,将试管Ⅰ内FeSO 溶液通过长导管压入试管Ⅱ内,在此过程中,液体都
4
处于H 环境,从而避免了被空气中的O 氧化,使得Fe(OH) 能保存更长时间。
2 2 2
方法三 电解时阳极Fe-2e-===Fe2+,阴极上2HO+2e-===H ↑+2OH-,或电解质溶液
2 2
能直接提供OH-。当Fe2+与OH-接触时Fe2++2OH-===Fe(OH) ↓,当电解液选用NaOH
2
溶液时,在阳极处立即产生白色沉淀,当选其他溶液时,只有迁移后两者相遇时才能产
生沉淀(大约在电池中部);当反接电源后,阳极4OH--4e-===2H O+O↑,产生的O 立
2 2 2
即把Fe(OH) 氧化为Fe(OH) 。
2 3
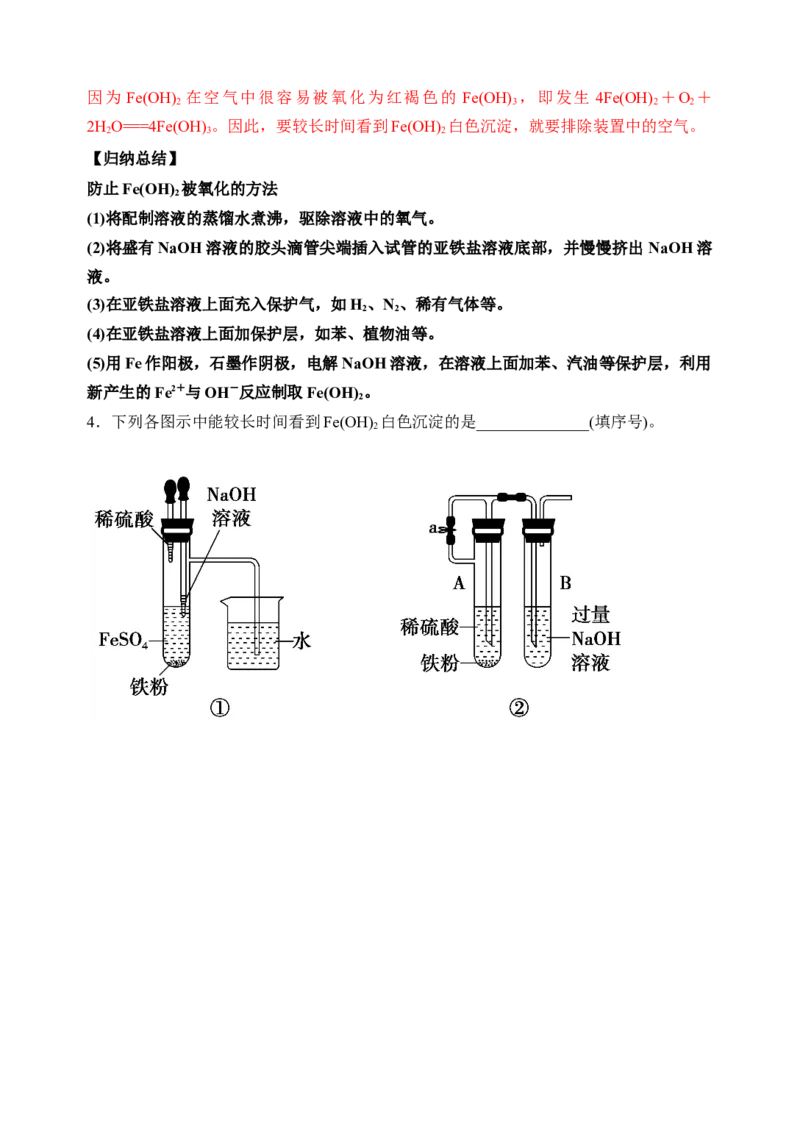
2.下列各图示中能较长时间看到Fe(OH) 白色沉淀的是________(填序号)。
2答案:①②③⑤
解析:因为Fe(OH) 在空气中很容易被氧化为红褐色的Fe(OH) ,即发生反应:4Fe(OH)
2 3 2
+O +2HO=== 4Fe(OH) 。因此要较长时间看到Fe(OH) 白色沉淀,就要排除装置中的氧
2 2 3 2
气或空气。①②原理一样,都是先用氢气将装置中的空气排尽,并使生成的Fe(OH) 处在
2
氢气的保护中;③的原理为铁作阳极产生Fe2+,与电解NaCl溶液产生的OH-结合生成
Fe(OH) ,且液面用汽油保护,能防止空气进入;⑤中液面加苯阻止了空气进入;④由于
2
带入空气中的氧气,能迅速将Fe(OH) 氧化,因而不能较长时间看到白色沉淀。
2
3.如下图所示,此装置可用来制取和观察Fe(OH) 在空气中被氧化的颜色变化。实验时
2
必须使用铁屑和6 mol·L-1的硫酸,其他试剂任选。填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中应预先加入的药品是__________。A中反应的离子
方程式是____________。
(2)实验开始时,先将止水夹a____________(填“打开”或“关闭”)。
(3)简述生成Fe(OH) 的操作过程________________________。
2
(4)实验完毕,打开 b 处止水夹,放入一部分空气,此时 B 瓶中发生的反应为
___________________________。
答案:(1)铁屑 Fe+2H+===Fe2++H↑
2
(2)打开
(3)待A装置反应一段时间后关闭止水夹a,将FeSO 溶液压入B中进行反应
4
(4)4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
解析:Fe+2H+===Fe2++H↑,产生的H 将Fe2+压入B中,Fe2++2OH-===Fe(OH) ↓;
2 2 2因为 Fe(OH) 在空气中很容易被氧化为红褐色的 Fe(OH) ,即发生 4Fe(OH) +O +
2 3 2 2
2HO===4Fe(OH) 。因此,要较长时间看到Fe(OH) 白色沉淀,就要排除装置中的空气。
2 3 2
【归纳总结】
防止Fe(OH) 被氧化的方法
2
(1)将配制溶液的蒸馏水煮沸,驱除溶液中的氧气。
(2)将盛有NaOH溶液的胶头滴管尖端插入试管的亚铁盐溶液底部,并慢慢挤出NaOH溶
液。
(3)在亚铁盐溶液上面充入保护气,如H、N、稀有气体等。
2 2
(4)在亚铁盐溶液上面加保护层,如苯、植物油等。
(5)用Fe作阳极,石墨作阴极,电解NaOH溶液,在溶液上面加苯、汽油等保护层,利用
新产生的Fe2+与OH-反应制取Fe(OH) 。
2
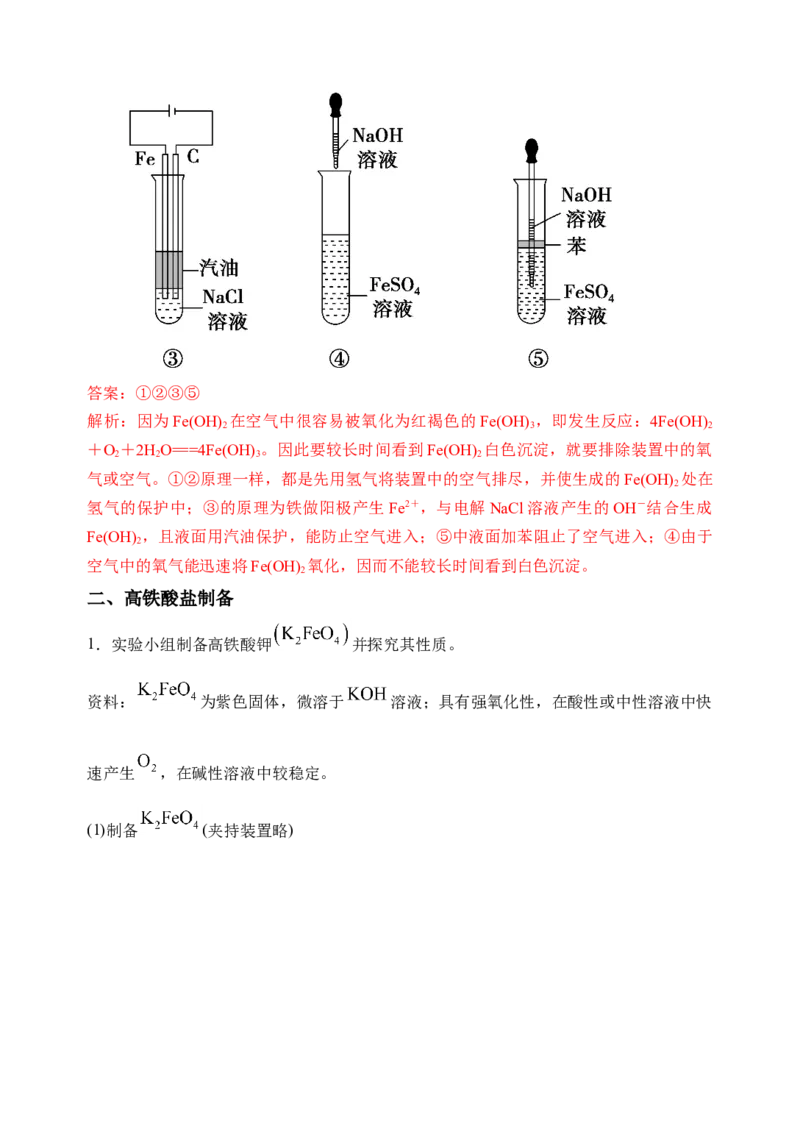
4.下列各图示中能较长时间看到Fe(OH) 白色沉淀的是______________(填序号)。
2答案:①②③⑤
解析:因为Fe(OH) 在空气中很容易被氧化为红褐色的Fe(OH) ,即发生反应:4Fe(OH)
2 3 2
+O +2HO===4Fe(OH) 。因此要较长时间看到Fe(OH) 白色沉淀,就要排除装置中的氧
2 2 3 2
气或空气。①②原理一样,都是先用氢气将装置中的空气排尽,并使生成的Fe(OH) 处在
2
氢气的保护中;③的原理为铁做阳极产生Fe2+,与电解NaCl溶液产生的OH-结合生成
Fe(OH) ,且液面用汽油保护,能防止空气进入;⑤中液面加苯阻止了空气进入;④由于
2
空气中的氧气能迅速将Fe(OH) 氧化,因而不能较长时间看到白色沉淀。
2
二、高铁酸盐制备
1.实验小组制备高铁酸钾 并探究其性质。
资料: 为紫色固体,微溶于 溶液;具有强氧化性,在酸性或中性溶液中快
速产生 ,在碱性溶液中较稳定。
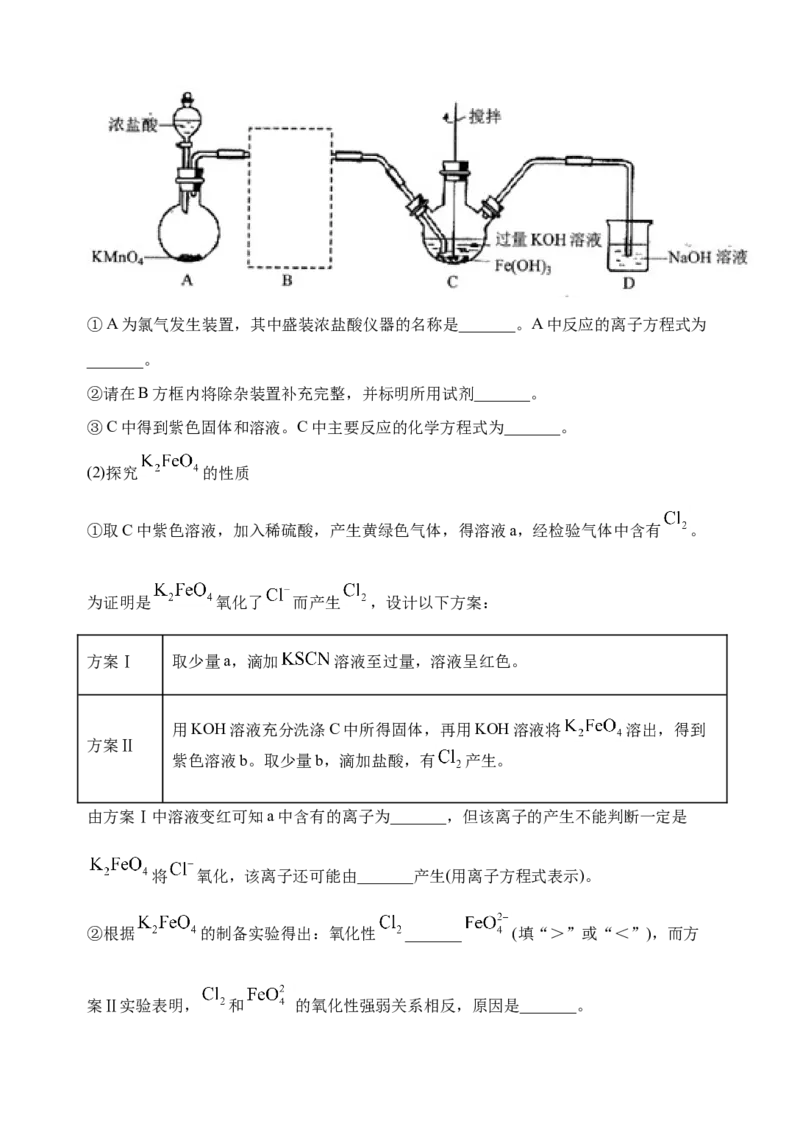
(1)制备 (夹持装置略)①A为氯气发生装置,其中盛装浓盐酸仪器的名称是_______。A中反应的离子方程式为
_______。
②请在B方框内将除杂装置补充完整,并标明所用试剂_______。
③C中得到紫色固体和溶液。C中主要反应的化学方程式为_______。
(2)探究 的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有 。
为证明是 氧化了 而产生 ,设计以下方案:
方案Ⅰ 取少量a,滴加 溶液至过量,溶液呈红色。
用KOH溶液充分洗涤C中所得固体,再用KOH溶液将 溶出,得到
方案Ⅱ
紫色溶液b。取少量b,滴加盐酸,有 产生。
由方案Ⅰ中溶液变红可知a中含有的离子为_______,但该离子的产生不能判断一定是
将 氧化,该离子还可能由_______产生(用离子方程式表示)。
②根据 的制备实验得出:氧化性 _______ (填“>”或“<”),而方
案Ⅱ实验表明, 和 的氧化性强弱关系相反,原因是_______。③资料表明,酸性溶液中的氧化性 ,验证实验如下:将溶液b滴入
和足量 的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
_______。
【答案】(1) ①分液漏斗 ②
③
(2) ①Fe3+ ② > 溶液的酸碱性不同
③ 能, 在过量酸的作用下完全转化为Fe3+和O,溶液浅紫色一定是 的颜
2
色。
【分析】
装置A制备氯气,装置B净化氯气,通入装置C中与氢氧化铁反应制备高铁酸钾,装置
D用来吸收尾气,据此解答。
【解析】
(1)①A为氯气发生装置,其中盛装浓盐酸仪器的名称是分液漏斗。高锰酸钾溶液和浓盐
酸反应生成氯化锰、氯化钾、氯气和水,故A中反应的离子方程式为:
。②制备的氯气中含有少量挥发出来的HCl气体,用饱和食盐水除去氯气中的HCl气体,
则除杂装置为: 。
③C中得到紫色固体为高铁酸钾,氯气与氢氧化钾和氢氧化铁反应生成高铁酸钾、氯化
钾和水,反应的化学方程式为:
。
(2)①方案Ⅰ中,滴加KSCN溶液至过量,溶液呈红色可知a中含有Fe3+,Fe3+产生不能判
断一定是 将Cl−氧化,还可能是在酸性环境下高铁酸钾发生歧化反应生成Fe3+,
其离子反应方程式为: 。
②制备 的反应为: ,
氯气作氧化剂,其氧化性 > ,而与方案Ⅱ实验的Cl 和 的氧化性强弱关
2
系相反的原因是溶液的酸碱性不同。
③该实验现象能证明氧化性: ,因为 在过量酸的作用下完全转化
为Fe3+和O,溶液浅紫色一定是 的颜色。
2
2.高铁酸盐是优良的多功能水处理剂。KFeO 为紫色固体,可溶于水,微溶于浓KOH
2 4
溶液,难溶于有机物;在0~5℃、强碱性溶液中比较稳定,在酸性、中性溶液中易分解
放出O。某实验小组制备高铁酸钾(K FeO)并测定产品纯度。回答下列问题:
2 2 4I.制备KFeO:装置如下图所示,夹持、加热等装置略。
2 4
(1)仪器a的名称是_______,装置B中除杂质所用试剂是_______。
(2)A中发生反应的离子方程式为_______。
(3)C中反应为放热反应,而反应温度须控制在0~5℃,采用的控温方法为__,反应中
KOH必须过量的原因是__。
(4)写出C中总反应的离子方程式:_______。C中混合物经重结晶、有机物洗涤纯化、真
空干燥,得到高铁酸钾晶体。
II.K FeO 产品纯度的测定
2 4
准确称取1.00 g制得的晶体,配成250 mL溶液,准确量取25.00 mL K FeO 溶液放入锥形
2 4
瓶,加入足量CrCl 和NaOH溶液,振荡,再加入稀硫酸酸化后得Fe3+和 ,滴入几
3
滴二苯胺磺酸钠作指示剂,用0.0500 mol/L(NH )Fe(SO ) 标准溶液滴定至终点(溶液显浅
4 2 4 2
紫红色),平行测定三次,平均消耗(NH )Fe(SO ) 标准溶液28.00mL。
4 2 4 2
(5)根据以上数据,样品中KFeO 的质量分数为_______。若(NH )Fe(SO ) 标准溶液部分
2 4 4 2 4 2
变质,会使测定结果_______(填“偏高”“偏低”或“无影响”)。
【答案】(1)圆底烧瓶 饱和食盐水 (2)2 Cl-+MnO+4H+ Mn2++Cl↑+2H O (3)
2 2 2
冰水浴 KFeO 在强碱性溶液中比较稳定 (4)3Cl +2Fe3++16OH-=2 +6Cl-+8H O
2 4 2 2
(5) 92.4% 偏高
【分析】根据装置图:首先制得氯气,氯气中混有氯化氢,根据题目信息:KFeO 强碱性溶液中
2 4
比较稳定,故须用饱和的食盐水除去氯化氢,再通入三氯化铁和过量的氢氧化钾混合溶
液中生成KFeO,氯气是有毒气体,需要氢氧化钠溶液吸收尾气。
2 4
【解析】
(1)仪器a是圆底烧瓶;装置B是为了除去氯中的氯化氢,则装置B中所用试剂是饱和食
盐水;
(2)装置A中,MnO 和浓盐酸在加热的条件下反应生成氯化锰、氯气和水,离子方程式为
2
MnO +4H+ Mn2++Cl↑+2H O;
2 2 2
(3)C中反应为放热反应,而反应温度须控制在0~5℃,采用的控温方法为冰水浴降温;
由于KFeO 在强碱性溶液中比较稳定,故反应中KOH必须过量;
2 4
(4)装置C中Cl 和FeCl 在碱性条件下反应生成 和KCl和水,离子方程式为:
2 3
3Cl+2Fe3++16OH-=2 +6Cl-+8H O;
2 2
(5)足量CrCl 和NaOH溶液形成CrO2-,CrO2-+ +2H O=Fe(OH) ↓+CrO 2-+OH-,6Fe2+
3 2 3 4
+ +14H+=6Fe3++2Cr3++7H O,得到定量关系为:
2
,则n=
,250ml溶液中含有 mol × = 测定该样品中KFeO 的质量分数为 ;若(NH )Fe(SO ) 标准溶
2 4 4 2 4 2
液部分变质,所耗(NH )Fe(SO ) 的体积偏大,带入关系式的数据偏大,使测定结果偏高。
4 2 4 2
3.高铁酸钾KFeO 是倍受关注的一类新型、高效、无毒的多功能水处理剂。实验室用如
2 4
图所示装置先制备氯气,再制备KClO溶液,并通过KClO溶液与Fe(NO ) 溶液的反应制
3 3
备高效水处理剂KFeO。
2 4
(1)装置D的作用是_______。
(2)实验过程中,装置A观察到的实验现象是_______。
(3)装置C中发生的反应方程式为_______。
(4)若要制备KFeO9.9 kg,计算所需Fe(NO ) 的质量______(假设铁元素完全转化到产物
2 4 3 3
中)
【答案】(1)吸收多余的Cl,防止污染环境 (2) 烧瓶中充满黄绿色气体
2
(3)2KOH+Cl =KCl+KClO+H O (4) 9.0kg
2 2
【分析】
根据实验装置图可知,A装置中用二氧化锰与浓盐酸共热反应制得氯气,氯气中有挥发
出的来的氯化氢,所以B装置中饱和食盐水是除去氯气中的氯化氢,装置C中用氯气与
氢氧化钾溶液应制得次氯酸钾,反应的尾气氯气用氢氧化钾吸收,据此分析解题。
【解析】(1)由于Cl 有毒,故多余的Cl 不能直接排放到空气中,故装置D的作用是吸收多余的
2 2
Cl,防止污染环境,故答案为:吸收多余的Cl,防止污染环境;
2 2
(2)由分析可知,实验过程中,装置A中有Cl 生成,故可观察到的实验现象是烧瓶中充满
2
黄绿色气体,故答案为:烧瓶中充满黄绿色气体;
(3)由分析可知,装置C中主要先制备KClO,故发生的反应方程式为
2KOH+Cl =KCl+KClO+H O,故答案为:2KOH+Cl =KCl+KClO+H O;
2 2 2 2
(4)根据铁元素守恒可计算出若要制备KFeO9.9 kg,所需Fe(NO ) 的质量为:
2 4 3 3
,50mol×180g·mol-1=9000g=9.0kg,故答案为:9.0kg。