文档内容
微专题20 海水资源的综合利用(提取溴和碘)
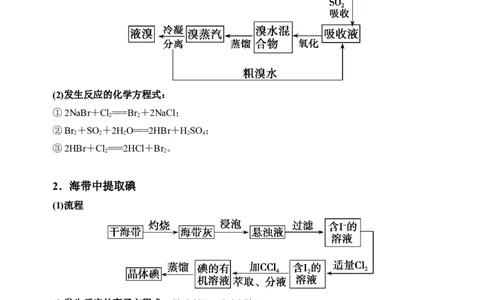
1.海水提取溴
(1)流程
(2)发生反应的化学方程式:
①2NaBr+Cl===Br +2NaCl;
2 2
②Br +SO +2HO===2HBr+HSO ;
2 2 2 2 4
③2HBr+Cl===2HCl+Br 。
2 2
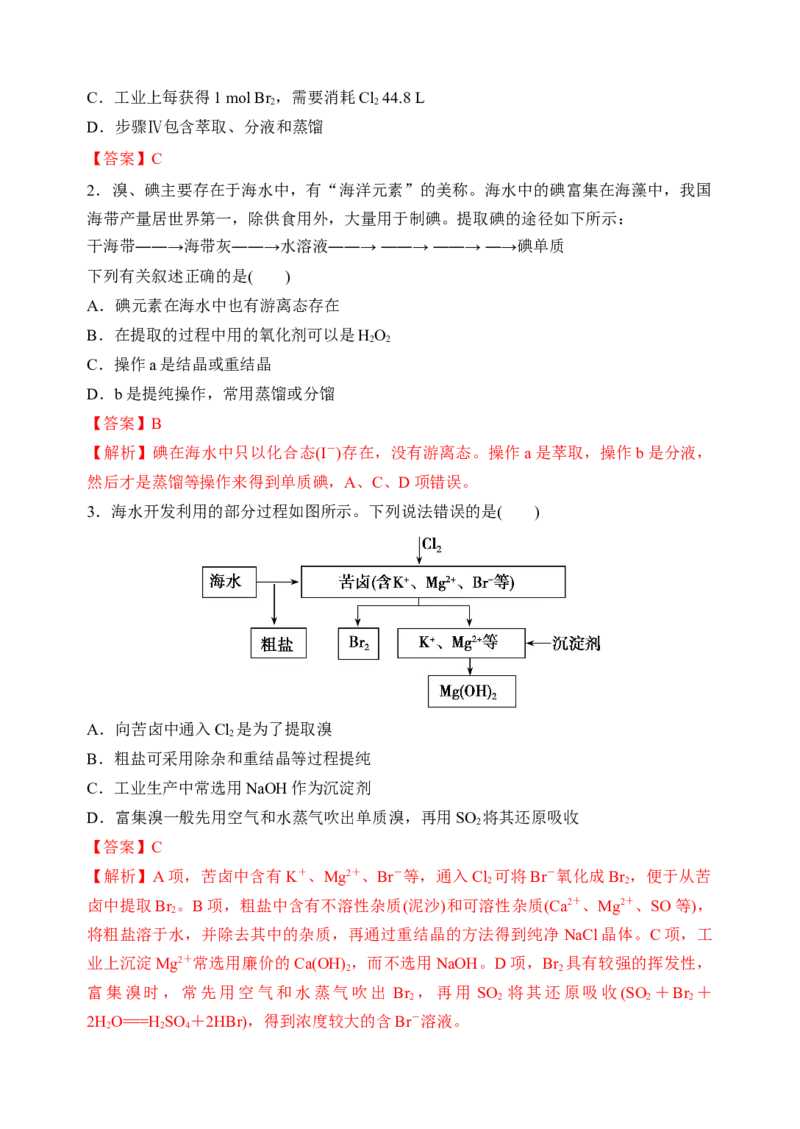
2.海带中提取碘
(1)流程
(2)发生反应的离子方程式:Cl+2I-===I +2Cl-。
2 2
【专题精练】
1.从淡化海水中提取溴的流程如下:
―――→――――――――→――――→→…→
下列有关说法不正确的是( )
A.X试剂可用NaSO 饱和溶液
2 3
B.步骤Ⅲ的离子反应:2Br-+Cl===2Cl-+Br
2 2C.工业上每获得1 mol Br ,需要消耗Cl 44.8 L
2 2
D.步骤Ⅳ包含萃取、分液和蒸馏
【答案】C
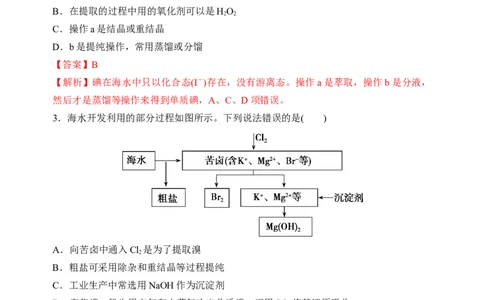
2.溴、碘主要存在于海水中,有“海洋元素”的美称。海水中的碘富集在海藻中,我国
海带产量居世界第一,除供食用外,大量用于制碘。提取碘的途径如下所示:
干海带――→海带灰――→水溶液――→ ――→ ――→ ―→碘单质
下列有关叙述正确的是( )
A.碘元素在海水中也有游离态存在
B.在提取的过程中用的氧化剂可以是HO
2 2
C.操作a是结晶或重结晶
D.b是提纯操作,常用蒸馏或分馏
【答案】B
【解析】碘在海水中只以化合态(I-)存在,没有游离态。操作a是萃取,操作b是分液,
然后才是蒸馏等操作来得到单质碘,A、C、D项错误。
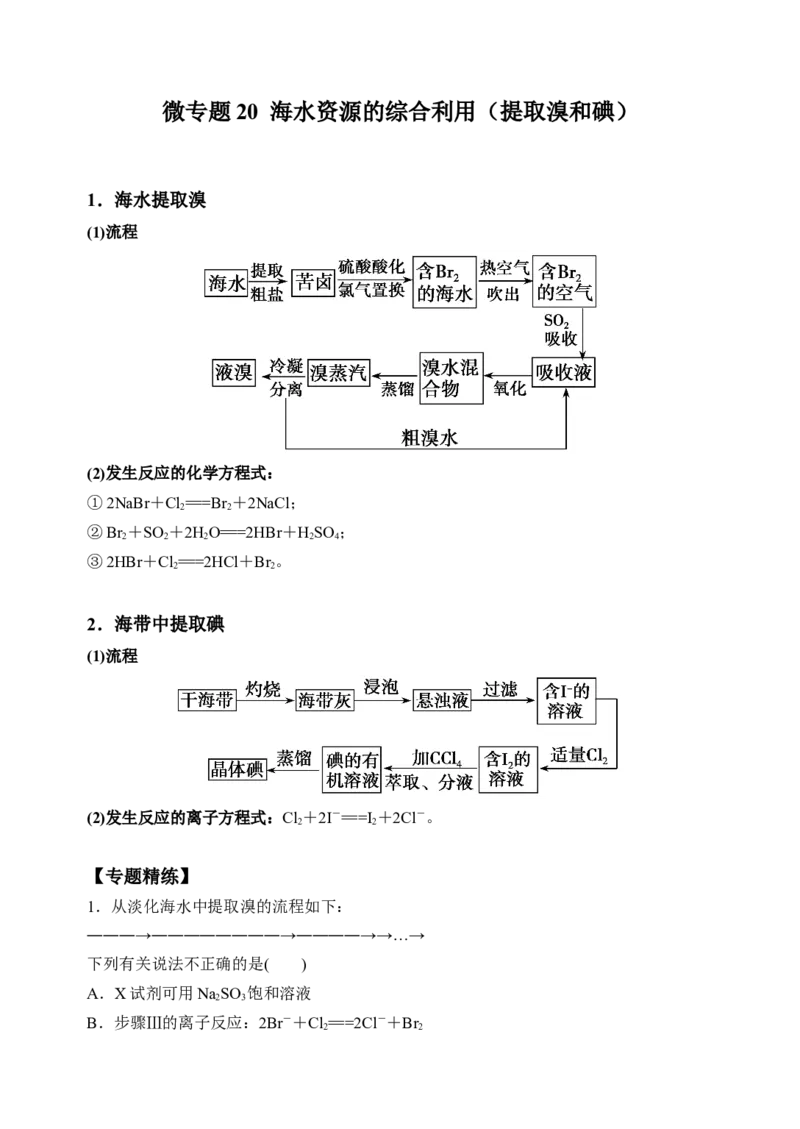
3.海水开发利用的部分过程如图所示。下列说法错误的是( )
A.向苦卤中通入Cl 是为了提取溴
2
B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产中常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO 将其还原吸收
2
【答案】C
【解析】A项,苦卤中含有K+、Mg2+、Br-等,通入Cl 可将Br-氧化成Br ,便于从苦
2 2
卤中提取Br 。B项,粗盐中含有不溶性杂质(泥沙)和可溶性杂质(Ca2+、Mg2+、SO等),
2
将粗盐溶于水,并除去其中的杂质,再通过重结晶的方法得到纯净NaCl晶体。C项,工
业上沉淀Mg2+常选用廉价的Ca(OH) ,而不选用NaOH。D项,Br 具有较强的挥发性,
2 2
富集溴时,常先用空气和水蒸气吹出 Br ,再用 SO 将其还原吸收(SO +Br +
2 2 2 2
2HO===H SO +2HBr),得到浓度较大的含Br-溶液。
2 2 44.溴主要以Br-形式存在于海水中,海水呈弱碱性。工业上制备Br 的操作步骤为
2
①一定条件下,将Cl 通入浓缩的海水中,生成Br
2 2
②利用热空气将Br 吹出,并用浓NaCO 溶液吸收,生成NaBr、NaBrO 等
2 2 3 3
③用硫酸酸化步骤②得到的混合物
完成下列填空:
(1)Cl 氧化Br-应在________条件下进行,目的是避免_______________。
2
(2)Br 可用热空气吹出,其原因是_______________。
2
(3)写出步骤③所发生的化学反应方程式:_________________。
用硫酸而不用盐酸酸化的原因可能是_____________________。
步骤②的产品有时运输到目的地后再酸化,主要是因为__________________________。
【答案】(1)酸性 氯气与碱发生歧化反应(或Br 歧化)
2
(2)Br 易挥发(或Br 沸点低)
2 2
(3)5NaBr+NaBrO +3HSO ===3Br +3NaSO +3HO 防止在酸性条件下,溴酸钠将Cl-
3 2 4 2 2 4 2
氧化为氯气,影响生成溴的纯度 溴具有强氧化性(或强腐蚀性)
4.从海带中提取碘单质,成熟的工艺流程如下。下列关于海水制碘的说法,不正确的是(
)
A.实验室在蒸发皿中灼烧干海带,并且用玻璃棒搅拌
B.在含I-的滤液中加入稀硫酸和双氧水后,碘元素发生氧化反应
C.在碘水中加入几滴淀粉溶液,溶液变蓝色
D.在碘水中加入CCl 得到I 的CCl 溶液,该操作为萃取
4 2 4
【答案】A
【解析】选A。灼烧干海带应在坩埚中进行。
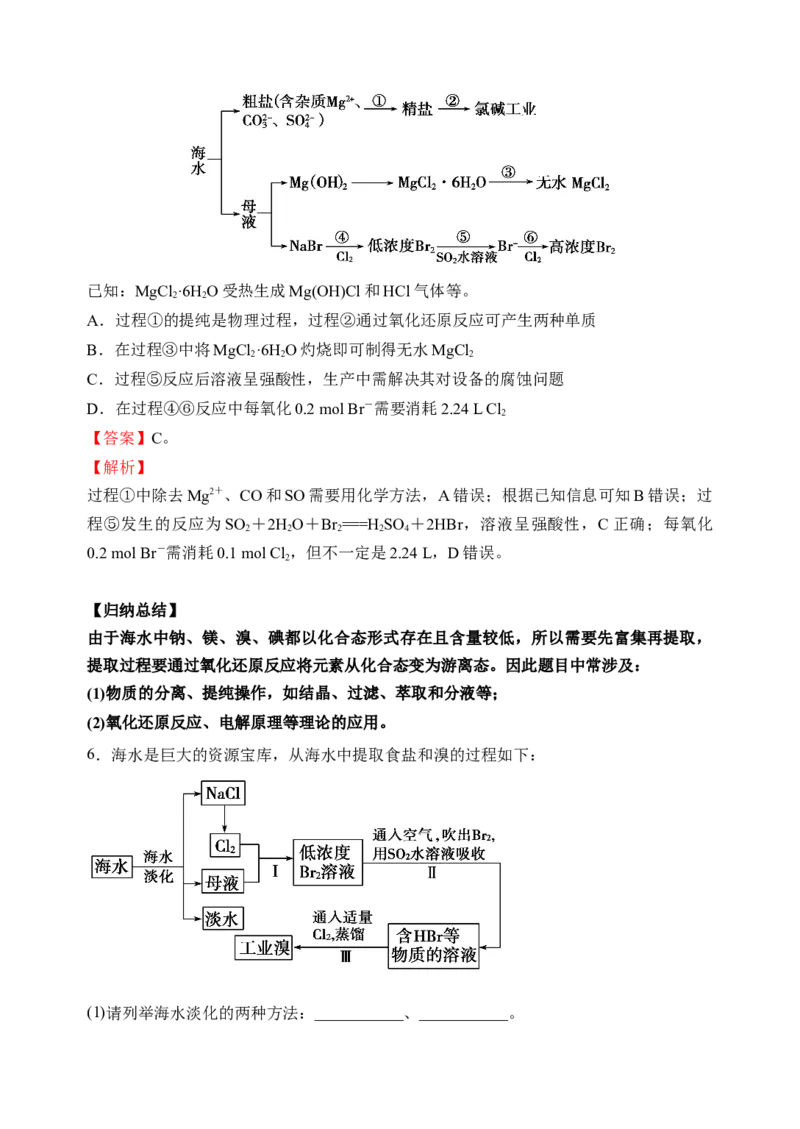
5.根据下图海水综合利用的工艺流程图,判断下列说法正确的是( )已知:MgCl ·6H O受热生成Mg(OH)Cl和HCl气体等。
2 2
A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生两种单质
B.在过程③中将MgCl ·6H O灼烧即可制得无水MgCl
2 2 2
C.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题
D.在过程④⑥反应中每氧化0.2 mol Br-需要消耗2.24 L Cl
2
【答案】C。
【解析】
过程①中除去Mg2+、CO和SO需要用化学方法,A错误;根据已知信息可知B错误;过
程⑤发生的反应为SO +2HO+Br ===H SO +2HBr,溶液呈强酸性,C正确;每氧化
2 2 2 2 4
0.2 mol Br-需消耗0.1 mol Cl ,但不一定是2.24 L,D错误。
2
【归纳总结】
由于海水中钠、镁、溴、碘都以化合态形式存在且含量较低,所以需要先富集再提取,
提取过程要通过氧化还原反应将元素从化合态变为游离态。因此题目中常涉及:
(1)物质的分离、提纯操作,如结晶、过滤、萃取和分液等;
(2)氧化还原反应、电解原理等理论的应用。
6.海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
(1)请列举海水淡化的两种方法:___________、___________。(2)步骤Ⅰ中已获得Br ,步骤Ⅱ中又将Br 还原为Br-,其目的是___________。
2 2
(3)步骤Ⅱ用SO 水溶液吸收Br ,吸收率可达95%,有关反应的离子方程式为
2 2
___________。
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br 的
2
沸点为59℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:
请你参与分析讨论:
①图中仪器B的名称是___________;
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是___________;
③实验装置气密性良好,要达到提纯溴的目的,操作中控制温度计b为 ___________℃
④C中溶液颜色为 ___________ ,为除去该产物中残留的Cl 可向其中加入NaBr溶液,
2
反应离子方程式为___________。
【答案】(1)蒸馏法、电渗析法、离子交换法及其他合理答案中的任意两种 (2) 富集溴元
素 (3) Br +SO +2HO=4H++SO +2Br- (4) ① 冷凝管 ② Br 腐蚀橡胶 ③ 59
2 2 2 2
④ 红棕色 2Br-+ Cl = Br+2Cl-
2 2
【分析】
利用海水淡化常见的方法主要有蒸馏法、电渗析法、离子交换法,氯碱工业得到的氯气
与溴离子反应生成低浓度的Br 溶液,此时蒸馏会消耗大量能源,成本较高,因此用热空
2
气吹出,用二氧化硫水溶液吸收得到硫酸和氢溴酸,再用氯气反应,得到较大浓度的Br
2溶液,再蒸馏得到Br ,蒸馏时要注意Br 的沸点为59 ℃,微溶于水,有毒并有强腐蚀性,
2 2
因此控制好温度,整个过程中不能使用橡皮管。
【解析】
(1)从海水中取淡水,有蒸留法、反渗透法、水合物法、溶剂萃取法和冰冻法,除去海水
中的盐分,有电渗拆法、离子交换法和压渗法,故答案为蒸馏法、电渗析法、离子交换
法等中的任意两种;
(2)虽然步骤Ⅰ中已获得Br ,但此时溴的浓度较低,提取时消耗过多的原料和能源,步骤
2
Ⅱ中又将Br 还原为Br-,转化为HBr后易被氧化剂氯气氧化为溴单质,用于富集溴元素,
2
故答案为富集溴元素;
(3)二氧化硫具有还原性,可以还原溴生成溴离子,自身被氧化成硫酸,根据电子守恒和
元素守恒可得化学方程式为:离子方程式为Br +SO +2HO=4H++SO +2Br-,故答案
2 2 2
为Br +SO +2HO=4H++SO +2Br-;
2 2 2
(4)①由装置图可知,提纯溴利用的原理是蒸馏,仪器B为冷凝管,故答案为冷凝管;
②溴单质是一种强氧化剂,易腐蚀橡胶制品,所以整套装置不能用橡胶塞和橡胶管,故
答案为Br 腐蚀橡胶;
2
③要达到提纯溴的目的,操作中应控制的关键条件是把温度控制在溴的沸点59°C,并收
集该温度下的馏分,故答案为:59;
④C中收集到的是液溴,其颜色为深红棕色。为除去液溴中残留的少量Cl,向其中加入
2
NaBr溶液,Cl 和NaBr反应生成NaCl和Br ,离子方程式为:2Br-+ Cl = Br+2Cl-。
2 2 2 2
7.在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用以下所给的工艺流程生产
单质碘:(1)碘位于元素周期表中的第______周期______族。
(2)步骤③加Fe的目的是______。
(3)写出步骤④的化学方程式:______。
(4)上述生产流程中,可以利用的副产物是______,考虑原料循环利用,若将该副产物制
成生产所需的试剂,先后还需加入______来进行处理。
(5)甲物质见光易变黑,其原因是(化学方程式表示):______。
(6)可采用如图所示的简易装置进行第⑤步操作,在扎有小孔的滤纸上有固体凝结,该分
离提纯方法的名称是______。
【答案】(1)五 ⅦA (2) 使碘化银转化为碘化亚铁(FeI )和单质银 (3) 2FeI +3Cl=2I
2 2 2 2
+2FeCl (4) Ag 稀硫酸、稀硝酸 (5) 2AgI 2Ag+I (6) 升华
3 2
【分析】
该实验的目的,是从富碘卤水中提取I。具体操作为:先将卤水中的碘元素转化为AgI,
2
再用Fe还原制得混有Fe的Ag及含有FeI 的乙溶液,再用过量Cl 将其氧化为I 和
2 2 2
FeCl ,最后将粗碘提纯。
3
【解析】
(1)在元素周期表中,碘与氟同主族且位于溴的下方,所以位于第五周期ⅦA族。答案为:
五;ⅦA;
(2)步骤③加Fe,是为了与AgI反应,将碘元素转化为可溶性物质,所以目的是使碘化银
转化为碘化亚铁(FeI )和单质银。答案为:使碘化银转化为碘化亚铁(FeI )和单质银;
2 2
(3)步骤④中,Cl 与FeI 反应,生成I 和FeCl ,化学方程式:2FeI+3Cl=2I +2FeCl 。
2 2 2 3 2 2 2 3答案为:2FeI+3Cl=2I +2FeCl ;
2 2 2 3
(4)上述生产流程中,可以利用的副产物是Ag,考虑原料循环利用,若将该副产物制成生
产所需的试剂(即硝酸银),应先除去混有的铁粉,再用稀硝酸溶解,所以先后还需加入稀
硫酸、稀硝酸来进行处理。答案为:Ag;稀硫酸、稀硝酸;
(5)甲物质为AgI,见光易分解生成银而变黑,其原因是:2AgI 2Ag+I。答案为:
2
2AgI 2Ag+I;
2
(6)第⑤步操作是将粗碘提纯,在扎有小孔的滤纸上有固体凝结,该分离提纯方法是先将
碘由固体变为蒸汽,然后再将蒸汽变为固体,所以名称是升华。答案为:升华。
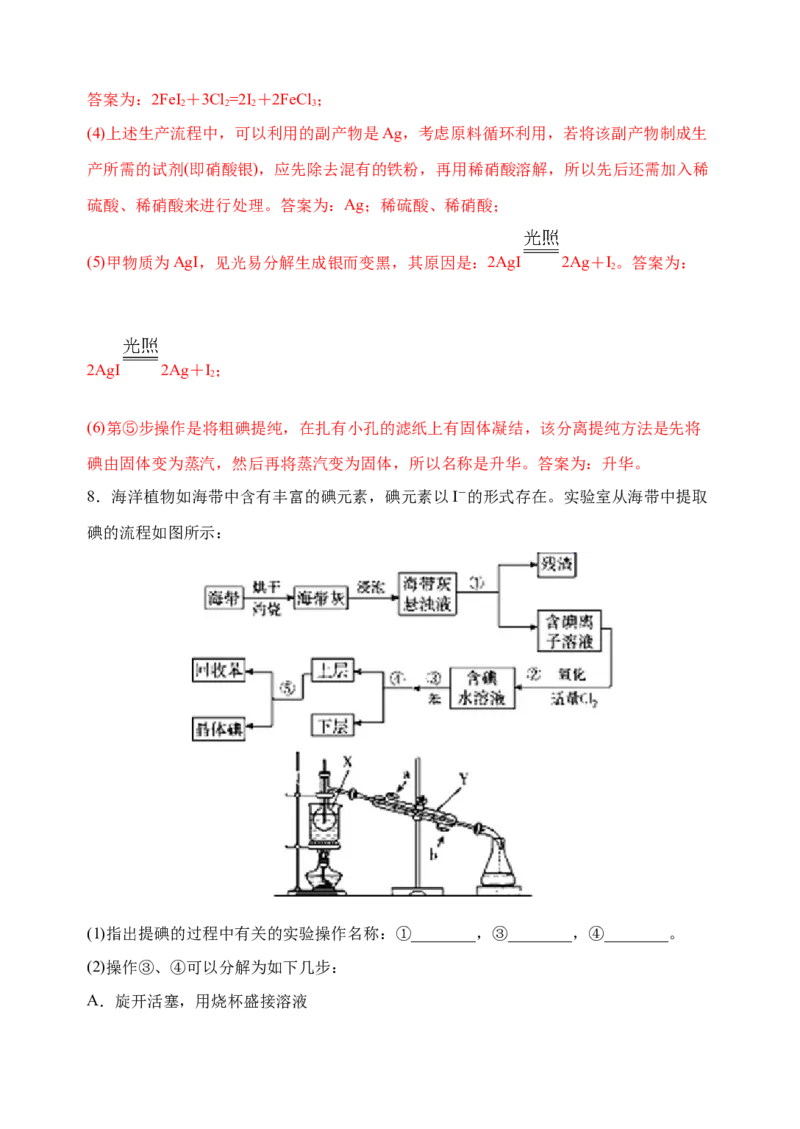
8.海洋植物如海带中含有丰富的碘元素,碘元素以I-的形式存在。实验室从海带中提取
碘的流程如图所示:
(1)指出提碘的过程中有关的实验操作名称:①________,③________,④________。
(2)操作③、④可以分解为如下几步:
A.旋开活塞,用烧杯盛接溶液B.从分液漏斗上口倒出上层溶液
C.打开分液漏斗上口玻璃塞或使塞上的凹槽对准漏斗上口的小孔
D.静置,分层 E.把盛有溶液的分液漏斗放在铁架台的铁圈上
F.把 50 mL 碘水和 15 mL 苯加入分液漏斗中,盖好玻璃塞
G.检查分液漏斗是否漏液 H.倒转分液漏斗,振荡
(ⅰ)正确的操作顺序是:G→________→________E→D→________→________→B。
(ⅱ)能选用苯作萃取剂的原因是_____________________________________。
(ⅲ)上述(C)这样操作的目的是________________________________________。
(3)流程图中,将操作④后的________层液体(填“上”或“下”)用上图仪器进行操作⑤,
写出仪器的名称:X_______、Y___________。请指出上图装置中存在的一处错误:
_____________。
【答案】(1)过滤 萃取 分液 (2) (ⅰ) F H C A (ⅱ) 苯与原溶液互不相溶且
不发生化学反应;碘在苯中的溶解度远大于在水中的溶解度 (ⅲ) 保持分液漏斗内外压强
平衡,使液体易于流下 (3) 上 蒸馏烧瓶 冷凝管 温度计水银球伸入液面以下
【分析】
海藻在坩埚中灼烧,加水浸泡,经过滤得到残渣和滤液,滤液中含有碘离子,通入过量
氯气,可生成碘的水溶液,然后加入苯萃取,经分液后得到碘的苯溶液,最后蒸馏可得
到碘,以此解答该题。
【解析】
海藻在坩埚中灼烧,加水浸泡,经过滤得到残渣和滤液,滤液中含有碘离子,通入过量
氯气,可生成碘的水溶液,然后加入苯萃取,经分液后得到碘的苯溶液,最后蒸馏可得
到碘,
(1)由以上分析可知①为过滤,③为萃取,④为分液,
故答案为过滤;萃取;分液;
(2)(i)③、④顺序为:检查分液漏斗是否漏液→把50mL碘水和15mL苯加入分液漏
斗中,盖好玻璃塞→倒转分液漏斗,振荡→把盛有溶液的分液漏斗放在铁架台的铁圈上
→静置,分层→打开分液漏斗上口玻璃塞或使塞上的凹槽对准漏斗上口的小孔→旋开活塞,用烧杯盛接溶液→从分液漏斗上口倒出上层溶液,
故答案为F;H;C;A;
(ii)苯不溶于水,且碘在苯中溶解度大于水,所应可用苯作萃取剂,
故答案为苯与原溶液互不相溶且不发生化学反应,碘在苯中的溶解度远大于在水中的溶
解度;
(iii)不打开活塞,液体在大气压作用下无法流出,目的是保持分液漏斗内外压力平衡,
使液体易于流下,
故答案为保持分液漏斗内外压力平衡,使液体易于流下;
(3)苯的密度比水小,则苯在上层,苯中溶解碘,分离二者,可用蒸馏的方法,蒸馏装
置中的仪器名称:X为蒸馏烧瓶、Y为冷凝管。蒸馏时温度计水银球应位于蒸馏烧瓶支管
口处,温度计水银球伸入液面以下是错误的,
故答案为上;蒸馏烧瓶;冷凝管;温度计水银球伸入液面以下。
3.工业上以浓缩海水为原料提取溴的部分过程如图所示。
某课外小组在实验室模拟上述过程设计了如图所示装置进行实验(所有橡胶制品均已被保
护,夹持装置已略去)。
(1)A装置中通入a气体时,发生反应的离子方程式为_____。
(2)A装置中通人a气体一段时间后,停止通入,改通入热空气。通入热空气的目的是
____。
(3)实验过程中,B装置中产生的两种主要阴离子为_____。(4)C装置的作用是____。
【答案】(1)Cl +2Br-=2Cl-+Br (2) 将单质溴从蒸馏烧瓶中吹出 (3) 、Br- (4) 吸收
2 2
未反应完的Cl、Br 、SO 等有毒气体,防止污染空气
2 2 2
【分析】
以浓缩海水为原料提取溴,氯气与溴离子反应生成溴,热空气吹出溴后,溴与二氧化硫
发生氧化还原反应生成硫酸、HBr,装置C可吸收尾气。
【解析】
(1)根据工业流程可知a气体是氯气,能把溴离子氧化成单质溴,发生反应的离子方程式
是Cl+2Br-=2Cl-+Br ;
2 2
(2)通入的热空气能将单质溴从蒸馏烧瓶中吹出;
(3)根据工业流程可知b气体是SO ,Br 能把SO 氧化成HSO ,而自身被还原为Br-,所
2 2 2 2 4
以B装置中产生的两种主要阴离子为 、Br-;
(4)氢氧化钠溶液能吸收未反应完的Cl、Br 、SO 等有毒气体,防止污染空气。
2 2 2