文档内容
微专题突破2 氧化还原反应 离子反应
一、选择题
1.(2023·南京二模)2023年3月,“三星堆”遗址考古又发掘出大量青铜器。火法炼铜主要发生
的反应为Cu S+O====2Cu+SO ,下列说法正确的是
2 2 2
A.Cu S中铜的化合价为+2 B.该反应为复分解反应
2
C.SO 是酸性氧化物 D.反应中氧化剂仅为O
2 2
2.(2022·北京)下列物质混合后,因发生氧化还原反应使溶液pH减小的是
A.向NaHSO 溶液中加入少量BaCl 溶液,生成白色沉淀
4 2
B.向NaOH和Fe(OH) 的悬浊液中通入空气,生成红褐色沉淀
2
C.向NaHCO 溶液中加入少量CuSO 溶液,生成蓝绿色沉淀[Cu (OH)CO]
3 4 2 2 3
D.向HS溶液中通入氯气,生成黄色沉淀
2
3.(2022·辽宁)镀锌铁钉放入棕色的碘水中,溶液褪色;取出铁钉后加入少量漂白粉,溶液恢复
棕色;加入CCl ,振荡,静置,液体分层。下列说法正确的是
4
A.褪色原因为I 被Fe还原 B.液体分层后,上层呈紫红色
2
C.镀锌铁钉比镀锡铁钉更易生锈 D.溶液恢复棕色的原因为I-被氧化
4.(2024·扬州市高三下学期开学考)反应4Au+8NaCN+2HO+O=4Na[Au(CN)]+4NaOH可
2 2 2
用于冶金。下列说法正确的是
A.Au是一种活泼金属 B.NaCN溶液显酸性
C.Na[Au(CN)]不属于配合物 D.若无NaCN作用,Au难被O 氧化
2 2
5.(2024·浙江6月卷)下列离子方程式正确的是
A.用CuSO 溶液除HS气体:Cu2++S2-=CuS↓
4 2
B.HSO 溶液中滴加Ba(NO ) 溶液:HSO+Ba2+=BaSO↓+2H+
2 3 3 2 2 3 3
C.NaHCO 溶液中通入少量Cl:2HCO -+Cl=2CO+Cl-+ClO-+HO
3 2 3 2 2 2
D.用FeCl 溶液刻蚀覆铜板制作印刷电路板:2Fe3++Cu=2Fe2++Cu2+
3
6.(2024·淮安市高三上学期开学考)炼油、石化等含S2-工业废水可通过催化氧化法进行处理。
将MnO 嵌于聚苯胺(高温会分解)表面制成催化剂,碱性条件下,催化氧化废水的机理如图所示。下列有
2
关说法不正确的是
A.催化剂因S覆盖表面或进入空位而失效,高温灼烧后也不可继续使用
B.该反应过程的总方程式为O+2HO+2S2-======4OH-+2S↓
2 2
C.反应过程中只有硫元素被氧化
D.反应III的∆H>0
7.(2023·苏锡常镇调研)铁铵矾[NH Fe(SO )·12HO]常用于制备高铁酸盐。下列反应的离子方
4 4 2 2
程式正确的是
A.铁铵矾溶液与氨水混合反应:Fe3++3OH-=Fe(OH)↓
3
B.向铁铵矾溶液中通入HS气体:2Fe3++HS=2Fe2++S↓+2H+
2 2
C.在强碱溶液中,铁铵矾与NaClO反应生成NaFeO:3ClO-+2Fe3++6OH-=2FeO+3Cl-+HO+4H+
2 4 2
D.向铁铵矾溶液中加入过量Ba(OH) 溶液:Fe3++2SO+2Ba2++3OH-=Fe(OH)↓+2BaSO↓
2 3 4
8.(2024·全国甲卷)下列过程对应的离子方程式正确的是
A.用氢氟酸刻蚀玻璃:SiO2-+4F-+6H+=SiF↑+3HO
3 4 2
B.用三氯化铁溶液刻制覆铜电路板:2Fe3++3Cu=3Cu2++2Fe
C.用硫代硫酸钠溶液脱氯:SO2-+2Cl+3HO=2SO2-+4Cl-+6H+
2 3 2 2 3微专题突破2 氧化还原反应 离子反应
D.用碳酸钠溶液浸泡锅炉水垢中的硫酸钙:CaSO+CO2-=CaCO+SO 2-
4 3 3 4
9.(2024·甘肃卷)兴趣小组设计了从 中提取 的实验方案,下列说法正确的是
A.还原性:Ag>Cu>Fe
B.按上述方案消耗1 mol Fe可回收1 mol Ag
C.反应①的离子方程式是[Cu(NH )]2++4H+=Cu2++4NH
3 4
D.溶液①中的金属离子是Fe2+
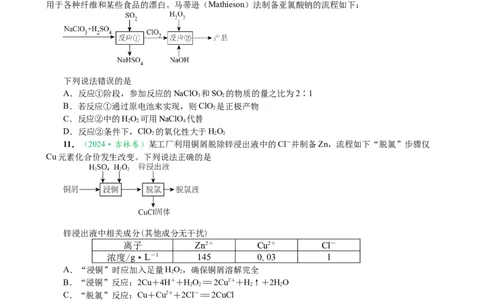
10.(2024·江苏省南通市、盐城市二模)亚氯酸钠(NaClO)是一种高效的漂白剂和氧化剂,可
2
用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如下:
下列说法错误的是
A.反应①阶段,参加反应的NaClO 和SO 的物质的量之比为2∶1
3 2
B.若反应①通过原电池来实现,则ClO 是正极产物
2
C.反应②中的HO 可用NaClO 代替
2 2 4
D.反应②条件下,ClO 的氧化性大于HO
2 2 2
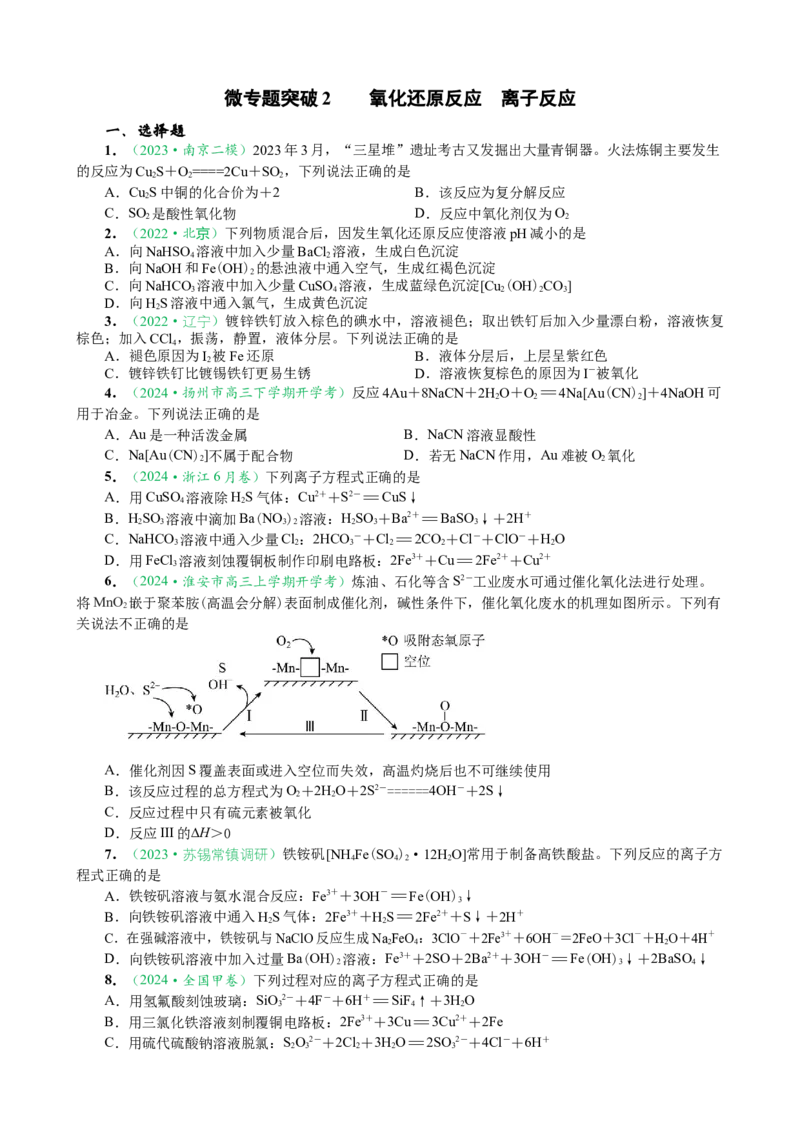
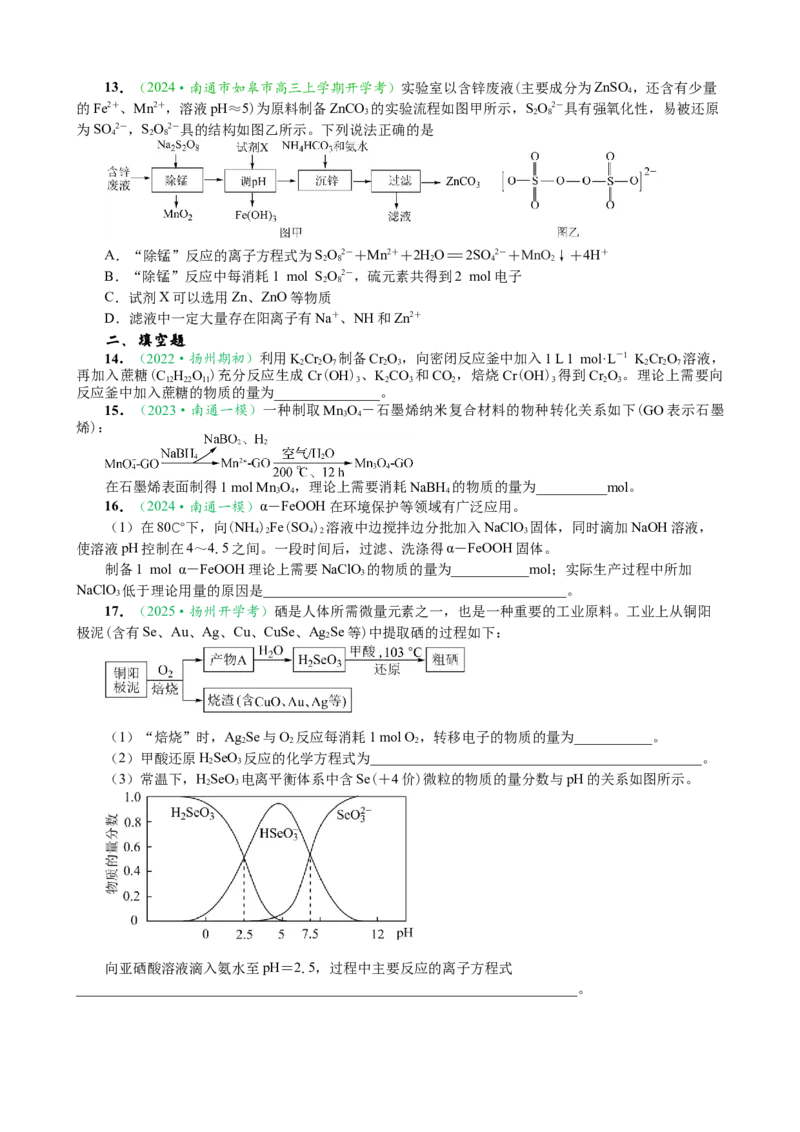
11.(2024·吉林卷)某工厂利用铜屑脱除锌浸出液中的Cl-并制备Zn,流程如下“脱氯”步骤仅
Cu元素化合价发生改变。下列说法正确的是
锌浸出液中相关成分(其他成分无干扰)
离子 Zn2+ Cu2+ Cl-
浓度/g·L-1 145 0.03 1
A.“浸铜”时应加入足量HO,确保铜屑溶解完全
2 2
B.“浸铜”反应:2Cu+4H++HO=2Cu2++H↑+2HO
2 2 2 2
C.“脱氯”反应:Cu+Cu2++2Cl-=2CuCl
D.脱氯液净化后电解,可在阳极得到Zn
12.(2023·南通崇川阶段考试)工业上以锌渣(主要成分为ZnO,含有少量FeO、Fe O 、CuO)为
2 3
主要原料制备硫酸锌的工艺流程如图所示。下列说法正确的是
A.“沉铜”后的滤液中含有的阳离子:Zn2+、Fe2+、H+
B.“氧化”时的离子方程式为2HO+2Fe2+=2Fe3++2HO+O↑
2 2 2 2
C.“滤渣2”的主要成分为Fe O
2 3
D.“操作”为蒸发结晶
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找13.(2024·南通市如皋市高三上学期开学考)实验室以含锌废液(主要成分为ZnSO,还含有少量
4
的Fe2+、Mn2+,溶液pH≈5)为原料制备ZnCO 的实验流程如图甲所示,SO2-具有强氧化性,易被还原
3 2 8
为SO 2-,SO2-具的结构如图乙所示。下列说法正确的是
4 2 8
A.“除锰”反应的离子方程式为SO2-+Mn2++2HO=2SO 2-+MnO ↓+4H+
2 8 2 4 2
B.“除锰”反应中每消耗1 mol SO2-,硫元素共得到2 mol电子
2 8
C.试剂X可以选用Zn、ZnO等物质
D.滤液中一定大量存在阳离子有Na+、NH和Zn2+
二、填空题
14.(2022·扬州期初)利用KCr O 制备Cr O,向密闭反应釜中加入1 L 1 mol·L-1 KCr O 溶液,
2 2 7 2 3 2 2 7
再加入蔗糖(C H O )充分反应生成Cr(OH) 、KCO 和CO ,焙烧Cr(OH) 得到Cr O 。理论上需要向
12 22 11 3 2 3 2 3 2 3
反应釜中加入蔗糖的物质的量为_______________。
15.(2023·南通一模)一种制取MnO -石墨烯纳米复合材料的物种转化关系如下(GO表示石墨
3 4
烯):
在石墨烯表面制得1 mol Mn O,理论上需要消耗NaBH 的物质的量为__________mol。
3 4 4
16.(2024·南通一模)α-FeOOH在环境保护等领域有广泛应用。
(1)在80℃下,向(NH )Fe(SO ) 溶液中边搅拌边分批加入NaClO 固体,同时滴加NaOH溶液,
4 2 4 2 3
使溶液pH控制在4~4.5之间。一段时间后,过滤、洗涤得α-FeOOH固体。
制备1 mol α-FeOOH理论上需要NaClO 的物质的量为___________mol;实际生产过程中所加
3
NaClO 低于理论用量的原因是___________________________________________。
3
17.(2025·扬州开学考)硒是人体所需微量元素之一,也是一种重要的工业原料。工业上从铜阳
极泥(含有Se、Au、Ag、Cu、CuSe、Ag Se等)中提取硒的过程如下:
2
(1)“焙烧”时,Ag Se与O 反应每消耗1 mol O ,转移电子的物质的量为___________。
2 2 2
(2)甲酸还原HSeO 反应的化学方程式为_______________________________________________。
2 3
(3)常温下,HSeO 电离平衡体系中含Se(+4价)微粒的物质的量分数与pH的关系如图所示。
2 3
向亚硒酸溶液滴入氨水至pH=2.5,过程中主要反应的离子方程式
_______________________________________________________________________。