文档内容
微专题突破9 化学反应原理透视二
一、选择题
1.(2024·江苏盐城市高三期中)碳元素及其化合物在自然界广泛存在且具有重要应用。12C、
13C、14C是碳元素的3种核素,碳元素不仅可以形成金刚石等单质,还能形成 CO 、CH 、CHOH、
2 4 3
CHCHOH、HCOONa、NaHCO 等重要化合物。CH 具有较大的燃烧热(890.3 kJ·mol-1),是常见燃料。
3 2 3 4
用NaOH溶液吸收CO 生成NaHCO 溶液是CO“固定”再利用的方法之一、电解NaHCO 溶液可获得
2 3 2 3
CH;向NaHCO 溶液中加入铁粉,反应初期产生H 并生成FeCO,FeCO 迅速转化为活性Fe O ,活性
4 3 2 3 3 3 4-x
Fe O -x催化HCO -加氢生成HCOO-。“侯氏制碱法”是以CO 、NH 、NaCl为原料制备NaCO 。活
3 4 3 2 3 2 3
性Fe O 催化HCO -加氢生成HCOO-的总反应为:HCO -+H========HCOO-+3HO,可能的反应历
3 4-x 3 3 2 2
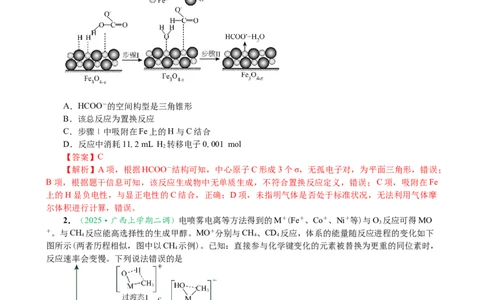
程如下图所示。下列说法正确的是
A.HCOO-的空间构型是三角锥形
B.该总反应为置换反应
C.步骤Ⅰ中吸附在Fe上的H与C结合
D.反应中消耗11.2 mL H 转移电子0.001 mol
2
【答案】C
【解析】A项,根据HCOO-结构可知,中心原子C形成3个σ,无孤电子对,为平面三角形,错误;
B项,根据题干信息可知,该反应生成物中无单质生成,不符合置换反应定义,错误;C项,吸附在Fe
上的H显负电性,与显正电性的C结合,正确;D项,未指明气体是否处于标准状况,无法利用气体摩
尔体积进行计算,错误。
2.(2025·广西上学期二调)电喷雾电离等方法得到的M+(Fe+、Co+、Ni+等)与O 反应可得MO
3
+。与CH 反应能高选择性的生成甲醇。MO+分别与CH、CD 反应,体系的能量随反应进程的变化如下
4 4 4
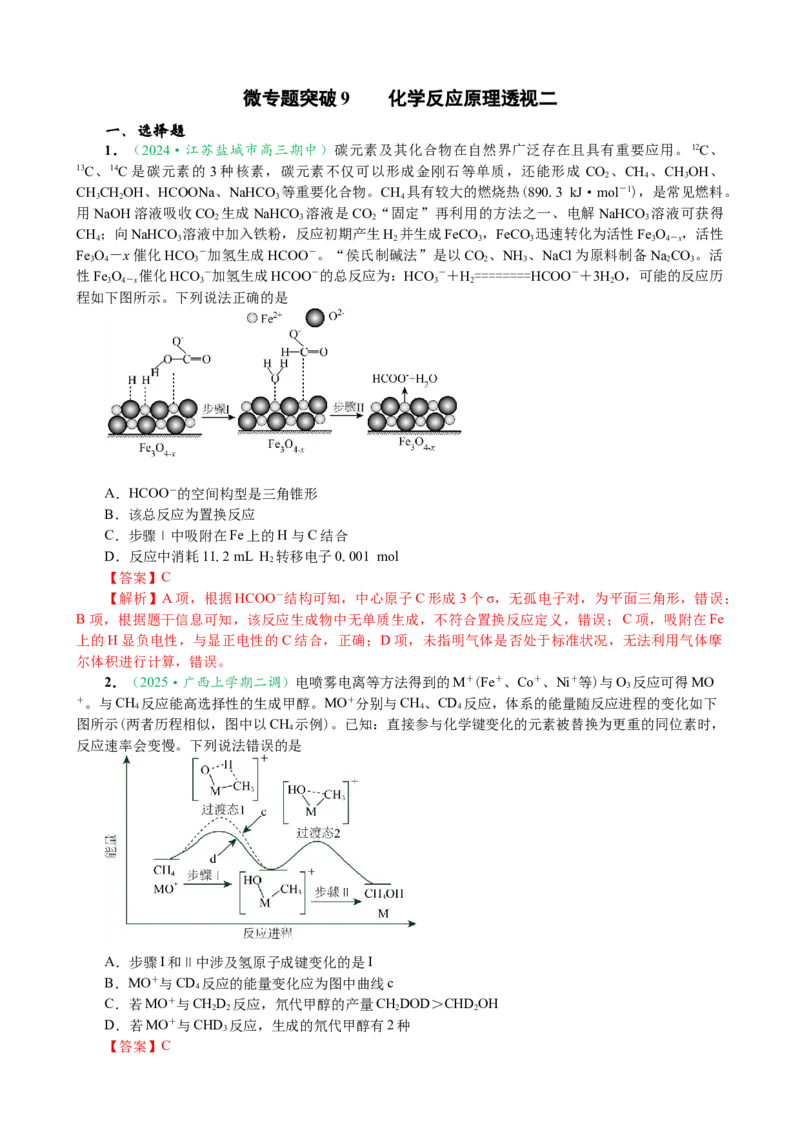
图所示(两者历程相似,图中以CH 示例)。已知:直接参与化学键变化的元素被替换为更重的同位素时,
4
反应速率会变慢。下列说法错误的是
A.步骤I和Ⅱ中涉及氢原子成键变化的是I
B.MO+与CD 反应的能量变化应为图中曲线c
4
C.若MO+与CHD 反应,氘代甲醇的产量CHDOD>CHD OH
2 2 2 2
D.若MO+与CHD 反应,生成的氘代甲醇有2种
3
【答案】C微专题突破9 化学反应原理二
【解析】A项,由图可知,步骤Ⅰ涉及碳氢键的断裂和氢氧键的形成,步骤Ⅱ中涉及碳氧键形成,
所以涉及氢原子成键变化的是步骤Ⅰ,正确;B项,直接参与化学键变化的元素被替换为更重的同位素时,
反应速率会变慢,说明正反应活化能会增大,则MO+与CD 反应的能量变化应为图中曲线c,正确;C项,
4
直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则氧更容易和H而不是和D生
成羟基,故氘代甲醇的产量CHDOD<CHD OH,错误;D项,根据反应机理可知,若MO+与CHD 反应,
2 2 2
生成的氘代甲醇可能为CHD OD或CDOH,共2种,正确。
2 3
3.(2023·南京模拟)草酸亚铁(FeC O)是生产磷酸铁锂电池的原料,实验室可通过如图反应制取:
2 4
已知室温时:K (HC O)=5.6×10-2、K (HC O)=1.5×10-4、K (FeC O)=2.1×10-7。
a1 2 2 4 a2 2 2 4 sp 2 4
下列说法正确的是
A.酸化、溶解后的溶液中存在:2c(Fe2+)+c(H+)<c(NH)+c(OH-)
B.室温下,0.10 mol·L-1NaHC O 溶液中存在:c(C O)<c(HC O)
2 4 2 2 2 4
C.向稀硫酸酸化的KMnO 溶液中滴加NaC O 溶液至溶液褪色,反应的离子方程式为5C O+2MnO
4 2 2 4 2
+8HO=0CO↑+2Mn2++16OH-
2 2
D.室温时反应Fe2++HC O=FeC O+2H+的平衡常数K=40
2 2 4 2 4
【答案】D
【解析】A项,酸化、溶解后的溶液中存在电荷守恒:2c(Fe2+)+c(H+)+c(NH)=2c(SO)+c(OH
-),c(SO)>c(NH),则2c(Fe2+)+c(H+)>c(NH)+c(OH-),错误;B项,室温下,0.10 mol·L-
1NaHC O 溶液中,K (HC O)=1.5×10-4>K (HC O)=,说明HC O的电离程度大于其水解程度,则存
2 4 a2 2 2 4 h 2 2
在c(HC O)<c(C O),错误;C项,向稀硫酸酸化的KMnO 溶液中滴加NaC O 溶液至溶液褪色,反应
2 2 4 2 4 2 2 4
的离子方程式为5C O+2MnO+16H+=10CO↑+2Mn2++8HO,错误;D项,室温时反应Fe2++
2 2 2
HC O=FeC O+2H+的平衡常数K======40,正确。
2 2 4 2 4
4.(2023·苏州中学、淮阴中学、姜堰中学、海门中学联考)已知:室温下,K (HS)=10-7,
a1 2
K (HS)=10-12.9。通过下列实验探究含硫化合物的性质。
a2 2
实验1:测得0.1 mol·L-1 NaHS溶液的pH>7。
实验2:向0.1 mol·L-1 NaHS溶液中通入过量Cl,无淡黄色沉淀产生。
2
实验3:向0.1 mol·L-1 NaHS溶液中加入等体积0.1 mol·L-1 NaHCO 溶液充分混合,无气泡产生。
3
下列说法正确的是
A.由实验1可知:c(H+)·c(S2-)>c(HS)·c(OH-)
2
B.实验2说明HS-不能被Cl 氧化
2
C.实验3所得溶液中:c(S2-)+c(HS-)+c(HS)>c(CO)+c(HCO)+c(HCO)
2 2 3
D.0.001 mol·L-1 Na S溶液中:c(Na+)>c(S2-)>c(OH-)>c(H+)
2
【答案】D
【解析】A项,NaHS溶液的pH>7,说明HS-的水解程度大于其电离程度,则c(HS)>c(S2-),
2
c(OH-)>c(H+),故c(H+)·c(S2-)<c(HS)·c(OH-),错误;B项,HS-能被Cl 氧化,实验2没有淡
2 2
黄色沉淀产生,可能是Cl 将HS-氧化为SO,错误;C项,向0.1 mol·L-1 NaHS溶液中加入等体积0.1
2
mol·L-1 NaHCO 溶液充分混合,无气泡产生,C、S原子守恒知,c(S2-)+c(HS-)+c(HS)=c(CO)+
3 2
c(HCO)+c(H CO),错误;D项,0.001 mol·L-1 Na S溶液中,S2-发生两步微弱水解,第一步水解产生
2 3 2
OH-和HS-,第二步水解产生OH-和HS,溶液呈碱性,则c(Na+)>c(S2-)>c(OH-)>c(H+),正确。
2
5.(2024·南通海安期末)室温下,通过下列实验探究NaHS溶液的性质。
实验 实验操作和现象
1 向0.1 mol·L-1NaHS溶液中滴加几滴酚酞试剂,溶液变红
2 向0.1 mol·L-1NaHS溶液中加入等体积0.1 mol·L-1NaOH溶液充分混合
3 向0.1 mol·L-1NaHS溶液中通入少量氯气,有淡黄色沉淀产生
4 向0.1 mol·L-1NaHS溶液中加入等体积0.1 mol·L-1HCl溶液,有气体放出
下列有关说法正确的是
A.实验1中0.1 mol·L-1NaHS溶液中:c(S2-)>c(HS)
2
B.实验2中所得溶液中:c(Na+)=c(S2-)+c(HS-)+c(HS)
2
C.实验3中反应的离子方程式:HS-+Cl=S↓+H++2Cl-
2
D.实验4中所得溶液中:c(S2-)+c(OH-)=c(HS)+c(H+)
2
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找【答案】C
【解析】A项,NaHS溶液中加酚酞溶液变红,说明溶液显碱性,HS-的水解程度大于其电离程度,
故c(HS)>c(S2-),错误;B项,等体积等浓度NaHS溶液与NaOH溶液混合后恰好反应生成NaS,
2 2
NaS溶液中存在物料守恒:c(Na+)=2[c(S2-)+c(HS-)+c(HS)],错误;C项,NaHS溶液中通入氯气
2 2
产生淡黄色沉淀,说明氯气将硫元素氧化为硫单质,对应离子方程式为HS-+Cl =S↓+H++2Cl-,正
2
确;D项,NaHS与盐酸反应生成NaCl和HS,故c(Na+)=c(Cl-),结合电荷守恒:2c(S2-)+c(OH-)
2
+c(HS-)+c(Cl-)=c(Na+)+c(H+),得2c(S2-)+c(OH-)+c(HS-)=c(H+),若HS未逸出,则存在
2
物料守恒:c(Na+)=c(HS)+c(S2-)+c(HS-),联立电荷守恒得:c(S2-)+c(OH-)+c(Cl-)=c(H+)+
2
c(HS),D项中等式不成立,若HS部分逸出,由物料守恒可知c(Na+)>c(HS)+c(S2-)+c(HS-),D
2 2 2
项等式不成立,错误。
6.(2023·泰州期末)室温下,某兴趣小组通过下列实验制备少量NaHCO 并探究其性质。
3
实验1:测得100 mL 14 mol·L-1 氨水的pH约为12。
实验2:向上述氨水中加NaCl粉末至饱和,通入足量CO 后析出晶体。
2
实验3:将所得混合物静置后过滤、洗涤、干燥,得到NaHCO 。
3
实验4:配制100 mL一定浓度的NaHCO 溶液,测得pH为8.0。
3
下列说法正确的是
A.依据实验1推测K (NH ·HO)≈7×10-26
b 3 2
B.依据实验2推测溶解度:NaHCO >NaCl
3
C.实验3所得滤液中:c(NH)+c(H+)=c(Cl-)+c(OH-)
D.实验4的溶液中:c(HCO)-c(CO)=9.9×10-7 mol·L-1
2 3
【答案】D
【解析】A项,测得100 mL 14 mol·L-1氨水的pH约为12,c(H+)=10-12 mol·L-1,c(OH-)=10-2
mol·L-1,则K (NH ·HO)==>7×10-26,错误;B项,实验2中发生的反应为NaCl+CO+HO+NH
b 3 2 2 2 3
=NaHCO ↓+NH Cl,析出NaHCO ,说明溶解度:NaHCO <NaCl,错误;C项,实验3所得滤液中
3 4 3 3
主要含有NH Cl,且含有少量NaHCO ,由电荷守恒知,溶液中存在:c(Na+)+c(NH)+c(H+)=c(OH
4 3
-)+c(Cl-)+2c(CO)+c(HCO),错误;D项,实验4的溶液为NaHCO 溶液,存在质子守恒:c(CO)+
3
c(OH-)=c(H+)+c(HCO),则c(HCO)-c(CO)=c(OH-)-c(H+)=(10-6-10-8) mol·L-1=9.9×10-
2 3 2 3
7 mol·L-1,正确。
7.(2024·常州高级中学开学考试)室温下,通过下列实验探究NaCO 的性质。已知:25 ℃时,
2 3
HSO 的K =1.4×10-2、K =1.0×10-7,HCO 的K =4.3×10-7、K =5.6×10-11。
2 3 a1 a2 2 3 a1 a2
实验1:配制50 mL 0.1 mol·L-1 Na CO 溶液,测得溶液pH约为12;
2 3
实验2:取10 mL 0.1 mol·L-1 Na CO 溶液,向其中加入一定量CaSO 固体充分搅拌,一段时间后过
2 3 4
滤,向滤渣中加入足量稀盐酸,固体部分溶解;
实验3:取10 mL 0.1 mol·L-1 Na CO 溶液,向其中缓慢滴入等体积0.1 mol·L-1稀盐酸。
2 3
下列说法正确的是
A.实验1所得溶液中,c(Na+)<c(CO)+c(HCO)
B.实验2,加入稀盐酸后的上层清液中c(Ca2+)=c(SO)
C.实验3反应后溶液中存在:c(Na+)=c(CO)+c(HCO)+c(HCO)
2 3
D.25 ℃时,反应CO+HSO HCO+HSO的平衡常数K=2.5×108
2 3
【答案】D
【解析】A项,NaCO 溶液呈碱性,c(OH-)>c(H+),电荷守恒关系为c(Na+)+c(H+)=c(HCO)
2 3
+2c(CO)+c(OH-),则c(Na+)>c(HCO)+2c(CO)>c(CO)+c(HCO),错误;B项,向滤渣中加入足
量稀盐酸,固体部分溶解,则滤渣为CaCO 和CaSO 的混合物,CaCO 溶于盐酸生成CaCl ,CaSO 存在
3 4 3 2 4
溶解平衡,则实验2加入稀盐酸后的上层清液中c(Ca2+)>c(SO),错误;C项,NaCO 溶液中滴入等体
2 3
积0.1 mol·L-1稀盐酸后生成NaHCO 和NaCl,存在c(Na+)=c(CO)+c(HCO)+c(HCO)+c(Cl-),则
3 2 3
c(Na+)>c(CO)+c(HCO)+c(HCO),错误;D项,反应CO+HSO HCO+HSO的平衡常数K=
2 3 2 3
===2.5×108,正确。
8.(2024·扬州期末)室温下取NH Cl、氨水进行如下实验。
4
实验1:将0.1 mol·L-1NH Cl 溶液和0.1 mol·L-1氨水等体积混合,混合溶液的pH>7。
4微专题突破9 化学反应原理二
实验2:将0.1 mol·L-1氨水与0.1 mol·L-1 FeCl 溶液等体积混合,生成红褐色沉淀。
3
实验3:向0.1 mol·L-1 NH Cl溶液中通入少量NH 。
4 3
实验4:向10 mL0.1 mol·L-1氨水中滴加20 mL 0.1 mol·L-1 盐酸。
下列说法正确的是
A.K (NH ·HO)<10-7
b 3 2
B.实验2说明混合时溶液中存在:K [Fe(OH)]>c3(OH-)·c(Fe3+)
sp 3
C.实验3中NH的水解程度减小
D.实验4所得混合溶液中c(H+)<c(NH)+c(NH ·HO)+c(OH-)
3 2
【答案】C
【解析】A项,若K (NH ·HO)<10-7,则铵根离子水解平衡常数K >10-7,则0.1 mol·L-
b 3 2 h
1NH Cl 溶液和0.1 mol·L-1氨水等体积混合时溶液呈酸性,而与题意相违背,错误;B项,实验2说明
4
混合时溶液中存在Q>K [Fe(OH)],因此有沉淀生成,错误;C项,向0.1 mol·L-1 NH Cl溶液中通入
sp 3 4
少量NH ,一水合氨浓度增大,铵根离子水解平衡逆向移动,因此实验3中NH的水解程度减小,正确;
3
D项,向10 mL 0.1 mol·L-1氨水中滴加20 mL 0.1 mol·L-1盐酸,溶质是氯化铵和HCl且两者浓度相
等,根据电荷守恒得c(NH)+c(H+)=c(Cl-)+c(OH-),根据物料守恒得c(Cl-)=2c(NH)+
2c(NH ·HO),两式联立得到c(H+)=c(NH)+2c(NH ·HO)+c(OH-),因此实验4所得混合溶液中
3 2 3 2
c(H+)>c(NH)+c(NH ·HO)+c(OH-),错误。
3 2
9.(2023·南通一模)常温下,将FeSO 溶液与NH HCO 溶液混合可制得FeCO ,混合过程中有气
4 4 3 3
体产生。已知:K (NH ·HO)=1.8×10-5,K (HCO)=4.5×10-7,K (HCO)=4.7×10-11,
b 3 2 a1 2 3 a2 2 3
K (FeCO)=3.13×10-11。下列说法不正确的是
sp 3
A.向100 mL pH=10氨水中通入少量CO,反应后溶液中存在:c(CO)>c(HCO)
2
B.0.1 mol·L-1 NH HCO 溶液中:c(HCO)>c(CO)+c(NH ·HO)
4 3 2 3 3 2
C.生成FeCO 的离子方程式为Fe2++2HCO=FeCO↓+CO↑+HO
3 3 2 2
D.生成FeCO 沉淀后的上层清液中:c(Fe2+)·c(CO)=K (FeCO)
3 sp 3
【答案】A
【解析】A项,通入少量CO,pH仍约为10,CO+2NH ·HO=(NH )CO+HO,K (HCO)=
2 2 3 2 4 2 3 2 a2 2 3
==4.7×10-11,则=<1,可知c(CO)<c(HCO),错误;B项,K (NH)==<K (HCO)==,则HCO
h h
的水解程度大于NH的水解程度,溶液呈碱性:c(OH-)>c(H+),NH HCO 溶液的质子守恒式为c(H+)
4 3
+c(HCO)=c(OH-)+c(CO)+c(NH ·HO),则c(HCO)>c(CO)+c(NH ·HO),正确;C项,
2 3 3 2 2 3 3 2
HCO电离出CO和H+,Fe2+结合CO生成FeCO ,H+结合HCO生成CO 和HO,离子方程式为Fe2++
3 2 2
2HCO=FeCO↓+CO↑+HO,正确;D项,生成FeCO 沉淀后的上层清液为FeCO 的饱和溶液,溶
3 2 2 3 3
液中:c(Fe2+)·c(CO)=K (FeCO),正确。
sp 3
10.(2025·连云港市上学期期中)室温下,通过下列实验探究NaS溶液的性质。
2
实验1:用pH计测量0.1 mol·L-1 NaS溶液的pH,测得pH为12.65。
2
实验2:向0.1 mol·L-1的NaS溶液中通入HCl气体至pH=7(忽略溶液体积的变化及HS的挥发)。
2 2
实验3:向1 mL 0.1 mol·L-1的NaS溶液中加入1 mL 0.1 mol·L-1 HS溶液。
2 2
已知:K (HS)=9.1×10-8,K (HS)=1.0×10-12,K (HCO)=4.3×10-7,K (HCO)=5.6×10-
a1 2 a2 2 a1 2 3 a2 2 3
11。
下列说法正确 的是
A.实验1所得溶液中:c(S2-)<c(HS-)
B.实验2所得溶液中:c(Cl-)+c(S2-)-c(HS)=0.1 mol·L-1
2
C.实验3中:反应S2-+HS=2HS-的平衡常数K=9.1×10-20
2
D.向NaS溶液中通入少量CO 的离子方程式CO+S2-+HO=HS↑+CO2-
2 2 2 2 2 3
【答案】B
【解析】A项,用pH计测量0.1 mol·L-1 NaS溶液的pH,测得pH为12.65,溶液呈碱性,S2-水解
2
生成HS-,水解是微弱的,则c(S2-)>c(HS-),错误;B项,向0.1 mol·L-1的NaS溶液中通入HCl气
2
体至pH=7,溶液呈中性,c(H+)=c(OH-),溶液中存在物料守恒:c(S2-)+c(HS)+c(HS-)=0.1
2
mol·L-1,电荷守恒:2c(S2-)+c(HS-)+c(OH-)+c(Cl-)=c(Na+)+c(H+),c(Na+)=0.2 mol·L-1,
结合上式可得c(Cl-)+c(S2-)-c(HS)=0.1 mol·L-1,正确;C项,反应S2-+HS=2HS-的平衡常数
2 2
K======9.1×104,错误;D项,电离常数越大,酸性越强,则酸性:HCO>HS>HCO ->HS
2 3 2 3
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找-,根据强酸制取弱酸的原理,向NA2S溶液中通入少量CO 生成NaHS和NaCO,离子方程式为:CO
2 2 3 2
+2S2-+HO=2HS-+CO2-,错误。
2 3
的
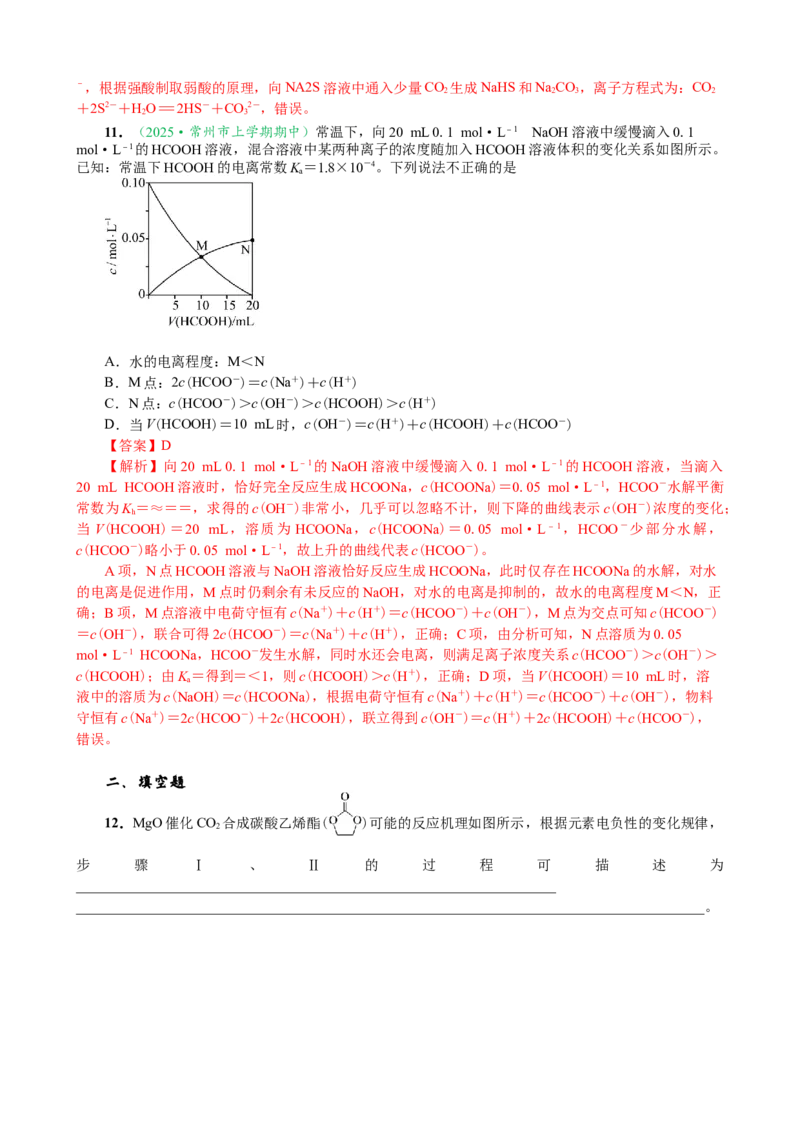
11.(2025·常州市上学期期中)常温下,向20 mL 0.1 mol·L-1 NaOH溶液中缓慢滴入0.1
mol·L-1的HCOOH溶液,混合溶液中某两种离子的浓度随加入HCOOH溶液体积的变化关系如图所示。
已知:常温下HCOOH的电离常数K=1.8×10-4。下列说法不正确的是
a
A.水的电离程度:M<N
B.M点:2c(HCOO-)=c(Na+)+c(H+)
C.N点:c(HCOO-)>c(OH-)>c(HCOOH)>c(H+)
D.当V(HCOOH)=10 mL时,c(OH-)=c(H+)+c(HCOOH)+c(HCOO-)
【答案】D
【解析】向20 mL 0.1 mol·L-1的NaOH溶液中缓慢滴入0.1 mol·L-1的HCOOH溶液,当滴入
20 mL HCOOH溶液时,恰好完全反应生成HCOONa,c(HCOONa)=0.05 mol·L-1,HCOO-水解平衡
常数为K =≈==,求得的c(OH-)非常小,几乎可以忽略不计,则下降的曲线表示c(OH-)浓度的变化;
h
当 V(HCOOH)=20 mL,溶质为 HCOONa,c(HCOONa)=0.05 mol·L-1,HCOO-少部分水解,
c(HCOO-)略小于0.05 mol·L-1,故上升的曲线代表c(HCOO-)。
A项,N点HCOOH溶液与NaOH溶液恰好反应生成HCOONa,此时仅存在HCOONa的水解,对水
的电离是促进作用,M点时仍剩余有未反应的NaOH,对水的电离是抑制的,故水的电离程度M<N,正
确;B项,M点溶液中电荷守恒有c(Na+)+c(H+)=c(HCOO-)+c(OH-),M点为交点可知c(HCOO-)
=c(OH-),联合可得2c(HCOO-)=c(Na+)+c(H+),正确;C项,由分析可知,N点溶质为0.05
mol·L-1 HCOONa,HCOO-发生水解,同时水还会电离,则满足离子浓度关系c(HCOO-)>c(OH-)>
c(HCOOH);由K=得到=<1,则c(HCOOH)>c(H+),正确;D项,当V(HCOOH)=10 mL时,溶
a
液中的溶质为c(NaOH)=c(HCOONa),根据电荷守恒有c(Na+)+c(H+)=c(HCOO-)+c(OH-),物料
守恒有c(Na+)=2c(HCOO-)+2c(HCOOH),联立得到c(OH-)=c(H+)+2c(HCOOH)+c(HCOO-),
错误。
二、填空题
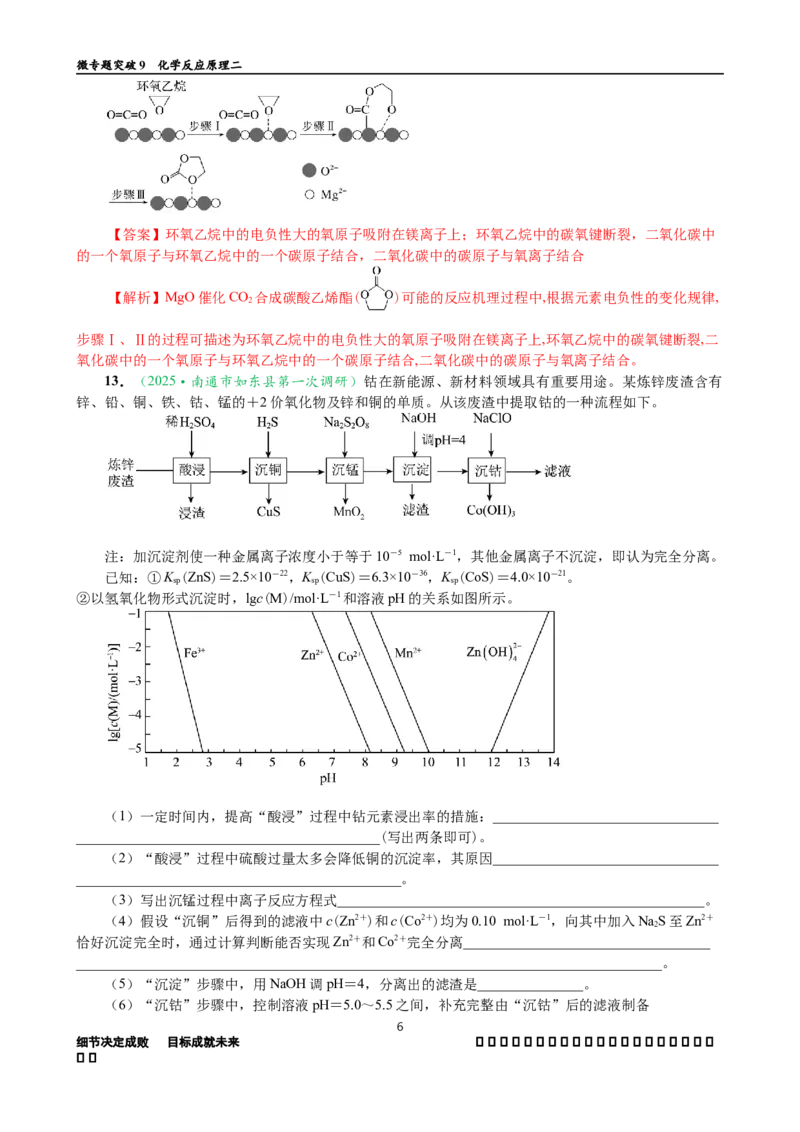
12.MgO催化CO 合成碳酸乙烯酯( )可能的反应机理如图所示,根据元素电负性的变化规律,
2
步 骤 Ⅰ 、 Ⅱ 的 过 程 可 描 述 为
____________________________________________________________________
_________________________________________________________________________________________。微专题突破9 化学反应原理二
【答案】环氧乙烷中的电负性大的氧原子吸附在镁离子上;环氧乙烷中的碳氧键断裂,二氧化碳中
的一个氧原子与环氧乙烷中的一个碳原子结合,二氧化碳中的碳原子与氧离子结合
【解析】MgO催化CO 合成碳酸乙烯酯( )可能的反应机理过程中,根据元素电负性的变化规律,
2
步骤Ⅰ、Ⅱ的过程可描述为环氧乙烷中的电负性大的氧原子吸附在镁离子上,环氧乙烷中的碳氧键断裂,二
氧化碳中的一个氧原子与环氧乙烷中的一个碳原子结合,二氧化碳中的碳原子与氧离子结合。
13.(2025·南通市如东县第一次调研)钴在新能源、新材料领域具有重要用途。某炼锌废渣含有
锌、铅、铜、铁、钴、锰的+2价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
注:加沉淀剂使一种金属离子浓度小于等于10-5 mol·L-1,其他金属离子不沉淀,即认为完全分离。
已知:①K (ZnS)=2.5×10-22,K (CuS)=6.3×10-36,K (CoS)=4.0×10-21。
sp sp sp
②以氢氧化物形式沉淀时,lgc(M)/mol·L-1和溶液pH的关系如图所示。
(1)一定时间内,提高“酸浸”过程中钻元素浸出率的措施:________________________________
___________________________________________(写出两条即可)。
(2)“酸浸”过程中硫酸过量太多会降低铜的沉淀率,其原因________________________________
______________________________________________。
(3)写出沉锰过程中离子反应方程式____________________________________________________。
(4)假设“沉铜”后得到的滤液中c(Zn2+)和c(Co2+)均为0.10 mol·L-1,向其中加入NaS至Zn2+
2
恰好沉淀完全时,通过计算判断能否实现Zn2+和Co2+完全分离___________________________________
___________________________________________________________________________________。
(5)“沉淀”步骤中,用NaOH调pH=4,分离出的滤渣是_______________。
(6)“沉钴”步骤中,控制溶液pH=5.0~5.5之间,补充完整由“沉钴”后的滤液制备
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找ZnSO •7HO的实验方案:
4 2
__________________________________________________________________________
___________________________________________________________________________________________
__________________________________________________________________________________。(实验中
可选用的试剂:NaOH溶液、稀硫酸)
【答案】(1)粉碎炼锌废渣、适当提高硫酸浓度、适当升高温度、搅拌等 (2)酸性过强,HS的
2
溶解度减小,c(S2-)减小,CuS沉淀时的速率减小 (3)SO2-+Mn2++2HO=2SO 2-+MnO ↓+4H+
2 8 2 4 2
(4)Zn2+沉淀完全时,溶液中c(S2-)==2.5×10-17 mol·L-1,Q (CoS)=0.10×2.5×10-17=2.5×10-18>
C
K (CoS),有CoS沉淀生成,所以不能实现Zn2+和Co2+完全分离或Zn2+完全沉淀时,c(Co2+)==1.6×10
sp
-4 mol·L-1>10-5 mol·L-1,所以不能实现Zn2+和Co2+完全分离 (5)Fe(OH) (6)边搅拌边向滤液
3
中滴加NaOH溶液,控制溶液的pH接近12但不大于12,过滤,向沉淀中滴加入稀硫酸溶液直至固体完
全溶解,蒸发浓缩、冷却结晶、过滤、洗涤、低温干燥
【解析】炼锌废渣含有锌、铅、铜、铁、钴、锰的+2价氧化物及锌和铜的单质,经稀硫酸酸浸时,
铜不溶解,Zn及其他价氧化物除铅元素转化为硫酸铅沉淀外,其他均转化为相应的+2价阳离子进入溶
液;然后通入硫化氢沉铜生成CuS沉淀;过滤后,滤液中加入NaSO 将锰离子氧化为二氧化锰除去,同
2 2 8
时亚铁离子也被氧化为铁离子;再次过滤后,用氢氧化钠调节 pH=4,铁离子完全转化为氢氧化铁沉淀
除去;第三次过滤后的滤液中加入次氯酸钠沉钴,得到Co(OH) 。
3
(1)“酸浸”前,将废渣粉碎炼锌废渣、适当提高硫酸浓度、适当升高温度、搅拌增大固体与酸反
应的接触面积,提高钴元素的浸出效率;故答案为:粉碎炼锌废渣、适当提高硫酸浓度、适当升高温度、
搅拌;(2)酸性过强,HS的溶解度减小,c(S2-)减小,CuS沉淀时的速率减小,“酸浸”过程中硫酸
2
过量太多会降低铜的沉淀率;故答案为:酸性过强,HS的溶解度减小,c(S2-)减小,CuS沉淀时的速率
2
减小;(3)“沉锰”步骤中,NaSO 将Mn2+氧化为二氧化锰除去,发生的反应为SO2-+Mn2++2HO
2 2 8 2 8 2
=2SO 2-+MnO ↓+4H+;故答案为:SO2-+Mn2++2HO=2SO 2-+MnO ↓+4H+;(4)假设“沉
4 2 2 8 2 4 2
铜”后得到的滤液中c(Zn2+)和c(Co2+)均为0.10 mol·L-1,向其中加入NaS至Zn2+沉淀完全,此时溶液
2
中c(S2-)= mol·L-1=2.5×10-17 mol·L-1,Q(CoS)=2.5×10−18>K (CoS),有CoS沉淀生成,所以不能
c sp
实现Zn2+和Co2+完全分离或Zn2+完全沉淀时,c(Co2+)==1.6×10−4 mol·L-1>10−5 mol·L-1,所以不能
实现Zn2+和Co2+完全分离;故答案为:Zn2+沉淀完全时,溶液中c(S2-)=2.5×10−17 mol·L-1,Q(CoS)
c
=2.5×10−18 mol·L-1>K (CoS),有CoS沉淀生成,所以不能实现Zn2+和Co2+完全分离或Zn2+完全时,
sp
c(Co2+)=1,6×10−4 mol·L-1>10−5 mol·L-1,所以不能实现Zn2+和Co2+完全分离;(5)“沉锰”步骤中,
SO2-同时将Fe2+氧化为Fe3+,“沉淀”步骤中用NaOH调pH=4,Fe3+可以完全沉淀为Fe(OH),因此,
2 8 3
分离出的滤渣是Fe(OH);故答案为:Fe(OH);(6)根据题中给出的信息,“沉钴”后的滤液的pH=
3 3
5.0~5.5,溶液中有元素以形式存在,当pH>12后氢氧化锌会溶解转化为Zn(OH)2-,因此,边搅拌边
4
向滤液中滴加NaOH溶液,控制溶液的pH接近12但不大于12,过滤,向沉淀中滴加入稀硫酸溶液直至
固体完全溶解,蒸发浓缩、冷却结晶、过滤、洗涤、低温干燥;故答案为:边搅拌边向滤液中滴加NaOH
溶液,控制溶液的pH接近12但不大于12,过滤,向沉淀中滴加入稀硫酸溶液直至固体完全溶解,蒸发
浓缩、冷却结晶、过滤、洗涤、低温干燥。