文档内容
押江苏卷第 14 题
化工流程综合题
核心考点 考情统计 考向预测 备考策略
1.重点关注与化学实验、化学反
2023·江苏卷,14
应原理等其他模块交叉知识,高考
物质转化与应 2022·江苏卷,14 结合工艺流程综合考查元素化合物 题经常综合考查;
的转化关系、实验操作、归因分
用 2021·江苏卷,15 析、化学计算相关知识 2.以物质制备、物质提纯为主线
的工艺流程题考查形式为主,考查
元素化学、实验化学以及反应原理
1.(2023·江苏卷,14) 催化剂能催化 脱除烟气中的NO,反应为
。
(1)催化剂的制备。将预先制备的一定量的 粉末置于80℃的水中,在搅拌下加入一定量的
溶液,经蒸发、焙烧等工序得到颗粒状 催化剂。在水溶液中 水解为
沉淀的离子方程式为 ;反应选用 溶液而不选用 溶液的原因是 。
(2)催化剂的应用。将一定物质的量浓度的NO、 、 (其余为 )气体匀速通过装有
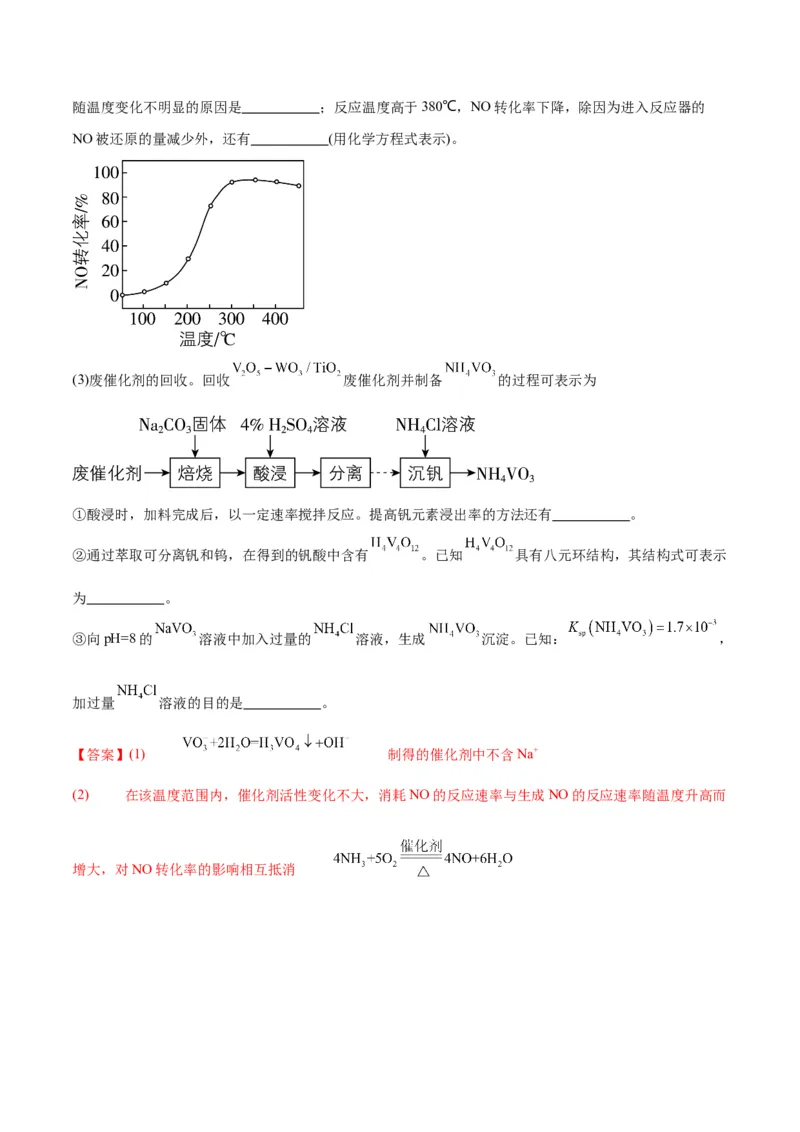
催化剂的反应器,测得NO的转化率随温度的变化如题图所示。反应温度在320~360℃范围内,NO转化率随温度变化不明显的原因是 ;反应温度高于380℃,NO转化率下降,除因为进入反应器的
NO被还原的量减少外,还有 (用化学方程式表示)。
(3)废催化剂的回收。回收 废催化剂并制备 的过程可表示为
①酸浸时,加料完成后,以一定速率搅拌反应。提高钒元素浸出率的方法还有 。
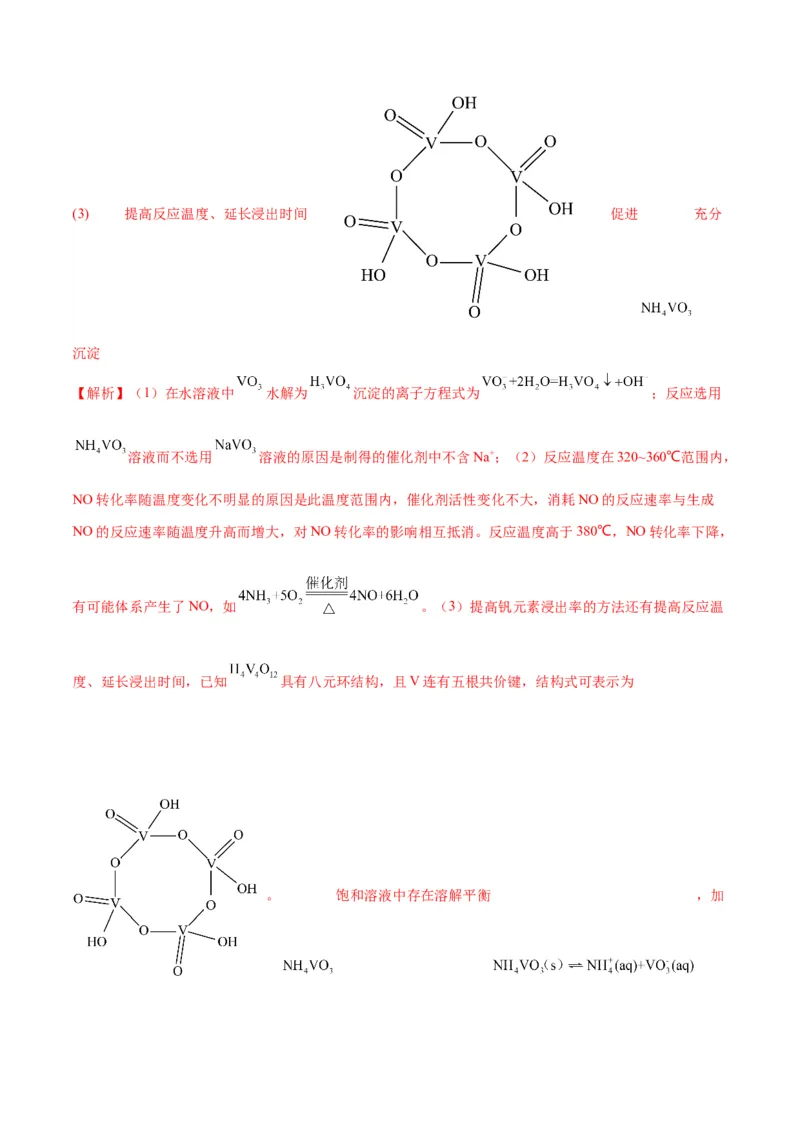
②通过萃取可分离钒和钨,在得到的钒酸中含有 。已知 具有八元环结构,其结构式可表示
为 。
③向pH=8的 溶液中加入过量的 溶液,生成 沉淀。已知: ,
加过量 溶液的目的是 。
【答案】(1) 制得的催化剂中不含Na+
(2) 在该温度范围内,催化剂活性变化不大,消耗NO的反应速率与生成NO的反应速率随温度升高而
增大,对NO转化率的影响相互抵消(3) 提高反应温度、延长浸出时间 促进 充分
沉淀
【解析】(1)在水溶液中 水解为 沉淀的离子方程式为 ;反应选用
溶液而不选用 溶液的原因是制得的催化剂中不含Na+;(2)反应温度在320~360℃范围内,
NO转化率随温度变化不明显的原因是此温度范围内,催化剂活性变化不大,消耗NO的反应速率与生成
NO的反应速率随温度升高而增大,对NO转化率的影响相互抵消。反应温度高于380℃,NO转化率下降,
有可能体系产生了NO,如 。(3)提高钒元素浸出率的方法还有提高反应温
度、延长浸出时间,已知 具有八元环结构,且V连有五根共价键,结构式可表示为
。 饱和溶液中存在溶解平衡 ,加过量 溶液有利于增加铵根离子浓度,促进平衡向析出沉淀的方向移动,提高 的含量,促进
充分沉淀。
2.(2022·江苏卷,14)硫铁化合物( 、 等)应用广泛。
(1)纳米 可去除水中微量六价铬 。在 的水溶液中,纳米 颗粒表面带正电荷,
主要以 、 、 等形式存在,纳米 去除水中 主要经过“吸附→反应→沉淀”的过
程。
已知: , ; 电离常数分别为 、 。
①在弱碱性溶液中, 与 反应生成 、 和单质S,其离子方程式为_______。
②在弱酸性溶液中,反应 的平衡常数K的数值为_______。
③在 溶液中,pH越大, 去除水中 的速率越慢,原因是_______。
(2) 具有良好半导体性能。 的一种晶体与 晶体的结构相似,该 晶体的一个晶胞中
的数目为_______,在 晶体中,每个S原子与三个 紧邻,且 间距相等,如图给出了 晶胞
中的 和位于晶胞体心的 ( 中的 键位于晶胞体对角线上,晶胞中的其他 已省略)。如图中用
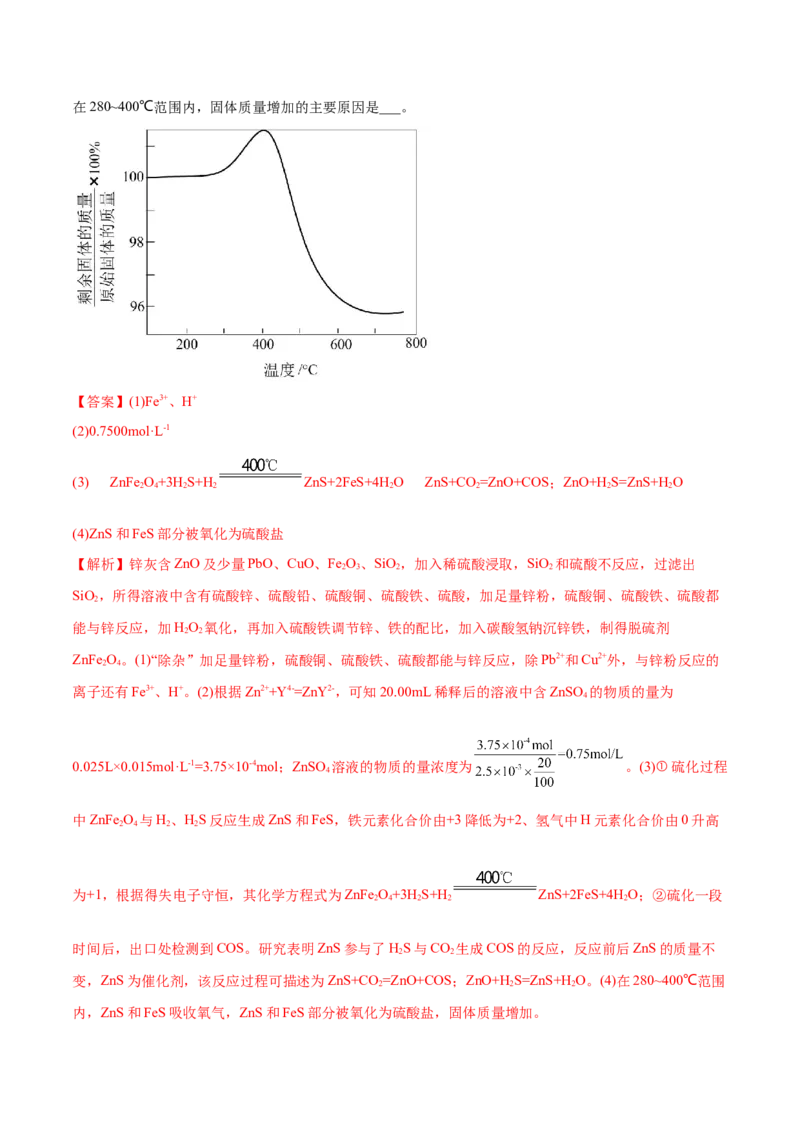
“-”将其中一个S原子与紧邻的 连接起来_______。(3) 、 在空气中易被氧化,将 在空气中氧化,测得氧化过程中剩余固体的质量与起始 的
质量的比值随温度变化的曲线如图所示。 时, 氧化成含有两种元素的固体产物为_______(填化
学式,写出计算过程)。
【答案】(1) 5 c(OH-)越大, 表面吸附的
的量越少, 溶出量越少, 中 物质的量分数越大
(2)4
(3)Fe O;设 氧化成含有两种元素的固体产物化学式为FeO, ,则
2 3 x,则56+16x=80.04,x= ,即固体产物为Fe O
2 3
【解析】(1)在弱碱性溶液中, 与 反应生成 、 和单质S的离子方程式为:
;反应 的平衡常数K=
,由题目信息可知, , 电离常数 ,所以
K= = =5 ;在 溶液中,pH越大, 去除水中 的速率越慢,
是由于c(OH-)越大, 表面吸附的 的量越少, 溶出量越少, 中 物质的量分数越大。
(2)因为 的晶体与 晶体的结构相似,由NaCl晶体结构可知,一个 晶胞含有4个 和4
个Cl,则该 晶体的一个晶胞中 的数目也为4; 晶体中,每个S原子与三个 紧邻,且
间距相等,根据 晶胞中的 和 的位置( 中的 键位于晶胞体对角线上)可知,每个S原子与
键所在体对角线上距离最近的顶点相邻的三个面的三个面心位置的 紧邻且间距相等,其中一个S
原子与紧邻的 连接图如下: 。(3)有图可知, 时,氧化过程中剩余固体的质量与起始 的质量的比值为66.7%,设 氧化成含有两种元素的固体产物化学式为FeO,
x
,则 ,56+16x=80.04,x= ,所以固体产物为
Fe O;故答案为:Fe O;设 氧化成含有两种元素的固体产物化学式为FeO, ,则
2 3 2 3 x
,则56+16x=80.04,x= ,即固体产物为Fe O。
2 3
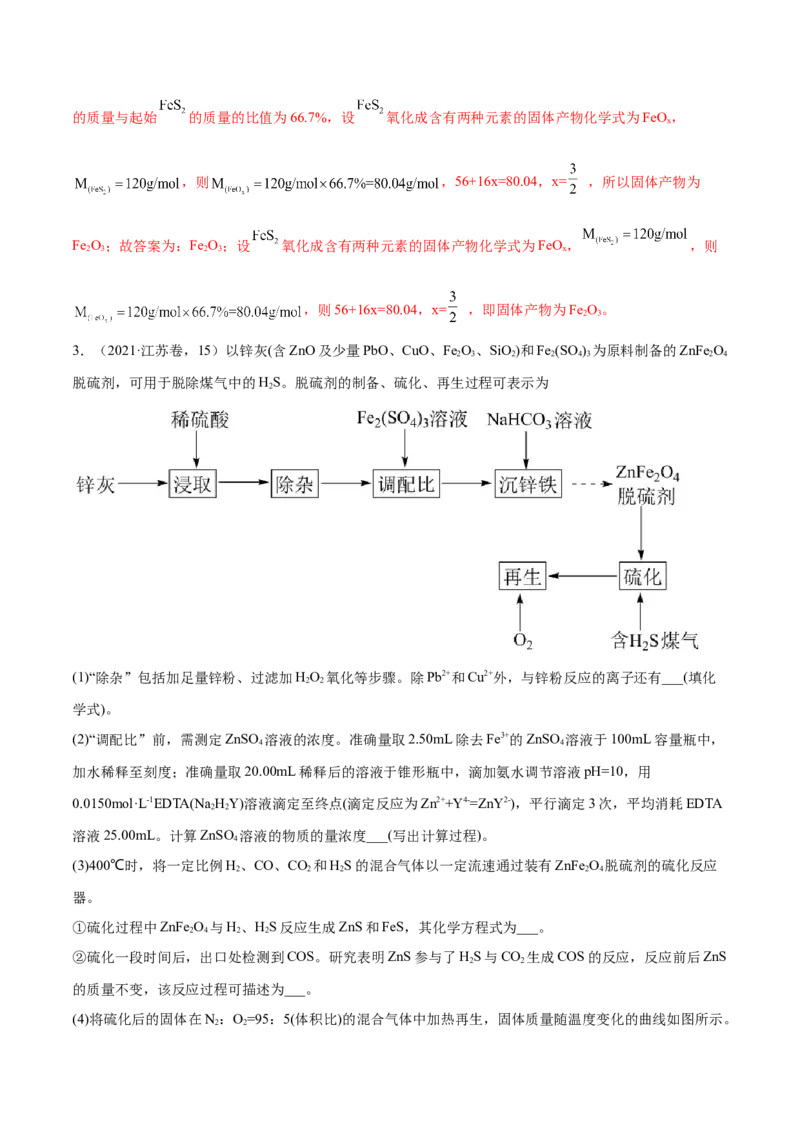
3.(2021·江苏卷,15)以锌灰(含ZnO及少量PbO、CuO、Fe O、SiO)和Fe (SO ) 为原料制备的ZnFe O
2 3 2 2 4 3 2 4
脱硫剂,可用于脱除煤气中的HS。脱硫剂的制备、硫化、再生过程可表示为
2
(1)“除杂”包括加足量锌粉、过滤加HO 氧化等步骤。除Pb2+和Cu2+外,与锌粉反应的离子还有___(填化
2 2
学式)。
(2)“调配比”前,需测定ZnSO 溶液的浓度。准确量取2.50mL除去Fe3+的ZnSO 溶液于100mL容量瓶中,
4 4
加水稀释至刻度;准确量取20.00mL稀释后的溶液于锥形瓶中,滴加氨水调节溶液pH=10,用
0.0150mol·L-1EDTA(Na HY)溶液滴定至终点(滴定反应为Zn2++Y4-=ZnY2-),平行滴定3次,平均消耗EDTA
2 2
溶液25.00mL。计算ZnSO 溶液的物质的量浓度___(写出计算过程)。
4
(3)400℃时,将一定比例H、CO、CO 和HS的混合气体以一定流速通过装有ZnFe O 脱硫剂的硫化反应
2 2 2 2 4
器。
①硫化过程中ZnFe O 与H、HS反应生成ZnS和FeS,其化学方程式为___。
2 4 2 2
②硫化一段时间后,出口处检测到COS。研究表明ZnS参与了HS与CO 生成COS的反应,反应前后ZnS
2 2
的质量不变,该反应过程可描述为___。
(4)将硫化后的固体在N:O=95:5(体积比)的混合气体中加热再生,固体质量随温度变化的曲线如图所示。
2 2在280~400℃范围内,固体质量增加的主要原因是___。
【答案】(1)Fe3+、H+
(2)0.7500mol·L-1
(3) ZnFe O+3H S+H ZnS+2FeS+4H O ZnS+CO =ZnO+COS;ZnO+H S=ZnS+H O
2 4 2 2 2 2 2 2
(4)ZnS和FeS部分被氧化为硫酸盐
【解析】锌灰含ZnO及少量PbO、CuO、Fe O、SiO,加入稀硫酸浸取,SiO 和硫酸不反应,过滤出
2 3 2 2
SiO,所得溶液中含有硫酸锌、硫酸铅、硫酸铜、硫酸铁、硫酸,加足量锌粉,硫酸铜、硫酸铁、硫酸都
2
能与锌反应,加HO 氧化,再加入硫酸铁调节锌、铁的配比,加入碳酸氢钠沉锌铁,制得脱硫剂
2 2
ZnFe O。(1)“除杂”加足量锌粉,硫酸铜、硫酸铁、硫酸都能与锌反应,除Pb2+和Cu2+外,与锌粉反应的
2 4
离子还有Fe3+、H+。(2)根据Zn2++Y4-=ZnY2-,可知20.00mL稀释后的溶液中含ZnSO 的物质的量为
4
0.025L×0.015mol·L-1=3.75×10-4mol;ZnSO 溶液的物质的量浓度为 。(3)①硫化过程
4
中ZnFe O 与H、HS反应生成ZnS和FeS,铁元素化合价由+3降低为+2、氢气中H元素化合价由0升高
2 4 2 2
为+1,根据得失电子守恒,其化学方程式为ZnFe O+3H S+H ZnS+2FeS+4H O;②硫化一段
2 4 2 2 2
时间后,出口处检测到COS。研究表明ZnS参与了HS与CO 生成COS的反应,反应前后ZnS的质量不
2 2
变,ZnS为催化剂,该反应过程可描述为ZnS+CO =ZnO+COS;ZnO+H S=ZnS+H O。(4)在280~400℃范围
2 2 2
内,ZnS和FeS吸收氧气,ZnS和FeS部分被氧化为硫酸盐,固体质量增加。1.化工流程图的结构特点
2.流程中的操作及条件控制
(1)物质的分离与提纯
操作目的 答题指导
固体与液体的分离;要分清楚需要的物质在滤液中还是在滤渣中。滤渣是难
过滤
溶的物质,如SiO、PbSO、难溶的金属氢氧化物和碳酸盐等
2 4
选用合适的萃取剂(如四氯化碳、金属萃取剂),萃取后,静置、分液——将
萃取与分液 分液漏斗玻璃塞的凹槽与分液漏斗口的小孔对准。下层液体从下口放出,上
层液体从上口倒出
①转化为目标产物的价态
加入氧化剂
(或还原剂) ②除去杂质离子(如把Fe2+氧化成 Fe3+,而后调溶液的 pH,使其转化为
Fe(OH) 沉淀除去)
3
①生成硫化物沉淀(如加入硫化钠、硫化铵、硫化亚铁等)
加入沉淀剂 ②加入可溶性碳酸盐,生成碳酸盐沉淀
③加入氟化钠,除去Ca2+、Mg2+
洗涤试剂 适用范围 目的
除去固体表面吸附着的××杂
冷水 产物不溶于水 质;可适当降低固体因为溶解
而造成的损失
蒸馏水
有特殊的物质其溶 除去固体表面吸附着的××杂
热水 解度随着温度升高 质;可适当降低固体因为温度
而下降 变化溶解而造成的损失
洗涤晶体 有机溶剂 固体易溶于水、难 减少固体溶解;利用有机溶剂
的挥发性除去固体表面的水
(酒精、丙酮等) 溶于有机溶剂 分,产品易干燥
对纯度要求不高的
饱和溶液 减少固体溶解
产品
除去固体表面吸附着的可溶于
酸、碱溶液 产物不溶于酸、碱
酸、碱的杂质;减少固体溶解
洗涤沉淀方法:向过滤器中加入蒸馏水至浸没沉淀,待水自然流下后,重复
以上操作2~3次
(2)常见的流程中的条件控制
条件控制 答题指导
控制溶液的 ①调节溶液的酸碱性,使金属离子形成氢氧化物沉淀析出(或抑制水解)②“酸作用”还可除去氧化物(膜)
pH ③“碱作用”还可除去油污,除去铝片氧化膜,溶解铝、二氧化硅等
④特定的氧化还原反应需要的酸性条件(或碱性条件)
①防止副反应的发生
②使化学平衡移动;控制化学反应的方向
③控制固体的溶解与结晶
控制温度(常 ④控制反应速率;使催化剂达到最大活性
用水浴、冰 ⑤升温:促进溶液中的气体逸出,使某物质达到沸点挥发
水浴或油浴)
⑥加热煮沸:促进水解,聚沉后利于过滤分离
⑦趁热过滤:减少因降温而析出的溶质的量
⑧降温:防止物质高温分解或挥发;降温(或减压)可以减少能源成本,降低
对设备的要求
(3) 对所加试剂的要求
试剂 目的 追问
酸液不能加过多,否则会造
硫酸 酸溶
成后续调pH时消耗过多试剂
盐酸不能加过多,否则后续
盐酸 酸溶 可能会与KMnO 等氧化剂反应
4
并生成有毒气体Cl
2
碱液不能加过多,否则会造
碱液 碱溶(溶解Al、AlO 等物质)
2 3
成后续调pH时消耗过多试剂
作还原剂(还原MnO、Fe3+ 温度不宜过高,温度越高,
2
SO
2
等) SO 的溶解度越小
2
作还原剂(还原MnO、Fe3+ 实际用量高于理论量:部分
2
Na SO
2 3
等) Na SO 被空气中的O 氧化
2 3 2
锌粉过量的目的:将溶液中
Zn 置换溶液中的Cu2+
的Cu2+除净
pH太小,Ca2+、Mg2+去除率
NHF、 降低的原因:pH太小,溶液
4
除去Ca2+、Mg2+
NaF 中的F-与H+结合生成HF,
使溶液中的F-浓度减小
pH太小,Cu2+、Hg2+去除率
降低的原因:pH太小,溶液
NaS、 除重金属离子(如Cu2+、Hg2
2
中的S2-与H+结合生成HS-、
FeS +)
HS,使溶液中的S2-浓度减
2
小
3.破题方法
(1)首尾分析法
破解无机物制备工艺流程原理与过程。对一些线性流程工艺(从原料到产品为“一条龙”的生产工序)题,首先对比分析流程图中第一种物质(原材料)与最后一种物质(产品),找出原材料与产品之间的关系,弄清
生产过程中原材料转化为产品的基本原理和分离、提纯的化工工艺,然后结合题设的问题,逐一推敲解答。
(2)截段分析法
对于用同样的原材料生产两种或多种产品(包括副产品)的工艺流程题,用截段分析法更容易找到解题的切
入点。关键在于看清主、副产品是如何分开的,以此确定截几段更合适,一般截段以产品为基准点。
(3)交叉分析法
有些化工生产选用多组原材料,先合成一种或几种中间产品,再用这一中间产品与部分其他原材料生产所
需的主要产品,这种题适合用交叉分析法。就是将提供的工艺流程示意图结合常见化合物的制取原理划分
成几条生产流水线,然后上下交叉分析。
(4)掌握“5种”原料预处理(研磨、水浸、酸浸、灼烧、煅烧)的作用和“5种”控制反应条件(调溶液
pH、控制温度、使用催化剂、趁热过滤、冰水洗涤)的目的。
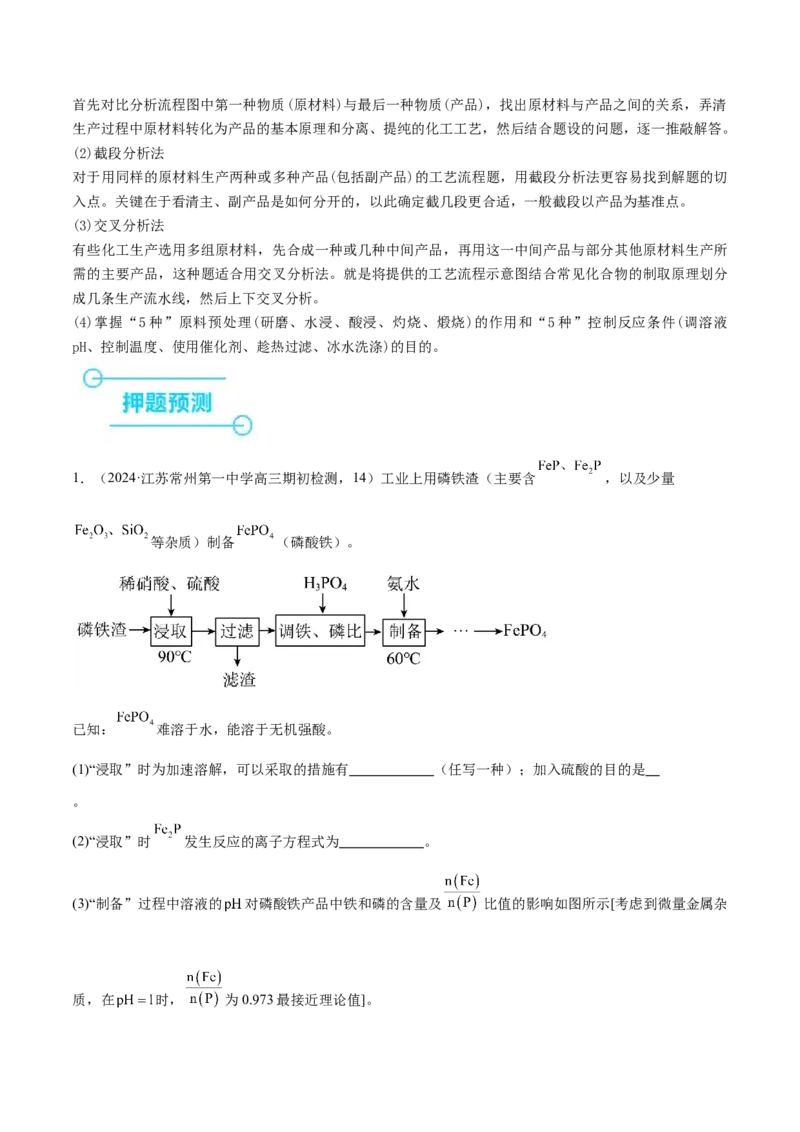
1.(2024·江苏常州第一中学高三期初检测,14)工业上用磷铁渣(主要含 ,以及少量
等杂质)制备 (磷酸铁)。
已知: 难溶于水,能溶于无机强酸。
(1)“浸取”时为加速溶解,可以采取的措施有 (任写一种);加入硫酸的目的是
。
(2)“浸取”时 发生反应的离子方程式为 。
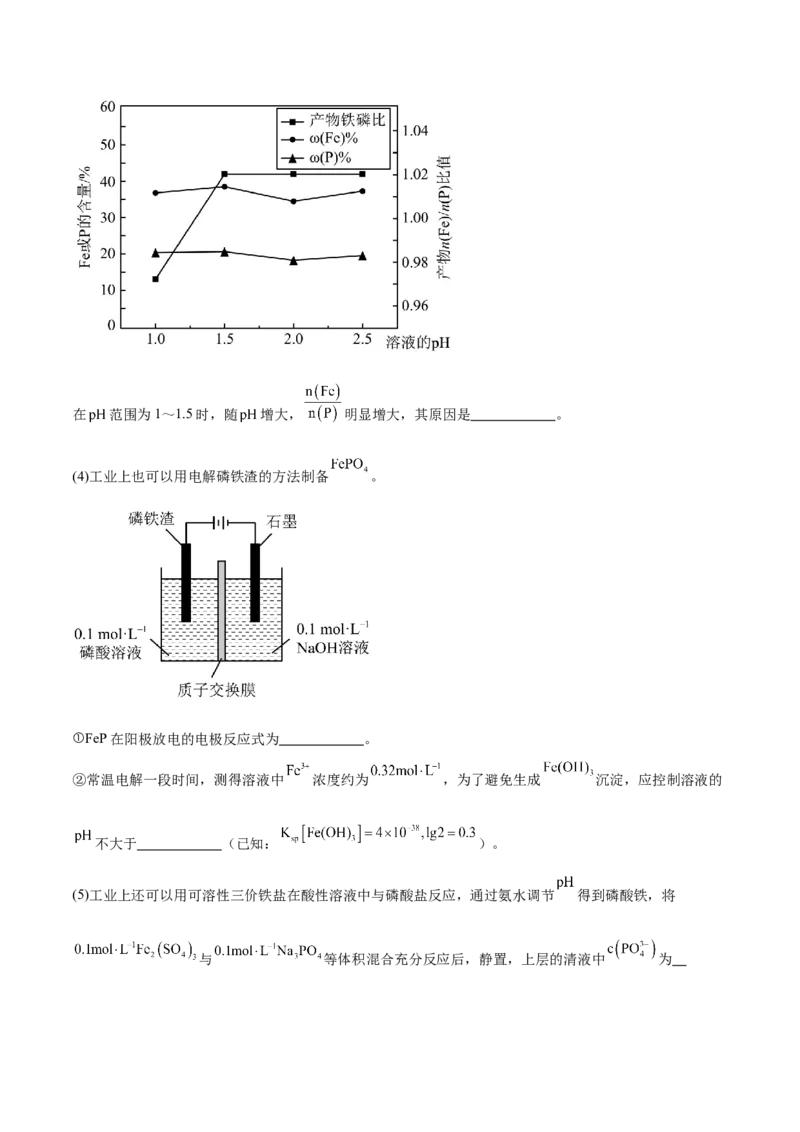
(3)“制备”过程中溶液的 对磷酸铁产品中铁和磷的含量及 比值的影响如图所示[考虑到微量金属杂
质,在 时, 为0.973最接近理论值]。在 范围为1~1.5时,随 增大, 明显增大,其原因是 。
(4)工业上也可以用电解磷铁渣的方法制备 。
①FeP在阳极放电的电极反应式为 。
②常温电解一段时间,测得溶液中 浓度约为 ,为了避免生成 沉淀,应控制溶液的
不大于 (已知: )。
(5)工业上还可以用可溶性三价铁盐在酸性溶液中与磷酸盐反应,通过氨水调节 得到磷酸铁,将
与 等体积混合充分反应后,静置,上层的清液中 为。【已知: 】
【答案】(1) 将磷铁渣粉碎或适当增大硝酸浓度或搅拌 保持体系的酸度,防止生成FePO
4
(2)3Fe P+29H++11NO =6Fe3++11NO↑+3H PO +10H O
2 3 4 2
(3)pH增大,促进促进Fe3+水解,生成了难溶性的氢氧化铁混入产品中
(4) FeP+4HO—8e—=FePO+8H+ 1.7
2 4
(5)2.6×10−21
【解析】由题给流程控制,向磷铁渣中加入稀硝酸和硫酸在90℃条件下浸取,将铁元素和磷元素转化为铁
离子和磷酸,二氧化硅与混酸不反应,过滤得到含有二氧化硅的滤渣和滤液;向滤液中加入磷酸调节溶液
中铁元素和磷元素的含量比,加入氨水调节溶液pH,在60℃条件下将溶液中的铁元素、磷元素转化为磷
酸铁沉淀,经分离提纯得到磷酸铁。(1)将磷铁渣粉碎、适当增大硝酸浓度、搅拌等措施可以加快“浸
取”等溶解速率;硝酸具有强氧化性,由分析可知,加入稀硝酸和硫酸在90℃条件下浸取的目的是将铁元
素和磷元素转化为铁离子和磷酸,则加入硫酸的目的是为了保持体系的酸度,防止生成磷酸铁沉淀。
(2)由分析可知,加入稀硝酸和硫酸在90℃条件下浸取的目的是将铁元素和磷元素转化为铁离子和磷酸,
则Fe P与混酸反应生成铁离子、磷酸、一氧化氮和水,反应的离子方程式为3Fe P+29H++11NO =6Fe3+
2 2
+11NO↑+3H PO +10H O。(3)铁离子在溶液中水解生成氢氧化铁和氢离子,溶液pH增大时,铁离子的
3 4 2
水解程度增大生成氢氧化铁沉淀,导致在pH范围为1~1.5时,随pH增大, 明显增大。(4)①由
图可知,与直流电源正极相连的磷铁渣为电解池的阳极,水分子作用下FeP在阳极失去电子发生氧化反应
生成磷酸铁和氢离子,电极反应式为FeP+4HO—8e—=FePO+8H+;②由溶度积可知,为了避免溶液中铁离
2 4
子转化为氢氧化铁沉淀,溶液中氢氧根离子浓度小于 =5×10—13mol/L,则溶液的pH小于14—
12—lg2=1.7。(5)由题意可知,浓度均为0.1mol/L 硫酸铁和磷酸钠等体积混合后,溶液中铁离子浓度为
=0.05mol/L,则由溶度积可知,溶液中磷酸根离子的浓度为 =2.6×10−21mol/L。
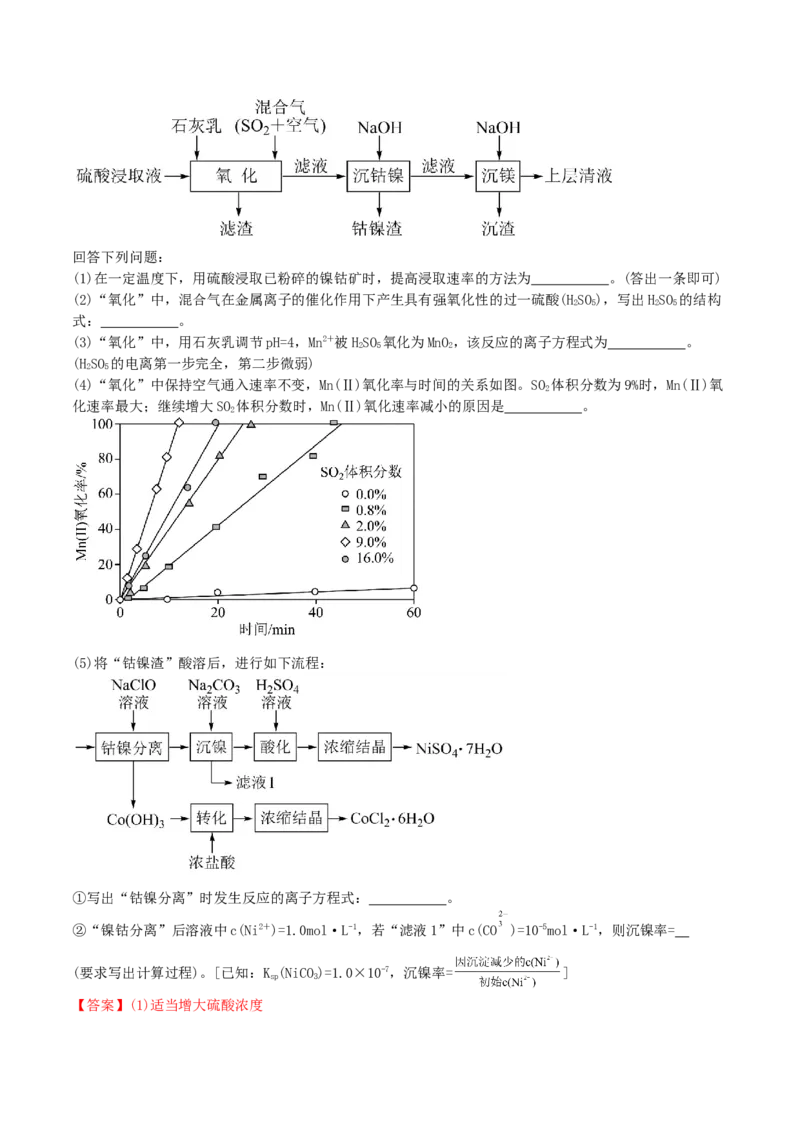
2.(2024·江苏南通如东中学,如东一高等高三12月学情调研,14)某工厂采用如下工艺处理镍钴矿硫
酸浸取液(含Ni2+、Co2+、Fe2+、Fe3+、Mg2+和Mn2+),实现镍、钴、镁元素的回收。回答下列问题:
(1)在一定温度下,用硫酸浸取已粉碎的镍钴矿时,提高浸取速率的方法为 。(答出一条即可)
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO),写出HSO 的结构
2 5 2 5
式: 。
(3)“氧化”中,用石灰乳调节pH=4,Mn2+被HSO 氧化为MnO,该反应的离子方程式为 。
2 5 2
(HSO 的电离第一步完全,第二步微弱)
2 5
(4)“氧化”中保持空气通入速率不变,Mn(Ⅱ)氧化率与时间的关系如图。SO 体积分数为9%时,Mn(Ⅱ)氧
2
化速率最大;继续增大SO 体积分数时,Mn(Ⅱ)氧化速率减小的原因是 。
2
(5)将“钴镍渣”酸溶后,进行如下流程:
①写出“钴镍分离”时发生反应的离子方程式: 。
②“镍钴分离”后溶液中c(Ni2+)=1.0mol·L-1,若“滤液1”中c(CO )=10-5mol·L-1,则沉镍率=
(要求写出计算过程)。[已知:K (NiCO)=1.0×10-7,沉镍率= ]
sp 3
【答案】(1)适当增大硫酸浓度(2)
(3)HO+Mn2++HSO=MnO+SO+3H+
2 2
(4)SO 有还原性,过多将会降低HSO 的浓度,降低Mn(Ⅱ)氧化速率
2 2 5
(5) ① ClO-+2Co2++5HO=2Co(OH)↓+Cl-+4H+ ②99%或0.99
2 3
【解析】混合气中的氧气具有强氧化性,酸性条件下,将Fe2+和Mn2+转化为为Fe(OH) 和MnO,Ca2+被与
3 2
SO反应生成CaSO 沉淀,Ni2+、Mg2+先后转化为氢氧化物沉淀,而实现镍、钴、镁元素的回收。(1)提高
4
浸取率可以适当增大硫酸浓度、适当升高温度、将镍钴矿粉碎增大接触面积等方法。(2)过一硫酸可以
看做过氧化氢中的一个氢原子被磺酸基取代,因此结构式为 。(3)HSO 的电离第一步完
2 5
全,第二步微弱,S主要以HSO存在,-1价的O将Mn2+氧化为MnO,方程式为HO+Mn2++HSO=MnO+SO+
2 2 2
3H+。(4)SO 有还原性,SO 的体积分数较大时,SO 将HSO 还原,Mn(Ⅱ)氧化速率减小。(5)滤液中加
2 2 2 2 5
NaClO将Co2+氧化为Co(OH),反应的离子方程式为ClO-+2Co2++5HO=2Co(OH)↓+Cl-+4H+;再加NaCO,将
3 2 3 2 3
Ni2+转化为NiCO 沉淀,离子方程式为Ni2++CO=NiCO↓;NiCO 中加HSO,反应生成NiSO,经蒸发浓缩、冷
3 3 3 2 4 4
却结晶,可得NiSO∙7HO;。c(CO)=10-5mol/L,根据K(NiCO)=1.0×10-7可知,c(Ni2+)=
4 2 sp 3
=0.01mol/L,沉镍率= = =0.99。
3.(2024·江苏南京金陵中学期中,14)工业上可由菱锌矿(主要成分为 ,还含有Ni、Cd、Fe、Mn
等元素)制备ZnO。工艺如图所示:
已知:①“酸浸”后的溶液 ,所含金属离子主要有 、 、 、 、 。
②弱酸性溶液中 氧化 时,产物中含Mn元素物质只有 。
(1)“氧化除杂”时, 与 的离子方程式为 。
(2)“沉锌”生成碱式碳酸锌[ ]沉淀,写出生成该沉淀的化学方程式: 。
(3)“高温灼烧”后获得ZnO。已知ZnO的一种晶体晶胞是立方晶胞(如图),请在下图中画出该晶胞沿z轴方
向的平面投影图 。(4)测定氧化锌样品纯度(杂质不参与反应):称取1.000g样品,酸溶后,配制成250mL溶液。用移液管移取
25.00mL溶液于锥形瓶,调节pH至7~8,加入几滴铬黑T(用 表示)做指示剂,用 的
EDTA( )标准液滴定其中的 (反应方程式为 , ),
平行滴定三次,平均消耗EDTA标准液15.12mL。(已知 呈蓝色、 呈无色、 呈酒红色)。
①滴定终点时的现象为 。
②计算ZnO样品的纯度 。(保留四位有效数字,写出计算过程)
(5)ZnO有棒状ZnO(r-ZnO)、片状ZnO(p-ZnO)两种。均可用作 选择性加氢转化为 的催化剂。在
ZnO催化剂存在下,将 与 混合,同时发生以下两个反应:
反应Ⅰ
反应Ⅱ
控制一定的 和 初始投料比,在相同压强下,经过相同反应时间测得如下实验数据(其中“甲醇选择
性”是指转化的 中生成甲醇的百分比)已知:p-ZnO表面合成 的生成活化能 ,r-ZnO表面合成 的生成活化能
①在280~320℃范围内,相同催化剂条件下,随温度升高, 与CO的产率均提高,而甲醇的选择性
降低的可能原因是 ;
②在280~320℃范围内,比较图a和图b两种ZnO催化剂催化 加氢性能,说明在 加氢合成甲醇时
优先选用p-ZnO催化剂的原因: 。
【答案】(1)2MnO +3Mn2++2H O=5MnO ↓+4H+
2 2
(2)
(3)
(4) 加入最后半滴标准液,溶液由酒红色变为蓝色,且30s不变色
(5) 反应Ⅰ正反应放热,升高温度,平衡逆向移动,导致温度升高甲醇的选择性降低 选用p-ZnO
催化剂使反应Ⅰ速率快,在相同时间内生成的甲醇多
【解析】由菱锌矿(主要成分为 ,还含有Ni、Cd、Fe、Mn等元素)制备ZnO,加入稀硫酸“溶浸”
后得到含 、 、 、 、 的滤液,滤渣为不溶于酸的杂质,滤液调节pH后使铁离子转
化为Fe(OH) ,加入KMnO “氧化除杂”使锰离子转化为MnO ,除去Fe3+、Mn2+;接着“还原除杂”除去
3 4 2Ni2+、Cd2+;最后向含ZnSO 的溶液中加入NaCO 溶液生成碱式碳酸锌[ ]沉淀,
4 2 3
碱式碳酸锌经“高温灼烧”得到ZnO。(1)在“氧化除杂”时, 与 发生氧化还原反应产生
MnO ,根据得失电子守恒、电荷守恒及原子守恒,可得反应的离子方程式为2MnO +3Mn2+
2
+2H O=5MnO ↓+4H+。(2)根据分析,向含ZnSO 的溶液中加入NaCO 溶液生成碱式碳酸锌[
2 2 4 2 3
]沉淀,反应的化学的方程式为
。(3)观察题给晶胞结构可知,
晶胞在z轴的投影情况是锌原子位于正方形的四个顶点上、四条棱的中心和面心上,4个氧原子分别位于
面对角线离顶点 处,可用图示表示为 。(4)①滴入 标准溶液前,Zn2+与X-
形成ZnX+使溶液呈酒红色,达到滴定终点时,Zn2+被完全消耗生成无色的ZnY2-,溶液中含有X-而呈蓝色,
由此可得出滴定终点时的现象为:加入最后半滴标准液,溶液由酒红色变为蓝色,且30s不变色;②根据
滴定原理可得关系式ZnO~Zn2+~H Y2-,则产品中
2
,故ZnO的含量为
。(5)①生成甲醇的反应是反应Ⅰ,反应Ⅰ正反应放热,在
280~320℃范围内,相同催化剂条件下,升高温度,平衡逆向移动,导致温度升高甲醇的选择性降低;②
催化剂只影响速率而不能改变平衡,图中数据不是达到平衡后测得的数据,而是反应相同时间测得的数据,
p-ZnO表面合成 的生成活化能比r-ZnO表面合成 的生成活化能小,活化能越小,反应速率越快,因此选用p-ZnO催化剂使反应Ⅰ速率快,在相同时间内生成的甲醇多。
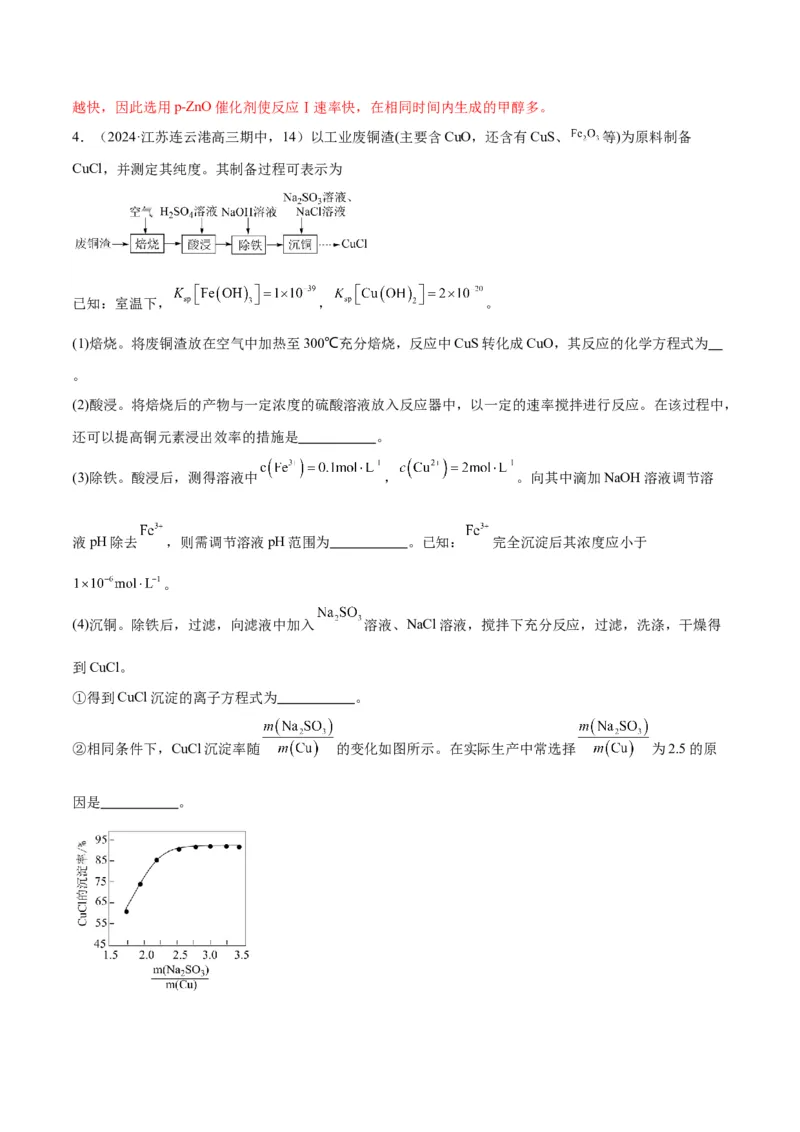
4.(2024·江苏连云港高三期中,14)以工业废铜渣(主要含CuO,还含有CuS、 等)为原料制备
CuCl,并测定其纯度。其制备过程可表示为
已知:室温下, , 。
(1)焙烧。将废铜渣放在空气中加热至300℃充分焙烧,反应中CuS转化成CuO,其反应的化学方程式为
。
(2)酸浸。将焙烧后的产物与一定浓度的硫酸溶液放入反应器中,以一定的速率搅拌进行反应。在该过程中,
还可以提高铜元素浸出效率的措施是 。
(3)除铁。酸浸后,测得溶液中 , 。向其中滴加NaOH溶液调节溶
液pH除去 ,则需调节溶液pH范围为 。已知: 完全沉淀后其浓度应小于
。
(4)沉铜。除铁后,过滤,向滤液中加入 溶液、NaCl溶液,搅拌下充分反应,过滤,洗涤,干燥得
到CuCl。
①得到CuCl沉淀的离子方程式为 。
②相同条件下,CuCl沉淀率随 的变化如图所示。在实际生产中常选择 为2.5的原
因是 。(5)测定CuCl的纯度。称取0.2500g样品,迅速加入装有足量三氯化铁溶液的锥形瓶中不断摇动,待样品溶
解后加适量水和2滴邻菲啰啉-硫酸亚铁指示液,用 标准溶液滴定至终点,消耗
溶液24.00mL。已知: , 。计算样品中
CuCl的纯度 。(写出计算过程,否则不得分!)
【答案】(1)
(2)适当升高反应的温度
(3)
(4) ① ②加快还原 的反应速率;随着反应的进行,溶
液的酸性逐渐增强, 与 结合生成 从溶液中逸出
(5) ,由题意可得关系式: ,
,
,CuCl的纯度
【解析】废铜渣经空气焙烧后得到 、CuO和SO , 、CuO加入硫酸酸浸得到Fe3+、Cu2+,加入
2
NaOH调节pH使Fe3+沉淀完全,向溶液中加入亚硫酸钠溶液和NaCl溶液使其转化为CuCl,再经洗涤、干
燥可得产品。(1)空气中氧气具有氧化性,“焙烧”时空气中氧气在加热条件下将铜元素充分氧化为氧
化铜、硫元素氧化为二氧化硫气体, 。(2)提高铜元素浸出效率的措施是适当升高反应的温度、适当提高酸液的浓度、将焙烧产物粉碎等。(3)铁离子完全沉淀,则
,pOH=11,pH=3;;沉淀过程中铜离子不能
沉淀,则 ,pOH=10,pH=4;故需调节溶液
pH范围为 。(4)①得到CuCl沉淀的反应为铜离子和还原剂亚硫酸根离子发生氧化还原反应
得到硫酸根离子和亚铜离子,亚铜离子和氯离子生成氯化亚铜沉淀,离子方程式为
。②在实际生产中常选择 为2.5的原因是:此时亚
硫酸钠加快还原 的反应速率已经使得氯化亚铜的沉淀率较高,且反应后溶液显酸性,如果继续增加亚
硫酸钠量,则会导致 与 结合生成 从溶液中逸出。(5)由关系式可知, ,则
样品中CuCl的物质的量为 ,CuCl的纯度
。
5.(2024·江苏百师联盟高三开学考试,14)石油开采和炼制过程中产生的污水含有溶解性的 以及难
溶的硫化物,对污水进行处理的同时可回收化工原料。已知: 在水中溶解度为1∶2.6,易挥发。回答下
列问题:
(1)沉淀法处理含硫废水:
向含硫废水中加入适量 的溶液,产生黑色沉淀且溶液的pH降低。解释溶液的pH降低的原因:
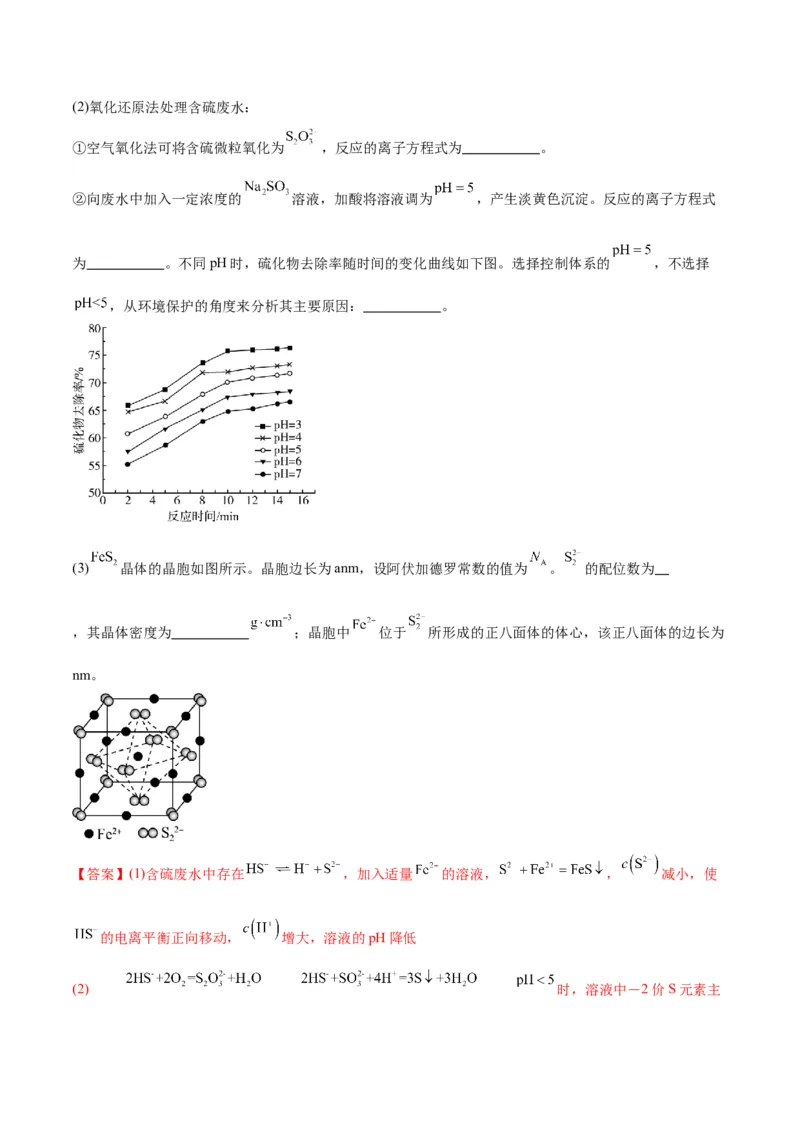
。(2)氧化还原法处理含硫废水:
①空气氧化法可将含硫微粒氧化为 ,反应的离子方程式为 。
②向废水中加入一定浓度的 溶液,加酸将溶液调为 ,产生淡黄色沉淀。反应的离子方程式
为 。不同pH时,硫化物去除率随时间的变化曲线如下图。选择控制体系的 ,不选择
,从环境保护的角度来分析其主要原因: 。
(3) 晶体的晶胞如图所示。晶胞边长为anm,设阿伏加德罗常数的值为 。 的配位数为
,其晶体密度为 ;晶胞中 位于 所形成的正八面体的体心,该正八面体的边长为
nm。
【答案】(1)含硫废水中存在 ,加入适量 的溶液, , 减小,使
的电离平衡正向移动, 增大,溶液的pH降低
(2) 时,溶液中―2价S元素主要以 的形式存在,常温下 的溶解度为1∶2.6,酸性强使 更易逸出, 有剧毒会污染环境
(3) 6
【解析】(1)污水含有溶解性的 ,存在 ,加入适量 的溶液, ,
减小,使 的电离平衡正向移动, 增大,溶液的pH降低。(2)①氧气具有氧化性,
被 氧化为 ,根据得失电子守恒,反应的离子方程式为 ;② 具有还原性,
和氧化性离子 在酸性条件下发生归中反应生成S,同时生成水,反应的离子方程式为
;酸性太强,容易发生 ,通过已知信息 在水中溶解度为
1∶2.6,可知 易挥发,生成的 以气体的形式逸出, 有剧毒,会污染环境。(3)由图可知,
处于 构成的八面体中,结合化学式 可知,与 等距离且最近的 有6个,所以 的配位数是
6;晶胞边长为 ,晶胞体积 ,该晶胞中 个数 , 个数
,晶胞质量为 , ;分析晶胞结构可
知,晶胞中 位于 所形成的正八面体的体心,该正八面体的边长为每个面对角线长度的一半,即正
八面体的边长 。
6.(2024·江苏海安高三第一次考试,14)门捷列夫在研究周期表时预言了“类铝”元素镓,镓(Ga)位于
元素周期表第IIIA族,高纯镓广泛用于半导体材料、光电材料、光学材料等领域。(1)一种利用炼锌渣(主要含Pb、Zn、Cu、Fe的氧化物和一定量GaCl )为原料制备高纯镓的流程如图所示:
3
已知:(i)电解步骤制取镓时两极均采用惰性电极。
(ii)Cu+Cu2++2Cl-=2CuCl↓,CuCl难溶于水和稀酸;ZnS、GaS 均难溶于水。
2 3
(iii)20℃,K(NH •H O)≈2.0×10-5,K [Ga(OH)]≈1.0×10-35。
b 3 2 sp 3
回答下列问题:
①试剂a(Cu)的主要作用是 。
②滤渣4的主要成份为 。
③已知:Ga3++4OH- [Ga(OH)]- K≈1.0×1034。为探究Ga(OH) 在氨水中能否溶解,计算反应
4 3
Ga(OH) +NH•H O [Ga(OH)]-+NH 的平衡常数K= 。
3 3 2 4
④电解步骤中,阴极的电极反应式为 。
(2)砷化镓(GaAs)太阳能电池为我国“玉兔二号”月球车提供充足能量。GaAs的晶胞结构如图甲所示,将
Mn掺杂到GaAs的晶体中得到稀磁性半导体材料如图乙所示。
①GaAs中Ga的化合价为 。
②在Mn掺杂到GaAs的晶体中每个Mn最近且等距离的As的数目为 。
【答案】(1) ①除去Cl-,防止对电解时产生Cl 污染环境 ②Cu ③2×10-6 ④[Ga(OH) ]-+3e-
2 4
=Ga+4OH-
(2) ①+3 ②4
【解析】炼锌渣主要含Pb、Zn、Cu、Fe的氧化物和一定量GaCl ,用稀硫酸溶解,PbO和硫酸反应生成
3
PbSO 沉淀,过滤得到硫酸锌、硫酸亚铁、硫酸铜、GaCl 溶液,加双氧水把Fe2+氧化为Fe3+,加ZnO调节
4 3
pH生成Fe(OH) 沉淀除Fe,加铜发生Cu+Cu2++2Cl-=2CuCl↓除Cl-,加锌置换出Cu,加氢氧化钠使Ga3+转
3化为[Ga(OH)]-,加NaS生成ZnS沉淀除Zn,电解Na[Ga(OH) ]得到Ga。(1)①根据Cu+Cu2++2Cl-
4 2 4
=2CuCl↓,CuCl难溶于水和稀酸,加入Cu发生反应Cu+Cu2++2Cl-=2CuCl↓除去Cl-,防止对电解时产生Cl
2
污染环境;②金属锌能置换出铜单质,滤渣4的主要成份为Cu;③K(NH •H O)= 2.0×10-
b 3 2
5,K [Ga(OH)]= 1.0×10-35; 1.0×1034,Ga(OH) +NH•H O
sp 3 3 3 2
[Ga(OH)]-+NH 的平衡常数K= 。
4
④电解步骤中,阴极[Ga(OH)]-得电子生成Ga和氢氧根离子,阴极的电极反应式为[Ga(OH)]-+3e-
4 4
=Ga+4OH-。(2)①GaAs中As为-3价,则Ga的化合价为+3。②根据c原子可知,每个Mn最近且等距离
的As的数目为4。
7.(2024·江苏常州高级中学高三开学考试,14)从废钼催化剂(主要成分为MoO 、MoS ,含少量NiS、
3 2
NiO、Fe O 等)中回收利用金属的一种工艺流程如图所示。
2 3
已知:①“沉钼”前钼元素主要以MoO 形式存在;
②该条件下K (NiCO)=1.5×10-7。
sp 3
(1)“焙烧”生成的气体主要成分为 (填化学式)。
(2)“沉钼”的离子方程式为 。
(3)“酸浸”时,控制硫酸浓度,加料完成后,在一定的温度下发生反应。提高镍元素浸出率的方法还有
。(4)“除铁”后所得滤液中c(Ni2+)=1.0mol·L-1,“沉镍”后所得滤液中c( )=1.0×10-5mol·L-1,则沉镍率=
[沉镍率= ×100%,计算过程中不考虑溶液体积变化]。
(5)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
温度 低于30.8℃ 30.8~53.8℃ 53.8~280℃ 高于280℃
晶体形
NiSO •7H O NiSO •6H O 多种结晶水合物 NiSO
态 4 2 4 2 4
从NiSO 溶液获得稳定的NiSO •6H O晶体的操作是: 、洗涤、干燥等。
4 4 2
(6)硫酸镍晶体溶于氨水形成[Ni(NH )]SO 蓝色溶液。[Ni(NH )]SO 中的阳离子具有正八面体结构,该配离
3 6 4 3 6 4
子的结构可表示为 。
【答案】(1)CO 、SO
2 2
(2)2NH +4MoO +6H+= ( NH)MoO · 2H O↓+HO
4 2 4 13 2 2
(3)充分搅拌 、延长浸出时间
(4)98.5%
(5)稍低于53.8℃蒸发浓缩,降温至稍高于30.8℃,趁热过滤
(6)
【解析】废钼催化剂加入纯碱、空气焙烧生成气体有二氧化碳、二氧化硫,物质有钼酸钠、铁、镍的氧化
物,水浸后过滤滤液中的钼酸钠用硝酸铵、硝酸沉钼得到钼酸铵沉淀,滤渣用硫酸酸浸,加碳酸钠沉铁,
加碳酸氢钠沉镍,最后经一系列操作转化为硫酸镍晶体。(1)焙烧时MoO 与碳酸钠发生NaCO+MoO
3 2 3 3
NaMoO +CO ↑、2MoS +2Na CO+7O 2NaMoO +2CO ↑+4SO↑, 根据流程可知,该步骤中Ni
2 4 2 2 2 3 2 2 4 2 2
元素转化成NiO,有2NiS+3O 2NiO+2SO ↑,因此生成气体是二氧化碳和二氧化硫气体。 (2)沉钼
2 2最后得到( NH)MoO · 2H O沉淀,反应的离子有NH 、MoO 和氢离子,离子方程式为2NH +4MoO
4 2 4 13 2
+6H+= ( NH)MoO · 2H O↓+HO。(3)“酸浸”时,控制硫酸浓度,加料完成后,在一定的温度下发
4 2 4 13 2 2
生反应,提高镍元素浸出率的方法还有充分搅拌 、延长浸出时间。(4)根据K (NiCO)=c(Ni2+)·c(CO
sp 3
),“沉镍”后滤液中c(CO )=1.0×10-5mol/L,此时溶液中c(Ni2+)= =1.5×10-2mol/L,
沉镍率= =98.5%。(5)根据流程图可知,制备NiSO •6H O,依据表中信
4 2
息可知,温度在30.8~53.8℃范围析出晶体为NiSO •6H O,因此从NiSO 溶液获得稳定的NiSO •6H O晶体
4 2 4 4 2
的操作是:稍低于53.8℃蒸发浓缩,降温至稍高于30.8℃,趁热过滤、洗涤、干燥等。(6)[Ni(NH )]2+中
3 6
Ni2+提供空轨道,NH 提供孤对电子,形成配合物,该配离子具有正八面体结构,其结构可表示为
3
。
8.(2024·江苏连云港高三第一次调研考试,14)以含钼(Mo)废催化剂(含MoS 以及AlO 、FeO 、CuO
2, 2 3 2 3
等)为原料制备MoO,其过程表示如下:
3
(1) 焙烧。将废催化剂和足量NaOH固体置于焙烧炉中,通入足量空气加热至750 ℃充分反应。焙烧过程
中MoS 转化为NaMoO 的化学方程式为________。
2 2 4
(2) 浸取。将焙烧所得固体加水浸泡,然后过滤、洗涤。过滤后所得滤液中存在的阴离子有 OH-、MoO、
______________ 。 欲 提 高 单 位 时 间 内 钼 的 浸 取 率 , 可 以 采 取 的 措 施 有
____________________________________________________________(任写一点)。
(3) 除 杂 。 向 浸 取 后 的 滤 液 中 通 入 过 量 CO , 过 滤 。 通 入 过 量 CO 的 目 的 是
2 2
______________________________________________________________________________。
(4) 制备。向上述(3)所得滤液中加入硝酸调节溶液的pH小于6,使MoO转化为MoO,然后加入NHNO 充分
7 4 3
反应,析出(NH)MoO ·4HO,灼烧后可得到 MoO 。灼烧(NH)MoO ·4HO 得到 MoO 的化学方程式为
4 6 7 24 2 3 4 6 7 24 2 3
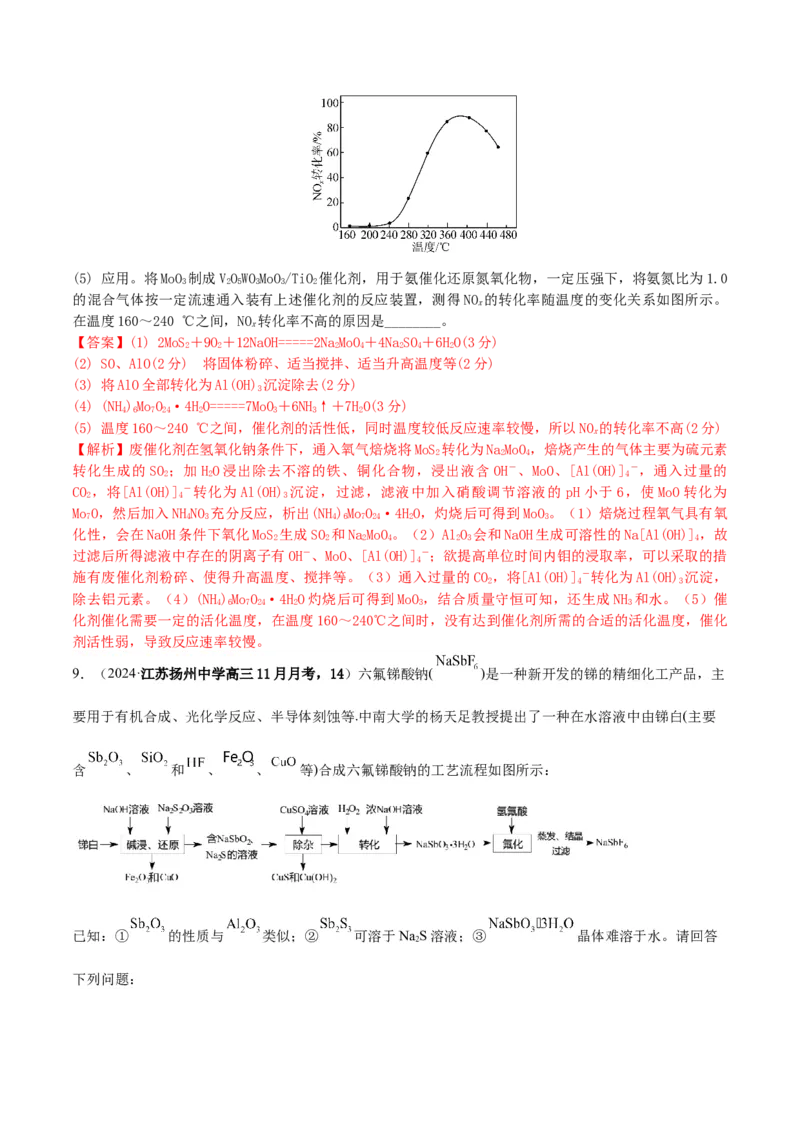
________。(5) 应用。将MoO 制成VOWOMoO/TiO 催化剂,用于氨催化还原氮氧化物,一定压强下,将氨氮比为1.0
3 2 5 3 3 2
的混合气体按一定流速通入装有上述催化剂的反应装置,测得NO 的转化率随温度的变化关系如图所示。
x
在温度160~240 ℃之间,NO 转化率不高的原因是________。
x
【答案】(1) 2MoS+9O+12NaOH=====2NaMoO+4NaSO+6HO(3分)
2 2 2 4 2 4 2
(2) SO、AlO(2分) 将固体粉碎、适当搅拌、适当升高温度等(2分)
(3) 将AlO全部转化为Al(OH) 沉淀除去(2分)
3
(4) (NH)MoO ·4HO=====7MoO+6NH↑+7HO(3分)
4 6 7 24 2 3 3 2
(5) 温度160~240 ℃之间,催化剂的活性低,同时温度较低反应速率较慢,所以NO 的转化率不高(2分)
x
【解析】废催化剂在氢氧化钠条件下,通入氧气焙烧将MoS 转化为NaMoO,焙烧产生的气体主要为硫元素
2 2 4
转化生成的SO ;加HO浸出除去不溶的铁、铜化合物,浸出液含 OH-、MoO、[Al(OH)] -,通入过量的
2 2 4
CO ,将[Al(OH)] -转化为Al(OH) 沉淀,过滤,滤液中加入硝酸调节溶液的 pH小于6,使MoO转化为
2 4 3
MoO,然后加入NHNO 充分反应,析出(NH)MoO ·4HO,灼烧后可得到MoO 。(1)焙烧过程氧气具有氧
7 4 3 4 6 7 24 2 3
化性,会在NaOH条件下氧化MoS 生成SO 和NaMoO 。(2)AlO 会和NaOH生成可溶性的Na[Al(OH)] ,故
2 2 2 4 2 3 4
过滤后所得滤液中存在的阴离子有OH-、MoO、[Al(OH)] -;欲提高单位时间内钼的浸取率,可以采取的措
4
施有废催化剂粉碎、使得升高温度、搅拌等。(3)通入过量的CO ,将[Al(OH)] -转化为Al(OH) 沉淀,
2 4 3
除去铝元素。(4)(NH)MoO ·4HO灼烧后可得到MoO ,结合质量守恒可知,还生成NH 和水。(5)催
4 6 7 24 2 3 3
化剂催化需要一定的活化温度,在温度160~240℃之间时,没有达到催化剂所需的合适的活化温度,催化
剂活性弱,导致反应速率较慢。
9.(2024·江苏扬州中学高三11月月考,14)六氟锑酸钠( )是一种新开发的锑的精细化工产品,主
要用于有机合成、光化学反应、半导体刻蚀等.中南大学的杨天足教授提出了一种在水溶液中由锑白(主要
含 、 和 、 、 等)合成六氟锑酸钠的工艺流程如图所示:
已知:① 的性质与 类似;② 可溶于NaS溶液;③ 晶体难溶于水。请回答
2
下列问题:(1) 在元素周期表中的位置是 ,属于 区元素
(2)“碱浸、还原”时, 发生反应的离子方程式为 ;若 与 反应计量关系为2∶1,
则氧化产物为
(3)“除杂”时,当溶液中出现蓝色沉淀,立即停止加入 溶液,测得此时溶液的 ,则此时溶液
中残留的 [结果保留两位有效数字,常温下, ,
]
(4)“转化”时控温约 的原因是
(5)“氟化”中发生的反应化学方程式为 ,此过程不能选择玻璃仪器,是因为
(6)氟锑酸化学式为 ,酸性比纯硫酸要强 倍,称为超强酸,其与HF作用生成 ,
离子的空间构型为
【答案】(1)第5周期第ⅤA族 p
(2) 或
(3)
(4)温度过低,反应速率太慢,温度过高, 易分解损失
(5) 玻璃中的 会与HF反应而使玻璃腐蚀
(6)V形
【解析】锑白加NaOH溶液、NaSO 溶液进行碱浸、还原,Sb O、Sb S 直接与碱反应,Sb O 与被硫代
2 2 3 2 3 2 3 2 5
硫酸钠还原,Sb元素转化为NaSbO ,Sb S 中的S元素转化为NaS,CuS、氧化铁不反应,过滤除去;含
2 2 3 2
NaSbO 、NaS的溶液加硫酸铜将硫离子转化为CuS,将过量的氢氧根离子转化为氢氧化铜除去得到主要溶
2 2
质为NaSbO 的溶液,NaSbO 溶液加过氧化氢、浓NaOH转化得到NaSbO •3H O,再用HF进行氟化得到
2 2 3 2
NaSbF 。(1) 是51号元素,价电子排布为5s25p3,在元素周期表中的位置是第5周期第ⅤA族,属
6于p区元素。(2)由流程可知Sb S 中Sb转化为NaSbO ,S转化为NaS,则Sb S 发生反应的离子方程式
2 3 2 2 2 3
为 ,“碱浸、还原”时,Sb由+5价降为+3价,则Sb O 作氧化剂,NaSO 被氧
2 5 2 2 3
化,若Sb O 与NaSO 反应计量关系为2:1,根据得失电子守恒有2×2×(5-3)=1×2×x,其中x为S元素化
2 5 2 2 3
合价升高数,解得x=4,则NaSO 中S被氧化为+(2+4)=+6价,则氧化产物为 或NaSO ; 故答案为:
2 2 3 2 4
; 或NaSO 。(3)溶液的 ,常温下此时
2 4
,则c(Cu2+)= ,则
mol/L。(4)“转化”时反应物有HO,HO 受热易分解,控温
2 2 2 2
约80°C的原因是温度过低,反应速率太慢,温度过高,HO 易分解损失;故答案为:温度过低,反应速
2 2
率太慢,温度过高, 易分解损失。(5)“氟化”时HF和NaSbO •3H O反应得到NaSbF ,无元素价
3 2 6
态变化,为非氧化还原反应,根据电荷守恒、原子守恒可知反应的方程式为
,此过程不能选择玻璃仪器,是因为玻璃中的 会与HF反应而使玻
璃腐蚀。(6)[H F]+的价层电子数=2+ =4,含有两对孤电子对,则[H F]+离子的空间构型为V形。
2 2
10.(2024·江苏靖江高级中学、华罗庚中学高三阶段考试,17)某兴趣小组用铬铁矿[Fe(CrO )]制备
2 2
KCr O 晶体,流程如下:
2 2 7
已知:NaFeO 遇水强烈水解;
2
回答以下问题:(1)步骤I中铬铁矿转化为NaCrO 和NaFeO ,化学反应方程式为 。
2 4 2
(2)步骤III中加入硫酸不宜过多的原因是 。
(3)步骤IV,所得滤渣的主要成分是 。
(4)为了测定KCr O(摩尔质量为294g/mol)产品的纯度,可采用氧化还原滴定法:称取重铬酸钾试样2.500g
2 2 7
配成500mL溶液,取出25.00mL于锥形瓶中,加10mL2mo/LH SO 和足量碘化钾(铬的还原产物为Cr3+),
2 4
放于暗处5min,然后加入100mL水,加入淀粉溶液做指示剂,用0.1200mol/LNa SO 标准溶液滴定
2 2 3
(I+2S O =2I-+S O ),用去20.00mLNa SO 标准溶液,则该样品的纯度为 。(写出计算过程)
2 2 4 2 2 3
(5)PbCrO 是一种黄色颜料,难溶于水。请设计由KCr O 溶液制备PbCrO 的实验方案: ,静置,
4 2 2 7 4
过滤,洗涤,干燥,得PbCrO 。[实验中须使用的试剂有:6mol·L-1的KOH溶液,0.5mol·L-1Pb(NO ) 溶液]。
4 3 2
已知:①Pb(OH) 开始沉淀时pH为7.2,完全沉淀时pH为8.7。
2
②PbCrO 可由沸腾的铬酸盐溶液与铅盐溶液反应制得,含PbCrO 晶种时更易生成。
4 4
③六价铬在溶液中物种分布分数与pH关系如图所示。
【答案】(1)4Fe(CrO )+ 10Na CO+ 7 O 8NaCrO+ 4NaFeO + 10CO
2 2 2 3 2 2 4 2 2
(2)防止酸性太强,Cr O 氧化性增强,后续步骤中氧化Cl—
2
(3)Na SO
2 4
(4)94.08%
(5)向KCr O 溶液中加入6mol·L-1的KOH溶液,至pH略小于7.2,加热溶液至沸腾,先加入一滴0.5
2 2 7
mol·L-1 Pb(NO ) 溶液搅拌片刻产生少量沉淀,继续滴加至不再产生沉淀
3 2
【解析】由题给流程可知,铬铁矿与碳酸钠、氧气高温条件下反应生成NaCrO、NaFeO ,冷却后,向熔
2 4 2
渣中加入水,使NaFeO 水解转化为氢氧化铁沉淀,过滤、洗涤得到NaCrO 溶液;向NaCrO 溶液加入稀
2 2 4 2 4
硫酸,将NaCrO 转化为NaCr O,将酸化后的溶液蒸发结晶、过滤、洗涤得到含有硫酸钠的滤渣和
2 4 2 2 7NaCr O 溶液;向NaCr O 溶液中加入氯化钾固体,将蒸发浓缩、冷却结晶、洗涤、过滤、干燥得到
2 2 7 2 2 7
KCr O。(1)由分析可知,步骤I中发生的反应为铬铁矿与碳酸钠、氧气高温条件下反应生成NaCrO、
2 2 7 2 4
NaFeO 和二氧化碳,反应的化学方程式为。(2)若步骤III中加入硫酸不宜过多,加入氯化钾固体时,酸
2
性条件下重铬酸根离子会将氯离子氧化,造成重铬酸钾的产率降低。(3)由分析可知,步骤IV所得滤渣
的主要成分是硫酸钠。(4)由得失电子数目守恒可得如下关系式:KCr O~3I ~6Na SO,滴定消耗
2 2 7 2 2 2 3
20.00mL0.1200mol/L硫代硫酸钠溶液,则2.5g样品中重铬酸钾的纯度为
×100%=94.08%。 (5)由六价铬与pH关系图知,在碱性条件下,
主要以铬酸根存在,但是氢氧化铅在pH为7.2时开始沉淀,所以溶液pH不能超过7.2,铬酸根与铅离子在
沸腾时会生成铬酸铅沉淀,所以制备铬酸铅沉淀的实验方案为向KCr O 溶液中加入6mol·L-1的KOH溶液,
2 2 7
至pH略小于7.2,加热溶液至沸腾,先加入一滴0.5 mol·L-1 Pb(NO ) 溶液搅拌片刻产生少量沉淀,继续滴
3 2
加至不再产生沉淀。