文档内容
易错专题 22 有机推断解题策略
聚焦易错点:
一、依据有机反应条件进行推断
1. 这是烷烃和烷基中的氢被取代的反应条件。如:①烷烃的取代;芳香烃或芳香族化合物侧链烷
基的取代;③不饱和烃中烷基的取代。
2. 这是乙醇脱水生成乙烯的反应条件。
3. 或 为不饱和键加氢反应的条件,包括:-C=C-、=C=O、-C≡C-的加成。
4. 是①醇消去HO生成烯烃或炔烃;②醇分子间脱水生成醚的反应;③酯化反应的反应条件。
2
5. 是①卤代烃水解生成醇;②酯类水解反应的条件。
6. 是卤代烃消去HX生成不饱和烃的反应条件。
7. 是①酯类水解(包括油脂的酸性水解);②糖类的水解
8. 或 是醇氧化的条件。
9. 或 是不饱和烃加成反应的条件。
10. 是苯的同系物侧链氧化的反应条件(侧链烃基被氧化成-COOH)。
11.显色现象:苯酚遇FeCl 溶液显紫色;与新制Cu(OH) 悬浊液反应的现象:1、沉淀溶解,出现深蓝色
3 2
溶液则有多羟基存在;2、沉淀溶解,出现蓝色溶液则有羧基存在;3、加热后有红色沉淀出现则有醛基存
在。
二、常用的合成路线
有机合成往往要经过多步反应才能完成,因此确定有机合成的途径和路线时,要进行合理选择。
1.一元合成路线
R—CH=CH 卤代烃 一元醇 一元醛 一元羧酸 酯
2
2.二元合成路线CH CH CHX—CH X CHOH—CH OH
2 2 2 2 2 2
HOOC—COOH 链酯、环酯、聚酯
3.芳香化合物的合成路线
①
② 芳香酯
注意: 与Cl 反应时条件不同所得产物不同,光照时,只取代侧链甲基上的氢原子,生成
2
;而Fe作催化剂时,取代苯环上甲基邻、对位上的氢原子,生成 。
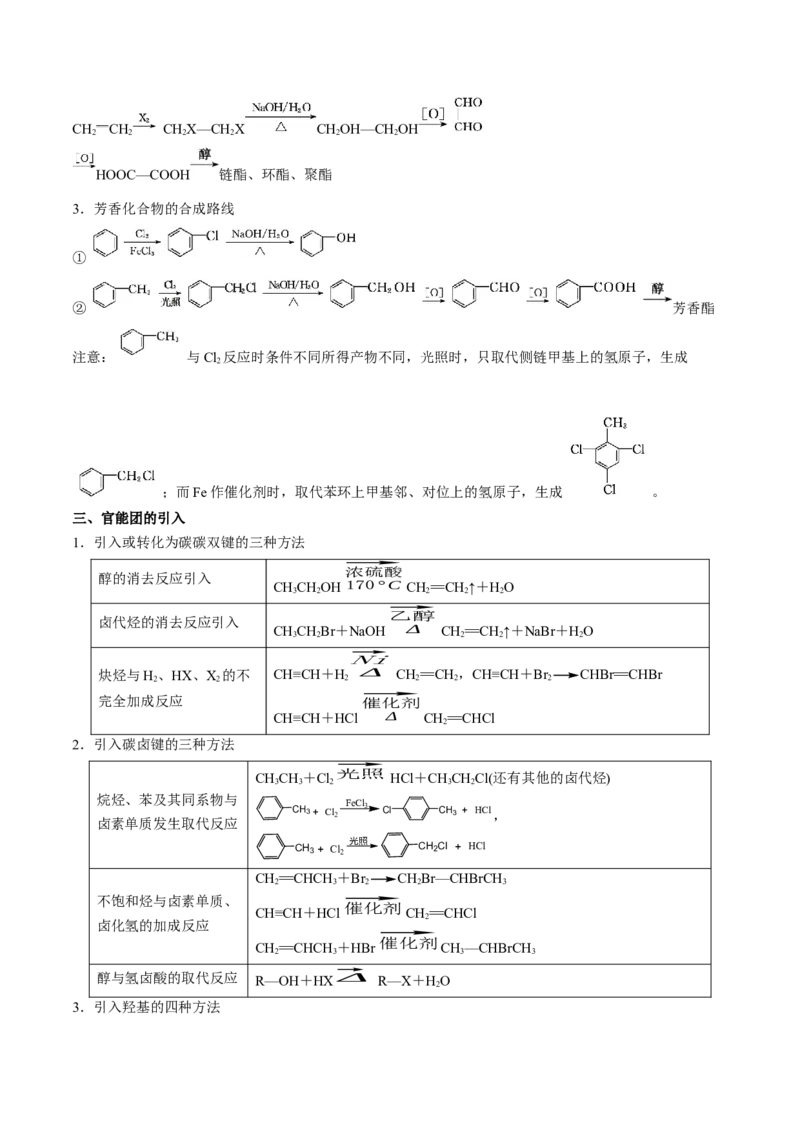
三、官能团的引入
1.引入或转化为碳碳双键的三种方法
⃗浓硫酸
醇的消去反应引入
CHCHOH 170°C CH==CH↑+HO
3 2 2 2 2
⃗乙醇
卤代烃的消去反应引入
CHCHBr+NaOH Δ CH==CH↑+NaBr+HO
3 2 2 2 2
N⃗i
炔烃与H、HX、X 的不 CH≡CH+H Δ CH==CH,CH≡CH+Br CHBr==CHBr
2 2 2 2 2 2
完全加成反应 ⃗催化剂
CH≡CH+HCl Δ CH==CHCl
2
2.引入碳卤键的三种方法
CHCH+Cl
⃗光照
HCl+CHCHCl(还有其他的卤代烃)
3 3 2 3 2
烷烃、苯及其同系物与
CH3+ Cl2
FeCl3
Cl CH3+ HCl,
卤素单质发生取代反应
CH 3+ Cl 2 光照 CH 2 Cl + HCl
CH==CHCH +Br CHBr—CHBrCH
2 3 2 2 3
不饱和烃与卤素单质、 ⃗催化剂
CH≡CH+HCl CH==CHCl
2
卤化氢的加成反应
⃗催化剂
CH==CHCH +HBr CH—CHBrCH
2 3 3 3
醇与氢卤酸的取代反应 R—OH+HX ⃗Δ R—X+HO
2
3.引入羟基的四种方法⃗催化剂
烯烃与水加成生成醇
CH==CH+HO加热、加压CHCH—OH
2 2 2 3 2
⃗
水
卤代烃的碱性水解成醇
CHCH—Br+NaOH Δ CHCH—OH+NaBr
3 2 3 2
O
催化剂
醛或酮与氢气加成生成 CH 3 C H+H 2 CH3CH2 OH
醇
O OH
催化剂
CH3 C CH3 +H2 CH3 CH CH3
酯水解生成醇 CHCOOCH CH+HO CHCOOH+CHCHOH
3 2 3 2 3 3 2
4.引入碳氧双键(醛基或羰基)的方法
C⃗u
2CHCHCHOH+O Δ 2CHCHCHO+2HO
醇的催化氧化生成醛 3 2 2 2 3 2 2
(酮) OH O
Cu
2CH
3
—CH—CH
3
+O
2 r
2CH
3
—C—CH
3
+2H
2
O
连在同一个碳上的两个羟 OH O
—H2O
基脱水
CH3 C OH CH3 C H
H
含碳碳三键的物质与水加 O
成 CH 3 C CH+H 2 O 催化剂 CH 3 C CH 3
5.引入羧基的2种方法
⃗催化剂
醛基氧化
2CHCHO+O Δ 2CHCOOH
3 2 3
酯、肽、蛋白质、羧酸盐的水
CHCOOCH CH+HO CHCOOH+CHCHOH
3 2 3 2 3 3 2
解
四、官能团的保护与恢复
1.碳碳双键:易与卤素单质加成,易被氧气、臭氧、双氧水、酸性高锰酸钾溶液氧化
方法:在氧化其他基团前可以利用其与HCl等的加成反应将其保护起来,后再利用消去反应转变为碳碳
双键
CH COOH CHCOOH
2
如:
HOCH CH CHCH OH
HCl
HOCH CH CHClCH OH
KMnO
4
/H+
Cl CH COOH
jNaOH/醇
CHCOOH
2 2 2 2 2 k酸化
2.酚羟基:易被氧气、臭氧、双氧水、酸性高锰酸钾溶液氧化
方法①:在氧化其他基团前用碘甲烷(CHI)先转化为苯甲醚,后用氢碘酸酸化重新转化为酚
3
CH 3 I HI
OH OCH OH
如: 3
方法②:在氧化其他基团前用NaOH溶液先转化为酚钠,后酸化重新转化为酚
NaOH溶液 H+
OH ONa OH
如:
3.醛基:易被氧化方法:在氧化其他基团前可以用乙醇(或乙二醇)加成保护
O O
OC H
C H OH 2 5 H+/H O
如:R
C H
2
HC
5
l R C OC 2 H 5
2
R C H
H
4.氨基:易被氧气、臭氧、双氧水、酸性高锰酸钾溶液氧化
方法:在氧化其他基团前可以用醋酸酐将氨基转化为酰胺,然后再水解转化为氨基。
NH2 (CH CO) O NHCOCH3 OH-/H O NH2
3 2 2
如:
考点精练
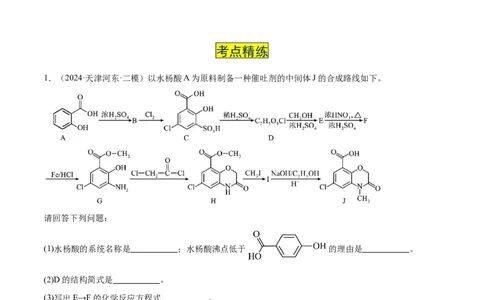
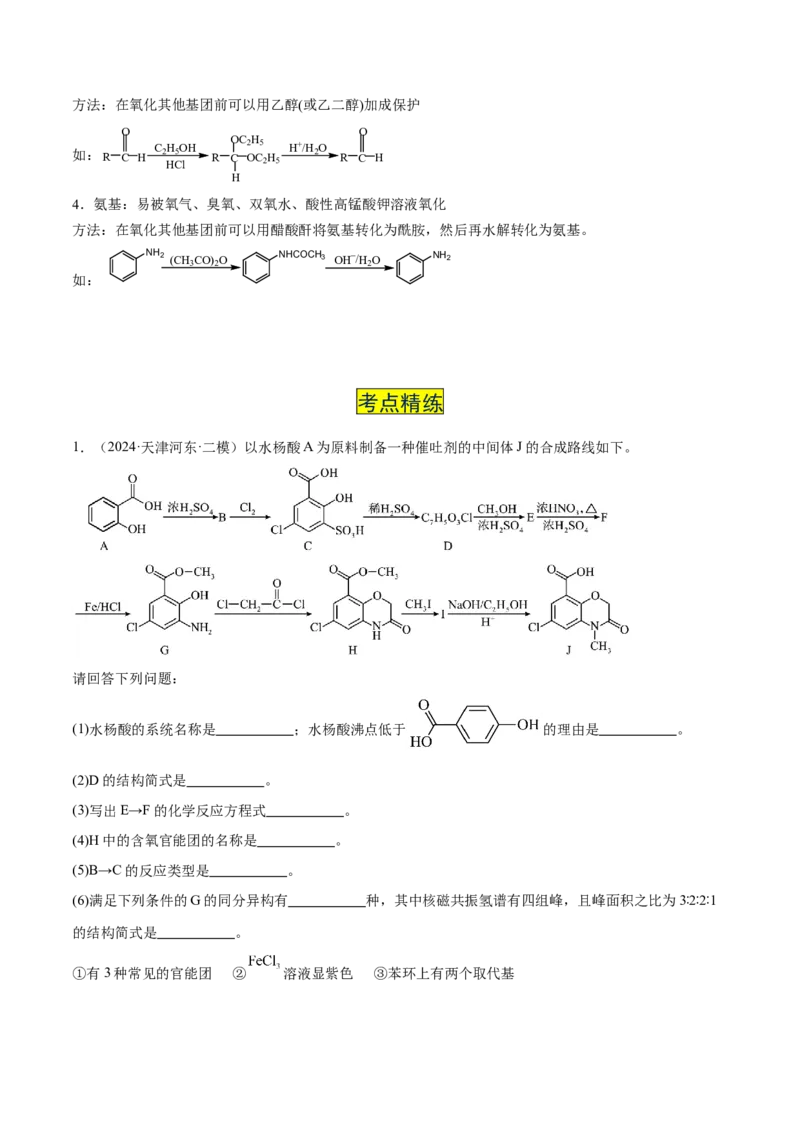
1.(2024·天津河东·二模)以水杨酸A为原料制备一种催吐剂的中间体J的合成路线如下。
请回答下列问题:
(1)水杨酸的系统名称是 ;水杨酸沸点低于 的理由是 。
(2)D的结构简式是 。
(3)写出E→F的化学反应方程式 。
(4)H中的含氧官能团的名称是 。
(5)B→C的反应类型是 。
(6)满足下列条件的G的同分异构有 种,其中核磁共振氢谱有四组峰,且峰面积之比为3∶2∶2∶1
的结构简式是 。
①有3种常见的官能团 ② 溶液显紫色 ③苯环上有两个取代基(7)参照以上合成路线,若以 为原料制备 (其他试剂自选),则其合成路线为
。
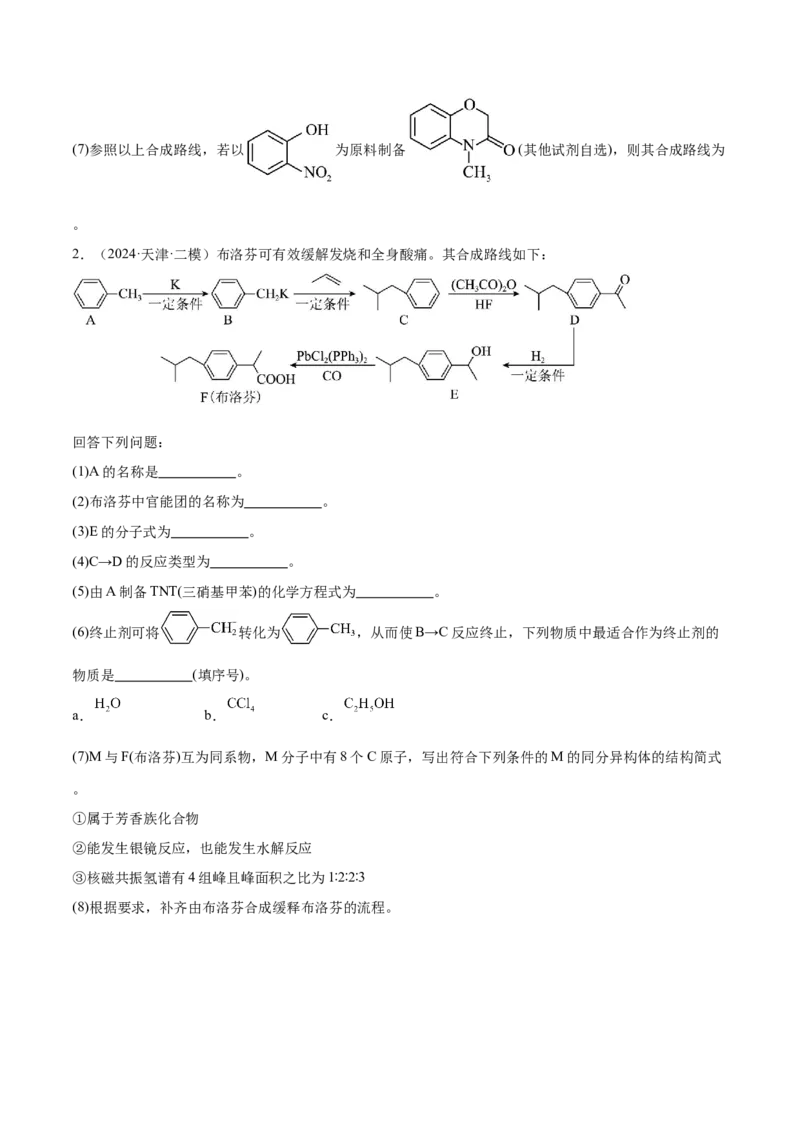
2.(2024·天津·二模)布洛芬可有效缓解发烧和全身酸痛。其合成路线如下:
回答下列问题:
(1)A的名称是 。
(2)布洛芬中官能团的名称为 。
(3)E的分子式为 。
(4)C→D的反应类型为 。
(5)由A制备TNT(三硝基甲苯)的化学方程式为 。
(6)终止剂可将 转化为 ,从而使B→C反应终止,下列物质中最适合作为终止剂的
物质是 (填序号)。
a. b. c.
(7)M与F(布洛芬)互为同系物,M分子中有8个C原子,写出符合下列条件的M的同分异构体的结构简式
。
①属于芳香族化合物
②能发生银镜反应,也能发生水解反应
③核磁共振氢谱有4组峰且峰面积之比为1∶2∶2∶3
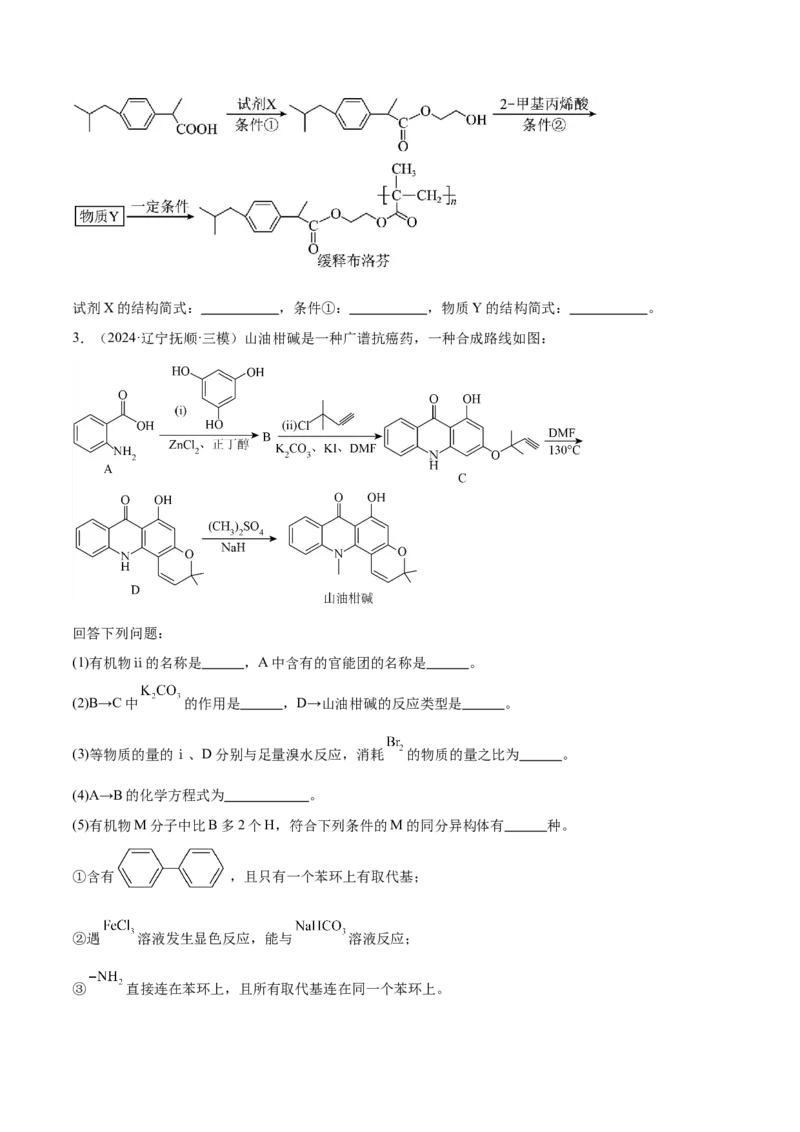
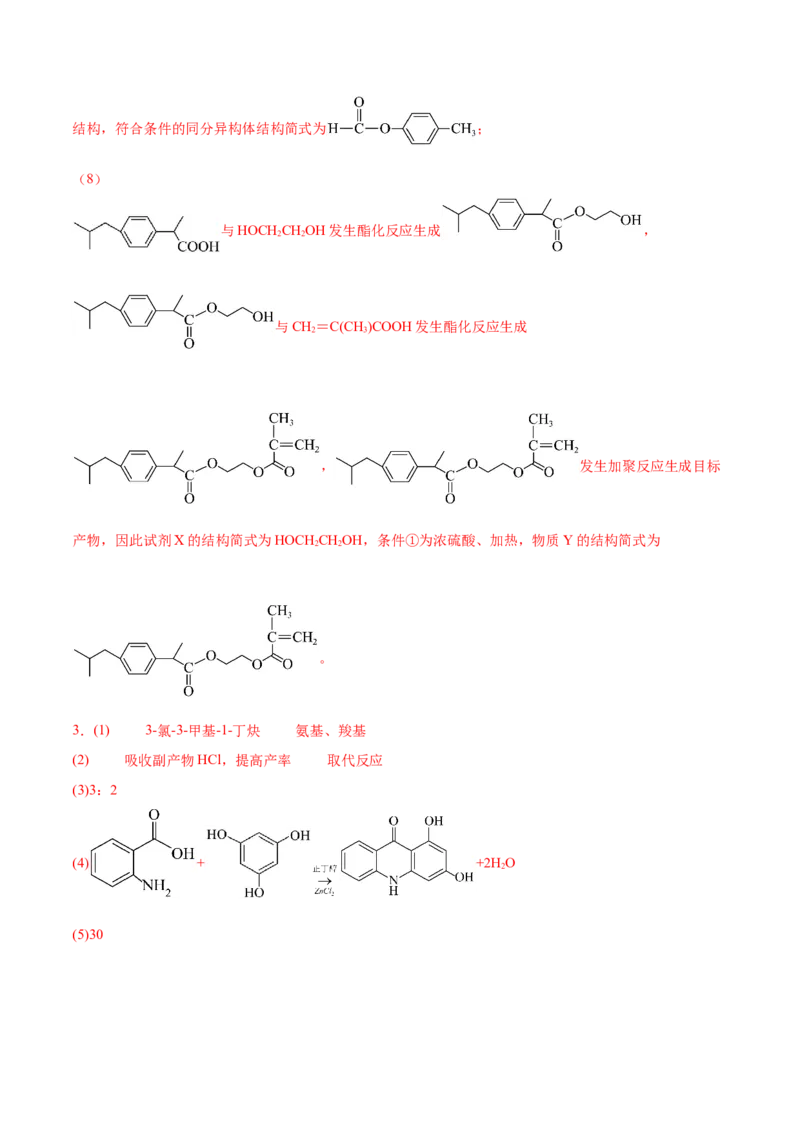
(8)根据要求,补齐由布洛芬合成缓释布洛芬的流程。试剂X的结构简式: ,条件①: ,物质Y的结构简式: 。
3.(2024·辽宁抚顺·三模)山油柑碱是一种广谱抗癌药,一种合成路线如图:
回答下列问题:
(1)有机物ⅱ的名称是 ,A中含有的官能团的名称是 。
(2)B→C中 的作用是 ,D→山油柑碱的反应类型是 。
(3)等物质的量的ⅰ、D分别与足量溴水反应,消耗 的物质的量之比为 。
(4)A→B的化学方程式为 。
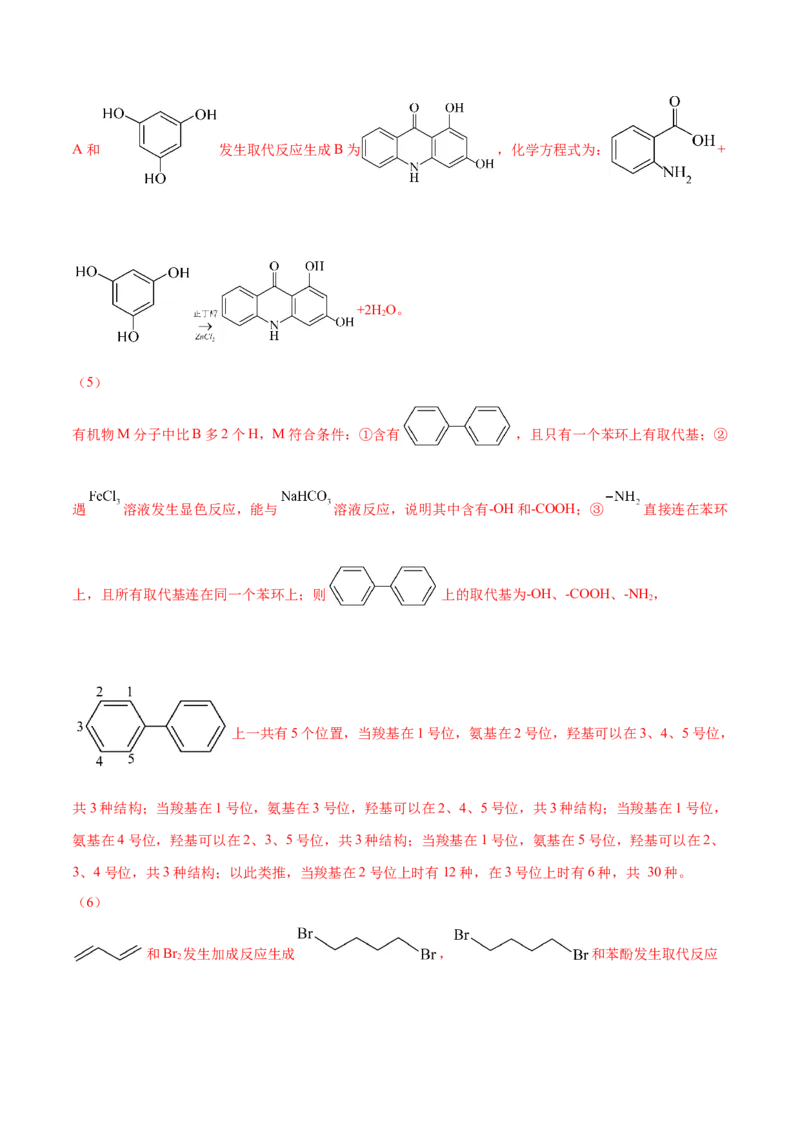
(5)有机物M分子中比B多2个H,符合下列条件的M的同分异构体有 种。
①含有 ,且只有一个苯环上有取代基;
②遇 溶液发生显色反应,能与 溶液反应;
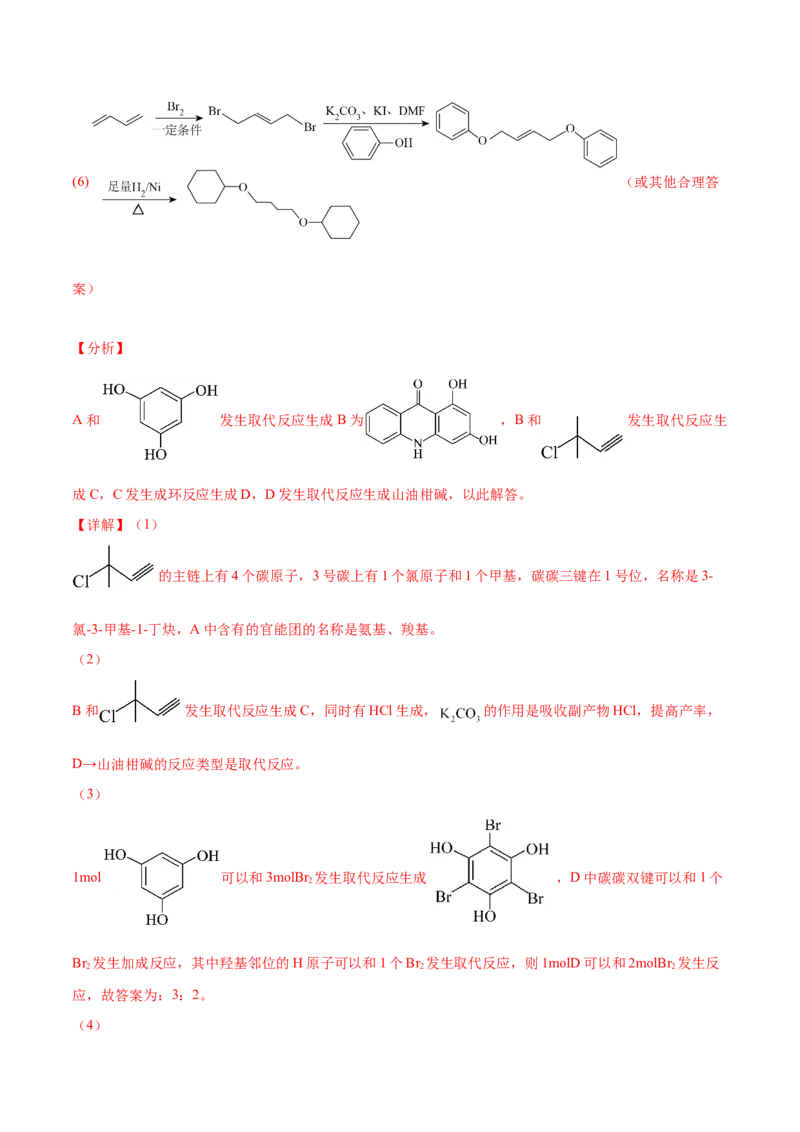
③ 直接连在苯环上,且所有取代基连在同一个苯环上。(6)以苯酚和1,3-丁二烯为原料合成 ,设计合成路线 (其他试剂任
选)。
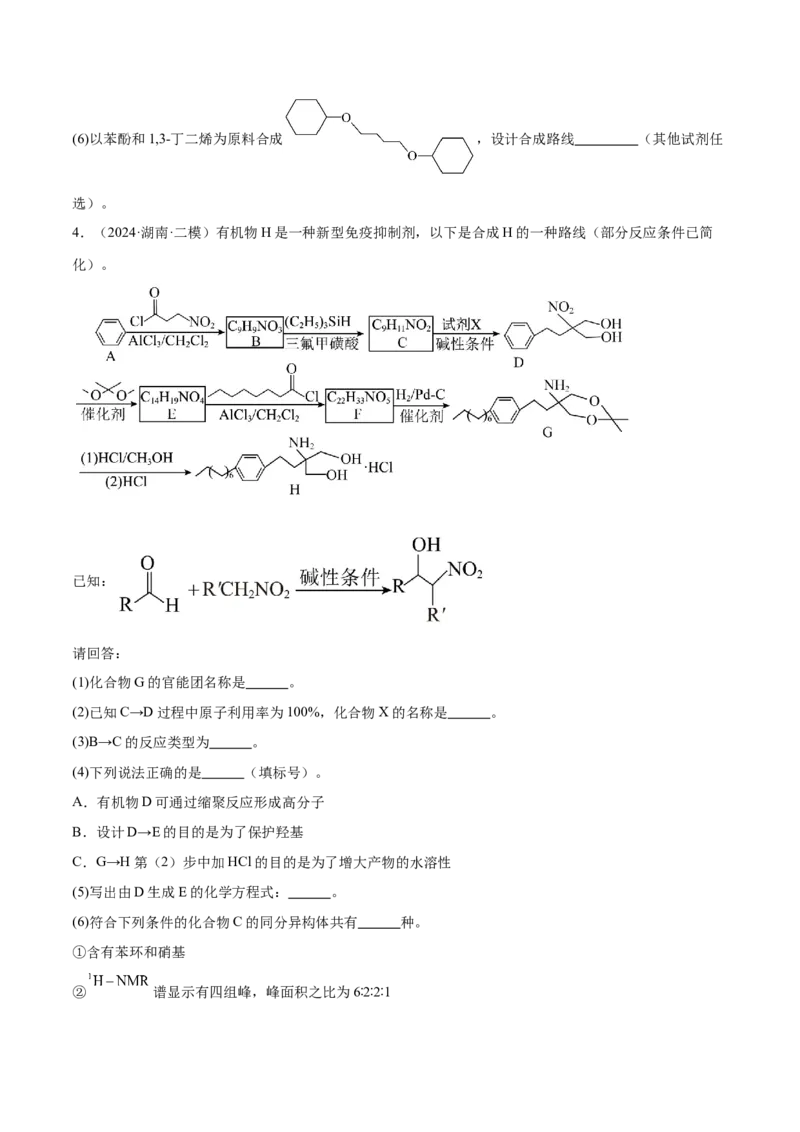
4.(2024·湖南·二模)有机物H是一种新型免疫抑制剂,以下是合成H的一种路线(部分反应条件已简
化)。
已知:
请回答:
(1)化合物G的官能团名称是 。
(2)已知C→D过程中原子利用率为100%,化合物X的名称是 。
(3)B→C的反应类型为 。
(4)下列说法正确的是 (填标号)。
A.有机物D可通过缩聚反应形成高分子
B.设计D→E的目的是为了保护羟基
C.G→H第(2)步中加HCl的目的是为了增大产物的水溶性
(5)写出由D生成E的化学方程式: 。
(6)符合下列条件的化合物C的同分异构体共有 种。
①含有苯环和硝基
② 谱显示有四组峰,峰面积之比为6∶2∶2∶1(7)设计以苯甲醇和 为原料,合成 的路线 (用流程图表示,无机试
剂任选)。
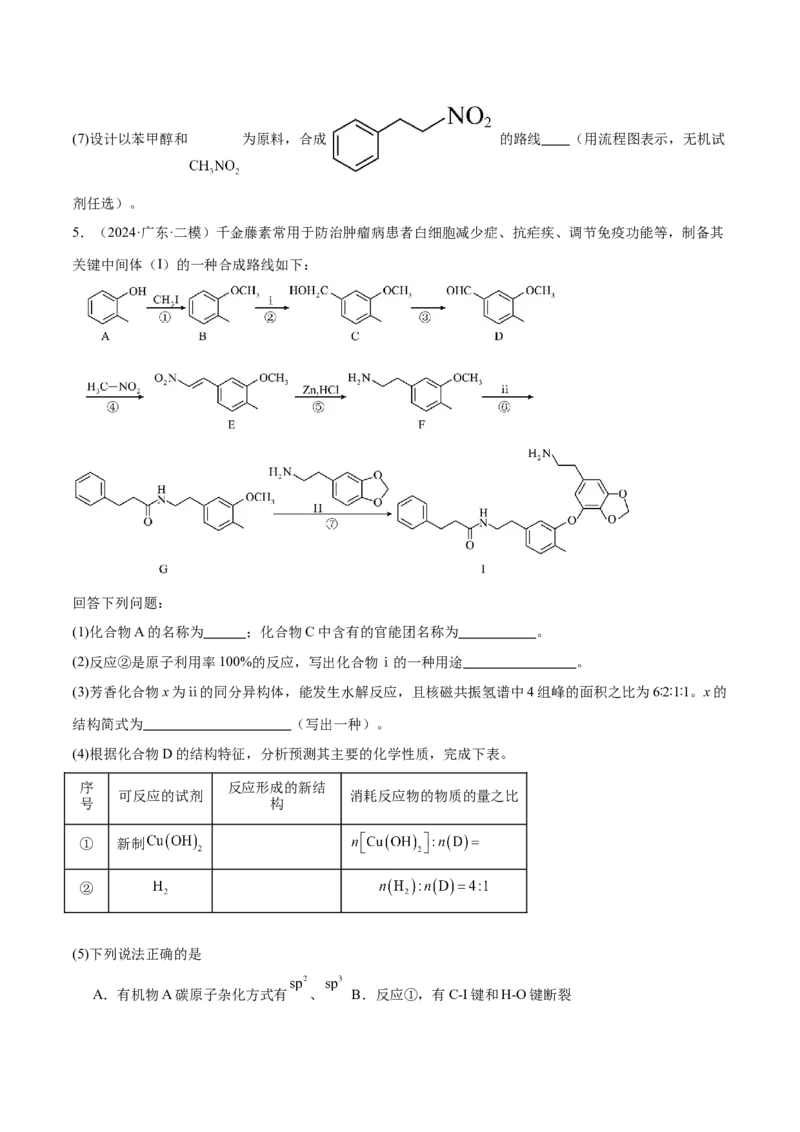
5.(2024·广东·二模)千金藤素常用于防治肿瘤病患者白细胞减少症、抗疟疾、调节免疫功能等,制备其
关键中间体(I)的一种合成路线如下:
回答下列问题:
(1)化合物A的名称为 ;化合物C中含有的官能团名称为 。
(2)反应②是原子利用率100%的反应,写出化合物ⅰ的一种用途 。
(3)芳香化合物x为ⅱ的同分异构体,能发生水解反应,且核磁共振氢谱中4组峰的面积之比为6∶2∶1∶1。x的
结构简式为 (写出一种)。
(4)根据化合物D的结构特征,分析预测其主要的化学性质,完成下表。
序 反应形成的新结
可反应的试剂 消耗反应物的物质的量之比
号 构
① 新制
②
(5)下列说法正确的是
A.有机物A碳原子杂化方式有 、 B.反应①,有C-I键和H-O键断裂C.1mol化合物B中,含 键16 个 D.产品I属于极性分子,易溶于水和酒精
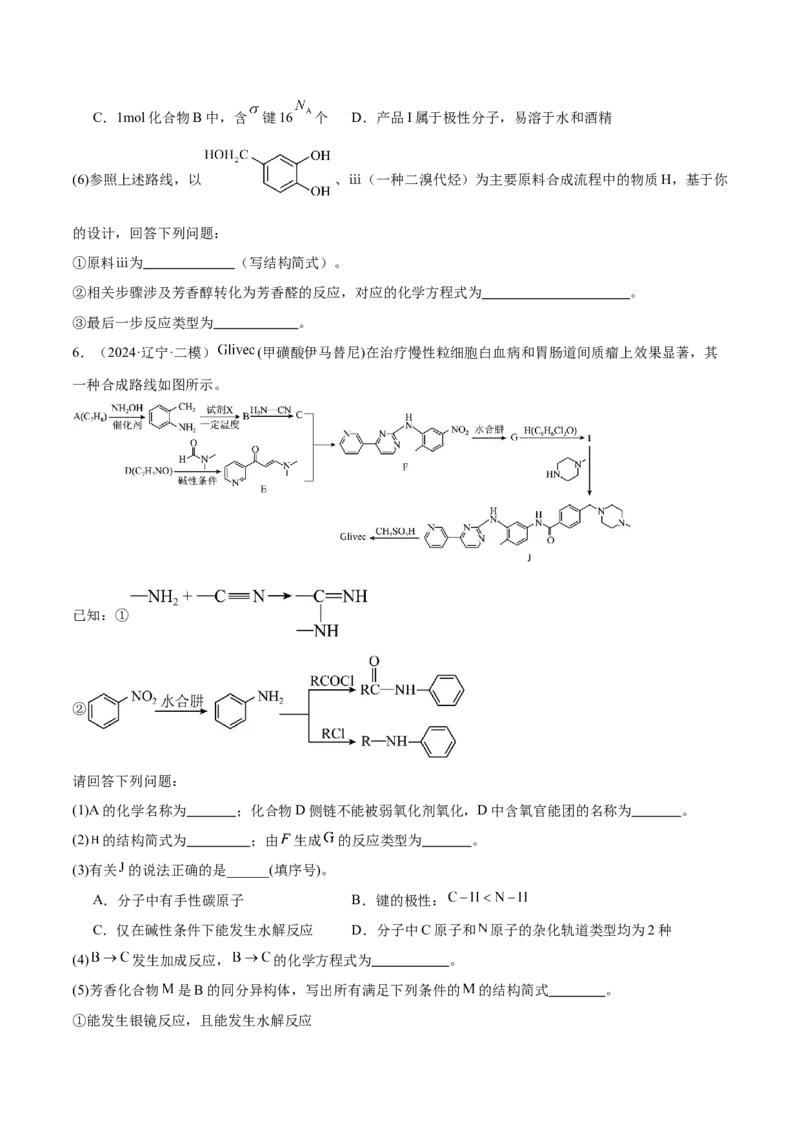
(6)参照上述路线,以 、ⅲ(一种二溴代烃)为主要原料合成流程中的物质H,基于你
的设计,回答下列问题:
①原料ⅲ为 (写结构简式)。
②相关步骤涉及芳香醇转化为芳香醛的反应,对应的化学方程式为 。
③最后一步反应类型为 。
6.(2024·辽宁·二模) (甲磺酸伊马替尼)在治疗慢性粒细胞白血病和胃肠道间质瘤上效果显著,其
一种合成路线如图所示。
已知:①
②
请回答下列问题:
(1)A的化学名称为 ;化合物D侧链不能被弱氧化剂氧化,D中含氧官能团的名称为 。
(2) 的结构简式为 ;由 生成 的反应类型为 。
(3)有关 的说法正确的是______(填序号)。
A.分子中有手性碳原子 B.键的极性:
C.仅在碱性条件下能发生水解反应 D.分子中C原子和 原子的杂化轨道类型均为2种
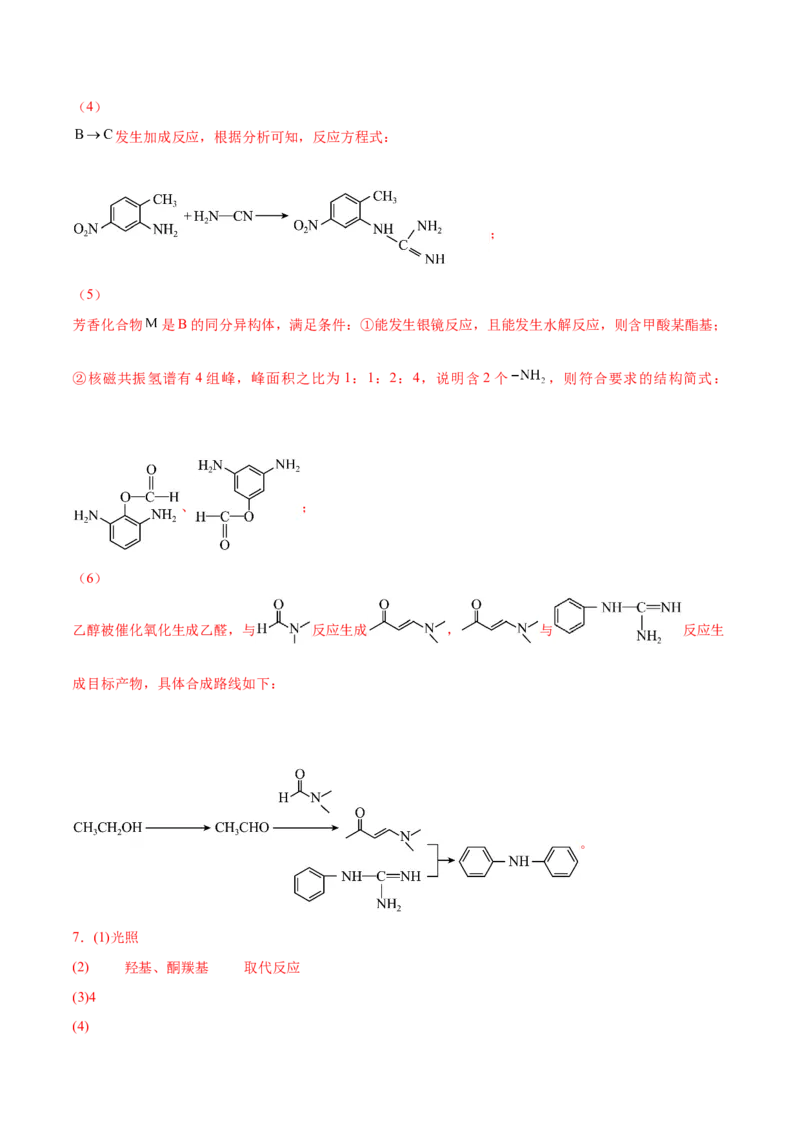
(4) 发生加成反应, 的化学方程式为 。
(5)芳香化合物 是B的同分异构体,写出所有满足下列条件的 的结构简式 。
①能发生银镜反应,且能发生水解反应②核磁共振氢谱有4组峰,峰面积之比为
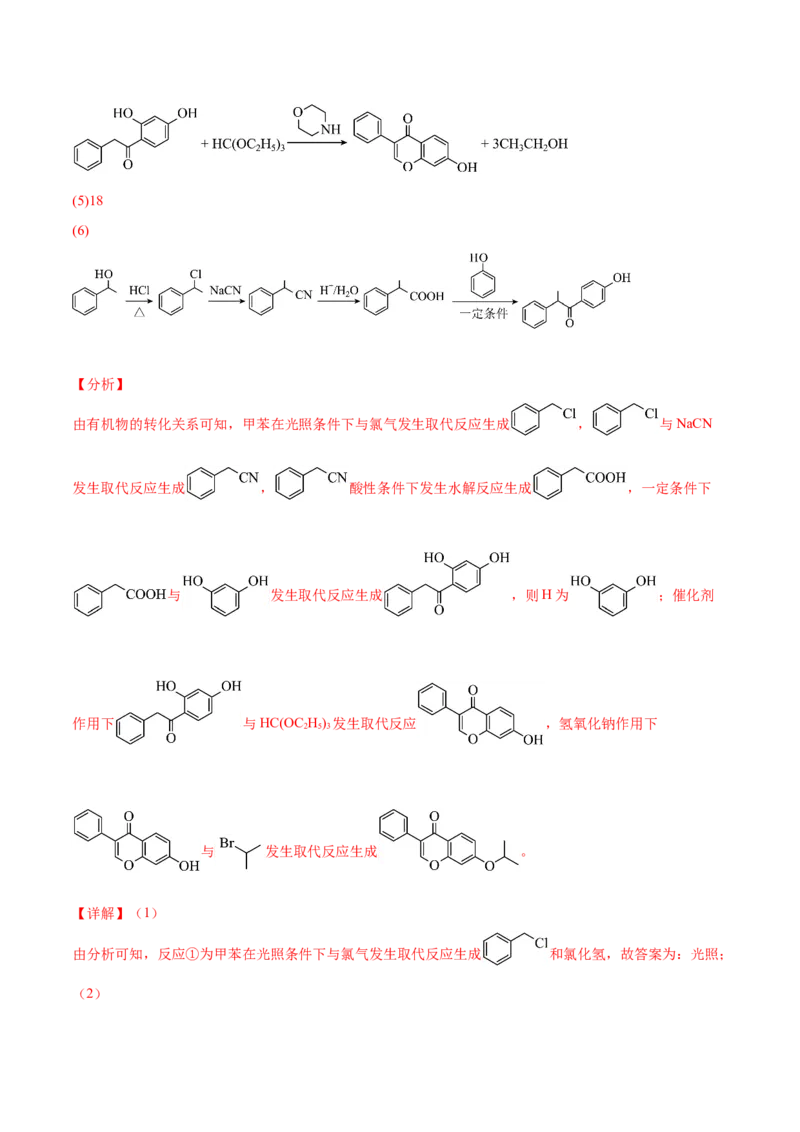
(6)以 、 和 为原料制备 ,设计合成路线(无
机试剂与有机溶剂任选) 。
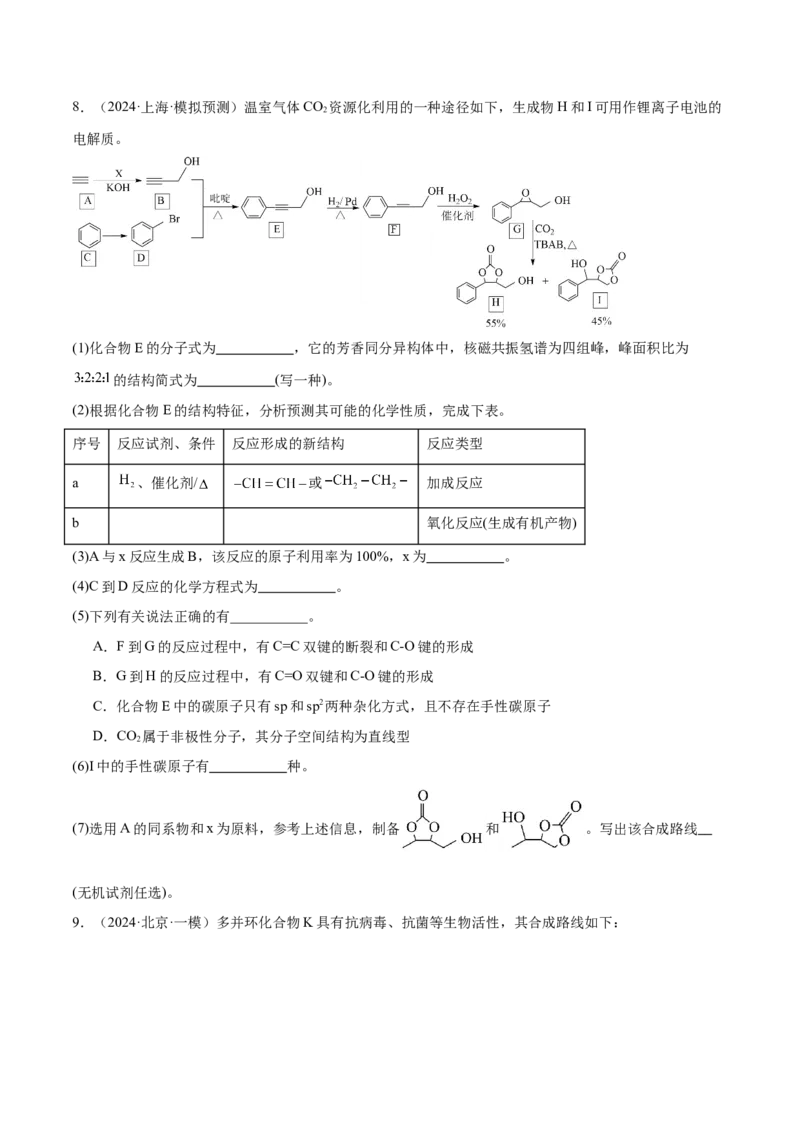
7.(2024·陕西宝鸡·三模)化合物G俗称依普黄酮,是一种抗骨质疏松药物的主要成分。以甲苯为原料合
成该化合物的路线如下图所示:
已知:
(1)反应①的反应条件为 。
(2)E中官能团的名称为 ,反应F→G的反应类型为 。
(3)E与足量的 完全加成后所生成的化合物中手性碳原子(碳原子上连接四个不同的原子或基团)的个数为
。
(4)已知N为催化剂,则 的化学方程式为 。
(5)K是D的同系物,其相对分子质量比D多14,满足下列条件的K的同分异构体共有 种。
①苯环上只有两个取代基;
②能与Na反应生成 ;
③能与银氨溶液发生银镜反应。
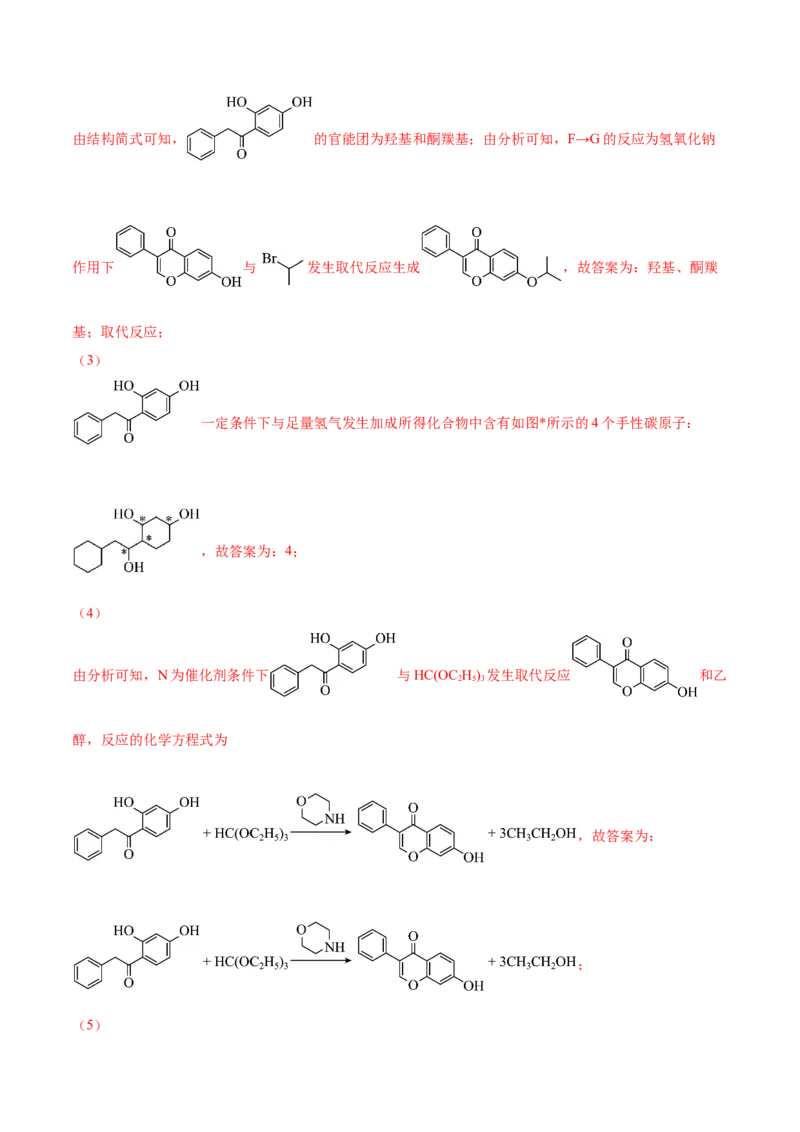
(6)根据上述信息,设计以苯酚和 为原料,制备 的合成路线(无机试剂任选)
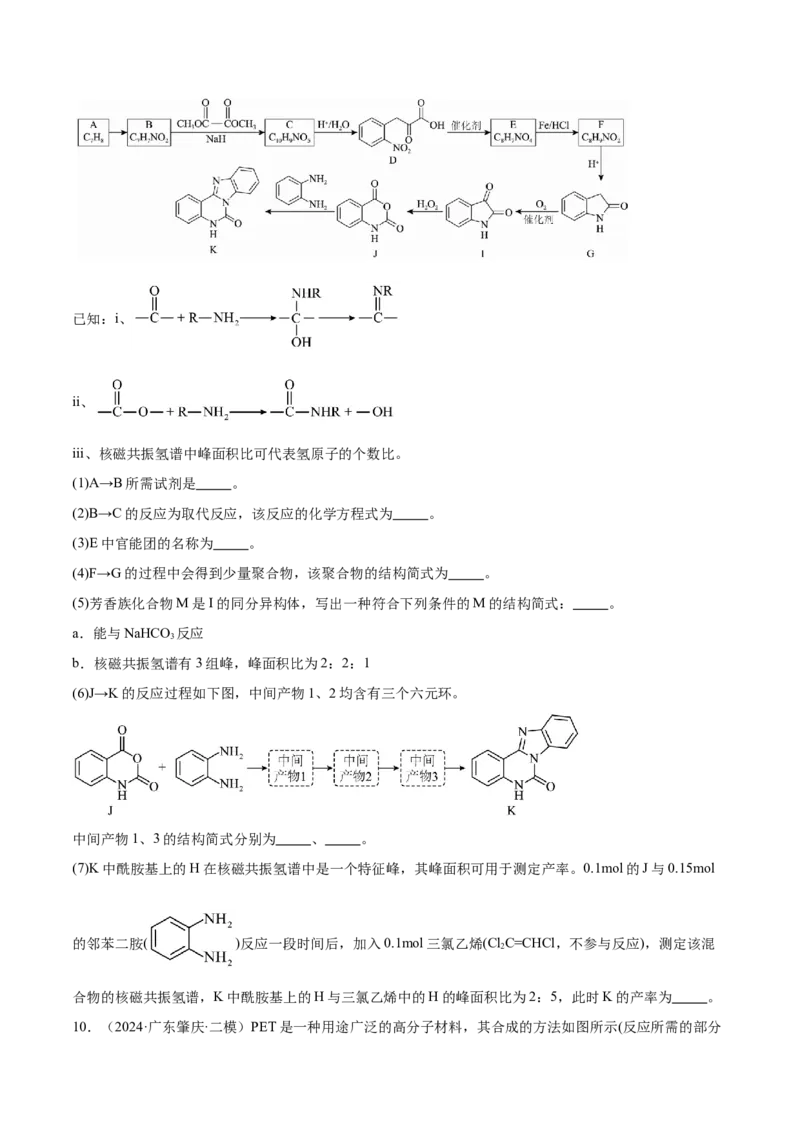
。8.(2024·上海·模拟预测)温室气体CO 资源化利用的一种途径如下,生成物H和I可用作锂离子电池的
2
电解质。
(1)化合物E的分子式为 ,它的芳香同分异构体中,核磁共振氢谱为四组峰,峰面积比为
的结构简式为 (写一种)。
(2)根据化合物E的结构特征,分析预测其可能的化学性质,完成下表。
序号 反应试剂、条件 反应形成的新结构 反应类型
a 、催化剂/ 或 加成反应
b 氧化反应(生成有机产物)
(3)A与x反应生成B,该反应的原子利用率为100%,x为 。
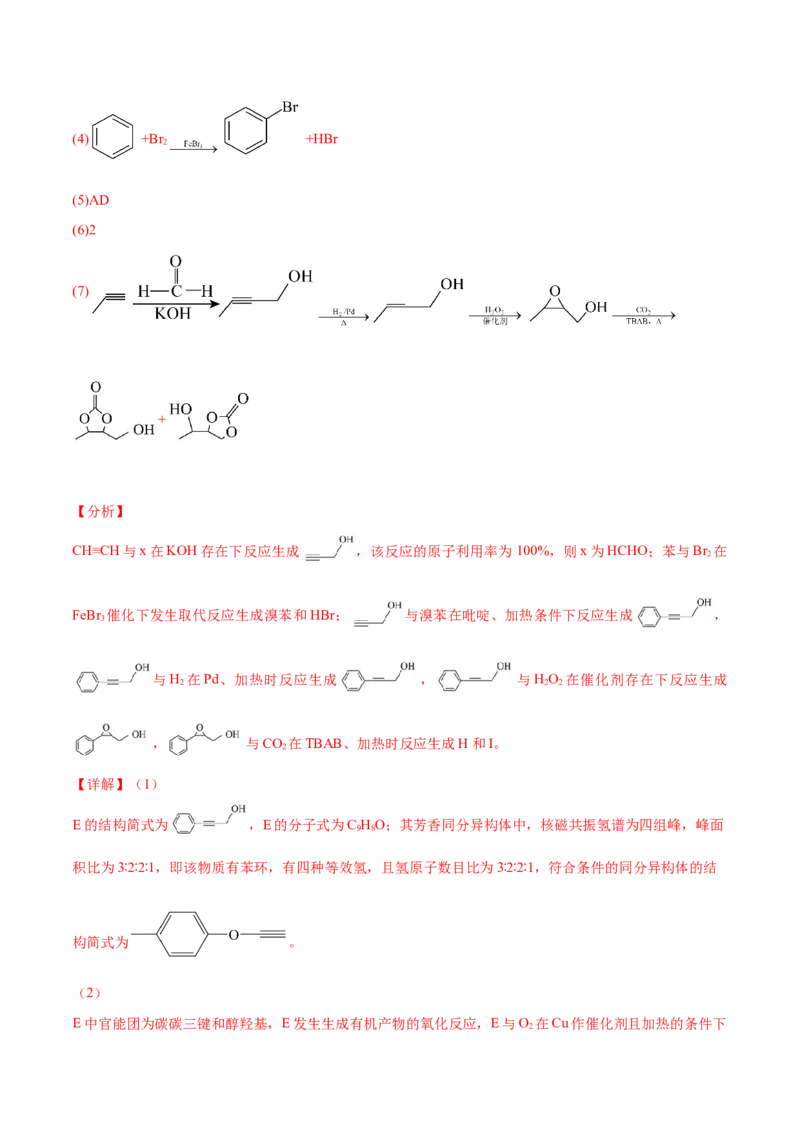
(4)C到D反应的化学方程式为 。
(5)下列有关说法正确的有___________。
A.F到G的反应过程中,有C=C双键的断裂和C-O键的形成
B.G到H的反应过程中,有C=O双键和C-O键的形成
C.化合物E中的碳原子只有sp和sp2两种杂化方式,且不存在手性碳原子
D.CO 属于非极性分子,其分子空间结构为直线型
2
(6)I中的手性碳原子有 种。
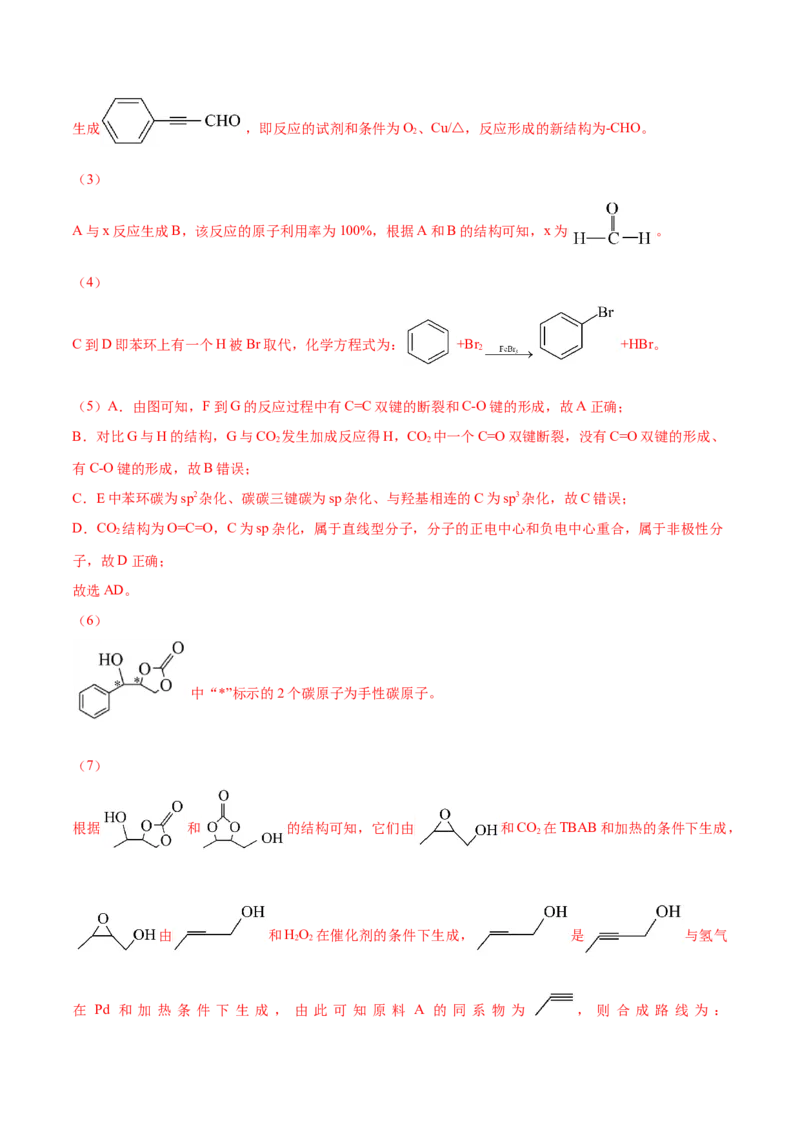
(7)选用A的同系物和x为原料,参考上述信息,制备 和 。写出该合成路线
(无机试剂任选)。
9.(2024·北京·一模)多并环化合物K具有抗病毒、抗菌等生物活性,其合成路线如下:已知:i、
ii、
iii、核磁共振氢谱中峰面积比可代表氢原子的个数比。
(1)A→B所需试剂是 。
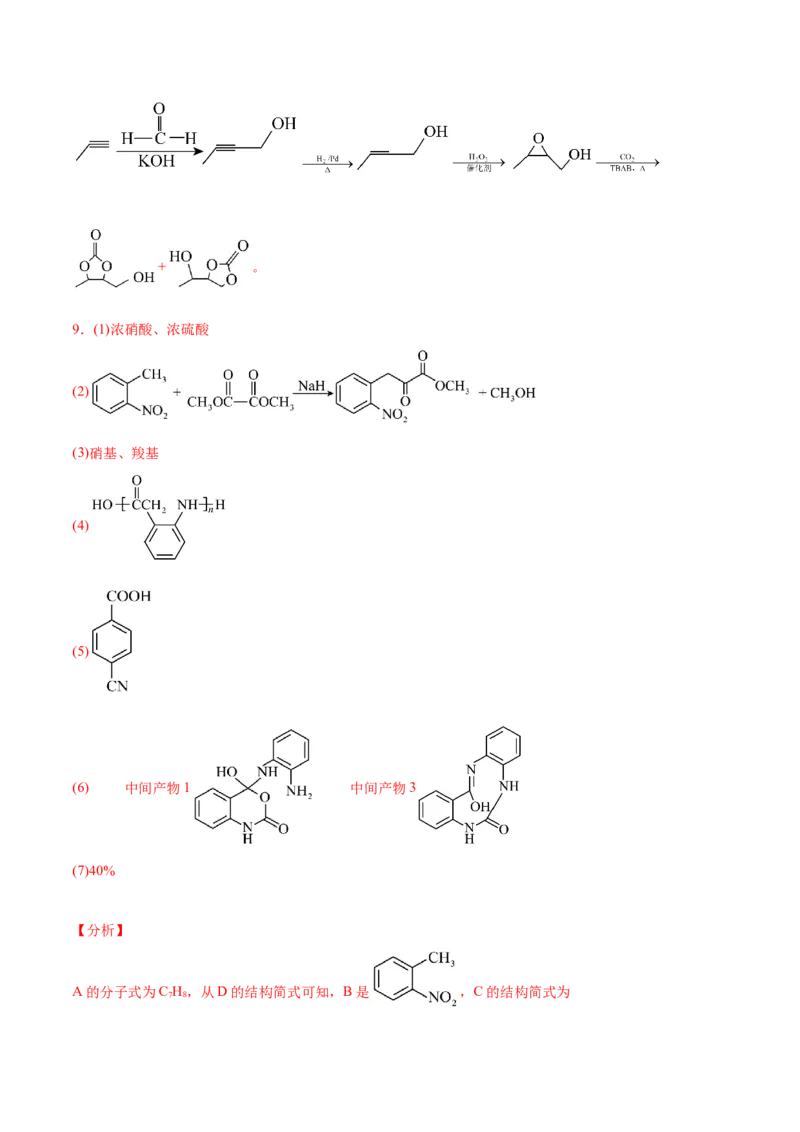
(2)B→C的反应为取代反应,该反应的化学方程式为 。
(3)E中官能团的名称为 。
(4)F→G的过程中会得到少量聚合物,该聚合物的结构简式为 。
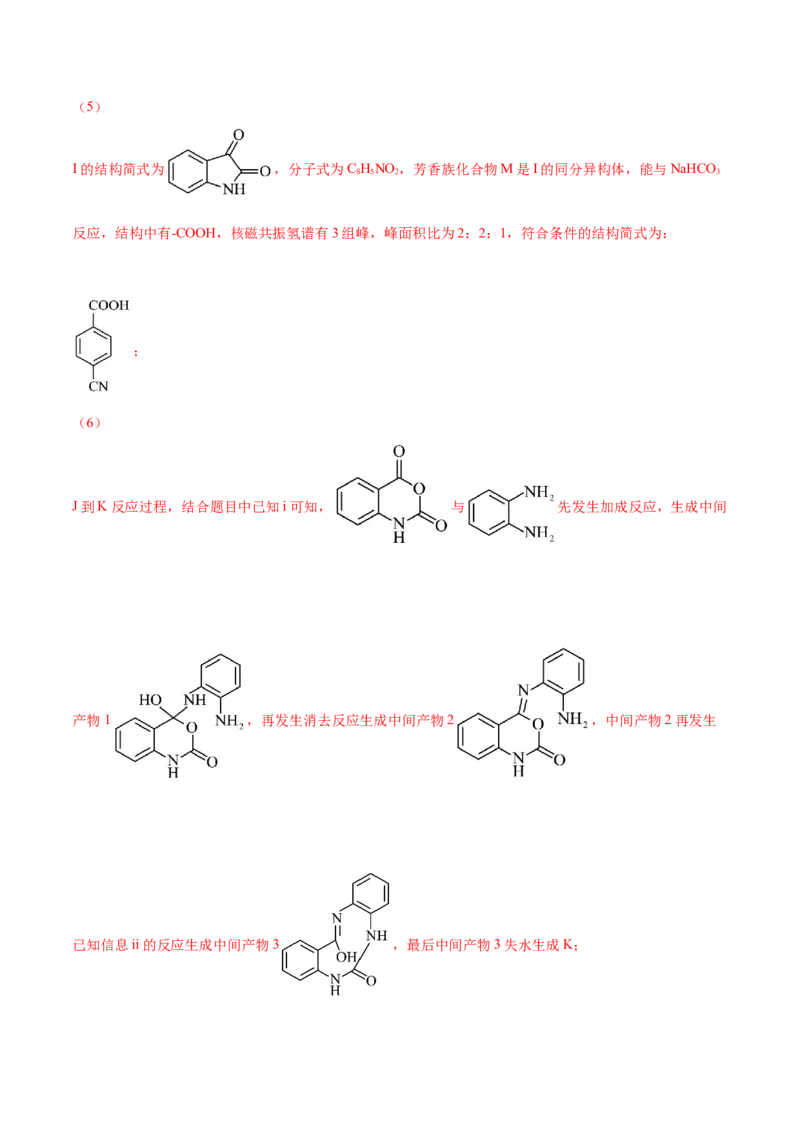
(5)芳香族化合物M是I的同分异构体,写出一种符合下列条件的M的结构简式: 。
a.能与NaHCO 反应
3
b.核磁共振氢谱有3组峰,峰面积比为2:2:1
(6)J→K的反应过程如下图,中间产物1、2均含有三个六元环。
中间产物1、3的结构简式分别为 、 。
(7)K中酰胺基上的H在核磁共振氢谱中是一个特征峰,其峰面积可用于测定产率。0.1mol的J与0.15mol
的邻苯二胺( )反应一段时间后,加入0.1mol三氯乙烯(Cl C=CHCl,不参与反应),测定该混
2
合物的核磁共振氢谱,K中酰胺基上的H与三氯乙烯中的H的峰面积比为2:5,此时K的产率为 。
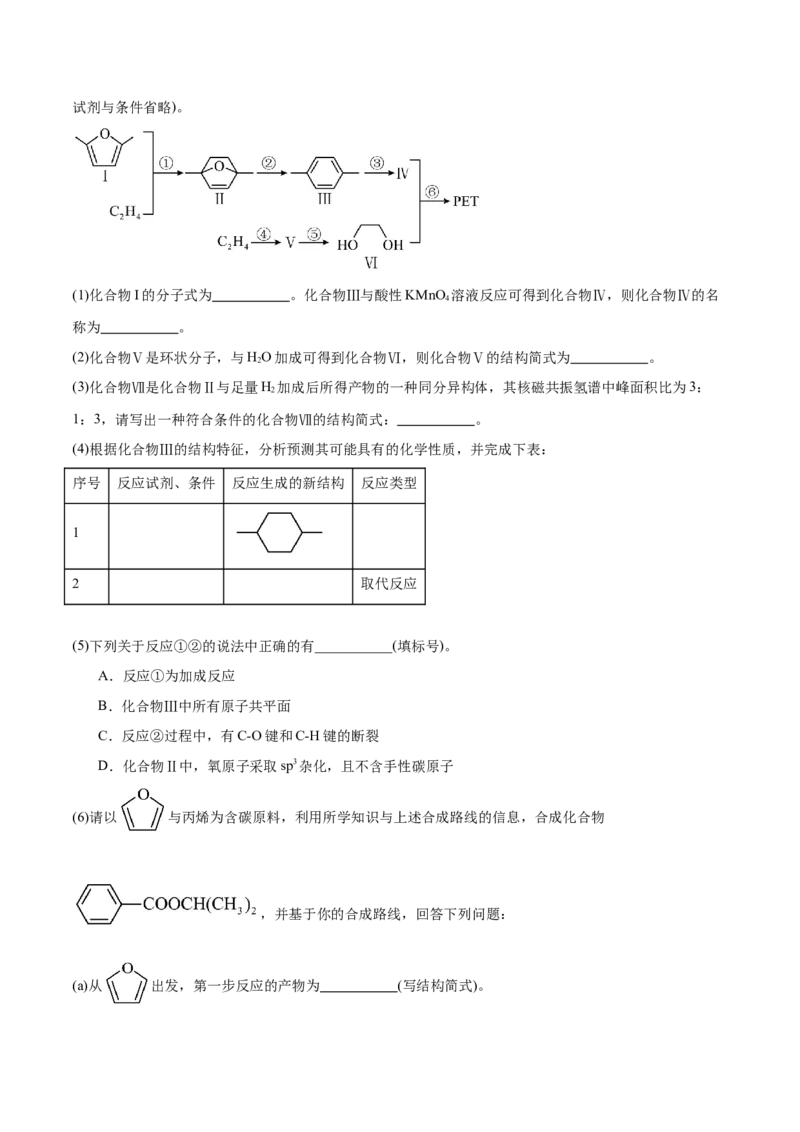
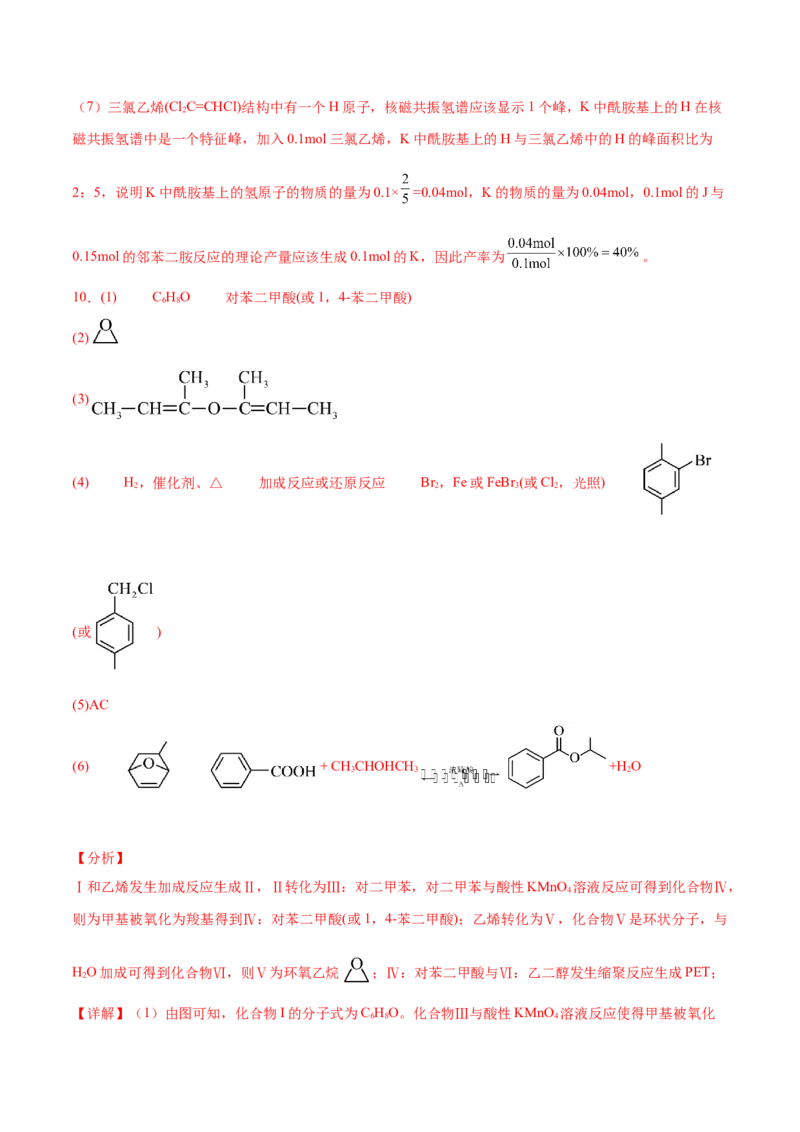
10.(2024·广东肇庆·二模)PET是一种用途广泛的高分子材料,其合成的方法如图所示(反应所需的部分试剂与条件省略)。
(1)化合物I的分子式为 。化合物Ⅲ与酸性KMnO 溶液反应可得到化合物Ⅳ,则化合物Ⅳ的名
4
称为 。
(2)化合物Ⅴ是环状分子,与HO加成可得到化合物Ⅵ,则化合物Ⅴ的结构简式为 。
2
(3)化合物Ⅶ是化合物Ⅱ与足量H 加成后所得产物的一种同分异构体,其核磁共振氢谱中峰面积比为3:
2
1:3,请写出一种符合条件的化合物Ⅶ的结构简式: 。
(4)根据化合物Ⅲ的结构特征,分析预测其可能具有的化学性质,并完成下表:
序号 反应试剂、条件 反应生成的新结构 反应类型
1
2 取代反应
(5)下列关于反应①②的说法中正确的有___________(填标号)。
A.反应①为加成反应
B.化合物Ⅲ中所有原子共平面
C.反应②过程中,有C-O键和C-H键的断裂
D.化合物Ⅱ中,氧原子采取sp3杂化,且不含手性碳原子
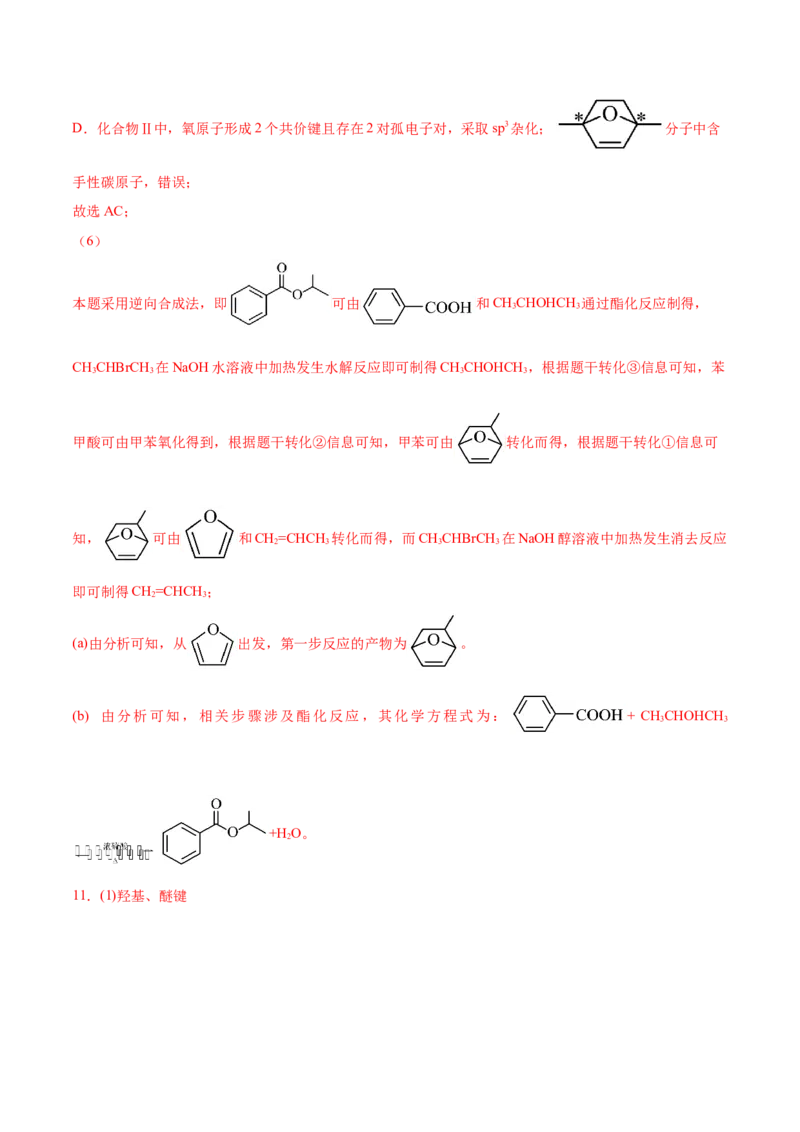
(6)请以 与丙烯为含碳原料,利用所学知识与上述合成路线的信息,合成化合物
,并基于你的合成路线,回答下列问题:
(a)从 出发,第一步反应的产物为 (写结构简式)。(b)相关步骤涉及酯化反应,其化学方程式为 (注明反应条件)。
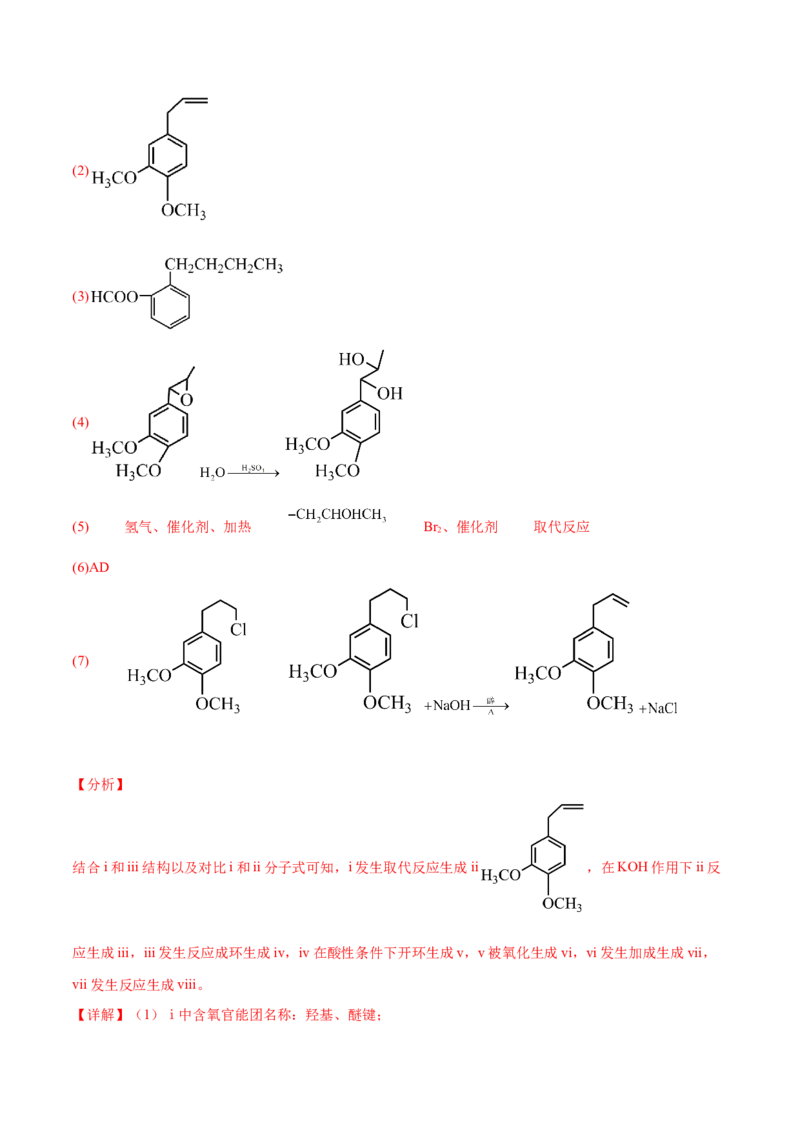
11.(2024·广东佛山·二模)左旋甲基多巴可用于治疗高血压、帕金森等疾病,合成左旋甲基多巴(ⅷ)的一
种路线如图所示。
回答下列问题:
(1)ⅰ中含氧官能团名称为 。
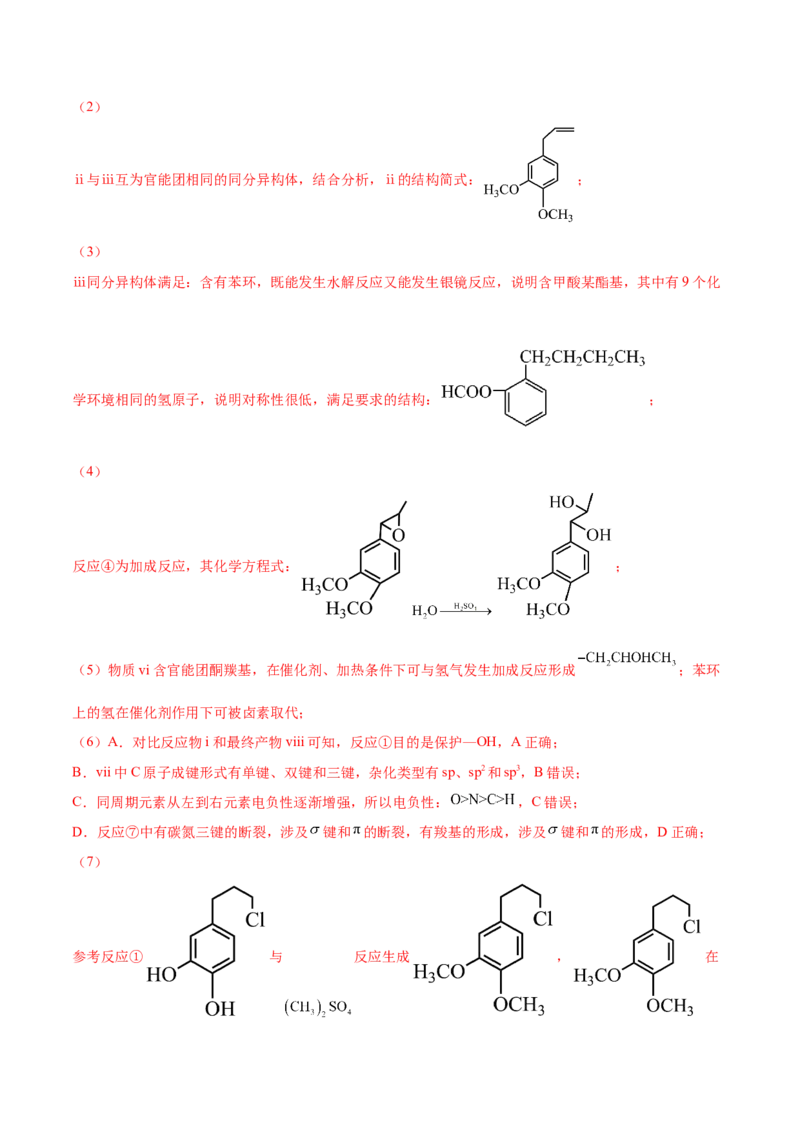
(2)ⅱ与ⅲ互为官能团相同的同分异构体,ⅱ的结构简式为 。
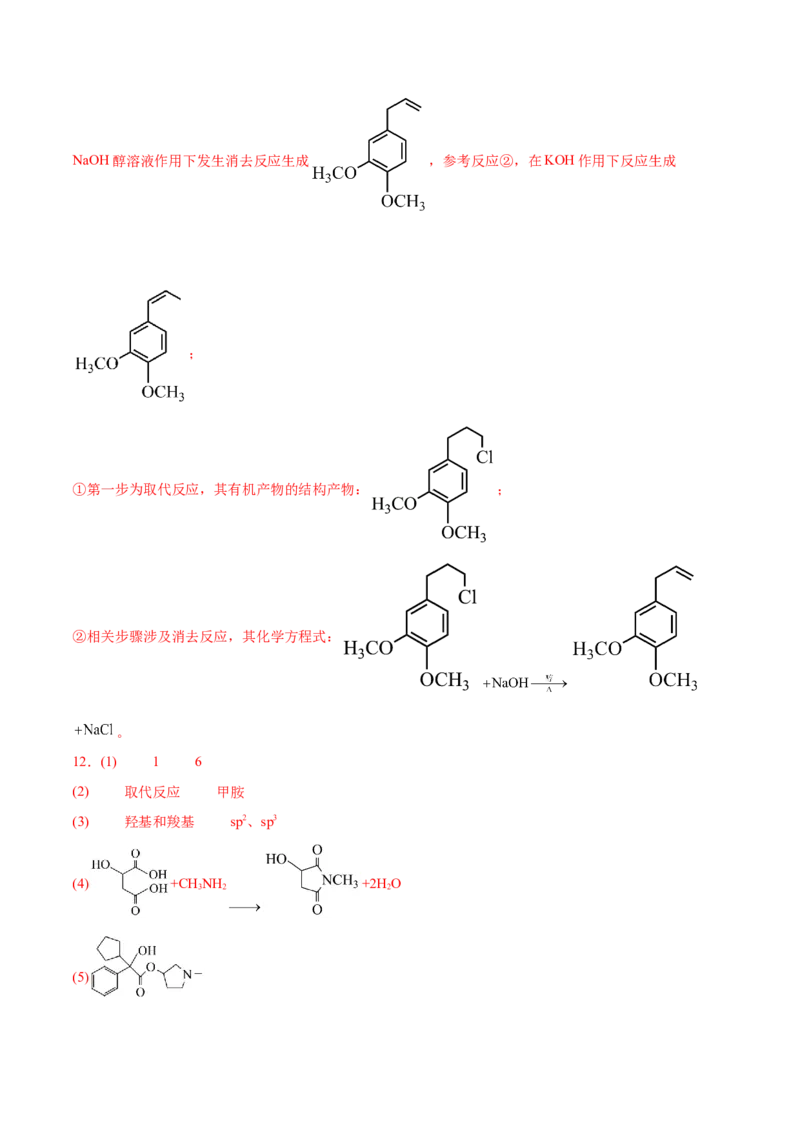
(3)ⅲ还有多种同分异构体,其中含有苯环,既能发生水解反应又能发生银镜反应,有9个化学环境相同的
氢原子的结构为 (任写1个)。
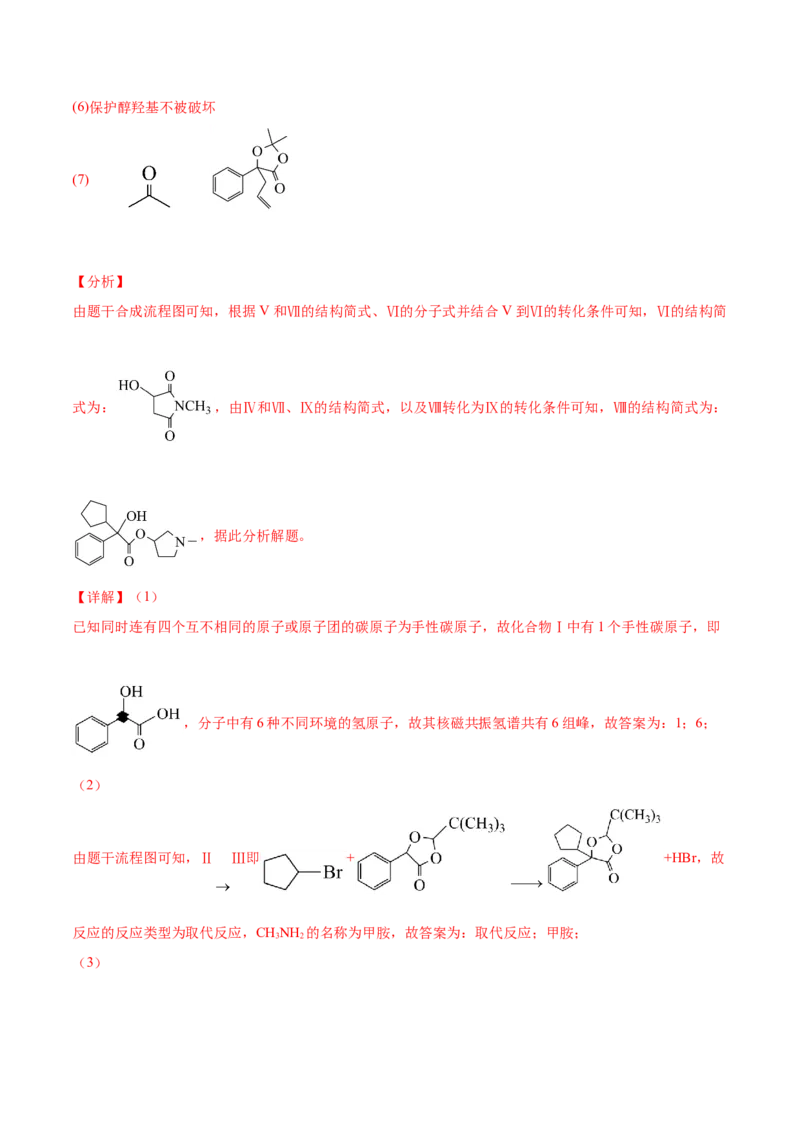
(4)反应④为加成反应,其化学方程式为 。
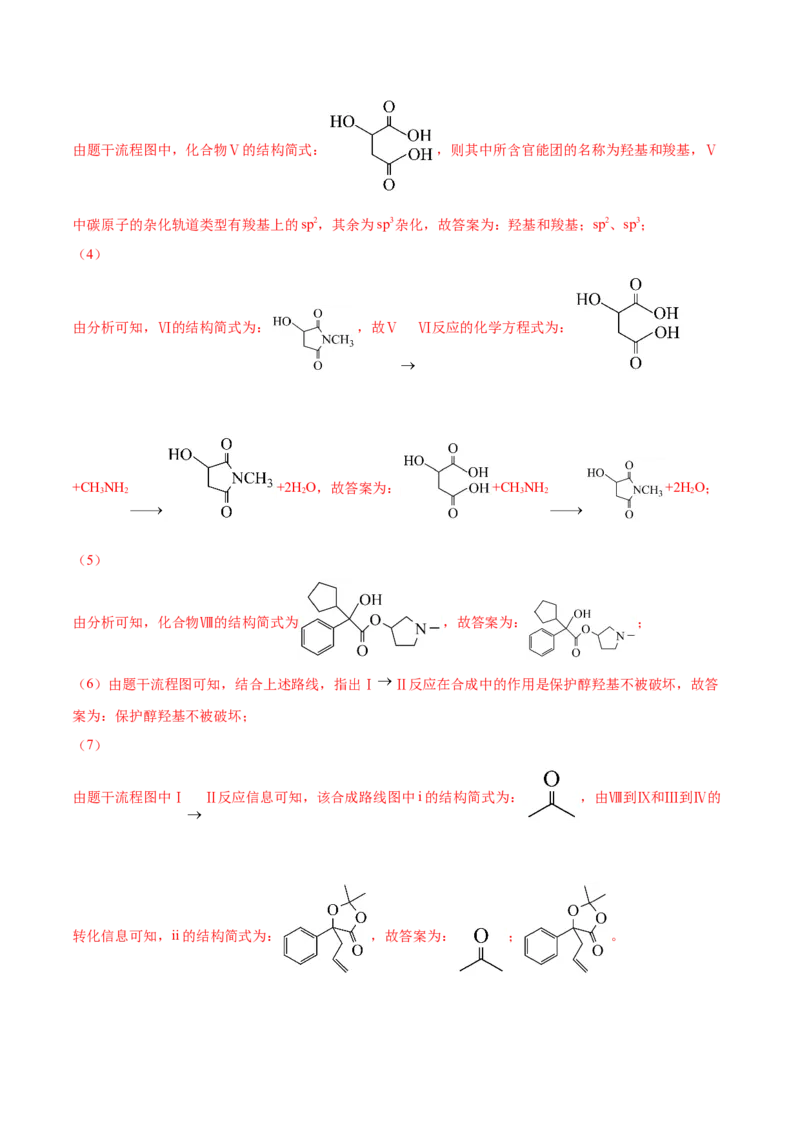
(5)根据ⅵ的结构特征,分析预测其可能的化学性质,完成下表
序号 反应试剂、条件 反应形成的新结构 反应类型
① 还原反应
②
(6)关于上述合成路线,下列说法不正确的是___________(填标号)。
A.反应①目的是保护—OH B.ⅶ中碳原子仅有sp、 两种杂化方式
C.ⅷ中原子的电负性:N>O>C>H D.反应⑦中有 键、 键的断裂和生成(7)以 、 为原料合成化合物 (无机试剂任选),基于你设计的合成
路线,回答下列问题:
①第一步为取代反应,其有机产物的结构产物为 。
②相关步骤涉及消去反应,其化学方程式为 (注明反应条件)。
12.(2024·贵州·二模)索匹溴铵(Ⅸ)是一种抗胆碱能药物,一种以扁桃酸(Ⅰ)和苹果酸(Ⅴ)为原料的合成
路线如图所示(部分条件已省略):
回答下列问题:
(1)化合物Ⅰ中有 个手性碳原子,其核磁共振氢谱共有 组峰。
(2)Ⅱ Ⅲ的反应类型为 , 的名称为 。
(3)化合物Ⅴ中所含官能团的名称为 ,Ⅴ中碳原子的杂化轨道类型有 。
(4)写出Ⅴ Ⅵ反应的化学方程式 。
(5)化合物Ⅷ的结构简式为 。
(6)结合上述路线,指出Ⅰ Ⅱ反应在合成中的作用是 。
(7)参照上述路线,如图所示合成路线中ⅰ、ⅱ的结构简式分别为 和 。参考答案
1.(1) 2-羟基苯甲酸 形成分子间氢键,使沸点更高;而水杨酸形成分子
内氢键,沸点较低
(2)
(3)
(4)酯基、醚键、酰胺基
(5)取代反应
(6) 9
(7)
【分析】
由流程可知,A发生磺化反应在酚羟基邻位引入-SO H得到B,B和氯气发生取代反应在酚羟基对位引入
3
氯原子得到C,结合D化学式,可知C在硫酸作用下失去-SO H得到D: ,D和甲醇发
3生酯化反应生成E ,E发生硝化反应在酚羟基邻位引入硝基得到F
,F中硝基被还原为氨基得到G,G中酚羟基、氨基和ClCH CHOCl发生取代反应得到H,H中氨基氢和
2
CHI发生取代反应在N原子上引入甲基生成I,I中酯基转化为羧基得到J。
3
【详解】(1)
水杨酸的系统名称为2-羟基苯甲酸; 形成分子间氢键,使沸点更高,而水杨酸形
成分子内氢键,沸点较低,故两者比较,水杨酸沸点较低,故答案为:2-羟基苯甲酸;
形成分子间氢键,使沸点更高;而水杨酸形成分子内氢键,沸点较低;
(2)
由分析可知,D为 ,故答案为: ;
(3)
E发生硝化反应在酚羟基邻位引入硝基得到F,反应方程式为:
;
(4)由H结构可知,H含有酯基、醚键、酰胺基;
(5)B→C的反应类型是为取代反应;
(6)
G除苯环外含有1个氯、1个氮、3个氧、2个碳、不饱和度为1,满足下列条件的G的同分异构:①有3
种常见的官能团,FeCl 溶液显紫色,含有酚羟基,③苯环上有两个取代基;则除酚羟基外,另一个取代基
3可以为-CCl(NO )CH、-CH(NO )CHCl、-CHClCH NO ,每种情况均存在邻间对3种情况,共9种情
2 3 2 2 2 2
况,其中核磁共振氢谱有四组峰,且峰面积之比为3:2:2:1,则分子结构对称,且含有甲基,结构简式
为 ,故答案为:9; ;
(7)
中硝基还原为氨基,再和ClCH CHOCl发生取代反应成环得到 ,再和一碘
2
甲烷发生取代反应生成产物,反应为:
。
2.(1)甲苯
(2)羧基
(3)
(4)取代反应
(5)
(6)a
(7)(8) 浓硫酸、加热
【分析】A和K反应生成B,B和丙烯反应生成C,C与乙酸酐发生取代反应生成D和CHCOOH,D和氢
3
气发生加成反应生成E,E与CO发生反应生成F(布洛芬),据此解答。
【详解】(1)
A的结构简式为 ,A的名称是甲苯,故答案为:甲苯;
(2)
布洛芬的结构简式为 ,含有官能团是羧基,故答案为:羧基;
(3)由结构简式可知,E的分子式为 ,故答案为: ;
(4)根据以上分析可知C→D的类型为取代反应,故答案为:取代反应;
(5)
在浓硫酸作催化剂、加热条件下,甲苯和浓硝酸发生取代反应生成TNT,由甲苯制备TNT(三硝基甲苯)
的化学反应方程式为 ;
(6)
终止剂可将 转化为 ,从而使B→C反应终止,则终止剂能提供氢离子,HO、
2
CCl 、C HOH三种物质中,水可以电离出离子,最适合作为终止剂的物质是水,故答案为:a;
4 2 5
(7)
M与F(布洛芬)互为同系物,M分子中有8个C原子,M含有1个苯环、1个羧基,苯环侧链没有其它
不饱和,M的同分异构体满足下列条件:①属于芳香族化合物,说明含有苯环;②能发生银镜反应,也能
发生水解反应,说明含有-OOCH;③核磁共振氢谱有4组峰且峰面积之比为1:2:2:3,说明存在对称结构,符合条件的同分异构体结构简式为 ;
(8)
与HOCH CHOH发生酯化反应生成 ,
2 2
与CH=C(CH)COOH发生酯化反应生成
2 3
, 发生加聚反应生成目标
产物,因此试剂X的结构简式为HOCH CHOH,条件①为浓硫酸、加热,物质Y的结构简式为
2 2
。
3.(1) 3-氯-3-甲基-1-丁炔 氨基、羧基
(2) 吸收副产物HCl,提高产率 取代反应
(3)3:2
(4) + +2H O
2
(5)30(6) (或其他合理答
案)
【分析】
A和 发生取代反应生成B为 ,B和 发生取代反应生
成C,C发生成环反应生成D,D发生取代反应生成山油柑碱,以此解答。
【详解】(1)
的主链上有4个碳原子,3号碳上有1个氯原子和1个甲基,碳碳三键在1号位,名称是3-
氯-3-甲基-1-丁炔,A中含有的官能团的名称是氨基、羧基。
(2)
B和 发生取代反应生成C,同时有HCl生成, 的作用是吸收副产物HCl,提高产率,
D→山油柑碱的反应类型是取代反应。
(3)
1mol 可以和3molBr 发生取代反应生成 ,D中碳碳双键可以和1个
2
Br 发生加成反应,其中羟基邻位的H原子可以和1个Br 发生取代反应,则1molD可以和2molBr 发生反
2 2 2
应,故答案为:3:2。
(4)A和 发生取代反应生成B为 ,化学方程式为: +
+2H O。
2
(5)
有机物M分子中比B多2个H,M符合条件:①含有 ,且只有一个苯环上有取代基;②
遇 溶液发生显色反应,能与 溶液反应,说明其中含有-OH和-COOH;③ 直接连在苯环
上,且所有取代基连在同一个苯环上;则 上的取代基为-OH、-COOH、-NH ,
2
上一共有5个位置,当羧基在1号位,氨基在2号位,羟基可以在3、4、5号位,
共3种结构;当羧基在1号位,氨基在3号位,羟基可以在2、4、5号位,共3种结构;当羧基在1号位,
氨基在4号位,羟基可以在2、3、5号位,共3种结构;当羧基在1号位,氨基在5号位,羟基可以在2、
3、4号位,共3种结构;以此类推,当羧基在2号位上时有12种,在3号位上时有6种,共 30种。
(6)
和Br 发生加成反应生成 , 和苯酚发生取代反应
2生成 , 和H 发生加成反应生成
2
,合成路线为:
(或其他合理答案)。
4.(1)氨基、醚键
(2)甲醛
(3)还原反应
(4)ABC
(5)
(6)4
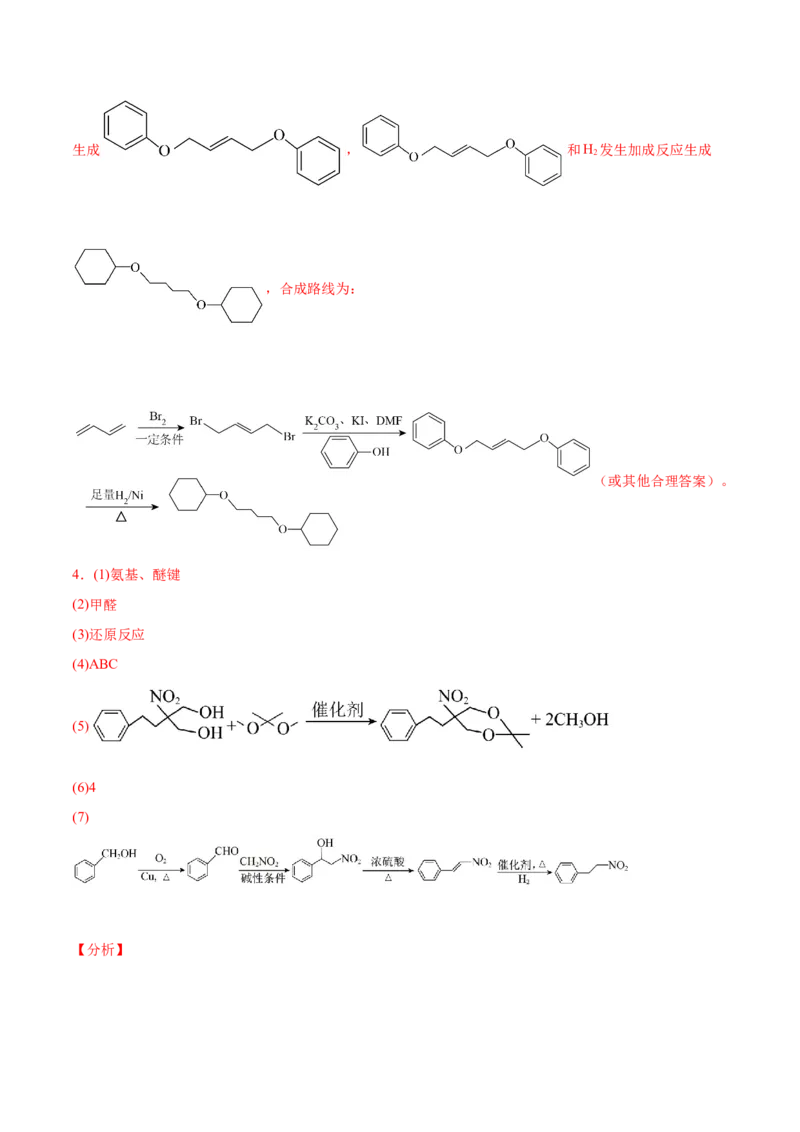
(7)
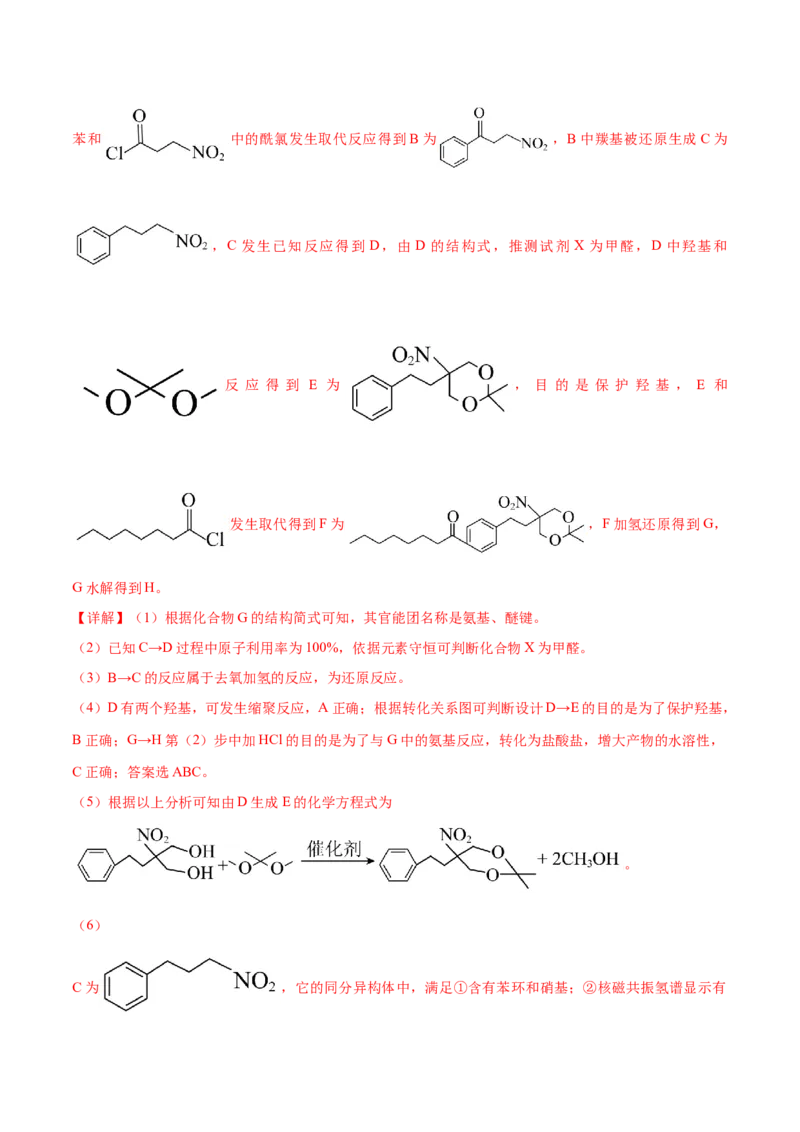
【分析】苯和 中的酰氯发生取代反应得到B为 ,B中羰基被还原生成C为
,C 发生已知反应得到 D,由 D 的结构式,推测试剂 X 为甲醛,D 中羟基和
反 应 得 到 E 为 , 目 的 是 保 护 羟 基 , E 和
发生取代得到F为 ,F加氢还原得到G,
G水解得到H。
【详解】(1)根据化合物G的结构简式可知,其官能团名称是氨基、醚键。
(2)已知C→D过程中原子利用率为100%,依据元素守恒可判断化合物X为甲醛。
(3)B→C的反应属于去氧加氢的反应,为还原反应。
(4)D有两个羟基,可发生缩聚反应,A正确;根据转化关系图可判断设计D→E的目的是为了保护羟基,
B正确;G→H第(2)步中加HCl的目的是为了与G中的氨基反应,转化为盐酸盐,增大产物的水溶性,
C正确;答案选ABC。
(5)根据以上分析可知由D生成E的化学方程式为
。
(6)
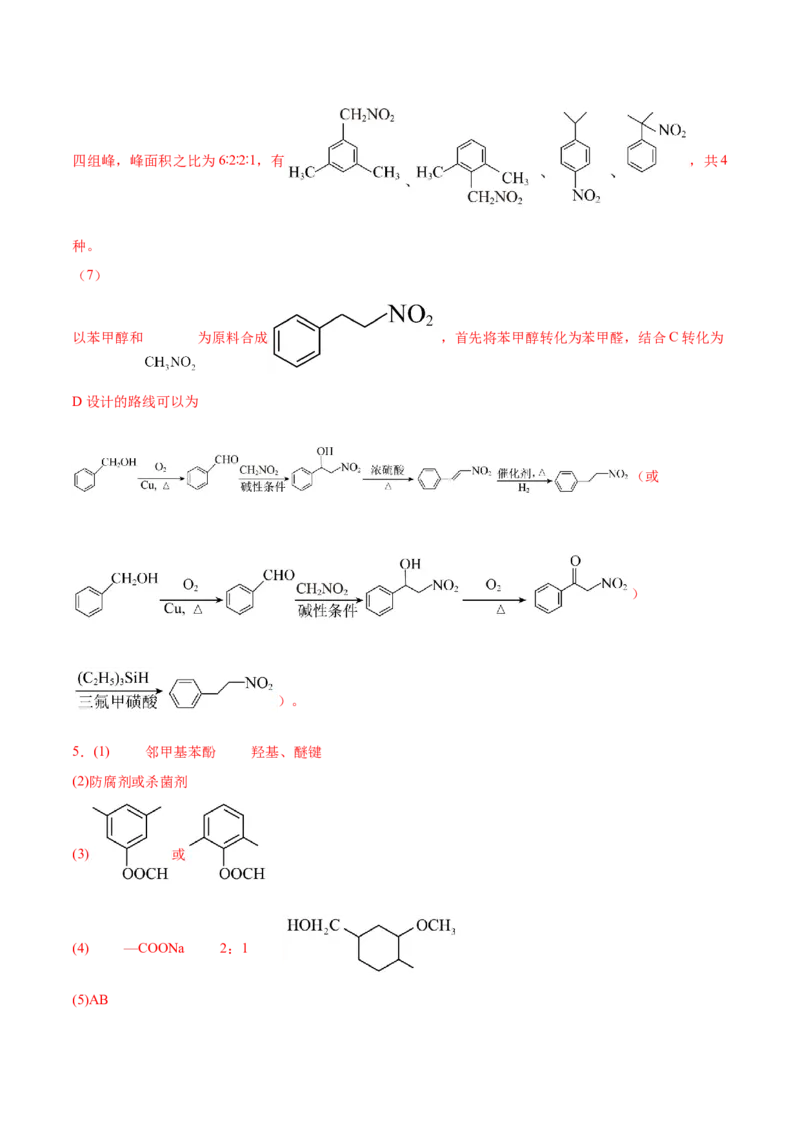
C为 ,它的同分异构体中,满足①含有苯环和硝基;②核磁共振氢谱显示有四组峰,峰面积之比为6∶2∶2∶1,有 ,共4
种。
(7)
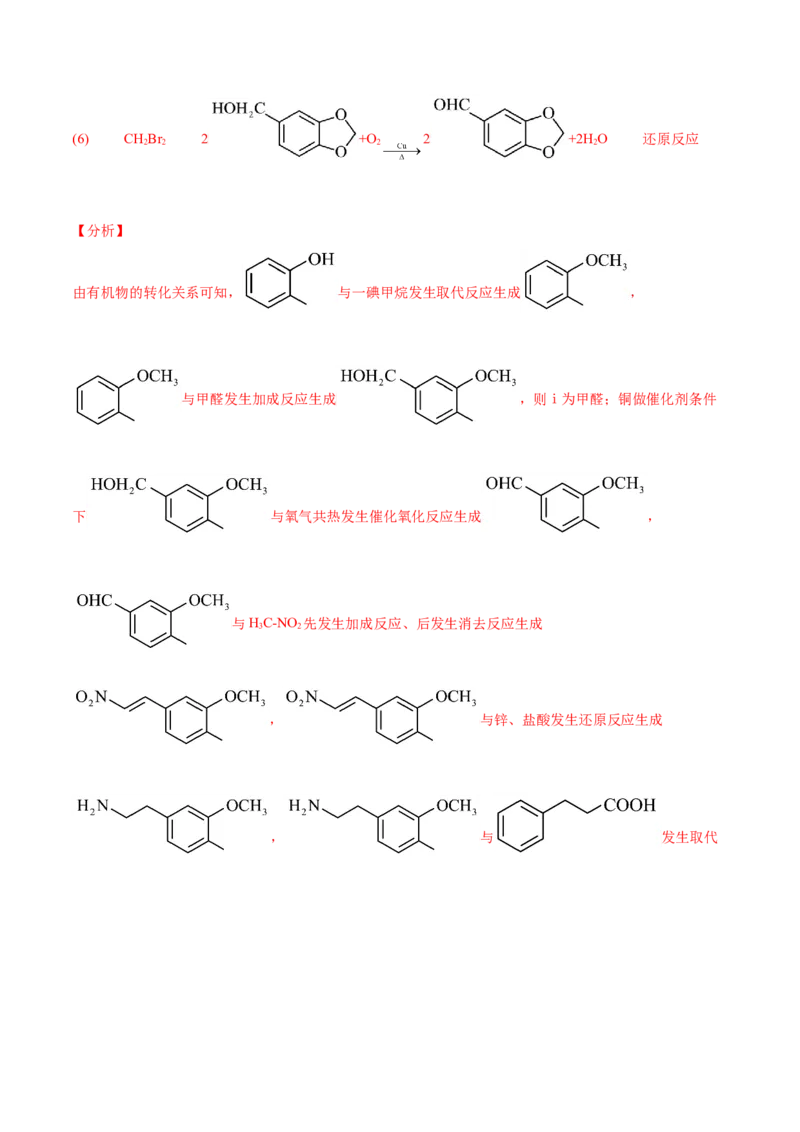
以苯甲醇和 为原料合成 ,首先将苯甲醇转化为苯甲醛,结合C转化为
D设计的路线可以为
(或
)
)。
5.(1) 邻甲基苯酚 羟基、醚键
(2)防腐剂或杀菌剂
(3) 或
(4) —COONa 2:1
(5)AB(6) CH Br 2 +O 2 +2H O 还原反应
2 2 2 2
【分析】
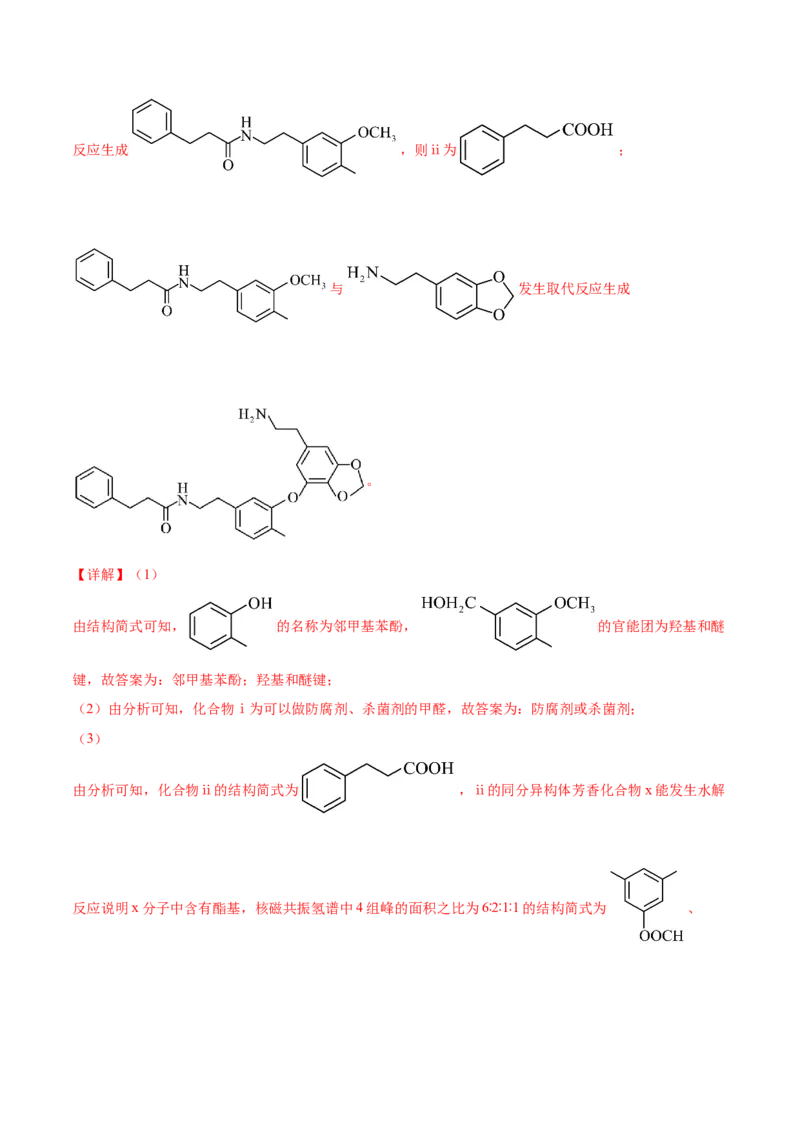
由有机物的转化关系可知, 与一碘甲烷发生取代反应生成 ,
与甲醛发生加成反应生成 ,则ⅰ为甲醛;铜做催化剂条件
下 与氧气共热发生催化氧化反应生成 ,
与HC-NO 先发生加成反应、后发生消去反应生成
3 2
, 与锌、盐酸发生还原反应生成
, 与 发生取代反应生成 ,则ⅱ为 ;
与 发生取代反应生成
。
【详解】(1)
由结构简式可知, 的名称为邻甲基苯酚, 的官能团为羟基和醚
键,故答案为:邻甲基苯酚;羟基和醚键;
(2)由分析可知,化合物ⅰ为可以做防腐剂、杀菌剂的甲醛,故答案为:防腐剂或杀菌剂;
(3)
由分析可知,化合物ⅱ的结构简式为 ,ⅱ的同分异构体芳香化合物x能发生水解
反应说明x分子中含有酯基,核磁共振氢谱中4组峰的面积之比为6∶2∶1∶1的结构简式为 、,故答案为: 或 ;
(4)
由结构简式可知, 分子中含有的醛基能与新制氢氧化铜悬浊液发生氧化反应生成
、氧化亚铜和水,反应的化学方程式为
+2Cu(OH) +NaOH +Cu O↓+3HO,则D与新制氢氧化铜悬浊液反应时,
2 2 2
消耗氢氧化铜和D的物质的量之比2:1,反应形成的新结构为—COONa; 分子
中含有的醛基和苯环一定条件下能与氢气发生加成反应生成 ,故答案为:—
COONa;2:1; ;
(5)
A.由结构简式可知, 分子中苯环上碳原子的杂化方式为sp2杂化,饱和碳原子的杂化方式
为sp3杂化,故正确;
B.由分析可知,反应①为 与一碘甲烷发生取代反应生成 和碘化氢,反应
中有C-I键和H-O键断裂,故正确;C.由结构简式可知, 分子中含有的σ键数目为19,则1mol化合物B中含有σ键的数目
为19 N ,故错误;
A
D.由结构简式可知,产品I属于极性分子,但分子中憎水基的结构远大于亲水基氨基,所以产品I难溶于
水,故错误;
故选AB;
(6)
由有机物的转化关系可知,以 、CHBr 为主要原料合成流程中的物质H的合成步
2 2
骤为 与CHBr 发生取代反应生成 ,铜做催化剂条件下
2 2
与氧气共热发生催化氧化反应生成 , 与
HC-NO 先发生加成反应、后发生消去反应生成 ,
3 2
与铁、盐酸发生还原反应生成 ;
①由分析可知,原料ⅲ的结构简式为CHBr ,故答案为:CHBr ;
2 2 2 2
②由分析可知,芳香醇转化为芳香醛的反应为铜做催化剂条件下 与氧气共热发生催化氧化反应生成 和水,反应的化学方程式为2 +O 2
2
+2H O,故答案为:2 +O 2 +2H O;
2 2 2
③由分析可知,最后一步反应为 与铁、盐酸发生还原反应生成
,故答案为:还原反应。
6.(1) 甲苯 酮羰基
(2) 还原
(3)BD
(4)
(5) 、
(6)
【分析】根据A分子式及反应产物可知,A为甲苯,发生取代反应生成 , 发生硝化反应生成
B ,根据已知①可知B反应生成C ;根据D分子式及E结构简式可知D
;根据已知②可知G结构简式 ,根据J结构简式及反应条件
可知 I 发生取代反应,则 I 结构简式: ,则 H 结构简式:
;
【详解】(1)
根据分析可知,A为甲苯;D结构简式: ,含氧官能团为酮羰基;
(2)
根据分析可知,H结构简式: ;由F反应生成G的反应过程中,硝基被还原为氨基,反
应类型为还原反应;
(3)A.连接4个不同的原子或原子团的碳原子为手性碳原子,根据J结构简式可知,J中无手性碳原子,
A错误;
B.电负性: ,键的极性: ,B正确;
C.J中含氨基和酰胺基,在酸性条件下也可水解,C错误;
D.根据成键可知J中N原子和C原子的杂化轨道类型均有2种,分别为sp2、sp3杂化,D正确;(4)
发生加成反应,根据分析可知,反应方程式:
;
(5)
芳香化合物 是B的同分异构体,满足条件:①能发生银镜反应,且能发生水解反应,则含甲酸某酯基;
②核磁共振氢谱有4组峰,峰面积之比为1:1:2:4,说明含2个 ,则符合要求的结构简式:
、 ;
(6)
乙醇被催化氧化生成乙醛,与 反应生成 , 与 反应生
成目标产物,具体合成路线如下:
。
7.(1)光照
(2) 羟基、酮羰基 取代反应
(3)4
(4)(5)18
(6)
【分析】
由有机物的转化关系可知,甲苯在光照条件下与氯气发生取代反应生成 , 与NaCN
发生取代反应生成 , 酸性条件下发生水解反应生成 ,一定条件下
与 发生取代反应生成 ,则H为 ;催化剂
作用下 与HC(OC H) 发生取代反应 ,氢氧化钠作用下
2 5 3
与 发生取代反应生成 。
【详解】(1)
由分析可知,反应①为甲苯在光照条件下与氯气发生取代反应生成 和氯化氢,故答案为:光照;
(2)由结构简式可知, 的官能团为羟基和酮羰基;由分析可知,F→G的反应为氢氧化钠
作用下 与 发生取代反应生成 ,故答案为:羟基、酮羰
基;取代反应;
(3)
一定条件下与足量氢气发生加成所得化合物中含有如图*所示的4个手性碳原子:
,故答案为:4;
(4)
由分析可知,N为催化剂条件下 与HC(OC H) 发生取代反应 和乙
2 5 3
醇,反应的化学方程式为
,故答案为:
;
(5)相对分子质量比D多14的同系物K的苯环上只有两个取代基,能与Na反应生成H2,说明同分异构体分
子中含有羟基,能与银氨溶液发生银镜反应,说明同分异构体分子中含有醛基,则两个取代基可能为—
OH和—CHCHCHO,或—OH和—CH(CH )CHO,或—CHOH和—CHCHO,或—CHCHOH、—
2 2 3 2 2 2 2
CHO,或—CH(OH)CH 和—CHO,或—CH 和 ,取代基在苯环上都有邻间对3种位置异构,
3 3
所以满足条件的K的同分异构体共有18种,故答案为:18;
(6)
由题给信息可知,以苯酚和 为原料制备 的合成步骤为 与HCl发生取
代反应生成 , 与NaCN发生取代反应生成 , 酸性条件下发生水解反
应生成 , 一定条件下与苯酚发生取代反应生成 ,合成路
线为 。
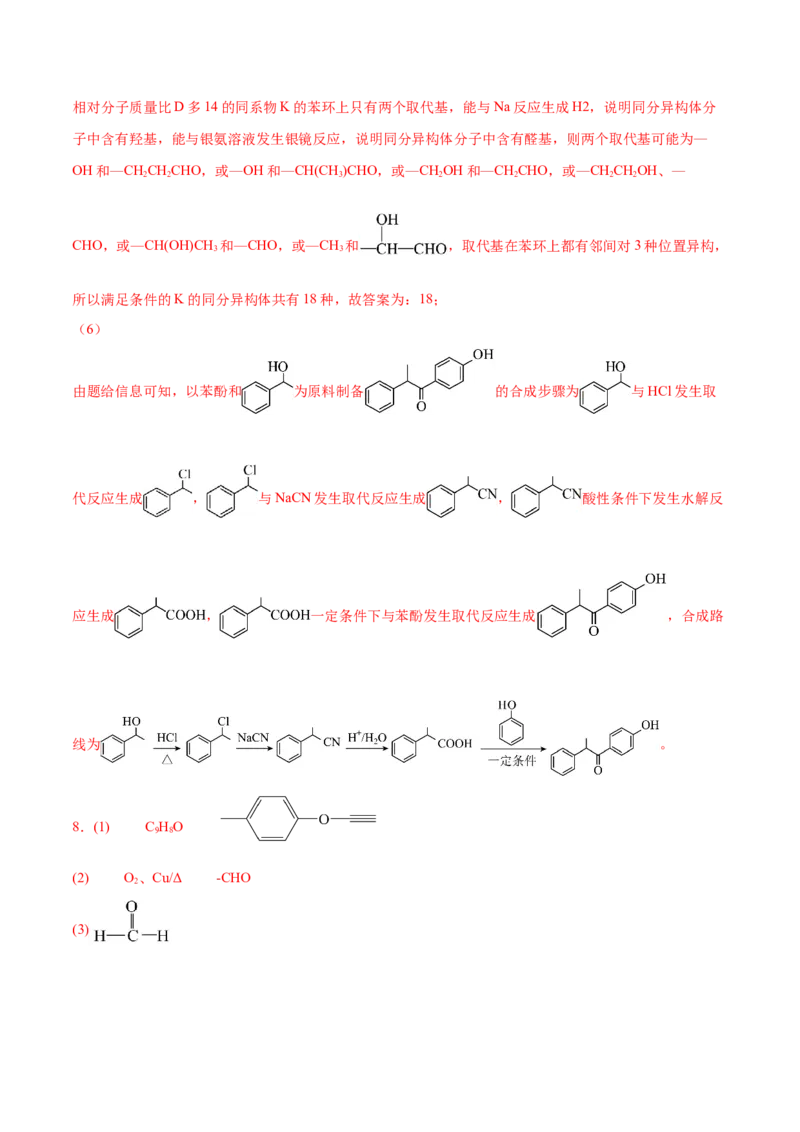
8.(1) C HO
9 8
(2) O 、Cu/Δ -CHO
2
(3)(4) +Br +HBr
2
(5)AD
(6)2
(7)
+
【分析】
CH≡CH与x在KOH存在下反应生成 ,该反应的原子利用率为100%,则x为HCHO;苯与Br 在
2
FeBr 催化下发生取代反应生成溴苯和HBr; 与溴苯在吡啶、加热条件下反应生成 ,
3
与H 在Pd、加热时反应生成 , 与HO 在催化剂存在下反应生成
2 2 2
, 与CO 在TBAB、加热时反应生成H和I。
2
【详解】(1)
E的结构简式为 ,E的分子式为C HO;其芳香同分异构体中,核磁共振氢谱为四组峰,峰面
9 8
积比为3∶2∶2∶1,即该物质有苯环,有四种等效氢,且氢原子数目比为3∶2∶2∶1,符合条件的同分异构体的结
构简式为 。
(2)
E中官能团为碳碳三键和醇羟基,E发生生成有机产物的氧化反应,E与O 在Cu作催化剂且加热的条件下
2生成 ,即反应的试剂和条件为O、Cu/r,反应形成的新结构为-CHO。
2
(3)
A与x反应生成B,该反应的原子利用率为100%,根据A和B的结构可知,x为 。
(4)
C到D即苯环上有一个H被Br取代,化学方程式为: +Br +HBr。
2
(5)A.由图可知,F到G的反应过程中有C=C双键的断裂和C-O键的形成,故A正确;
B.对比G与H的结构,G与CO 发生加成反应得H,CO 中一个C=O双键断裂,没有C=O双键的形成、
2 2
有C-O键的形成,故B错误;
C.E中苯环碳为sp2杂化、碳碳三键碳为sp杂化、与羟基相连的C为sp3杂化,故C错误;
D.CO 结构为O=C=O,C为sp杂化,属于直线型分子,分子的正电中心和负电中心重合,属于非极性分
2
子,故D正确;
故选AD。
(6)
中“*”标示的2个碳原子为手性碳原子。
(7)
根据 和 的结构可知,它们由 和CO 在TBAB和加热的条件下生成,
2
由 和HO 在催化剂的条件下生成, 是 与氢气
2 2
在 Pd 和 加 热 条 件 下 生 成 , 由 此 可 知 原 料 A 的 同 系 物 为 , 则 合 成 路 线 为 :+ 。
9.(1)浓硝酸、浓硫酸
(2)
(3)硝基、羧基
(4)
(5)
(6) 中间产物1 中间产物3
(7)40%
【分析】
A的分子式为C H,从D的结构简式可知,B是 ,C的结构简式为
7 8,C水解生成D,根据G的结构简式,结合已知信息ii,可知F的结构简式为
,E的结构简式为 ,F到G失水发生取代反应形成环状结构,G到I发生
氧化反应,I与HO 反应生成J,J转化为K。
2 2
【详解】(1)A→B发生甲苯苯环上硝化反应,所需试剂是:浓硝酸、浓硫酸;
(2)
B→C的反应为取代反应,该反应的化学方程式为:
;
(3)
E的结构简式为 ,所含官能团的名称为:硝基、羧基;
(4)
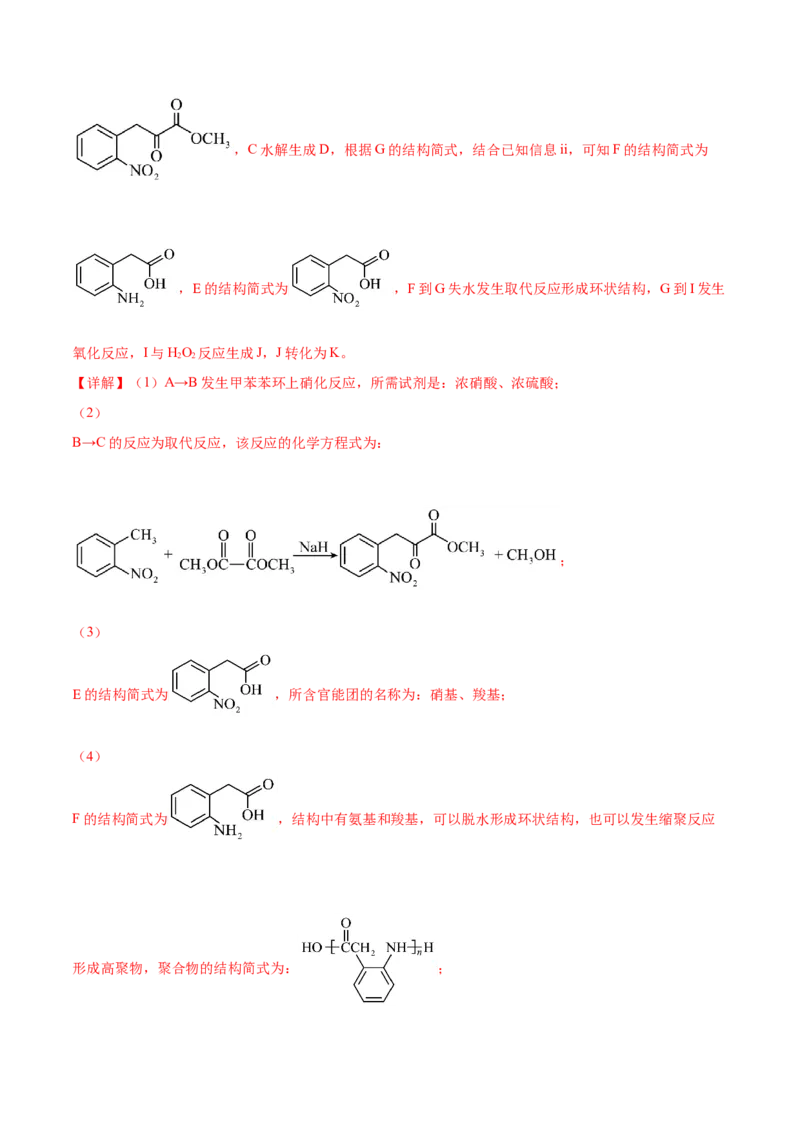
F的结构简式为 ,结构中有氨基和羧基,可以脱水形成环状结构,也可以发生缩聚反应
形成高聚物,聚合物的结构简式为: ;(5)
I的结构简式为 ,分子式为C HNO ,芳香族化合物M是I的同分异构体,能与NaHCO
8 5 2 3
反应,结构中有-COOH,核磁共振氢谱有3组峰,峰面积比为2:2:1,符合条件的结构简式为:
;
(6)
J到K反应过程,结合题目中已知i可知, 与 先发生加成反应,生成中间
产物1 ,再发生消去反应生成中间产物2 ,中间产物2再发生
已知信息ii的反应生成中间产物3 ,最后中间产物3失水生成K;(7)三氯乙烯(Cl C=CHCl)结构中有一个H原子,核磁共振氢谱应该显示1个峰,K中酰胺基上的H在核
2
磁共振氢谱中是一个特征峰,加入0.1mol三氯乙烯,K中酰胺基上的H与三氯乙烯中的H的峰面积比为
2:5,说明K中酰胺基上的氢原子的物质的量为0.1× =0.04mol,K的物质的量为0.04mol,0.1mol的J与
0.15mol的邻苯二胺反应的理论产量应该生成0.1mol的K,因此产率为 。
10.(1) C HO 对苯二甲酸(或1,4-苯二甲酸)
6 8
(2)
(3)
(4) H ,催化剂、△ 加成反应或还原反应 Br ,Fe或FeBr (或Cl,光照)
2 2 3 2
(或 )
(5)AC
(6) + CHCHOHCH +H O
3 3 2
【分析】
Ⅰ和乙烯发生加成反应生成Ⅱ,Ⅱ转化为Ⅲ:对二甲苯,对二甲苯与酸性KMnO 溶液反应可得到化合物Ⅳ,
4
则为甲基被氧化为羧基得到Ⅳ:对苯二甲酸(或1,4-苯二甲酸);乙烯转化为Ⅴ,化合物Ⅴ是环状分子,与
HO加成可得到化合物Ⅵ,则Ⅴ为环氧乙烷 ;Ⅳ:对苯二甲酸与Ⅵ:乙二醇发生缩聚反应生成PET;
2
【详解】(1)由图可知,化合物I的分子式为C HO。化合物Ⅲ与酸性KMnO 溶液反应使得甲基被氧化
6 8 4为羧基得到化合物Ⅳ,则化合物Ⅳ的名称为对苯二甲酸(或1,4-苯二甲酸);
(2)
由分析可知,化合物Ⅴ的结构简式为 ;
(3)
化合物Ⅱ与足量H 加成后得到 ,分子中含有8个碳、1个氧、不饱和度为2,其同分异构体
2
中核磁共振氢谱中峰面积比为3:1:3,则为对称结构且应该含有2组每组2个甲基,结构可以为:
;
(4)
苯在催化剂加热条件下和氢气发生加成反应生成 ,故答案为: H,催化剂、△;加成反
2
应或还原反应;
Ⅲ中苯环氢、甲基氢均可以发生取代反应,在铁催化作用下苯环氢可以被溴取代生成 ;在光照
条件下,甲基氢可以被氯气中氯取代生成 ;故答案为:Br ,Fe 或 FeBr (或 Cl ,光照);
2 3 2
(或 );
(5)A.反应①得到产物的不饱和度减小,为加成反应,正确;
B.化合物Ⅲ中含有甲基,甲基为四面体结构,所有原子不共平面,错误;
C.反应②过程中,有C-O键和C-H键的断裂,反应生成苯环和小分子水,正确;D.化合物Ⅱ中,氧原子形成2个共价键且存在2对孤电子对,采取sp3杂化; 分子中含
手性碳原子,错误;
故选AC;
(6)
本题采用逆向合成法,即 可由 和CHCHOHCH 通过酯化反应制得,
3 3
CHCHBrCH 在NaOH水溶液中加热发生水解反应即可制得CHCHOHCH ,根据题干转化③信息可知,苯
3 3 3 3
甲酸可由甲苯氧化得到,根据题干转化②信息可知,甲苯可由 转化而得,根据题干转化①信息可
知, 可由 和CH=CHCH 转化而得,而CHCHBrCH 在NaOH醇溶液中加热发生消去反应
2 3 3 3
即可制得CH=CHCH;
2 3
(a)由分析可知,从 出发,第一步反应的产物为 。
(b) 由分析可知,相关步骤涉及酯化反应,其化学方程式为: + CH CHOHCH
3 3
+H O。
2
11.(1)羟基、醚键(2)
(3)
(4)
(5) 氢气、催化剂、加热 Br 、催化剂 取代反应
2
(6)AD
(7)
【分析】
结合i和iii结构以及对比i和ii分子式可知,i发生取代反应生成ii ,在KOH作用下ii反
应生成iii,iii发生反应成环生成iv,iv在酸性条件下开环生成v,v被氧化生成vi,vi发生加成生成vii,
vii发生反应生成viii。
【详解】(1)ⅰ中含氧官能团名称:羟基、醚键;(2)
ⅱ与ⅲ互为官能团相同的同分异构体,结合分析,ⅱ的结构简式: ;
(3)
ⅲ同分异构体满足:含有苯环,既能发生水解反应又能发生银镜反应,说明含甲酸某酯基,其中有9个化
学环境相同的氢原子,说明对称性很低,满足要求的结构: ;
(4)
反应④为加成反应,其化学方程式: ;
(5)物质vi含官能团酮羰基,在催化剂、加热条件下可与氢气发生加成反应形成 ;苯环
上的氢在催化剂作用下可被卤素取代;
(6)A.对比反应物i和最终产物viii可知,反应①目的是保护—OH,A正确;
B.vii中C原子成键形式有单键、双键和三键,杂化类型有sp、sp2和sp3,B错误;
C.同周期元素从左到右元素电负性逐渐增强,所以电负性: ,C错误;
D.反应⑦中有碳氮三键的断裂,涉及 键和 的断裂,有羧基的形成,涉及 键和 的形成,D正确;
(7)
参考反应① 与 反应生成 , 在NaOH醇溶液作用下发生消去反应生成 ,参考反应②,在KOH作用下反应生成
;
①第一步为取代反应,其有机产物的结构产物: ;
②相关步骤涉及消去反应,其化学方程式:
。
12.(1) 1 6
(2) 取代反应 甲胺
(3) 羟基和羧基 sp2、sp3
(4) +CH NH +2H O
3 2 2
(5)(6)保护醇羟基不被破坏
(7)
【分析】
由题干合成流程图可知,根据V和Ⅶ的结构简式、Ⅵ的分子式并结合V到Ⅵ的转化条件可知,Ⅵ的结构简
式为: ,由Ⅳ和Ⅶ、Ⅸ的结构简式,以及Ⅷ转化为Ⅸ的转化条件可知,Ⅷ的结构简式为:
,据此分析解题。
【详解】(1)
已知同时连有四个互不相同的原子或原子团的碳原子为手性碳原子,故化合物Ⅰ中有1个手性碳原子,即
,分子中有6种不同环境的氢原子,故其核磁共振氢谱共有6组峰,故答案为:1;6;
(2)
由题干流程图可知,Ⅱ Ⅲ即 + +HBr,故
反应的反应类型为取代反应,CHNH 的名称为甲胺,故答案为:取代反应;甲胺;
3 2
(3)由题干流程图中,化合物Ⅴ的结构简式: ,则其中所含官能团的名称为羟基和羧基,Ⅴ
中碳原子的杂化轨道类型有羧基上的sp2,其余为sp3杂化,故答案为:羟基和羧基;sp2、sp3;
(4)
由分析可知,Ⅵ的结构简式为: ,故Ⅴ Ⅵ反应的化学方程式为:
+CH NH +2H O,故答案为: +CH NH +2H O;
3 2 2 3 2 2
(5)
由分析可知,化合物Ⅷ的结构简式为 ,故答案为: ;
(6)由题干流程图可知,结合上述路线,指出Ⅰ Ⅱ反应在合成中的作用是保护醇羟基不被破坏,故答
案为:保护醇羟基不被破坏;
(7)
由题干流程图中Ⅰ Ⅱ反应信息可知,该合成路线图中i的结构简式为: ,由Ⅷ到Ⅸ和Ⅲ到Ⅳ的
转化信息可知,ii的结构简式为: ,故答案为: ; 。