文档内容
易错点 12 硅元素及其化合物
易错题【01】硅及其化合物的性质
(1)自然界中无游离态的硅,通常原子晶体不导电,但硅是很好的半导体材料,是制作光电
池的材料。SiO 不导电,是制作光导纤维的材料。
2
(2)工业上制备粗硅,是用过量的C和SiO 在高温下反应,由于C过量,生成的是CO而不
2
是CO,该反应必须在隔绝空气的条件下进行。
2
(3)氢氟酸不能用玻璃容器盛放;NaOH溶液能用玻璃试剂瓶,但不能用玻璃塞。
(4)酸性氧化物一般能与水反应生成酸,但SiO 不溶于水;酸性氧化物一般不与酸作用,但
2
SiO 能与HF反应。
2
(5)硅酸盐大多难溶于水,常见可溶性硅酸盐是硅酸钠,其水溶液称为泡花碱或水玻璃,但
却是盐溶液。硅胶(mSiO·nHO)是一种很好的无毒干燥剂。
2 2
(6)H CO 的酸性大于HSiO 的,所以有NaSiO +CO(少量)+HO===H SiO↓+NaCO ,
2 3 2 3 2 3 2 2 2 3 2 3
但高温下NaCO +SiO NaSiO +CO↑也能发生,原因可从两方面解释:①硅酸盐
2 3 2 2 3 2
比碳酸盐稳定;②从化学平衡角度,由高沸点难挥发固体SiO 制得低沸点易挥发的CO 气
2 2
体。
(7)水泥、玻璃与陶瓷是三大传统无机非金属材料;碳化硅、氮化硅等是新型无机非金属材
料。
易错题【02】新型无机非金属材料
材料类型 主要特性 示例 用途
能承受高温,强度 汽轮机叶片、轴承、永久性模具
高温结构陶瓷 氮化硅陶瓷
高 等
半导体陶瓷 具有电学特性 二氧化锡陶瓷 集成电路中的半导体
光学材料 具有光学特性 光导纤维 光缆通讯、医疗、照明等
生物陶瓷 具有生物功能 氧化铝陶瓷 人造骨骼、人造关节、接骨螺钉
易错题【03】常考非金属及其化合物的性质与用途的对应关系
重要性质 主要用途
① 硅是常用半导体材料 用于制造芯片、硅太阳能电池
② SiO 导光性能强、抗干扰性能好 用于生产光导纤维
2
③ 二氧化硫与O 反应 用作葡萄酒中食品添加剂
2
④ 液氨汽化时吸收大量的热 用作制冷剂
⑤ 氢氟酸与玻璃中SiO 反应 用氢氟酸刻蚀玻璃工艺
2
⑥ 次氯酸盐(如NaClO等) 用于漂白棉、麻、纸张等
具有强氧化性
⑦ 硫酸钡难溶于水和盐酸 医疗上用作“钡餐”
易错题【03】(1)硅元素的原子序数为14,基态原子的简化电子排布式为[Ne] 3s23p2,核外电子的空间
运动状态有7种,不成对电子数有2种;单晶硅为原子晶体,晶体中每个Si原子以sp3杂化,
分别与4个相邻的Si 原子形成4个σ键,Si原子的配位数为4,晶体中最小的环是6元环,
1个环中平均含有2Si原子,含Si-Si键数为3。
(2)二氧化硅是直接由原子构成的原子晶体,晶体中Si原子均以sp3杂化,分别与4个O
原子成键,每个O原子与2个Si原子成键,晶体中的最小环为12元环,其中有6个Si原
子和6个O原子,含有12个Si-O键;每个Si原子被12个环共有,每个O原子被4个环共
有,每个Si-O键被4个环共有,Si原子数与O原子数之比为1:2。二氧化硅不溶于水,熔
沸点和硬度高于分子晶体干冰。
典例分析
例1、陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关
系。下列说法错误的是
A.实验室熔融烧碱时,不可选用陶瓷坩埚
B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成
C.陶瓷是应用较早的人造材料,主要化学成分是二氧化硅
D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点
C【解析】A.陶瓷含有二氧化硅,烧碱为氢氧化钠,能够与陶瓷中的二氧化硅反应,熔融
烧碱不能选用玻璃坩埚,故A正确;
B.陶瓷的传统概念是指所有以黏土等无机非金属矿物为原材料,经过高温烧制而成的产
品,闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成,故B正确;
C.陶瓷由黏土经高温烧结而成,主要化学成分是硅酸盐,在新石器时代就已经开始使用,
应用较早,故C错误;
D.硅酸盐材料的化学性质不活泼,具有耐酸碱腐蚀,抗氧化等有点,故D正确。
例2、晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅
②粗硅与干燥HCl气体反应制得SiHCl :Si+3HCl=SiHCl +H
3 3 2
③SiHCl 与过量H 在1 100 ℃反应制得纯硅,已知SiHCl 能与HO强烈反应,在空气中易
3 2 3 2
自燃。
请回答下列问题:
(1)第①步制备粗硅的化学反应方程式为_____。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl (沸点33.0 ℃)中含有少量SiCl (沸点57.6
3 4
℃)和HCl(沸点-84.7 ℃),提纯SiHCl 采用的方法为_____。
3(3)用SiHCl 与过量H 反应制备纯硅的装置如图(热源及夹持装置略去):
3 2
①装置B中的试剂是_____,装置C中的烧瓶需要加热,其目的是______。
②反应一段时间后,装置D中观察到的现象是____,装置D中发生反应的化学方程式为
____。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以
及____。
④为鉴定产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需再加入的试
剂是____(填写字母代号)。
a.碘水 b.氯水 c.NaOH溶液 d.KSCN溶液 e.Na SO 溶液
2 3
【答案】(1)SiO+2C Si+2CO↑(2)蒸馏(3) ①浓硫酸;使滴入烧瓶中的SiHCl 气化②有
2 3
固体物质生成;SiHCl +H Si+3HCl③排尽装置中的空气④bd
3 2
【解析】本实验是利用SiHCl 和氢气反应制取纯硅,首先在装置A利用稀硫酸和锌粒反应
3
制取氢气,SiHCl 能与HO强烈反应、在空气中易自燃,所以需要装置B中盛放浓硫酸将
3 2
生成的氢气进行干燥、并用氢气排尽装置中的空气;水浴加热装置C,使SiHCl 挥发,和
3
氢气一同进入石英管中在高温条件下反应制取纯硅。
(1)高温下,SiO 和C反应生成Si和CO,反应的化学方程式为SiO+2C Si+2CO↑;
2 2
(2)沸点不同的液体混合物可以采用蒸馏的方法分离,这几种物质沸点不同,所以采用蒸馏
的方法分离;
(3)①为防止SiHCl 与HO强烈反应,需要干燥剂干燥氢气,浓硫酸具有吸水性且不和氢气
3 2
反应,所以装置B中可以盛放浓硫酸;加热装置C中烧瓶,升高温度能使SiHCl 气化,从
3
而使SiHCl 和氢气在D中反应;
3②D中发生反应SiHCl +H Si+3HCl,Si为固态,所以看到的现象是有固体物质生成;
3 2
③SiHCl 能与HO强烈反应、在空气中易自燃,且Si是亲氧元素,为防止SiHCl 自燃和
3 2 3
Si被氧化,需要排尽装置中的空气;
④若含铁单质,加入稀盐酸后溶液中应含Fe2+;检验Fe2+先加入KSCN溶液无明显现象,
再加入氯水溶液变红色即可,故选b、d。
例3、含硅元素的化合物广泛存在于自然界中,与其他矿物共同构成岩石.晶体硅(熔点
1410℃)用途广泛,制取与提纯方法有多种。
(1)炼钢开始和结束阶段都可能发生反应:Si+2FeO 2Fe+SiO ,其目的是________。
2
A.得到副产品硅酸盐水泥 B.制取SiO,提升钢的硬度
2
C.除去生铁中过多的Si杂质 D.除过量FeO,防止钢变脆
(2)一种由粗硅制纯硅过程如下:Si(粗) SiCl SiCl (纯) Si(纯),在上
4 4
述由SiCl 制纯硅的反应中,测得每生成 1.12kg纯硅需吸收a kJ热量,写出该反应的热化
4
学方程式:________________;对于钠的卤化物(NaX)和硅的卤化物(SiX)下列叙述正确的
4
是________________。
A.NaX易水解
B.SiX 是共价化合物
4
C.NaX的熔点一般高于SiX
4
D.SiF 晶体是由共价键形成的空间网状结构
4
(3)粗硅经系列反应可生成硅烷(SiH),硅烷分解也可以生成高纯硅.硅烷的热稳定性弱于
4
甲烷,所以Si元素的非金属性弱于C元素,用原子结构解释其原因:_______。
(4)此外,还可以将粗硅转化成三氯氢硅(SiHCl ),通过反应:SiHCl (g)+H(g) Si(s)
3 3 2
+3HCl(g)制得高纯硅.不同温度下,SiHCl 的平衡转化率随反应物的投料比(反⇌应初始时,
3
各反应物的物质的量之比)的变化关系如图所示.下列说法正确的是_______(填字母序号)。a.该反应的平衡常数随温度升高而增大
b.横坐标表示的投料比应该是
c.实际生产中为提高SiHCl 的利用率,可适当降低压强
3
(5)硅元素最高价氧化物对应的水化物是HSiO.室温下,0.1mol/L的硅酸钠溶液和
2 3
0.1mol/L的碳酸钠溶液,碱性更强的是___________,其原因是________________。已知:
HSiO:K =2.0×10﹣10、K =1.0×10﹣12,HCO:K =4.3×10﹣7K =5.6×10 ﹣11。
2 3 a1 a2 2 3 a1 a2
【答案】(1)CD(2)SiCl (g)+2H(g)=Si(s)+4HCl(g) H=+0.025akJ/mol;BC(3)C和Si最外层电
4 2
子数相同(或“是同主族元素”),C原子半径小于△ Si(或“C原子电子层数少于Si”) Si元素
的非金属性弱于C元素,硅烷的热稳定性弱于甲烷(4)ac(5)硅酸钠;硅酸的K 小于碳酸的
a2
K ,硅酸钠更易水解
a2
【解析】(1)炼钢的要求把生铁中的含碳量去除到规定范围,并使其它元素的含量减少或增
加到规定范围的过程,简单地说,是对生铁降碳、去硫磷、调硅锰含量的过程,这一过程
基本上是一个氧化过程,是用不同来源的氧(如空气中的氧、纯氧气、铁矿石中的氧)来氧
化铁水中的碳、硅、锰等元素.化学反应主要是2FeO+Si 2Fe+SiO 、FeO+Mn
2
Fe+MnO;在使碳等元素降到规定范围后,钢水中仍含有大量的氧,是有害的杂质,使钢
塑性变坏,轧制时易产生裂纹,故炼钢的最后阶段必须加入脱氧剂(例如锰铁、硅铁和铝
等),以除去钢液中多余的氧:Mn+FeO MnO+Fe,Si+2FeO SiO+2Fe,
22Al+3FeO Al O+3Fe,故答案选CD;
2 3
(2)由题意可知:每生成1.12kg纯硅需吸收akJ热量,即生成 =40mol纯硅吸收的
热量为akJ热量,则生成1mol纯硅吸收的热量为 kJ=0.025akJ,所以该反应
的热化学方程式:SiCl (g)+2H(g)=Si(s)+4HCl(g) H=+0.025akJ/mol;
4 2
A.钠的强酸盐不水解,NaX(NaF除外)不易水解△,故A错误;
B.硅的卤化物(SiX)是由非金属元素原子间通过共用电子对形成的化合物,是共价化合物,
4
故B正确;
C.钠的卤化物(NaX)为离子化合物属于离子晶体,硅的卤化物(SiX)为共价化合物属于分
4
子晶体,离子晶体的熔点大于分子晶体的熔点,即NaX的熔点一般高于SiX,故C正确;
4
D.SiF 晶体是由分子间作用力结合而成,故D错误;
4
故答案为BC;
(3)C和Si最外层电子数相同(或“是同主族元素”),C原子半径小于Si(或“C原子电子层
数少于Si”) Si元素的非金属性弱于C元素,硅烷的热稳定性弱于甲烷,故硅烷的分解温度
远低于甲烷;
(4)a.因为随着温度的升高,SiHCl 的转化率增大,平衡右移,则该反应的平衡常数随温度
3
升高而增大,故a正确;
b.增大一种反应物的浓度,能提高其它反应物的转化率,而本身的转化率反而降低,故横
坐标表示的投料比应该是 ,故b错误;
c.SiHCl (g)+H(g) Si(s)+3HCl(g)正向为气体系数增大的方向,降低压强平衡向气体系数
3 2
增大方向移动,可以⇌提高SiHCl 的利用率,故c正确;
3
故答案选a、c;
(5)依据所给数据可知:硅酸的K 小于碳酸的K ,依据“越弱越水解”可知硅酸钠更易水
a2 a2
解。1.(2022·广东·高考真题)广东一直是我国对外交流的重要窗口,馆藏文物是其历史见证。
下列文物主要由硅酸盐制成的是
文
物
选 D.铜镀金钟
A.南宋鎏金饰品 B.蒜头纹银盒 C.广彩瓷咖啡杯
项 座
2.(2022·河北·高考真题)定窑是宋代五大名窑之一,其生产的白瓷闻名于世。下列说法
正确的是
A.传统陶瓷是典型的绝缘材料 B.陶瓷主要成分为 和
C.陶瓷烧制的过程为物理变化 D.白瓷的白色是因铁含量较高
3.(2022·湖北·高考真题) 在高温高压下可转变为具有一定导电性、高硬度的非晶态
碳玻璃。下列关于该碳玻璃的说法错误的是
A.具有自范性 B.与 互为同素异形体
C.含有 杂化的碳原子 D.化学性质与金刚石有差异
4.(2022·广东·模拟预测)寿山石是中国传统四大印章石之一,含叶蜡石、高岭石等黏土
矿物。下列说法错误的是
A.寿山石的硬度与金刚石相当 B.叶蜡石、高岭石的主要成分属于硅酸盐
C.寿山石的红色条纹与Fe O 含量有关 D.寿山石印章要避免与强酸、强碱接触
2 3
5.(2022·广东茂名·一模)硅及其化合物在人类进步中发挥了重要作用。 和 用于制
造芯片, 用于制造光纤, 用作木材防火剂。下列说法正确的是A. 在自然界以游离态存在 B. 和 具有优良的导电性
C. 不与酸反应 D. 溶液可与 反应
6.(2022·江苏·高考真题)下列说法正确的是
A.金刚石与石墨烯中的 夹角都为
B. 、 都是由极性键构成的非极性分子
C.锗原子( )基态核外电子排布式为
D.ⅣA族元素单质的晶体类型相同
7.(2022·天津天津·二模)氮化硅(熔点1900℃)具有高强度、高韧性,通过SiH 与NH 发
4 3
生反应3SiH+4NH=Si N+12H 制得。下列说法错误的是
4 3 3 4 2
A.Si的电负性小于N的电负性 B.SiH 的稳定性强于NH 的稳定性
4 3
C.Si N 属于共价晶体 D.SiH 为非极性分子
3 4 4
8.(2022·河南焦作·一模)2020年12月17日,嫦娥五号带回了近2公斤的月壤样品。将
月壤进行20倍放大后能明显看到褐色的玻璃状物质。下列有关玻璃的说法中正确的是
A.普通玻璃的原料是烧碱、石英、石灰石
B.普通玻璃和石英玻璃都属于硅酸盐产品
C.制备普通玻璃时的反应有NaCO + SiO CO↑+ Na SiO
2 3 2 2 2 3
D.普通玻璃用于镶嵌建筑物的门窗、墙面,但其不具有保温和防辐射等特征
9.(2022·湖北·天门市教育科学研究院模拟预测)“液态阳光”由中国科学院液态阳光研
究组命名,指的是利用太阳能、风能等可再生能源分解水制氢,再将空气中的CO 加氢制
2
成CHOH等液体燃料。该过程零污染、零排放,并且可形成循环,是迄今为止人类制备
3
CHOH最清洁环保的方式之一,下列说法错误的是( )
3
A.即使使用高效催化剂,改变反应历程,CO 和HO合成CHOH和O 也为吸热反应
2 2 3 2
B.SiO 的熔点比CO 的高,原因是SiO 的分子间作用力更大
2 2 2
C.CO 是直线形分子
2
D.甲醇的沸点介于水和甲硫醇( CH SH)之间
3
10.(2022·河北衡水中学一模)无机非金属材料在生产生活中应用广泛。下列说法错误的
是A.玻璃纤维用于高强度复合材料,其主要成分为玻璃
B.陶瓷是一种常见硅酸盐材料,可以用陶瓷坩埚熔融纯碱
C.碳纳米材料是一类新型无机非金属材料,其中石墨烯具有导电性
D.碳化硅俗称金刚砂,可用作砂纸、砂轮的磨料
11.(2022·全国·模拟预测)“千淘万漉虽辛苦,吹尽狂沙始到金。”诗句中的“沙”的
主要成分是 ,下列说法错误的是
A. 属于酸性氧化物,不与任何酸反应
B.“水玻璃”可以由 与NaOH溶液反应制得
C. 是制取传统硅酸盐产品玻璃的原料之一
D.通常所说的“从沙滩到用户”,这句话涉及工业上制备粗硅的工艺
12.(2021·浙江·模拟预测)根据“玉兔二号”提供的一个暗绿色闪光的石块信息进行分
析,发现石块主要由约 的斜长石( )、 的辉石 ( 、 为单
核离子, )和 的橄榄石( , 为 、 )组成。下列关于上述“三石”
的说法正确的是
A.既是硅酸盐材料,又是金属材料
B.斜长石( )不稳定易水解
C.若辉石中 、 为 时, 可能是
D.橄榄石的氧化物形式一定为
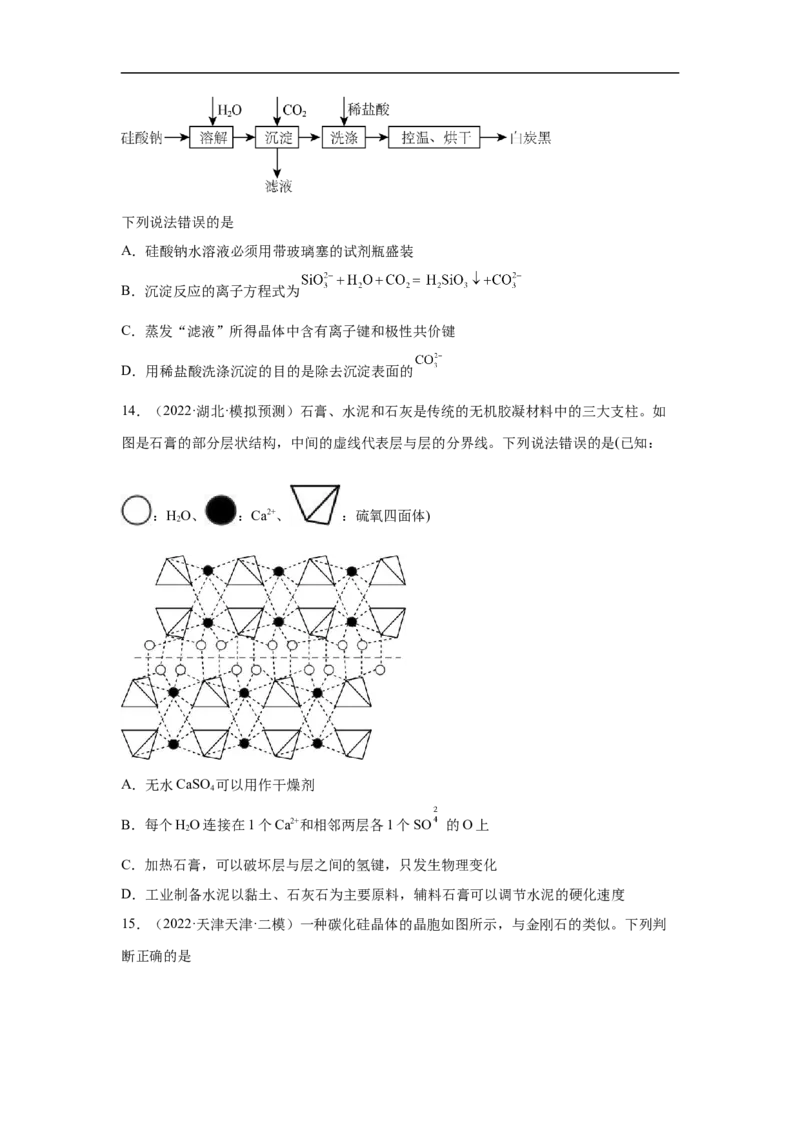
13.(2022·山东潍坊·三模)白炭黑(可用 表示其组成)可广泛应用于日用化工、
橡胶制品、电子工业等许多领域。以硅酸钠和二氧化碳为原料制备白炭黑的工艺流程如下:下列说法错误的是
A.硅酸钠水溶液必须用带玻璃塞的试剂瓶盛装
B.沉淀反应的离子方程式为
C.蒸发“滤液”所得晶体中含有离子键和极性共价键
D.用稀盐酸洗涤沉淀的目的是除去沉淀表面的
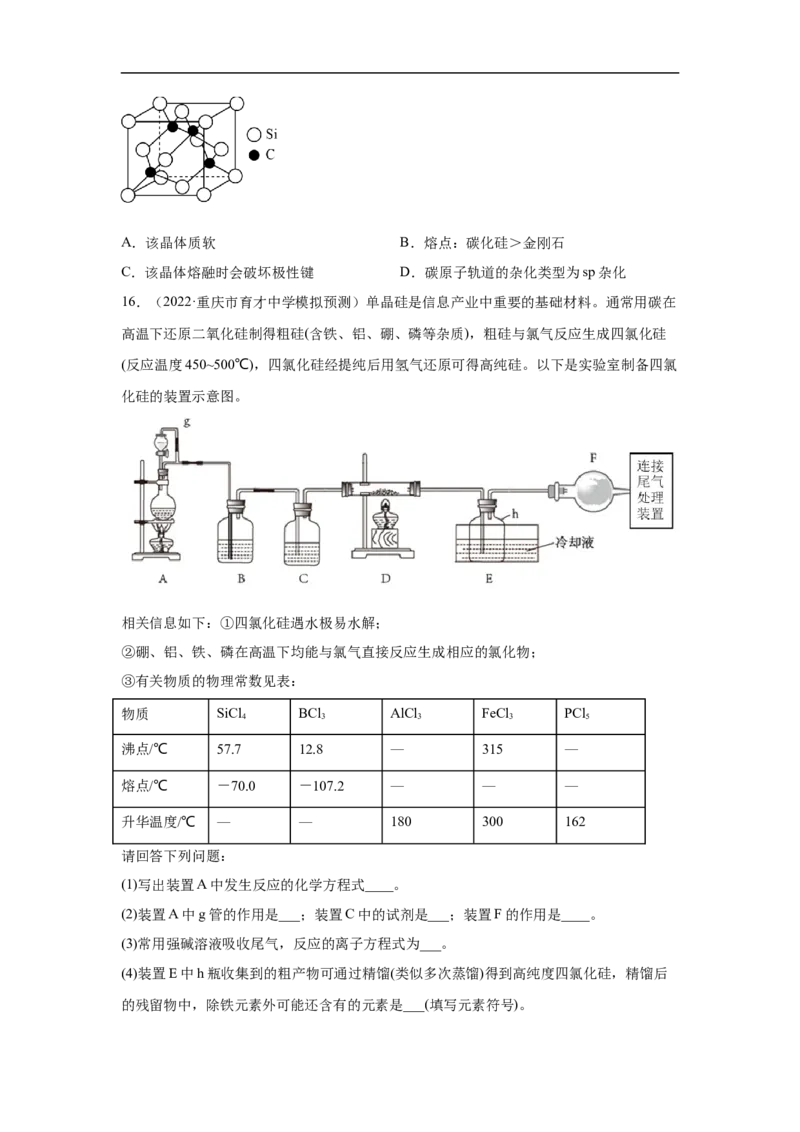
14.(2022·湖北·模拟预测)石膏、水泥和石灰是传统的无机胶凝材料中的三大支柱。如
图是石膏的部分层状结构,中间的虚线代表层与层的分界线。下列说法错误的是(已知:
:HO、 :Ca2+、 :硫氧四面体)
2
A.无水CaSO 可以用作干燥剂
4
B.每个HO连接在1个Ca2+和相邻两层各1个SO 的O上
2
C.加热石膏,可以破坏层与层之间的氢键,只发生物理变化
D.工业制备水泥以黏土、石灰石为主要原料,辅料石膏可以调节水泥的硬化速度
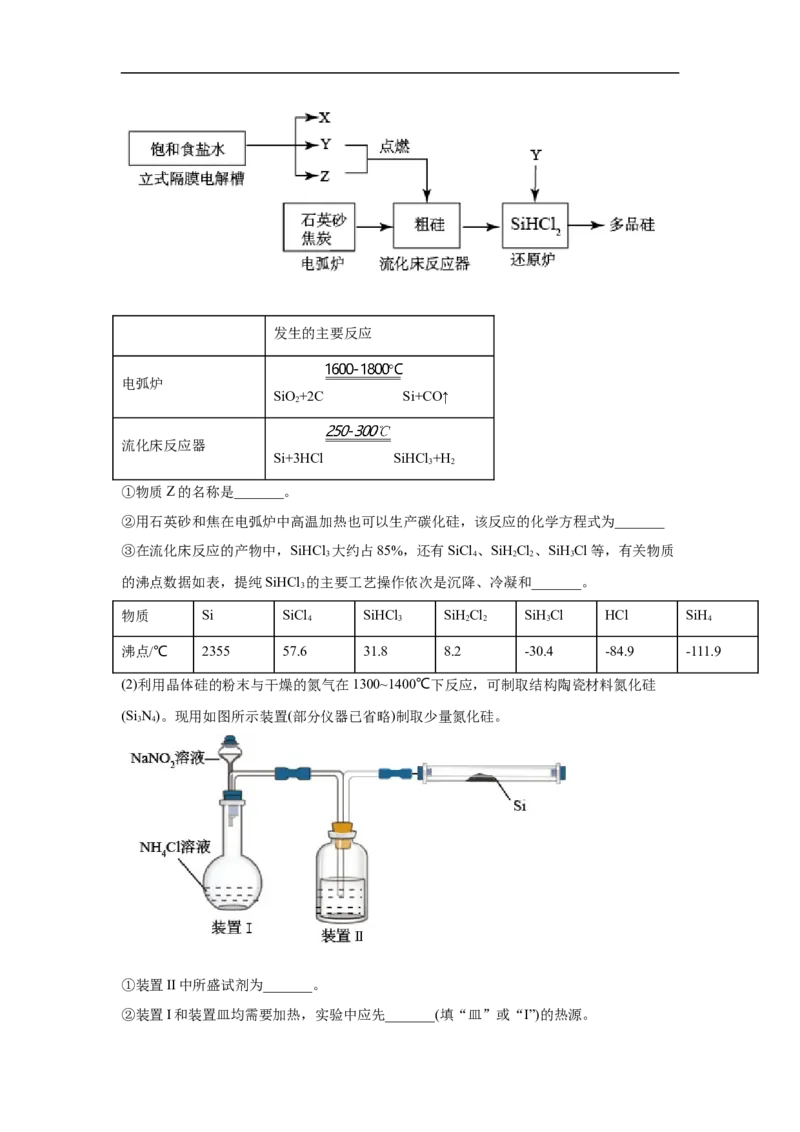
15.(2022·天津天津·二模)一种碳化硅晶体的晶胞如图所示,与金刚石的类似。下列判
断正确的是A.该晶体质软 B.熔点:碳化硅>金刚石
C.该晶体熔融时会破坏极性键 D.碳原子轨道的杂化类型为sp杂化
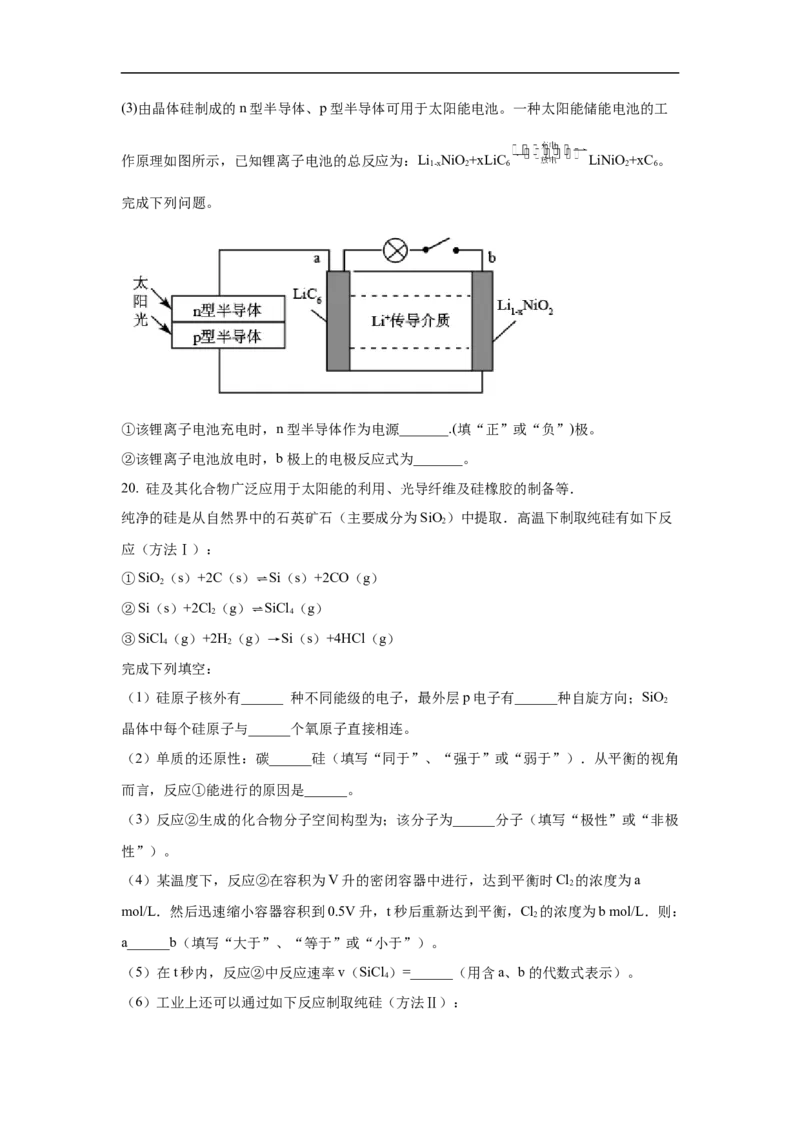
16.(2022·重庆市育才中学模拟预测)单晶硅是信息产业中重要的基础材料。通常用碳在
高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅
(反应温度450~500℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯
化硅的装置示意图。
相关信息如下:①四氯化硅遇水极易水解;
②硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
③有关物质的物理常数见表:
物质 SiCl BCl AlCl FeCl PCl
4 3 3 3 5
沸点/℃ 57.7 12.8 — 315 —
熔点/℃ -70.0 -107.2 — — —
升华温度/℃ — — 180 300 162
请回答下列问题:
(1)写出装置A中发生反应的化学方程式____。
(2)装置A中g管的作用是___;装置C中的试剂是___;装置F的作用是____。
(3)常用强碱溶液吸收尾气,反应的离子方程式为___。
(4)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后
的残留物中,除铁元素外可能还含有的元素是___(填写元素符号)。(5)为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用
KMnO 标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是___。
4
17.作为推行“低碳经济”的重要科技进步,太阳能光伏发电成为重要的新型能源。太阳
能光伏发电最关键的材料是高纯硅,三氯甲硅烷( )还原法是当前制备高纯硅( )的主
要方法,生产流程示意如下:
(1)石英砂的主要成分是 ,其能与 反应生成硅酸钠和水,则 是_______(酸性
氧化物或碱性氧化物),写出该反应化学方程式_______。
(2)“精馏”也是蒸馏的一种形式,通过蒸馏可把液体混合物分离开,原理是利用混合物各
成分的_______(填“熔点”或“沸点”)不同。
(3)制取粗 的反应为: (未配平),该条件下, 气体和足
量硅充分反应生成 气体和 ,则 化学式为_______。
(4)整个制备过程必须达到无水无氧,在 还原 过程中若混入 ,除了生成 外,
还可能引起的后果是_______。
(5)为达到绿色化学和资源综合利用的目的,在生产过程中物质A需要循环使用,A的化学
式是_______。
18.(2022·湖北·模拟预测)多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电池
及高纯硅制品的主要原料。
(1)已知多晶硅第三代工业制取流程如图所示。发生的主要反应
电弧炉
SiO+2C Si+CO↑
2
流化床反应器
Si+3HCl SiHCl +H
3 2
①物质Z的名称是_______。
②用石英砂和焦在电弧炉中高温加热也可以生产碳化硅,该反应的化学方程式为_______
③在流化床反应的产物中,SiHCl 大约占85%,还有SiCl 、SiHCl、SiHCl等,有关物质
3 4 2 2 3
的沸点数据如表,提纯SiHCl 的主要工艺操作依次是沉降、冷凝和_______。
3
物质 Si SiCl SiHCl SiHCl SiHCl HCl SiH
4 3 2 2 3 4
沸点/℃ 2355 57.6 31.8 8.2 -30.4 -84.9 -111.9
(2)利用晶体硅的粉末与干燥的氮气在1300~1400℃下反应,可制取结构陶瓷材料氮化硅
(Si N)。现用如图所示装置(部分仪器已省略)制取少量氮化硅。
3 4
①装置II中所盛试剂为_______。
②装置I和装置皿均需要加热,实验中应先_______(填“皿”或“I”)的热源。(3)由晶体硅制成的n型半导体、p型半导体可用于太阳能电池。一种太阳能储能电池的工
作原理如图所示,已知锂离子电池的总反应为:Li NiO+xLiC LiNiO +xC 。
1-x 2 6 2 6
完成下列问题。
①该锂离子电池充电时,n型半导体作为电源_______.(填“正”或“负”)极。
②该锂离子电池放电时,b极上的电极反应式为_______。
20. 硅及其化合物广泛应用于太阳能的利用、光导纤维及硅橡胶的制备等.
纯净的硅是从自然界中的石英矿石(主要成分为SiO)中提取.高温下制取纯硅有如下反
2
应(方法Ⅰ):
①SiO
2
(s)+2C(s)⇌Si(s)+2CO(g)
②Si(s)+2Cl
2
(g)⇌SiCl
4
(g)
③SiCl (g)+2H (g)→Si(s)+4HCl(g)
4 2
完成下列填空:
(1)硅原子核外有______ 种不同能级的电子,最外层p电子有______种自旋方向;SiO
2
晶体中每个硅原子与______个氧原子直接相连。
(2)单质的还原性:碳______硅(填写“同于”、“强于”或“弱于”).从平衡的视角
而言,反应①能进行的原因是______。
(3)反应②生成的化合物分子空间构型为;该分子为______分子(填写“极性”或“非极
性”)。
(4)某温度下,反应②在容积为V升的密闭容器中进行,达到平衡时Cl 的浓度为a
2
mol/L.然后迅速缩小容器容积到0.5V升,t秒后重新达到平衡,Cl 的浓度为b mol/L.则:
2
a______b(填写“大于”、“等于”或“小于”)。
(5)在t秒内,反应②中反应速率v(SiCl )=______(用含a、b的代数式表示)。
4
(6)工业上还可以通过如下反应制取纯硅(方法Ⅱ):④Si(粗)+3HCl(g) SiHCl (l)+H (g)+Q(Q>0)
3 2
⑤SiHCl (g)+H (g) Si(纯)+3HCl(g)
3 2
提高反应⑤中Si(纯)的产率,可采取的措施有:______、______。