文档内容
素养说明:阿伏加德罗常数的正误判断一直保持着较高的稳定性与连续性。在命
题思路上主要以阿伏加德罗常数为载体,结合气体摩尔体积、物质的组成或原子
结构、氧化还原反应及电离、水解等基本概念和基本理论,考查常用化学计量的
相关计算。充分体现了能从不同视角对纷繁复杂的化学变化进行分类研究,逐步
揭示各类变化的特征和规律,从而逐步提高化学核心素养。
1.真题研究
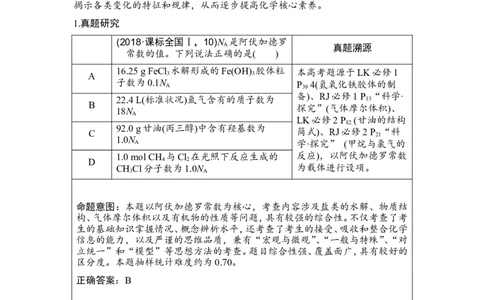
(2018·课标全国Ⅰ,10)N 是阿伏加德罗
A 真题溯源
常数的值。下列说法正确的是( )
A
16.25 g FeCl
3
水解形成的Fe(OH)
3
胶体粒 本高考题源于LK必修1
子数为0.1N A P 39 4(氢氧化铁胶体的制
备)、RJ必修1 P “科学·
22.4 L(标准状况)氩气含有的质子数为 13
B
探究”(气体摩尔体积)、
18N
A
LK必修2 P (甘油的结构
82
92.0 g甘油(丙三醇)中含有羟基数为
C 简式)、RJ必修2 P “科
21
1.0N
A 学·探究” (甲烷与氯气的
1.0 mol CH 与Cl 在光照下反应生成的 反应),以阿伏加德罗常数
D 4 2
CH Cl分子数为1.0N 为载体进行设项。
3 A
命题意图:本题以阿伏加德罗常数为核心,考查内容涉及盐类的水解、物质结
构、气体摩尔体积以及有机物的性质等问题,具有较强的综合性。不仅考查了考
生的基础知识掌握情况、概念辨析水平,还考查了考生的接受、吸收和整合化学
信息的能力,以及严谨的思维品质,兼有“宏观与微观”、“一般与特殊”、“对
立统一”和“模型”等思想方法的考查。题目综合性强、覆盖面广,具有较好的
区分度。本题抽样统计难度约为0.70。
正确答案:B
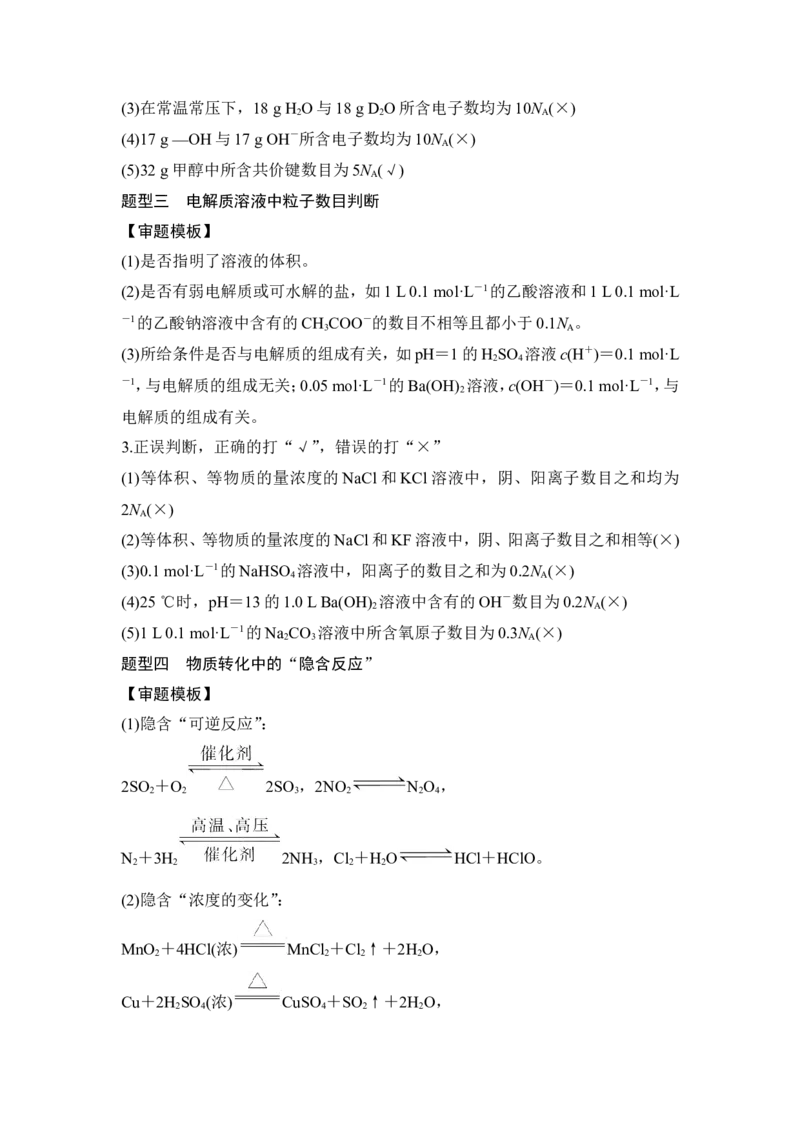
2.解题关键:“阿伏加德罗常数”所涉微粒数目转换[题型专练]
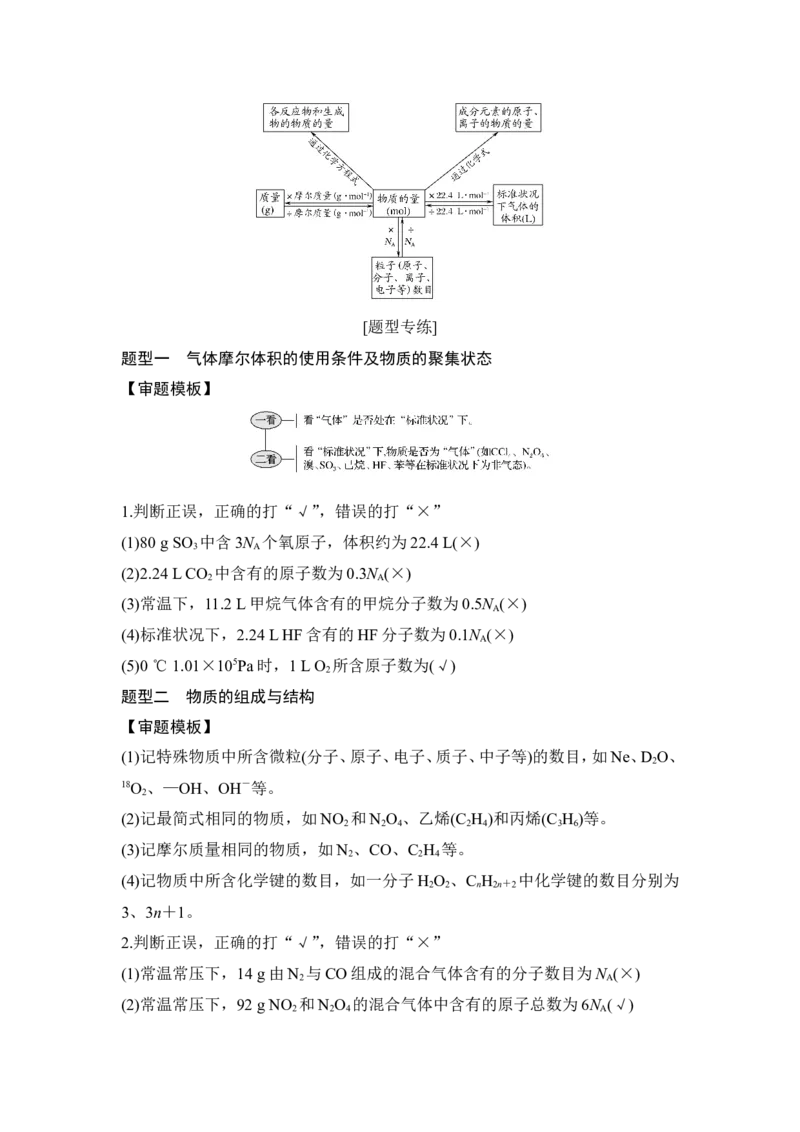
题型一 气体摩尔体积的使用条件及物质的聚集状态
【审题模板】
1.判断正误,正确的打“√”,错误的打“×”
(1)80 g SO 中含3N 个氧原子,体积约为22.4 L(×)
3 A
(2)2.24 L CO 中含有的原子数为0.3N (×)
2 A
(3)常温下,11.2 L甲烷气体含有的甲烷分子数为0.5N (×)
A
(4)标准状况下,2.24 L HF含有的HF分子数为0.1N (×)
A
(5)0 ℃ 1.01×105Pa时,1 L O 所含原子数为(√)
2
题型二 物质的组成与结构
【审题模板】
(1)记特殊物质中所含微粒(分子、原子、电子、质子、中子等)的数目,如Ne、D O、
2
18O 、—OH、OH-等。
2
(2)记最简式相同的物质,如NO 和N O 、乙烯(C H )和丙烯(C H )等。
2 2 4 2 4 3 6
(3)记摩尔质量相同的物质,如N 、CO、C H 等。
2 2 4
(4)记物质中所含化学键的数目,如一分子H O 、C H 中化学键的数目分别为
2 2 n 2n+2
3、3n+1。
2.判断正误,正确的打“√”,错误的打“×”
(1)常温常压下,14 g由N 与CO组成的混合气体含有的分子数目为N (×)
2 A
(2)常温常压下,92 g NO 和N O 的混合气体中含有的原子总数为6N (√)
2 2 4 A(3)在常温常压下,18 g H O与18 g D O所含电子数均为10N (×)
2 2 A
(4)17 g —OH与17 g OH-所含电子数均为10N (×)
A
(5)32 g甲醇中所含共价键数目为5N (√)
A
题型三 电解质溶液中粒子数目判断
【审题模板】
(1)是否指明了溶液的体积。
(2)是否有弱电解质或可水解的盐,如1 L 0.1 mol·L-1的乙酸溶液和1 L 0.1 mol·L
-1的乙酸钠溶液中含有的CH COO-的数目不相等且都小于0.1N 。
3 A
(3)所给条件是否与电解质的组成有关,如pH=1的H SO 溶液c(H+)=0.1 mol·L
2 4
-1,与电解质的组成无关;0.05 mol·L-1的Ba(OH) 溶液,c(OH-)=0.1 mol·L-1,与
2
电解质的组成有关。
3.正误判断,正确的打“√”,错误的打“×”
(1)等体积、等物质的量浓度的NaCl和KCl溶液中,阴、阳离子数目之和均为
2N (×)
A
(2)等体积、等物质的量浓度的NaCl和KF溶液中,阴、阳离子数目之和相等(×)
(3)0.1 mol·L-1的NaHSO 溶液中,阳离子的数目之和为0.2N (×)
4 A
(4)25 ℃时,pH=13的1.0 L Ba(OH) 溶液中含有的OH-数目为0.2N (×)
2 A
(5)1 L 0.1 mol·L-1的Na CO 溶液中所含氧原子数目为0.3N (×)
2 3 A
题型四 物质转化中的“隐含反应”
【审题模板】
(1)隐含“可逆反应”:
2SO +O 2SO ,2NO N O ,
2 2 3 2 2 4
N +3H 2NH ,Cl +H O HCl+HClO。
2 2 3 2 2
(2)隐含“浓度的变化”:
MnO +4HCl(浓) MnCl +Cl ↑+2H O,
2 2 2 2
Cu+2H SO (浓) CuSO +SO ↑+2H O,
2 4 4 2 2Cu+4HNO (浓)===Cu(NO ) +2NO ↑+2H O。
3 3 2 2 2
(3)隐含“钝化”
常温下,铁、铝遇浓硫酸、浓硝酸发生“钝化”。
4.判断正误,正确的划“√”,错误的划“×”
(1)密闭容器中2 mol NO与1 mol O 充分反应,产物的分子数为2N (×)
2 A
(2)1 mol SO 和4 mol O 在一定条件下,充分反应后,转移电子数为2N (×)
2 2 A
(3)100 g 17%的氨水,溶液中含有的NH 分子数为N (×)
3 A
(4)向2 L 2 mol·L-1的盐酸中,加入足量MnO ,充分反应后,生成的Cl 在标准状
2 2
况下为22.4 L(×)
(5)将0.1 mol Cl 通入足量水中,充分反应后,转移电子的个数为0.1N (×)
2 A
题型五 氧化还原反应中电子转移的数目
【审题模板】
(1)明确三步确定电子转移数目
(2)熟记常考氧化还原反应转移的电子数
反应 物质 转移电子的物质的量或电子数目
1 mol Na O 1 mol或N
2 2 A
Na O +CO (或H O)
2 2 2 2
1 mol O 2 mol或2N
2 A
Cl +NaOH 1 mol Cl 1 mol或N
2 2 A
1 mol Cl 2 mol或2N
2 A
Cl +Fe
2
1 mol Fe 3 mol或3N
A
5.正误判断,正确的打“√”,错误的打“×”。
(1)5.6 g铁粉与硝酸反应失去的电子数一定为0.3N (×)
A(2)1 mol Na 与足量 O 反应,生成 Na O 和 Na O 的混合物,转移的电子数为
2 2 2 2
N (√)
A
(3)1 mol Na O 与足量CO 充分反应转移的电子数为2N (×)
2 2 2 A
(4)向FeI 溶液中通入适量Cl ,当有1 mol Fe2+被氧化时,共转移的电子的数目为
2 2
N (×)
A
(5)1 mol Cl 参加反应转移电子数一定为2N (×)
2 A