文档内容
素养说明:化学核心素养要求考生能依据新发现、新信息,分析、评价已有的认识
模型,能指出存在问题,提出改进、优化模型的意见。通过对图像、表格类试题信
息的规范审读,进一步提高学生获取信息的能力。
[获取信息类型]
类型一:从表格信息总结规律
类型二:从图中信息总结规律
类型三:从题中信息总结规律并作图
类型四:从题中信息总结规律并分析原因
分析方法:
1.提取什么?
审清题,明确目标,并做好标注。
2.怎么提取?
分析变化趋势和斜率变化。
3.答题模板:其他条件不变,随着自变量(横坐标)变化(增大或减少),XX因变量
(纵坐标)逐渐(增大/减少)。或者就横坐标、自变量分区作答(非单调曲线)。
写规律时的原则:先整体后局部。
分析原因型分析方法:
答题模板:什么因素的改变使什么平衡向什么方向移动,结果是什么。
作图策略:
分析图表信息,确定横纵坐标,做好“三点一变化”:起点、终点、转折点和变化趋
势。
【例】 用CaSO 代替O 与燃料CO反应,既可提高燃烧效率,又能得到高纯
4 2
CO ,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副
2
反应。
① 1/4CaSO (s)+CO(g) 1/4CaS(s)+CO (g)
4 2ΔH =-47.3 kJ·mol-1
1
② CaSO (s)+CO(g) CaO(s)+CO (g) +SO (g)
4 2 2
ΔH =+210.5 kJ·mol-1
2
③ CO(g) 1/2C(s)+1/2CO (g)
2
ΔH =-86.2 kJ·mol-1
3
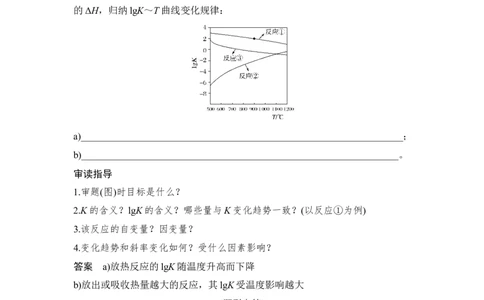
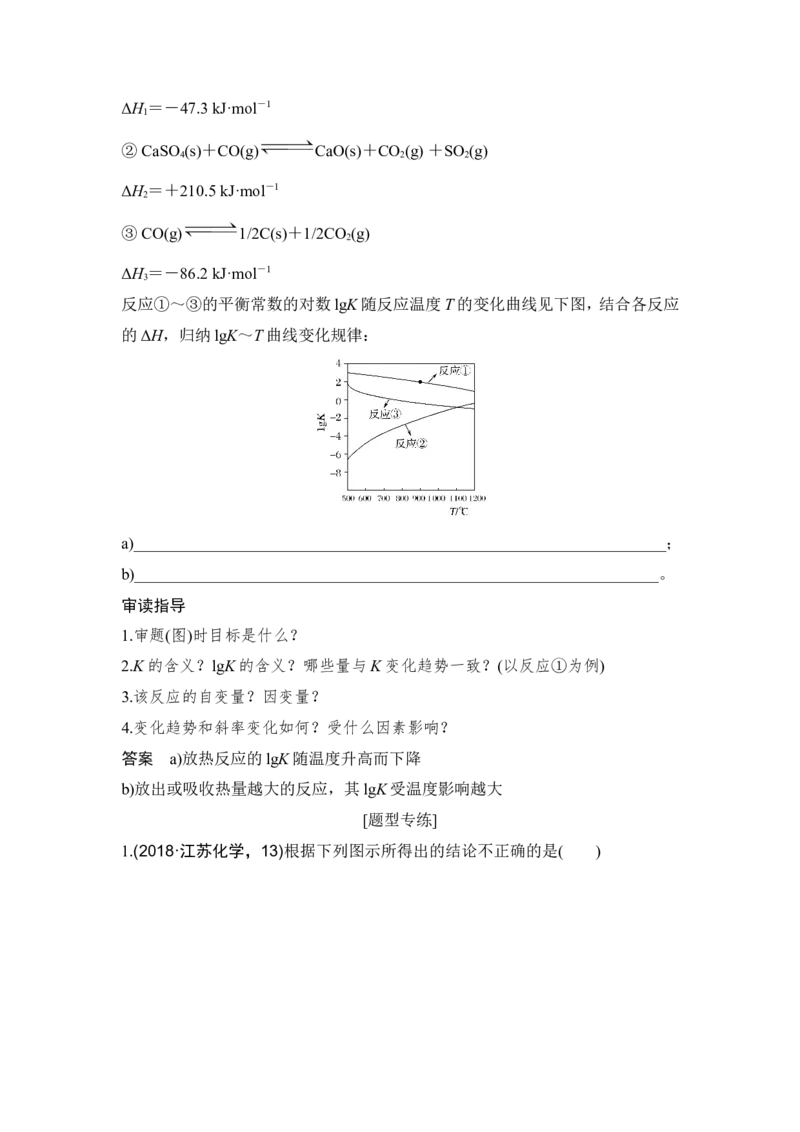
反应①~③的平衡常数的对数lgK随反应温度T的变化曲线见下图,结合各反应
的ΔH,归纳lgK~T曲线变化规律:
a)__________________________________________________________________;
b)_________________________________________________________________。
审读指导
1.审题(图)时目标是什么?
2.K的含义?lgK的含义?哪些量与K变化趋势一致?(以反应①为例)
3.该反应的自变量?因变量?
4.变化趋势和斜率变化如何?受什么因素影响?
答案 a)放热反应的lgK随温度升高而下降
b)放出或吸收热量越大的反应,其lgK受温度影响越大
[题型专练]
1.(2018·江苏化学,13)根据下列图示所得出的结论不正确的是( )A.图甲是CO(g)+H O(g)===CO (g)+H (g)的平衡常数与反应温度的关系曲线,
2 2 2
说明该反应的ΔH<0
B.图乙是室温下H O 催化分解放出氧气的反应中c(H O )随反应时间变化的曲线,
2 2 2 2
说明随着反应的进行H O 分解速率逐渐减小
2 2
C.图丙是室温下用0.100 0 mol·L-1NaOH溶液滴定20.00 mL 0.100 0 mol·L-1某一
元酸HX的滴定曲线,说明HX是一元强酸
D.图丁是室温下用Na SO 除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+)
2 4
与c(SO)的关系曲线,说明溶液中c(SO)越大c(Ba2+)越小
解析 图甲中,温度升高,lg K减小,即K减小,说明升高温度平衡逆向移动,则
该反应为放热反应,A项正确;图乙中,曲线的斜率的绝对值逐渐减小,说明随着
反应进行,H O 分解速率逐渐减小,B项正确;图丙中,没有滴入NaOH溶液时,
2 2
0.100 0 mol·L-1HX溶液的pH大于1,则HX为一元弱酸,C项错误;图丁中,曲
线上的点均为沉淀溶解平衡的点,c(SO)与c(Ba2+)成反比,D项正确。
答案 C
2.近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过
程如下:
(1)反应Ⅰ:2H SO (l)===2SO (g)+2H O(g)+O (g)
2 4 2 2 2ΔH=+551 kJ·mol-1
反应Ⅲ:S(s)+O (g)===SO (g) ΔH=-297 kJ·mol-1
2 2
反应Ⅱ的热化学方程式:____________________________________________
_____________________________________________________________________
。
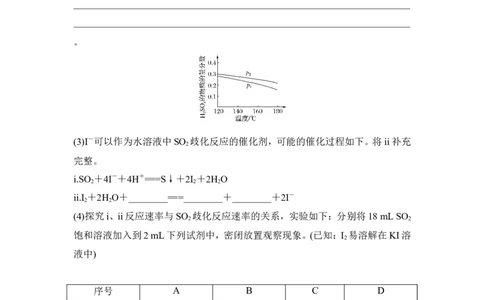
(2)对反应Ⅱ,在某一投料比时,两种压强下,H SO 在平衡体系中物质的量分数随
2 4
温度的变化关系如图所示。p ________p (填“>”或“<”),得出该结论的理由是
2 1
_____________________________________________________________________
_____________________________________________________________________
。
(3)I-可以作为水溶液中SO 歧化反应的催化剂,可能的催化过程如下。将ii补充
2
完整。
i.SO +4I-+4H+===S↓+2I +2H O
2 2 2
ii.I +2H O+________===________+________+2I-
2 2
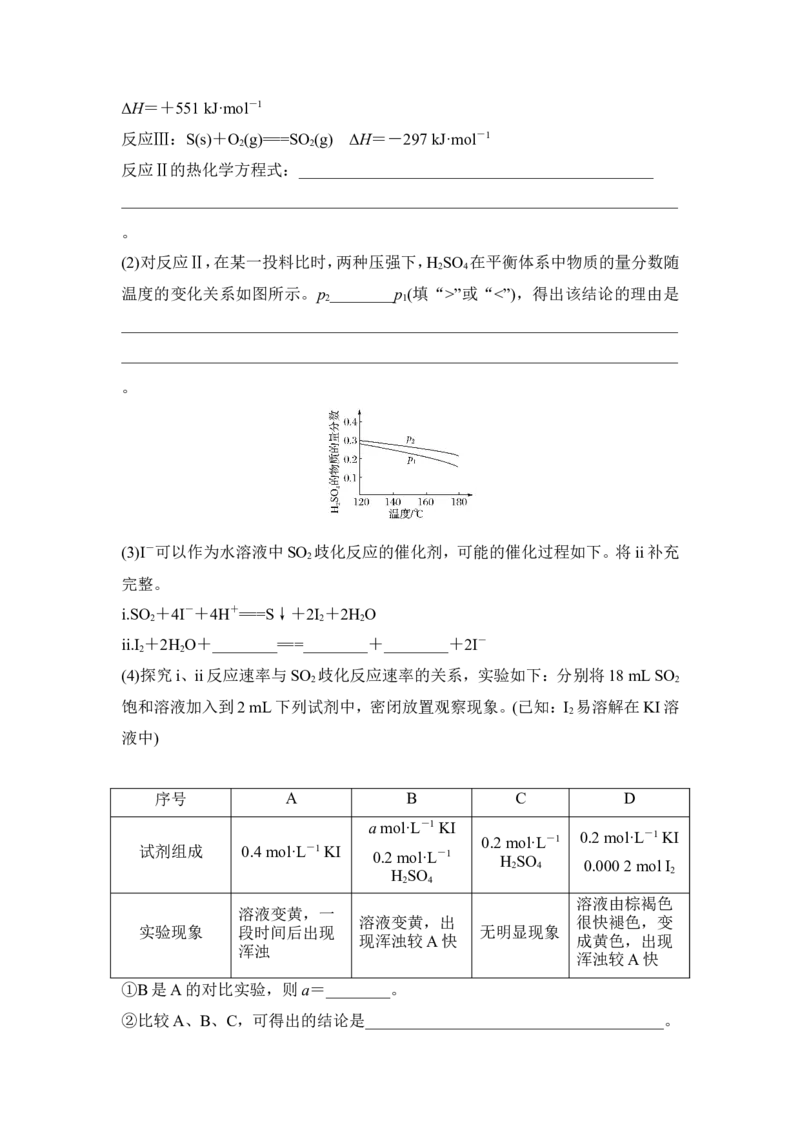
(4)探究i、ii反应速率与SO 歧化反应速率的关系,实验如下:分别将18 mL SO
2 2
饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I 易溶解在KI溶
2
液中)
序号 A B C D
a mol·L-1 KI
0.2 mol·L-1 0.2 mol·L-1 KI
试剂组成 0.4 mol·L-1 KI 0.2 mol·L-1 H SO
2 4 0.000 2 mol I
H SO 2
2 4
溶液由棕褐色
溶液变黄,一
溶液变黄,出 很快褪色,变
实验现象 段时间后出现 无明显现象
现浑浊较A快 成黄色,出现
浑浊
浑浊较A快
①B是A的对比实验,则a=________。
②比较A、B、C,可得出的结论是_____________________________________。③实验表明,SO 的歧化反应速率 D>A。结合 i、ii 反应速率解释原因:
2
____________________________________________________________________。
解析 (1)由于反应Ⅱ是二氧化硫的歧化反应,且由题意可知其氧化产物和还原
产物分别为H SO 和S,根据得失电子守恒和元素守恒可写出反应Ⅱ的化学方程
2 4
式为:3SO (g)+2H O(g)===2H SO (l)+S(s)。根据盖斯定律,反应Ⅰ与反应Ⅲ的
2 2 2 4
热化学方程式相加得:2H SO (l)+S(s)===3SO (g)+2H O(g) ΔH=+254 kJ·mol
2 4 2 2
-1,所以反应Ⅱ的热化学方程式为:3SO (g)+2H O(g)===2H SO (l)+S(s) ΔH =
2 2 2 4 2
-254 kJ·mol-1。(3)由题意知二氧化硫的歧化反应可由i与ii相加所得,所以反应
Ⅱ的离子方程式 3SO +2H O===4H++2SO+S↓,减去 i式得:2I +4H O+
2 2 2 2
2SO ===2SO+8H++4I-,化简得到:I +2H O+SO ===SO+4H++2I-。(4)①由
2 2 2 2
于B是A的对比实验,所以两组实验中KI的浓度必须相同,即a=0.4。②A说明
I-能催化二氧化硫发生歧化反应。C中无明显现象,说明H+单独存在时不具有催
化作用,不能使二氧化硫歧化反应速率加快。B中溶液变黄,出现浑浊较A快,结
合C可知,增强溶液的酸性,可增强I-的催化效果。③由于I-催化二氧化硫的歧
化反应是i与ii两个过程分步进行,所以两个反应中任何一个反应的速率都会影
响总反应的速率。D中直接加入I ,故反应ii可立即发生,而由反应ii产生的H+
2
可使反应i速率加快,所以D的反应速率比A快。
答案 (1)3SO (g)+2H O(g)===2H SO (l)+S(s) ΔH =-254 kJ·mol-1
2 2 2 4 2
(2)> 反应Ⅱ是气体物质的量减小的反应,温度一定时,增大压强使反应正向移
动,H SO 的物质的量增大,体系总物质的量减小,H SO 的物质的量分数增大
2 4 2 4
(3)SO SO 4H+
2
(4)①0.4
②I-是SO 歧化反应的催化剂,H+单独存在时不具有催化作用,但H+可以加快
2
歧化反应速率
③反应ii比i快;D中由反应ii产生的H+使反应i加快