文档内容
素养说明:通过强酸(碱)与弱酸(碱)的性质比较总结,体现了考生对强弱电解质概
念的理解,以及考生理论与实际的联系能力。
1.强、弱电解质的实验设计
实验设计思路:以证明室温下某酸(HA)是弱酸为例
实验方法 结论
pH=2,HA为强酸
①测0.01 mol·L-1 HA溶液的pH
pH>2,HA为弱酸
pH=7,HA为强酸
②测NaA溶液的pH
pH>7,HA为弱酸
③相同条件下,测相同浓度的HA和 若HA溶液的导电能力比HCl(强酸)溶
HCl(强酸)溶液的导电能力 液的弱,则HA为弱酸
④测相同pH的HA溶液与盐酸稀释相 若HA溶液的pH变化较小,则HA为弱
同倍数前后的pH变化 酸
⑤测等体积、等pH的HA溶液、盐酸分
若HA溶液反应过程中产生H 较快且
别与足量锌反应产生H 的快慢及H 的 2
2 2 最终产生H 的量较多,则HA为弱酸
量 2
⑥测等体积、等pH的HA溶液和盐酸中
若HA溶液耗碱量大,则HA为弱酸
和等浓度碱所需消耗的碱的量
2.两方面突破一元强酸与一元弱酸比较
(1)相同物质的量浓度、相同体积的一元强酸与一元弱酸的比较
比较 与足量Zn 开始与金
中和碱
项目 c(H+) pH 反应产生 属反应的
的能力
酸 H 的量 速率
2
一元强酸 大 小 大
相同 相同
一元弱酸 小 大 小
(2)相同pH、相同体积的一元强酸与一元弱酸的比较
比较 与足量Zn 开始与金
中和碱
项目 c(H+) c(酸) 反应产生 属反应的
的能力
酸 H 的量 速率
2
一元强酸 相同 小 小 少 相同一元弱酸 大 大 多
说明:一元强碱与一元弱碱的比较规律与以上类似。
3.图像法理解一强一弱的稀释规律
(1)相同体积、相同浓度的盐酸、醋酸
加水稀释到相同的倍数,醋酸的pH 加水稀释到相同的pH,盐酸加入的水
大 多
(2)相同体积、相同pH的盐酸、醋酸
加水稀释相同的倍数,盐酸的pH 加水稀释到相同的pH,醋酸加入的水
大 多
[题型专练]
1.(2017·浙江卷)室温下,下列事实不能说明NH ·H O为弱电解质的是( )
3 2
A.0.1 mol·L-1 NH ·H O的pH小于13
3 2
B.0.1 mol·L-1 NH Cl溶液的pH小于7
4
C.相同条件下,浓度均为0.1 mol·L-1 NaOH溶液和氨水,氨水的导电能力弱
D.0.1 mol·L-1 NH ·H O能使无色酚酞试液变红色
3 2
解析 0.1 mol·L-1的NH ·H O中c(OH-)小于0.1 mol·L-1 ,说明部分电离,A项
3 2
正确;0.1 mol·L-1的NH Cl溶液呈酸性,说明NH 水解,B项正确;同浓度时,氨
4
水的导电能力弱于一元强碱,说明部分电离,C项正确;D项,只能说明NH ·H O
3 2
显碱性,不能说明其是弱碱,错误。
答案 D
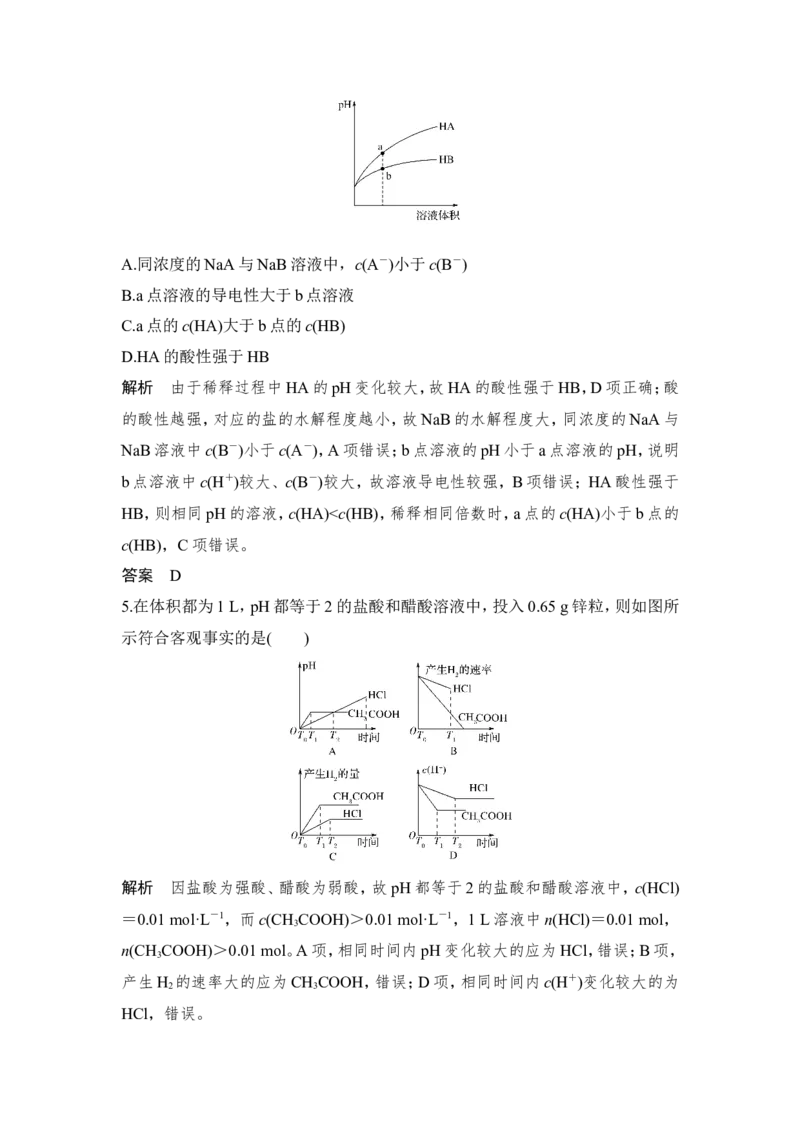
2.(2016·上海卷)能证明乙酸是弱酸的实验事实是( )A.CH COOH溶液与Zn反应放出H
3 2
B.0.1 mol/L CH COONa溶液的pH大于7
3
C.CH COOH溶液与Na CO 反应生成CO
3 2 3 2
D.0.1 mol/L CH COOH溶液可使紫色石蕊变红
3
解析 A.只能证明乙酸具有酸性,不能证明其酸性强弱,错误;B.该盐溶液显碱
性,由于NaOH是强碱,故可以证明乙酸是弱酸,正确;C.可以证明乙酸的酸性比
碳酸强,但是不能证明其酸性强弱,错误;D.可以证明乙酸具有酸性,但是不能证
明其酸性强弱,错误。
答案 B
3.(2015·海南高考)下列曲线中,可以描述乙酸(甲,K =1.8×10-5)和一氯乙酸(乙,
a
K =1.4×10-3)在水中的电离度与浓度关系的是( )
a
解析 这两种物质都是弱电解质,在温度不变、浓度相等时,电离程度CH COOH
3
<CH ClCOOH,排除A、C;当浓度增大时,物质的电离程度减小,排除D选项,
2
正确选项是B。
答案 B
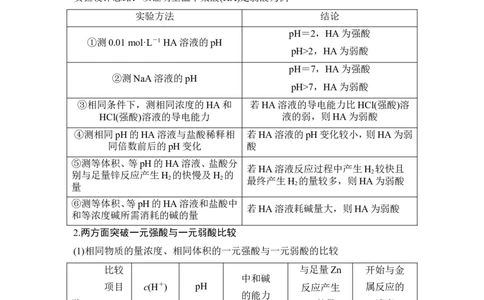
4.25 ℃时,相同pH的两种一元弱酸HA与HB溶液分别加水稀释,溶液pH随溶
液体积变化的曲线如图所示。下列说法正确的是( )A.同浓度的NaA与NaB溶液中,c(A-)小于c(B-)
B.a点溶液的导电性大于b点溶液
C.a点的c(HA)大于b点的c(HB)
D.HA的酸性强于HB
解析 由于稀释过程中HA的pH变化较大,故HA的酸性强于HB,D项正确;酸
的酸性越强,对应的盐的水解程度越小,故NaB的水解程度大,同浓度的NaA与
NaB溶液中c(B-)小于c(A-),A项错误;b点溶液的pH小于a点溶液的pH,说明
b点溶液中c(H+)较大、c(B-)较大,故溶液导电性较强,B项错误;HA酸性强于
HB,则相同pH的溶液,c(HA)