文档内容
素养说明:酸碱中和滴定曲线是近几年热点题型,通过分析建模,让考生形成解
题程序,也体现大纲对考生对图形的识别与分析的能力要求。
1.酸碱中和滴定曲线图示
氢氧化钠滴定等浓度等体积的盐酸、醋 盐酸滴定等浓度等体积的氢氧化钠、氨
酸的滴定曲线 水的滴定曲线
曲线起点不同:强碱滴定强酸、弱酸的曲线,强酸起点低;强酸滴定强碱、弱碱的曲
线,强碱起点高
突跃点变化范围不同:强碱与强酸反应(强酸与强碱反应)的突跃点变化范围大于
强碱与弱酸反应(强酸与弱碱反应)
室温下pH=7不一定是终点:强碱与强酸反应时,终点是pH=7;强碱与弱酸(强
酸与弱碱)反应时,终点不是pH=7(强碱与弱酸反应终点是pH>7,强酸与弱碱反
应终点是pH<7)
2.滴定曲线分析的方法
(1)分析步骤:首先看纵坐标,搞清楚是酸加入碱中,还是碱加入酸中;其次看起点
起点可以看出酸性或碱性的强弱,这在判断滴定终点时至关重要;再次找滴定终
点和pH=7的中性点,判断滴定终点的酸碱性,然后确定中性点(pH=7)的位置;
最后分析其他的特殊点(如滴定一半点,过量一半点等),分析酸、碱过量情况。
(2)滴定过程中的定量关系:①电荷守恒关系在任何时候均存在;②物料守恒可以
根据加入酸的物质的量和加入碱的物质的量进行确定,但不一定为等量关系。
[题型专练]
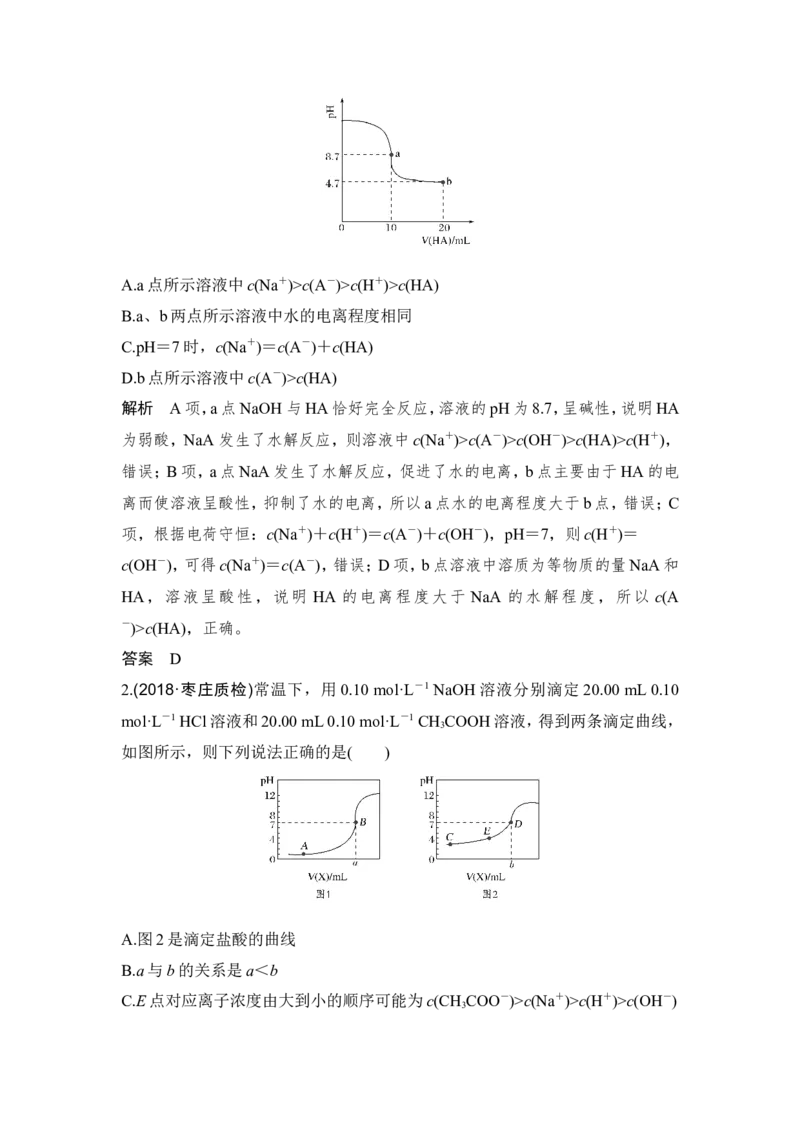
1.(山东卷)室温下向 10 mL 0.1 mol·L-1NaOH溶液中加入 0.1 mol·L-1的一元酸
HA,溶液pH的变化曲线如图所示。下列说法正确的是( )A.a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,c(Na+)=c(A-)+c(HA)
D.b点所示溶液中c(A-)>c(HA)
解析 A项,a点NaOH与HA恰好完全反应,溶液的pH为8.7,呈碱性,说明HA
为弱酸,NaA发生了水解反应,则溶液中c(Na+)>c(A-)>c(OH-)>c(HA)>c(H+),
错误;B项,a点NaA发生了水解反应,促进了水的电离,b点主要由于HA的电
离而使溶液呈酸性,抑制了水的电离,所以a点水的电离程度大于b点,错误;C
项,根据电荷守恒:c(Na+)+c(H+)=c(A-)+c(OH-),pH=7,则c(H+)=
c(OH-),可得c(Na+)=c(A-),错误;D项,b点溶液中溶质为等物质的量NaA和
HA,溶液呈酸性,说明 HA 的电离程度大于 NaA 的水解程度,所以 c(A
-)>c(HA),正确。
答案 D
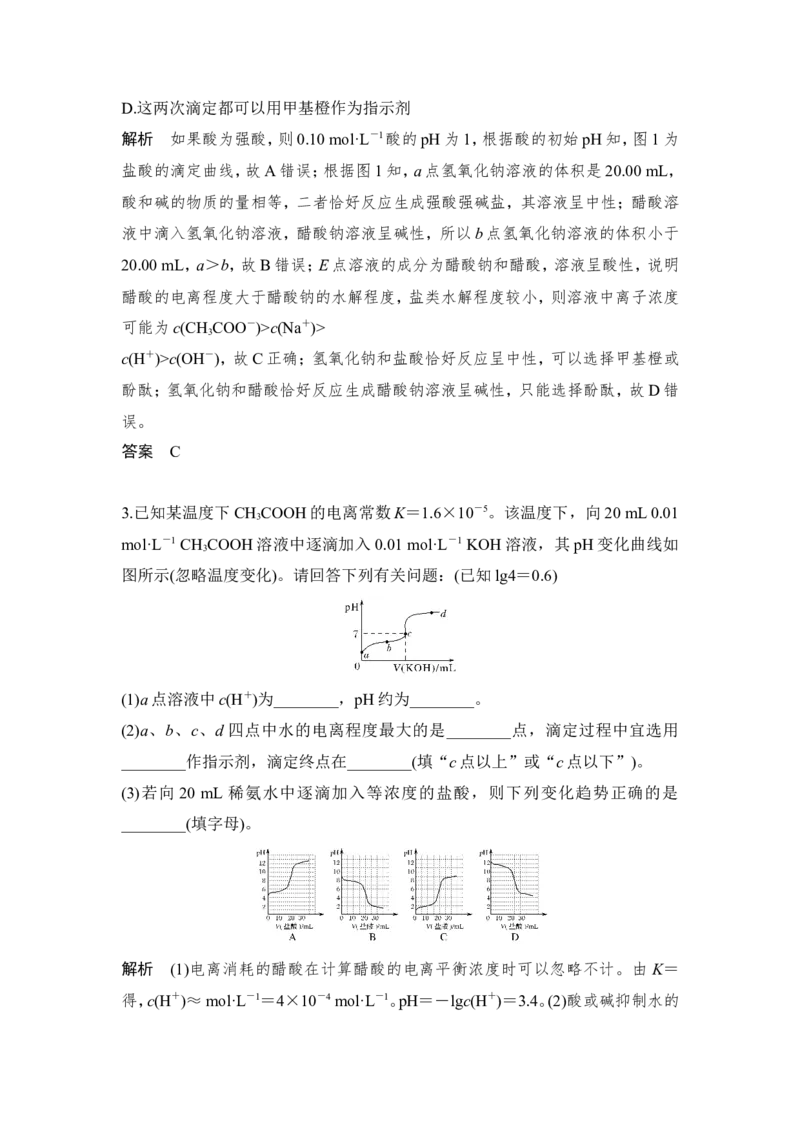
2.(2018·枣庄质检)常温下,用 0.10 mol·L-1 NaOH溶液分别滴定 20.00 mL 0.10
mol·L-1 HCl溶液和20.00 mL 0.10 mol·L-1 CH COOH溶液,得到两条滴定曲线,
3
如图所示,则下列说法正确的是( )
A.图2是滴定盐酸的曲线
B.a与b的关系是a<b
C.E点对应离子浓度由大到小的顺序可能为c(CH COO-)>c(Na+)>c(H+)>c(OH-)
3D.这两次滴定都可以用甲基橙作为指示剂
解析 如果酸为强酸,则0.10 mol·L-1酸的pH为1,根据酸的初始pH知,图1为
盐酸的滴定曲线,故A错误;根据图1知,a点氢氧化钠溶液的体积是20.00 mL,
酸和碱的物质的量相等,二者恰好反应生成强酸强碱盐,其溶液呈中性;醋酸溶
液中滴入氢氧化钠溶液,醋酸钠溶液呈碱性,所以b点氢氧化钠溶液的体积小于
20.00 mL,a>b,故B错误;E点溶液的成分为醋酸钠和醋酸,溶液呈酸性,说明
醋酸的电离程度大于醋酸钠的水解程度,盐类水解程度较小,则溶液中离子浓度
可能为c(CH COO-)>c(Na+)>
3
c(H+)>c(OH-),故C正确;氢氧化钠和盐酸恰好反应呈中性,可以选择甲基橙或
酚酞;氢氧化钠和醋酸恰好反应生成醋酸钠溶液呈碱性,只能选择酚酞,故D错
误。
答案 C
3.已知某温度下CH COOH的电离常数K=1.6×10-5。该温度下,向20 mL 0.01
3
mol·L-1 CH COOH溶液中逐滴加入0.01 mol·L-1 KOH溶液,其pH变化曲线如
3
图所示(忽略温度变化)。请回答下列有关问题:(已知lg4=0.6)
(1)a点溶液中c(H+)为________,pH约为________。
(2)a、b、c、d四点中水的电离程度最大的是________点,滴定过程中宜选用
________作指示剂,滴定终点在________(填“c点以上”或“c点以下”)。
(3)若向 20 mL 稀氨水中逐滴加入等浓度的盐酸,则下列变化趋势正确的是
________(填字母)。
解析 (1)电离消耗的醋酸在计算醋酸的电离平衡浓度时可以忽略不计。由 K=
得,c(H+)≈ mol·L-1=4×10-4 mol·L-1。pH=-lgc(H+)=3.4。(2)酸或碱抑制水的电离a、b点溶液呈酸性,d点溶液呈碱性,都抑制水的电离,c点呈中性,水自然
电离,故电离程度最大。由于酸碱恰好完全反应时溶液显碱性,故应该选择在碱
性范围内变色的指示剂酚酞。滴定终点应在c点以上。(3)由于稀氨水显碱性,首
先排除选项A和C;两者恰好反应时溶液显酸性,排除选项D。
答案 (1)4×10-4 mol·L-1 3.4 (2)c 酚酞 c点以上 (3)B