文档内容
模板 06 晶体结构的分析与计算
本节导航
识·题型解读 考情分析+命题预测/技巧解读
明 ·模板构建 答题模板 + 技巧点拨
技法01 常见晶体结构模型 技法02 有关晶胞的计算
技法03 晶胞中原子坐标与投影图 技法04 晶体的熔、沸点比较
通·模板运用 真题示例+模板答题+变式训练
练 ·模板演练 最新模拟、预测考向
晶体结构分析及相关计算在高考考查中难度较大,命题时多以新技术、新发明为情景,以化学式或晶
胞中微粒数确定为基础,考查晶体的密度、相对原子质量、N 等计算、配位数确定等。晶体熔、沸点
A
多结合元素的推断进行考查,题目难度较大。
第一步:仔细审题 阅读题目获取对解题有价值的信息,排除无效信息,并作标记。
第二步:判断晶胞 找出晶胞,确定晶胞内所有原子或离子的种类和位置。
结构
第三步:计算微粒 用“均摊法”计算晶胞中微粒的数目,确定晶体的化学式。
数
第四步:进行晶体 根据选项计算晶体的密度、空间利用率,确定原子分数坐标等。
相关计算
技法01 常见晶体的结构模型1.4类典型晶体结构模型
(1)典型离子晶体结构模型
晶体 NaCl CsCl ZnS CaF
2
晶胞
配位数 6 8 4 F-:4;Ca2+:8
4个Na+ 1个Cs+ 4个S2- 4个Ca2+
粒子数目
4个Cl- 1个Cl- 4个Zn2+ 8个F-
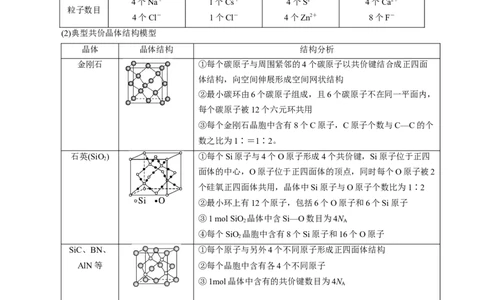
(2)典型共价晶体结构模型
晶体 晶体结构 结构分析
金刚石 ①每个碳原子与周围紧邻的4个碳原子以共价键结合成正四面
体结构,向空间伸展形成空间网状结构
②最小碳环由6个碳原子组成,且6个碳原子不在同一平面内,
每个碳原子被12个六元环共用
③每个金刚石晶胞中含有8个C原子,C原子个数与C—C的个
数之比为1∶=1∶2。
石英(SiO) ①每个Si原子与4个O原子形成4个共价键,Si原子位于正四
2
面体的中心,O原子位于正四面体的顶点,同时每个O原子被2
个硅氧正四面体共用,晶体中Si原子与O原子个数比为1∶2
②最小环上有12个原子,包括6个O原子和6个Si原子
③1 mol SiO 晶体中含Si—O数目为4N
2 A
④每个SiO 晶胞中含有8个Si原子和16个O原子
2
SiC、BN、 ①每个原子与另外4个不同原子形成正四面体结构
AlN等 ②每个晶胞中含有各4个不同原子
③1mol晶体中含有的共价键数目为4N
A
(3)典型分子晶体——干冰晶体结构模型
①CO 分子位于立方体晶胞的顶点和面心
2
②干冰中的CO 分子间只存在范德华力,不存在氢键
2
③每个晶胞有4个CO 分子,12个原子。每个CO 分子周围有12个紧邻分子,密度比冰的高
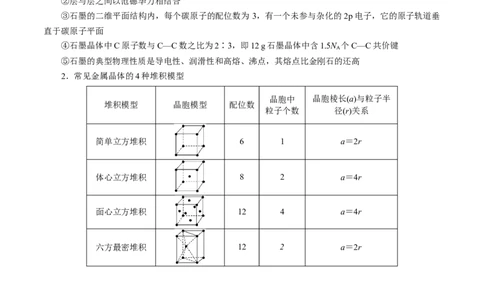
2 2(4)混合型晶体——石墨晶体
①同层内,碳原子采用sp2杂化,以共价键相结合形成平面六元并环结构。所有碳原子的p轨道相互平
行且相互重叠,使p轨道中电子可在整个平面中运动
②层与层之间以范德华力相结合
③石墨的二维平面结构内,每个碳原子的配位数为 3,有一个未参与杂化的2p电子,它的原子轨道垂
直于碳原子平面
④石墨晶体中C原子数与C—C数之比为2∶3,即12 g石墨晶体中含1.5N 个C—C共价键
A
⑤石墨的典型物理性质是导电性、润滑性和高熔、沸点,其熔点比金刚石的还高
2.常见金属晶体的4种堆积模型
晶胞中 晶胞棱长(a)与粒子半
堆积模型 晶胞模型 配位数
粒子个数 径(r)关系
简单立方堆积 6 1 a=2r
体心立方堆积 8 2 a=4r
面心立方堆积 12 4 a=4r
六方最密堆积 12 2 a=2r
晶体 NaCl CsCl ZnS CaF 金刚石
2
晶体结构
4个Na+,4个 1个Cs+,1个 4个S2-,4个 4个Ca2+,8个F
粒子数目 8个C
Cl- Cl- Zn2+ -
晶体 简单立方 体心立方 面心立方 氮化硼 干冰晶体结构
粒子数目 1个原子 2个原子 4个原子 4个B,4个N 4个CO
2
技法02 有关晶胞的计算
1.用“均摊法”计算晶胞中的微粒数
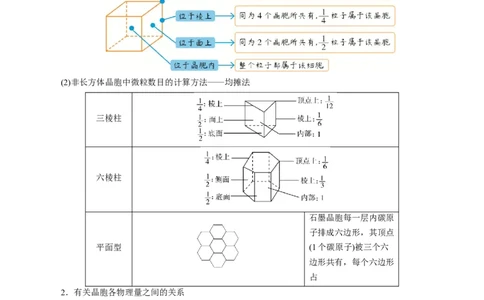
(1)平行六面体晶胞中微粒计算方法
(2)非长方体晶胞中微粒数目的计算方法——均摊法
三棱柱
六棱柱
石墨晶胞每一层内碳原
子排成六边形,其顶点
平面型 (1个碳原子)被三个六
边形共有,每个六边形
占
2.有关晶胞各物理量之间的关系
(1)晶体密度与微观晶胞参数的关系
(2)晶体中粒子间距离的计算技法03 晶胞中原子的分数坐标与投影图
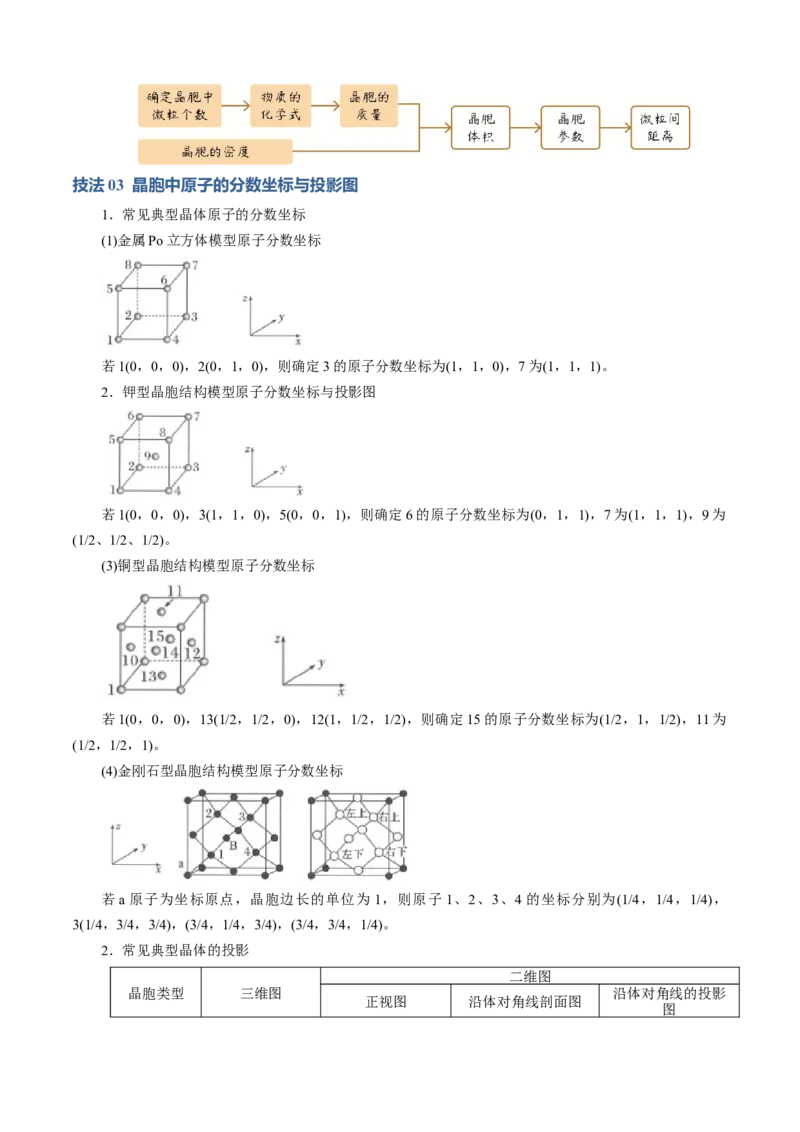
1.常见典型晶体原子的分数坐标
(1)金属Po立方体模型原子分数坐标
若1(0,0,0),2(0,1,0),则确定3的原子分数坐标为(1,1,0),7为(1,1,1)。
2.钾型晶胞结构模型原子分数坐标与投影图
若1(0,0,0),3(1,1,0),5(0,0,1),则确定6的原子分数坐标为(0,1,1),7为(1,1,1),9为
(1/2、1/2、1/2)。
(3)铜型晶胞结构模型原子分数坐标
若1(0,0,0),13(1/2,1/2,0),12(1,1/2,1/2),则确定15的原子分数坐标为(1/2,1,1/2),11为
(1/2,1/2,1)。
(4)金刚石型晶胞结构模型原子分数坐标
若a原子为坐标原点,晶胞边长的单位为 1,则原子1、2、3、4的坐标分别为(1/4,1/4,1/4),
3(1/4,3/4,3/4),(3/4,1/4,3/4),(3/4,3/4,1/4)。
2.常见典型晶体的投影
二维图
晶胞类型 三维图 沿体对角线的投影
正视图 沿体对角线剖面图
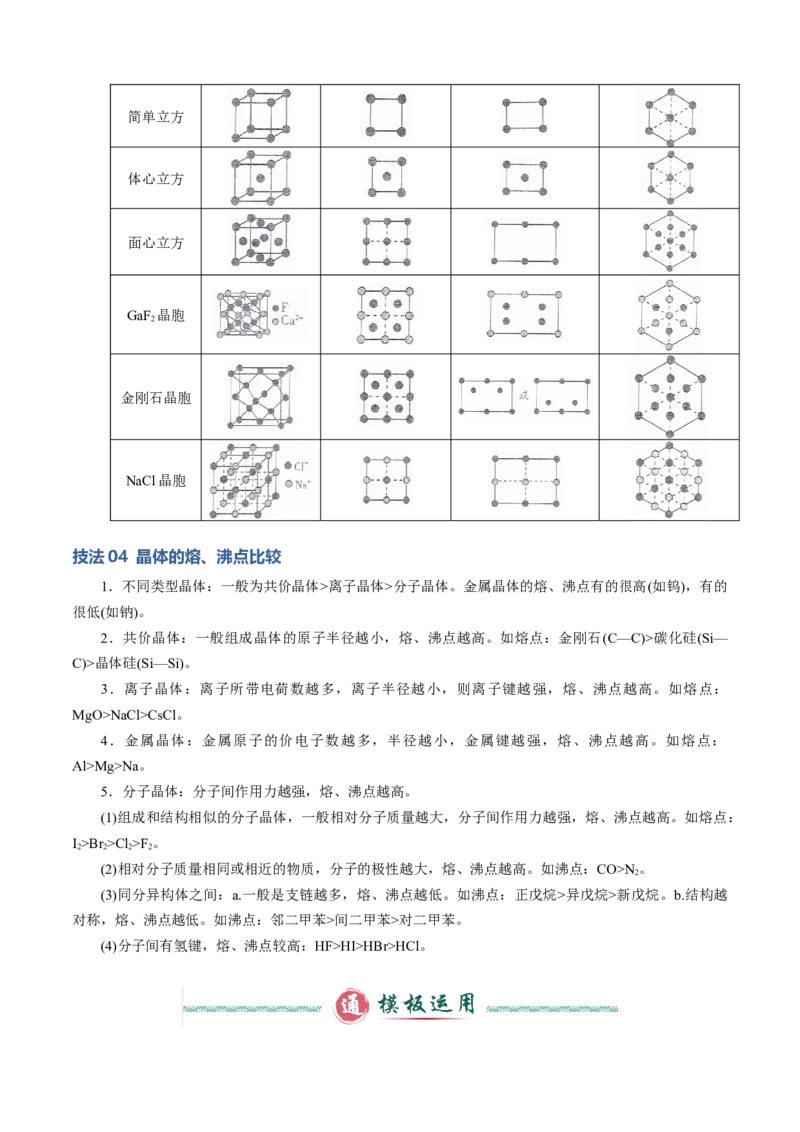
图简单立方
体心立方
面心立方
GaF 晶胞
2
金刚石晶胞
NaCl晶胞
技法04 晶体的熔、沸点比较
1.不同类型晶体:一般为共价晶体>离子晶体>分子晶体。金属晶体的熔、沸点有的很高(如钨),有的
很低(如钠)。
2.共价晶体:一般组成晶体的原子半径越小,熔、沸点越高。如熔点:金刚石(C—C)>碳化硅(Si—
C)>晶体硅(Si—Si)。
3.离子晶体:离子所带电荷数越多,离子半径越小,则离子键越强,熔、沸点越高。如熔点:
MgO>NaCl>CsCl。
4.金属晶体:金属原子的价电子数越多,半径越小,金属键越强,熔、沸点越高。如熔点:
Al>Mg>Na。
5.分子晶体:分子间作用力越强,熔、沸点越高。
(1)组成和结构相似的分子晶体,一般相对分子质量越大,分子间作用力越强,熔、沸点越高。如熔点:
I>Br >Cl>F 。
2 2 2 2
(2)相对分子质量相同或相近的物质,分子的极性越大,熔、沸点越高。如沸点:CO>N。
2
(3)同分异构体之间:a.一般是支链越多,熔、沸点越低。如沸点:正戊烷>异戊烷>新戊烷。b.结构越
对称,熔、沸点越低。如沸点:邻二甲苯>间二甲苯>对二甲苯。
(4)分子间有氢键,熔、沸点较高:HF>HI>HBr>HCl。类型01 立方晶胞图像
1.(2024·河北卷)金属铋及其化合物广泛应用于电子设备、医药等领域。如图是铋的一种氟化物的
立方晶胞及晶胞中MNPQ点的截面图,晶胞的边长为a pm,N 为阿伏加德罗常数的值。下列说法错误的
A
是
A.该铋氟化物的化学式为BiF
3
B.粒子S、T之间的距离为
C.该晶体的密度为
D.晶体中与铋离子最近且等距的氟离子有6个
【答案】D
【第一步 判断晶体结构】该晶胞为立方晶胞。
以晶胞体心处铋离子为分析对象,距离其最近且等距的氟离子位于晶胞体内,为将晶胞均分为 8个小立方
体后,每个小立方体的体心的F-,即有8个,D错误。
【第二步 计算微粒数】
Bi位于棱心(12个)和体心(1个),每个晶胞中含有 个Bi,F位于顶点(8个)、面心(6
个)、体内(8个),每个晶胞中含有 个F,故化学式为BiF ,A正确。
3
【第三步 进行晶体相关计算】
将晶胞均分为8个小立方体,由晶胞中MNPQ点的截面图可知,晶胞体内的8个F-位于8个小立方体的体
心,以M为原点建立坐标系,令N的原子分数坐标为 ,与Q、M均在同一条棱上的F-的原子分数坐
标为 ,则T的原子分数坐标为 , S的原子分数坐标为 ,所以粒子S、T之间的距
离为 ,B正确。由A项分析可知,每个晶胞中有4个Bi3+、12个F-,晶胞体积为 ,则晶体密度为
= ,C正确。
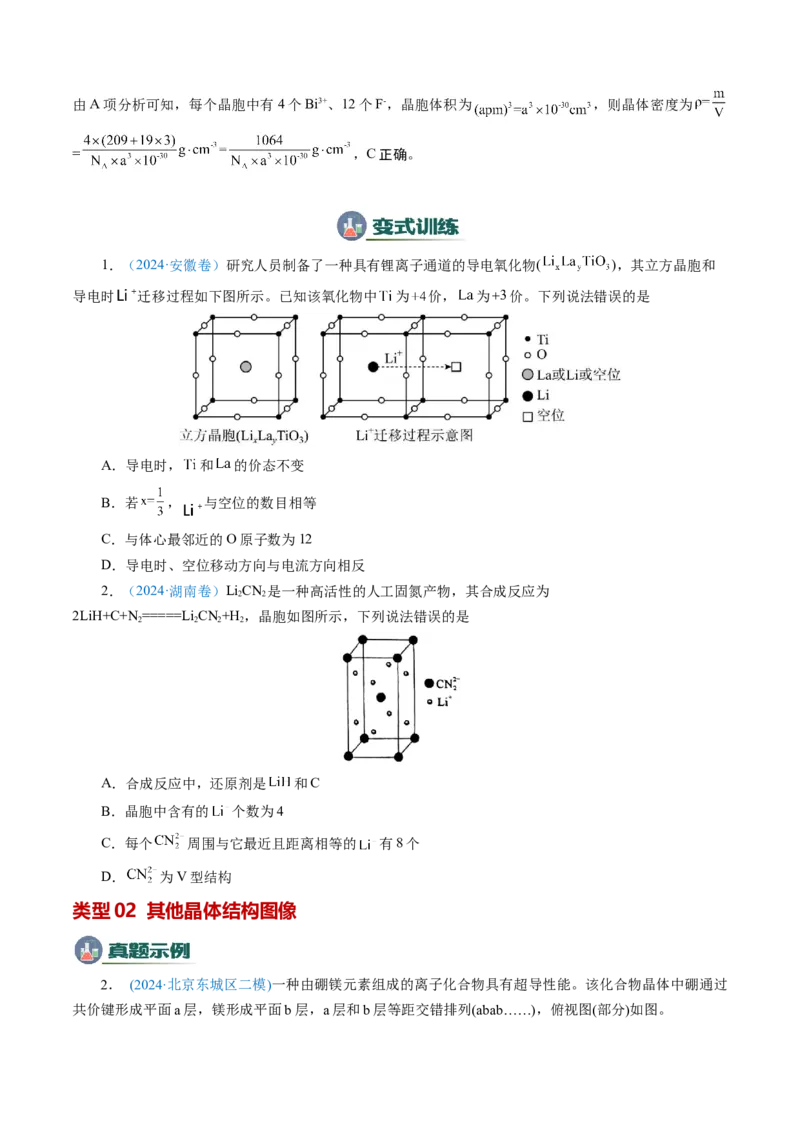
1.(2024·安徽卷)研究人员制备了一种具有锂离子通道的导电氧化物( ),其立方晶胞和
导电时 迁移过程如下图所示。已知该氧化物中 为 价, 为 价。下列说法错误的是
A.导电时, 和 的价态不变
B.若 , 与空位的数目相等
C.与体心最邻近的O原子数为12
D.导电时、空位移动方向与电流方向相反
2.(2024·湖南卷)LiCN 是一种高活性的人工固氮产物,其合成反应为
2 2
2LiH+C+N=====LiCN+H ,晶胞如图所示,下列说法错误的是
2 2 2 2
A.合成反应中,还原剂是 和C
B.晶胞中含有的 个数为4
C.每个 周围与它最近且距离相等的 有8个
D. 为V型结构
类型02 其他晶体结构图像
2. (2024·北京东城区二模)一种由硼镁元素组成的离子化合物具有超导性能。该化合物晶体中硼通过
共价键形成平面a层,镁形成平面b层,a层和b层等距交错排列(abab……),俯视图(部分)如图。下列说法正确的是( )
A.硼层中硼的杂化类型为sp3
B.该化合物的化学式为MgB
2
C.镁周围最近且等距的硼有6个
D.镁层内存在离子键
【答案】B
【第一步 判断晶体结构】该晶体为平面结构,晶体中硼通过共价键形成平面a层,镁形成平面b层。
【第二步 计算微粒数】由投影图可知,每个镁原子上层距离其最近的硼原子有6个,下层距离其最近的硼
原子也有6个,共12个,每个硼原子上层距离其最近的镁原子有3个,下层距离其最近的镁原子也有3个,
共6个,则Mg、B原子个数比为1∶2,化学式为MgB ,故B正确,C错误。
2
【第三步 进行晶体有关计算】
由投影图可知,硼层中硼原子连接3个σ键,B原子价电子有3个,全部用于形成σ键,无孤电子对,价
层电子对数为3+0=3,杂化类型为sp2,故A错误。
Mg层内存在金属键,不存在离子键,故D错误。
1.(2024·贵州卷)我国科学家首次合成了化合物[K(2,2,2-crypt)][K@Au Sb ]。其阴离子
12 20
[K@Au Sb ]5-为全金属富勒烯(结构如图),具有与富勒烯C 相似的高对称性。下列说法错误的是
12 20 60
A.富勒烯C 是分子晶体
60
B.图示中的K+位于Au形成的二十面体笼内
C.全金属富勒烯和富勒烯C 互为同素异形体
60
D.锑(Sb)位于第五周期第ⅤA族,则其基态原子价层电子排布式是5s25p3
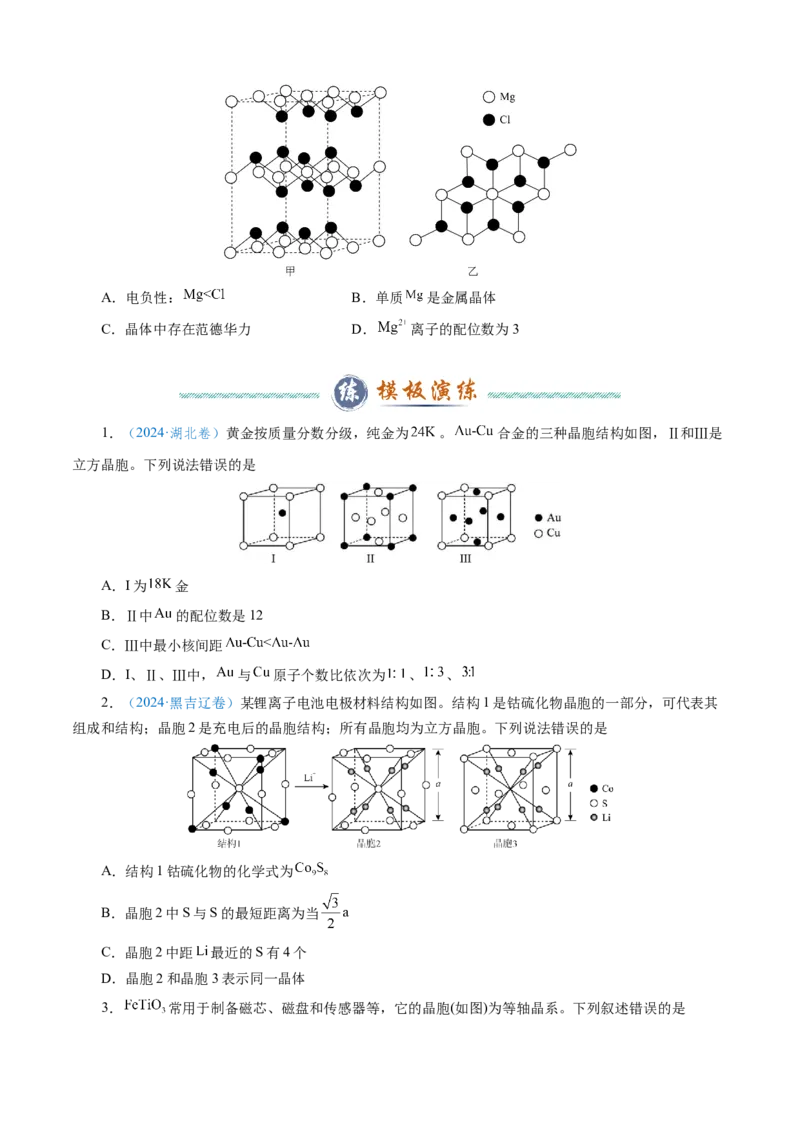
2.(2024·甘肃卷) 晶体中,多个晶胞无隙并置而成的结构如图甲所示,其中部分结构显示
为图乙,下列说法错误的是A.电负性: B.单质 是金属晶体
C.晶体中存在范德华力 D. 离子的配位数为3
1.(2024·湖北卷)黄金按质量分数分级,纯金为 。 合金的三种晶胞结构如图,Ⅱ和Ⅲ是
立方晶胞。下列说法错误的是
A.I为 金
B.Ⅱ中 的配位数是12
C.Ⅲ中最小核间距
D.I、Ⅱ、Ⅲ中, 与 原子个数比依次为 、 、
2.(2024·黑吉辽卷)某锂离子电池电极材料结构如图。结构1是钴硫化物晶胞的一部分,可代表其
组成和结构;晶胞2是充电后的晶胞结构;所有晶胞均为立方晶胞。下列说法错误的是
A.结构1钴硫化物的化学式为
B.晶胞2中S与S的最短距离为当
C.晶胞2中距 最近的S有4个
D.晶胞2和晶胞3表示同一晶体
3. 常用于制备磁芯、磁盘和传感器等,它的晶胞(如图)为等轴晶系。下列叙述错误的是已知:晶胞参数为 , 为阿伏加德罗常数的值。
A. 的分数坐标为
B.氧离子构成正八面体形
C. 和 之间的距离为
D. 晶体密度为
4.下图是氮化镓的一种晶体结构, 表示阿伏加德罗常数的值。下列说法正确的是
A.每个 原子周围距离最近的 原子数目为4
B.氮化镓分子式为
C.a、b原子坐标参数依次为 、 、则c原子坐标参数为
D.已知该晶体密度为 ,则镓氮原子间最短距离为
5.镧镍合金是一种储氢材料,其晶胞可认为由两种结构不同的层交替堆积而成,如下图所示。已知
该合金的密度为 ,该合金的晶胞中最多可容纳9个氢原子。下列叙述错误的是
A.基态Ni原子的价电子排布式为
B.该合金的化学式为
C.假定吸氢后体积不变,则合金中氢的最大密度为D.设A处La的原子坐标为 ,则晶胞底面上Ni的原子坐标为 或
6.砷化镓是重要的半导体材料,用于制作微波集成电路、红外线发光二极管等元件,砷化镓立方晶
胞结构如图所示,晶胞参数为a pm。下列说法正确的是( )
A.每个Ga周围距离最近的Ga原子个数为8
B.Ga原子与As原子的最短距离为a pm
C.该晶胞的质量为 g(N 为阿伏加德罗常数的值)
A
D.一个晶胞中含有4个As原子和14个Ga原子
7. 超导现象一直吸引着广大科学家的关注。某超导材料的晶体结构属于四方晶系,其晶胞如图所示。
下列说法错误的是( )
A.第一电离能:I(Cu)>I(Ba)
1 1
B.与Ba2+等距且最近的Cu2+有12个
C.该超导材料的化学式为HgBa CuO
2 4
D.该晶体的密度为 g·cm-3
8.砷化镓是一种新型半导体材料,应用广泛。图甲为它的立方晶胞结构,图乙为该晶胞沿y轴的投影
图。该晶胞的边长为d pm,在三维坐标系中a、b两点的原子坐标分别为(0,1,0),(1,0,1)。下列说法错误的
是( )
A.As和Ga原子间的最近距离为d pm
B.Ga原子的配位数为4
C.c点的原子坐标为
D.As原子填充在Ga原子围成的“正四面体空隙”中9.晶体世界丰富多彩、复杂多样,各类晶体具有的不同结构特点,决定着它们具有不同的性质和用
途。氢化铝钠(NaAlH )是一种新型轻质储氢材料,其晶胞结构如图所示,为长方体。设阿伏加德罗常数的
4
值为N 。下列说法错误的是( )
A
A.AlH中中心原子Al的杂化方式为sp3杂化
B.NaAlH 晶体中,与AlH紧邻且等距的Na+有4个
4
C.NaAlH 晶体的密度为 g·cm-3
4
D.若NaAlH 晶胞上下面心处的Na+被Li+取代,得到的晶体的化学式为NaLi(AlH )
4 3 4 4
10.某晶体立方晶胞如图所示。已知图中微粒1的分数坐标是,阿伏加德罗常数的值为N 。下列说法
A
正确的是( )
A.Ag+周围距离最近且相等的N个数是6
B.微粒2的分数坐标是
C.已知银与铜位于同一族,银元素位于元素周期表的d区
D.若晶胞边长为a pm,则晶体密度为 g·cm-3
11.XeF 晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为 90°。以晶胞参数为单位长度建立
2
的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为。已知Xe—F键
长为r pm,下列说法不正确的是( )
A.该晶体的密度为 g/cm3
B.B点原子的分数坐标为(0,0,r)
C.晶胞中A、B间距离d= pm
D.基态F原子的核外电子空间运动状态有5种12.镧La和H可以形成一系列晶体材料LaH ,在储氢和超导等领域具有重要应用。LaH 属于立方晶
n n
系,晶胞结构和参数如图所示。高压下,LaH 中的每个H结合4个H形成类似CH 的结构,即得到晶体
2 4
LaH。下列说法错误的是( )
x
A.LaH 晶体中La的配位数为8
2
B.晶体中H和H的最短距离:LaH >LaH
2 x
C.在LaH 晶胞中,H形成一个顶点数为40的闭合多面体笼
x
D.LaH 单位体积中含氢质量的计算式为 g·cm-3
x
13.硒(Se)是一种有抗癌、抗氧化作用的元素,可形成多种化合物。某化合物是潜在热电材料之一,
其晶胞结构如图甲所示,晶胞参数为a pm,沿x、y、z轴方向的投影均如图乙所示。
下列说法错误的是( )A.基态钾原子核外电子有10种空间运动状态
B.Se和K的最短距离为a pm
C.该化合物的化学式为KSeBr
4
D.距离Se最近的Se有12个
14.硫代硫酸盐是具有应用前景的浸金试剂。硫代硫酸根离子(S O)可看作SO中的一个O原子被S原
2
子替代的产物。MgS O·6H O的晶胞形状为长方体,边长分别为a nm、b nm、c nm,其结构如图所示,
2 3 2
已知MgS O·6H O的摩尔质量是M g·mol-1,N 为阿伏加德罗常数的值,下列说法正确的是( )
2 3 2 A
A.晶胞中[Mg(H O) ]2+的个数为3
2 6
B.若晶胞中A的分数坐标为(0,0,0),则B的分数坐标为(a,0,c)
C.SO的中心硫原子的杂化方式为sp3
2
D.该晶体的密度为 g·cm-3
15.(2023·新课标卷)一种可吸附甲醇的材料,其化学式为 ,部分晶体
结构如下图所示,其中 为平面结构。
下列说法正确的是
A.该晶体中存在N-H…O氢键
B.基态原子的第一电离能:C