文档内容
郑州外国语学校2022-2023学年高三上期调研4
化 学
(90分钟 100分)
可能用到的相对原子质量:H-1 D-2 C-12 N-14 O-16 Cl-35.5 Na-23
一、选择题(本题包括15小题,每小题3分,每小题只有一个选项符合题意)
1.化学与日常生活息息相关。下列说法错误的是
A.牙膏中添加氟化物用于预防龋齿
B.温室气体是形成酸雨(pH<5.6)的主要气体
C.棉花和麻均为碳水化合物
D.华为5G手机芯片的主要成分是硅
2.下列化学用语表示正确的是
A.CO 的分子模型示意图:
2
B.除去氯化铵中氯化镁杂质的离子方程式:Mg2++2OH-=Mg(OH) ↓
2
C.M2+核外有a个电子,b个中子的原子符号:
D.乙烯的电子式:
3.某有机物X的结构简式如图所示,则下列有关说法正确的是
A.X的分子式为C H O
12 12 3
B.X在一定条件下,最多能与1mol H 发生加成反应
2
C.不可用酸性高锰酸钾溶液区分苯和X
D.X分别与Na、NaOH反应,消耗的物质的量之比是1:1
4.N 表示阿伏伽德罗常数,下列说法正确的是
A
A.60g二氧化硅晶体中含有的硅氧键数目为4N
A
B.常温下,78g苯完全转化为溴苯,增加了N 个共价键
A
C.27gAl无论和足量盐酸还是足量NaOH溶液反应都生成氢气33.6L
D.某温度下,1L pH=9的NaCO 溶液中,水电离产生的OH-数目为10-5N
2 3 A
5.一定条件下 A、B、C 能实现如下图所示的转化关系(部分产物已省略),且△H=△H
+△H。下列说法不正确的是
1 2
A.若A为短周期元素的气态氢化物,则B可能为固态单质,也可能为气态化合物
B.若A为短周期非金属元素固态单质,则C的水化物可能为强酸,也可能为弱酸C.若A、C均为含铝化合物,二者能反应生成B,则X可能为强酸,也可能为强碱
D.若A为焰色反应呈黄色的化合物,则C可能为离子化合物,也可能为共价化合物
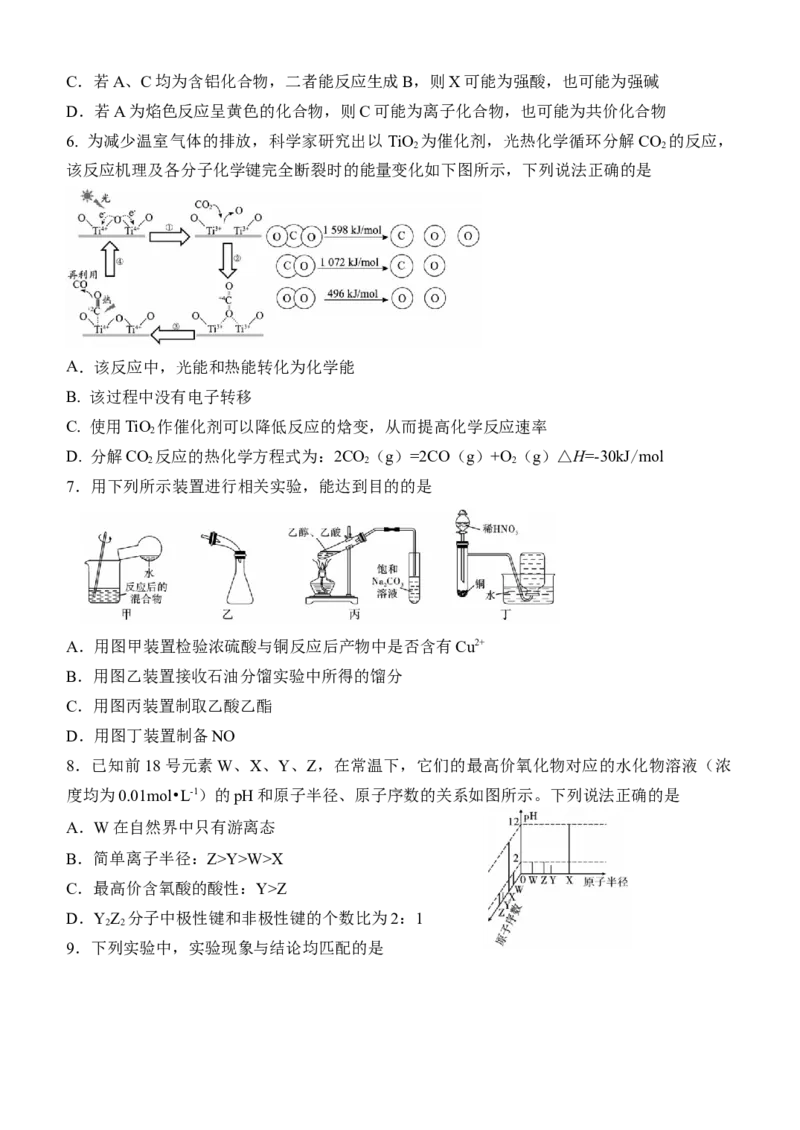
6. 为减少温室气体的排放,科学家研究出以TiO 为催化剂,光热化学循环分解CO 的反应,
2 2
该反应机理及各分子化学键完全断裂时的能量变化如下图所示,下列说法正确的是
A.该反应中,光能和热能转化为化学能
B. 该过程中没有电子转移
C. 使用TiO 作催化剂可以降低反应的焓变,从而提高化学反应速率
2
D. 分解CO 反应的热化学方程式为:2CO(g)=2CO(g)+O (g)△H=-30kJ/mol
2 2 2
7.用下列所示装置进行相关实验,能达到目的的是
A.用图甲装置检验浓硫酸与铜反应后产物中是否含有Cu2+
B.用图乙装置接收石油分馏实验中所得的馏分
C.用图丙装置制取乙酸乙酯
D.用图丁装置制备NO
8.已知前18号元素W、X、Y、Z,在常温下,它们的最高价氧化物对应的水化物溶液(浓
度均为0.01mol•L-1)的pH和原子半径、原子序数的关系如图所示。下列说法正确的是
A.W在自然界中只有游离态
B.简单离子半径:Z>Y>W>X
C.最高价含氧酸的酸性:Y>Z
D.YZ 分子中极性键和非极性键的个数比为2:1
2 2
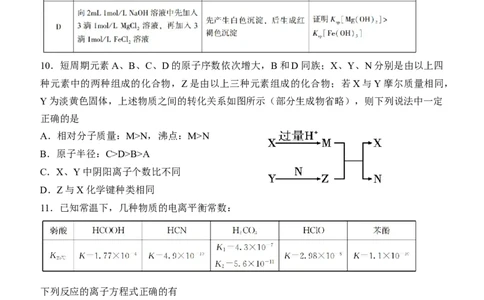
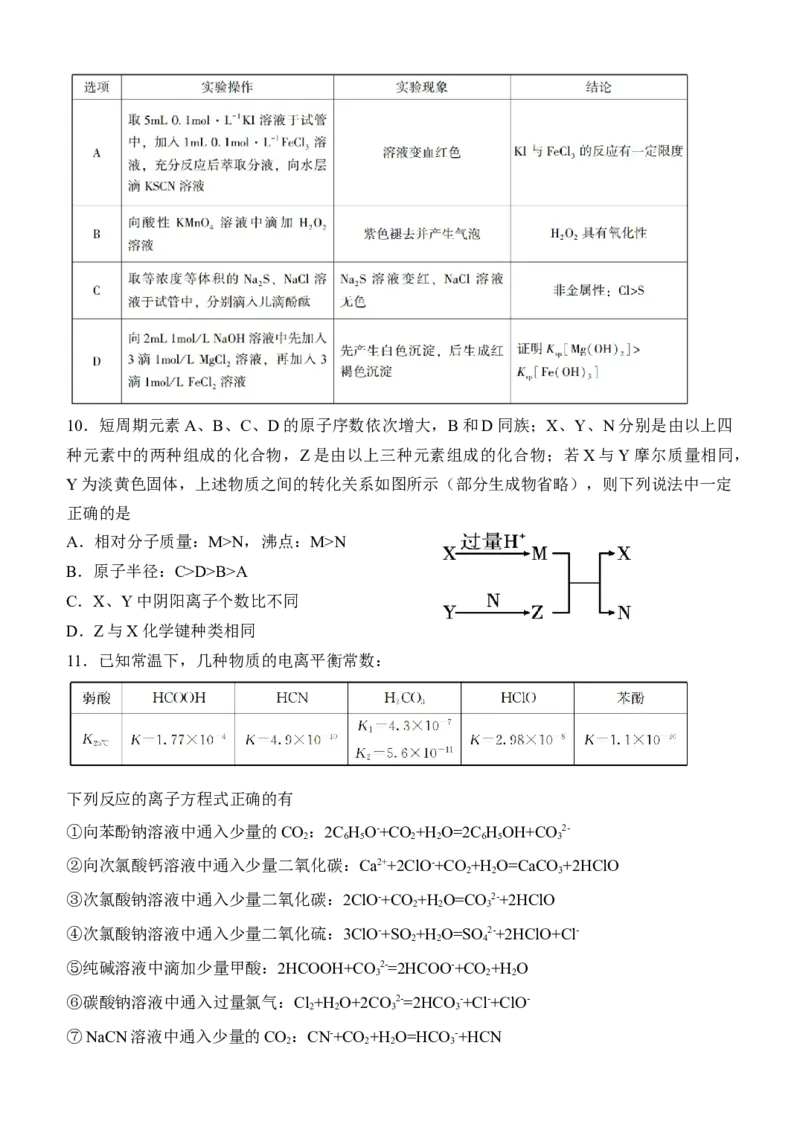
9.下列实验中,实验现象与结论均匹配的是10.短周期元素A、B、C、D的原子序数依次增大,B和D同族;X、Y、N分别是由以上四
种元素中的两种组成的化合物,Z是由以上三种元素组成的化合物;若X与Y摩尔质量相同,
Y为淡黄色固体,上述物质之间的转化关系如图所示(部分生成物省略),则下列说法中一定
正确的是
A.相对分子质量:M>N,沸点:M>N
B.原子半径:C>D>B>A
C.X、Y中阴阳离子个数比不同
D.Z与X化学键种类相同
11.已知常温下,几种物质的电离平衡常数:
下列反应的离子方程式正确的有
①向苯酚钠溶液中通入少量的CO:2C HO-+CO +H O=2C HOH+CO 2-
2 6 5 2 2 6 5 3
②向次氯酸钙溶液中通入少量二氧化碳:Ca2++2ClO-+CO +H O=CaCO +2HClO
2 2 3
③次氯酸钠溶液中通入少量二氧化碳:2ClO-+CO +H O=CO2-+2HClO
2 2 3
④次氯酸钠溶液中通入少量二氧化硫:3ClO-+SO+H O=SO 2-+2HClO+Cl-
2 2 4
⑤纯碱溶液中滴加少量甲酸:2HCOOH+CO2-=2HCOO-+CO +H O
3 2 2
⑥碳酸钠溶液中通入过量氯气:Cl+H O+2CO2-=2HCO -+Cl-+ClO-
2 2 3 3
⑦NaCN溶液中通入少量的CO:CN-+CO +H O=HCO -+HCN
2 2 2 3A.2个 B.3个 C.4个 D.5个
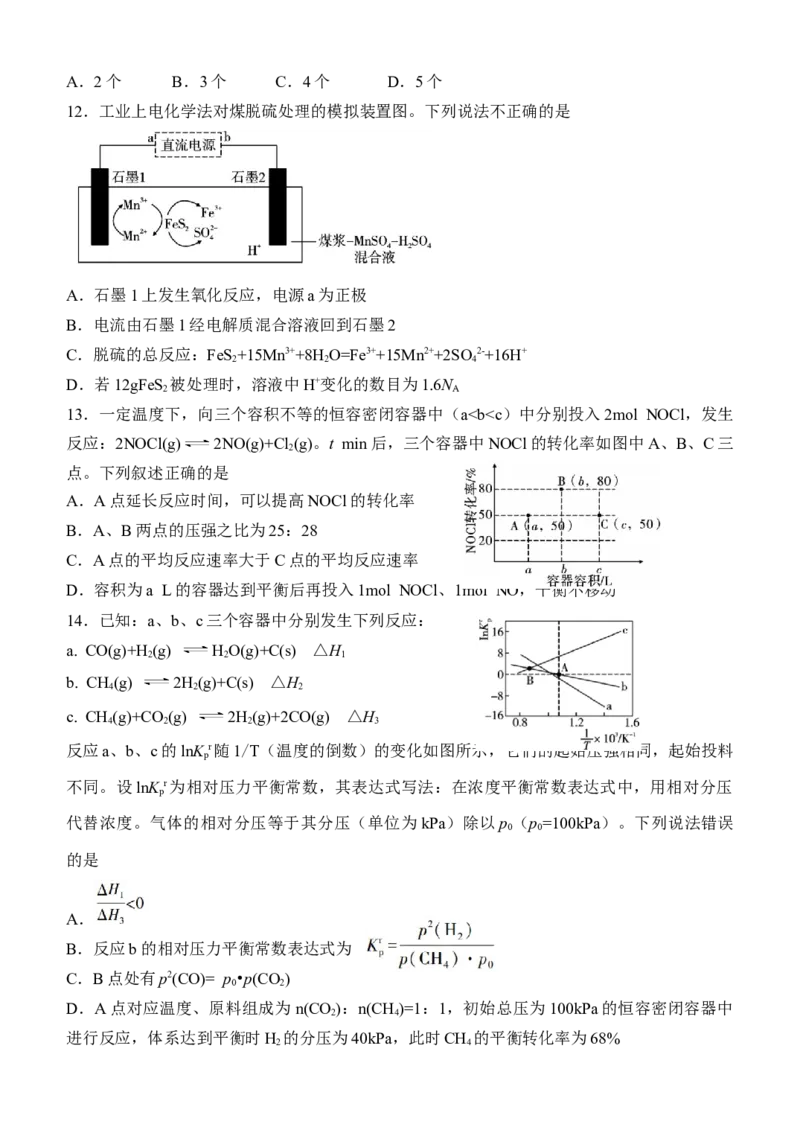
12.工业上电化学法对煤脱硫处理的模拟装置图。下列说法不正确的是
A.石墨1上发生氧化反应,电源a为正极
B.电流由石墨1经电解质混合溶液回到石墨2
C.脱硫的总反应:FeS+15Mn3++8H O=Fe3++15Mn2++2SO2-+16H+
2 2 4
D.若12gFeS 被处理时,溶液中H+变化的数目为1.6N
2 A
13.一定温度下,向三个容积不等的恒容密闭容器中(aa>b
B.曲线Ⅰ、Ⅱ、Ⅲ分别代表的粒子为A2-、HA-、HA
2
C.滴定过程中 先增大再减小
D.c点溶液满足c(K+)<0.1+ c(HA-)
二、非选择题(共55分)
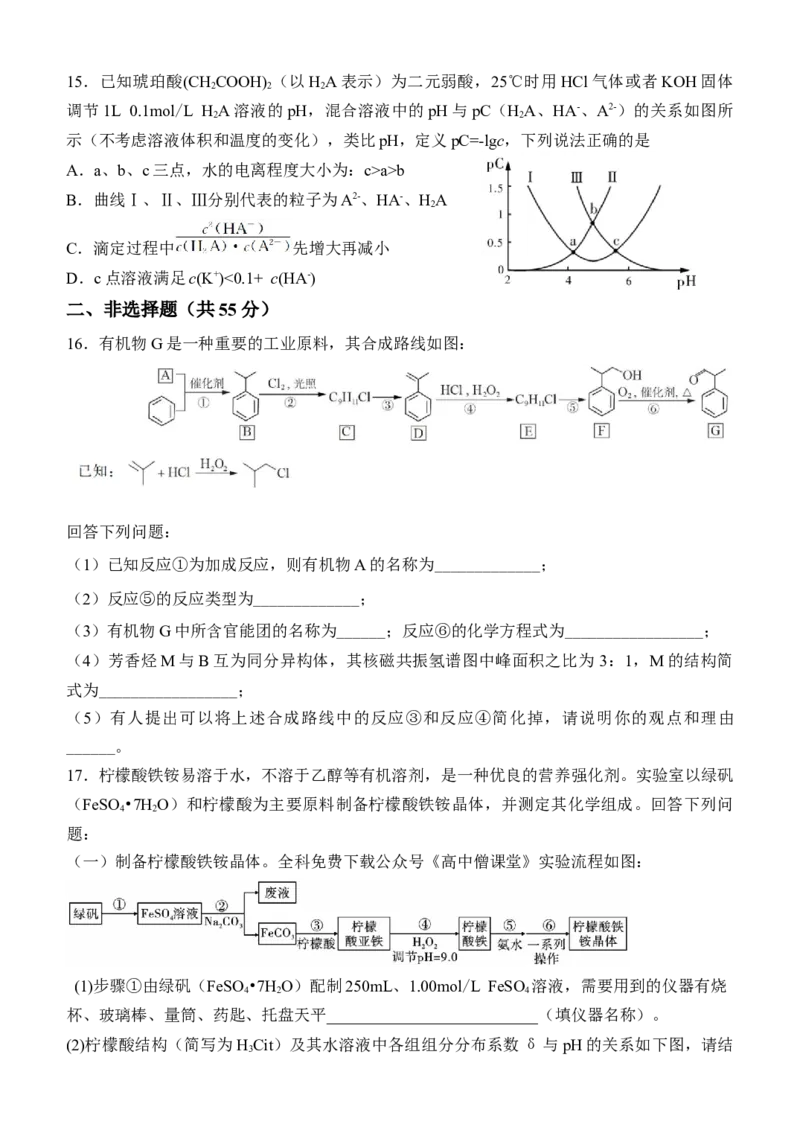
16.有机物G是一种重要的工业原料,其合成路线如图:
回答下列问题:
(1)已知反应①为加成反应,则有机物A的名称为_____________;
(2)反应⑤的反应类型为_____________;
(3)有机物G中所含官能团的名称为______;反应⑥的化学方程式为_________________;
(4)芳香烃M与B互为同分异构体,其核磁共振氢谱图中峰面积之比为 3:1,M的结构简
式为_________________;
(5)有人提出可以将上述合成路线中的反应③和反应④简化掉,请说明你的观点和理由
______。
17.柠檬酸铁铵易溶于水,不溶于乙醇等有机溶剂,是一种优良的营养强化剂。实验室以绿矾
(FeSO •7HO)和柠檬酸为主要原料制备柠檬酸铁铵晶体,并测定其化学组成。回答下列问
4 2
题:
(一)制备柠檬酸铁铵晶体。全科免费下载公众号《高中僧课堂》实验流程如图:
(1)步骤①由绿矾(FeSO •7HO)配制250mL、1.00mol/L FeSO 溶液,需要用到的仪器有烧
4 2 4
杯、玻璃棒、量筒、药匙、托盘天平__________________________(填仪器名称)。
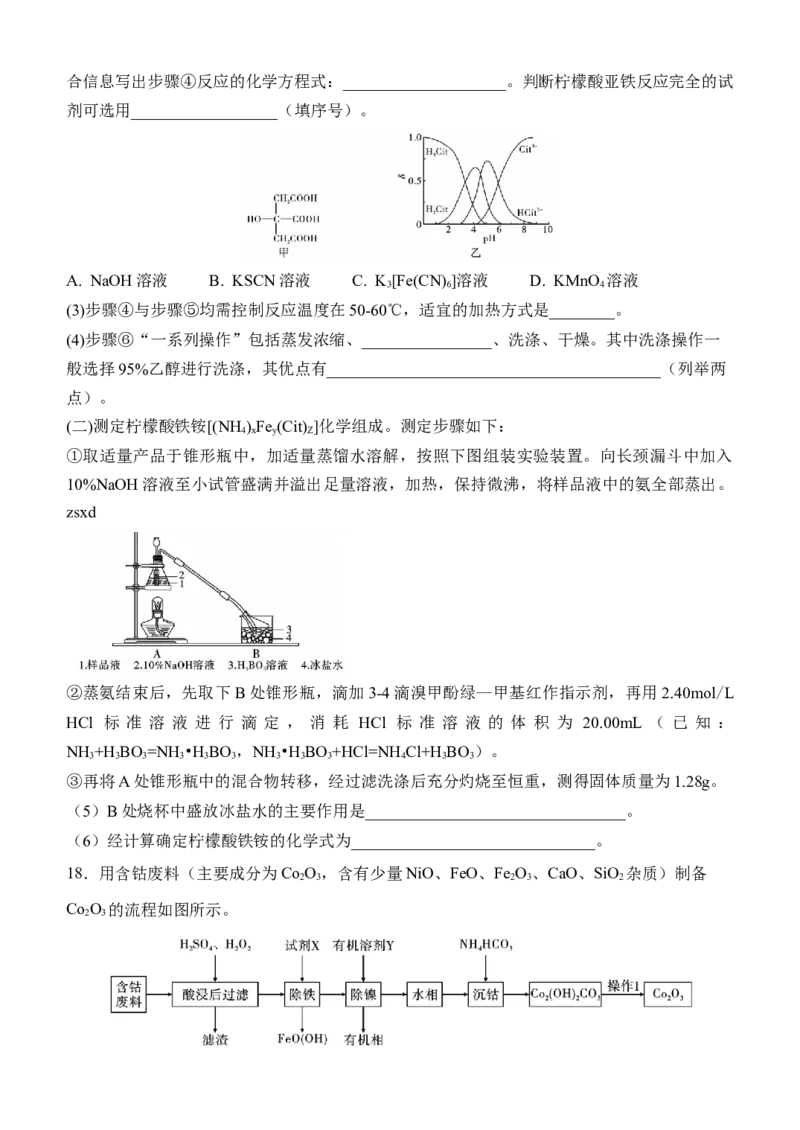
(2)柠檬酸结构(简写为HCit)及其水溶液中各组组分分布系数δ与pH的关系如下图,请结
3合信息写出步骤④反应的化学方程式:____________________。判断柠檬酸亚铁反应完全的试
剂可选用__________________(填序号)。
A. NaOH溶液 B. KSCN溶液 C. K[Fe(CN) ]溶液 D. KMnO 溶液
3 6 4
(3)步骤④与步骤⑤均需控制反应温度在50-60℃,适宜的加热方式是________。
(4)步骤⑥“一系列操作”包括蒸发浓缩、________________、洗涤、干燥。其中洗涤操作一
般选择95%乙醇进行洗涤,其优点有_________________________________________(列举两
点)。
(二)测定柠檬酸铁铵[(NH )Fe (Cit) ]化学组成。测定步骤如下:
4 x y Z
①取适量产品于锥形瓶中,加适量蒸馏水溶解,按照下图组装实验装置。向长颈漏斗中加入
10%NaOH溶液至小试管盛满并溢出足量溶液,加热,保持微沸,将样品液中的氨全部蒸出。
zsxd
②蒸氨结束后,先取下B处锥形瓶,滴加3-4滴溴甲酚绿—甲基红作指示剂,再用2.40mol/L
HCl 标 准 溶 液 进 行 滴 定 , 消 耗 HCl 标 准 溶 液 的 体 积 为 20.00mL ( 已 知 :
NH +H BO=NH•HBO,NH •HBO+HCl=NH Cl+H BO)。
3 3 3 3 3 3 3 3 3 4 3 3
③再将A处锥形瓶中的混合物转移,经过滤洗涤后充分灼烧至恒重,测得固体质量为1.28g。
(5)B处烧杯中盛放冰盐水的主要作用是________________________________。
(6)经计算确定柠檬酸铁铵的化学式为______________________________。
18.用含钴废料(主要成分为Co O,含有少量NiO、FeO、Fe O、CaO、SiO 杂质)制备
2 3 2 3 2
Co O 的流程如图所示。
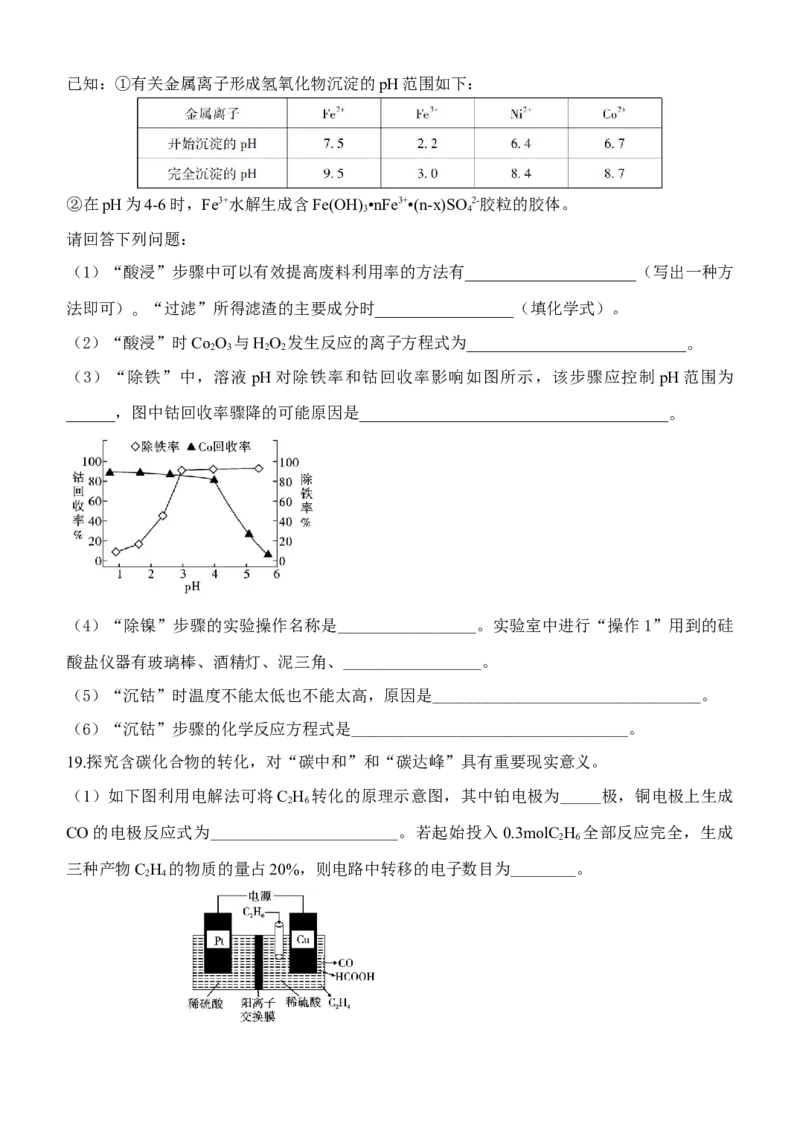
2 3已知:①有关金属离子形成氢氧化物沉淀的pH范围如下:
②在pH为4-6时,Fe3+水解生成含Fe(OH) •nFe3+•(n-x)SO2-胶粒的胶体。
3 4
请回答下列问题:
(1)“酸浸”步骤中可以有效提高废料利用率的方法有_____________________(写出一种方
法即可)。“过滤”所得滤渣的主要成分时_________________(填化学式)。
(2)“酸浸”时Co O 与HO 发生反应的离子方程式为___________________________。
2 3 2 2
(3)“除铁”中,溶液pH对除铁率和钴回收率影响如图所示,该步骤应控制pH范围为
______,图中钴回收率骤降的可能原因是______________________________________。
(4)“除镍”步骤的实验操作名称是_________________。实验室中进行“操作1”用到的硅
酸盐仪器有玻璃棒、酒精灯、泥三角、_________________。
(5)“沉钴”时温度不能太低也不能太高,原因是_________________________________。
(6)“沉钴”步骤的化学反应方程式是__________________________________。
19.探究含碳化合物的转化,对“碳中和”和“碳达峰”具有重要现实意义。
(1)如下图利用电解法可将C H 转化的原理示意图,其中铂电极为_____极,铜电极上生成
2 6
CO的电极反应式为_______________________。若起始投入0.3molC H 全部反应完全,生成
2 6
三种产物C H 的物质的量占20%,则电路中转移的电子数目为________。
2 4(2)总浓度为c mol•L-1的CO 和H 混合气体,按n(CO):n(H )=1:3投料,催化发生反应:
2 2 2 2
2CO(g)+6H(g)=C H(g)+4HO(g) △H<0。恒容条件下,各物质平衡浓度
2 2 2 4 2
与温度的变化关系如图所示:
①曲线b代表__________(填化学式);
②A点时,HO的产率为__________(用c、c表示,化为最简整数比)。
2 o
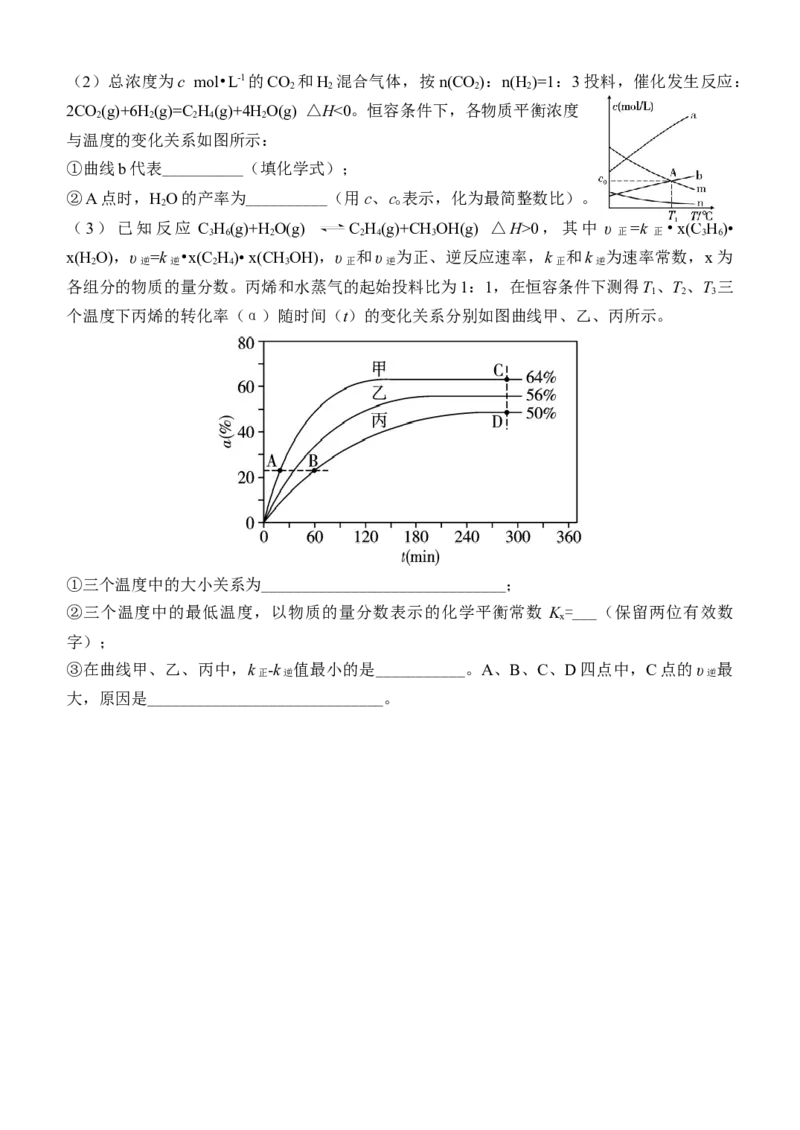
(3)已知反应 C H(g)+HO(g) C H(g)+CH OH(g) △H>0,其中 υ =k •x(C H)•
3 6 2 2 4 3 正 正 3 6
x(HO),υ =k •x(C H)• x(CHOH),υ 和υ 为正、逆反应速率,k 和k 为速率常数,x为
2 逆 逆 2 4 3 正 逆 正 逆
各组分的物质的量分数。丙烯和水蒸气的起始投料比为1:1,在恒容条件下测得T、T、T 三
1 2 3
个温度下丙烯的转化率(α)随时间(t)的变化关系分别如图曲线甲、乙、丙所示。
①三个温度中的大小关系为______________________________;
②三个温度中的最低温度,以物质的量分数表示的化学平衡常数 K =___(保留两位有效数
x
字);
③在曲线甲、乙、丙中,k -k 值最小的是___________。A、B、C、D四点中,C点的υ 最
正 逆 逆
大,原因是_____________________________。