文档内容
2023 届 雅礼中学化学试卷(六)
时量:75分钟 满分:100分
可能用到的相对原子质量:H~1 C~12 N~14 O~16 F~19 Na~23 Al~27 Si~28 S~32
Cl~35.5 Ca~40 Fe~56 Ba~137
第Ⅰ卷(选择题 共42分)
一、选择题(本题共14小题,每小题3分,共42分,每小题只有一个选项符合题意。)
1.成语、古诗词、谚语等都是我国传统文化的瑰宝。下列有关解读错误的是( )
A.“水滴石穿”过程中发生了化学变化
B.“雨过天晴云破处,这般颜色做将来”所描述的瓷器青色,不是来自氧化铁
C.“三月打雷麦谷堆”是指在雷电作用下,N 最终转化成被作物吸收的化合态氮
2
D.“日照香炉生紫烟”描述的是碘的升华
2.N 为阿伏加德罗常数的值,下列说法错误的是( )
A
A.已知11B4 HeR1H,14gR含有的中子数为8N
5 2 1 A
B.0.4mol联氨(N H )中含有共价键数目为2N
2 4 A
C.138gNO 与H O完全反应时转移的电子数为3N
2 2 A
D.常温下,1LpH=12的CH COONa溶液中,H O电离出的OH数为0.01N
3 2 A
3.周期表中第ⅥA族元素及其化合物应用广泛。用硫黄熏蒸中药材的传统由来已久;H S是一种易燃的有
2
毒气体(燃烧热为562.2kJmol1),可制取各种硫化物;硫酸、硫酸盐是重要化工原料;硫酰氯(SO Cl )
2 2
是重要的化工试剂,常作氯化剂或氯磺化剂。硒( Se)和碲( Te)的单质及其化合物在电子、冶金、材
34 52
料等领域有广阔的发展前景,工业上以精炼铜的阳极泥(含CuSe)为原料回收Se,以电解强碱性Na TeO
2 3
溶液制备Te。下列化学反应表示正确的是( )
A.H S的燃烧:2H S(g)3O (g) 2SO (g)2H O(g) H 1124.4kJmol1
2 2 2 2 2
B.SO Cl 遇水强烈水解生成两种强酸:SO Cl 2H O 4H SO2 2Cl
2 2 2 2 2 3
C.电解强碱性Na TeO 溶液的阴极反应:TeO2 4e 3H O Te6OH
2 3 3 2
D.CuSe和浓硝酸反应:CuSe2HNO Cu(NO ) H Se
3 3 2 2
4.某100mL溶液可能含有Na+、NH、Fe3+、CO2、SO2、Cl中的若干种,取该溶液进行连续实验,实
4 3 4
验过程如图(所加试剂均过量,气体全部逸出)。下列说法正确的是( )
A.原溶液可能存在Cl和Na+
B.原溶液一定存在CO2、SO2和NH,一定不存在Fe3+、Na+、Cl
3 4 4C.原溶液中c(CO2)是0.01molL1
3
D.若原溶液中不存在Na+,则c(Cl)0.1molL1
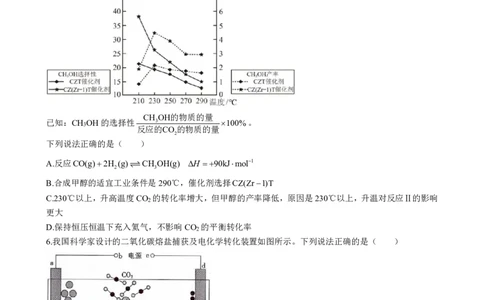
5.恒压条件下,密闭容器中将CO 、H 按照体积比为1:3合成CH OH,其中涉及的主要反应如下:
2 2 3
Ⅰ.CO (g)3H (g)CH OH(g)H O(g) H 49kJmol1
2 2 3 2 1
Ⅱ.CO (g)H (g)CO(g)H O(g) H 41kJmol1
2 2 2 2
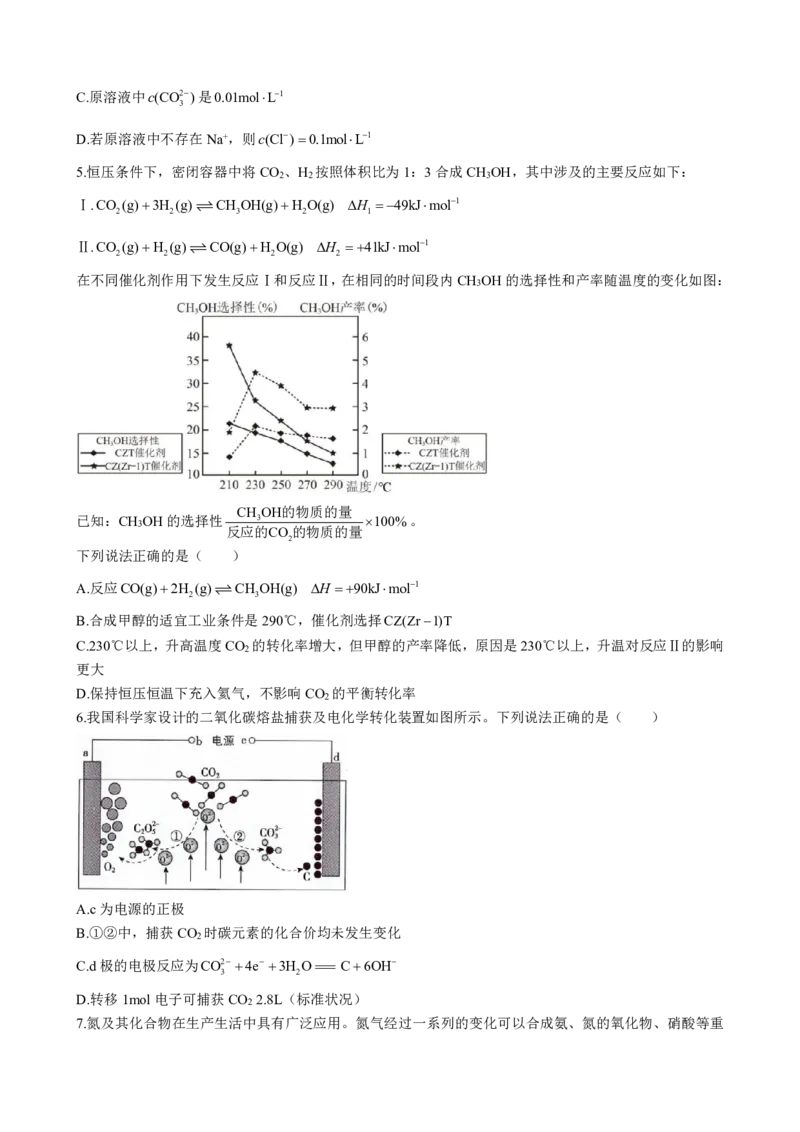
在不同催化剂作用下发生反应Ⅰ和反应Ⅱ,在相同的时间段内CH OH的选择性和产率随温度的变化如图:
3
CH OH的物质的量
已知:CH OH的选择性 3 100%。
3
反应的CO的物质的量
2
下列说法正确的是( )
A.反应CO(g)2H (g)CH OH(g) H 90kJmol1
2 3
B.合成甲醇的适宜工业条件是290℃,催化剂选择CZ(Zr1)T
C.230℃以上,升高温度CO 的转化率增大,但甲醇的产率降低,原因是230℃以上,升温对反应Ⅱ的影响
2
更大
D.保持恒压恒温下充入氦气,不影响CO 的平衡转化率
2
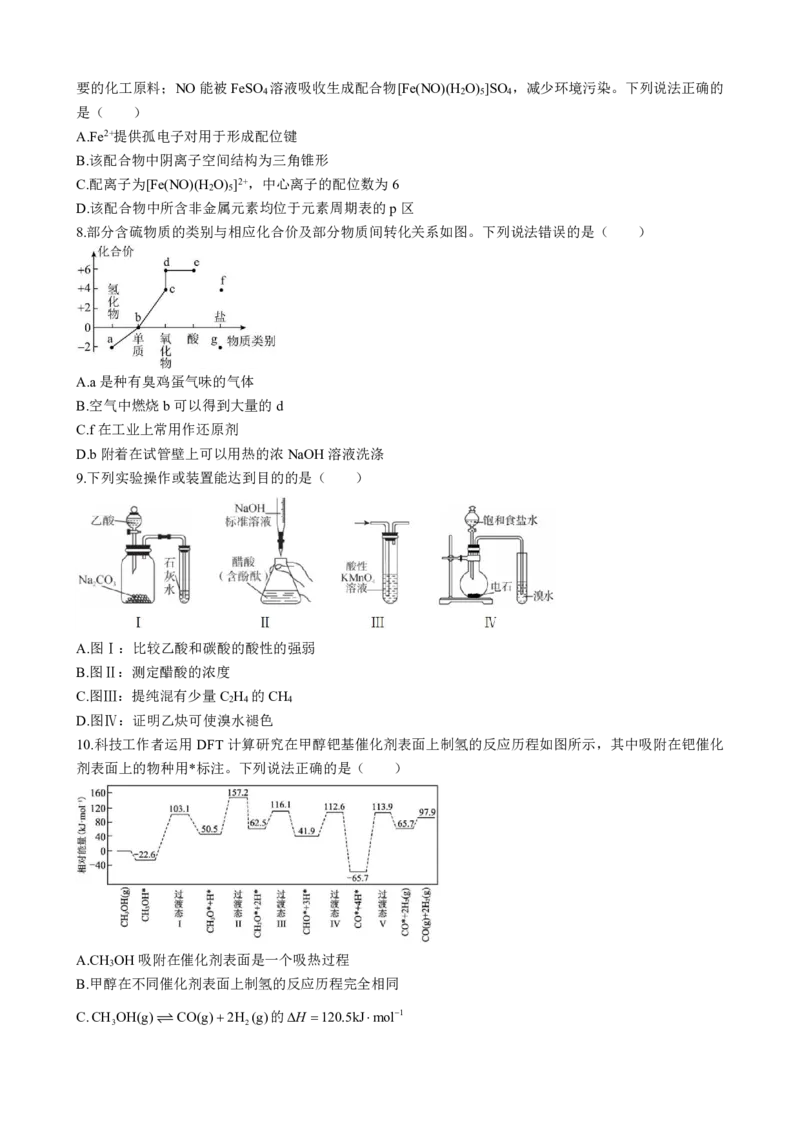
6.我国科学家设计的二氧化碳熔盐捕获及电化学转化装置如图所示。下列说法正确的是( )
A.c为电源的正极
B.①②中,捕获CO 时碳元素的化合价均未发生变化
2
C.d极的电极反应为CO2 4e 3H O C6OH
3 2
D.转移1mol电子可捕获CO 2.8L(标准状况)
2
7.氮及其化合物在生产生活中具有广泛应用。氮气经过一系列的变化可以合成氨、氮的氧化物、硝酸等重要的化工原料;NO能被FeSO 溶液吸收生成配合物[Fe(NO)(H O) ]SO ,减少环境污染。下列说法正确的
4 2 5 4
是( )
A.Fe2+提供孤电子对用于形成配位键
B.该配合物中阴离子空间结构为三角锥形
C.配离子为[Fe(NO)(H O) ]2+,中心离子的配位数为6
2 5
D.该配合物中所含非金属元素均位于元素周期表的p区
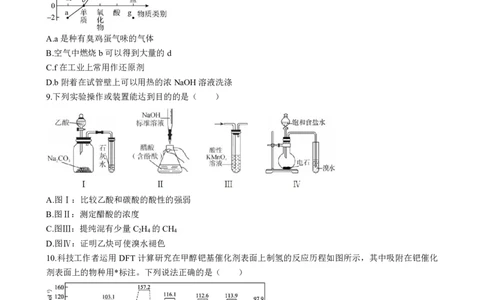
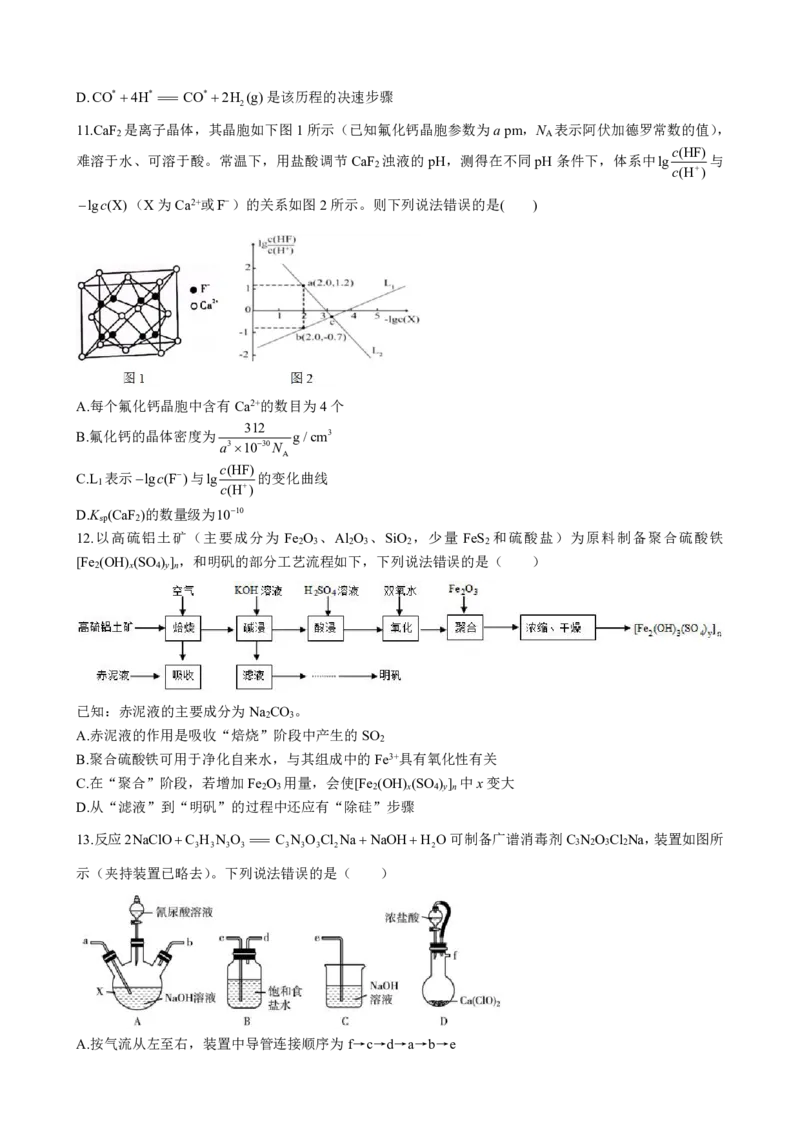
8.部分含硫物质的类别与相应化合价及部分物质间转化关系如图。下列说法错误的是( )
A.a是种有臭鸡蛋气味的气体
B.空气中燃烧b可以得到大量的d
C.f在工业上常用作还原剂
D.b附着在试管壁上可以用热的浓NaOH溶液洗涤
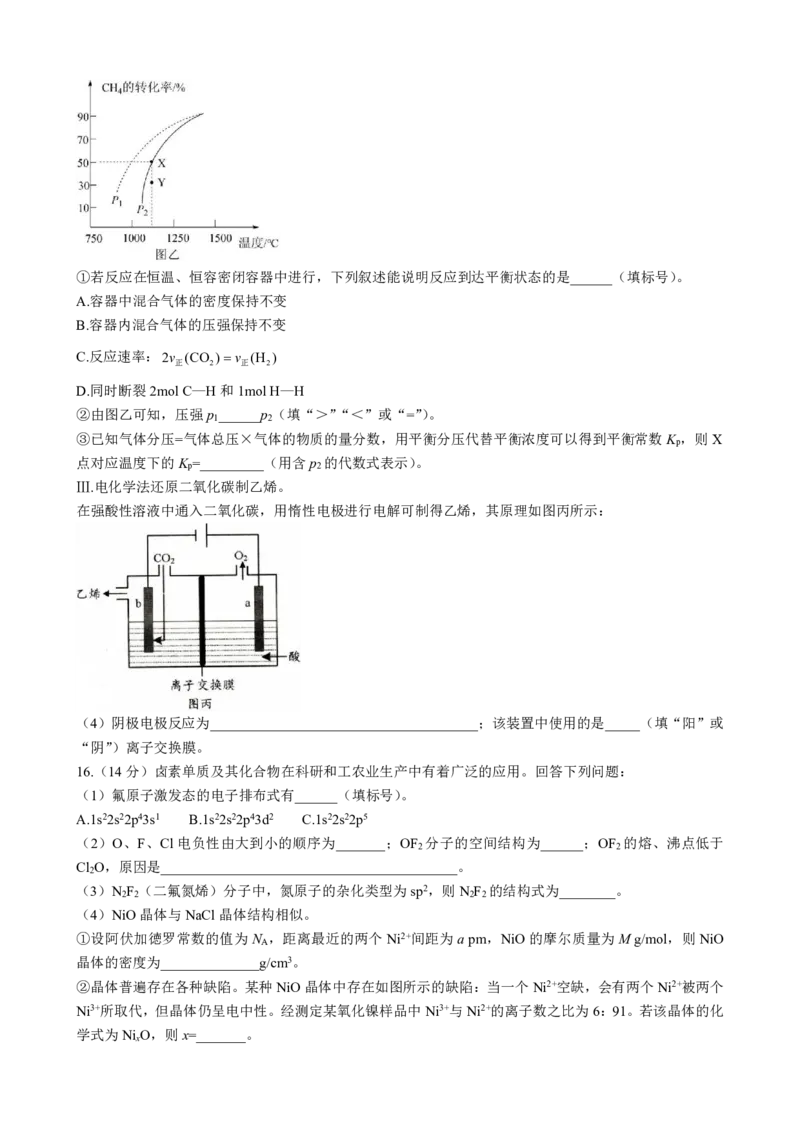
9.下列实验操作或装置能达到目的的是( )
A.图Ⅰ:比较乙酸和碳酸的酸性的强弱
B.图Ⅱ:测定醋酸的浓度
C.图Ⅲ:提纯混有少量C H 的CH
2 4 4
D.图Ⅳ:证明乙炔可使溴水褪色
10.科技工作者运用DFT计算研究在甲醇钯基催化剂表面上制氢的反应历程如图所示,其中吸附在钯催化
剂表面上的物种用*标注。下列说法正确的是( )
A.CH OH吸附在催化剂表面是一个吸热过程
3
B.甲醇在不同催化剂表面上制氢的反应历程完全相同
C.CH OH(g)CO(g)2H (g)的H 120.5kJmol1
3 2D.CO*4H* CO*2H (g)是该历程的决速步骤
2
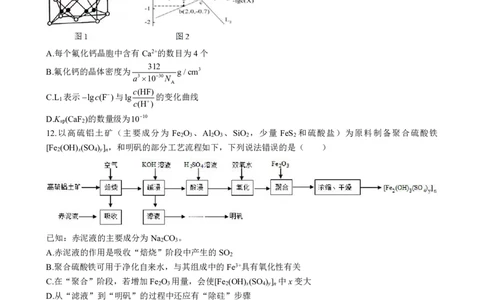
11.CaF 是离子晶体,其晶胞如下图1所示(已知氟化钙晶胞参数为apm,N 表示阿伏加德罗常数的值),
2 A
c(HF)
难溶于水、可溶于酸。常温下,用盐酸调节CaF 浊液的pH,测得在不同pH条件下,体系中lg 与
2 c(H)
lgc(X)(X为Ca2+或F)的关系如图2所示。则下列说法错误的是( )
A.每个氟化钙晶胞中含有Ca2+的数目为4个
312
B.氟化钙的晶体密度为 g/cm3
a31030N
A
c(HF)
C.L 表示lgc(F)与lg 的变化曲线
1 c(H)
D.K (CaF )的数量级为1010
sp 2
12.以高硫铝土矿(主要成分为 Fe O 、Al O 、SiO ,少量 FeS 和硫酸盐)为原料制备聚合硫酸铁
2 3 2 3 2 2
[Fe (OH) (SO ) ] ,和明矾的部分工艺流程如下,下列说法错误的是( )
2 x 4 y n
已知:赤泥液的主要成分为Na CO 。
2 3
A.赤泥液的作用是吸收“焙烧”阶段中产生的SO
2
B.聚合硫酸铁可用于净化自来水,与其组成中的Fe3+具有氧化性有关
C.在“聚合”阶段,若增加Fe O 用量,会使[Fe (OH) (SO ) ] 中x变大
2 3 2 x 4 y n
D.从“滤液”到“明矾”的过程中还应有“除硅”步骤
13.反应2NaClOC H N O C N O Cl NaNaOHH O可制备广谱消毒剂C N O Cl Na,装置如图所
3 3 3 3 3 3 3 2 2 3 2 3 2
示(夹持装置已略去)。下列说法错误的是( )
A.按气流从左至右,装置中导管连接顺序为f→c→d→a→b→eB.升高温度不利于装置A中产品的生成
C.当加入4molNaOH时,最多消耗氰尿酸(C H N O )1mol
3 3 3 3
D.装置D中橡皮管可平衡气压,便于浓盐酸顺利流下
14.X、Y、Z、Q、E、M六种元素中,X的原子的基态价电子排布式为2s2,Y的基态原子核外有5种运动
状态不同的电子,Z元素的两种同位素原子通常作为示踪原子研究生物化学反应和测定文物的年代,Q是
元素周期表中电负性最大的元素,E的阳离子通常存在于硝石、明矾和草木灰中,M的原子序数比E大1。
下列说法正确的是( )
A.EYQ 中阴离子中心原子的杂化方式为sp3杂化
4
B.X、Y元素的第一电离能大小关系:X