文档内容
专项训练 电化学中电极质量、溶液质量变化的计算(解析
版)
1.(2023·全国·高三统考专题练习)科学家设计了一种能产生羟基自由基(·OH)的原电
池—电解池组合装置,·OH能将苯酚氧化为CO 和H O,实现发电、环保二位一体,如
2 2
图所示。下列说法错误的是
A.a极为正极,N为阴离子交换膜
B.d极的电极反应式为H O−e−=· OH+H+
2
C.a极区每产生1molCr(OH) ,c极区溶液质量减轻3g
3
D.b极区消耗1molC H OH,理论上电路中转移电子28mol
6 5
【答案】C
【分析】由图可知,a极上Cr O2-发生还原反应生成Cr(OH) ,b电极上苯酚发生氧化
2 7 3
反应生成CO,则a电极为正极,b电极为负极,正极反应为Cr O2-+6e-
2 2 7
+7H O=2Cr(OH) +8OH-,负极反应为C HOH-28e-+11H O═6CO ↑+28H+;c电极为电解
2 3 6 5 2 2
池阴极,d电极为电解池阳极,阴极反应为2H++2e-=H ↑,阳极反应为HO-e-=H+
2 2
+•OH,羟基自由基(•OH)具有强氧化性,进一步氧化苯酚达到除去苯酚的目的,发生
的反应为C HOH+28•OH═6CO ↑+17H O,据此分析解答。
6 5 2 2
【详解】A.由上述分析可知,左侧装置为原电池,右侧装置为电解池,a电极为正极,
b电极为负极,负极方程式为:C HOH-28e-+11H O═6CO ↑+28H+,阳离子浓度增大,
6 5 2 2
则Cl-通过N膜计入b极区,N为阴离子交换膜,故A正确;
B.d电极为电解池阳极,阳极上HO失电子生成H+、•OH,阳极反应为HO-e-=H+
2 2
+•OH,故B正确;
C.正极反应为Cr O❑ 2− +6e-+7H O=2Cr(OH) +8OH-,a极区每产生1mol Cr(OH) 时转
2 7 2 3 3
移3mol电子,通过质子交换膜移向阴极的n(H+)=3mol,阴极反应为2H++2e-=H ↑,
2
试卷第1页,共27页
学科网(北京)股份有限公司2
1
n(H )=
n(H+)=1.5mol,m(H)=1.5mol×2g/mol=3g,即c极区溶液质量不变,故C错
2 2 2
误;
D.由分析可知,b极区电极方程式为:C HOH-28e-+11H O═6CO ↑+28H+,消耗1mol
6 5 2 2
C H OH,理论上电路中转移电子28mol,故D正确;
6 5
故选C。
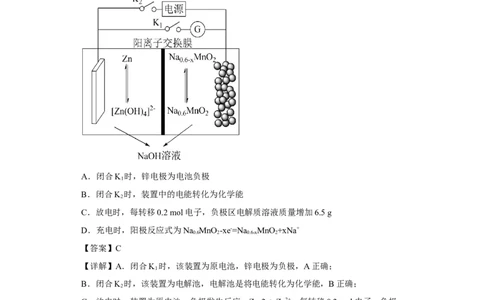
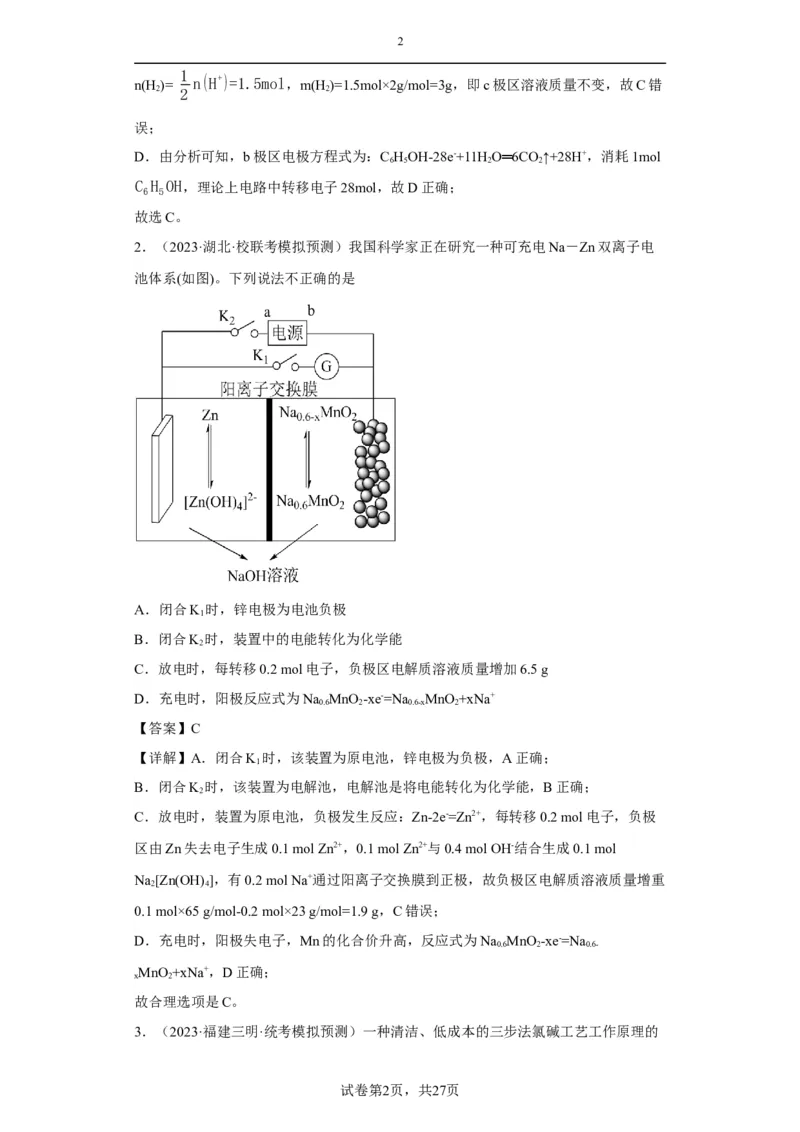
2.(2023·湖北·校联考模拟预测)我国科学家正在研究一种可充电Na-Zn双离子电
池体系(如图)。下列说法不正确的是
A.闭合K 时,锌电极为电池负极
1
B.闭合K 时,装置中的电能转化为化学能
2
C.放电时,每转移0.2 mol电子,负极区电解质溶液质量增加6.5 g
D.充电时,阳极反应式为Na MnO -xe-=Na MnO +xNa+
0.6 2 0.6-x 2
【答案】C
【详解】A.闭合K 时,该装置为原电池,锌电极为负极,A正确;
1
B.闭合K 时,该装置为电解池,电解池是将电能转化为化学能,B正确;
2
C.放电时,装置为原电池,负极发生反应:Zn-2e-=Zn2+,每转移0.2 mol电子,负极
区由Zn失去电子生成0.1 mol Zn2+,0.1 mol Zn2+与0.4 mol OH-结合生成0.1 mol
Na[Zn(OH) ],有0.2 mol Na+通过阳离子交换膜到正极,故负极区电解质溶液质量增重
2 4
0.1 mol×65 g/mol-0.2 mol×23 g/mol=1.9 g,C错误;
D.充电时,阳极失电子,Mn的化合价升高,反应式为Na MnO -xe-=Na
0.6 2 0.6-
MnO +xNa+,D正确;
x 2
故合理选项是C。
3.(2023·福建三明·统考模拟预测)一种清洁、低成本的三步法氯碱工艺工作原理的
试卷第2页,共27页示意图如下,下列说法错误的是
A.第一步中阳极的电极反应式为Na MnO -xe-=Na MnO +xNa+
0.4 2 0.44-x 2
B.第二步中正极质量每增加4.6g,负极质量减少21.6g
C.第三步的总反应为2AgCl=2Ag+Cl ↑
2
D.与传统氯碱工艺相比,该方法不需要使用离子交换膜
【答案】B
【详解】A.第一步为电解池,阳极为与电池正极相连接的电极,失去电子电极反应
为Na MnO -xe-=Na MnO +xNa+ ,故A正确;
0.4 2 0.44-x 2
B.第二步为原电池,正极得到电子电极反应为Na MnO +xNa++xe-=Na MnO ,
0.44-x 2 0.4 2
负极电极反应为Ag+Cl--e-=AgCl↓,正极增加的为钠离子,负极生成的为氯化银是
沉淀,质量增加,故B错误;
C.第三步为电解池,阳极反应为:2Cl--2e-=Cl ↑,阴极反应为:
2
AgCl+e-=Ag+Cl-,总反应为2AgCl=2Ag+Cl ↑,故C正确;
2
D.该方法不需要使用离子交换膜,传统氯碱工艺需要,该方法优点是不需要使用离
子交换膜,故D正确;
故选:B。
4.(2023春·辽宁·高一校联考期中)科学家研发一种“全氢电池”,其工作时原理如
图所示:
试卷第3页,共27页
学科网(北京)股份有限公司4
下列说法错误的是
A.电子移动方向
B.M极电极反应:H −2e−+2OH−=2H O
2 2
C.保证稳定通入H 一段时间后,电流表示数可能归零
2
D.标准状况下,右侧电池产生22.4LH 时,两侧电解质溶液质量差46g
2
【答案】D
【分析】吸附层a吸收H,作负极,发生的电极反应:H −2e−+2OH−=2H O,吸附
2 2 2
层b释放H,作正极,发生的电极反应:2H++2e-=H ↑,离子交换膜为阳离子交换膜,
2 2
钠离子从左边移动到右边,电池的总反应为H++OH-=H O,据此分析解答。
2
【详解】A.电子移动方向,从负极出发通过导线到达正极,A正确;
B.由分析M极电极反应:H −2e−+2OH−=2H O,B正确;
2 2
C.电池的总反应为H++OH-=H O,所以通入H 一段时间后,电流表示数可能归零,C
2 2
正确;
D.由电极反应2H++2e-=H ↑,标准状况下右侧电池产生22.4LH 时转移电子2摩尔,
2 2
所以有2摩尔钠离子通过离子交换膜移动到右侧,右侧质量增加(2×23-1×2)g=44g,
左侧质量减少为(2×23-1×2)g=44g,两侧电解质溶液质量差88g,D错误;
故选D。
5.(2023春·河南·高二洛宁县第一高级中学校联考期中)基于硫化学的金属硫电池是
有望替代当前锂离子电池技术,满足人类社会快速增长的能源需要,该电池的结构及
原理如图所示。下列有关叙述正确的是
试卷第4页,共27页A.该电池可采用含K⁺的水溶液或有机物为电解质溶液
B.放电时,电子的移动方向:电极a→电极b →隔膜→电极a
C.充电时,电路中转移2mole⁻时,负极质量减重78 g
D.充电时,正极区可能发生的反应有 xKS-6e⁻=3S2− +2xK⁺
2 3 x
【答案】D
【详解】A.该电池的负极为金属K,易与H₂O发生反应,不能用含K⁺的水溶液为电
解质溶液,A错误;
B.由分析可知,放电时,电极a为负极,电子从电极a 通过导线流向电极b,在内电
路是K⁺的定向移动形成电流,B错误;
C.充电时,电路中转移2mol e⁻时,负极(即充电时的阴极)发生的反应
为 K++e-=K, 故电极应增重78g,C错误;
D.由分析可知,充电时,电极b接电源的正极,发生氧化反应,其电子反应可能存在
K S -2e-=3S+2K+ 或8K S −10e−=3S2−+16K+
2 3 2 3 8
或 xK S −(2x−6)e-=3S2-+2xK+ 或 4K S −2e- =3S2−+8K+ ,D正确;
2 3 x 2 3 4
故选D。
6.(2023·山东烟台·校联考模拟预测)盐酸羟胺(NH OH⋅HCl)可用作合成抗癌药,其
2
化学性质类似NH Cl。工业上制备盐酸羟胺的装置及含Fe的催化电极反应机理如图。
4
下列说法正确的是
试卷第5页,共27页
学科网(北京)股份有限公司6
A.电子从含Fe的催化电极流出沿导线流入Pt电极
B.电池工作一段时间后,正极区溶液的pH减小
C.电池工作时,当有标准状况下3.36 L H 参与反应,左室溶液质量增加3.3 g
2
D.X为H+和e﹣,Y为NH OH+
3
【答案】C
【分析】由图可知,氢气在Pt电极失电子,Pt电极为负极,电极反应式为H﹣2e﹣=
2
2H+,含Fe的催化电极上NO→NH OH⋅HCl,N元素化合价降低,为正极,电极反应
2
式为NO+3e﹣+4H++Cl﹣=NH OH⋅HCl,据此作答。
2
【详解】A.由分析知,Pt电极为负极,含Fe的催化电极为正极,原电池中电子从负
极流出,流入正极,即电子从Pt电极流出沿导线流入含Fe的催化电极,故A错误;
B.由分析知,含Fe的催化电极为正极,正极电极反应为:NO+3e﹣+4H++Cl﹣=
NH OH⋅HCl,正极区H+浓度减小,pH增大,故B错误;
2
C.由分析知,负极上H~2e﹣,正极上NO~3e﹣,当有标准状况下3.36LH (即
2 2
0.15molH)参与反应时,根据得失电子守恒可知,左室中含Fe的催化电极上参与反应
2
的NO为0.1mol,电极反应式为NO+3e﹣+4H++Cl﹣=NH OH⋅HCl,左室增加的质量为
2
0.1molNO和从右室迁移过来的0.3mol H+的质量,即0.1mol×30g/mol+0.3mol×1g/mol=
3.3g,故C正确;
D.由题意“盐酸羟胺(NH OH⋅HCl)的化学性质类似NH Cl”可知,NH OH具有和氨气
2 4 2
类似的弱碱性,可以和盐酸反应生成盐酸羟胺(NH OH⋅HCl),所以图中缺少的一步
2
反应为NH OH+H+=NH OH+,图2中则X为H+,Y为NH OH+,故D错误;
2 3 3
故选:C。
7.(2023·全国·模拟预测)某课题组设计了一种新型的A位K/Na掺杂
Ni−Co−Zn−Mn钙钛矿氟化物(K/Na-NCZMF)电极材料,并构建了先进的水系锌基电
池,如图所示。下列叙述正确的是
试卷第6页,共27页A.放电时,N极电势高于M极电势
B.放电时,Mn O 转化成MnOOH
3 4
C.充电时,OH−向K/Na-NCZMF极迁移
D.充电时,转移2mol电子理论上N极净增16g
【答案】C
【详解】A.放电时,N极为负极,M极为正极,负极电势低于正极,故A错误;
B.放电时,M极为正极,发生还原反应,锰的化合价降低,MnOOH生成Mn O ,故
3 4
B错误;
C.充电时,M极为阳极。N极为阴极,阴离子向阳极迁移,故C正确;
D.充电时,氧化锌转化成锌,N极质量减轻,故D错误;
故答案选C。
8.(2023·新疆阿勒泰·统考二模)钾氧电池是一种新型金属-空气可充电电池,其使用
双酰亚胺钾( KTFSI)与乙醚(DME)组成的电解液,石墨和液态Na-K合金作为电极,相
关装置如图所示。下列说法错误的是
A.放电时,a为负极,发生氧化反应
B.放电时,正极的电极反应式为K++e- +O =KO
2 2
C.充电时,电流由b电极经电解液流向a电极
D.充电时,b极生成2.24 L(标准状况下)O 时,a极质量增重15.6g
2
【答案】D
【分析】由电路中电子移动方向可知a为负极,b为正极,K在负极失去电子生成
K+,电离方程式为:K-e-=K+,O 在正极得到电子生成KO ,电极方程式为:K++e-
2 2
+O =KO,以此解答。
2 2
试卷第7页,共27页
学科网(北京)股份有限公司8
【详解】A.由分析可知,a为负极,K在负极失去电子生成K+,发生氧化反应,A正
确;
B.由分析可知,b为正极,O 在正极得到电子生成KO ,电极方程式为:K++e-
2 2
+O =KO,B正确;
2 2
C.由分析可知,a为负极,b为正极,充电时,a为阴极,b为阳极,电流由b电极经
电解液流向a电极,C正确;
D.充电时,b为阳极,电极方程式为:KO -e-=K++O ,a为阴极,电极方程式为:K+
2 2
+e-= K,b极生成2.24 L(标准状况下)O 时,O 的物质的量为0.1mol,转移0.1mol电子,
2 2
阴极生成0.1molK,a极质量增重3.9g,D错误;
故选D。
9.(2023·湖北·高三统考专题练习)双极膜是阴、阳复合膜,在直流电的作用下,阴、
阳膜复合层间的H O解离成H+和OH−,作为H+和OH−离子源。利用双极膜制取NaOH和
2
H PO ,产品室1的产品是NaOH,其装置如图所示。
3 4
已知:产品室1的产品是NaOH,则下列说法正确的是
A.a为铅蓄电池的正极,电子由b极流出经装置流入a极
B.膜1为阴离子交换膜,膜2为阳离子交换膜
C.电极Ⅱ的电极反应式为2H O+4e−=O ↑+4H+
2 2
D.若要制60g NaOH,理论上铅蓄电池的负极增重72g
【答案】D
【分析】已知产品室1的产品是NaOH,说明原料室中Na+往左移动,电极Ⅰ是阴极,
a为铅蓄电池的负极,b为铅蓄电池的正极,膜1为阳离子交换膜,HPO❑ −向右移动
2 4
到产品室2中,膜2为阴离子交换膜,双极膜向左解离生成氢离子,从而得到磷酸,
解离生成的氢氧根离子向右移动到电极Ⅱ(阳极)区,阳极发生失电子的氧化反应,
据此分析解答。
【详解】A.根据上述分析可知,a为铅蓄电池的负极,电子由a极流出经装置流入b
极,A错误;
试卷第8页,共27页B.结合上述分析可知,膜1为阴离子交换膜,膜2为阳离子交换膜,B错误;
C.电极Ⅱ为阳极,水发生失电子的氧化反应,其电极反应式为:
2H O−4e−=O ↑+4H+ ,C错误;
2 2
D.铅蓄电池的负极反应为:Pb−2e−+SO2−=PbSO ,当转移2mol电子时,负极增加
4 4
1mol SO2−的质量,即96g,生成的60g NaOH,即为1.5mol,转移的Na+也是1.5mol,
4
电路中转移1.5mol电子,负极增重的质量为72g,故D正确;
故选D。
10.(2023·辽宁·高三统考专题练习)某研究团队发现向锂空气电池
( 放电 )
2Li+O 2 ⇌ Li 2 O 2 的有机电解液中添加LiNO 3 ,充电时可发生如图转化(图中所示不
充电
完全)而使充电过程更稳定。下列说法错误的是
A.电极Li与NO−反应生成NO−和Li O
3 2 2
B.充电时,阳极区域涉及反应:Li O +2NO =2Li++O +2NO−
2 2 2 2 2
C.充电时,每转移1mol电子,阳极质量增加23g
D.放电时,Li+由a极移至b极
【答案】C
【详解】A.电解液中的NO−由Li与NO−反应得来,故电极Li与NO−发生反应:
2 3 3
2Li+NO−
3
¿Li
2
O+NO−
2,A正确;
¿
B.由题图可知,充电时,发生反应:
NO−
2
−e− ¿NO
2和
Li
2
O
2
+2NO
2
¿2Li++O
2
+2NO−
2,
¿ ¿
即在阳极区产生氧气,B正确;
试卷第9页,共27页
学科网(北京)股份有限公司10
C.由B项分析可知,充电时,阳极反应式为
Li
2
O
2
−2e− ¿2Li++O
2
↑
,每转移1mol
¿
电子,阳极消耗0.5molLi O ,质量减少23g,C错误;
2 2
D.由上述分析可知,充电时b为阳极,a为阴极,则放电时a为负极,b为正极,Li+
由负极(a极)移至正极(b极),D正确;
故选C。
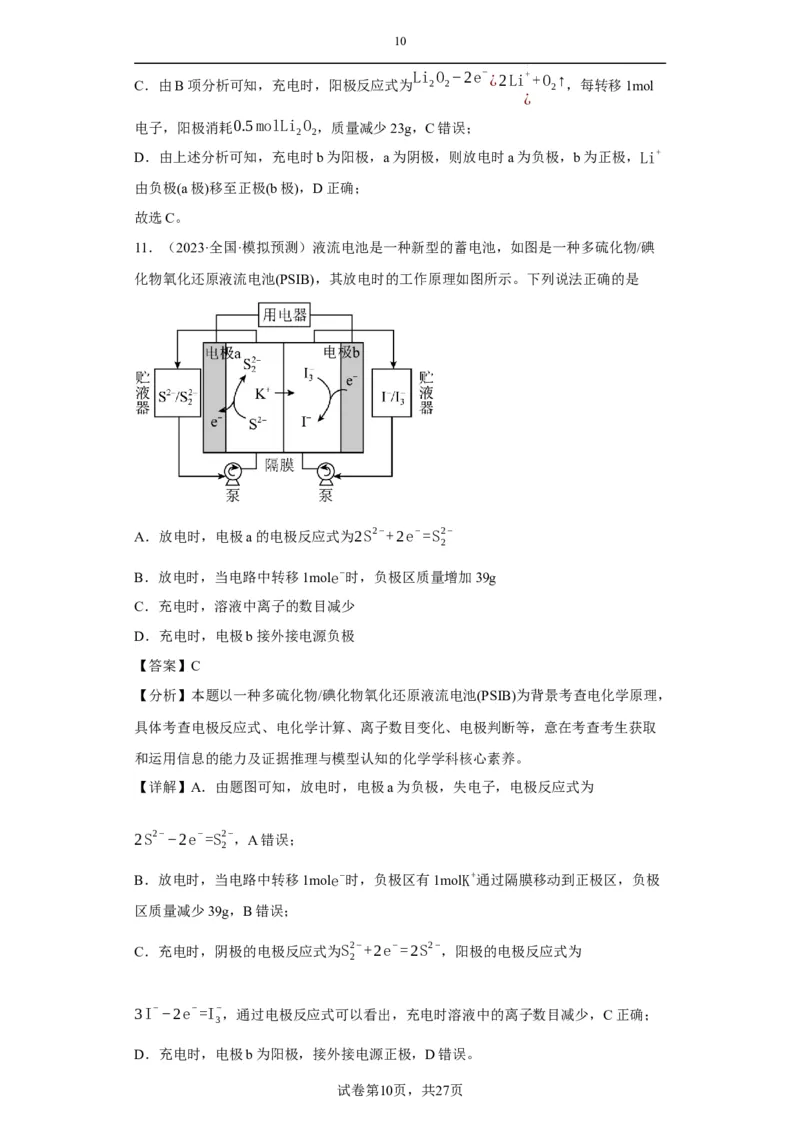
11.(2023·全国·模拟预测)液流电池是一种新型的蓄电池,如图是一种多硫化物/碘
化物氧化还原液流电池(PSIB),其放电时的工作原理如图所示。下列说法正确的是
A.放电时,电极a的电极反应式为2S2−+2e−=S2−
2
B.放电时,当电路中转移1mole−时,负极区质量增加39g
C.充电时,溶液中离子的数目减少
D.充电时,电极b接外接电源负极
【答案】C
【分析】本题以一种多硫化物/碘化物氧化还原液流电池(PSIB)为背景考查电化学原理,
具体考查电极反应式、电化学计算、离子数目变化、电极判断等,意在考查考生获取
和运用信息的能力及证据推理与模型认知的化学学科核心素养。
【详解】A.由题图可知,放电时,电极a为负极,失电子,电极反应式为
2S2−−2e−=S2−
,A错误;
2
B.放电时,当电路中转移1mole−时,负极区有1molK+通过隔膜移动到正极区,负极
区质量减少39g,B错误;
C.充电时,阴极的电极反应式为S2−+2e−=2S2−,阳极的电极反应式为
2
3I−−2e−=I−
,通过电极反应式可以看出,充电时溶液中的离子数目减少,C正确;
3
D.充电时,电极b为阳极,接外接电源正极,D错误。
试卷第10页,共27页故选C。
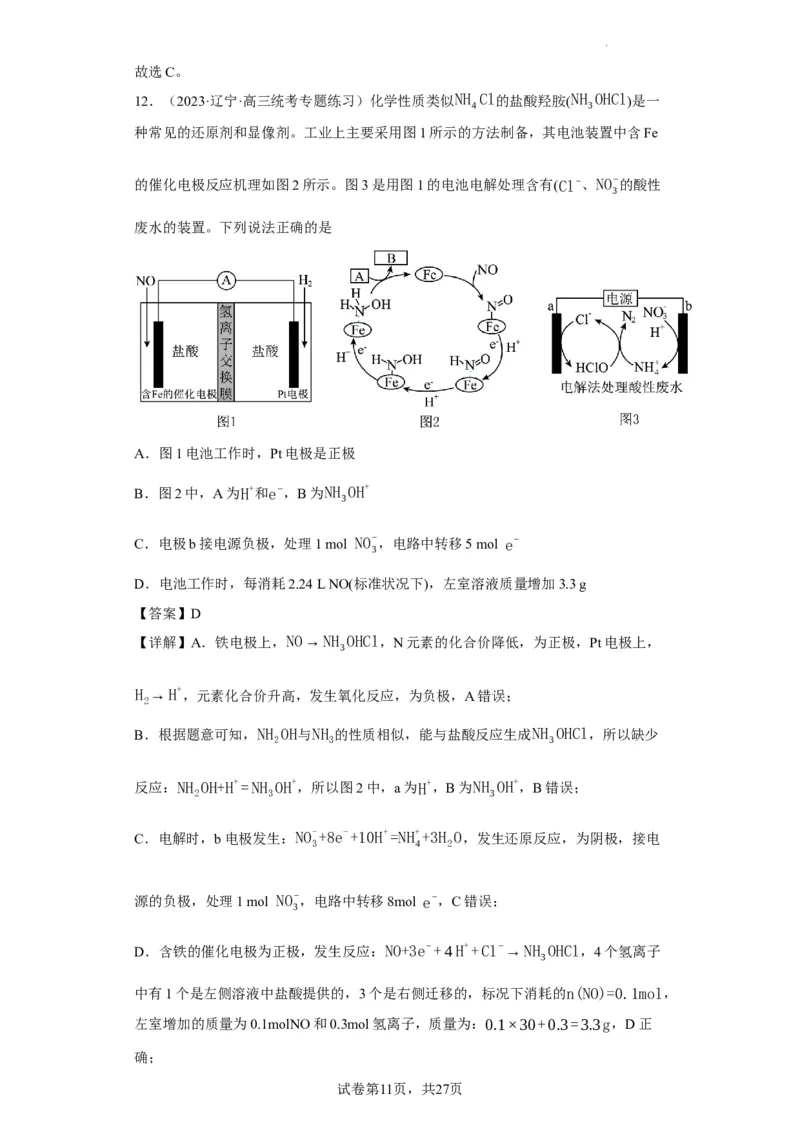
12.(2023·辽宁·高三统考专题练习)化学性质类似NH Cl的盐酸羟胺(NH OHCl)是一
4 3
种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe
的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有(Cl−、NO−的酸性
3
废水的装置。下列说法正确的是
A.图1电池工作时,Pt电极是正极
B.图2中,A为H+和e−,B为NH OH+
3
C.电极b接电源负极,处理1 mol NO−,电路中转移5 mol e−
3
D.电池工作时,每消耗2.24 L NO(标准状况下),左室溶液质量增加3.3 g
【答案】D
【详解】A.铁电极上,NO→NH OHCl,N元素的化合价降低,为正极,Pt电极上,
3
H →H+ ,元素化合价升高,发生氧化反应,为负极,A错误;
2
B.根据题意可知,NH OH与NH 的性质相似,能与盐酸反应生成NH OHCl,所以缺少
2 3 3
反应:NH OH+H+=NH OH+,所以图2中,a为H+,B为NH OH+ ,B错误;
2 3 3
C.电解时,b电极发生:NO-+8e-+10H+=NH++3H O,发生还原反应,为阴极,接电
3 4 2
源的负极,处理1 mol NO−,电路中转移8mol e−,C错误;
3
D.含铁的催化电极为正极,发生反应:NO+3e−+4H++Cl−→NH OHCl,4个氢离子
3
中有1个是左侧溶液中盐酸提供的,3个是右侧迁移的,标况下消耗的n(NO)=0.1mol,
左室增加的质量为0.1molNO和0.3mol氢离子,质量为:0.1×30+0.3=3.3g,D正
确;
试卷第11页,共27页
学科网(北京)股份有限公司12
故选D。
13.(2023春·四川·高二遂宁中学校考期中)科学家基于Cl 易溶于CCl 的性质,发展
2 4
了一种新型储能氯流电池(如图),其中电极a为NaTi (PO )/Na Ti (PO ) 通过风力发电
2 4 3 3 2 4 3
进行充电时,电极a的反应为NaTi (PO )+2Na++2e-=Na Ti (PO );下列说法错误的是
2 4 3 3 2 4 3
A.放电时,电子的流向:电极a→输电网→电极b
B.充电时,电极b为阳极,发生氧化反应
放电
C.放电时总反应:NaTi 2 (PO 4 ) 3 +2NaCl ¿ Na 3 Ti 2 (PO 4 ) 3 +Cl 2 ↑
¿
D.充电时,每转移0.2mol电子,NaCl溶液质量减少11.7g
【答案】C
【分析】充电时,电极a的反应为NaTi (PO )+2Na++2e-=Na Ti (PO ),a极发生还原反
2 4 3 3 2 4 3
应,a为阴极,b为阳极;那么放电时a为负极、b为正极;
【详解】A.由分析可知,放电时a为负极,则电子的流向为负极流向正极:电极a→
输电网→电极b,A正确;
B.充电时,电极b为阳极,失去电子发生氧化反应,B正确;
C.放电时总反应为NaTi (PO ) 失去电子发生氧化反应生成钠离子、氯气得到电子发
3 2 4 3
放电
生还原反应生成氯离子,总反应为:Na 3 Ti 2 (PO 4 ) 3 +Cl 2 ¿ NaTi 2 (PO 4 ) 3 +2NaCl,C错误;
¿
D.充电时,根据电子守恒可知,2Na+~2e-~2NaCl,每转移0.2mol电子,NaCl溶液质
量减少0.2mol ×58.5g/mol=11.7g,D正确;
故选C。
14.(2023·重庆·高三重庆巴蜀中学校考阶段练习)微信山城学术圈刊登了一种Zn﹣
PbO 电池,电解质为KSO 、HSO 和KOH,通过a和b两种离子交换膜将电解质溶
2 2 4 2 4
液隔开(减少参加电极反应的离子的迁移更有利于放电),形成M、R、N三个电解质溶
液区域,结构示意图如图所示。下列说法正确的是
试卷第12页,共27页A.a为阴离子交换膜,b为阳离子交换膜
B.电池放电后R区域的电解质溶液浓度增大
C.充电时,Zn电极反应为Zn﹣2e﹣+4OH﹣=Zn(OH)❑ 2−
4
D.放电时,消耗13gZn,N区域电解质溶液减少39.2g
【答案】B
【分析】由图可知,原电池工作时,Zn为负极,被氧化生成Zn(OH)2-,PbO 为正极,
4 2
发生还原反应,电解质溶液M为KOH,R为KSO ,N为HSO ,原电池工作时,负
2 4 2 4
极反应为Zn﹣2e﹣+4OH﹣=Zn(OH)2-,则消耗OH﹣,钾离子向正极移动,正极电极反
4
应式为PbO +SO2- +2e﹣+4H+=PbSO+2H O,正极消耗氢离子,阴离子向负极移动,则a
2 4 4 2
是阳离子交换膜,b是阴离子交换膜,在同一闭合回路中电子转移数目相等,结合溶
液酸碱性及电极材料书写电极反应式和总反应的方程式,以此解答该题。
【详解】A.Zn为负极,负极反应为Zn﹣2e﹣+4OH﹣=Zn(OH)2-,则消耗OH﹣,钾离
4
子向正极移动,则a是阳离子交换膜,PbO 为正极,正极电极反应式为PbO +SO2- +2e
2 2 4
﹣+4H+=PbSO+2H O,消耗H+的物质的量为SO2-的4倍,则SO2-离子向负极移动,b是
4 2 4 4
阴离子交换膜,A错误;
B.原电池工作时,负极反应为Zn﹣2e﹣+4OH﹣=Zn(OH)2-,则消耗OH﹣,钾离子向正
4
试卷第13页,共27页
学科网(北京)股份有限公司14
极移动,正极电极反应式为PbO +SO2- +2e﹣+4H+=PbSO+2H O,正极消耗氢离子,阴
2 4 4 2
离子向负极移动,电池放电后R区域的电解质溶液浓度增大,B正确;
C.充电时,Zn为阴极,Zn电极反应为Zn(OH)2- +2e﹣=Zn+4OH﹣,C错误;
4
D.13gZn的物质的量为0.2mol,负极反应为Zn﹣2e﹣+4OH﹣=Zn(OH)2-,电路中转移
4
电子0.4mol,N区域转移0.2molSO2-,正极反应为PbO +SO2- +2e﹣
4 2 4
+4H+=PbSO+2H O,电路中转移电子0.4mol,消耗0.2molSO2-,溶液中增加0.4molO
4 2 4
原子,所以N区域电解质溶液减少的质量为0.4mol×96g/mol﹣0.4mol×16g/mol=32.0g,
D错误;
故选B。
【点睛】根据电极材料金属的活泼性判断出正负极,书写出电极反应,从而可以确定
各区域的电解质溶液种类,根据阴阳离子的移动方向可以确定离子交换膜种类,进行
电解质溶液质量计算时要综合考虑离开体系和进入体系的粒子。
15.(2023·全国·高三专题练习)电化学合成是种环境友好的化学合成方法 ,以对硝
基苯甲酸( )为原料,采用电解法合成对氨基苯甲酸
( ) 的装置如图所示。下列说法正确的是
A.a极电势低于b极电势
B.离子交换膜为阴离子交换膜
C.每生成0.2mol对氨基苯甲酸,阳极室电解液质量减少10.8 g
D.生成 的 总反应为:
试卷第14页,共27页【答案】C
【详解】A.根据装置示意图可知,碘单质在N极得电子生成碘离子,故N极为阴极,
b极为负极,则a极电势高于b极电势,A错误;
B.对硝基苯甲酸转化成对氨基苯甲酸需要氢离子,故离子交换膜为阳离子交换膜,B
错误;
C.每生成0.2mol对氨基苯甲酸需要1.2molI-和1.2molH+,根据电极反应式I+2e-=2I-可
2
知电路中要转移1.2mol电子,阳极发生反应2HO-4e-=O ↑+4H+,阳极要产生
2 2
0.3molO,迁移向N极1.2molH+,阳极室电解质液质量减少10.8g, C正确;
2
D.生成对氨基苯甲酸的总反应为: +6I-+6H+=
+3I +2H O,D错误;
2 2
答案选C。
16.(2023·高二课时练习)内重整碳酸盐燃料电池(熔融Li CO 和K CO 为电解质)的
2 3 2 3
原理如图所示,下列说法不正确的是
A.常温下,1mol甲烷参加反应正极需要通入2molO
2
B.以甲烷为燃料气时,负极反应式为CH −8e−+4CO2−=5CO +2H O
4 3 2 2
C.该电池使用过程中需补充CO2−
3
D.以此电池为电源精炼铜,当有0.2mole−转移时,阴极增重6.4g
【答案】C
【详解】A. 常温下,负极电极反应式:CH+4 - 8e - =5CO +2H O,1mol甲烷
4 CO2− 2 2
3
参加反应,转移的电子数为8mol,正极电极反应式O+4e- +2CO =2 ,需要通入
2 2 CO2-
3
试卷第15页,共27页
学科网(北京)股份有限公司16
2molO ,故A正确;
2
B. 若以甲烷为燃料气时负极电极反应式为CH+4CO2− - 8e - =5CO +2H O,故B正
4 3 2 2
确;
C.
总反应为燃料和氧气反应,所以使用过程中不需补充CO2−,故C错误;
3
D. 以此电池为电源精炼铜,阴极电极反应Cu2++2e-=Cu,当有0.2mole−转移时,增重
6.4g,故D正确;
选D。
17.(2023·河北石家庄·高三专题练习)我国科学家研发了一种水系可逆Zn-CO 电池,
2
电池工作原理如图所示,电极材料为金属锌和选择性催化材料,图中的双极膜层间的
HO解离成H+和OH-,并在直流电场作用下分别向两极迁移。下列说法正确的是
2
A.电解质溶液2一定是碱性溶液
B.充电时,每生成标况下11.2 L O 在阳极可生成65 g Zn
2
C.放电时,1 mol CO 转化为HCOOH,转移的电子数为2N
2 A
D.放电时,电池总反应为2Zn+ O+ 4OH-+ 2H O= 2Zn(OH) 2-
2 2 4
【答案】C
【分析】由图可知,放电时,锌为原电池负极,碱性条件下失去电子发生氧化反应生
成四羟基合锌离子,电极反应式为Zn-2e-+4OH-=Zn(OH) 2-,右侧电极为正极,酸性条
4
件下二氧化碳在正极得到电子发生还原反应生成甲酸,电极反应式为CO+2e-
2
+2H+=HCOOH;充电时,锌与直流电源的负极相连,做电解池的阴极,电极反应式为
Zn(OH) 2- +2e-=Zn+4OH-,右侧电极为阳极,水在阳极失去电子发生氧化反应生成氧气
4
和氢离子,电极反应式为2HO-4e-=O ↑+4H+,则电解质溶液1是碱性溶液、电解质溶
2 2
液2是酸性溶液。
试卷第16页,共27页【详解】A.由分析可知电解质溶液2是酸性溶液,A错误;
B.充电时阴极反应式为Zn(OH) 2- +2e-=Zn+4OH-,阳极反应式为2HO-4e-=O ↑+4H+,则
4 2 2
电池总反应式为2Zn(OH) 2- +2H O=2Zn+4OH-+O2↑+4H O。
4 2 2
11.2L
n(O )= =0.5mol,生成1molO 时生成2molZn,则生成0.5molO,生成
2 22.4L/mol 2 2
0.5mol
n(Zn)= ×2mol=1mol,m(Zn)=1mol×65g/mol=65g,则阴极上生成65gZn,B
1mol
错误;
C.放电时,正极反应式为CO+2e-+2H+=HCOOH,则1molCO 转化为HCOOH转移电
2 2
子的物质的量为2mol,转移电子数为2N ,C正确;
A
D.放电时,负极反应式为Zn-2e-+4OH-=Zn(OH) 2-、正极反应式为CO+2e-
4 2
+2H+=HCOOH,则电池总反应式为Zn+CO +2OH-+2H O=Zn(OH) 2- +HCOOH,D错误;
2 2 4
故选C。
18.(2023春·宁夏石嘴山·高二平罗中学校考阶段练习)利用电化学原理可将CO 电催
2
化还原为C H ,装置如图所示。下列说法正确的是
2 4
A.玻碳电极连接电源的负极
B.若有2mol电子通过外电路,玻碳电极上生成11.2LO
2
C.若有1mol电子通过外电路,理论上右侧溶液质量减少9g
D.阴极电极反应只有2CO +12H++12e−=C H +4H O
2 2 4 2
【答案】C
【分析】由图示可知,玻碳电极发生的电极反应为: ,为阳极
2H O−4e−=O ↑+4H+
2 2
反应故应连接电源的正极,则铂电极为阴极,电极反应除了
试卷第17页,共27页
学科网(北京)股份有限公司18
,还有 。
2CO +12H++12e−=C H +4H O AgCl+e−=Ag+Cl−
2 2 4 2
【详解】A.由图示可知,玻碳电极发生的电极反应为:2H O−4e−=O ↑+4H+ ,为
2 2
阳极反应故应连接电源的正极,故A错误;
B.没有说明标准状况,故B错误;
C.若有1mol电子通过外电路,右侧发生的电极反应2H O−4e−=O ↑+4H+ ,理论上
2 2
减少了0.25molO ,另有1molH+通过质子交换膜迁移到阴极区,故理论上右侧溶液质
2
量减少9g,故C正确;
D.阴极电极反应除了2CO +12H++12e−=C H +4H O,还有AgCl+e−=Ag+Cl−,
2 2 4 2
故D错误。
故选C。
19.(2023·天津和平·耀华中学校考一模)近期,科学家研发出了一种新型铝电池。该
电池电极分别为铝和硒,熔盐电解质由氯化钠(NaCl)、氯化钾(KCl)和氯化铝( AlCl )组
3
成(如图所示)。其中,电池放电过程中会形成Al Cl− ,放电总反应的离子方程式为
n 3n+1
2Al+3Se=Al Se .下列说法错误的是
2 3
A.充电时,电极Al为阴极
B.放电时,Al电极附近的阴离子浓度降低
C.放电时,电路中每转移1 mol电子,理论上正极质量增加9 g
D.充电时,阳极的电极反应式为(n-1)Al-3(n-1)e-+(3n+1)AlCl-=4Al Cl-
4 n 3n+1
【答案】D
【分析】放电总反应的离子方程式为2Al+3Se=Al Se ,则反应中铝发生氧化反应为负
2 3
极、惰性电极为正极;
【详解】A.放电时铝发生氧化反应为负极,则充电时,电极Al为阴极,故A正确;
试卷第18页,共27页B.电池放电过程中铝极反应为nAl-3ne-+(3n+1)Cl-=Al Cl- ,Al电极附近的阴离
n 3n+1
子浓度降低,故B正确;
C.放电时,电路中每转移1 mol电子,Al∼3e-,结合反应2Al+3Se=Al Se ,则电
2 3
路中每转移1 mol电子,理论上正极质量增加9 g,故C正确;
D.充电时,阳极的电极反应与放电时正极反应有关,反应为
nAl Se -6ne-+2(3n+1)Cl-=2Al Cl- +3nSe,故D错误;
2 3 n 3n+1
故选D。
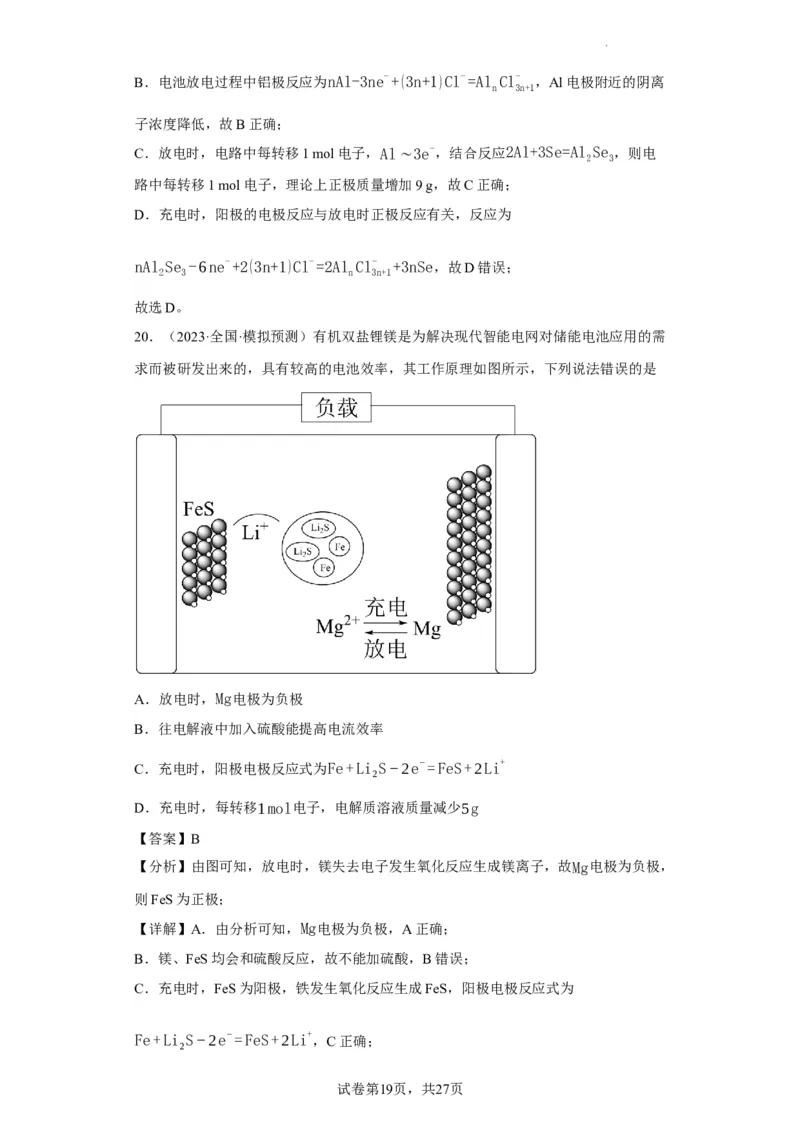
20.(2023·全国·模拟预测)有机双盐锂镁是为解决现代智能电网对储能电池应用的需
求而被研发出来的,具有较高的电池效率,其工作原理如图所示,下列说法错误的是
A.放电时,Mg电极为负极
B.往电解液中加入硫酸能提高电流效率
C.充电时,阳极电极反应式为Fe+Li S−2e−=FeS+2Li+
2
D.充电时,每转移1mol电子,电解质溶液质量减少5g
【答案】B
【分析】由图可知,放电时,镁失去电子发生氧化反应生成镁离子,故Mg电极为负极,
则FeS为正极;
【详解】A.由分析可知,Mg电极为负极,A正确;
B.镁、FeS均会和硫酸反应,故不能加硫酸,B错误;
C.充电时,FeS为阳极,铁发生氧化反应生成FeS,阳极电极反应式为
Fe+Li S−2e−=FeS+2Li+ ,C正确;
2
试卷第19页,共27页
学科网(北京)股份有限公司20
D.充电时,阳极电极反应式为Fe+Li S−2e−=FeS+2Li+ ,阴极反应为
2
Mg2++2e−=Mg,则每转移1mol电子,生成1mol锂离子、消耗0.5mol镁离子,电解
质溶液质量减少12g-7g=5g,D正确;
故选B。
21.(2023·全国·高三专题练习)镁锂双盐电池是结合镁离子电池和锂离子电池而设计
的新型二次离子电池。其工作原理如图所示,已知放电时,b极转化关系为:
VS →Li VS 。下列说法正确的是
2 x 2
A.充电或放电时,a极电势均高于b极
B.放电过程中正极质量减少,负极质量增加
C.充电时阳极的电极反应式为Li VS −xe−=VS +xLi+
x 2 2
D.该电池工作时,若通过电路转移电子的物质的量为0.1mol,则负极质量变化2.4g
【答案】C
【分析】镁锂双盐电池的工作原理为:放电时,电池负极材料金属镁失去电子生成
Mg2+ ,电解液中的Li+得到电子嵌入正极材料,达到电荷平衡;充电时,电池正极材
料中LiVS 失去电子,生成Li+ ,电解液中的Mg2+得到电子沉积到金属镁负极上去,
x 2
再次达到电荷平衡。放电时负极反应为Mg-2e- =Mg2+ ,正极反应为VS +xe-+xLi+
2
=Li VS ,总反应为xMg+ 2VS +2xLi+=2Li VS +xMg2+。
x 2 2 x 2
【详解】A.Mg为负极,VS 为正极,所以充电或放电时,b极电势均高于a极,选项
2
A错误;
B.放电过程中正极质量增加,负极质量减少,选项B错误;
C.充电时,阳极的电极反应式为LiVS - xe- =VS+xLi+ ,选项C正确;
x 2 2
D.该电池负极为Mg电极,通过电路转移电子的物质的量为0.1mol时,负极质量变
化为0.05mol×24g/mol=1.2g,选项D错误;
答案选C。
试卷第20页,共27页22.(2023秋·山东日照·高三统考期末)工业上利用电解含有NaHPbO 的废液回收
2
Pb,装置如图。下列说法错误的是
A.M的电极电势高于N
B.若转移2mol电子,阴极室溶液质量减少207g
C.阴极电极式为HPbO❑ − +2e-+H O=Pb+3OH-
2 2
D.将阳离子交换膜换成阴离子交换膜,对Pb的产率无影响
【答案】B
【分析】左侧电极OH-失去电子生成O,则为阳极,电极反应为4OH-+4e-=O +2H O,
2 2 2
M为正极;右侧电极HPbO❑ −得到电子生成Pb,为阴极,电极反应为HPbO❑ − +2e-
2 2
+H O=Pb+3OH-,N为负极,钠离子由左侧经阳离子交换膜到达右侧,据此解答。
2
【详解】A.根据分析,M为正极,N为负极,M的电极电势高于N,A正确;
B.阴极电极反应为HPbO❑ − +2e-+H O=Pb+3OH-,转移2mol电子,钠离子由左侧经阳
2 2
离子交换膜到达右侧为2mol,阴极室溶液质量减少207g-2mol×23g/mol=161g,B错误;
C.根据分析,阴极电极式为HPbO❑ − +2e-+H O=Pb+3OH-,C正确;
2 2
D.将阳离子交换膜换成阴离子交换膜,多余的氢氧根离子经右侧到达左侧,对Pb的
产率无影响,D正确;
故选B。
23.(2023·全国·高三专题练习)我国某科研机构设计如图所示的电池,利用K Cr O
2 2 7
实现含苯酚废水的有效处理,处理后的废水毒性降低且不引入其他杂质。一段时间后,
中间室中NaCl溶液的浓度减小。下列说法错误的是
试卷第21页,共27页
学科网(北京)股份有限公司22
A.工作时,N极附近溶液的pH增大
B.工作时,每转移3mol电子,N极室和M极室质量变化相差65g
C.a为质子交换膜,b为OH−交换膜
D.N极的电极反应式为Cr O2−+6e−+7H O=2Cr(OH) +8OH−
2 7 2 3
【答案】B
【详解】A.工作时,N极室中的Cr O2−转化为Cr(OH) ,Cr的化合价降低,则N极
2 7 3
为正极,电极反应式为Cr O2−+6e−+7H O═2Cr(OH) +8OH− ,则N极附近溶液的
2 7 2 3
pH增大,A正确;
B.由以上分析可知M极为负极,电极反应式为
C H OH−28e−+11H O═6CO ↑+28H+ ,每转移3mol电子,M极室减少3mol H+和
6 5 2 2
9
mol CO ,质量约31.3g;N极室减少3mol OH−,质量共51g,因此N极室和M极
14 2
室质量变化相差19.7g,B错误;
C.由于该装置的目的是对废水进行有效处理且不引入其他杂质,则M极室生成的H+
应迁移到中间室,a为质子交换膜,N极室生成的OH−迁移到中间室,与H+反应生成
H O,NaCl溶液的浓度减小,b为OH−交换膜,C正确;
2
D.根据A分析,N极为正极,电极反应式为
Cr O2−+6e−+7H O═2Cr(OH) +8OH− ,D正确;
2 7 2 3
故选B。
24.(2023·黑龙江绥化·统考模拟预测)天津大学化学团队以CO 和辛胺为原料实现了
2
甲酸和辛腈的高选择性合成,装置工作原理如图(隔膜a只允许OH−通过,右池反应无
试卷第22页,共27页气体生成)。下列说法错误的是
A.Ni P电极的电势比In/In O 电极的高
2 2 3-x
B.阴极发生的电极反应为CO +2e−+H O=HCOO−+OH−
2 2
C.电解过程中,OH−由In/In O 电极区向Ni P电极区迁移
2 3-x 2
D.当电路中有2mol电子转移时,阳极区液体质量增加10g(不考虑气体的溶解)
【答案】D
【分析】由图中In/In O 电极上CO→HCOO-可知,CO 发生得电子的还原反应,In/
2 3-x 2 2
InO 电极为阴极,阴极反应为:CO+2e-+H O═HCOO-+OH-,则Ni P电极为阳极,辛
2 3-x 2 2 2
胺在阳极上发生失电子的氧化反应生成辛腈,电极反应为CH(CH)CHNH +4OH--4e-
3 2 6 2 2
=CH (CH)CN+4HO,据此分析解答。
3 2 6 2
【详解】A.根据分析,Ni P电极为阳极,连接电源的正极,电势比In/In O 电极
2 2 3-x
的高,A正确;
B.In/In O 电极为阴极,阴极反应为:CO+2e-+H O═HCOO-+OH-,B正确;
2 3-x 2 2
C.电解过程中,阴离子向阳极移动,则OH-由In/In O 电极区向Ni P电极区迁移,C
2 3-x 2
正确;
D.阳极上发生失电子的氧化反应生成辛腈,电极反应为CH(CH)CHNH +4OH--4e-
3 2 6 2 2
=CH (CH)CN+4HO,当电路中有2mol电子转移时,阳极区液体质量增加2mol氢氧
3 2 6 2
根离子的质量,为2mol×17g/mol=34g,D错误;
故选D。
25.(2023·上海·高三专题练习)电解K MnO 水溶液制备KMnO 的装置如图所示。电
2 4 4
解后测得b极区溶液中溶质的总物质的量增大。下列说法错误的是
试卷第23页,共27页
学科网(北京)股份有限公司24
A.K MnO 水溶液盛放在a极区
2 4
B.离子交换膜为阳离子交换膜
C.当外电路转移2 mol电子时,两极室溶液质量变化相差76 g
D.“电解法”所得副产品可用作“酸性歧化法”制备KMnO 的原料
4
【答案】C
【分析】电解K MnO 水溶液制备KMnO ,阳极反应为:MnO2−−e−=MnO− ,阴极反应
2 4 4 4 4
为:2H O+2e-=H ↑+2OH- ,K+向阴极移动,使KOH物质的量增大,所以b极为阴极,a
2 2
极为阳极;
【详解】A.a极为阳极,K MnO 水溶液盛放在a极区,A正确;
2 4
B.K+通过离子交换膜向阴极移动,所以离子交换膜为阳离子交换膜,B正确;
C.当外电路转移2 mol电子时,阴极反应2H O+2e-=H ↑+2OH-,有2 molK+移向阴极,
2 2
生成1molH ,阴极质量增大39×2−2=76g,阳极质量减少2×39=78g,两极室溶
2
液质量变化相差154 g,C错误;
D.“电解法”所得副产品KOH,可用作“酸性歧化法”制备KMnO 的原料,D正确;
4
故选C。
26.(2022秋·辽宁沈阳·高二东北育才学校校考期末)全固态锂硫电池能量密度高、
成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S 材料,电池反应为
8
16Li+xS =8Li S (2≤x≤8)。下列说法正确的是
8 2 x
试卷第24页,共27页A.电池工作时,正极可发生反应:Li S +2Li++2e−=2Li S
2 4 2 2
B.电池充电时间越长,电池中的Li S 量越多
2 2
C.电解质中加入硫酸能增强导电性
D.电池工作时,外电路中流过0.2mol电子,负极材料减重0.7g
【答案】A
【分析】根据电池反应16Li+xS=8Li S(2≤x≤8)可知负极锂失电子发生氧化反应,电极
8 2 x
反应为: Li-e-=Li+,Li+移向正极,所以a是正极,发生还原反应: S +2e-=S2-,S2-
8 8 8
+2Li+=Li S, 3LiS+2Li++2e-=4Li S, 2LiS+2Li++2e-=3Li S, LiS+2Li++2e-=2Li S
2 8 2 8 2 6 2 6 2 4 2 4 2 2
,根据电极反应式结合电子转移进行计算。
【详解】A.据分析,可知正极发生反应是2LiS+2Li++2e-=3Li S,为分析中的一种,
2 6 2 4
故A正确;
B.充电时a为阳极,与放电时的电极反应相反,则充电时间越长,电池中的LiS 量
2 2
就会越少,故B错误;
C.该电池的负极是金属锂,Li元素较活泼会和硫酸反应生成氢气,电解质中不能加
入硫酸,故C错误;
D.负极反应为:Li-e - =Li +,当外电路流过0. 2mol电子时,消耗的锂为0. 2mol,负
极减重的质量为0. 2mol×7g/mol=1.4g,故D错误;
正确答案是A。
27.(2023·江苏·高三专题练习)用惰性电极电解法制备硼酸[H BO]的工作原理如图
3 3
所示。下列有关说法正确的是
A.1膜为阴离子交换膜
B.电解过程中,b极室溶液的pH会变小,原料室溶液的浓度会降低(忽略溶液体积变
化)
C.产品室中发生的反应是B(OH)❑ − +H+=H BO+H O,硼酸为三元酸
4 3 3 2
D.每转移电子1mol,a极室溶液质量变化与b极室溶液质量变化之差为13g
【答案】D
试卷第25页,共27页
学科网(北京)股份有限公司26
【分析】由图可知,b电极为阳极,电解时阳极上水失电子生成O 和H+,a电极为阴
2
极,电解时阴极上水得电子生成H 和OH-,原料室中的Na+通过阳膜1进入a极室,溶
2
液中氢氧化钠浓度增大,原料室中B(OH)❑ −通过阴膜2进去产品室,b极室中氢离子
4
通入阳膜3进入产品室,B(OH)❑ −和H+发生反应生成HBO;a、b电极反应式分别为
4 3 3
2H O+2e-=H ↑+2OH- 、2H O-4e-=O ↑+4H+ 。
2 2 2 2
【详解】A.原料室中的Na+通过膜1进入a极室,所以1膜为阳离子交换膜,A错误;
B.原料室中B(OH)❑ −通过阴膜2进去产品室,b极室中氢离子通入阳膜3进入产品室,
4
B(OH)❑ −和H+发生反应生成HBO,所以pH基本不变,B错误;
4 3 3
C.硼酸为一元酸,C错误;
D.每转移电子1mol,则有1molNa+移向NaOH溶液,同时有0.5molH 生成,a极室溶
2
液质量增加22g,b极室生成0.25molO,同时1molH+移向产品室,b极室溶液质量减
2
少9g,所以a极室溶液质量变化与b极室溶液质量变化之差为13g,D正确;
故选D。
28.(2022秋·江苏·高三校联考阶段练习)利用垃圾假单胞菌株分解有机物的电化学
原理如图所示。下列说法正确的是
A.电子流向:电极B→负载→电极A
B.电极A上的反应式为:X−4e−=Y+4H+
C.若有机物为葡萄糖,处理0.25mol有机物,电路中转移电子6mol
D.若B电极上消耗标准状况下氧气22.4L,B电极区域溶液增重32g
【答案】C
【详解】A.由题中信息可知该装置为原电池,A为负极,B为正极,电子由负极流出
试卷第26页,共27页沿导线流入正极,所以电子流向:电极A→负载→电极B,A错误;
B.观察图中信息知X生成Y少了2个氢原子,化合价升高2,A电极的反应式为:
X−2e−=Y+2H+,B错误;
C.葡萄糖分子式C H O,反应后生成CO,C元素由0价升高到+4价,处理0.25mol
6 12 6 2
有机物,电路中转移电子0.25mol×4×6=6mol,C正确;
D.B电极上消耗标准状况下氧气22.4L,即消耗1molO ,质量为32g,O+4e-
2 2
+4H+=2H O,为维持电荷守恒,有4molH+由左侧移向右侧,所以B电极区域溶液增重
2
32g+4g=36g,D错误;
故答案选C。
29.(2022秋·福建泉州·高二石狮市第一中学校考阶段练习)一种新型镁硫二次电池
放电时的工作原理如图所示。下列说法正确的是
A.当石墨烯中的S均转化为MgS 时,电路中转移的电子数达到最大值
8
B.离子交换膜应为阴离子交换膜
C.充电时,阴极反应可能发生:Mg2++MgS +2e−=2MgS
2
D.放电时,若电路中转移1mol电子,则正极质量增加12g
【答案】D
【分析】由图可知,放电时,Mg作负极,电极反应式为:Mg-2e-= Mg2+,S作正极,
电极反应分别为:8S+Mg2++2e-=MgS,MgS + 3Mg2+ + 6e- = 4MgS ,Mg2++MgS+2e-
8 8 2 2
=2MgS,充电时,Mg极作阴极,S极作阳极,据此作答。
【详解】A.S作正极,电极反应分别为:8S+Mg2++2e-=MgS,MgS + 3Mg2+ + 6e- =
8 8
4MgS ,
2
Mg2++MgS+2e-=2MgS,故当石墨烯中的S均转化为S2-时,电路中转移的电子数达到最
2
大值,A错误;
B.放电时,负极生成Mg2+,正极消耗Mg2+,故Mg2+从左侧向右侧迁移,使用的隔膜
是阳离子交换膜,B错误;
C.充电时,阴极反应为Mg2++2e-=Mg,C错误;
试卷第27页,共27页
学科网(北京)股份有限公司28
D.正极反应包括:Mg2++MgS+2e-=2MgS,放电时,若电路中转移1mol电子,则正极
2
质量增加0.5mol×24g/mol=12g,D正确;
故本题选D。
30.(2022秋·江西·高三江西省安义中学校联考阶段练习)羟基(·OH)表现出极强的氧
化性。我国科学家设计了一种能将苯酚氧化为CO 和HO的原电池-电解池组合装置
2 2
(如下图所示),该装置能实现发电、环保二位一体。下列说法错误的是
A.该装置不宜在高温条件下运行,且b极为负极,d极为阳极
B.b电极区每产生3molCO ,c电极区溶液质量减轻14g
2
C.d电极的电极反应式:HO-e-=·OH+H+
2
D.工作时,如果II室中NaCl浓度减小,则M为阳离子交换膜
【答案】B
【分析】左侧装置为微生物电池,右侧装置为电解池,放电过程中,苯酚发生氧化反
应,失去电子,故b极为负极,a极为正极,c极为阴极,d极为阳极。
【详解】A.b极有微生物,高温会引起微生物死亡,故不宜高温条件下运行,分析结
果确定b极为负极,d极为阳极,A项正确;
B.c电极为阴极,电极反应为:2HO+2e-=H ↑+2OH-,每消耗2molH O同时有
2 2 2
2molH+从d电极区通过质子交换膜进入c电极区,与OH-反应又生成2molH O,因此不
2
管b电极区有多少CO 生成,c电极区溶液质量始终保持不变,B项错误;
2
C.d电极为阳极,装置图提示电极反应式为:HO-e-=·OH+H+,C项正确;
2
D.a电极反应为: Cr O2−+6e−+7H O=2Cr(OH) +8OH−,Cr O2−必须留存在Ⅰ室
2 7 2 3 2 7
反应,故M只能为阳离子交换膜,Na+将从Ⅱ室进入Ⅰ室,b电极反应为:
C H OH-28e−+11H O=6CO ↑+28H+ ,Cl-将从Ⅱ室进入Ⅲ室,故Ⅱ室NaCl浓度减小,
6 5 2 2
D项正确;
故选B。
试卷第28页,共27页试卷第29页,共27页
学科网(北京)股份有限公司