文档内容
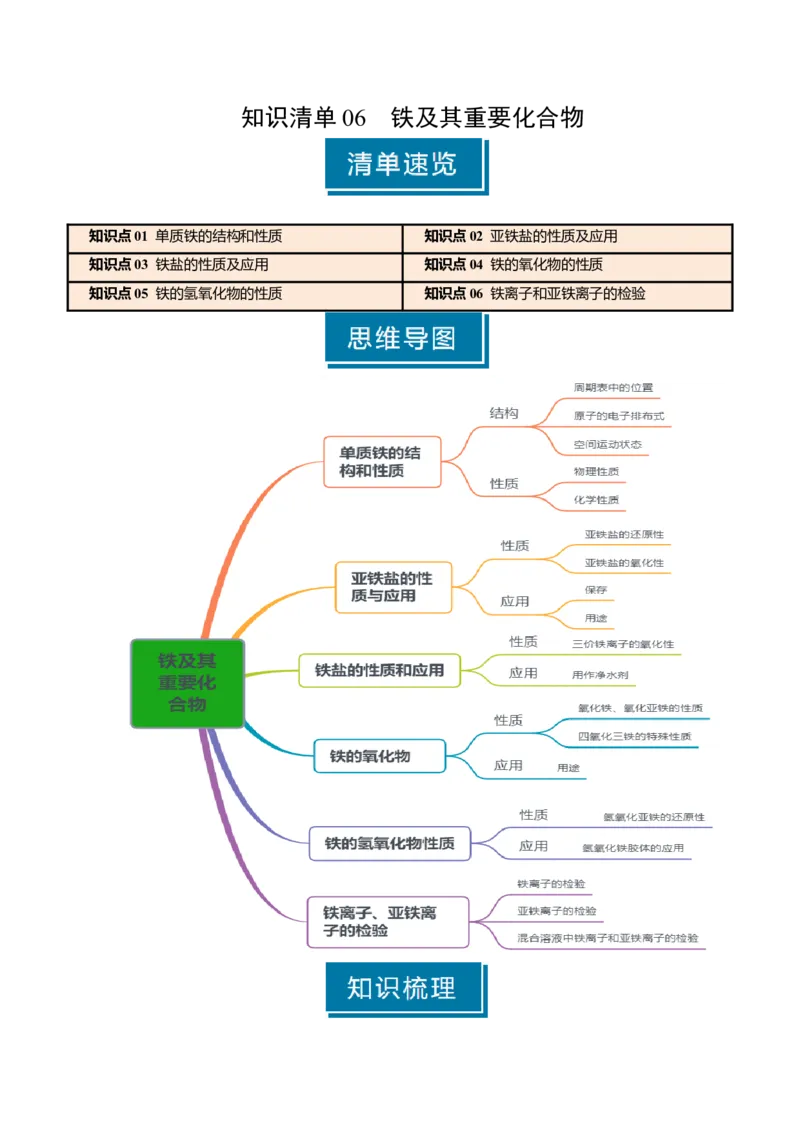
知识清单 06 铁及其重要化合物
知识点01 单质铁的结构和性质 知识点02 亚铁盐的性质及应用
知识点03 铁盐的性质及应用 知识点04 铁的氧化物的性质
知识点05 铁的氢氧化物的性质 知识点06 铁离子和亚铁离子的检验知识点 01 单质铁的结构和性质
1.铁的原子结构
(1)周期表中位置:第 周期第 族
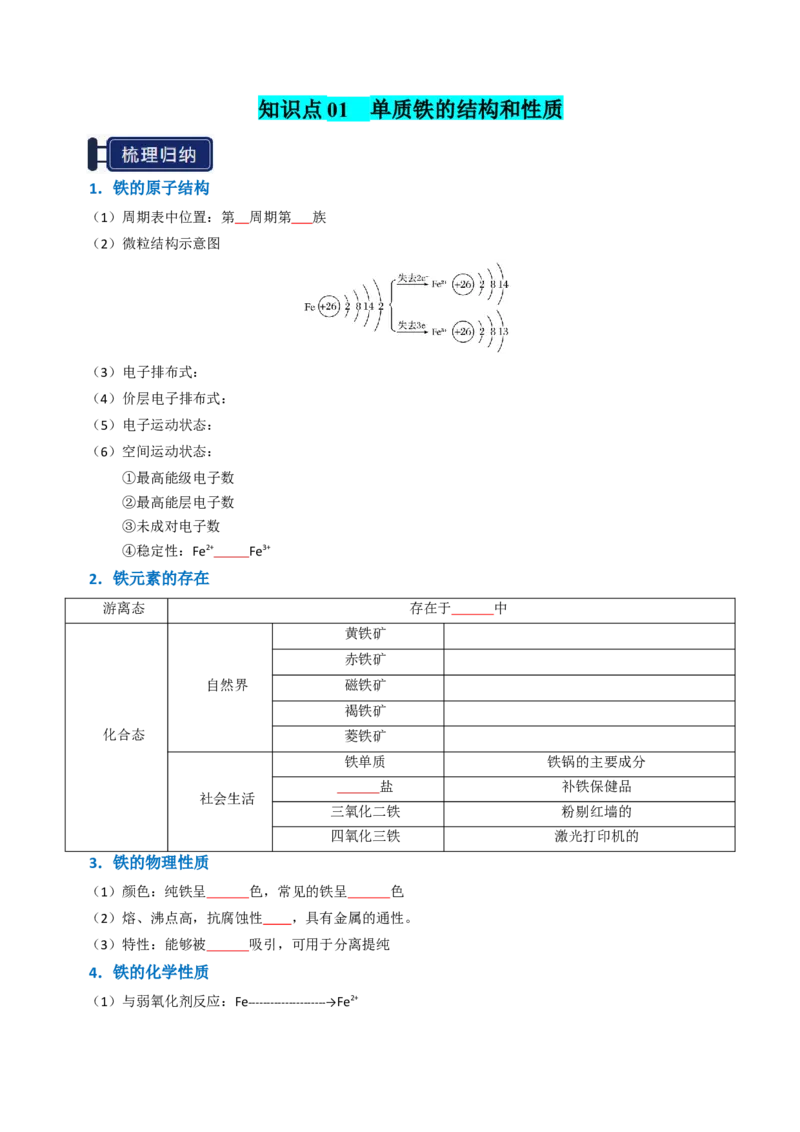
(2)微粒结构示意图
(3)电子排布式:
(4)价层电子排布式:
(5)电子运动状态:
(6)空间运动状态:
①最高能级电子数
②最高能层电子数
③未成对电子数
④稳定性:Fe2+ Fe3+
2.铁元素的存在
游离态 存在于 中
黄铁矿
赤铁矿
自然界 磁铁矿
褐铁矿
化合态 菱铁矿
铁单质 铁锅的主要成分
盐 补铁保健品
社会生活
三氧化二铁 粉剔红墙的
四氧化三铁 激光打印机的
3.铁的物理性质
(1)颜色:纯铁呈 色,常见的铁呈 色
(2)熔、沸点高,抗腐蚀性 ,具有金属的通性。
(3)特性:能够被 吸引,可用于分离提纯
4.铁的化学性质
(1)与弱氧化剂反应:Fe---------------------→Fe2+①Fe+S
②Fe+I
2
③Fe+H+ =
④Fe+Cu2+=
(2)与强氧化剂反应:Fe-----------------------------------------→Fe3+
①Fe---------→ ,生成 烟
②Fe----------→ ;Fe----------→ 或
③Fe----------→ ;Fe----------→ 或
④Fe-----------→ ;Fe-----------→
(3)生成Fe O 的反应
3 4
①O :
2
②水蒸气:
5.铁单质的制备方法
①工业上利用铁矿石在高炉中炼铁,以赤铁矿为例写出该反应的化学方程式_
②利用铝热反应焊接无缝钢轨,写出以氧化铁和铝粉为铝热剂反应的化学方程式_
铁的易错知识点
(1)Fe与O (点燃)、H O(g)(高温)反应的固体产物都是 而不是Fe O 。
2 2 2 3
(2)常温下,Fe、Al在冷的浓硫酸和浓硝酸中发生 ,但加热后能继续反应。
(3)Fe与Cl 反应时生成 ,与S反应时生成 ,说明Cl 的氧化性强于S。
2 2
(4)Fe与在少量Cl 中燃烧不能生成FeCl ,因为FeCl 和Fe必须在溶液中才能反应。所以无论Cl 是过量
2 2 3 2
还是少量,Fe与Cl 反应只生成 。
2
(5)Fe与盐酸反应生成 而不是FeCl ;Fe与I 反应生成 而不是FeI。
3 2 3
(6)铁与水蒸气的反应需用 ,加热仪器为酒精喷灯。
1.下列有关铁的说法正确的是( )
A.Fe在稀硝酸中发生钝化
B.将废铁屑加入FeCl 溶液中,可用于除去工业废气中的Cl
2 2
C.向FeCl 溶液中滴加NH SCN溶液,溶液显红色
2 4
D.镀锌铁不如镀锡铁耐腐蚀
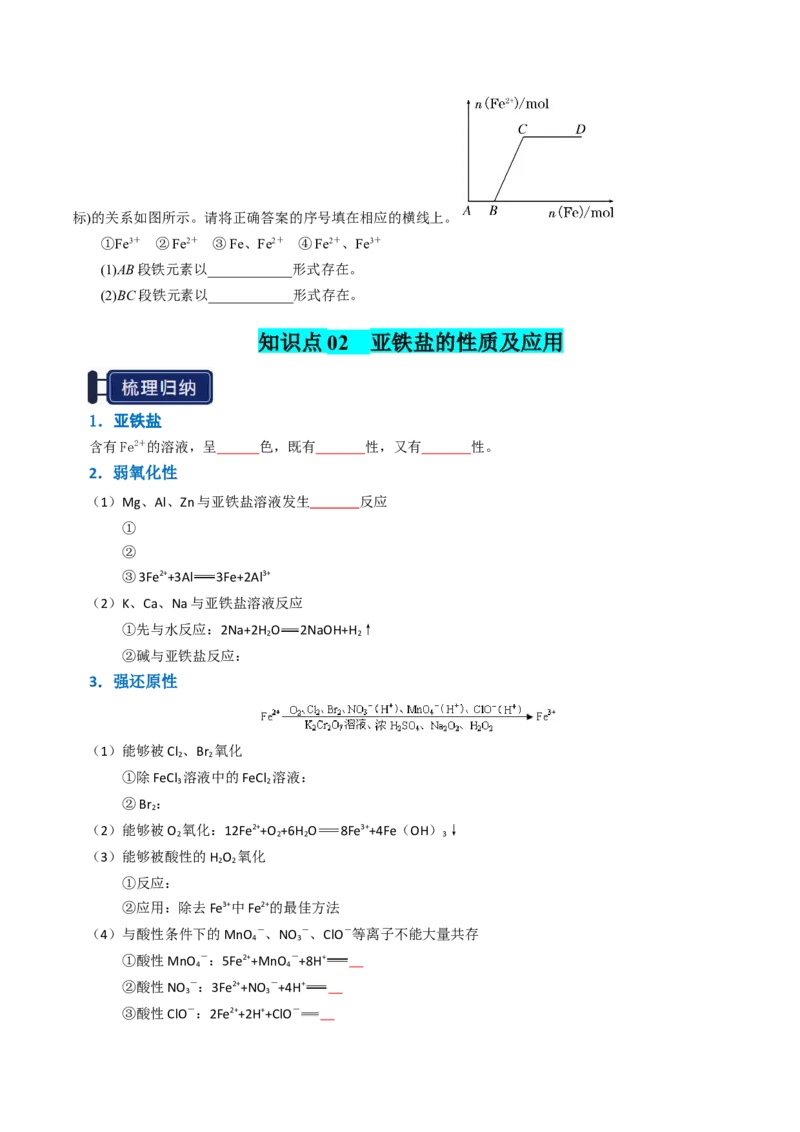
2.在一定量的稀HNO 中慢慢加入铁粉,得到的Fe2+的物质的量(纵坐标)与所加铁粉的物质的量(横坐
3标)的关系如图所示。请将正确答案的序号填在相应的横线上。
①Fe3+ ②Fe2+ ③Fe、Fe2+ ④Fe2+、Fe3+
(1)AB段铁元素以____________形式存在。
(2)BC段铁元素以____________形式存在。
知识点 02 亚铁盐的性质及应用
1.亚铁盐
含有Fe2+的溶液,呈 色,既有 性,又有 性。
2.弱氧化性
(1)Mg、Al、Zn与亚铁盐溶液发生 反应
①
②
③3Fe2++3Al 3Fe+2Al3+
(2)K、Ca、Na与亚铁盐溶液反应
①先与水反应:2Na+2H O 2NaOH+H ↑
2 2
②碱与亚铁盐反应:
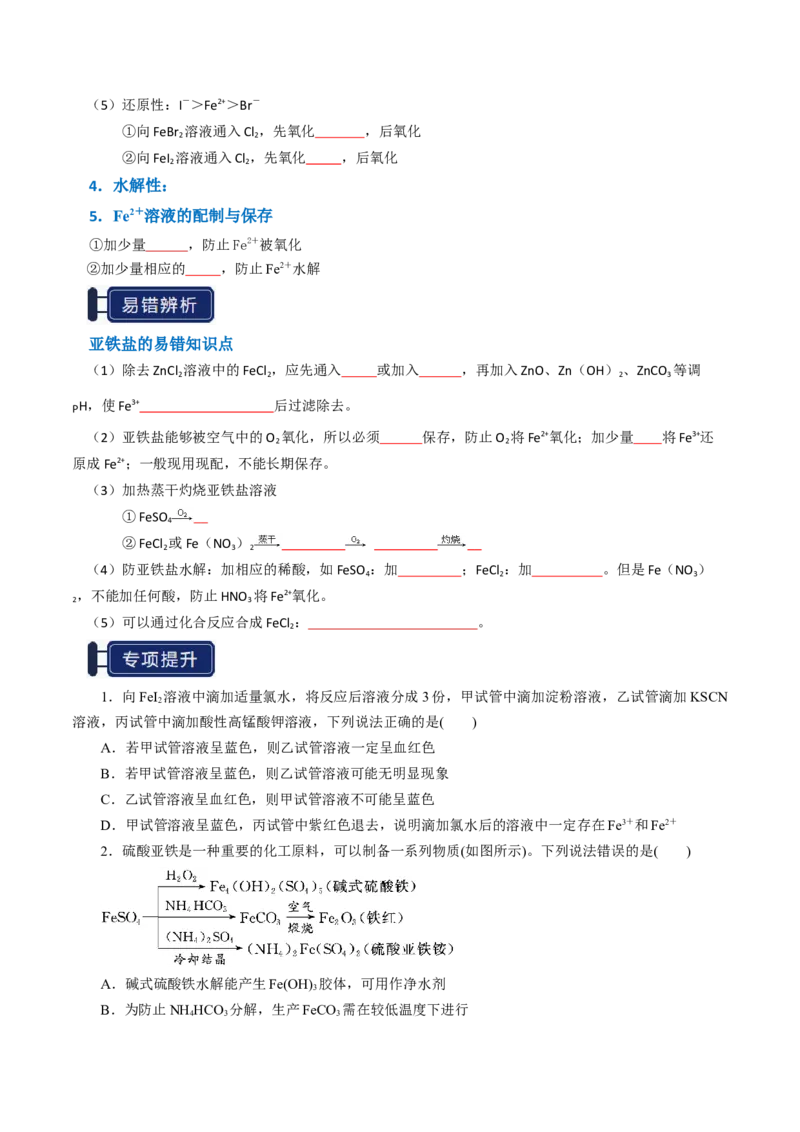
3.强还原性
(1)能够被Cl 、Br 氧化
2 2
①除FeCl 溶液中的FeCl 溶液:
3 2
②Br :
2
(2)能够被O 氧化:12Fe2++O +6H O 8Fe3++4Fe(OH) ↓
2 2 2 3
(3)能够被酸性的H O 氧化
2 2
①反应:
②应用:除去Fe3+中Fe2+的最佳方法
(4)与酸性条件下的MnO -、NO -、ClO-等离子不能大量共存
4 3
①酸性MnO -:5Fe2++MnO -+8H+
4 4
②酸性NO -:3Fe2++NO -+4H+
3 3
③酸性ClO-:2Fe2++2H++ClO-(5)还原性:I->Fe2+>Br-
①向FeBr 溶液通入Cl ,先氧化 ,后氧化
2 2
②向FeI 溶液通入Cl ,先氧化 ,后氧化
2 2
4.水解性:
5.Fe2+溶液的配制与保存
①加少量 ,防止Fe2+被氧化
②加少量相应的 ,防止Fe2+水解
亚铁盐的易错知识点
(1)除去ZnCl 溶液中的FeCl ,应先通入 或加入 ,再加入ZnO、Zn(OH) 、ZnCO 等调
2 2 2 3
PH,使Fe3+ 后过滤除去。
(2)亚铁盐能够被空气中的O 氧化,所以必须 保存,防止O 将Fe2+氧化;加少量 将Fe3+还
2 2
原成Fe2+;一般现用现配,不能长期保存。
(3)加热蒸干灼烧亚铁盐溶液
①FeSO
4
②FeCl 或Fe(NO )
2 3 2
(4)防亚铁盐水解:加相应的稀酸,如FeSO :加 ;FeCl :加 。但是Fe(NO )
4 2 3
,不能加任何酸,防止HNO 将Fe2+氧化。
2 3
(5)可以通过化合反应合成FeCl : 。
2
1.向FeI 溶液中滴加适量氯水,将反应后溶液分成3份,甲试管中滴加淀粉溶液,乙试管滴加KSCN
2
溶液,丙试管中滴加酸性高锰酸钾溶液,下列说法正确的是( )
A.若甲试管溶液呈蓝色,则乙试管溶液一定呈血红色
B.若甲试管溶液呈蓝色,则乙试管溶液可能无明显现象
C.乙试管溶液呈血红色,则甲试管溶液不可能呈蓝色
D.甲试管溶液呈蓝色,丙试管中紫红色退去,说明滴加氯水后的溶液中一定存在Fe3+和Fe2+
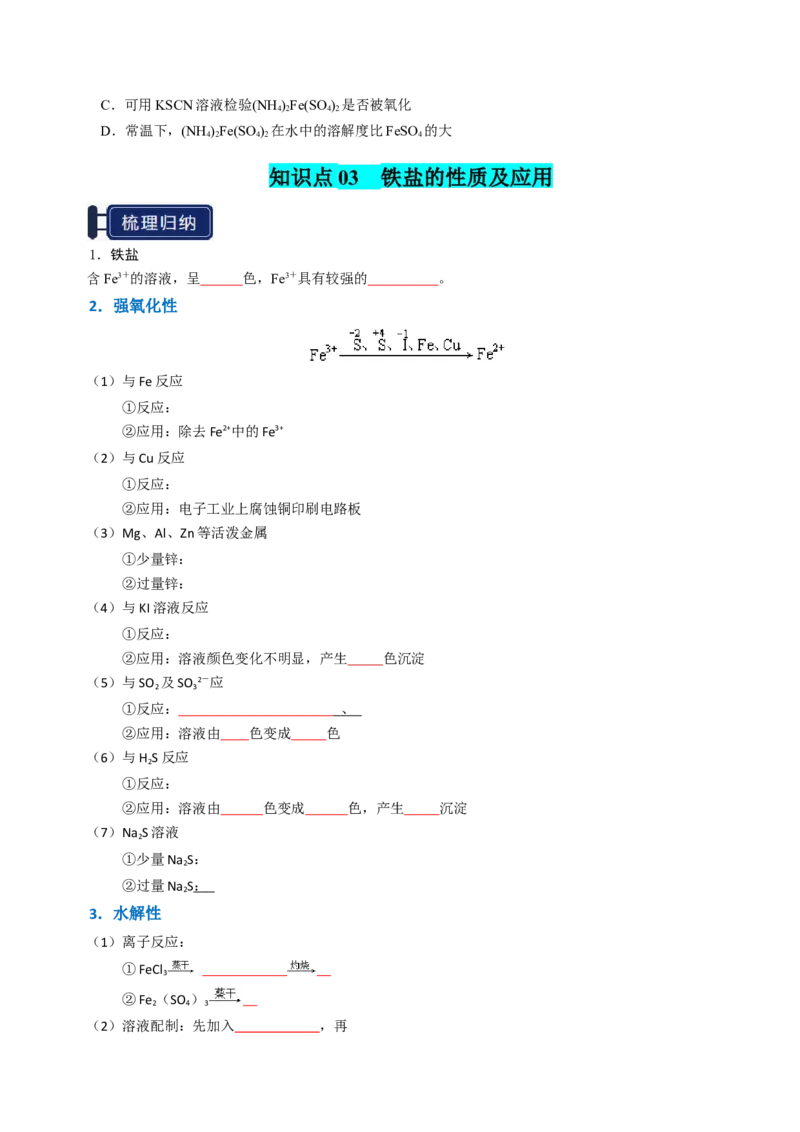
2.硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如图所示)。下列说法错误的是( )
A.碱式硫酸铁水解能产生Fe(OH) 胶体,可用作净水剂
3
B.为防止NH HCO 分解,生产FeCO 需在较低温度下进行
4 3 3C.可用KSCN溶液检验(NH )Fe(SO ) 是否被氧化
4 2 4 2
D.常温下,(NH )Fe(SO ) 在水中的溶解度比FeSO 的大
4 2 4 2 4
知识点 03 铁盐的性质及应用
1.铁盐
含Fe3+的溶液,呈 色,Fe3+具有较强的 。
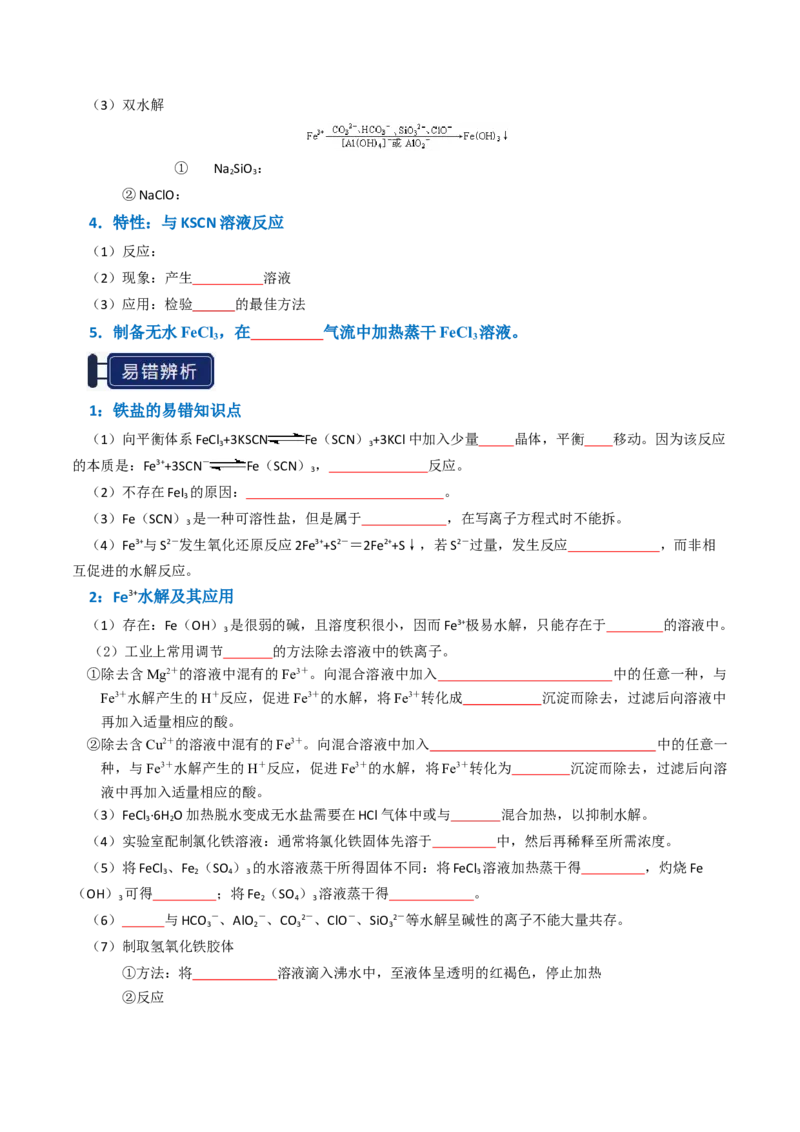
2.强氧化性
(1)与Fe反应
①反应:
②应用:除去Fe2+中的Fe3+
(2)与Cu反应
①反应:
②应用:电子工业上腐蚀铜印刷电路板
(3)Mg、Al、Zn等活泼金属
①少量锌:
②过量锌:
(4)与KI溶液反应
①反应:
②应用:溶液颜色变化不明显,产生 色沉淀
(5)与SO 及SO 2-应
2 3
①反应: 、
②应用:溶液由 色变成 色
(6)与H S反应
2
①反应:
②应用:溶液由 色变成 色,产生 沉淀
(7)Na S溶液
2
①少量Na S:
2
②过量Na S:
2
3.水解性
(1)离子反应:
①FeCl
3
②Fe (SO )
2 4 3
(2)溶液配制:先加入 ,再(3)双水解
① Na SiO :
2 3
②NaClO:
4.特性:与KSCN溶液反应
(1)反应:
(2)现象:产生 溶液
(3)应用:检验 的最佳方法
5.制备无水FeCl ,在 气流中加热蒸干FeCl 溶液。
3 3
1:铁盐的易错知识点
(1)向平衡体系FeCl +3KSCN Fe(SCN) +3KCl中加入少量 晶体,平衡 移动。因为该反应
3 3
的本质是:Fe3++3SCN- Fe(SCN) , 反应。
3
(2)不存在FeI 的原因: 。
3
(3)Fe(SCN) 是一种可溶性盐,但是属于 ,在写离子方程式时不能拆。
3
(4)Fe3+与S2-发生氧化还原反应2Fe3++S2-=2Fe2++S↓,若S2-过量,发生反应 ,而非相
互促进的水解反应。
2:Fe3+水解及其应用
(1)存在:Fe(OH) 是很弱的碱,且溶度积很小,因而Fe3+极易水解,只能存在于 的溶液中。
3
(2)工业上常用调节 的方法除去溶液中的铁离子。
①除去含Mg2+的溶液中混有的Fe3+。向混合溶液中加入 中的任意一种,与
Fe3+水解产生的H+反应,促进Fe3+的水解,将Fe3+转化成 沉淀而除去,过滤后向溶液中
再加入适量相应的酸。
②除去含Cu2+的溶液中混有的Fe3+。向混合溶液中加入 中的任意一
种,与Fe3+水解产生的H+反应,促进Fe3+的水解,将Fe3+转化为 沉淀而除去,过滤后向溶
液中再加入适量相应的酸。
(3)FeCl ·6H O加热脱水变成无水盐需要在HCl气体中或与 混合加热,以抑制水解。
3 2
(4)实验室配制氯化铁溶液:通常将氯化铁固体先溶于 中,然后再稀释至所需浓度。
(5)将FeCl 、Fe (SO ) 的水溶液蒸干所得固体不同:将FeCl 溶液加热蒸干得 ,灼烧Fe
3 2 4 3 3
(OH) 可得 ;将Fe (SO ) 溶液蒸干得 。
3 2 4 3
(6) 与HCO -、AlO -、CO 2-、ClO-、SiO 2-等水解呈碱性的离子不能大量共存。
3 2 3 3
(7)制取氢氧化铁胶体
①方法:将 溶液滴入沸水中,至液体呈透明的红褐色,停止加热
②反应1.FeCl 溶液发生反应时的变色总结
3
(1)向FeCl 溶液中加几滴KSCN溶液后,溶液呈 色;
3
(2)FeCl 溶液能使紫色石蕊试液呈 色;
3
(3)FeCl 与NaOH溶液反应,生成 色沉淀;
3
(4)向FeCl 溶液中通入HS气体,生成 色沉淀;
3 2
(5)向FeCl 溶液中加入几滴NaS溶液,生成 色沉淀,当加入的NaS溶液过量时,又生成 色
3 2 2
沉淀;
(6)向FeCl 溶液中加入过量Fe粉,溶液变成 色;
3
(7)向FeCl 溶液中加入过量Cu粉,溶液变成 色;
3
(8)将FeCl 溶液滴入淀粉碘化钾溶液中,溶液变成 色。
3
(9)向FeCl 溶液中滴入苯酚溶液,溶液变成 色;
3
(10)将FeCl 溶液滴入AgNO 溶液中,生成 沉淀;
3 3
(11)将FeCl 溶液与NaHCO 溶液混合,放出气体,生成 色沉淀;
3 3
(12)将饱和FeCl 溶液滴入沸水中,加热生成 色Fe(OH) 胶体。
3 3
2.下列各组物质反应产生的气体分别通入Fe (SO ) 溶液中,能与Fe (SO ) 发生反应的是( )
2 4 3 2 4 3
①NaO 和CO ②NaS和盐酸 ③MnO 和浓盐酸共热 ④铜片和浓硫酸加热
2 2 2 2 2
A.只有①② B.只有①③
C.只有②③ D.只有②④
知识点 04 铁的氧化物的性质
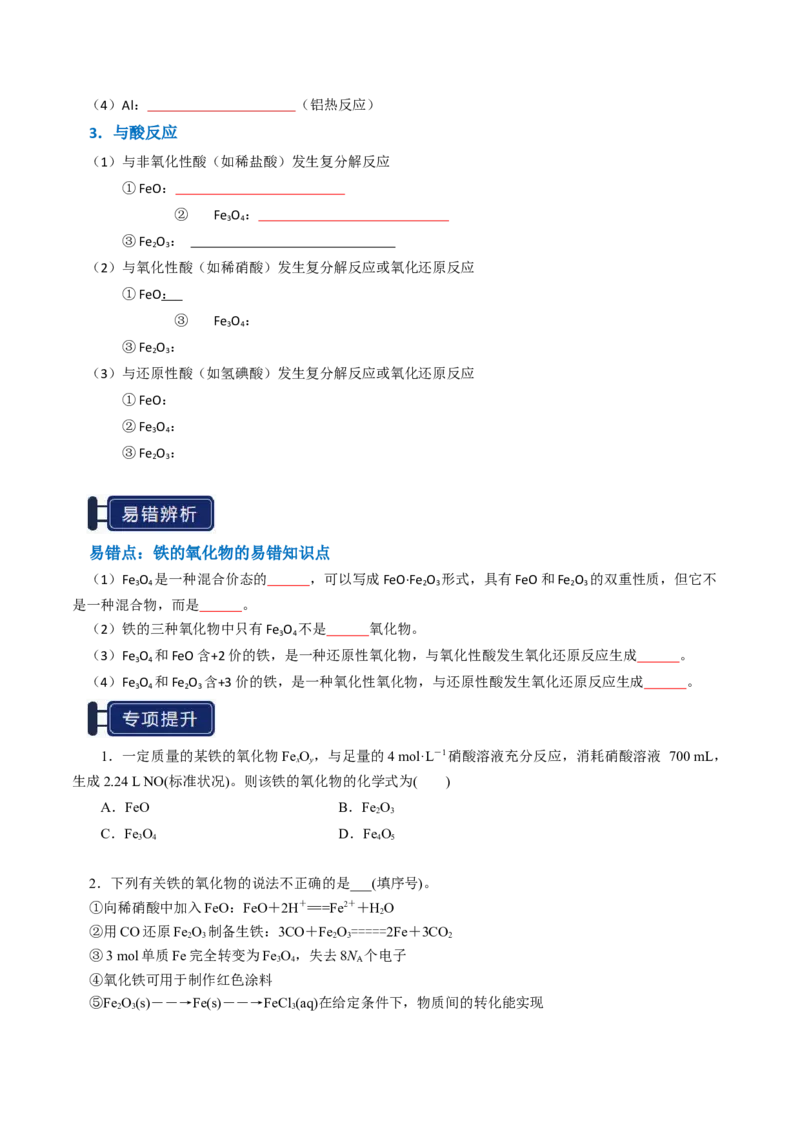
1.物理性质和用途
名称 氧化亚铁 四氧化三铁 氧化铁
化学式 FeO Fe O Fe O
3 4 2 3
铁的化合价 +2 +3
氧化物类型 氧化物 氧化物 氧化物
颜色状态 粉末 晶体 粉末
、铁
俗 名
锈
用 途 材料 颜料
2.能够被某些还原剂还原:FeO---------------------→Fe
x y
(1)H :FeO+H Fe+H O
2 2 2
(2)CO: ( 高炉炼铁的主反应)
(3)C:Fe O +2C 3Fe+2CO ↑
3 4 2(4)Al: (铝热反应)
3.与酸反应
(1)与非氧化性酸(如稀盐酸)发生复分解反应
①FeO:
② Fe O :
3 4
③Fe O :
2 3
(2)与氧化性酸(如稀硝酸)发生复分解反应或氧化还原反应
①FeO:
③ Fe O :
3 4
③Fe O :
2 3
(3)与还原性酸(如氢碘酸)发生复分解反应或氧化还原反应
①FeO:
②Fe O :
3 4
③Fe O :
2 3
易错点:铁的氧化物的易错知识点
(1)Fe O 是一种混合价态的 ,可以写成FeO·Fe O 形式,具有FeO和Fe O 的双重性质,但它不
3 4 2 3 2 3
是一种混合物,而是 。
(2)铁的三种氧化物中只有Fe O 不是 氧化物。
3 4
(3)Fe O 和FeO含+2价的铁,是一种还原性氧化物,与氧化性酸发生氧化还原反应生成 。
3 4
(4)Fe O 和Fe O 含+3价的铁,是一种氧化性氧化物,与还原性酸发生氧化还原反应生成 。
3 4 2 3
1.一定质量的某铁的氧化物FeO,与足量的4 mol·L-1硝酸溶液充分反应,消耗硝酸溶液 700 mL,
x y
生成2.24 L NO(标准状况)。则该铁的氧化物的化学式为( )
A.FeO B.Fe O
2 3
C.Fe O D.Fe O
3 4 4 5
2.下列有关铁的氧化物的说法不正确的是___(填序号)。
①向稀硝酸中加入FeO:FeO+2H+===Fe2++HO
2
②用CO还原Fe O 制备生铁:3CO+Fe O=====2Fe+3CO
2 3 2 3 2
③3 mol单质Fe完全转变为Fe O,失去8N 个电子
3 4 A
④氧化铁可用于制作红色涂料
⑤Fe O(s)――→Fe(s)――→FeCl (aq)在给定条件下,物质间的转化能实现
2 3 3知识点 05 铁的氢氧化物的性质
1.铁的氢氧化物的制备
(1)制备氢氧化铁
①烧碱:
②氨水:
(2)氢氧化亚铁
①烧碱:
②氨水:
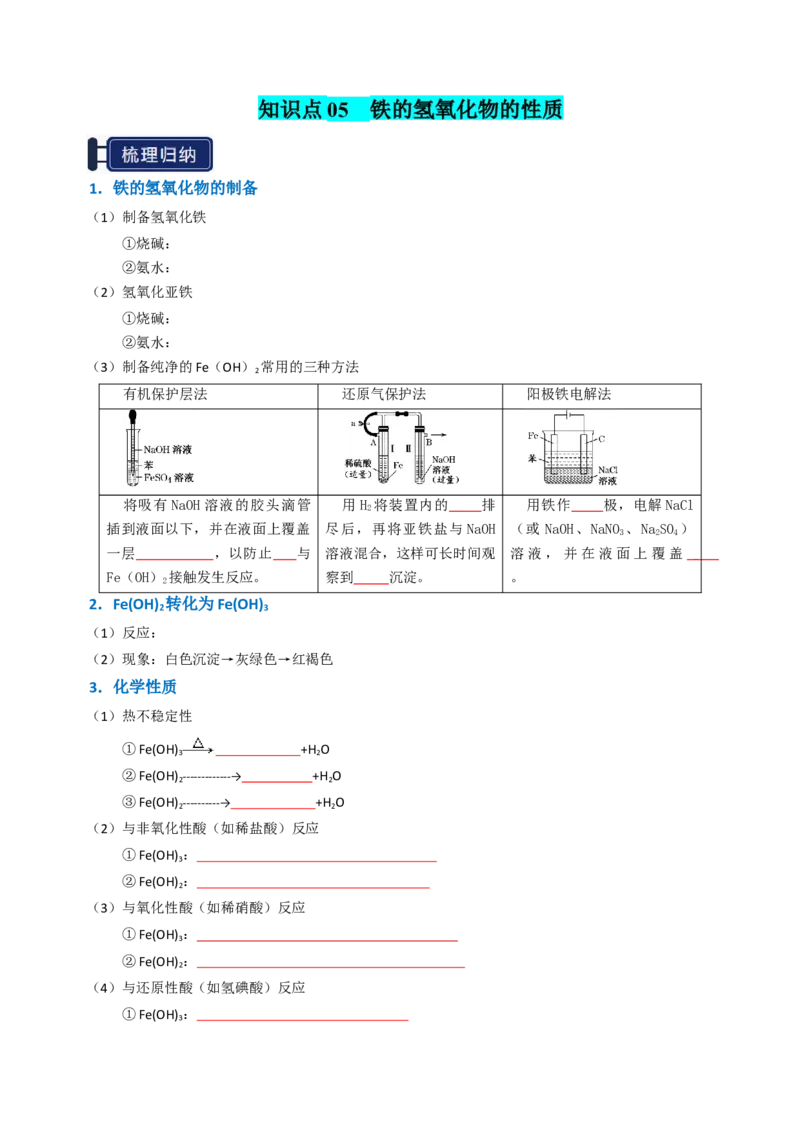
(3)制备纯净的Fe(OH) 常用的三种方法
2
有机保护层法 还原气保护法 阳极铁电解法
将吸有 NaOH 溶液的胶头滴管 用H 将装置内的 排 用铁作 极,电解NaCl
2
插到液面以下,并在液面上覆盖 尽后,再将亚铁盐与 NaOH (或 NaOH、NaNO 、NaSO )
3 2 4
一层 ,以防止 与 溶液混合,这样可长时间观 溶液,并在液面上覆盖
Fe(OH) 接触发生反应。 察到 沉淀。 。
2
2.Fe(OH) 转化为Fe(OH)
2 3
(1)反应:
(2)现象:白色沉淀→灰绿色→红褐色
3.化学性质
(1)热不稳定性
①Fe(OH) +H O
3 2
②Fe(OH) -------------→ +H O
2 2
③Fe(OH) ----------→ +H O
2 2
(2)与非氧化性酸(如稀盐酸)反应
①Fe(OH) :
3
②Fe(OH) :
2
(3)与氧化性酸(如稀硝酸)反应
①Fe(OH) :
3
②Fe(OH) :
2
(4)与还原性酸(如氢碘酸)反应
①Fe(OH) :
3②Fe(OH) :
2
易错点:铁的氢氧化物易错知识点
(1)制备纯净的Fe(OH) 沉淀排除氧气的干扰的基本方法是: 、 、 。
2
(2)Fe(OH) 是 性氢氧化物,在空气中加热会被氧化成Fe(OH) ,进一步分解成Fe O 。
2 3 2 3
(3)酸碱不一定发生中和反应(复分解反应),如 性酸(如硝酸)和 性碱(如Fe(OH) ),
2
还原性酸(如氢碘酸)和氧化性碱(如Fe(OH) )则发生氧化还原反应。
3
1.某学生以铁丝和Cl 为原料进行下列三个实验。下列从分类角度分析正确的是( )
2
A.实验①、③反应制得的物质均为纯净物
B.实验②、③均未发生氧化还原反应
C.实验①、③均为放热反应
D.实验①、②所涉及的物质均为电解质
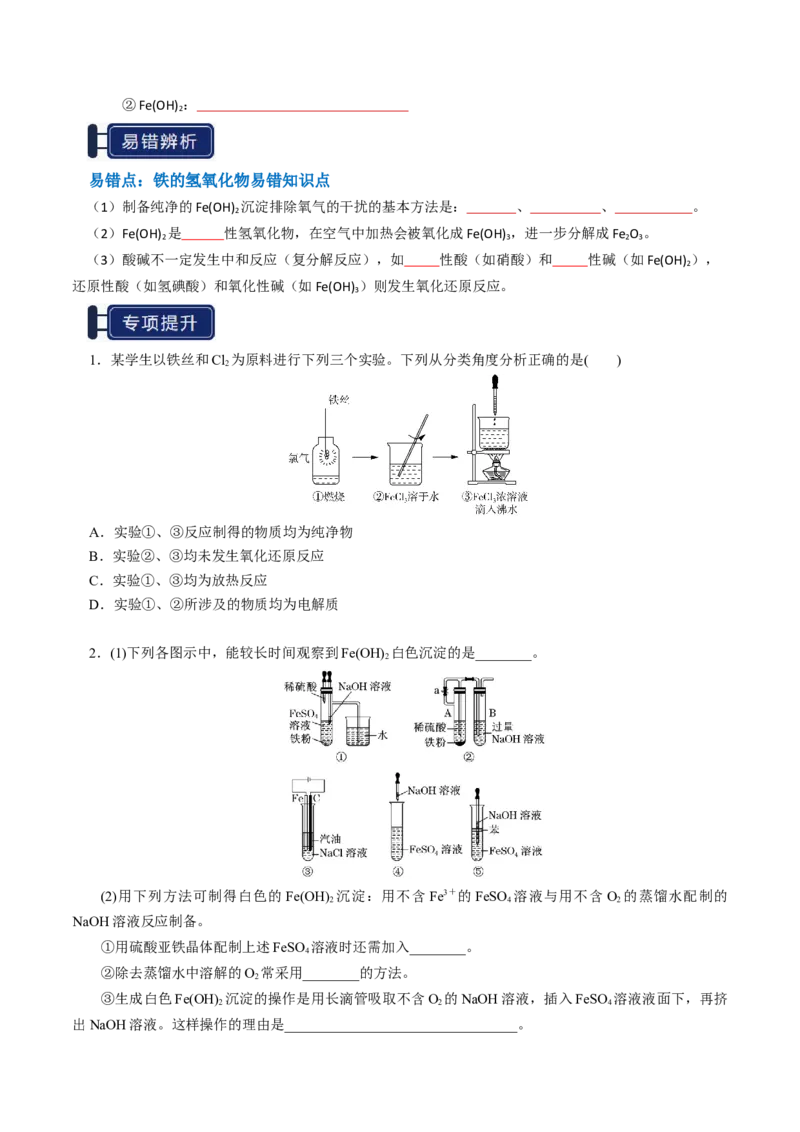
2.(1)下列各图示中,能较长时间观察到Fe(OH) 白色沉淀的是________。
2
(2)用下列方法可制得白色的 Fe(OH) 沉淀:用不含Fe3+的FeSO 溶液与用不含O 的蒸馏水配制的
2 4 2
NaOH溶液反应制备。
①用硫酸亚铁晶体配制上述FeSO 溶液时还需加入________。
4
②除去蒸馏水中溶解的O 常采用________的方法。
2
③生成白色Fe(OH) 沉淀的操作是用长滴管吸取不含O 的NaOH溶液,插入FeSO 溶液液面下,再挤
2 2 4
出NaOH溶液。这样操作的理由是_________________________________。知识点 06 铁离子和亚铁离子的检验
1.Fe3+的检验
(1)试液 溶液(最佳方法)
(2)试液 产生 沉淀
(3)苯酚法
①反应:6C H OH+Fe3+ [Fe(OC H ) ]3-+6H+
6 5 6 5 6
②现象:溶液变成
2.Fe2+的检验
(1)试液 溶液
(2)溶液 先产生 沉淀,迅速变成 色,最后变成 色
(3)铁氰化钾K [Fe(CN) ]法
3 6
①反应:3Fe2++2[Fe(CN) ]3-=Fe [Fe(CN) ] ↓
6 3 6 2
②现象:产生 沉淀
3.Fe3+和Fe2+混合液
(1)检验Fe2+
①试液 高锰酸钾溶液 (用 酸化)
②试液
③试液
(2)检验Fe3+
①试液 溶液
②试液 试纸
铁离子和亚铁离子检验的易错知识点
(1)向含Fe2+的溶液中加入硝酸、氯水等具有 性的物质时,溶液会出现 色→ 色的颜色
变化,该现象可用于Fe2+的检验。
(2)在用强氧化剂(H O 或氯水)和KSCN溶液联合检验Fe2+的存在时,要特别注意加入试剂的 ,
2 2
先加 溶液无明显变化,说明溶液中无 ;再加强氧化剂(H O 或氯水)后溶液 色,说明
2 2
原溶液中含有Fe2+。
(3)检验Fe (SO ) 溶液中是否含FeSO 溶液,可以用酸性 溶液,因为Fe2+能使其褪色。
2 4 3 4
(4)检验FeCl 溶液中是否含FeCl 溶液,不能用酸性高锰酸钾溶液,因为 也能使其褪色,应该用铁
3 2氰化 钾 溶液。
1.下列离子的检验方法合理的是( )
A.向某溶液中滴入KSCN溶液呈红色,说明不含Fe2+
B.向某溶液中通入Cl,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+
2
C.向某溶液中加入NaOH溶液,得红褐色沉淀,说明溶液中含有Fe3+
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明该溶液中只含有Fe2
+,不含有Mg2+
2.下列有关铁离子及亚铁离子检验的说法正确的是( )
A.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe3+
B.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+
C.证明某溶液只含有Fe2+而不含有Fe3+的实验方法是滴加NaOH溶液,先产生白色沉淀,后变灰绿色,
最后呈红褐色
D.向某溶液中滴加K[Fe(CN) ]溶液,产生蓝色沉淀,说明原溶液中有Fe2+,无Fe3+
3 6
3.下列除杂的操作不正确的是( )
A.MgCl 溶液中混有少量FeCl :加入足量镁充分反应后过滤
2 3
B.FeCl 溶液中混有少量FeCl :加入过量铁粉充分反应后过滤
2 3
C.CuCl 溶液中混有少量FeCl :加入NaOH溶液充分反应后过滤
2 3
D.CuCl 溶液中混有少量FeCl :先加入HO 将Fe2+氧化成Fe3+,再加入CuO充分反应后过滤
2 2 2 2