文档内容
第 01 讲 化学反应的热效应
目录
01 模拟基础练
【题型二】反应过程与能量变化
【题型二】反应热与能量变化图象分析
【题型二】反应热与键能
【题型二】热化学方程式书写及正误判断
【题型二】中和反应热测定
【题型二】盖斯定律及应用
02 重难创新练
03 真题实战练
题型一 反应过程与能量变化
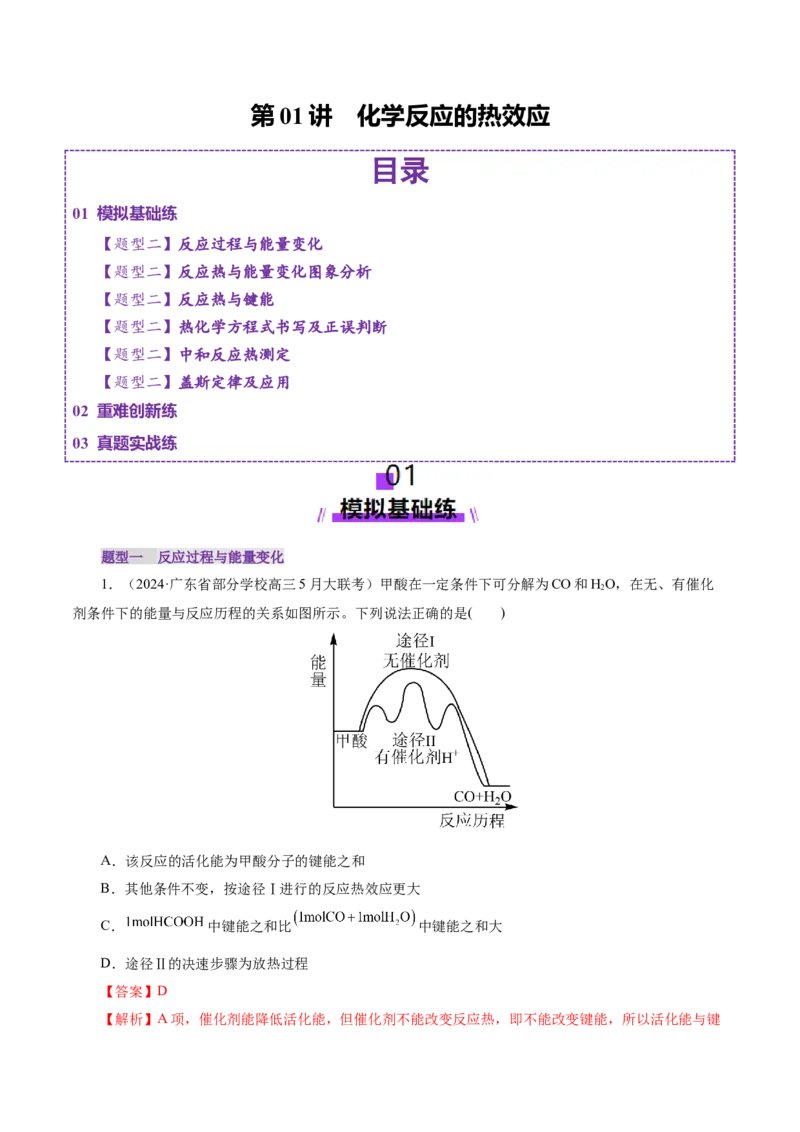
1.(2024·广东省部分学校高三5月大联考)甲酸在一定条件下可分解为CO和HO,在无、有催化
2
剂条件下的能量与反应历程的关系如图所示。下列说法正确的是( )
A.该反应的活化能为甲酸分子的键能之和
B.其他条件不变,按途径Ⅰ进行的反应热效应更大
C. 中键能之和比 中键能之和大
D.途径Ⅱ的决速步骤为放热过程
【答案】D
【解析】A项,催化剂能降低活化能,但催化剂不能改变反应热,即不能改变键能,所以活化能与键能之和无直接关系,A错误;B项,催化剂能降低反应的活化能,不能改变反应的化学平衡,即不能改变
反应的热效应,B错误;C项,由图可知,该反应为放热反应,所以反应物总键能小于生成物总键能,因
此 中键能之和比 中键能之和小,C错误;D项,由图可知,途径Ⅱ的第
二步的活化能最大,即途径Ⅱ的决速步骤为第二步,图像显示第二步中反应物的总能量高于生成物的总能
量,即为放热过程,D正确;故选D。
2.丙烷与溴原子能发生以下两种反应:
①CHCHCH(g)+Br·(g) CHCHCH·(g)+HBr(g)。
3 2 3 3 2 2
②CHCHCH(g)+Br·(g) CHCH·CH (g)+HBr(g)。
3 2 3 3 3
反应过程的能量变化如图所示。下列说法正确的是( )
A.反应①是放热反应
B.反应②使用了催化剂
C.产物中 CHCHCH·(g)的含量比CHCH·CH (g)低
3 2 2 3 3
D.CHCHCH·(g)转变为 CHCH·CH (g)时需要吸热
3 2 2 3 3
【答案】C
【解析】由反应过程的能量变化图可知,反应①和②生成物的能量都高于反应物的能量,属于吸热反
应,故A错误;无法判断反应②是否使用了催化剂,故B错误;反应①的活化能比反应②活化能高,因此
反应②更容易进行,反应②产物CHCH·CH(g)含量高,故 C正确;由反应过程的能量变化图可知,
3 3
CHCH·CH(g)能量低,CHCHCH·(g)能量高,CHCHCH·(g)转变为 CHCH·CH(g)时需要放热,故D错
3 3 3 2 2 3 2 2 3 3
误。
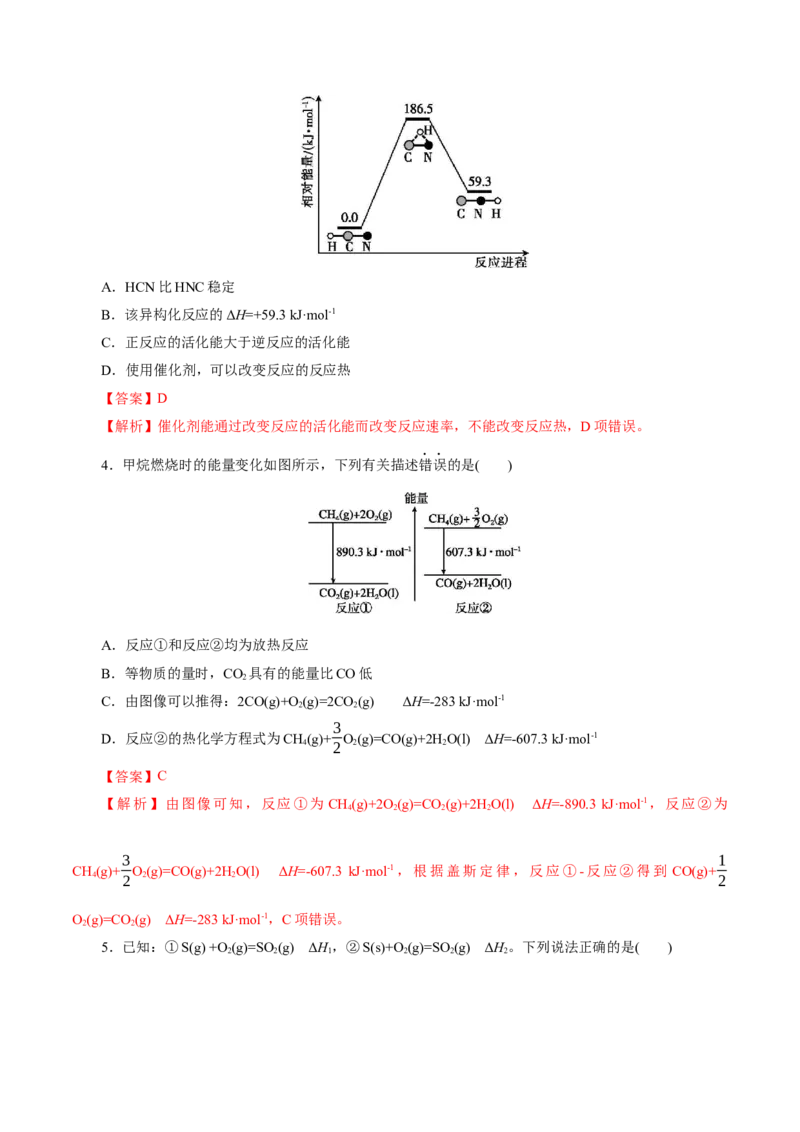
3.理论研究表明,在101 kPa和298 K下,HCN(g) HNC(g)异构化反应过程的能量变化如图所示。
下列说法错误的是( )A.HCN比HNC稳定
B.该异构化反应的ΔH=+59.3 kJ·mol-1
C.正反应的活化能大于逆反应的活化能
D.使用催化剂,可以改变反应的反应热
【答案】D
【解析】催化剂能通过改变反应的活化能而改变反应速率,不能改变反应热,D项错误。
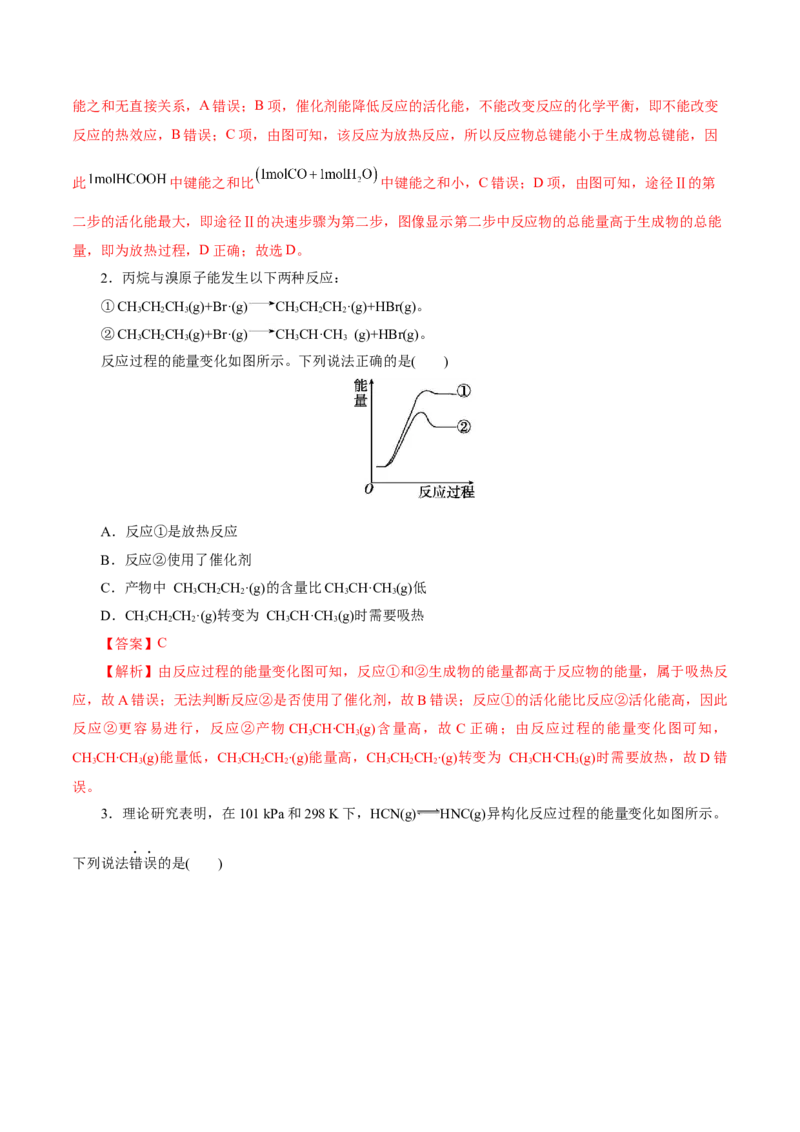
4.甲烷燃烧时的能量变化如图所示,下列有关描述错误的是( )
A.反应①和反应②均为放热反应
B.等物质的量时,CO 具有的能量比CO低
2
C.由图像可以推得:2CO(g)+O(g)=2CO (g) ΔH=-283 kJ·mol-1
2 2
3
D.反应②的热化学方程式为CH(g)+ O(g)=CO(g)+2HO(l) ΔH=-607.3 kJ·mol-1
4 2 2 2
【答案】C
【解析】由图像可知,反应①为 CH(g)+2O(g)=CO (g)+2HO(l) ΔH=-890.3 kJ·mol-1,反应②为
4 2 2 2
3 1
CH(g)+ O(g)=CO(g)+2HO(l) ΔH=-607.3 kJ·mol-1,根据盖斯定律,反应①-反应②得到 CO(g)+
4 2 2 2 2
O(g)=CO (g) ΔH=-283 kJ·mol-1,C项错误。
2 2
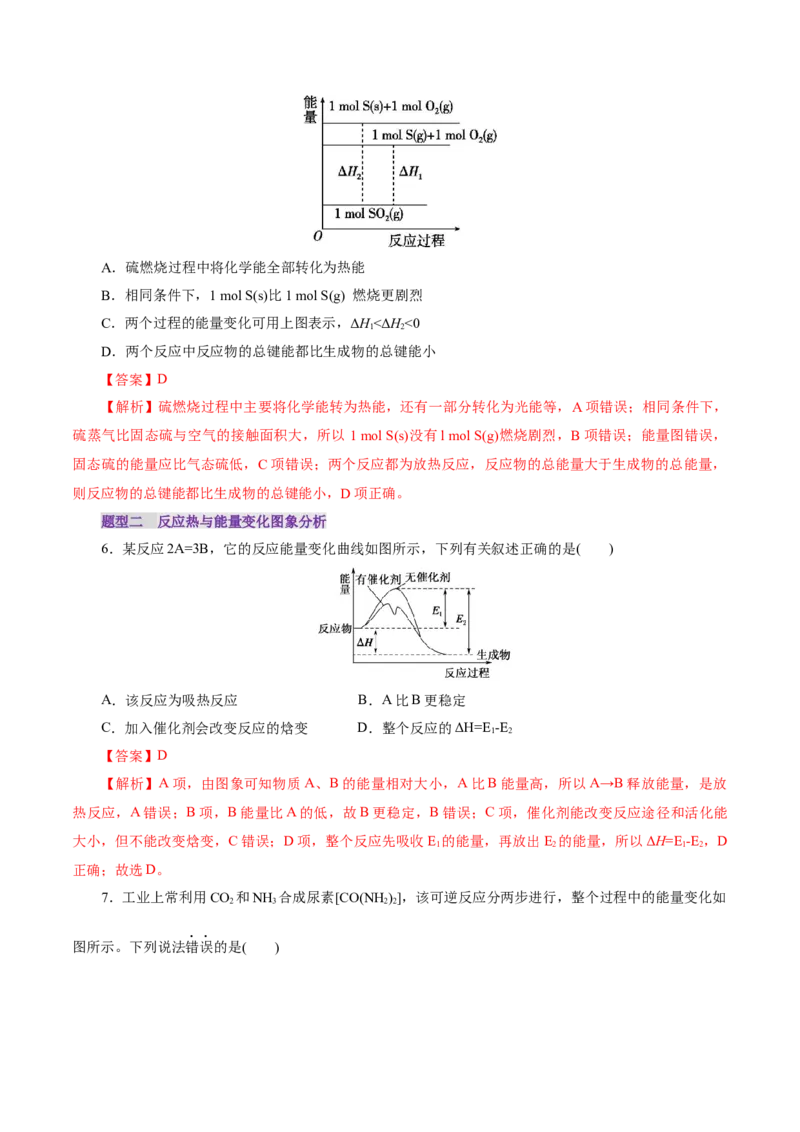
5.已知:①S(g) +O (g)=SO(g) ΔH,②S(s)+O (g)=SO(g) ΔH。下列说法正确的是( )
2 2 1 2 2 2A.硫燃烧过程中将化学能全部转化为热能
B.相同条件下,1 mol S(s)比1 mol S(g) 燃烧更剧烈
C.两个过程的能量变化可用上图表示,ΔH<ΔH<0
1 2
D.两个反应中反应物的总键能都比生成物的总键能小
【答案】D
【解析】硫燃烧过程中主要将化学能转为热能,还有一部分转化为光能等,A项错误;相同条件下,
硫蒸气比固态硫与空气的接触面积大,所以 1 mol S(s)没有l mol S(g)燃烧剧烈,B项错误;能量图错误,
固态硫的能量应比气态硫低,C项错误;两个反应都为放热反应,反应物的总能量大于生成物的总能量,
则反应物的总键能都比生成物的总键能小,D项正确。
题型二 反应热与能量变化图象分析
6.某反应2A=3B,它的反应能量变化曲线如图所示,下列有关叙述正确的是( )
A.该反应为吸热反应 B.A比B更稳定
C.加入催化剂会改变反应的焓变 D.整个反应的ΔH=E -E
1 2
【答案】D
【解析】A项,由图象可知物质A、B的能量相对大小,A比B能量高,所以A→B释放能量,是放
热反应,A错误;B项,B能量比A的低,故B更稳定,B错误;C项,催化剂能改变反应途径和活化能
大小,但不能改变焓变,C错误;D项,整个反应先吸收E 的能量,再放出E 的能量,所以ΔH=E-E ,D
1 2 1 2
正确;故选D。
7.工业上常利用CO 和NH 合成尿素[CO(NH)],该可逆反应分两步进行,整个过程中的能量变化如
2 3 2 2
图所示。下列说法错误的是( )A.NH COONH 为合成尿素反应的中间产物
2 4
B.反应Ⅰ逆反应的活化能>反应Ⅱ正反应的活化能
C.反应Ⅱ在热力学上进行趋势较小
D.2NH (g)+CO (g) CO(NH)(l)+H O(l)的ΔH=E-E
3 2 2 2 2 1 2
【答案】D
【解析】反应Ⅱ为吸热反应,在热力学上进行的趋势较小,C项正确;2NH (g)+CO (g) CO(NH)(l)
3 2 2 2
+H O(l)为放热反应,ΔH =生成物的总能量-反应物的总能量<0,即ΔH=E-E,D项错误。
2 2 1
8.H 与ICl的反应分①②两步进行,其能量曲线如图所示。下列有关说法错误的是( )
2
A.反应①、反应②均为放热反应
B.反应①、反应②均为氧化还原反应
C.反应①比反应②的速率慢,与相应正反应的活化能无关
D.反应①、反应②的焓变之和为ΔH=-218 kJ·mol-1
【答案】C
【解析】根据图像可知,反应①和反应②中反应物的总能量都大于生成物的总能量,则反应①②均为
放热反应,A项正确;反应①②中都存在元素化合价变化,所以反应①②都是氧化还原反应,B项正确;
反应①比反应②的速率慢,是因为反应①中正反应的活化能较大,则反应速率与活化能有关,C项错误;
反应①、反应②的总能量变化为218 kJ·mol-1,根据盖斯定律可知,反应①、反应②的焓变之和为ΔH=-218
kJ·mol-1,D项正确。
9.101 kPa、25 ℃时,部分物质转化的能量变化如图所示,下列说法正确的是( )A.H 的燃烧热ΔH=-572 kJ· mol-1
2
B.4E(H—O)-2E(H—H)-E(O=O)=-572 kJ· mol-1
C.燃烧热:ΔH(C)<ΔH(CH)
4
D.C(s)+2H(g) =CH (g)(g) ΔH=-75 kJ·mol-1
2 4
【答案】D
【解析】H 的燃烧热ΔH=(-572 kJ· mol-1)÷2=-286 kJ· mol-1,A项错误;焓变等于反应物中总键能与产
2
物中总键能之差,该项对应的热化学方程式为 2H(g)+O(g)=2HO(l) ΔH=-572 kJ·mol-1,在用键能计算反
2 2 2
应热时,有关物质均为气体,而HO为液态,不能计算,B项错误;物质的量相同时,甲烷完全燃烧放出
2
的热量更多,因为ΔH为负值,C项错误;根据盖斯定律,C(s)+2H(g)=CH (g) ΔH=(-572-394+891) kJ·
2 4
mol-1=-75 kJ· mol-1,D项正确。
题型三 反应热与键能
10.(2024·湖北省部分学校高三三模)如表所示为部分化学键的键能数据,由键能数据大小,不能解
释下列事实的是( )
化学键
键能/( kJ·mol−1) 413 348 745 326 318 226 452 347
A.硬度:金刚石 碳化硅
B.熔、沸点:金刚石>CO
2
C.SiH 的稳定性小于CH,更易生成氧化物
4 4
D.硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多
【答案】B
【解析】A项,由题干表中数据可知,C-C键的键能>Si-C键的键能,故硬度:金刚石>碳化硅,A
不合题意;B项,已知金刚石是共价晶体,而CO 为分子晶体,熔沸点受范德华力影响与键能无关,故熔、
2
沸点:金刚石>CO,但不能用键能的数据来解释,B符合题意;C项,由题干表中数据可知,Si-H的键
2
能比C-H的键能更小,故SiH 的稳定性小于CH,更易生成氧化物,C不合题意;D项,由题干表中数据
4 4
可知,Si-H的键能比C-H的键能更小,C-C键的键能>Si-Si键的键能,则硅与碳同族,也有系列氢化物,
但硅烷在种类和数量上都远不如烷烃多,D不合题意;故选C。
11.已知H(g)+Br (l)=2HBr(g) ΔH=-72 kJ·mol-1。蒸发1 mol Br (l)需要吸收的能量为30 kJ,其他相关
2 2 2数据如下表所示:
共价键 H—H H—Br
键能/(kJ·mol-1) 436 369
下列说法正确的是( )
A.Br (l)=Br (g) ΔH=-30kJ·mol-1
2 2
B.2Br(g)=Br (g) ΔH=230 kJ·mol-1
2
C.2HBr(g)=H (g)+Br (g) ΔH=+102 kJ·mol-1
2 2
D.H(g)+Br (l)=2HBr(g) ΔH=-72 kJ·mol-1表示一个氢气分子和一个液溴分子完全反应放出72 kJ热量
2 2
【答案】C
【解析】已知蒸发1 mol Br (l)需要吸收的能量为30 kJ,则Br (l)=Br (g) ΔH=+30 kJ·mol-1,A项错误;
2 2 2
H(g)+Br (l)=2HBr(g) ΔH=-72 kJ·mol-1,由盖斯定律、结合选项 A 知,H(g)+Br (g)=2HBr(g) ΔH=-102
2 2 2 2
kJ·mol-1,反应的焓变=反应物总键能-生成物总键能,436 kJ·mol-1+Br—Br 的键能-2×369 kJ·mol-1=-102
kJ·mol-1,则Br—Br的键能为200 kJ·mol-1,即2Br(g)=Br (g) ΔH=-200 kJ·mol-1,B项错误;结合选项B知:
2
H(g)+Br (g)=2HBr(g) ΔH=-102 kJ·mol-1,则 2HBr(g)=H (g)+Br (g) ΔH=+102 kJ·mol-1,C项正确;H(g)
2 2 2 2 2
+Br (l)=2HBr(g) ΔH=-72 kJ·mol-1表示1 mol氢气分子和1 mol液溴分子完全反应放出72 kJ热量,D项错误。
2
12.标准状态下,1mol纯物质的相对能量及解离为气态原子时所消耗的能量如下表所示:
物质 O(g) N(g) NO g) C(s,石墨) CH(g) CO(g)
2 2 2 4 2
相对能量/ kJ·mol−1 0 0 x 0 -75 -393.5
解离总耗能/kJ 498 946 632 717 1656 y
下列说法正确的是( )
A.x =180
B.逐级断开CH(g)中的每摩尔C—H所消耗的能量均为414kJ
4
C.解离每摩尔C(s,石墨)中的碳碳键平均耗能为239kJ
D.根据NO(g)+CH(g) CO(g)+N(g)+2H O(g)的ΔH可计算出H—O键能
4 2 2
【答案】D
【解析】A项,焓变=生成物总能量-反应物总能量,则N(g)+O(g) 2NO(g) ΔH=2x
2 2
kJ·mol−1,焓变=反应物总键能-生成物总键能,即498+946-632×2=2x,x =90,故A错误;B项,逐级断开
CH(g)中的每摩尔C—H所消耗的能量不相等,故B错误;C项,石墨晶体中每个碳原子形成3条共价键,
4
两个碳原子形成1条键,则1mol石墨含有1.5molC-C键,解离每摩尔C(s,石墨)中的碳碳键平均耗能为
478kJ,故C错误;D项,焓变=反应物总键能-生成物总键能,C(s,石墨)+O (g) CO(g)的ΔH可计算
2 2
出y值,再根据NO(g)+CH(g) CO(g)+N(g)+2H O(g)的ΔH可计算出H—O键能,故D正确;故选
4 2 2
D。13.(2024·浙江省义乌中学高三适应性考试)标准状态下,气态反应物、生成物及活化分子[A(B)表示
“A+B→产物”的活化分子]的相对能量如表所示:
物质 NO(g) NO (g) SO (g) SO (g) O(g) O(g) NO(O) SO (O )
2 2 3 2 3 3 2 3
相对能量/ 91.3 33.2 -296.8 -395.7 0 142.7 237.2 -96.1
下列说法不正确的是( )
A.NO (g)+SO (g) NO (g)+ SO (g) ΔH=-40.8 kJ·mol-1
2 2 3
B.3O(g) 2O(g)反应不能自发进行
2 3
C.相同条件下,SO (g)+O(g) O (g)+ SO (g)比NO (g)+O(g) O (g)+ NO (g)速率快
2 3 2 3 3 2 2
D.1mol NO (g)的总键能大于1mol NO(g)总键能
2
【答案】C
【解析】A项,NO (g)+SO(g) NO (g)+ SO (g) ΔH=生成物总能量-反应物总能量=91.3kJ/mol+
2 2 3
(-395.7kJ/mol)-[33.2kJ/mol+(-296.8kJ/mol)]=-40.8kJ/mol,故A正确;B项,3O(g) 2O(g) H=生成物
2 3
总能量-反应物总能量=+285.4kJ/mol>0,且 S<0,则任何温度下 H-T S>0,即反应3O(g)
2
2O(g)不能自发进行,故B正确;C项,反应SO (g)+O(g) O (g)+ SO (g)的活化能=活化分子能量-
3 2 3 2 3
反应物总能量=-96.1kJ/mol-(-296.8kJ/mol+142.7kJ/mol)=58kJ/mol,反应NO (g)+O(g) O (g)+ NO (g)
3 2 2
的活化能为237.2kJ/mol-(91.3kJ/mol+142.7kJ/mol)=3.2kJ/mol<58kJ/mol,反应的活化能越高,反应速率越慢,
则相同条件下,SO (g)+O(g) O (g)+ SO (g)比NO (g)+O(g) O (g)+ NO (g)速率慢,故C错
2 3 2 3 3 2 2
误;D项,反应2NO (g)+O(g) 2NO (g)ΔH=生成物总能量-反应物总能
2 2
量=2×33.2kJ/mol-2×91.3kJ/mol-0kJ/mol=-116.2kJ/mol,为放热反应,焓变△H=反应物总键能-生成物总键能,
则该反应反应物总键能<生成物总键能,即1molNO(g)和0.5molO 总键能<1molNO (g)的总键能,所以
2 2
1molNO (g)的总键能大于1molNO(g)总键能,故D正确;故选C。
2
14.(2024·江西省九江市十校高三联考)有机物a、b、c、d分别与氢气发生加成反应生成1mol环己烷(
)的能量变化如图所示,下列推理正确的是( )
A.由ΔH 的值可知,a分子中碳碳双键的键能为120kJ/mol
1
B.ΔH<ΔH,说明单双键交替的两个碳碳双键间存在相互作用,不利于物质稳定
2 3C.2ΔH≈ΔH,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
1 2
D.ΔH-ΔH <0,ΔH-ΔH >0,说明苯分子具有特殊稳定性
3 1 4 3
【答案】D
【解析】A项, 由ΔH 的值可知,2摩尔碳氢键和1摩尔碳碳单键的键能和比1摩尔氢氢键的键能和
1
1摩尔碳碳双键之和多120千焦,A错误;B项,ΔH<ΔH,即单双键交替的物质能量低,更稳定,说明
2 3
单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定,B错误;C项,虽然2ΔH≈ΔH,但两者并
1 2
不相等,说明碳碳双键加氢放出的热量与分子内碳碳双键数目、双键的位置有关,不能简单的说碳碳双键
加氢放出的热量与分子内碳碳双键数目成正比,C错误;D项,由图示可知,反应I为: (l)+H (g)→
2
(l) ΔH ,反应III为: (l)+2H (g) → (l) ΔH 反应IV为: +3H (g)→ (l) ΔH ,ΔH-
1 2 3, 2 4 3
ΔH<0即 (l)+H (g) → (l) ΔH<0,ΔH-ΔH >0即 +H (g)→ (l) ΔH>0,则说明 具
1 2 4 3 2
有的总能量小于 ,能量越低越稳定,则说明苯分子具有特殊稳定性,D正确;故选D。
题型四 热化学方程式书写及正误判断
15.已知一定温度和压强下:2H(g)+O(g)=2HO(g) ΔH=-a kJ·mol-1。下列叙述不正确的是( )
2 2 2
A.2 mol H (g)和1 mol O (g)完全反应生成2 mol H O(g)时放出a kJ的热量
2 2 2
B.2 mol H O(g)完全分解为2 mol H (g)和1 mol O (g)时吸收a kJ的热量
2 2 2
C.2 mol H (g)和1 mol O (g)完全反应生成2 mol H O(l)时放出的热量小于a kJ
2 2 2
D.1 mol H (g)和0.5 mol O(g)完全反应生成1 mol H O(g)时放出0.5a kJ的热量
2 2 2
【答案】C
【解析】由热化学方程式可知,A项正确;反应逆向发生时,热量的数值不变,B项正确;等量的反
应物生成液态水比生成气态水放出的热量多,C项错误;反应物的物质的量减半,反应热也减半,D项正
确。
16.工业生产硫酸过程中,SO 在接触室中被催化氧化为SO 气体,已知该反应为放热反应。现将2
2 3
mol SO 、1 mol O 充入一密闭容器充分反应后,放出热量98.3 kJ,此时测得SO 的转化率为50%,则下列
2 2 2
热化学方程式正确的是( )A.2SO (g)+O(g) 2SO (g) ΔH=+196.6 kJ·mol-1
2 2 3
B.2SO (g)+O(g) 2SO (g) ΔH=-98.3 kJ·mol-1
2 2 3
C.SO (g)+ O(g) SO (g) ΔH=-98.3 kJ·mol-1
2 2 3
D.SO (g)+ O(g) SO (g) ΔH=-196.6 kJ·mol-1
2 2 3
【答案】C
【解析】2mol SO 、1mol O 充入恒容容器中,达平衡时,SO 的转化率为50%,则反应了的SO 的物
2 2 2 2
质的量为1mol,放出热量98.3kJ,则每反应1molSO ,放出98.3kJ的热量,故热化学方程式为:2SO (g)
2 2
+O (g) 2SO (g) H=-196.6 kJ•mol-1或SO (g)+ O(g) SO (g),△H=-98.3 kJ•mol-1,由此判
2 3 2 2 3
△
断各选项热化学方程式正误。A项,反应是放热反应,ΔH小于0,故A错误;B项,热化学方程式中反应
热和对应二氧化硫的量不符合,故B错误;C项,选项中的热化学方程式符合题意,故C正确;D项,热
化学方程式中反应热和对应二氧化硫的量不符合,故D错误;故选C。
17.工业生产硫酸过程中,SO 在接触室中被催化氧化为SO 气体,已知该反应为放热反应。现将2
2 3
mol SO 、1 mol O 充入一密闭容器充分反应后,放出热量98.3 kJ,此时测得SO 的转化率为50%,则下列
2 2 2
热化学方程式正确的是( )
A.2SO (g)+O(g) 2SO (g) ΔH=+196.6 kJ·mol-1
2 2 3
B.2SO (g)+O(g) 2SO (g) ΔH=-98.3 kJ·mol-1
2 2 3
C.SO (g)+ O(g) SO (g) ΔH=-98.3 kJ·mol-1
2 2 3
D.SO (g)+ O(g) SO (g) ΔH=-196.6 kJ·mol-1
2 2 3
【答案】C
【解析】2mol SO 、1mol O 充入恒容容器中,达平衡时,SO 的转化率为50%,则反应了的SO 的物
2 2 2 2
质的量为1mol,放出热量98.3kJ,则每反应1molSO ,放出98.3kJ的热量,故热化学方程式为:2SO (g)
2 2
+O (g) 2SO (g) H=-196.6 kJ•mol-1或SO (g)+ O(g) SO (g),△H=-98.3 kJ•mol-1,由此判
2 3 2 2 3
△
断各选项热化学方程式正误。A项,反应是放热反应,ΔH小于0,故A错误;B项,热化学方程式中反应
热和对应二氧化硫的量不符合,故B错误;C项,选项中的热化学方程式符合题意,故C正确;D项,热化学方程式中反应热和对应二氧化硫的量不符合,故D错误;故选C。
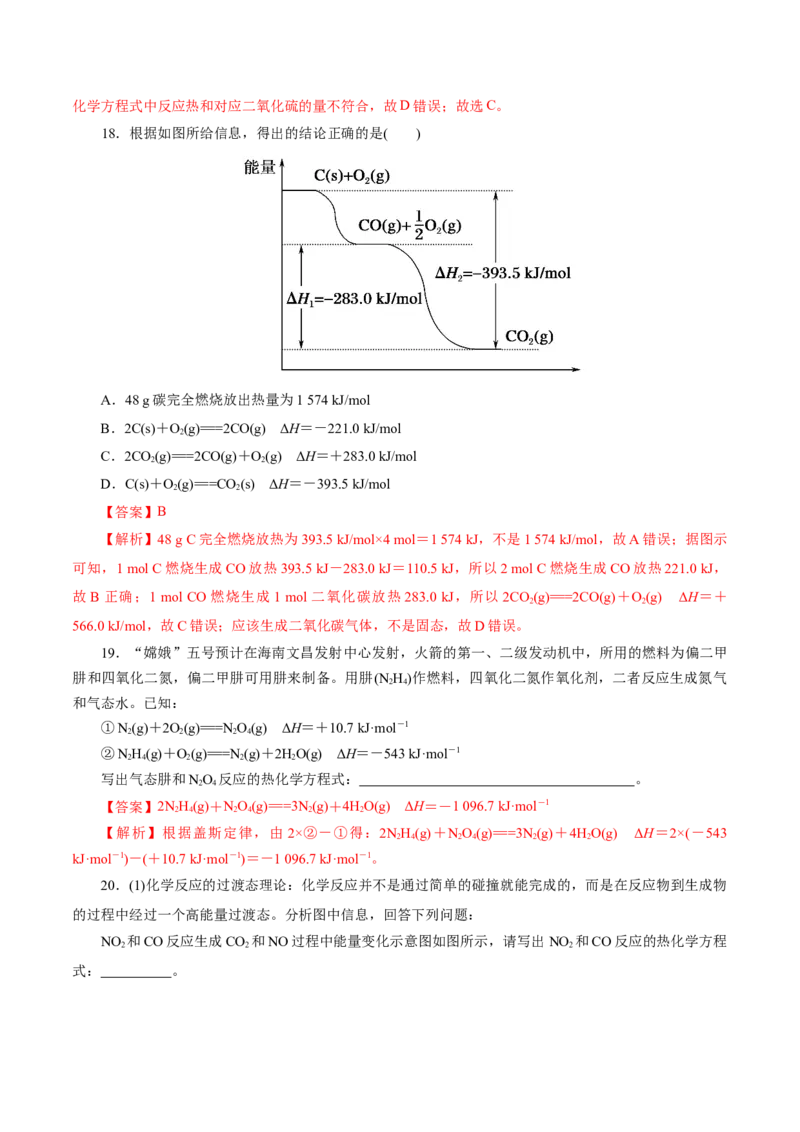
18.根据如图所给信息,得出的结论正确的是( )
A.48 g碳完全燃烧放出热量为1 574 kJ/mol
B.2C(s)+O(g)===2CO(g) ΔH=-221.0 kJ/mol
2
C.2CO(g)===2CO(g)+O(g) ΔH=+283.0 kJ/mol
2 2
D.C(s)+O(g)===CO (s) ΔH=-393.5 kJ/mol
2 2
【答案】B
【解析】48 g C完全燃烧放热为393.5 kJ/mol×4 mol=1 574 kJ,不是1 574 kJ/mol,故A错误;据图示
可知,1 mol C燃烧生成CO放热393.5 kJ-283.0 kJ=110.5 kJ,所以2 mol C燃烧生成CO放热221.0 kJ,
故B正确;1 mol CO燃烧生成1 mol二氧化碳放热283.0 kJ,所以2CO(g)===2CO(g)+O(g) ΔH=+
2 2
566.0 kJ/mol,故C错误;应该生成二氧化碳气体,不是固态,故D错误。
19.“嫦娥”五号预计在海南文昌发射中心发射,火箭的第一、二级发动机中,所用的燃料为偏二甲
肼和四氧化二氮,偏二甲肼可用肼来制备。用肼(N H)作燃料,四氧化二氮作氧化剂,二者反应生成氮气
2 4
和气态水。已知:
①N(g)+2O(g)===N O(g) ΔH=+10.7 kJ·mol-1
2 2 2 4
②NH(g)+O(g)===N (g)+2HO(g) ΔH=-543 kJ·mol-1
2 4 2 2 2
写出气态肼和NO 反应的热化学方程式: 。
2 4
【答案】2NH(g)+NO(g)===3N (g)+4HO(g) ΔH=-1 096.7 kJ·mol-1
2 4 2 4 2 2
【解析】根据盖斯定律,由 2×②-①得:2NH(g)+NO(g)===3N (g)+4HO(g) ΔH=2×(-543
2 4 2 4 2 2
kJ·mol-1)-(+10.7 kJ·mol-1)=-1 096.7 kJ·mol-1。
20.(1)化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物
的过程中经过一个高能量过渡态。分析图中信息,回答下列问题:
NO 和CO反应生成CO 和NO过程中能量变化示意图如图所示,请写出NO 和CO反应的热化学方程
2 2 2
式: 。(2)CO 的回收与利用是科学家研究的热点课题,可利用CH 与CO 制备“合成气”(CO、H),还可制
2 4 2 2
备甲醇、二甲醚、碳基燃料等产品。
科学家提出制备“合成气”反应历程分两步:
第一步:CH(g) C(ads)+2H(g)(慢反应);
4 2
第二步:C(ads)+CO (g) 2CO(g)(快反应)。
2
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:
CH 与CO 制备“合成气”的热化学方程式为 。
4 2
【答案】(1)NO (g)+CO(g)=CO (g)+NO(g) ΔH=-234 kJ·mol-1
2 2
(2)CH (g)+CO (g) 2CO(g)+2H(g) ΔH=+(E-E ) kJ·mol-1
4 2 2 3 1
【解析】(1)根据图像分析,该反应的热化学方程式为 NO (g)+CO(g)=CO (g)+NO(g) ΔH=+134
2 2
kJ·mol-1 -368 kJ·mol-1 =-234 kJ·mol-1。(2)由图可知,CH 与CO 制备“合成气”的热化学方程式为 CH(g)
4 2 4
+CO (g) 2CO(g)+2H(g) ΔH=+(E-E ) kJ· mol-1。
2 2 3 1
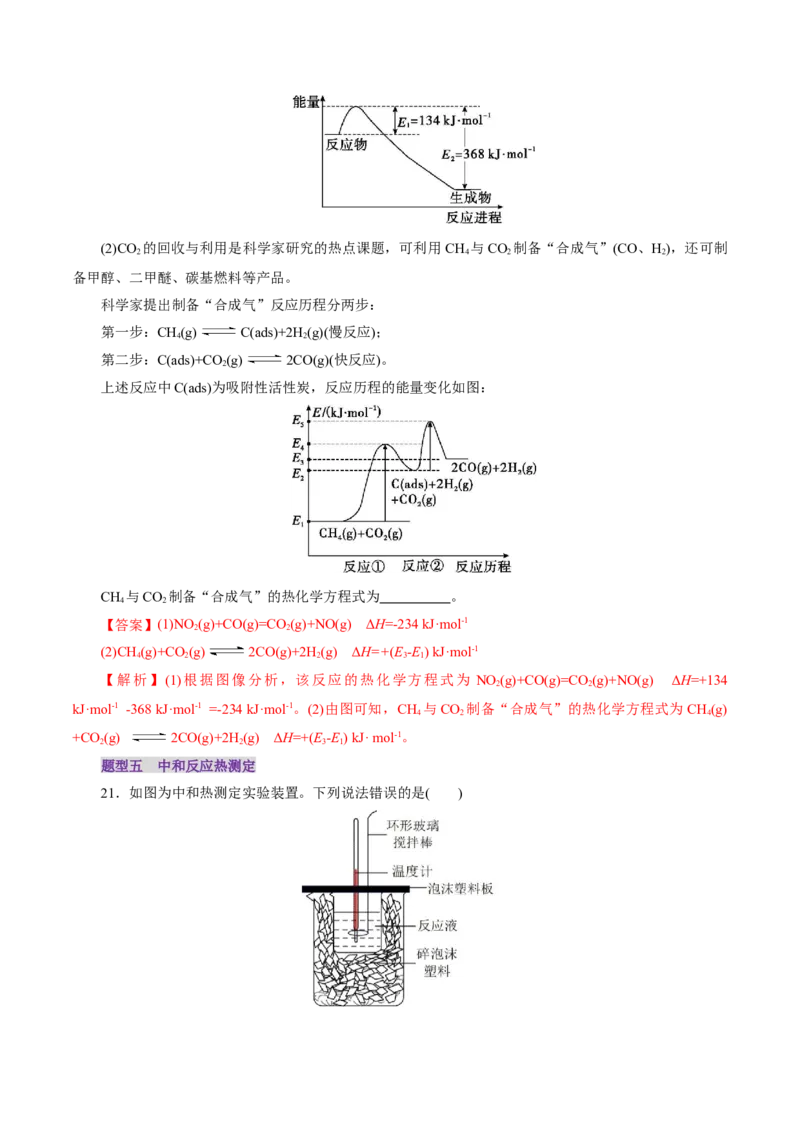
题型五 中和反应热测定
21.如图为中和热测定实验装置。下列说法错误的是( )A.使用环形玻璃搅拌棒是为了使反应更充分
B.用硫酸和Ba(OH) 溶液代替盐酸和氢氧化钠溶液,测得的中和热数值相同
2
C.温度计测量过盐酸的温度后,应先把温度计上的酸用水冲洗干净后,再测量NaOH溶液的温度
D.小烧杯和大烧杯的杯口相平
【答案】B
【解析】A项,使用环形玻璃搅拌棒是为了使反应物充分混合,反应更充分,故A正确;B项,用硫
酸和Ba(OH) 溶液代替盐酸和氢氧化钠溶液,除了发生中和反应,还生成了BaSO 沉淀,生成沉淀的过程
2 4
会放热,使测得的中和热数值偏大,故B错误;C项,温度计上残留的酸需要清洗干净,否则会和NaOH
溶液反应,使测得NaOH溶液的温度偏高,故C正确;D项,两杯口相平,可使盖板把杯口尽量盖严,从
而减少热量散失,故D正确;故选B。
22.将温度为20.0℃、浓度为0.50mol·L-1的盐酸和0.55mol·L-1的NaOH溶液各50mL(溶液密度均为
1g·mL-1)在简易量热计中混合,生成溶液的比热容c=4.18J·g-1·℃-1,轻轻搅动,测得混合溶液的终止温度是
23.4℃。下列说法错误的是
A.实验中测得的终止温度应是混合溶液的最高温度
B.实验中测得的中和热ΔH=-56.8kJ·mol-1
C.如果用50mL0.025mol·L-1的浓硫酸代替盐酸进行实验,测得的中和热△H会增大
D.如果用等体积等浓度的醋酸代替盐酸,其他均不变,则测得混合溶液的终止温度低于23.4℃
【答案】C
【解析】A项,实验中终止温度是充分反应后混合液的最高温度,A项正确;B项,酸为0.025mol,
碱是过量的,应根据酸的量进行计算,即反应生成了0.025molHO,根据实验数据算出生成1molH O所放
2 2
出的热量,即中和热ΔH=-[4.18×(50+50)×(23.4-20.0)×10-3]÷0.025=-56.8kJ/mol,B项正确;C项,采用浓硫
酸进行实验,放出的热量更多,ΔH减小,C项错误;D项,由于醋酸电离吸热,所以反应放出的热量会减
少,混合溶液的终止温度会低于23.4°C,D项正确;故选C。
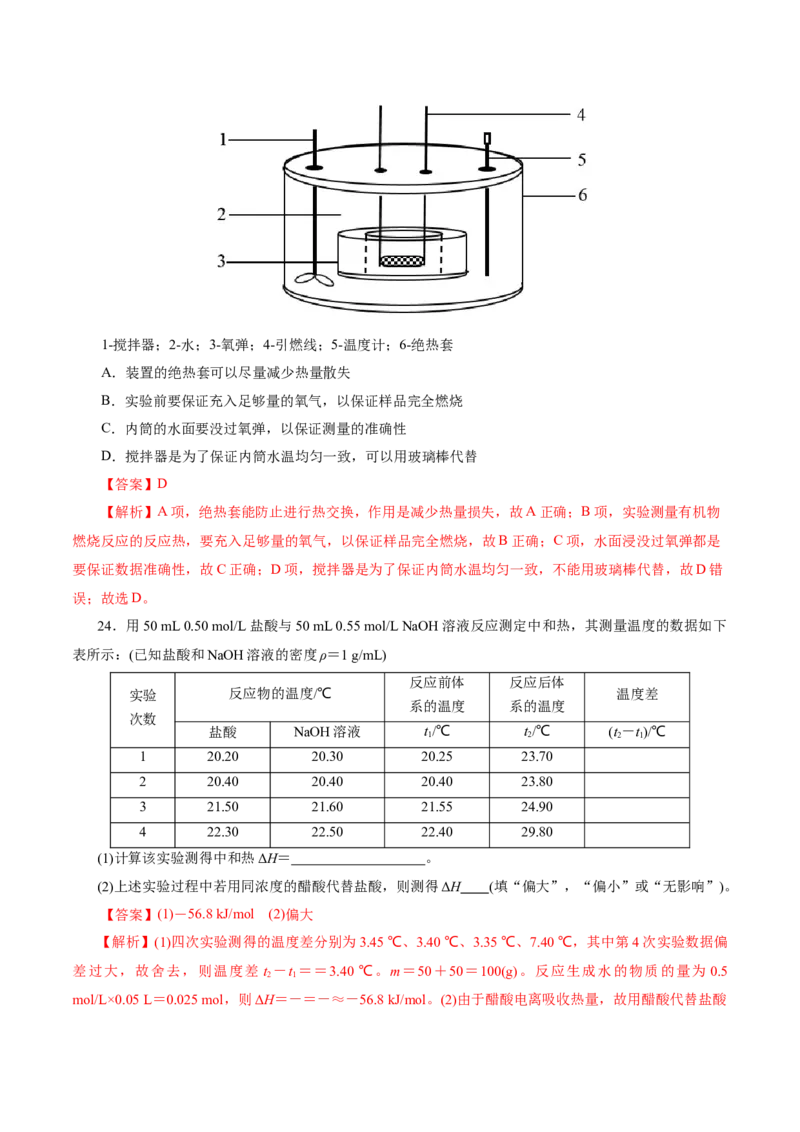
23.如图是一种弹式热量计装置,测量有机物燃烧反应的恒容反应热。通常的使用过程是将样品放入
不锈钢氧弹内,并充入氧气进行点火燃烧,整个氧弹放入装有水的内筒中,由温度传感器实时记录温度数
据进行热量计算。下列说法不正确的是1-搅拌器;2-水;3-氧弹;4-引燃线;5-温度计;6-绝热套
A.装置的绝热套可以尽量减少热量散失
B.实验前要保证充入足够量的氧气,以保证样品完全燃烧
C.内筒的水面要没过氧弹,以保证测量的准确性
D.搅拌器是为了保证内筒水温均匀一致,可以用玻璃棒代替
【答案】D
【解析】A项,绝热套能防止进行热交换,作用是减少热量损失,故A正确;B项,实验测量有机物
燃烧反应的反应热,要充入足够量的氧气,以保证样品完全燃烧,故B正确;C项,水面浸没过氧弹都是
要保证数据准确性,故C正确;D项,搅拌器是为了保证内筒水温均匀一致,不能用玻璃棒代替,故D错
误;故选D。
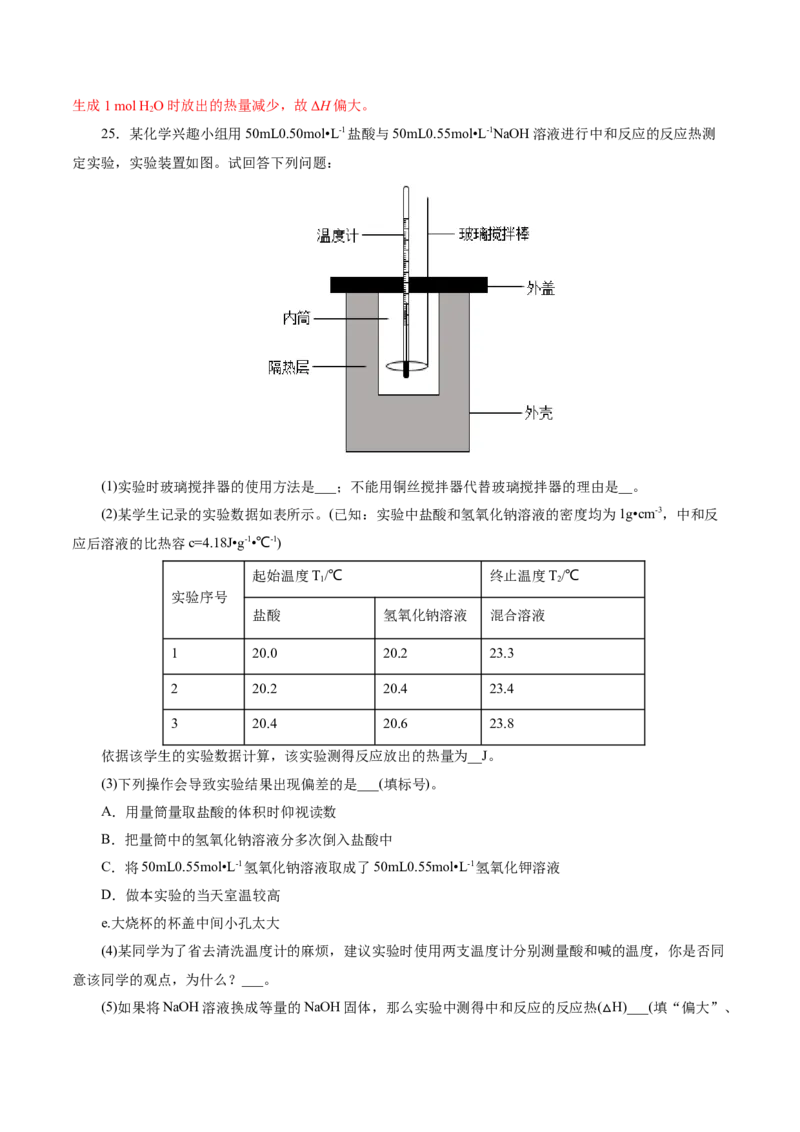
24.用50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液反应测定中和热,其测量温度的数据如下
表所示:(已知盐酸和NaOH溶液的密度ρ=1 g/mL)
反应前体 反应后体
实验 反应物的温度/℃ 温度差
系的温度 系的温度
次数
盐酸 NaOH溶液 t/℃ t/℃ (t-t)/℃
1 2 2 1
1 20.20 20.30 20.25 23.70
2 20.40 20.40 20.40 23.80
3 21.50 21.60 21.55 24.90
4 22.30 22.50 22.40 29.80
(1)计算该实验测得中和热ΔH= 。
(2)上述实验过程中若用同浓度的醋酸代替盐酸,则测得ΔH (填“偏大”,“偏小”或“无影响”)。
【答案】(1)-56.8 kJ/mol (2)偏大
【解析】(1)四次实验测得的温度差分别为3.45 ℃、3.40 ℃、3.35 ℃、7.40 ℃,其中第4次实验数据偏
差过大,故舍去,则温度差 t -t ==3.40 ℃。m=50+50=100(g)。反应生成水的物质的量为 0.5
2 1
mol/L×0.05 L=0.025 mol,则ΔH=-=-≈-56.8 kJ/mol。(2)由于醋酸电离吸收热量,故用醋酸代替盐酸生成1 mol H O时放出的热量减少,故ΔH偏大。
2
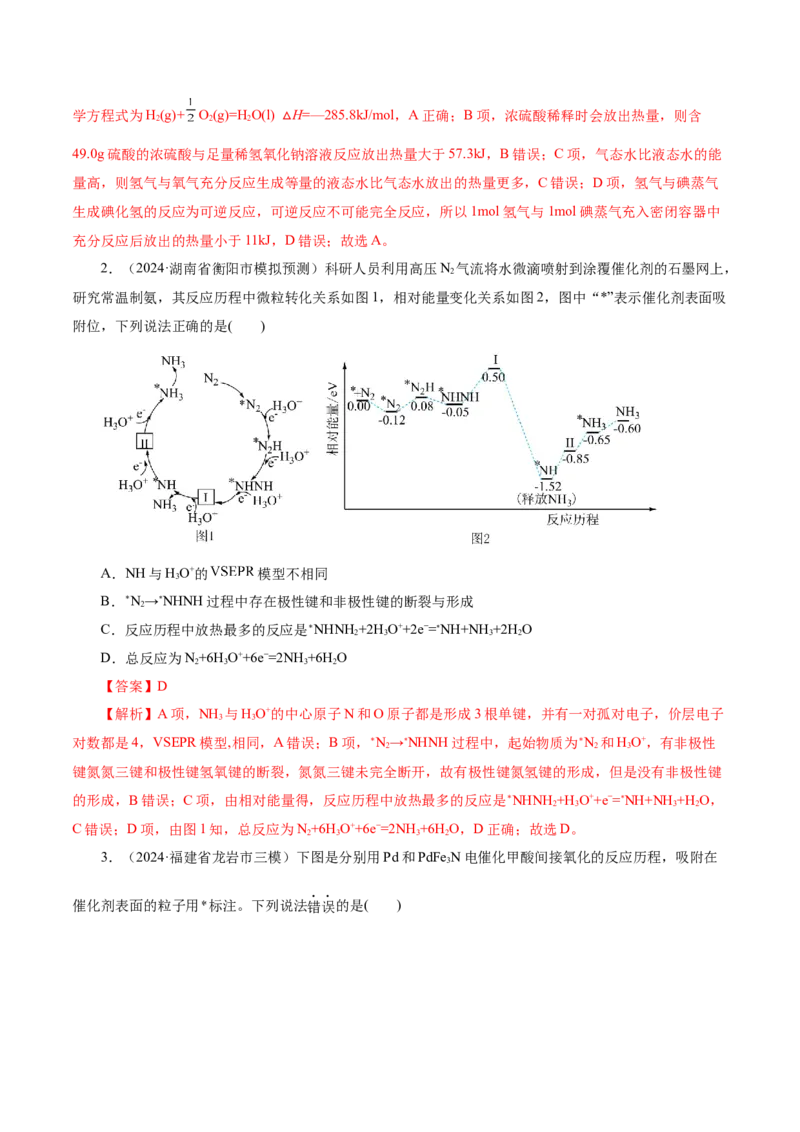
25.某化学兴趣小组用50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行中和反应的反应热测
定实验,实验装置如图。试回答下列问题:
(1)实验时玻璃搅拌器的使用方法是___;不能用铜丝搅拌器代替玻璃搅拌器的理由是__。
(2)某学生记录的实验数据如表所示。(已知:实验中盐酸和氢氧化钠溶液的密度均为1g•cm-3,中和反
应后溶液的比热容c=4.18J•g-1•℃-1)
起始温度T/℃ 终止温度T/℃
1 2
实验序号
盐酸 氢氧化钠溶液 混合溶液
1 20.0 20.2 23.3
2 20.2 20.4 23.4
3 20.4 20.6 23.8
依据该学生的实验数据计算,该实验测得反应放出的热量为__J。
(3)下列操作会导致实验结果出现偏差的是___(填标号)。
A.用量筒量取盐酸的体积时仰视读数
B.把量筒中的氢氧化钠溶液分多次倒入盐酸中
C.将50mL0.55mol•L-1氢氧化钠溶液取成了50mL0.55mol•L-1氢氧化钾溶液
D.做本实验的当天室温较高
e.大烧杯的杯盖中间小孔太大
(4)某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别测量酸和喊的温度,你是否同
意该同学的观点,为什么?___。
(5)如果将NaOH溶液换成等量的NaOH固体,那么实验中测得中和反应的反应热( H)___(填“偏大”、
△“偏小”或“不变”)。
(6)如果用60mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行实验,与上述实验相比,二者所放
出的热量___(填“相等”或“不相等”,下同),所求的中和反应H+(aq)+OH-(aq)=H O(1) H的反应热
2
( H)___。 △
△ 【答案】(1)上下搅动 Cu是热的良导体,传热快,热量损失大
(2)1337.6 (3)abe
(4)不同意,因为不同的温度计误差不同
(5)偏小 (6) 不相等 相等
【解析】(1)实验时为防止打断温度计,玻璃搅拌器的使用方法是上下搅动;Cu是热的良导体,传热
快,热量损失大,所以不能用铜丝搅拌器代替玻璃搅拌器;(2)三次温度差分别为:3.2℃、3.1℃、3.3℃,
温度的平均值为3.2℃,溶液的总质量为100g,该实验测得反应放出的热量为Q=
;(3)a项,用量筒量取盐酸的体积时仰视读数,使盐酸的体积不准确,
会导致实验结果出现偏差,故a选;b项,把量筒中的氢氧化钠溶液分多次倒入盐酸中,会使热量散失,
会导致实验结果出现偏差,故b选;c项,将50mL0.55mol•L-1氢氧化钠溶液取成了50mL0.55mol•L-1氢氧化
钾溶液,氢氧根的量不变,对实验结果没有影响,故c不选;d项,做本实验的当天室温较高,但测量的
是温度差,与室温无关,对实验结果没有影响,故d不选;e项,大烧杯的杯盖中间小孔太大,会使热量
散失,会导致实验结果出现偏差,故e选;故选abe;(4)因为不同的温度计误差不同,所以不能使用两支
温度计分别测量酸和喊的温度;(5)如果将NaOH溶液换成等量的NaOH固体,由于氢氧化钠固体溶解会放
出热量,导致放热增多,使实验测得中和反应的反应热( H)偏小;(6)如果用60mL0.50mol•L-1盐酸与
50mL0.55mol•L-1NaOH溶液进行实验,由于试剂的量不同△,所放出的热量与上述实验不相等,但中和热是
换算成生成1mol水时放出的热量,所求的中和反应的反应热( H)与上述反应相等。
题型六 盖斯定律及应用 △
26.黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为S(s)+2KNO (s)+3C(s)=K S(s)+N (g)
3 2 2
+3CO (g) ΔH=x kJ·mol-1。
2
已知:碳的燃烧热ΔH=a kJ·mol-1;
1
S(s)+2K(s)=K S(s) ΔH=b kJ·mol-1;
2 2
2K(s)+N (g)+3O(g)=2KNO (s) ΔH=c kJ·mol-1。
2 2 3 3
则x为 ( )
A.3a+b-c B.c+3a-b C.a+b-c D.c+a-b
【答案】A
【解析】已知碳的燃烧热为ΔH=a kJ·mol-1,则碳燃烧的热化学方程式为①C(s)+O(g)=CO (g) ΔH=a
1 2 2 1
kJ·mol-1 , 又 已 知 ② S(s)+2K(s)=K S(s) ΔH=b kJ·mol-1 , ③ 2K(s)+N (g)+3O(g)=2KNO (s) ΔH=c
2 2 2 2 3 3kJ·mol-1,根据盖斯定律,可得ΔH=3ΔH+ΔH—ΔH,即x=3a+b-c,A项正确。
1 2 3
27.通过以下反应可获得新型能源二甲醚(CHOCH )。下列说法不正确的是( )
3 3
①C(s)+HO(g)=CO(g)+H (g) ΔH=a kJ·mol-1
2 2 1
②CO(g)+HO(g)=CO(g)+H(g) ΔH=b kJ·mol-1
2 2 2 2
③CO(g)+3H(g)=CH OH(g)+H O(g) ΔH=c kJ·mol-1
2 2 3 2 3
④2CHOH(g)=CH OCH (g)+HO(g) ΔH=d kJ·mol-1
3 3 3 2 4
A.反应①②为反应③提供原料气
B.反应③也是CO 资源化利用的方法之一
2
1 1 d
C.反应CHOH(g)= CHOCH (g)+ HO(l)的ΔH= kJ·mol-1
3 2 3 3 2 2 2
D.反应2CO(g)+4H(g)=CH OCH (g)+HO(g)的ΔH=(2b+2c+d) kJ·mol-1
2 3 3 2
【答案】C
【解析】反应①的产物为CO和H,反应②的产物为CO 和H,反应③的原料为CO 和H,A项正确;
2 2 2 2 2
反应③将温室气体CO 转化为燃料CHOH,B项正确;反应④生成物中HO为气态,C项生成物中HO为
2 3 2 2
d
液态,故C项中反应的焓变不为 kJ·mol-1,C项错误;依据盖斯定律可知,由②×2+③×2+④可得所求反
2
应及其焓变,D项正确。
28.已知室温下,将 CuSO ·5H O(s)溶于水会使溶液温度降低, 将 CuSO (s)溶于水会使溶液温度升
4 2 4
高。则下列能量转化关系的判断不正确的是
A. △H>0 B. △H>△H C. △H>△H D. △H= H+ H
1 2 3 3 1 2 1 3
【答案】C △ △
【解析】A项,将 CuSO ·5H O(s)溶于水会使溶液温度降低,说明是吸热反应,△H>0,△H>0,A
4 2 1 2
正确;B项,由CuSO ·5H O(s)= CuSO (s) +·5H O(l),知△H>△H,B正确;C项,将 CuSO (s)溶于水会
4 2 4 2 2 3 4
使溶液温度升高说明是放热反应,△H<0因为△H>0故△H>△H 是错的;C错误;根据上述关系和盖
3 1 3 1
斯定律知△H= H+ H,D正确。
2 1 3
△ △
29.2 mol金属钠和l mol氯气反应的能量关系如图所示,下列说法不正确的是( )A.原子失电子为吸热过程,相同条件下,K(s)的( H'+△H')-( H+△H)
2 3 4 5 6 7
D.2Na(s)+Cl
2
(g)=2NaCl(s)在较低△温度下自发进行
【答案】C
【解析】A项,原子失电子为吸热过程,相同条件下,K与Na同一主族,电离能同主族从上到下逐渐
减小,K(s)的( H'+△H')0
2 6 2 4
【答案】C
【解析】A项,中间体1→过渡态2的正反应活化能最大,反应速率最慢,是决定反应速率的步骤,A
正确;B项,Co可活化C H 放出CH,Co-H键的形成使H原子发生了迁移,B正确;C项,根据反应历
2 6 4
程可知,涉及到C-C键的断裂和C-H键形成,没有涉及非极性键的形成,C错误;D项,由起点和终点物
质可知,反应物的总能量低于生成物的总能量,该反应是吸热反应,总反应为Co(s)+C H(g)→CoCH(s)
2 6 2
+CH (g)∆H>0,D正确;故选C。
4
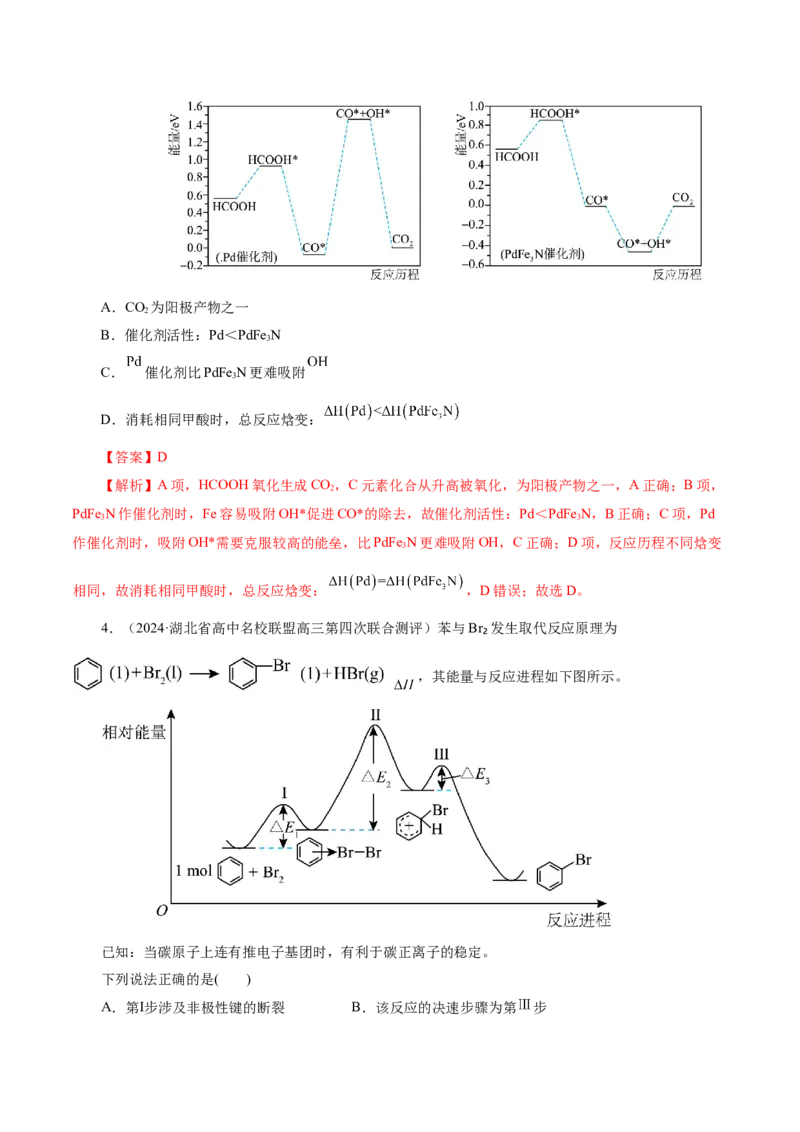
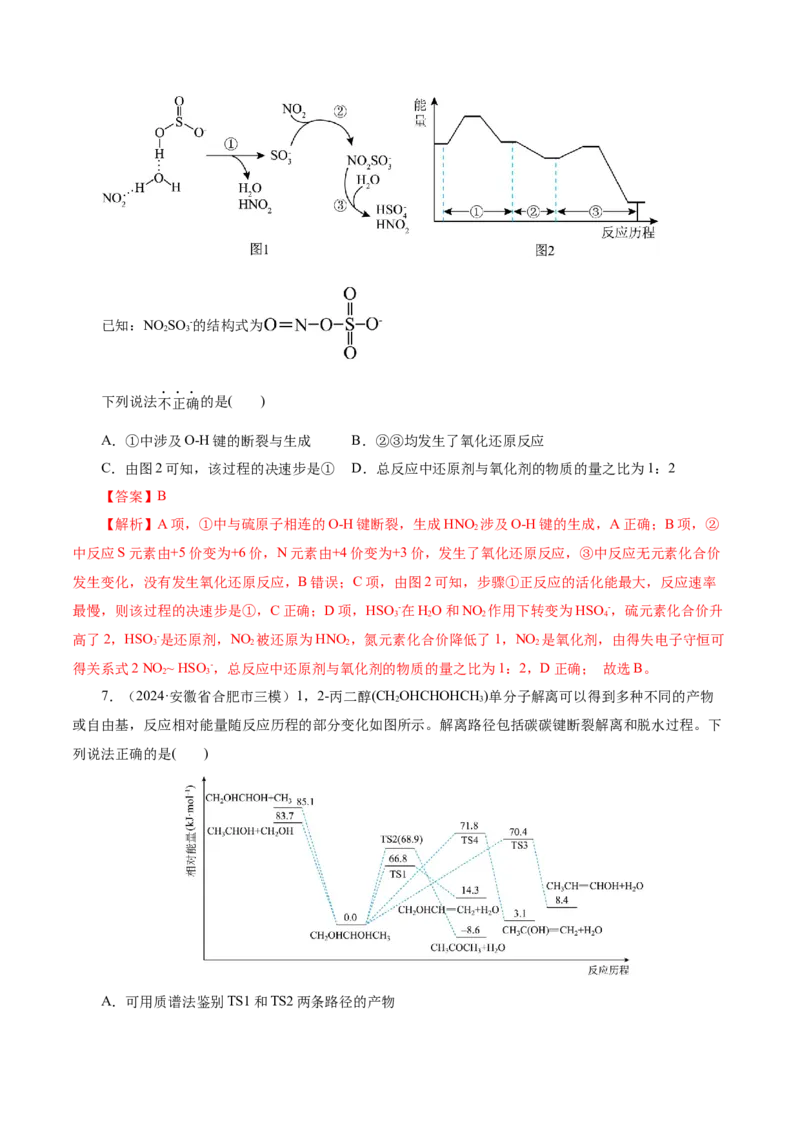
6.(2024·北京市东城区二模)科学家提出一种大气中HSO -在HO和NO 作用下转变为HSO -的机理
3 2 2 4
(图1),其能量变化如图2所示。已知:NO SO -的结构式为
2 3
下列说法不正确的是( )
A.①中涉及O-H键的断裂与生成 B.②③均发生了氧化还原反应
C.由图2可知,该过程的决速步是① D.总反应中还原剂与氧化剂的物质的量之比为1:2
【答案】B
【解析】A项,①中与硫原子相连的O-H键断裂,生成HNO 涉及O-H键的生成,A正确;B项,②
2
中反应S元素由+5价变为+6价,N元素由+4价变为+3价,发生了氧化还原反应,③中反应无元素化合价
发生变化,没有发生氧化还原反应,B错误;C项,由图2可知,步骤①正反应的活化能最大,反应速率
最慢,则该过程的决速步是①,C正确;D项,HSO -在HO和NO 作用下转变为HSO -,硫元素化合价升
3 2 2 4
高了2,HSO -是还原剂,NO 被还原为HNO,氮元素化合价降低了1,NO 是氧化剂,由得失电子守恒可
3 2 2 2
得关系式2 NO~ HSO -,总反应中还原剂与氧化剂的物质的量之比为1:2,D正确; 故选B。
2 3
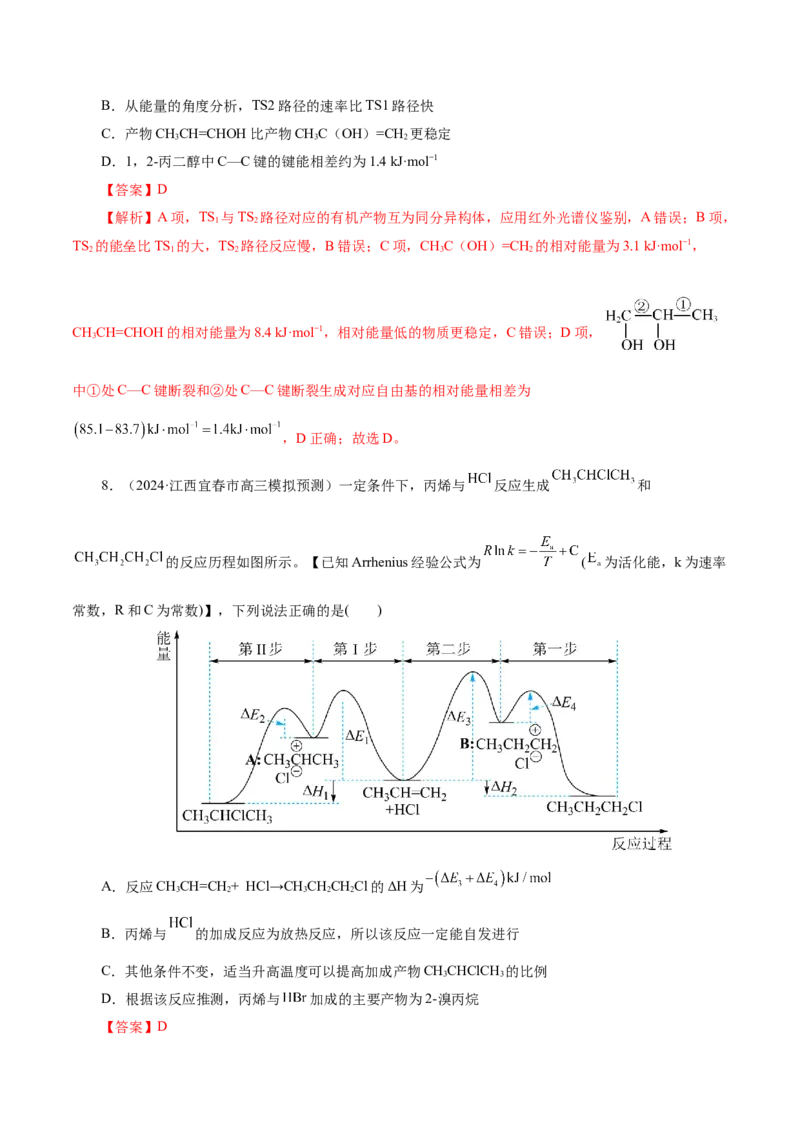
7.(2024·安徽省合肥市三模)1,2-丙二醇(CHOHCHOHCH )单分子解离可以得到多种不同的产物
2 3
或自由基,反应相对能量随反应历程的部分变化如图所示。解离路径包括碳碳键断裂解离和脱水过程。下
列说法正确的是( )
A.可用质谱法鉴别TS1和TS2两条路径的产物B.从能量的角度分析,TS2路径的速率比TS1路径快
C.产物CHCH=CHOH比产物CHC(OH)=CH 更稳定
3 3 2
D.1,2-丙二醇中C—C键的键能相差约为1.4 kJ·mol−1
【答案】D
【解析】A项,TS 与TS 路径对应的有机产物互为同分异构体,应用红外光谱仪鉴别,A错误;B项,
1 2
TS 的能垒比TS 的大,TS 路径反应慢,B错误;C项,CHC(OH)=CH 的相对能量为3.1 kJ·mol−1,
2 1 2 3 2
CHCH=CHOH的相对能量为8.4 kJ·mol−1,相对能量低的物质更稳定,C错误;D项,
3
中①处C—C键断裂和②处C—C键断裂生成对应自由基的相对能量相差为
,D正确;故选D。
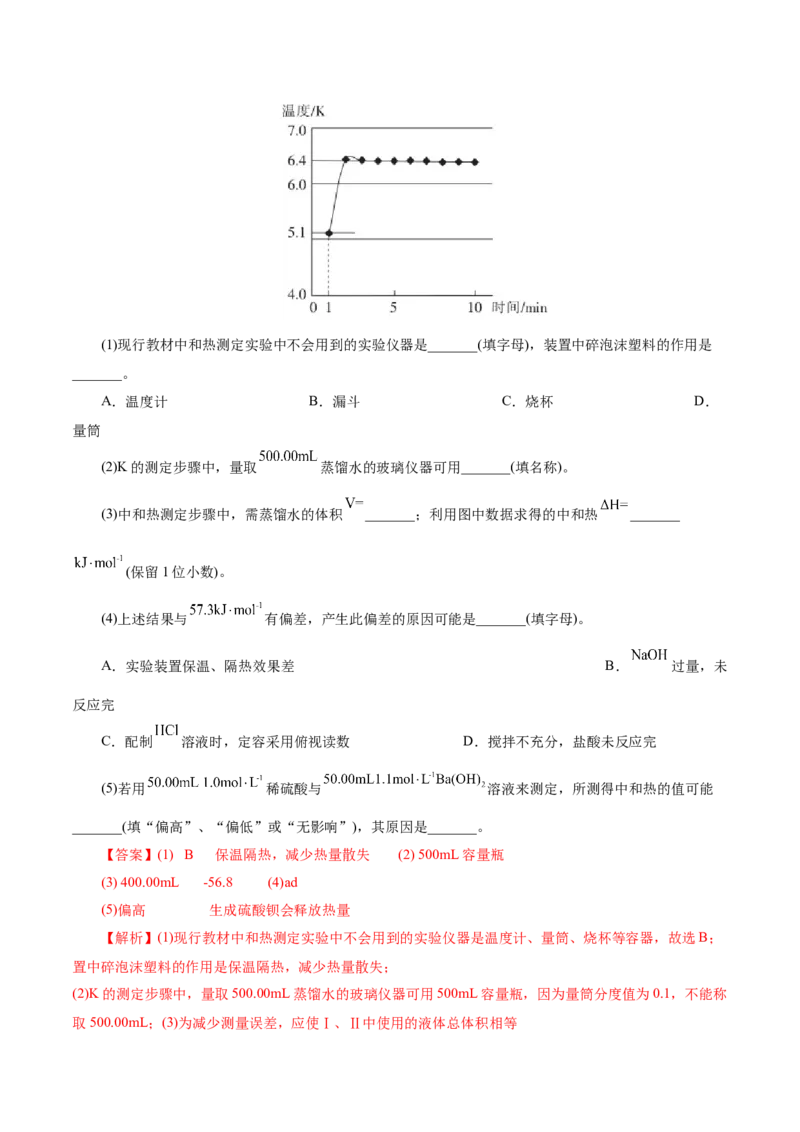
8.(2024·江西宜春市高三模拟预测)一定条件下,丙烯与 反应生成 和
的反应历程如图所示。【已知Arrhenius经验公式为 ( 为活化能,k为速率
常数,R和C为常数)】,下列说法正确的是( )
A.反应CHCH=CH+ HCl→CHCHCHCl的ΔH为
3 2 3 2 2
B.丙烯与 的加成反应为放热反应,所以该反应一定能自发进行
C.其他条件不变,适当升高温度可以提高加成产物CHCHClCH 的比例
3 3
D.根据该反应推测,丙烯与 加成的主要产物为2-溴丙烷
【答案】D【解析】A项,根据图示,不能求得反应CHCH=CH+ HCl→CHCHCHCl的ΔH,A错误;B项,
3 2 3 2 2
由图可知,丙烯与HCl加成生成CHCHClCH 或CHCHCHCl的反应都是放热反应,∆H<0,反应的∆S
3 3 3 2 2
<0,根据ΔH-TΔS<0时自发进行,反应在低温下能自发进行,B错误;C项,丙烯与HCl反应生成
CHCHClCH 和CHCHCHCl的反应都为放热反应,升高温度,反应都向着消耗CHCHClCH 和
3 3 3 2 2 3 3
CHCHCHCl的方向移动,CHCHClCH 和CHCHCHCl的比例都会降低,C错误;D项,由图中可以看
3 2 2 3 3 3 2 2
出生成CHCHClCH 的活化能较低,反应的主要产物为CHCHClCH ,类似的丙烯与HBr加成的主要产物
3 3 3 3
为2-溴丙烷,D正确;故选D。
9.随着科学技术的发展,实验仪器也在不断地变革。某化学兴趣小组利用如图所示的仪器来进行中
和热测定实验。
实验原理:
(K的物理意义是热量计升高 时所需的热量), (n为生成水的物质的量)。
实验步骤:
Ⅰ.热量计总热容常数K的测定:
反应瓶中放入 蒸馏水打开磁力搅拌器,搅拌。开启精密直流稳压电流,调节输出电压(电压
为5V)和电流.采集数据,并求出 。
Ⅱ.中和热的测定:
①将反应瓶中的水倒掉,用干布擦干,重新量取 蒸馏水注入其中,然后加入
溶液,再取 溶液注入储液管中。
②打开磁力搅拌器,搅拌。每分钟记录一次温差,记录到一分钟时,将玻璃棒提起,使储液管中碱与
酸混合反应。继续每分钟记录一次温差,测定10分钟。采集数据(如图所示)。(1)现行教材中和热测定实验中不会用到的实验仪器是_______(填字母),装置中碎泡沫塑料的作用是
_______。
A.温度计 B.漏斗 C.烧杯 D.
量筒
(2)K的测定步骤中,量取 蒸馏水的玻璃仪器可用_______(填名称)。
(3)中和热测定步骤中,需蒸馏水的体积 _______;利用图中数据求得的中和热 _______
(保留1位小数)。
(4)上述结果与 有偏差,产生此偏差的原因可能是_______(填字母)。
A.实验装置保温、隔热效果差 B. 过量,未
反应完
C.配制 溶液时,定容采用俯视读数 D.搅拌不充分,盐酸未反应完
(5)若用 稀硫酸与 溶液来测定,所测得中和热的值可能
_______(填“偏高”、“偏低”或“无影响”),其原因是_______。
【答案】(1) B 保温隔热,减少热量散失 (2) 500mL容量瓶
(3) 400.00mL -56.8 (4)ad
(5)偏高 生成硫酸钡会释放热量
【解析】(1)现行教材中和热测定实验中不会用到的实验仪器是温度计、量筒、烧杯等容器,故选B;
置中碎泡沫塑料的作用是保温隔热,减少热量散失;
(2)K的测定步骤中,量取500.00mL蒸馏水的玻璃仪器可用500mL容量瓶,因为量筒分度值为0.1,不能称
取500.00mL;(3)为减少测量误差,应使Ⅰ、Ⅱ中使用的液体总体积相等V=500.00mL-50.00mL-50.00mL=400.00mL,中和热测定步骤中,需蒸馏水的体积V=400.00mL;利用图中
数据可知起始温度为5.1K最后稳定温度为6.4K, T=6.4K-5.1K=1.3K,n=50.00mL×10-3×1.0
=0.05mol,求得的中和热 = ;(4)上述结果与
有偏差,产生此偏差的原因可能是:实验装置保温、隔热效果差导致热量损失,搅拌不充分,
盐酸未反应完,测得中和热不完全,故选ad;(5)若用 稀硫酸与
溶液来测定,所测得中和热的值可能偏高,其原因是生成硫酸钡会释放热量。
1.(2022·浙江省6月选考,18)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H O HO HO
2 2 2 2 2
24
能量/ kJ·mol-l 218 39 10 0 0
9
可根据HO(g)+HO(g)= H O(g)计算出HO 中氧氧单键的键能为214 kJ·mol-l。下列说法不正确的是(
2 2 2 2
)
A.H 的键能为436 kJ·mol-l
2
B.O 的键能大于HO 中氧氧单键的键能的两倍
2 2 2
C.解离氧氧单键所需能量: HOO<HO
2 2
D.HO(g)+O(g)= H O(g) ΔH=-143kJ·mol−1
2 2 2
【答案】C
【解析】A项,根据表格中的数据可知,H 的键能为218×2=436 kJ·mol-l,A正确;
2
B项,由表格中的数据可知O 的键能为:249×2=498 kJ·mol-l,由题中信息可知HO 中氧氧单键的键能为
2 2 2
214 kJ·mol-l,则O 的键能大于HO 中氧氧单键的键能的两倍,B正确;C项,由表格中的数据可知
2 2 2
HOO=HO+O,解离其中氧氧单键需要的能量为249+39-10=278 kJ·mol-l,HO 中氧氧单键的键能为214
2 2kJ·mol-l,C错误;D项,由表中的数据可知HO(g)+O(g)= H O(g)的 ,D
2 2 2
正确;故选C。
2.(2021•全国乙卷,1)我国提出争取在2030年前实现碳达峰,2060年实现碳中和,这对于改善环境,
实现绿色发展至关重要。碳中和是指CO 的排放总量和减少总量相当。下列措施中能促进碳中和最直接有
2
效的是
A.将重质油裂解为轻质油作为燃料
B.大规模开采可燃冰作为新能源
C.通过清洁煤技术减少煤燃烧污染
D.研发催化剂将CO 还原为甲醇
2
【答案】D
【解析】A项,将重质油裂解为轻质油并不能减少二氧化碳的排放量,达不到碳中和的目的,故A不
符合题意; B项,大规模开采可燃冰做为新能源,会增大二氧化碳的排放量,不符合碳中和的要求,故B
不符合题意;C项,通过清洁煤技术减少煤燃烧污染,不能减少二氧化碳的排放量,达不到碳中和的目的,
故C不符合题意;D项,研发催化剂将二氧化碳还原为甲醇,可以减少二氧化碳的排放量,达到碳中和的
目的,故D符合题意;故选D。
3.(2021•浙江6月选考,21)相同温度和压强下,关于反应的 ,下列判断正确的是( )
A.ΔH>0,ΔH>0 B.ΔH=ΔH+ΔH
1 2 3 1 2
C.ΔH>ΔH,ΔH>ΔH D.ΔH=ΔH+ΔH
1 2 3 2 2 3 4
【答案】C
【解析】一般的烯烃与氢气发生的加成反应为放热反应,但是,由于苯环结构的特殊性决定了苯环结
构的稳定性,苯与氢气发生加成反应生成1,3-环己二烯时,破坏了苯环结构的稳定性,因此该反应为吸
热反应。A项,环己烯、1,3-环己二烯分别与氢气发生的加成反应均为放热反应,因此,ΔH<0,ΔH<
1 2
0,A不正确;B项,苯分子中没有碳碳双键,其中的碳碳键是介于单键和双键之间的特殊的共价键,因此,
其与氢气完全加成的反应热不等于环己烯、1,3-环己二烯分别与氢气发生的加成反应的反应热之和,即
ΔH≠ΔH+ΔH,B不正确;C项,环己烯、1,3-环己二烯分别与氢气发生的加成反应均为放反应,ΔH<
3 1 2 1
0,ΔH<0,由于1mol 1,3-环己二烯与氢气完全加成后消耗的氢气是等量环己烯的2倍,故其放出的热量
2
更多,其ΔH>ΔH;苯与氢气发生加成反应生成1,3-环己二烯的反应为吸热反应(ΔH >0),根据盖斯定
1 2 4律可知,苯与氢气完全加成的反应热ΔH=ΔH+ΔH,因此ΔH>ΔH,C正确;D项,根据盖斯定律可知,
3 4 2 3 2
苯与氢气完全加成的反应热ΔH=ΔH+ΔH,因此ΔH=ΔH-ΔH,D不正确。故选C。
3 4 2 2 3 4
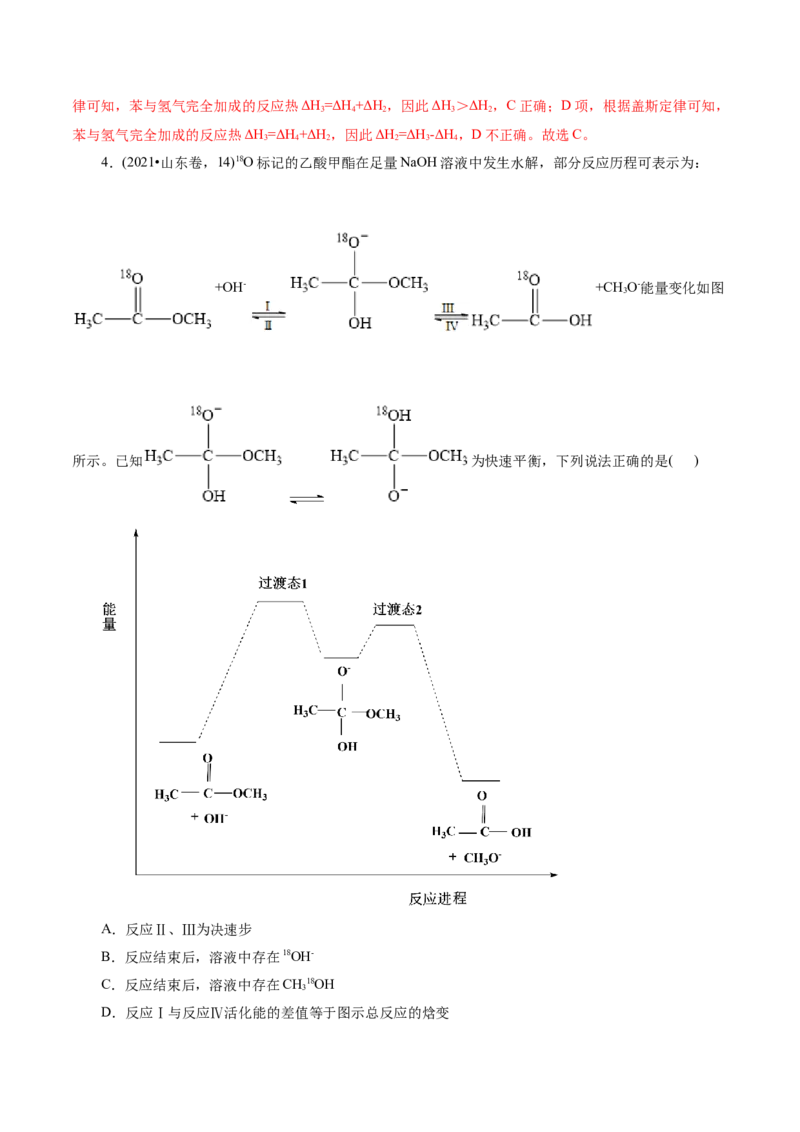
4.(2021•山东卷,14)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:
+OH- +CH O-能量变化如图
3
所示。已知 为快速平衡,下列说法正确的是( )
A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH18OH
3
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变【答案】B
【解析】A项,一般来说,反应的活化能越高,反应速率越慢,由图可知,反应I和反应IV的活化能
较高,因此反应的决速步为反应I、IV,故A错误;B项,反应I为加成反应,而 与
为快速平衡,反应II的成键和断键方式为 或 ,后者能生成
18OH-,因此反应结束后,溶液中存在18OH-,故B正确;C项,反应III的成键和断键方式为
或 ,因此反应结束后溶液中不会存在CH18H,故C错误;D项,该总反应对应反应物的总
3
能量高于生成物总能量,总反应为放热反应,因此 和CHO-的总能量与 和OH-的
3
总能量之差等于图示总反应的焓变,故D错误;故选B。
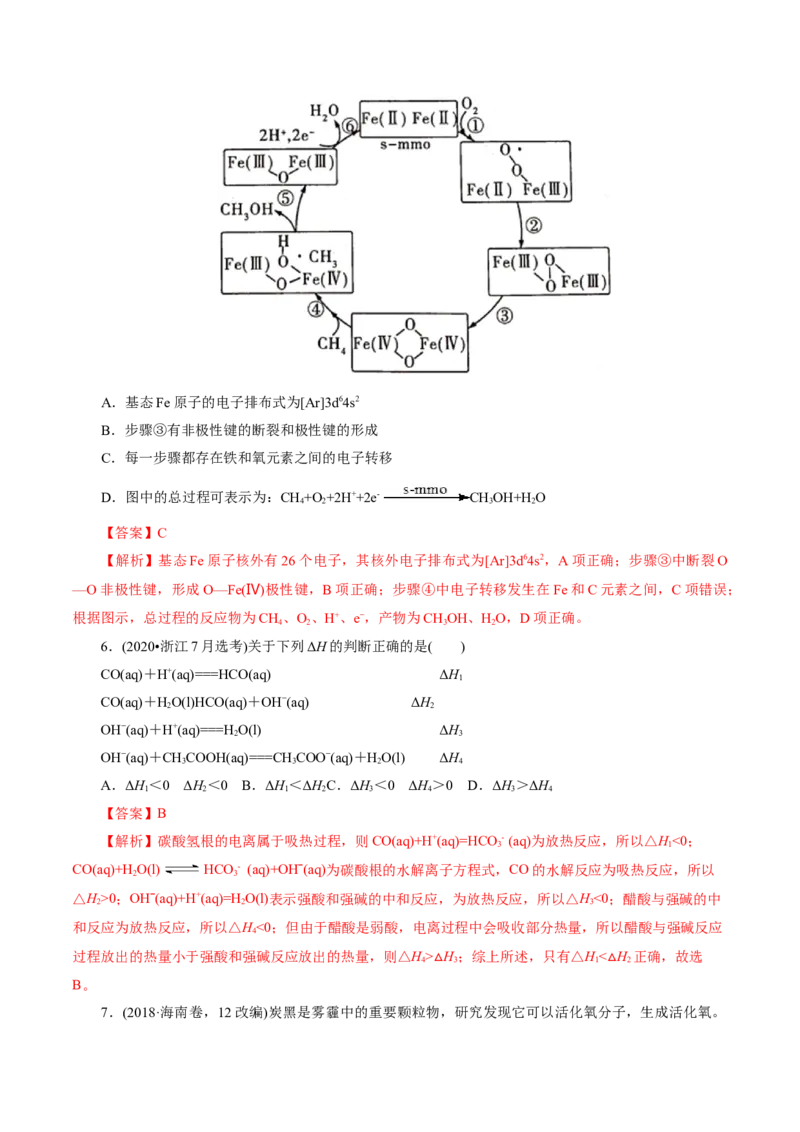
5.(2021•湖北选择性考试,12)甲烷单加氧酶(s-mmo)含有双核铁活性中心,是 O 氧化 CH 生成
2 4
CHOH的催化剂,反应过程如图所示。下列叙述错误的是( )
3A.基态Fe原子的电子排布式为[Ar]3d64s2
B.步骤③有非极性键的断裂和极性键的形成
C.每一步骤都存在铁和氧元素之间的电子转移
D.图中的总过程可表示为:CH+O +2H++2e- CHOH+H O
4 2 3 2
【答案】C
【解析】基态Fe原子核外有26个电子,其核外电子排布式为[Ar]3d64s2,A项正确;步骤③中断裂O
—O非极性键,形成O—Fe(Ⅳ)极性键,B项正确;步骤④中电子转移发生在Fe和C元素之间,C项错误;
根据图示,总过程的反应物为CH、O、H、e,产物为CHOH、HO,D项正确。
4 2 3 2
6.(2020•浙江7月选考)关于下列ΔH的判断正确的是( )
CO(aq)+H+(aq)===HCO(aq) ΔH
1
CO(aq)+HO(l)HCO(aq)+OH−(aq) ΔH
2 2
OH−(aq)+H+(aq)===HO(l) ΔH
2 3
OH−(aq)+CHCOOH(aq)===CHCOO−(aq)+HO(l) ΔH
3 3 2 4
A.ΔH<0 ΔH<0 B.ΔH<ΔH C.ΔH<0 ΔH>0 D.ΔH>ΔH
1 2 1 2 3 4 3 4
【答案】B
【解析】碳酸氢根的电离属于吸热过程,则CO(aq)+H+(aq)=HCO- (aq)为放热反应,所以△H<0;
3 1
CO(aq)+H O(l) HCO - (aq)+OHˉ(aq)为碳酸根的水解离子方程式,CO的水解反应为吸热反应,所以
2 3
△H>0;OHˉ(aq)+H+(aq)=H O(l)表示强酸和强碱的中和反应,为放热反应,所以△H<0;醋酸与强碱的中
2 2 3
和反应为放热反应,所以△H<0;但由于醋酸是弱酸,电离过程中会吸收部分热量,所以醋酸与强碱反应
4
过程放出的热量小于强酸和强碱反应放出的热量,则△H> H;综上所述,只有△H< H 正确,故选
4 3 1 2
B。 △ △
7.(2018·海南卷,12改编)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧。活化过程的能量变化模拟计算结果如图所示。活化氧可以快速氧化二氧化硫。下列说法正确的是( )
A.每活化一个氧分子吸收0.29 eV的能量
B.水可使氧分子活化反应的活化能降低0.42 eV
C.氧分子的活化是O—O键的断裂与C—O键的生成过程
D.炭黑颗粒不是大气中二氧化硫转化为三氧化硫的催化剂
【答案】C
【解析】根据能量变化图分析,最终结果为活化氧,体系能量降低,则每活化一个氧分子放出0.29 eV
的能量,故A项错误;根据能量图分析,没有水加入的反应活化能为 E=0.75 eV,有水加入的反应的活化
能为E=0.57 eV,所以水可使氧分子活化反应的活化能降低 0.75 eV-0.57 eV=0.18 eV,故B项错误;根
据图像分析,氧分子活化过程中O—O键断裂,生成C—O键,所以氧分子的活化是O—O键的断裂与C—
O键的生成过程,故C项正确;活化氧可以快速氧化SO ,而炭黑颗粒可以活化氧分子产生活化氧,所以
2
炭黑颗粒是大气中SO 转化为SO 的催化剂,故D项错误。
2 3