文档内容
第 02 讲 化学平衡状态、化学平衡的移动
01 模拟基础练
【题型一】化学平衡状态
【题型二】化学平衡移动
02 重难创新练
03 真题实战练
题型一 化学平衡状态
1.(2024·安徽六安·模拟预测)硫元素形成的化合物有着广泛的用途,其中过二硫酸 是一种强氧
化剂,可用作氧化剂和漂白剂,过二硫酸及其盐都是不稳定的,加热时分解,溶于水会发生一定程度的水
解,电解硫酸钾溶液可得过二硫酸钾。氮、硫的氧化物无害化、再利用具有重要意义,可利用下面反应进
行氮、硫的氧化物再利用:NO (g)+SO(g) SO (g)+NO(g) ΔH=-83.6 kJ∙mol−1。下面说法正确的是
2 2 3
A.NO 、SO 体积比保持不变可用来判定平衡状态
2 2
B.加压可加快反应速率,使平衡时SO 产量提高
3
C.恒容条件下,投料物质的量比为1:1,若NO 平衡转化率为60%,则平衡常数为2.25
2
D.NO可直接用NaOH溶液吸收,制取NaNO
2
【答案】C
【解析】A.不确定两者初始投料比,不确定NO 、SO 体积比是否为变量,其保持不变不可用来判定平衡
2 2
状态,A错误;B.反应为气体分子数不变的反应,加压可加快反应速率,但不会使平衡时SO 产量提
3
高,B错误;C.恒容条件下,投料物质的量比为1:1,假设投料均为1mol,若NO 平衡转化率为60%,
2
反应二氧化氮、二氧化硫0.6mol,平衡时二氧化氮、二氧化硫0.4mol,三氧化硫、一氧化氮0.6mol,则平
衡常数为 ,C正确;D.NO不和氢氧化钠反应,不可直接用NaOH溶液吸收,D错误;故
选C。
2.(2024·海南·三模) 是廉价的碳资源,将其甲烷化具有重要意义。其原理为
。在某密闭容器中,充入1mol 和4mol 发生上述反
应。下列叙述正确的是
A.反应物的总能量小于生成物时总能量B.恒温、恒压条件下,充入He,平衡向逆反应方向移动
C.在恒温、恒容条件下进行反应,容器中气体密度不再变化,说明已达到平衡状态
D.升高温度可增大活化分子的百分数及有效碰撞频率,因而温度越高越利于获得甲烷
【答案】B
【解析】A.该反应是放热反应,故反应物的总能量小于生成物时总能量,故A错误;B.恒温、恒压条
件下,充入He,容器体积增大,平衡向逆反应方向移动,故B正确;C.在恒温、恒容条件下进行反应,
气体的密度始终不变,不能说明达到平衡,故C错误;D.升高温度平衡逆向移动,甲烷的产率会降低,
故D错误。答案选B。
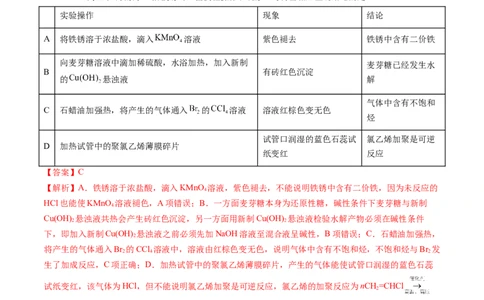
3.(22-23高三下·海南海口·阶段练习)由实验操作和现象,可得出相应正确结论的是
实验操作 现象 结论
A 将铁锈溶于浓盐酸,滴入 溶液 紫色褪去 铁锈中含有二价铁
向麦芽糖溶液中滴加稀硫酸,水浴加热,加入新制 麦芽糖已经发生水
B 有砖红色沉淀
的 悬浊液 解
气体中含有不饱和
C 石蜡油加强热,将产生的气体通入 的 溶液 溶液红棕色变无色
烃
试管口润湿的蓝色石蕊试 氯乙烯加聚是可逆
D 加热试管中的聚氯乙烯薄膜碎片
纸变红 反应
【答案】C
【解析】A.铁锈溶于浓盐酸,滴入KMnO 溶液,紫色褪去,不能说明铁锈中含有二价铁,因为未反应的
4
HCl也能使KMnO 溶液褪色,A项错误;B.一方面麦芽糖本身为还原性糖,碱性条件下麦芽糖与新制
4
Cu(OH) 悬浊液共热会产生砖红色沉淀,另一方面用新制Cu(OH) 悬浊液检验水解产物必须在碱性条件
2 2
下,即加入新制Cu(OH) 悬浊液之前必须先加NaOH溶液至混合液呈碱性,B项错误;C.石蜡油加强热,
2
将产生的气体通入Br 的CCl 溶液中,溶液由红棕色变无色,说明气体中含有不饱和烃,不饱和烃与Br 发
2 4 2
生了加成反应,C项正确;D.加热试管中的聚氯乙烯薄膜碎片,产生的气体能使试管口润湿的蓝色石蕊
试纸变红,该气体为HCl,但不能说明氯乙烯加聚是可逆反应,氯乙烯的加聚反应为nCH=CHCl
2
,D项错误;答案选C。
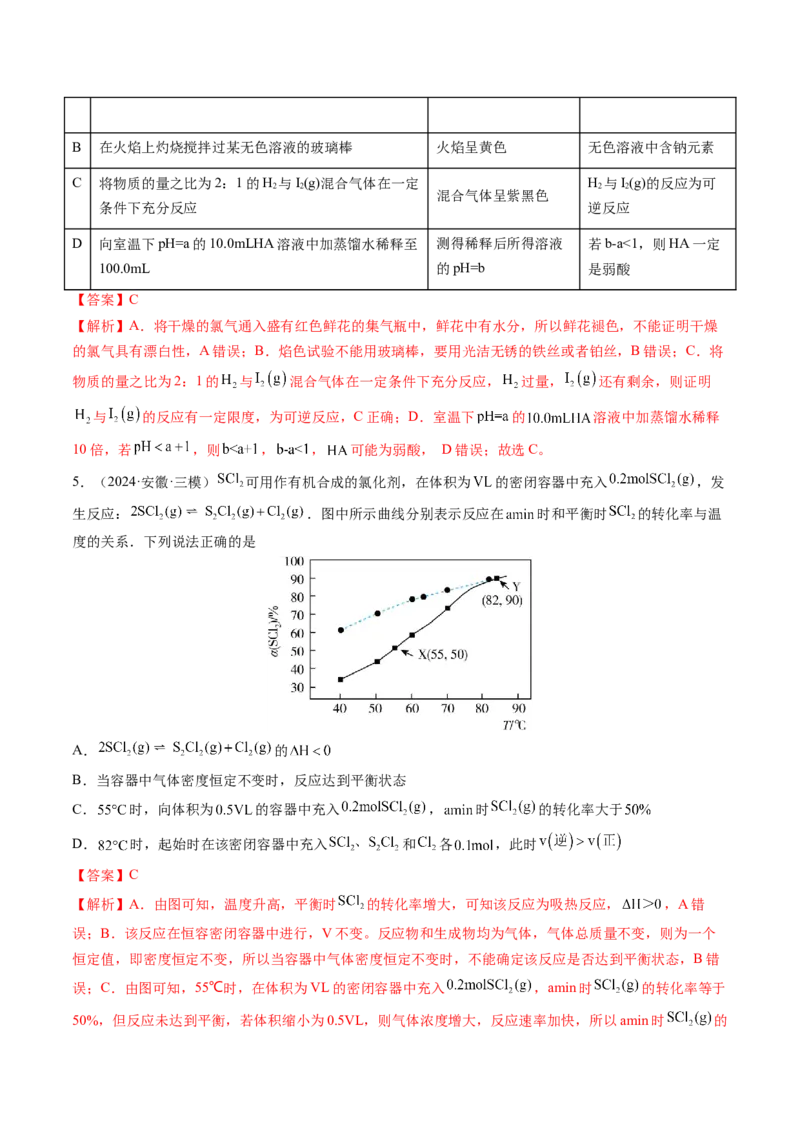
4.(2023·甘肃·二模)下列实验操作和现象,可得出正确结论的是
实验操作 实验现象 结论
A 将干燥的氯气通入盛有红色鲜花的集 鲜花的红色褪去 干燥的氯气具有漂白
气瓶中 性B 在火焰上灼烧搅拌过某无色溶液的玻璃棒 火焰呈黄色 无色溶液中含钠元素
C 将物质的量之比为2:1的H 与I(g)混合气体在一定 H 与I(g)的反应为可
2 2 2 2
混合气体呈紫黑色
条件下充分反应 逆反应
D 向室温下pH=a的10.0mLHA溶液中加蒸馏水稀释至 测得稀释后所得溶液 若b-a<1,则HA一定
100.0mL 的pH=b 是弱酸
【答案】C
【解析】A.将干燥的氯气通入盛有红色鲜花的集气瓶中,鲜花中有水分,所以鲜花褪色,不能证明干燥
的氯气具有漂白性,A错误;B.焰色试验不能用玻璃棒,要用光洁无锈的铁丝或者铂丝,B错误;C.将
物质的量之比为2:1的 与 混合气体在一定条件下充分反应, 过量, 还有剩余,则证明
与 的反应有一定限度,为可逆反应,C正确;D.室温下 的 溶液中加蒸馏水稀释
10倍,若 ,则 , , 可能为弱酸, D错误;故选C。
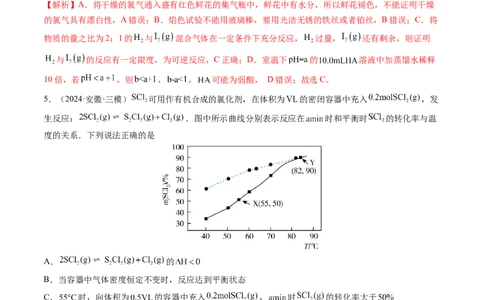
5.(2024·安徽·三模) 可用作有机合成的氯化剂,在体积为 的密闭容器中充入 ,发
生反应: .图中所示曲线分别表示反应在 时和平衡时 的转化率与温
度的关系.下列说法正确的是
A. 的
B.当容器中气体密度恒定不变时,反应达到平衡状态
C. 时,向体积为 的容器中充入 , 时 的转化率大于
D. 时,起始时在该密闭容器中充入 和 各 ,此时
【答案】C
【解析】A.由图可知,温度升高,平衡时 的转化率增大,可知该反应为吸热反应, ,A错
误;B.该反应在恒容密闭容器中进行,V不变。反应物和生成物均为气体,气体总质量不变,则为一个
恒定值,即密度恒定不变,所以当容器中气体密度恒定不变时,不能确定该反应是否达到平衡状态,B错
误;C.由图可知,55℃时,在体积为VL的密闭容器中充入 ,amin时 的转化率等于
50%,但反应未达到平衡,若体积缩小为0.5VL,则气体浓度增大,反应速率加快,所以amin时 的转化率大于50%,C正确;D.由图可知,82℃时 的转化率为90%,得出三段式(单位:
mol/L):
平衡常数K= ,在该密闭容然中充入 和 各 ,此时浓度商Q=1<K,平
衡正向移动,所以 ,D错误;答案选C。
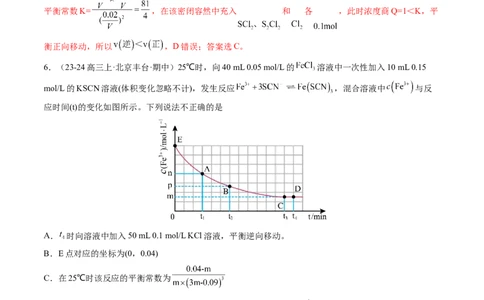
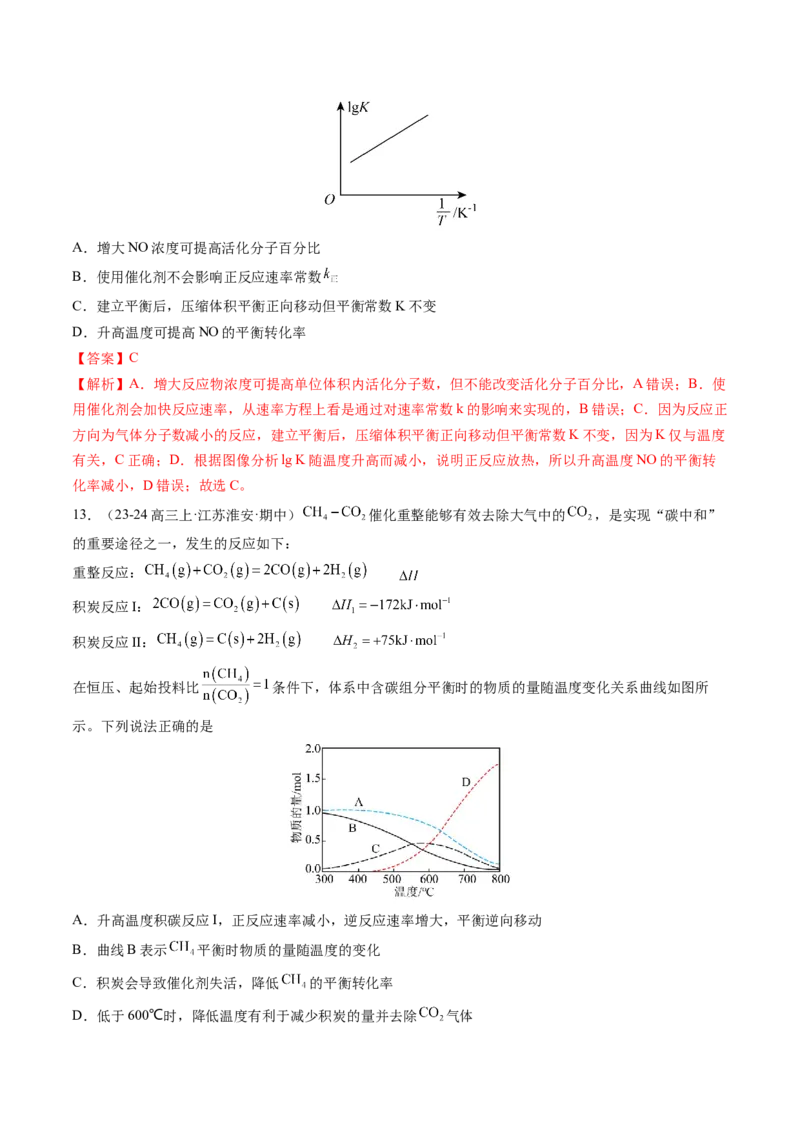
6.(23-24高三上·北京丰台·期中)25℃时,向40 mL 0.05 mol/L的 溶液中一次性加入10 mL 0.15
mol/L的KSCN溶液(体积变化忽略不计),发生反应 ,混合溶液中 与反
应时间(t)的变化如图所示。下列说法不正确的是
A. 时向溶液中加入50 mL 0.1 mol/L KCl溶液,平衡逆向移动。
B.E点对应的坐标为(0,0.04)
C.在25℃时该反应的平衡常数为
D. 分钟后加入少量KSCN固体,溶液红色加深,该现象可以证明 与SCN-的反应是可逆反应
【答案】D
【解析】A.t 时刻向溶液中加入50mL 0.1mol/L的KCl溶液,溶液总体积增大,离子浓度减小,化学平衡
4
向离子浓度增大的方向移动,即平衡逆向移动,A正确;B.40mL 0.05mol/L的FeCl 溶液中一次性加入
3
10mL0.15mol/L的KSCN溶液,t=0时刻反应尚未开始,溶液总体积为50mL,c(Fe3+)=
=0.04mol/L,E坐标为(0,0.04),B正确;C.从图中可知,平衡时c(Fe3+)=m mol/L,消耗掉Fe3+(0.002-
0.05m)mol,则消耗掉SCN-(0.006-0.15m)mol,平衡时c(SCN-)=(3m-0.09)mol/L,生成Fe(SCN) (0.002-
30.05m)mol,平衡时浓度为c=(0.04-m)mol/L,则该反应的平衡常数= ,C正确;D.Fe3+初始
物质的量为0.002mol,SCN-初始物质的量为0.0015mol,根据反应的方程式可知Fe3+过量,故即使该反应
不是可逆反应,加入KSCN固体后,剩余的铁离子也会与SCN-反应生成Fe(SCN) ,溶液红色加深,无法
3
证明该反应是可逆反应,D错误;故答案选D。
7.(2024·广西贵港·模拟预测)中国积极推动技术创新,力争2060年实现碳中和。 催化还原的主要
反应有:
①
②
向恒温恒压的密闭容器中通入 和 进行上述反应。 的平衡产率 、
的平衡转化率 随温度的变化关系如图所示。下列说法错误的是
A.反应②在较高温度下才能自发进行
B.若气体平均摩尔质量不再变化,则反应①和②均达到平衡状态
C.任意温度下的平衡转化率:
D.平衡时 随温度升高先减小后增大
【答案】A
【解析】A.由图像信息可知,随着温度的升高 的平衡产率减小,即升高温度反应②平衡逆向移
动,故反应②的 ,又因为该反应是气体分子数减少的反应, ,故该反应在较低的温度下能
自发进行,A错误;B.由题干信息可知,反应物质全部为气体,其中反应②为非等体积反应,故若气体
平均摩尔质量不再变化,则反应①和②均达到平衡状态,B正确;C.由题干方程式可知,若只发生反应
②,则 和 的平衡转化率相等,若只发生反应①,则 的平衡转化率小于 的,现同时发生反应
①和反应②,故任一温度下的平衡转化率: ,C正确;D.由题干图像信息可知,
的平衡产率随温度的升高一直在减小,而 的平衡转化率先减小后增大,说明温度较低时以反
应②为主,随着温度升高平衡逆向移动, 的物质的量减小,而温度较高时,以反应①为主,温度升高平衡正向移动, 的物质的量增大,即平衡时 随温度升高先减小后增大,D正确;故选A。
题型二 化学平衡移动
8.(2024·北京·三模)下列事实不能用化学平衡移动原理解释的是
A.锌片与稀 反应过程中,加入少量 固体,促进 的产生
B.密闭烧瓶内的 和 的混合气体,受热后颜色加深
C.水垢中含有 ,可先用 溶液浸泡处理,再用盐酸溶解
D. 的醋酸溶液加水稀释100倍,
【答案】A
【解析】A.加入硫酸铜以后,锌置换出铜可以构成原电池,反应速率加快,与平衡移动无关,A错误;
B. 转化为 的反应是放热反应,升温平衡逆向移动, 浓度增大,混合气体颜色加深,可以
用化学平衡移动原理解释,B正确;C.用 溶液浸泡处理水垢, 可以转化为 ,可以用
沉淀溶解平衡的原理解释,C正确;D.醋酸是弱酸,加水稀释会促进电离平衡正向移动,因此 的
醋酸溶液加水稀释100倍后, 大于 ,即溶液 ,D正确;答案选A。
9.(2024·北京·模拟预测)下列事实不能用平衡移动原理解释的是
A.镁条在水中产生少量气泡后反应停止,在1mol/L 溶液中持续产生气泡
B.二氧化锰与稀盐酸共热不产生氯气,与浓盐酸共热产生氯气
C.在硫酸铜溶液中加入氯化钠固体,充分溶解后溶液变为蓝绿色
D.在氯水中加入少量碳酸钙,可以增强氯水的氧化性
【答案】B
【解析】A.镁条在水中产生少量气泡后反应停止,在1mol/L 溶液中持续产生气泡,是因为氯化铵
溶液中 水解使溶液显酸性,Mg与H+反应促进水的电离正向进行,能用平衡移动原理解释,A不选;
B.二氧化锰与稀盐酸共热不产生氯气,与浓盐酸共热产生氯气,是因为浓盐酸中HCl的浓度大,HCl的
还原性更强,能发生氧化还原反应,不能用平衡移动原理解释,B选;C.在硫酸铜溶液中加入氯化钠固
体,充分溶解后溶液变为蓝绿色,是因为发生了反应 ,能用平衡移动
原理解释,C不选;D.在氯水中加入少量碳酸钙,可以增强氯水的氧化性,是因为碳酸钙和溶液中的
H+反应促进氯气和水的反应正向进行,能用平衡移动原理解释,D不选;故选B。
10.(2024·河北唐山·二模)催化剂a和b均能催化反应 。反应历程中,M为中间产物。其它
条件相同时,下列说法错误的是A.使用催化剂a和b,反应历程都分4步进行
B.反应达平衡后,升高温度,P的浓度增大
C.使用催化剂b时,反应体系更快达到平衡
D.使用催化剂a时,反应过程中M所能达到的最高浓度更大
【答案】C
【解析】A.根据图中信息得到使用催化剂a和b,反应历程都分4步进行,故A正确;B.根据图中信息
得到该反应是吸热反应,反应达平衡后,升高温度,平衡正向移动,则P的浓度增大,故B正确;C.使
用催化剂b时,活化能更大,则反应速率较慢,反应体系更慢达到平衡,故C错误;D.使用催化剂a
时,前两步反应速率较快,而第三步反应速率较慢,因此反应过程中更容易积累到M物质,因此M所能
达到的最高浓度更大,故D正确。综上所述,答案为C。
11.(2024·江苏南通·三模)下列关于反应 的说法正确的是
A.基态V原子核外电子排布为
B.反应达到平衡状态时,
C.使用 的目是为了增大 的平衡转化率
D.其他条件相同,增大压强,平衡常数增大
【答案】B
【解析】A.V为第23号元素,基态V原子核外电子排布为 ,A项不符合题意;B.反应
达到平衡状态时, ,B项符合题意;C.催化剂可以增大化学反应速率,不能使平衡移
动,不能改变平衡转化率,C项不符合题意;D.化学平衡常数只受温度的影响,温度改变,平衡常数才
会改变,D项不符合题意;故正确选项为B。
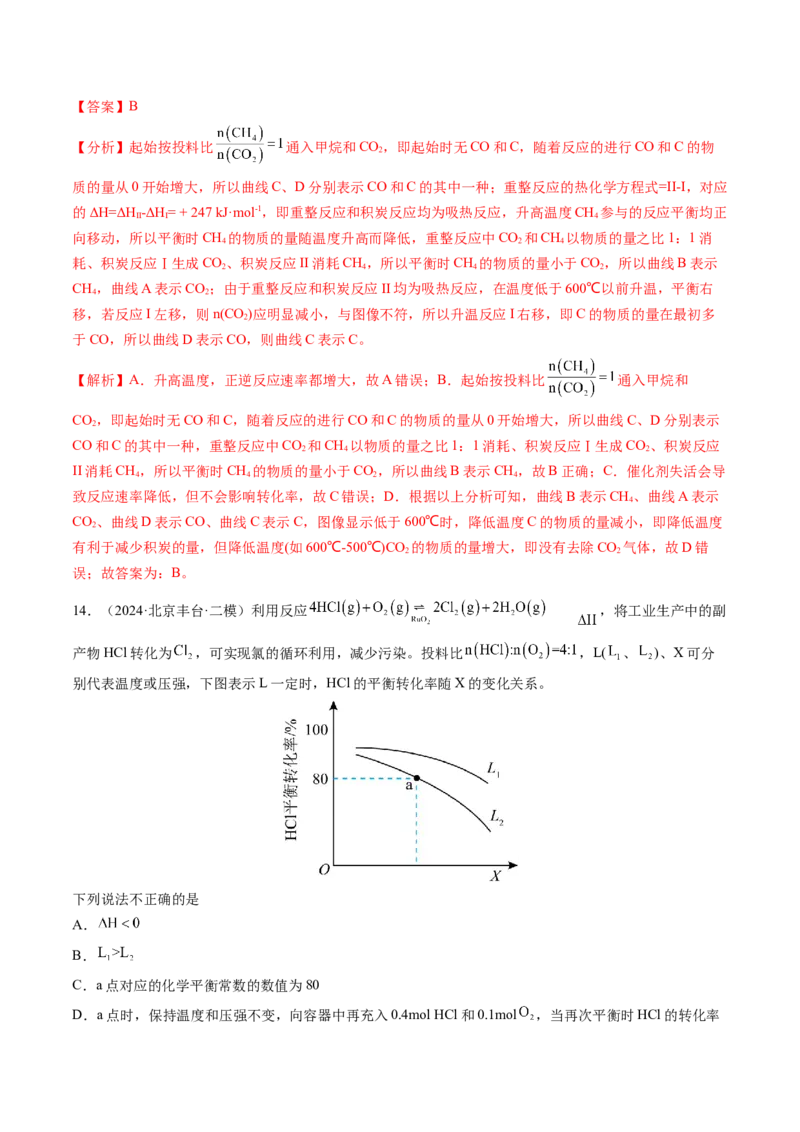
12.(2024·湖南长沙·三模)已知: 的正反应速率可表示为
( 为正反应速率常数),该反应平衡常数的对数与温度的倒数的关系如图所示,下
列说法正确的是A.增大NO浓度可提高活化分子百分比
B.使用催化剂不会影响正反应速率常数
C.建立平衡后,压缩体积平衡正向移动但平衡常数K不变
D.升高温度可提高NO的平衡转化率
【答案】C
【解析】A.增大反应物浓度可提高单位体积内活化分子数,但不能改变活化分子百分比,A错误;B.使
用催化剂会加快反应速率,从速率方程上看是通过对速率常数k的影响来实现的,B错误;C.因为反应正
方向为气体分子数减小的反应,建立平衡后,压缩体积平衡正向移动但平衡常数K不变,因为K仅与温度
有关,C正确;D.根据图像分析lg K随温度升高而减小,说明正反应放热,所以升高温度NO的平衡转
化率减小,D错误;故选C。
13.(23-24高三上·江苏淮安·期中) 催化重整能够有效去除大气中的 ,是实现“碳中和”
的重要途径之一,发生的反应如下:
重整反应:
积炭反应I:
积炭反应II:
在恒压、起始投料比 条件下,体系中含碳组分平衡时的物质的量随温度变化关系曲线如图所
示。下列说法正确的是
A.升高温度积碳反应I,正反应速率减小,逆反应速率增大,平衡逆向移动
B.曲线B表示 平衡时物质的量随温度的变化
C.积炭会导致催化剂失活,降低 的平衡转化率
D.低于600℃时,降低温度有利于减少积炭的量并去除 气体【答案】B
【分析】起始按投料比 通入甲烷和CO,即起始时无CO和C,随着反应的进行CO和C的物
2
质的量从0开始增大,所以曲线C、D分别表示CO和C的其中一种;重整反应的热化学方程式=II-I,对应
的ΔH=ΔH -ΔH= + 247 kJ·mol-1,即重整反应和积炭反应均为吸热反应,升高温度CH 参与的反应平衡均正
II I 4
向移动,所以平衡时CH 的物质的量随温度升高而降低,重整反应中CO 和CH 以物质的量之比1:1消
4 2 4
耗、积炭反应Ⅰ生成CO、积炭反应II消耗CH,所以平衡时CH 的物质的量小于CO,所以曲线B表示
2 4 4 2
CH,曲线A表示CO;由于重整反应和积炭反应II均为吸热反应,在温度低于600℃以前升温,平衡右
4 2
移,若反应I左移,则n(CO)应明显减小,与图像不符,所以升温反应I右移,即C的物质的量在最初多
2
于CO,所以曲线D表示CO,则曲线C表示C。
【解析】A.升高温度,正逆反应速率都增大,故A错误;B.起始按投料比 通入甲烷和
CO,即起始时无CO和C,随着反应的进行CO和C的物质的量从0开始增大,所以曲线C、D分别表示
2
CO和C的其中一种,重整反应中CO 和CH 以物质的量之比1:1消耗、积炭反应Ⅰ生成CO、积炭反应
2 4 2
II消耗CH,所以平衡时CH 的物质的量小于CO,所以曲线B表示CH,故B正确;C.催化剂失活会导
4 4 2 4
致反应速率降低,但不会影响转化率,故C错误;D.根据以上分析可知,曲线B表示CH、曲线A表示
4
CO、曲线D表示CO、曲线C表示C,图像显示低于600℃时,降低温度C的物质的量减小,即降低温度
2
有利于减少积炭的量,但降低温度(如600℃-500℃)CO 的物质的量增大,即没有去除CO 气体,故D错
2 2
误;故答案为:B。
14.(2024·北京丰台·二模)利用反应 ,将工业生产中的副
产物HCl转化为 ,可实现氯的循环利用,减少污染。投料比 ,L( 、 )、X可分
别代表温度或压强,下图表示L一定时,HCl的平衡转化率随X的变化关系。
下列说法不正确的是
A.
B.
C.a点对应的化学平衡常数的数值为80
D.a点时,保持温度和压强不变,向容器中再充入0.4mol HCl和0.1mol ,当再次平衡时HCl的转化率仍为80%
【答案】C
【分析】 ,正向放热,升高温度则HCl的转化率增大,正向体积减
小,增大压强平衡正向移动,HCl的转化率增大,综合对比可知X代表温度,L代表压强且L>L。
1 2
【解析】A.催化剂不影响焓变,该反应熵减,能自发进行则为放热反应,△H<0,故A正确;B.L表
示压强,反应正向体积减小,增大压强平衡正向移动,HCl的转化率增大,因此L>L,故B正确;C.
1 2
设起始时 , 则起始时 ,a点HCl的转化率为80%则转化氯化
氢的物质的量为3.2mol,可列三段式 ,平衡常
数为 ,体积未知无法计算,故C错误;D.a点时,保持温度和压强不变,则平衡
常数不变,向容器中再充入0.4mol HCl和0.1mol ,HCl和O 增加量之比和起始投料比相等,又是恒压
2
条件,与原平衡为等效平衡,因此当再次平衡时HCl的转化率仍为80%,故D正确;故选C。
15.(2024·广东·三模)一定温度下,向容积为 的恒容密闭容器中充入 和 ,发生反应
,测得 随时间的变化如下图实线
所示,下列说法正确的是
A.升高温度,可以提高上述反应的平衡产率
B.该反应在 内 的平均反应速率是
C.该反应在 后,容器内总压强不再改变
D.加入催化剂(其他条件相同), 随时间的变化会如上图虚线所示【答案】C
【解析】A.该反应为放热反应,升高温度,平衡向逆反应方向移动,生成物的产率减小,故A错误;
B.由图可知,1min时,氢气的物质的量为6mol,由方程式可知,0∼1min内二氧化碳的反应速率为
≈0.33 mol/(L·min),故B错误;C.由图可知,8min时氢气的物质的量和12min时氢气的
物质的量都为2mol,说明反应已经达到平衡,容器内总压强不再改变,故C正确;D.加入催化剂,化学
反应速率加快,但化学平衡不移动,氢气的物质的量不变,则氢气的物质的量随时间的变化不能用图中虚
线表示,故D错误;故选C。
16.(2024·湖南长沙·三模)已知: 的正反应速率可表示为
( 为正反应速率常数),该反应平衡常数的对数与温度的倒数的关系如图所示,下
列说法正确的是
A.增大NO浓度可提高活化分子百分比
B.使用催化剂不会影响正反应速率常数
C.建立平衡后,压缩体积平衡正向移动但平衡常数K不变
D.升高温度可提高NO的平衡转化率
【答案】C
【解析】A.增大反应物浓度可提高单位体积内活化分子数,但不能改变活化分子百分比,A错误;B.使
用催化剂会加快反应速率,从速率方程上看是通过对速率常数k的影响来实现的,B错误;C.因为反应正
方向为气体分子数减小的反应,建立平衡后,压缩体积平衡正向移动但平衡常数K不变,因为K仅与温度
有关,C正确;D.根据图像分析lg K随温度升高而减小,说明正反应放热,所以升高温度NO的平衡转
化率减小,D错误;故选C。
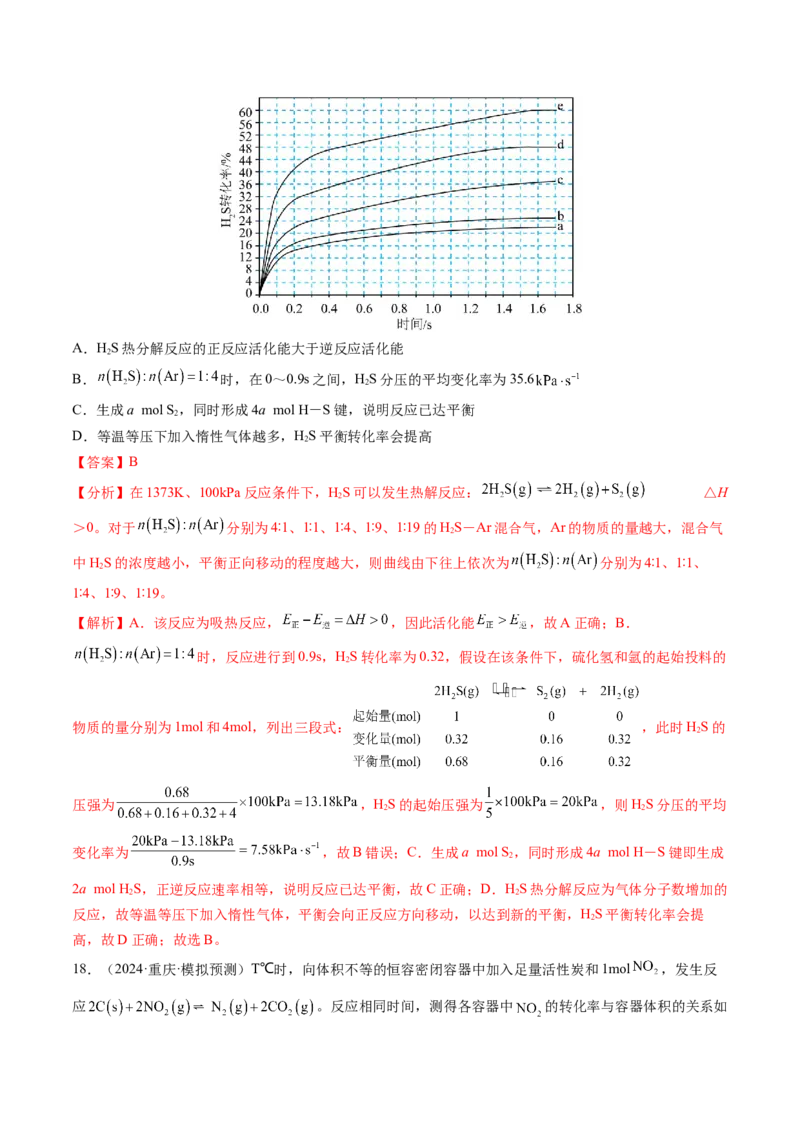
17.(2024·安徽合肥·三模)在1373K、100kPa反应条件下,HS可以发生热解反应:
2
△H>0。对于 分别为4∶1、1∶1、1∶4、1∶9、1∶19的HS-
2
Ar混合气,热分解反应过程中HS转化率随时间的变化如图所示。下列说法错误的是
2A.HS热分解反应的正反应活化能大于逆反应活化能
2
B. 时,在0~0.9s之间,HS分压的平均变化率为35.6
2
C.生成a mol S,同时形成4a mol H-S键,说明反应已达平衡
2
D.等温等压下加入惰性气体越多,HS平衡转化率会提高
2
【答案】B
【分析】在1373K、100kPa反应条件下,HS可以发生热解反应: △H
2
>0。对于 分别为4∶1、1∶1、1∶4、1∶9、1∶19的HS-Ar混合气,Ar的物质的量越大,混合气
2
中HS的浓度越小,平衡正向移动的程度越大,则曲线由下往上依次为 分别为4∶1、1∶1、
2
1∶4、1∶9、1∶19。
【解析】A.该反应为吸热反应, ,因此活化能 ,故A正确;B.
时,反应进行到0.9s,HS转化率为0.32,假设在该条件下,硫化氢和氩的起始投料的
2
物质的量分别为1mol和4mol,列出三段式: ,此时HS的
2
压强为 ,HS的起始压强为 ,则HS分压的平均
2 2
变化率为 ,故B错误;C.生成a mol S,同时形成4a mol H-S键即生成
2
2a mol HS,正逆反应速率相等,说明反应已达平衡,故C正确;D.HS热分解反应为气体分子数增加的
2 2
反应,故等温等压下加入惰性气体,平衡会向正反应方向移动,以达到新的平衡,HS平衡转化率会提
2
高,故D正确;故选B。
18.(2024·重庆·模拟预测)T℃时,向体积不等的恒容密闭容器中加入足量活性炭和1mol ,发生反
应 。反应相同时间,测得各容器中 的转化率与容器体积的关系如图所示,下列说法正确的是
A.a点对应容器中,反应未达到平衡状态
B.向b点对应容器中再充入一定量 ,达到新平衡时, 的转化率增大
C.缩小c点对应容器的体积增大压强,v(正)甲>乙(2)CD(3)>
【解析】(1)乙因为是绝热容器,该反应为放热反应,所以相对于甲,乙中温度比甲高,升高温度平衡
逆向移动, 的转化率降低;比较甲、丙,该反应为气体体积减小的反应,丙在恒压的条件下,甲相对
于丙,相对于减小压强,平衡逆向移动, 的转化率降低,综上所述,三个容器中 的转化率从大到
小的顺序为:丙>甲>乙,故答案为:丙>甲>乙;(2)A.甲为恒温恒容的密闭容器,所以温度一直保持
不变,则温度不变不能用于判断该反应是否处于平衡状态,故A不选;B.甲、乙均为恒容密闭容器,又
由于该反全为气体参加的反应,所以在恒容的密闭容器中密度始终保持不变,故B不选;C.在恒容的密
闭容器中,该反应为非等体积反应,所以压强不变时,该反应处于平很状态,故选C;D.一定条件下,
当 时,反应体系中所有参加反应的物质的物质的量或浓度保持恒定不变,则O 浓度保持
2
不变可用于判断该反应是否处于不平衡状态,故选D;故答案选CD;(3)丙为恒温恒压的密闭体系,所
以相同温度下在容器丙中分别投入4molSO 、2molO 和2molSO 、1molO 进行反应平衡不发生移动;则所
2 2 2 2
释放的能量前者为后者的两倍;若前者反应温度为400℃,后者反应温度为500℃,且该反应为放热反应,
所以平衡逆向移动,则前者释放的能量大于后者的两倍,故答案为:>;
1.(2024·浙江·高考真题)为探究化学平衡移动的影响因素,设计方案并进行实验,观察到相关现象。其
中方案设计和结论都正确的是
选 影响
方案设计 现象 结论
项 因素
向 溶液中加入 黄色溶液 增大反应物浓度,平衡向正反
A 浓度
溶液 变橙色 应方向移动
对于反应前后气体总体积不变
向恒温恒容密闭玻璃容器中充入 气 气体颜色
B 压强 的可逆反应,改变压强平衡不
体,分解达到平衡后再充入 不变
移动
将封装有 和 混合气体的烧瓶浸泡在热 气体颜色 升高温度,平衡向吸热反应方
C 温度
水中 变深 向移动
催化 向 乙酸乙酯中加入 溶 上层液体 使用合适的催化剂可使平衡向
D
剂 液,水浴加热 逐渐减少 正反应方向移动【答案】C
【解析】A. 在KCrO 溶液中存在平衡 ,且该溶液具有氧化
2 4
性,HBr具有还原性,向 溶液中加入 溶液,可发生氧化还原反应生
成Br 使溶液变为橙色,干扰探究浓度对化学平衡的影响,A错误;B.反应2HI H+I 为反应前后气体
2 2 2
总体积不变的可逆反应,向恒温恒容密闭玻璃容器中充入 气体,分解达到平衡后再充入
,平衡不发生移动,气体颜色不变,应得到的结论是:对于反应前后气体总体积不变的可逆反
应,恒温恒容时,改变压强平衡不移动,B错误;C.反应 为放热反应,升高温度,气体
颜色变深,说明平衡逆向移动,即向吸热反应方向移动,C正确;D.催化剂只会改变化学反应速率,不
影响平衡移动,D错误;答案选C。
2.(2024·浙江·高考真题)二氧化碳氧化乙烷制备乙烯,主要发生如下两个反应:
I.
II.
向容积为 的密闭容器中投入 和 ,不同温度下,测得 时(反应均未平衡)的相关
数据见下表,下列说法不正确的是
温度( ) 400 500 600
乙烷转化率( ) 2.2 9.0 17.8
乙烯选择性( ) 92.6 80.0 61.8
注:乙烯选择性
A.反应活化能:
B. 时, 反应I的平均速率为:
C.其他条件不变,平衡后及时移除 ,可提高乙烯的产率
D.其他条件不变,增大投料比 投料,平衡后可提高乙烷转化率
【答案】D
【解析】A.由表可知,相同温度下,乙烷在发生转化时,反应Ⅰ更易发生,则反应活化能:Ⅰ<Ⅱ,A正
确;B.由表可知,500℃时,乙烷的转化率为9.0%,可得转化的乙烷的总物质的量为
2mol×9.0%=0.18mol,而此温度下乙烯的选择性为80%,则转化为乙烯的乙烷的物质的量为
0.18mol×80%=0.144mol,根据方程式可得,生成乙烯的物质的量为0.144mol,则 反应I的平均速
率为: ,B正确;C.其他条件不变,平衡后及时移除,反应Ⅰ正向进行,可提高乙烯的产率,C正确;D.其他条件不变,增大投料比 投
料,平衡后CO 转化率提高,C H 转化率降低,D错误;答案选D。
2 2 6
3.(2023·广东·高考真题)催化剂Ⅰ和Ⅱ均能催化反应 。反应历程(下图)中,M为中间产物。
其它条件相同时,下列说法不正确的是
A.使用Ⅰ和Ⅱ,反应历程都分4步进行
B.反应达平衡时,升高温度,R的浓度增大
C.使用Ⅱ时,反应体系更快达到平衡
D.使用Ⅰ时,反应过程中M所能达到的最高浓度更大
【答案】C
【解析】A.由图可知两种催化剂均出现四个波峰,所以使用Ⅰ和Ⅱ,反应历程都分4步进行,A正确;
B.由图可知该反应是放热反应,所以达平衡时,升高温度平衡向左移动,R的浓度增大,B正确;C.由
图可知Ⅰ的最高活化能小于Ⅱ的最高活化能,所以使用Ⅰ时反应速率更快,反应体系更快达到平衡,C错
误;D.由图可知在前两个历程中使用Ⅰ活化能较低反应速率较快,后两个历程中使用Ⅰ活化能较高反应
速率较慢,所以使用Ⅰ时,反应过程中M所能达到的最高浓度更大,D正确;故选C。
4.(2023·北京·高考真题)下列事实能用平衡移动原理解释的是
A. 溶液中加入少量 固体,促进 分解
B.密闭烧瓶内的 和 的混合气体,受热后颜色加深
C.铁钉放入浓 中,待不再变化后,加热能产生大量红棕色气体
D.锌片与稀 反应过程中,加入少量 固体,促进 的产生
【答案】B
【解析】A.MnO 会催化 HO 分解,与平衡移动无关,A项错误;
2 2 2
B.NO 转化为NO 的反应是放热反应,升温平衡逆向移动, NO 浓度增大,混合气体颜色加深,B项正
2 2 4 2
确;C.铁在浓硝酸中钝化,加热会使表面的氧化膜溶解,铁与浓硝酸反应生成大量红棕色气体,与平衡
移动无关,C项错误;D.加入硫酸铜以后,锌置换出铜,构成原电池,从而使反应速率加快,与平衡移
动无关,D项错误;故选B。
5.(2022·天津·高考真题)向恒温恒容密闭容器中通入2mol 和1mol ,反应
达到平衡后,再通入一定量 ,达到新平衡时,下列有关判断错误的是A. 的平衡浓度增大 B.反应平衡常数增大
C.正向反应速率增大 D. 的转化总量增大
【答案】B
【解析】A.平衡后,再通入一定量 ,平衡正向移动, 的平衡浓度增大,A正确;B.平衡常数是
与温度有关的常数,温度不变,平衡常数不变,B错误;C.通入一定量 ,反应物浓度增大,正向反应
速率增大,C正确;D.通入一定量 ,促进二氧化硫的转化, 的转化总量增大,D正确;故选B。
6.(2022·浙江·统考高考真题)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下
列说法不正确的是
A.实验①, ,
B.实验②, 时处于平衡状态,
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
【答案】C
【解析】A.实验①中,0~20min,氨气浓度变化量为2.40 10-3mol/L-2.00 10-3mol/L=4.00 10-4mol/L,
v(NH )= =2.00 10-5mol/(L·min),反应速率之比等于化学计量数之比,v(N )= v(NH )=1.00
3 2 3
10-5mol/(L·min),A正确;B.催化剂表面积大小只影响反应速率,不影响平衡,实验③中氨气初始浓度
与实验①中一样,实验③达到平衡时氨气浓度为4.00 10-4mol/L,则实验①达平衡时氨气浓度也为4.00
10-4mol/L,而恒温恒容条件下,实验②相对于实验①为减小压强,平衡正向移动,氨气浓度减小,因此实
验②60min时处于平衡状态,根据等效平衡可以判断x<0.2,即x≠0.4,B正确;C.实验①、实验②中
0~20min、20min~40min氨气浓度变化量都是4.00 10-4mol/L,实验②中60min时反应达到平衡状态,实验
①和实验②催化剂表面积相同,实验①中氨气初始浓度是实验②中氨气初始浓度的两倍,实验①60min时
反应未达到平衡状态,相同条件下,增加氨气浓度,反应速率并没有增大,C错误;D.对比实验①和实
验③,氨气浓度相同,实验③中催化剂表面积是实验①中催化剂表面积的2倍,实验③先达到平衡状态,
实验③的反应速率大,说明相同条件下,增加催化剂的表面积,反应速率增大,D正确;答案选C。