文档内容
题型复习(四) 化学计算题
一、根据化学式的计算
1.(2017·山西)化学家戴维最早制得了曾用作麻醉剂的笑气(化学式为NO),其中氮元素的化合价是()
2
A.-1 B.-2
C.+1 D.+5
2.(2017·随州)“珍爱生命,远离毒品”。冰毒是一种毒品,能引发急性心脑疾病,并出现狂躁、暴力、自杀等倾向,
其主要成分为甲基苯丙胺(化学式为C H N)。下列有关甲基苯丙胺的说法正确的是()
10 15
A.相对分子质量是82
B.碳、氢、氮三种元素的质量比为10∶15∶1
C.是由C、H、N三种元素组成的有机物
D.充分燃烧只生成二氧化碳和水
3.(2017·临沂)豆腐是人们喜爱的食物,营养丰富,能为人体提供所需的多种氨基酸,其中含量最多的是亮氨酸
(C H NO ),关于亮氨酸的说法正确的是()
6 13 2
A.亮氨酸是氧化物
B.亮氨酸中碳元素的质量分数为27.3%
C.一个亮氨酸分子由22个原子构成
D.亮氨酸中碳、氢、氮、氧四种元素的质量比为6∶13∶1∶2
4.(2017·青岛)剧烈运动时肌肉里产生乳酸(C HO),会导致肌肉酸痛。下列说法错误的是()
3 6 3
A.乳酸的相对分子质量为90
B.乳酸由碳、氢、氧三种元素组成
C.乳酸中氧元素的质量分数最大
D.乳酸中碳、氢、氧元素质量之比为1∶2∶1
5.某硝酸铵(NH NO )样品(杂质不含氮)中氮元素的质量分数为28%,则其中硝酸铵的质量分数是()
4 3
A.20% B.70%
C.80% D.无法计算
6.某种含硫酸亚铁的药物可用于治疗缺铁性贫血。某贫血患者每天需服用这种含铁元素10%的药物112 mg,则
他每天服用的这种药物中含硫酸亚铁(FeSO )的质量是(该药物中其他成分不含铁元素)()
4
A.30.4 mg B.15.2 mg
C.22.4 mg D.22.6 mg
7.(2017·自贡)我国科学家屠呦呦发现并提纯抗疟疾药物青蒿素(C H O5)荣获2015年诺贝尔奖,请计算青蒿素
15 22
中碳、氢、氧元素的质量比为_____________。
8.(2017·济宁)观看足球比赛时,经常会看到绿茵场上运动员因拼抢摔倒受伤,医生向受伤部位喷射氯乙烷
(CHCHCl),并用药棉不断揉搓,运动员疼痛很快消除,重新投入比赛。请阅读信息后,回答:
3 2
(1)氯乙烷中C、H、Cl三种元素的原子个数比为____________;
(2)氯乙烷中C、H、Cl三种元素的质量比为____________。
9.(2017·泰安《) 舌尖上的中国》在央视上的热播让厨房再次成为人们施展厨艺的舞台。大多数厨师有个工作经验:
炒菜时,又加料酒又加醋,可使菜变得香美可口,原因是醋中的乙酸与料酒中的乙醇生成乙酸乙酯。下表中是几种常
见的酯,请完成下列问题:
酯的名称 甲酸甲酯 甲酸乙酯 乙酸甲酯 乙酸乙酯
化学式 C HO C HO C HO X
2 4 2 3 6 2 3 6 2
(1)甲酸甲酯(C HO)中碳元素、氢元素、氧元素的质量比为____________;
2 4 2
(2)甲酸乙酯(C HO)中碳元素的质量分数为________(计算结果精确到0.1%);
3 6 2
(3)比较归纳是学习化学的重要方法,据表推测X的化学式为________。二、选择型计算
1.(2017·河南)2.3 g铁和M的混合物与足量的盐酸反应,生成0.2 g氢气,则M可能是()
A.镁 B.铝
C.碳 D.钠
2.(2017·哈尔滨)现有部分被氧化的铜粉固体混合物,为研究铜粉的组成情况,取4 g混合物,先加热完全氧化后,
再加入60 g 9.8%的稀硫酸恰好完全反应,则固体混合物中铜单质的质量分数为()
A.80% B.64%
C.16% D.96%
3.(2017·广安)用足量的CO还原8.0 g某种铁的氧化物,生成的气体全部被足量的澄清石灰水吸收,得到沉淀
12.5 g,则这种铁的氧化物可能是()
A.FeO
B.Fe O 与Fe O 的混合物
2 3 3 4
C.FeO与Fe O 的混合物
3 4
D.Fe O
3 4
4.(双选)(2017·天津)下列说法中正确的是()
A.质量相等的氧化镁和硫酸镁中镁元素的质量比为3∶1
B.质量相等的硫和碳分别在氧气中充分燃烧,硫比碳消耗氧气的质量大
C.硝酸铵和氯化钾的混合物中氮元素质量分数为14%,该混合物中硝酸铵的质量分数为40%
D.质量和质量分数均相等的氢氧化钠溶液和稀硫酸,充分反应后,向所得溶液中滴加硫酸铜溶液,不会出现蓝
色沉淀
5.(2017·烟台)在托盘天平的两盘上各放一只质量相同的烧杯,分别加入等质量、等质量分数的足量稀盐酸,将天
平调节至平衡。然后向左盘的烧杯中加入4.0 g含钙元素的质量分数为50%的碳酸钙与氧化钙的固体混合物,使之完
全反应。欲使天平恢复平衡,可向右盘的烧杯中加入()
A.3.5 g氢氧化钠溶液 B.2.8 g氧化铁
C.2.8 g碳酸钠溶液 D.2.4 g镁
6.(2016·荆州)向一定量的NaCl溶液中加入足量的AgNO 溶液,所得沉淀的质量为原NaCl溶液质量的一半。则
3
原NaCl溶液中溶质的质量分数最接近于()
A.10% B.20%
C.30% D.40%
7.(2016·柳州)往800 g溶质质量分数为10%的氢氧化钠溶液中通入一定量的二氧化碳,当生成两种盐的质量相
等时,反应消耗二氧化碳的总质量约是(提示:NaCO+CO+HO===2NaHCO)()
2 3 2 2 3
A.44 g B.61 g
C.66 g D.72 g
8.(2017·桂林)密闭容器中盛有CH 和O 的混合气体,点燃使其充分反应,CH 全部转化为CO、CO 和HO,待容
4 2 4 2 2
器恢复至室温,测得容器内混合气体中碳元素的质量分数为36%。则反应前CH 和O 的质量比为()
4 2
A.4∶13 B.3∶10
C.2∶7 D.1∶4
9.(2017·湘潭)现有一包由3.2 g铜、13 g锌和2 g碳组成的粉末,放到一定量的AgNO 溶液中,完全反应后得到
3
的固体为m种,溶液中溶质为n种。下列说法中不正确的是()
A.若m=2,则n=2或3
B.若固体中金属的质量为48 g,则m=4
C.当m=3时,溶液可能呈蓝色
D.反应后固体的质量不可能超过56 g
10.(2016·河南)相同质量的镁、铝、锌分别与相同质量20%的盐酸充分反应,产生氢气质量(直接用各金属表示)
大小关系有以下几种猜测:①Mg>Al>Zn;②Al>Mg>Zn;③Al=Mg=Zn;④Al=Mg>Zn;⑤Al=Zn>Mg;
⑥Al>Mg=Zn。其中合理的个数为()
A.5个 B.4个C.3个 D.2个三、有关化学方程式与溶液的综合计算
题型之一 文字叙述型
1.(2017·青岛)实验室用100 g溶质质量分数为6.8%的过氧化氢溶液与少量二氧化锰混合制取氧气,计算完全反应后
生成氧气的质量是多少?(写出计算步骤,计算结果保留一位小数)
2.(2017·西宁)某兴趣小组用73 g溶质质量分数为20%的盐酸与足量锌粒反应,可制得氢气的质量是多少?
3.(2017·枣庄)一化工厂产生的废液中含有硫酸亚铁和硫酸铜(不考虑其他物质),为回收铜和硫酸亚铁,研究人
员设计出“用铁处理”的方案。取100 g上述废液,向其中加入2.8 g铁粉,恰好完全反应,测得反应后溶液中溶质的
质量分数为15%。求:
(1)回收得到铜的质量为________g。
(2)回收得到硫酸亚铁的质量是多少?(写出计算过程)
4.(2017·郴州)某工厂现有废硫酸9.8 t(HSO 的质量分数为10%),试计算:
2 4
(1)该9.8 t废硫酸中HSO 的质量为________t;
2 4
(2)如果用该9.8 t废硫酸去中和处理另一工厂的废碱液(主要成分为NaOH),恰好中和废碱液20 t,求废碱液中
NaOH的质量分数。(写出计算过程)5.(2017·威海)测定抗酸药物有效成分的含量,胃酸的主要成分为盐酸,胃酸太多导致胃不舒服时,可以考虑服用
抗酸药物来中和胃酸。某抗酸药物的有效成分为氢氧化镁,为测定氢氧化镁的含量,小霞同学取一片该药物(规格为1
g)于烧杯中,加入20 g溶质质量分数为3.65%的稀盐酸,恰好完全反应(假设药物中其他成分可溶于水,但不与盐酸反
应)。
(1)通过已知数据能求出的量有________(填字母编号,符合题意的选项都选)。
A.每片药物中氢氧化镁的含量
B.反应中生成氯化镁的质量
C.反应后溶液中氯化镁的质量分数
D.20 g稀盐酸中水的质量
(2)计算1 g该药物中含氢氧化镁的质量(要求写出计算过程)。
6.(2017·重庆A卷)合成氨工业中,常用碳酸钾溶液吸收产生的二氧化碳得到碳酸氢钾,反应的化学方程式为:
KCO+CO+HO===2KHCO 。现向碳酸钾溶液中通入二氧化碳,恰好完全反应,得到溶质质量分数为10%的溶液
2 3 2 2 3
50 g,试计算:
(1)碳酸钾中钾元素、碳元素、氧元素的质量比为________。
(2)若把该50 g溶液,稀释为质量分数为4%的溶液,需要加入水的质量。
(3)原碳酸钾溶液中溶质的质量分数(计算结果精确到0.1%)。
7.(2017·天津)现有碳酸钠和氯化钠的固体混合物12.6 g,其中含氧元素4.8 g,将该混合物加入到一定质量的稀盐酸中,恰好完全反应,得到137 g氯化钠溶液。计算:
(1)原固体混合物中碳酸钠的质量分数(结果保留至0.1%);
(2)所用稀盐酸中溶质的质量分数(结果保留至0.1%)。题型之二 表格数据型
1.(2017·滨州)小滨同学为了测定某珍珠粉中碳酸钙的质量分数,称取12.5 g珍珠粉样品,进行四次高温煅烧、冷
却、称量剩余固体的重复操作(杂质不参加反应),记录数据如下:
操作次数 第1次 第2次 第3次 第4次
剩余固体质量(g) 10.8 9.6 8.1 8.1
试计算:
(1)完全反应后生成二氧化碳的质量是________g;
(2)求珍珠粉中碳酸钙的质量分数。
2.(2017·菏泽)今天是某校实验室开放日,晓明同学用锌和稀硫酸反应制取氢气。先向气体发生装置中加入一定
量的锌粒,然后将60克稀硫酸分三次加入,每次生成气体的质量如下表:
次数 第一次 第二次 第三次
加入稀硫酸质量/g 20 20 20
生成氢气的质量/g 0.08 0.08 0.04
试计算:
(1)共制得氢气________g。
(2)实验所用稀硫酸中溶质的质量分数。(写出计算过程)
3.(2017·东营)醋的主要成分是醋酸,其化学式为CHCOOH。醋不仅是调味品,而且有较强的灭菌、抑毒的作用。
3
小明为判断家中的9°米醋(见标签)含酸量是否合格,取100 mL米醋于锥形瓶中,然后再向锥形瓶中逐渐加入一定溶质质量分数的碳酸氢钠溶液,反应过程中,当加入碳酸氢钠溶液的质量至以下数值时,对充分反应后锥形瓶中剩
余物质的质量进行了记录,测得的部分数据如下,请根据有关信息回答问题:(提示:化学方程式为CHCOOH+
3
NaHCO ===CH COONa+HO+CO↑)
3 3 2 2
加入碳酸氢钠溶液质量(g) 25 50 100 155 175
锥形瓶内剩余物质质量(g) 123.9 147.8 195.6 248.4 m
(1)醋酸中碳、氢、氧三种元素的质量比为_____________________。
(2)100 mL米醋与足量碳酸氢钠溶液反应产生的二氧化碳质量为________g,表中m的数值为________。
(3)请通过计算判断该产品含酸量是否合格?(写出计算过程)
4.(2017·宁波)实验室有一瓶碳酸钙和氯化钙粉末组成的均匀混合物,小科用相同溶质质量分数的稀盐酸和该混
合物反应(所得溶液均为不饱和溶液),四组实验数据记录如下表,请分析计算:
实验组别 一 二 三 四
稀盐酸质量/g 100.0 100.0 100.0 100.0
混合物质量/g 3.0 6.0 9.0 12.0
所得溶液质量/g 101.9 103.8 105.0 a
剩余固体质量/g 0 0 m n
(1)反应后,稀盐酸还有剩余的是第________组;
(2)求混合物中碳酸钙和氯化钙的质量之比________;
(3)求表中a的值为________;
(4)求表中m的值。
5.(2017·泰安)现有一家庭食用纯碱样品,其中含杂质氯化钠(不含其他杂质),为了测定样品中杂质氯化钠的质
量分数,李明同学进行了三次实验。实验数据如下表:
编号 第1次 第2次 第3次
所取固体样品的质量/g 15 12 12
加入氯化钙溶液的质量/g 100 100 150
反应后生成沉淀的质量/g 10 10 10
完成下列计算(计算结果精确到0.1%):(1)样品中氯化钠的质量分数;
(2)加入氯化钙溶液的溶质质量分数;
(3)恰好完全反应时,反应后所得溶液中氯化钠的质量分数。
题型之三 坐标图象题
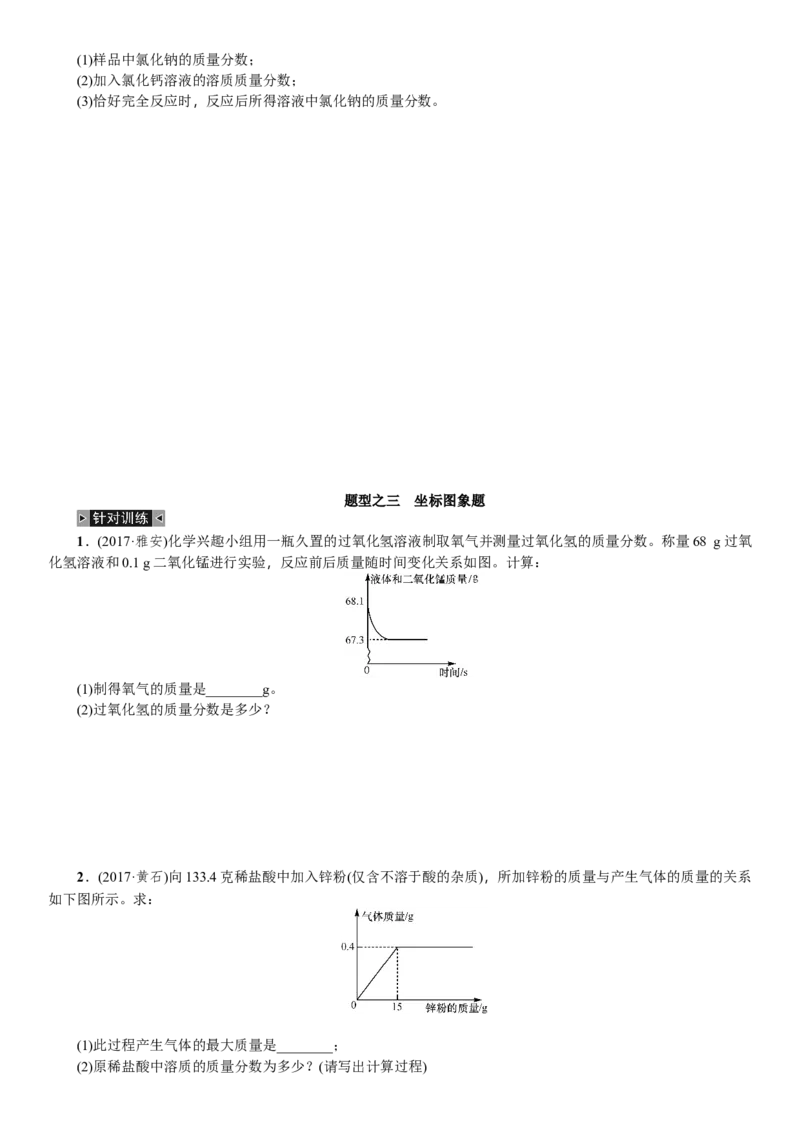
1.(2017·雅安)化学兴趣小组用一瓶久置的过氧化氢溶液制取氧气并测量过氧化氢的质量分数。称量68 g过氧
化氢溶液和0.1 g二氧化锰进行实验,反应前后质量随时间变化关系如图。计算:
(1)制得氧气的质量是________g。
(2)过氧化氢的质量分数是多少?
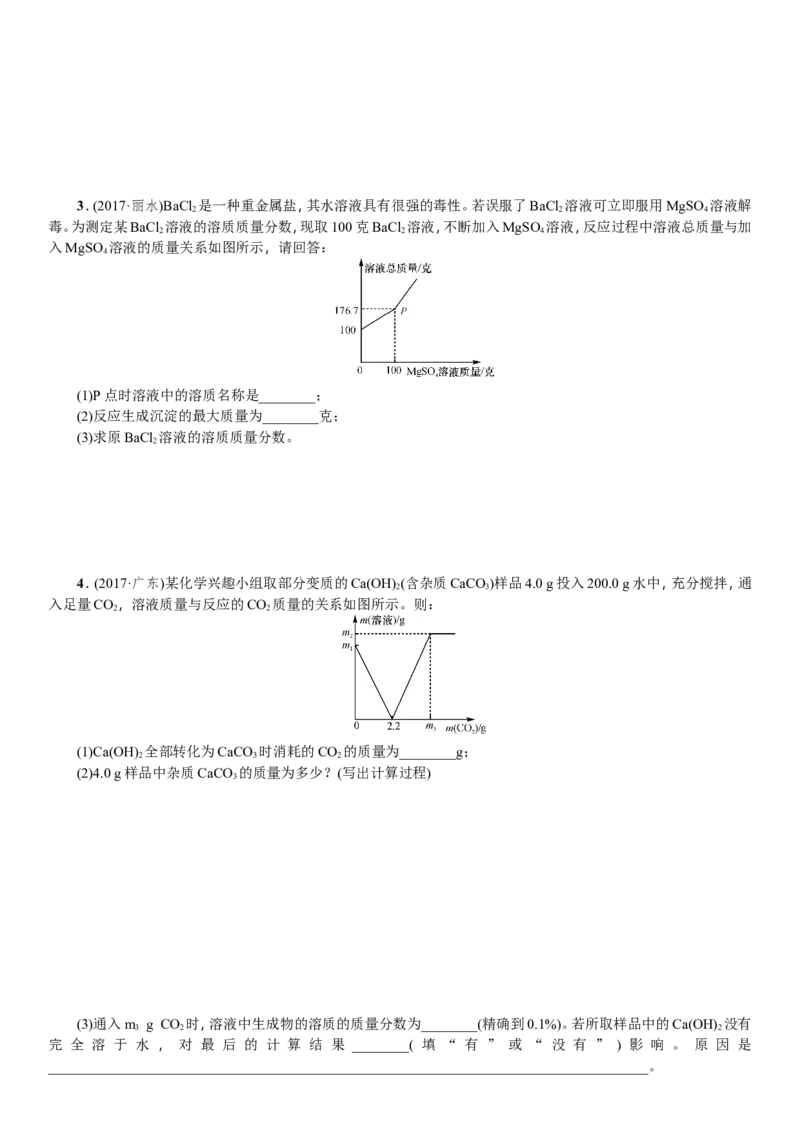
2.(2017·黄石)向133.4克稀盐酸中加入锌粉(仅含不溶于酸的杂质),所加锌粉的质量与产生气体的质量的关系
如下图所示。求:
(1)此过程产生气体的最大质量是________;
(2)原稀盐酸中溶质的质量分数为多少?(请写出计算过程)3.(2017·丽水)BaCl 是一种重金属盐,其水溶液具有很强的毒性。若误服了BaCl 溶液可立即服用MgSO 溶液解
2 2 4
毒。为测定某BaCl 溶液的溶质质量分数,现取100克BaCl 溶液,不断加入MgSO 溶液,反应过程中溶液总质量与加
2 2 4
入MgSO 溶液的质量关系如图所示,请回答:
4
(1)P点时溶液中的溶质名称是________;
(2)反应生成沉淀的最大质量为________克;
(3)求原BaCl 溶液的溶质质量分数。
2
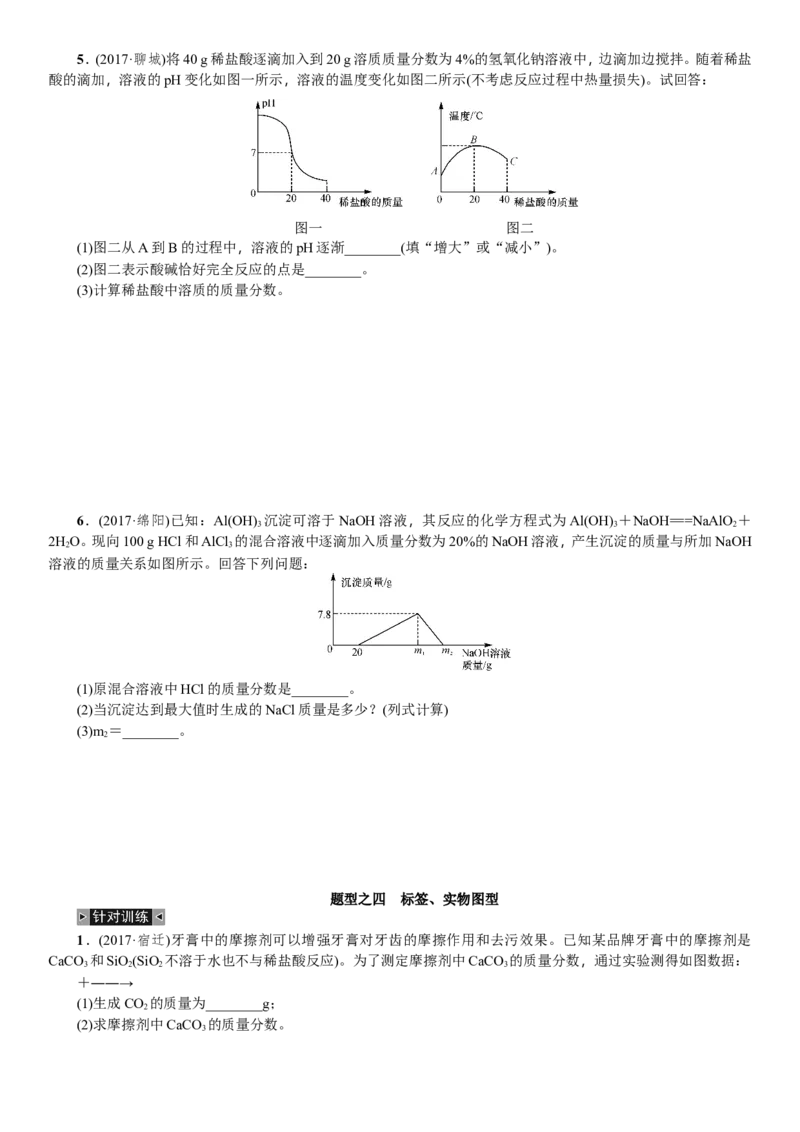
4.(2017·广东)某化学兴趣小组取部分变质的Ca(OH) (含杂质CaCO )样品4.0 g投入200.0 g水中,充分搅拌,通
2 3
入足量CO,溶液质量与反应的CO 质量的关系如图所示。则:
2 2
(1)Ca(OH) 全部转化为CaCO 时消耗的CO 的质量为________g;
2 3 2
(2)4.0 g样品中杂质CaCO 的质量为多少?(写出计算过程)
3
(3)通入m g CO 时,溶液中生成物的溶质的质量分数为________(精确到0.1%)。若所取样品中的Ca(OH) 没有
3 2 2
完 全 溶 于 水 , 对 最 后 的 计 算 结 果 ________( 填 “ 有 ” 或 “ 没 有 ” ) 影 响 。 原 因 是
_____________________________________________________________________________________。5.(2017·聊城)将40 g稀盐酸逐滴加入到20 g溶质质量分数为4%的氢氧化钠溶液中,边滴加边搅拌。随着稀盐
酸的滴加,溶液的pH变化如图一所示,溶液的温度变化如图二所示(不考虑反应过程中热量损失)。试回答:
图一 图二
(1)图二从A到B的过程中,溶液的pH逐渐________(填“增大”或“减小”)。
(2)图二表示酸碱恰好完全反应的点是________。
(3)计算稀盐酸中溶质的质量分数。
6.(2017·绵阳)已知:Al(OH) 沉淀可溶于NaOH溶液,其反应的化学方程式为Al(OH) +NaOH===NaAlO +
3 3 2
2HO。现向100 g HCl和AlCl 的混合溶液中逐滴加入质量分数为20%的NaOH溶液,产生沉淀的质量与所加NaOH
2 3
溶液的质量关系如图所示。回答下列问题:
(1)原混合溶液中HCl的质量分数是________。
(2)当沉淀达到最大值时生成的NaCl质量是多少?(列式计算)
(3)m =________。
2
题型之四 标签、实物图型
1.(2017·宿迁)牙膏中的摩擦剂可以增强牙膏对牙齿的摩擦作用和去污效果。已知某品牌牙膏中的摩擦剂是
CaCO 和SiO(SiO 不溶于水也不与稀盐酸反应)。为了测定摩擦剂中CaCO 的质量分数,通过实验测得如图数据:
3 2 2 3
+――→
(1)生成CO 的质量为________g;
2
(2)求摩擦剂中CaCO 的质量分数。
32.(2017·邵阳)某同学在实验室用氯酸钾和二氧化锰的混合物制取氧气,并对反应后固体剩余物进行回收、利用,
实验操作流程及数据记录如下:
请回答下列问题:
(1)滤液可作化肥使用,你认为它属于________________肥。
(2)该同学制得氧气的质量为________g。
(3)计算滤液中溶质质量分数。
3.(2017·孝感)某工厂排放的废水中含有亚硫酸钠(Na SO )未经处理,会造成污染。化学兴趣小组的同学对废水
2 3
处理设计了如图所示的实验方案:
试计算:
(l)反应完后生成亚硫酸钙沉淀的质量为________g。
(2)废水中亚硫酸钠的质量分数(请写出计算过程)。
(温馨提示:NaSO +CaCl ===CaSO ↓+2NaCl;氯化钙不与废水中的其他杂质反应)
2 3 2 3
4.(2017·南充)某化学兴趣小组欲测定一瓶过氧化氢溶液中溶质的质量分数,实验操作及相关数据如图所示:
(1)生成氧气的质量为________g;
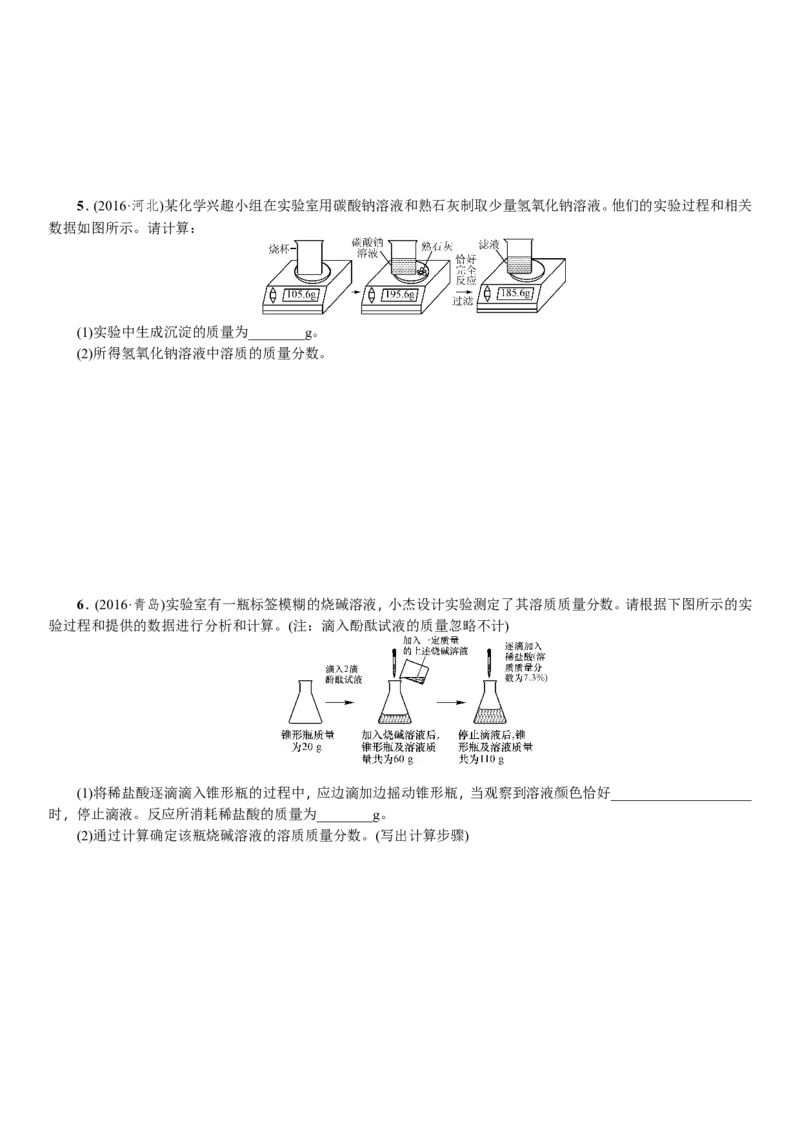
(2)这瓶过氧化氢溶液中溶质的质量分数是多少?(请写出计算过程)5.(2016·河北)某化学兴趣小组在实验室用碳酸钠溶液和熟石灰制取少量氢氧化钠溶液。他们的实验过程和相关
数据如图所示。请计算:
(1)实验中生成沉淀的质量为________g。
(2)所得氢氧化钠溶液中溶质的质量分数。
6.(2016·青岛)实验室有一瓶标签模糊的烧碱溶液,小杰设计实验测定了其溶质质量分数。请根据下图所示的实
验过程和提供的数据进行分析和计算。(注:滴入酚酞试液的质量忽略不计)
(1)将稀盐酸逐滴滴入锥形瓶的过程中,应边滴加边摇动锥形瓶,当观察到溶液颜色恰好____________________
时,停止滴液。反应所消耗稀盐酸的质量为________g。
(2)通过计算确定该瓶烧碱溶液的溶质质量分数。(写出计算步骤)(3)问题讨论:小红做同样的实验得到的结果比小杰得到的结果偏小,从实验操作的角度分析产生这种误差的原
因可能是________________________________________________________________________
________________________________________________________________________(填写一条即可)。
参考答案
题型复习(四) 化学计算题
一、根据化学式的计算
1.C 2.C 3.C 4.D 5.C 6.A 7.90∶11∶40 8.(1)2∶5∶1 (2)24∶5∶35.5(或 48∶10∶71) 9.
(1)6∶1∶8 (2)48.6% (3)C HO
4 8 2
二、选择型计算
1.B 2.A 3.C 4.AC 5.B 6.B 7.B 8.B 9.B 10.C
三、有关化学方程式与溶液的综合计算
题型之一 文字叙述型
1.过氧化氢的质量为100 g×6.8%=6.8 g
设生成氧气的质量为x。
2HO=====2HO+O↑
2 2 2 2
68 32
6.8 g x
= x=3.2 g答:完全反应后生成氧气的质量为3.2 g。
2.设可制得氢气的质量是x。
Zn+2HCl===ZnCl +H↑
2 2
73 2
73 g×20% x
= x=0.4 g
答:可制得氢气的质量是0.4 g。
3.(1)3.2
(2)设生成铜的质量为x。
Fe+CuSO ===FeSO+Cu
4 4
56 64
2.8 g x
= x=3.2 g
FeSO 的质量为(100 g+2.8 g-3.2 g)×15%=14.94 g
4
答:回收得到硫酸亚铁的质量是14.94 g。
4.(1)0.98
(2)设20 t废碱液中氢氧化钠的质量为x。
2NaOH+HSO ===Na SO +2HO
2 4 2 4 2
80 98
x 0.98 t
= x=0.8 t
废碱液中氢氧化钠的质量分数是×100%=4%。
答:回收废碱液中氢氧化钠的质量分数是4%。
5.(1)ABCD
(2)设1 g该药物中含有氢氧化镁的质量为x。
Mg(OH) +2HCl===MgCl +2HO
2 2 2
58 73
x 20 g×3.65%
= x=0.58 g
答:1 g该药物中含氢氧化镁0.58 g。
6.(1)13∶2∶8
(2)需要加入水的质量为50 g×10%÷4%-50 g=75 g
(3)设原溶液中碳酸钾的质量为x,通入的二氧化碳的质量为y。
KCO+CO+HO===2KHCO
2 3 2 2 3
138 44 200
x y 50 g×10%
= x=3.45 g
= y=1.1 g
所以原碳酸钾溶液的质量为50 g-1.1 g=48.9 g
故原碳酸钾溶液中溶质的质量分数为
×100%=7.1%
答:(2)需加入水的质量为75 g;(3)原碳酸钾溶液中溶质的质量分数为7.1%。
7.(1)由于氯化钠中不含氧元素,根据4.8 g氧元素可以求出碳酸钠的质量是
4.8 g÷(×100%)=10.6 g
碳酸钠的质量分数为×100%=84.1%
(2)设加入稀盐酸中溶质的质量为x,生成二氧化碳的质量为y。
2HCl+NaCO===2NaCl+HO+CO↑
2 3 2 2
73 106 44
x 10.6 g y= x=7.3 g
= y=4.4 g
加入稀盐酸的质量为137 g+4.4 g-12.6 g=128.8 g
所用稀盐酸中溶质的质量分数为×100%=5.7%。
答:(1)原固体混合物中碳酸钠的质量分数为84.1%;(2)所用稀盐酸中溶质的质量分数为5.7%。
题型之二 表格数据型
1.(1)4.4
(2)设样品珍珠粉中碳酸钙的质量为x。
CaCO =====CaO+CO↑
3 2
100 44
x 4.4 g
= x=10 g
珍珠粉中碳酸钙的质量分数为×100%=80%
答:珍珠粉中碳酸钙的质量分数为80%。
2.(1)0.2
(2)由表中数据可知,第一次20 g稀硫酸中的硫酸完全反应,设20 g稀硫酸中硫酸的质量为x。
Zn+HSO ===ZnSO +H↑
2 4 4 2
98 2
x 0.08 g
= x=3.92 g
实验所用稀硫酸中溶质的质量分数为×100%=19.6%
答:实验所用稀硫酸中溶质的质量分数为19.6%。
3.(1)6∶1∶8 (2)6.6 (3)设100 mL米醋中醋酸的质量为x。
CHCOOH+NaHCO ===CH COONa+HO+CO↑
3 3 3 2 2
60 44
x 6.6 g
= x=9 g
含酸量为9 g/100 mL
答:该产品含酸量为9 g/100 mL,合格。
4.(1)一、二 (2)5∶1 (3)105.5
(4)第三组中产生二氧化碳的质量为100.0 g+9.0 g-105.0 g-m=4.0 g-m
设反应的碳酸钙的质量为y。
CaCO +2HCl===CaCl +HO+CO↑
3 2 2 2
100 44
y 4.0 g-m
= y=
9.0 g混合物中的碳酸钙质量为9.0 g×=7.5 g
所以+m=7.5 g m=1.25
5.分析表中数据可知,第2次实验时,样品中的NaCO 与CaCl 溶液恰好完全反应。
2 3 2
设12 g样品中碳酸钠的质量为x,参加反应的CaCl 的质量为y,反应生成的NaCl的质量为z。
2
NaCO+CaCl ===CaCO ↓+2NaCl
2 3 2 3
106 111 100 117
x y 10 g z
= x=10.6 g
= y=11.1 g
= z=11.7 g
(1)样品中氯化钠的质量为12 g-10.6 g=1.4 g样品中氯化钠的质量分数:×100%=11.7%
(2)加入氯化钙溶液的溶质质量分数为
×100%=11.1%(3)反应后所得溶液中氯化钠的质量为
11.7 g+1.4 g=13.1 g
反应后所得溶液的质量为12 g+100 g-10 g=102 g
反应后所得溶液中氯化钠的质量分数为×100%=12.8%
答:略。
题型之三 坐标图象题
1.(1)0.8
设参加反应的过氧化氢的质量为x。
2HO=====2HO+O↑
2 2 2 2
68 32
x 0.8 g
= x=1.7 g
过氧化氢的质量分数:×100%=2.5%
答:过氧化氢的质量分数是2.5%。
2.(1)0.4 g (2)设原稀盐酸中溶质的质量分数为x。
Zn+2HCl===ZnCl +H↑
2 2
73 2
133.4 g×x 0.4 g
= x=10.9%
答:原稀盐酸中溶质的质量分数为10.9%。
3.(1)氯化镁 (2)23.3 (3)设原BaCl 溶液的溶质质量分数为x。
2
BaCl +MgSO ===BaSO ↓+MgCl
2 4 4 2
208 233
100 g×x 23.3 g
= x=20.8%
答:原BaCl 溶液的溶质质量分数为20.8%。
2
4.(1)2.2 (2)解:设4.0 g样品中Ca(OH) 的质量为x,产生碳酸钙的质量为y。
2
CO+Ca(OH) ===CaCO ↓+HO
2 2 3 2
44 74 100
2.2 g x y
= x=2.7 g
= y=5 g
4.0 g样品中杂质CaCO 的质量为4.0 g-3.7 g=0.3 g
3
答:样品中杂质CaCO 的质量为0.3 g。
3
(3)4.2% 没有 未溶于水的氢氧化钙固体也能与过量二氧化碳反应生成可溶于水的碳酸氢钙 5.(1)减小
(2)B
(3)设稀盐酸中溶质的质量分数为x。
NaOH + HCl===NaCl+HO
2
40 36.5
20 g×4% 20 g×x
= x=3.65%
答:稀盐酸中溶质的质量分数为3.65%。
6.(1)3.65%
(2)设与HCl反应生成NaCl的质量为x,与AlCl 反应生成NaCl的质量为y。
3
NaOH+HCl===NaCl+HO
2
40 58.5
20 g×20% x
= x=5.85 g
3NaOH+AlCl ===3NaCl+Al(OH) ↓
3 3175.5 78
y 7.8 g
= y=17.55 g
当沉淀达到最大值时生成NaCl的质量为17.55 g+5.85 g=23.4 g
答:当沉淀达到最大值时生成NaCl的质量为23.4 g。
(3)100
题型之四 标签、实物图型
1.2.2
(2)设摩擦剂中CaCO 的质量为x。
3
CaCO +2HCl===CaCl +CO↑+HO
3 2 2 2
100 44
x 2.2 g
= x=5 g
摩擦剂中碳酸钙的质量分数为×100%=50%
答:摩擦剂中碳酸钙的质量分数为50%。
2.(1)钾(或K) (2)4.8
(3)设生成KCl的质量为x。
2KClO=====2KCl+3O↑
3 2
149 96
x 4.8 g
= x=7.45 g
滤液中溶质质量分数为×100%=14.9%
答:滤液中溶质质量分数为14.9%。
3.(1)6
(2)设废水中亚硫酸钠的质量分数为x。
NaSO +CaCl ===CaSO ↓+2NaCl
2 3 2 3
126 120
50 g×x 6 g
= x=12.6%
答:废水中亚硫酸钠的质量分数为12.6%。
4.(1)1.6
(2)设加入的过氧化氢溶液中含过氧化氢的质量为x。
2HO=====2HO+O↑
2 2 2 2
68 32
x 1.6 g
= x=3.4 g
这瓶过氧化氢溶液中溶质的质量分数为×100%=5%
答:这瓶过氧化氢溶液中溶质的质量分数是5%。
5.(1)10
(2)设反应生成氢氧化钠的质量为x。
Ca(OH) +NaCO===CaCO ↓+2NaOH
2 2 3 3
100 80
10 g x
= x=8 g
所得溶液中溶质的质量分数为×100%=10%
答:所得氢氧化钠溶液中溶质的质量分数为10%。
6.(1)红色褪去(或变为无色) 50
(2)烧碱溶液的质量=60 g-20 g=40 g
盐酸的质量=110 g-60 g=50 g50 g稀盐酸中溶质的质量为50 g×7.3%=3.65 g
设烧碱溶液中氢氧化钠的质量为x。
NaOH+HCl===NaCl+HO
2
40 36.5
x 3.65 g
= x=4 g
该烧碱溶液中溶质的质量分数为×100%=10%
答:该烧碱溶液中溶质的质量分数是10%。
(3)滴加盐酸时的操作是边滴边振荡,振荡时有溶液溅出(合理即可)
滚动测试(一) 身边的化学物质
1.A 2.D 3.A 4.B 5.C 6.C 7.B 8.C 9.(1)H O (2)O (3)硬水 10.(1)t (2)丙 (3)丙>乙>甲 11.
2 2 2
(1)Fe O (2)①3CO+Fe O=====2Fe+3CO ②Fe+CuCl ===FeCl +Cu(或Fe+Cu(NO )===Fe(NO ) +Cu等合
2 3 2 3 2 2 2 3 2 3 2
理答案) (3)复分解反应 12.(1)分液漏斗 集气瓶 (2)A D CaCO +2HCl===CaCl +HO+CO↑ (3)①a
3 2 2 2
②C 25 13.(1)③ (2)碳酸钠 (3)取少量(1)中所得溶液于试管中,滴加过量的氯化钙溶液,然后向上层清液中加
入酚酞试液,若溶液变红,则说明原样品中还含有氢氧化钠 14.(1)96.36%
(2)完全反应生成CaCO 的质量为111 g+100 g-201 g=10 g
3
设所用氯化钙溶液中溶质的质量为x。
NaCO+CaCl ===CaCO ↓+2NaCl
2 3 2 3
111 100
x 10 g
= x=11.1 g
所用氯化钙溶液中溶质的质量分数:×100%=11.1%
答:所用氯化钙溶液中溶质的质量分数为11.1%。
滚动测试(二) 物质构成的奥秘
1.B 2.D 3.B 4.C 5.D 6.A 7.A 8.D 9.B 10.D 11.B 12.(1)C (2)12 (3)CaSiO 13.(1)79.90
3
(2)B (3)KBr (4)S2- 14.(1)MnO 2个氟原子 (2)Al3+ Al O 15.(1)①8 ②钠原子的质子数为11 ③Na+
2 3
(2)①BC ②分子种类 ③湿衣服在阳光下比在阴凉处干得快 16.(1)1 (2)Cl- (3)SiF (4)五 17.(1)78
4
(2)20∶19 (3)48.7% 18.(1)74.5
(2)设一个人每天摄入该品牌低钠盐不宜超过的质量为x。
x×70%×=2.3 g
x=8.4 g
答:一个人每天摄入该品牌低钠盐的质量不宜超过8.4 g。
滚动测试(三) 物质的化学变化
1.C 2.A 3.C 4.D 5.D 6.C 7.B 8.C 9.(1)2Mg+O=====2MgO (2)Zn+HSO ===ZnSO +H↑
2 2 4 4 2
(3)NaOH+HCl===NaCl+HO 10.(1)16 (2)O CH (3)一个碳原子和2个氧原子 (4)CH +2O=====2HO+
2 2 4 4 2 2
CO 11.(1)NaOH (2)CH +2O=====CO +2HO 13.(1)在金属活动性顺序表里排在氢元素之前的金属
2 4 2 2 2
(2)Cu(NO )(或CuSO 或CuCl ) (3)C+HO=====H+CO C (4)Cl S (5)属于 13.(1)C 碳、氢元素的质量比
3 2 4 2 2 2 2
为3∶1(或氢、碳元素的质量比为1∶3) (2)CAB 2HO=====2H↑+O↑
2 2 2
14.(1)生成硫酸钡的质量:15 g+180 g+100 g-271.7 g=23.3 g
设硫酸钠的质量为x,生成氯化钠的质量为y。
NaSO +BaCl ===BaSO ↓+2NaCl
2 4 2 4
142 233 117
x 23.3 g y
= x=14.2 g
= y=11.7 g
该混合物中硫酸钠的质量分数:
×100%=94.7%
(2)反应后所得滤液中氯化钠的质量为11.7 g+(15 g-14.2 g)=12.5 g
反应后所得滤液中溶质的质量分数:×100%=4.6%
答:(1)该混合物中硫酸钠的质量分数为94.7%;(2)反应后所得滤液中溶质的质量分数为4.6%。
滚动测试(四) 化学与社会发展
1.D 2.B 3.C 4.B 5.D 6.D 7.C 8.A 9.B 10.(1)金刚石 碳酸氢钠 维生素 (2)保持表面清洁干燥
(或涂油等) (3)涤纶 11.(1)隔绝氧气(空气) (2)维生素 (3)金属 (4)植树造林(或泥沙过滤污染物等,合理均可)
12.(1)D (2)②和④ (3)N (4)C H +5O=====3CO +4HO 13.(1)天然 (2)蛋白质 (3)肉松 (4)5∶48 14.(1)
2 3 8 2 2 2
奶茶样品种类单一(或奶茶样品种类不足) (2)AB (3)脂肪、糖类中不含氮元素 (4)AD 15.(1)1∶2∶1 40%
(2)设需要葡萄糖的质量为x。
C H O+2Ag(NH)OH=====C H ON+HO+
6 12 6 3 2 6 15 7 2
2Ag↓+3NH ↑
3
180 216
x 21.6 g
= x=18 g
答:需要葡萄糖的质量为18 g。
滚动测试(五) 科学探究
1.C 2.C 3.C 4.A 5.C 6.C 7.C 8.(1)外焰 (2)左 (3)温度达到可燃物的着火点 4P+5O=====2PO
2 2 5
(4)压强(或气压) 9.(1)氨气 (2)BaCl (3)NaOH、NaCl或NaOH、NaCl、NaSO 10.(1)B 2KMnO =====KMnO
2 2 4 4 2 4
+MnO +O↑ (2)② (3)①CaCO +2HCl===CaCl +HO+CO↑ ② O 浓硫酸 ③过滤 11.CuO+
2 2 3 2 2 2 2
HSO ===CuSO+HO 【猜想与假设】CuSO 、HSO 【反思与评价】甲(或乙) 氯化钡与硫酸、硫酸铜都能发生反
2 4 4 2 4 2 4
应,产生白色沉淀,不能判断溶液中是否含有硫酸(或加入铁粉后,有红色固体出现,只能证明溶液中有CuSO ,不能
4
判断溶液中是否有硫酸) 12.(1)不能
设固体混合物中NaCO 的质量为x。
2 3
NaCO+Ca(OH) ===CaCO ↓+2NaOH
2 3 2 3
106 100
x 2.0 g
= x=2.12 g
固体混合物中Na CO 的质量分数为×100%=21.2%
2 3
答:固体混合物中Na CO 的质量分数为21.2%。
2 3
滚动测试(六) 综合测试
1.D 2.D 3.B 4.B 5.B 6.A 7.A 8.B 9.(1)镁原子 一个二氧化碳分子中有2个氧原子 NH Cl (2)①
4
塑料拖鞋 元素 ②分子在不断运动 隔绝空气 10.(1)C(或CO) (2)产生蓝色沉淀 (3)①C+2CuO=====2Cu+
CO↑(或CO+CuO=====Cu+CO) ②NaCO +Ca(OH) ===CaCO ↓+2NaOH (4)灭火(或温室肥料或光合作用)
2 2 2 3 2 3
11.(1)锥形瓶 (2)2KMnO=====KMnO +MnO +O↑(或 2KClO=====2KCl+3O↑) (3)BD CaCO +
4 2 4 2 2 3 2 3
2HCl===CaCl +HO+CO↑ (4)C (5)①CO ②关闭活塞甲,打开活塞乙 12【. 作出猜想】HCl 【实验与结论】②
2 2 2
不能 酚酞在酸性溶液中也是无色的 ③碳酸钙 有气泡产生 【拓展与应用】①碳酸钙 ②腐蚀下水道 13.(1)设
碳酸钙的质量为x,生成氯化钙的质量为y。
CaCO +2HCl===CaCl +CO↑+HO
3 2 2 2
100 111 44
x y 8.8 g
= x=20 g
= y=22.2 g
“石头纸”中碳酸钙的质量分数:×100%=80%
(2)完全反应后烧杯内溶液的溶质的质量分数是
=14.1%
答:(1)“石头纸”中碳酸钙的质量分数为80%;(2)完全反应后烧杯内溶液的溶质的质量分数是14.1%。