文档内容
第 04 练
离子共存 离子方程式的正误判断
一、离子能否大量共存的判断方法
1.四种离子反应类型
反应类型 不能大量共存的离子
生成沉淀 Ba2+与CO、SO、SO;SiO与H+不能大量共存
复分
生成气体 H+与CO、HCO、S2-、SO等不能大量共存
解反
生成弱电解
应 H+与OH-、ClO-、F-、CHCOO-等不能大量共存
3
质
Fe3+能氧化S2-、I-等;MnO、ClO-在酸性、碱性、中性
氧化还原反应
条件下都有强氧化性,能将I-、Fe2+、SO等氧化
Al3+与AlO、HCO、CO、S2-、HS-等水解彻底;Fe3+与
盐类的双水解
AlO、HCO、CO等水解彻底,不能大量共存
Fe3+与SCN-;Ag+与NH ·H O;Fe2+和[Fe(CN) ]3-不能
3 2 6
络合反应
大量共存
2.离子共存的常见条件要求
条件类型 常见表述 点拨
(1)“一定大量共存”
题干要求 (2)“可能大量共存” 审清关键字词
(3)“不能大量共存”
Cu2+、Fe2+、Fe3+、
“无色” MnO-等有色离子不能
大量存在
“pH=1”或“pH=13” 溶液显酸性或碱性
只能是氧化性离子和还
常见的限制条件
原性离子不共存,并不
“因发生氧化还原反应而不
是其他离子反应,同时
能共存”
要注
意溶液酸碱性的影响
“透明” “透明”也可“有色”
二、离子方程式的正误判断方法1.检查拆分是否正确:“强酸强碱可溶性盐”要拆
易溶于水、易电离的强电解质用实际参加反应的离子表示:如强酸(HCl、稀HSO 、
2 4
HNO 、HBr、HI、HClO)拆分,但浓 HSO 不拆分;强碱[NaOH、Ba(OH) 、KOH、
3 4 2 4 2
Ca(OH) ]拆分,但浑浊石灰水不拆分;溶于水并且电离的盐拆分,如Fe(SCN) 虽然溶于
2 3
水,但不电离不能拆分。非电解质、弱电解质(弱酸、弱碱、水等)、难溶物、气体、氧化
物、单质等均用化学式表示。
2.检查生成物是否正确,即是否符合反应原理,检查离子方程式中各项是否都有公约
数,检查是否漏写某个反应。如Ba(OH) 与HSO 的反应不能书写成Ba2++OH-+SO+H+
2 2 4
===BaSO ↓+HO。
4 2
3.检查离子方程式两边是否符合质量(原子)守恒、电荷守恒、得失电子守恒。
4.注意限制反应条件的影响,如溶液的浓度,浓 HNO 与稀HNO 与金属反应;少量、
3 3
过量中生成物是否正确;注意溶液的环境(酸碱性);注意氧化性、还原性强弱引起的反应
顺序。
1.(2023·湖北·襄阳四中校考模拟预测)对于下列实验,其离子方程式描述错误的是
A.稀硝酸中加入少量铁粉:
B.将足量 溶液滴入 浊液中:
C. 通入冷的KOH溶液中:
D. 溶液中加入少量 溶液:
【答案】A
【详解】A.稀硝酸中加入少量铁粉生成硝酸铁和一氧化氮气体,
,A错误;
B.足量 溶液滴入 浊液中,氢氧化镁浊液转化为氢氧化铁浊液:
,B正确;
C. 通入冷的KOH溶液中生成氯化钾和次氯酸钾、水: ,C
正确;
D. 溶液中加入少量 溶液,钡离子和氢氧根离子完全反应生成硫酸钡沉
淀和水, ,D正确;
故选A。
2.(2023·广东·统考二模)下列有关含氮化合物的反应中,对应的离子方程式书写正确的
是A.将过量SO 通入冷氨水中:NH •H O+SO =HSO +NH
2 3 2 2
B.室温下用稀硝酸溶解铜:Cu+4H++2NO =Cu2++2NO↑+2H O
2 2
C.NO 溶于水制硝酸:2NO +2H O=H++NO +NO
2 2 2
D.等体积、等浓度的NH HSO 溶液与NaOH溶液混合:NH +OH-=NH•H O
4 4 3 2
【答案】A
【详解】A.过量SO 通入冷氨水,生成 和 ,离子方程式为NH •H O+SO =HSO
2 3 2 2
+NH ,A正确;
B.稀硝酸与铜反应生成NO而不是NO ,离子方程式为3Cu+8H++2 =3Cu2+
2
+2NO↑+4HO,B错误;
2
C.NO 溶于水生成HNO 和NO,离子方程式为3NO +H O=2H++2 +NO,C错误;
2 3 2 2
D.等体积、等浓度的NH HSO 溶液与NaOH溶液混合,离子方程式为H++OH-=H O,D
4 4 2
错误;
故答案选A。
3.(2023·河北石家庄·校联考模拟预测)离子反应在生产、生活中有许多应用。下列离子
方程式书写正确的是
A.氯气与烧碱溶液反应制备漂白液:
B.和面时用小苏打和食醋能使馒头蓬松:
C.漂白粉在空气中久置变质:
D.用氨水吸收烟气中的二氧化硫:
【答案】A
【详解】A.漂白液的有效成分是NaClO,氯气与烧碱反应的离子方程式为Cl+2OH-=Cl-
2
+ClO-+H O,故A正确;
2
B.食醋的主要成分是醋酸,醋酸是弱酸,不能拆分,故B错误;
C.漂白粉在空气中久置,会与空气中的二氧化碳发生反应得到次氯酸,不是水溶液中,
不存在离子反应,方程式为 ,故C错误;
D.NH ·H O是弱碱,不能拆分,故D错误;
3 2
答案为A。
4.(2023·上海虹口·统考二模)下列离子方程式正确的是
A.氨气溶于醋酸溶液:NH +H+=NH
3
B.碳酸钙与稀盐酸反应:CO +2H+=CO ↑+H O
2 2
C.硫酸铜溶液与氢氧化钡溶液反应:SO +Ba2+=BaSO ↓
4D.向氯化铜溶液中通入硫化氢气体:Cu2++H S=CuS↓+2H+
2
【答案】D
【详解】A.氨气溶于醋酸的离子方程式为NH +CH COOH=CH COO-+ ,A错误;
3 3 3
B.碳酸钙与稀盐酸反应的离子方程式为CaCO +2H+=Ca2++H O+CO↑,B错误;
3 2 2
C.硫酸铜和氢氧化钡反应,离子方程式为Cu2++ +Ba2++2OH-=BaSO ↓+Cu(OH) ↓,C
4 2
错误;
D.向氯化铜溶液中通入硫化氢,离子方程式为Cu2++H S=CuS↓+2H+,D正确;
2
故答案选D。
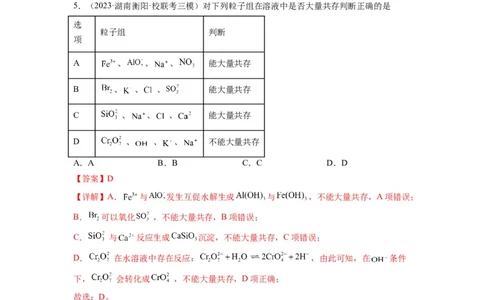
5.(2023·湖南衡阳·校联考三模)对下列粒子组在溶液中是否大量共存判断正确的是
选
粒子组 判断
项
A 、 、 、 能大量共存
B 、 、 、 能大量共存
C 、 、 、 能大量共存
D 、 、 、 不能大量共存
A.A B.B C.C D.D
【答案】D
【详解】A. 与 发生互促水解生成 与 ,不能大量共存,A项错误;
B. 可以氧化 ,不能大量共存,B项错误;
C. 与 反应生成 沉淀,不能大量共存,C项错误;
D. 在水溶液中存在反应: ,由此可知,在 条件
下, 会转化成 ,不能大量共存,D项正确;
故选:D。
6.(2023·广西·统考三模)下列方程式与所给事实不相符的是
A.将等物质的量浓度的NH HSO 溶液和NaOH溶液等体积混合:H++OH-=H O
4 4 2
B.用铁作电极电解饱和食盐水:2Cl-+2H O 2OH-+H ↑+Cl↑
2 2 2
C.NaSO 溶液中通入足量氯气: +4Cl+5H O=2 +8C1-+10H+
2 2 3 2 2
D.用碳酸钠溶液处理锅炉水垢:CaSO(s)+ (aq) CaCO (s)+ (aq)
4 3
【答案】B ⇌【详解】A.等物质的量浓度的NH HSO 溶液和NaOH溶液等体积混合,则反应为氢离子
4 4
和氢氧根离子生成水分子:H++OH-=H O,与所给事实相符,故A不符合题意;
2
B.用铁作电极电解饱和食盐水,阳极铁会发生氧化反应生成亚铁离子,与所给事实不相
符,故B符合题意;
C.NaSO 溶液中通入足量氯气发生氧化还原反应生成硫酸根离子和氯离子,
2 2 3
+4Cl+5H O=2 +8C1-+10H+,故与所给事实相符,C不符合题意;
2 2
D.碳酸钠溶液处理锅炉水垢可以将硫酸钙沉淀转化更难溶的碳酸钙:CaSO(s)+
4
(aq) CaCO (s)+ (aq),与所给事实相符,故D不符合题意;
3
故选⇌B。
7.(2023·河北·模拟预测)常温下,下列各组离子在指定溶液中一定能大量共存的是
A.澄清透明的溶液: 、 、 、 、
B.含有 的溶液: 、 、 、 、
C. 的溶液: 、 、 、 、
D.加入少量Al产生 的溶液: 、 、 、 、
【答案】B
【详解】A. 与 不能大量共存,故A不符合题意;
B.溶液中各离子相互不反应,能大量共存,故B符合题意;
C. 的溶液的 ,溶液呈酸性, 、 均不能大量存在,故C
不符合题意;
D.与Al反应产生 的溶液为强酸性溶液或强碱性溶液, 不能在碱性溶液中大量存在,
在酸性溶液中与Al反应不产生 ,故D不符合题意。
综上所述,答案为B。
8.(2023·湖南·校联考二模)下列离子反应方程式书写正确的是
A.向 溶液中滴加少量NaOH溶液:
B.小苏打溶液与明矾溶液混合:
C. 溶液中滴加KSCN溶液:
D.向 溶液中滴加少量 溶液:
【答案】B
【详解】A.与OH-的结合能力大小: ,少量氢氧根离子加入上述溶液中,应先与铝离子反应,A错误;
B.小苏打溶液与明矾溶液混合后,碳酸氢根和铝离子发生双水解,B正确;
C. 不是沉淀,C错误;
D.HS是弱酸,不能拆,D错误;
2
故选 B。
9.(2023·全国·模拟预测)下列各组离子在溶液中因发生氧化还原反应而不能大量共存的
是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
【答案】B
【详解】A. 与 因发生双水解反应生成 沉淀而不能大量共存,故A不符
合题意;
B. 在酸性条件下具有强氧化性,可以与 发生氧化还原反应而不能大量共存,故B
符合题意;
C. 与 因发生双水解反应而不能大量共存,故C不符合题意;
D.四种离子可以大量共存,故D不符合题意。
综上所述,答案为B。
10.(2023·上海崇明·统考二模)不能用离子方程式Ca2+ + = CaCO↓表示的反应是
3
A.澄清石灰水和NaHCO 溶液 B.澄清石灰水和NaCO 溶液
3 2 3
C.Ca(NO ) 溶液和(NH )CO 溶液 D.CaCl 溶液和KCO 溶液
3 2 4 2 3 2 2 3
【答案】A
【详解】A.澄清石灰水和NaHCO 溶液反应生成碳酸钙和碳酸钠,其离子方程式为2OH
3
-+2 +Ca2+=CaCO ↓+2HO+ ,故A符合题意;
3 2
B.澄清石灰水和NaCO 溶液反应生成碳酸钙和氢氧化钠,其离子方程式Ca2+ + =
2 3
CaCO ↓,故B不符合题意;
3
C.Ca(NO ) 溶液和(NH )CO 溶液反应生成碳酸钙和硝酸铵,其离子方程式Ca2+ + =
3 2 4 2 3
CaCO ↓,故C不符合题意;
3
D.CaCl 溶液和KCO 溶液反应生成碳酸钙和氯化钾,其离子方程式Ca2+ + =
2 2 3
CaCO ↓,故D不符合题意。
3
综上所述,答案为A。11.(2023·安徽宣城·统考一模)下列离子方程式表示正确的是
A.向KOH溶液中通入少量、过量HS的离子方程式均为:HS+2OH-=S2-+2H O
2 2 2
B.向FeBr 溶液中通少量、过量Cl 的离子方程式均为:2Fe2++2Br-+2Cl=2Fe3++Br +4Cl-
2 2 2 2
C.向NaHCO 溶液中加入少量、过量Ba(OH) 溶液的离子方程式均为:Ba2++OH-+HCO
3 2
=BaCO ↓+H O
3 2
D.向C HONa溶液中通入少量、过量CO 的离子方程式均为:HO+CO+C HO-→HCO
6 5 2 2 2 6 5
+C HOH
6 5
【答案】D
【详解】A.向KOH溶液中通入少量HS反应生成硫化钾和水:HS+2OH-=S2-+2H O;通
2 2 2
入过量HS生成硫氢化钾,HS+OH-=HS-+H O,A错误;
2 2 2
B.亚铁离子的还原性大于溴离子,向FeBr 溶液中通少量Cl,反应生成铁离子和氯离子:
2 2
2Fe2++Cl=2Fe3++2Cl-;通入过量Cl 生成铁离子和溴单质:2Fe2++4Br-+3Cl=2Fe3+
2 2 2
+2Br +6Cl-,B错误;
2
C.向NaHCO 溶液中加入少量Ba(OH) 溶液,钡离子、氢氧根离子完全反应生成碳酸钡沉
3 2
淀和碳酸根离子:Ba2++2OH-+2HCO =BaCO ↓+2H O+CO ;通入过量Ba(OH) 溶液,碳酸
3 2 2
氢根离子完全反应生成碳酸钡沉淀和水:Ba2++OH-+HCO =BaCO ↓+H O,C错误;
3 2
D.向C HONa溶液中通入少量、过量CO 均生成苯酚和碳酸氢根离子:HO+CO+C HO-
6 5 2 2 2 6 5
→HCO +C HOH,D正确;
6 5
故选D。
12.(2023·上海·模拟预测)下列化学反应,相应的离子方程式一定正确的是
A.向 溶液中加入少量 溶液:
B. 溶液与一定量氯气反应,转移电子数为6.02×1023时:
C.将2.24L(标准状况)CO 通入500mL 0.3 mol·L-1 溶液中:
2
D.向 溶液通入少量SO :
2
【答案】C
【详解】A.Fe3+结合OH-能力更强,先产生Fe(OH) ,A项错误;
3
B.计算得FeBr 物质的量为1mol。还原性强弱:Fe2+>Br-,转移6.02×1023电子时只有
2
Fe2+被氧化即2Fe2++Cl=2Cl-+2Fe3+,B项错误;
2C.CO 和NaOH物质的量之比为0.1:0.15=2:3,反应同时产生 和 ,该离子方程
2
式正确,C项正确;
D.HClO为强氧化性能将SO 氧化为 ,该反应表达错误,D项错误;
2
故选C。
13.(2023·天津·校联考一模)常温下,下列各组离子一定能在指定溶液中大量共存的是
A.加入铝产生氢气的溶液:
B.澄清透明的溶液:
C.能使甲基橙试液显红色的溶液:
D.水电离的 的溶液:
【答案】B
【详解】A.加入铝产生氢气的溶液可能是酸性或碱性,若为碱性,则氢氧根离子会和氢
离子、镁离子反应,不共存,A不符合题意;
B. 相互不反应,能共存,B符合题意;
C.能使甲基橙试液显红色的溶液为酸性,则氢离子和次氯酸根离子会结合为弱酸次氯酸,
C不符合题意;
D.水电离的 的溶液可能是酸性或碱性,若为酸性,则氢离子和碳酸
氢根离子、亚硫酸根离子反应;若为碱性,氢氧根离子会和碳酸氢根离子反应,不共存,
D不符合题意;
故选B。
14.(2023·安徽黄山·统考二模)下列化学反应对应的离子方程式表示正确的是
A.向NH Al(SO ) 中滴加Ba(OH) 使 恰好完全沉淀:Al3++2 +2Ba2++4OH-=
4 4 2 2
+2H O+2BaSO↓
2 4
B.向新制氯水中加入少量CaCO :2Cl+H O+CaCO =Ca2++2Cl-+CO ↑+2HClO
3 2 2 3 2
C.向NaHS溶液中滴加少量的CuSO 溶液:Cu2++HS-=CuS↓+H+
4
D.Fe O 溶于HI溶液:Fe O+8H+=Fe2++2Fe3++4H O
3 4 3 4 2
【答案】B
【详解】A.由于 恰好完全沉淀,说明NH Al(SO ) 与Ba(OH) 物质的量之比为1:2,
4 4 2 2
而与OH-反应的先后顺序为 ,故反应离子方程式为:
,A错误;
B.氯气溶于水生成盐酸和次氯酸,加入少量CaCO 后生成氯化钙、二氧化碳、水,故反
3
应离子方程式为 ,B正确;
C.HS-与Cu2+反应生成CuS和HS,故反应离子方程式为: ,C
2错误;
D.Fe O 溶于HI溶液生成Fe2+、I 和HO,反应离子方程式为:
3 4 2 2
,D错误。
故选B。
15.(2023·湖北武汉·校联考模拟预测)能正确表示下列反应的离子方程式为
A.向酸性KMnO 溶液中滴加双氧水:2MnO +H O+6H+=2Mn2++3O ↑+4H O
4 2 2 2 2
B.向硝酸铁溶液中通入少量的SO :2Fe3++SO+2H O=2Fe2++2H++SO
2 2 2
C.向次氯酸钠溶液中通入少量CO:ClO-+CO +H O=HC1O+HCO
2 2 2
D.侯氏制碱法的反应原理:NH +CO +H O=HCO +NH
3 2 2
【答案】C
【详解】A.向酸性KMnO 溶液中滴加双氧水,双氧水被氧化成氧气,其反应的离子方程
4
式为2MnO +5H O+6H+=2Mn2++5O ↑+8H O,A项错误;
2 2 2 2
B.硝酸的氧化性大于铁离子,因此向硝酸铁中加入少量SO 时,硝酸与SO 发生氧化还原
2 2
反应,B项错误;
C.由于酸性:HCO>HClO>HCO ,则向次氯酸钠溶液中通入少量的CO 生产次氯酸和
2 3 2
碳酸氢钠:ClO-+CO +H O=HClO+HCO ,C项正确;
2 2
D.侯氏制碱法中发生反应:NH +NaCl+HO+CO=NaHCO↓+NHCl,由于NaHCO 的溶解
3 2 2 3 4 3
度比碳酸钠小,能够从溶液中析出,故书写离子方程式时NaHCO 应写化学式,D项错误。
3
故选C。
16.(2023·浙江·高考真题)下列反应的离子方程式不正确的是
A. 通入氢氧化钠溶液:
B.氧化铝溶于氢氧化钠溶液:
C.过量 通入饱和碳酸钠溶液:
D. 溶液中滴入氯化钙溶液:
【答案】D
【详解】A. 通入氢氧化钠溶液中反应生成氯化钠、次氯酸钠和水,反应的离子方程式
为: ,选项A正确;
B.氧化铝溶于氢氧化钠溶液生成偏铝酸钠和水,反应的离子方程式为:
,选项B正确;C.过量 通入饱和碳酸钠溶液反应产生碳酸氢钠晶体,反应的离子方程式为:
,选项C正确;
D. 溶液中滴入氯化钙溶液,因亚硫酸酸性弱于盐酸,不能发生反应,选项D不正确;
答案选D。
17.(2022·天津·统考高考真题)25℃时,下列各组离子中可以在水溶液中大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
【答案】D
【详解】A. 与 反应生成次氯酸而不能大量共存,故A不符合题意;
B. 、 、 发生氧化还原反应而不能大量共存,故B不符合题意;
C. 与 反应生成氢氧化铝沉淀和二氧化碳气体而不能大量共存,故C不符合题意;
D. 、 、 、 是大量共存,故D符合题意。
综上所述,答案为D。
18.(2022·浙江·统考高考真题)下列反应的离子方程式不正确的是
A.盐酸中滴加 溶液:
B. 溶液中通入过量 :
C.乙醇与 酸性溶液反应:
D.溴与冷的 溶液反应:
【答案】D
【详解】A.盐酸中滴加 溶液,发生离子反应生成硅酸沉淀,该反应的离子方程式
为 ,A正确;
B.亚硫酸的酸性强于碳酸,因此, 溶液中通入过量 发生离子反应生成亚硫酸
氢钠和二氧化碳,该反应的离子方程式为 ,B正确;
C.乙醇与 酸性溶液反应发生反应,乙醇被氧化为乙酸, 被还原为 ,该
反应的离子方程式为 ,C正确;
D.类比氯气与碱反应可知,溴与冷的 溶液反应生成溴化钠、次溴酸钠和水,该反
应的离子方程式为 ,D不正确。
综上所述,本题选D。19.(2022·广东·高考真题)下列关于 的化合物之间转化反应的离子方程式书写正确的
是
A.碱转化为酸式盐:
B.碱转化为两种盐:
C.过氧化物转化为碱:
D.盐转化为另一种盐:
【答案】B
【详解】A.向氢氧化钠溶液中通入足量的二氧化碳,碱可以转化成酸式盐,离子方程式
为:CO+OH-= ,故A错误;
2
B.氯气通入NaOH溶液中可以生成氯化钠和次氯酸钠两种盐,其离子方程式为:
Cl+2OH-=Cl-+ClO-+H O,故B正确;
2 2
C.钠的过氧化物为NaO,可以和水反应生成氢氧化钠,但在离子方程式里NaO 不能拆
2 2 2 2
成离子,故C错误;
D.硅酸钠溶于水,在离子方程式里要写成离子,故D错误;
故选B。
20.(2022·全国·高考真题)能正确表示下列反应的离子方程式为
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B.明矾溶液与过量氨水混合:Al3++4NH+2H O=AlO +4NH
3 2
C.硅酸钠溶液中通入二氧化碳:SiO +CO +H O=HSiO +HCO
2 2
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO
2 4 4
=BaSO ↓+2H O
4 2
【答案】D
【详解】A.硝酸具有强氧化性,可以将S2-氧化为S单质,自身根据其浓度大小还原为NO
或NO ,反应的离子方程式为4H++2NO +S2-=S↓+2NO↑+2H O(浓)或8H++2NO +3S2-
2 2 2
=3S↓+2NO↑+4H O(稀),A错误;
2
B.明矾在水中可以电离出Al3+,可以与氨水电离出的OH-发生反应生成Al(OH) ,但由于
3
氨水的碱性较弱,生成的Al(OH) 不能继续与弱碱发生反应,故反应的离子方程式为Al3+
3
+3NH·H O=Al(OH) ↓+3NH ,B错误;
3 2 3
C.硅酸的酸性小于碳酸,向硅酸钠溶液中通入二氧化碳时,生成硅酸沉淀,二氧化碳则
根据其通入的量的多少反应为碳酸根或碳酸氢根,反应的离子方程式为SiO
+H O+CO=H SiO↓+CO (CO 少量)或SiO +2H O+2CO=H SiO↓+2HCO (CO 过量),C
2 2 2 3 2 2 2 2 3 2
错误;D.将等物质的量浓度的Ba(OH) 与NH HSO 溶液以体积比1:2混合,Ba(OH) 电离出的
2 4 4 2
OH-与NH HSO 电离出的H+反应生成水,Ba(OH) 电离出的Ba2+与NH HSO 电离出的SO
4 4 2 4 4
反应生成BaSO 沉淀,反应的离子方程为为Ba2++2OH-+2H++SO =BaSO ↓+2H O,D正确;
4 4 2
故答案选D。
21.(2022·浙江·统考高考真题)下列实验对应的离子方程式不正确的是
A.将碳酸氢钙溶液与过量的澄清石灰水混合: +Ca2++OH-=CaCO ↓+H O
3 2
B.将少量NO 通入NaOH溶液:2NO +2OH-= + +H O
2 2 2
C.将少量SO 通入NaClO溶液:SO +H O+2ClO-= +2HClO
2 2 2
D.向氨水中滴入少量硝酸银溶液:Ag++2NH·H O= +2H O
3 2 2
【答案】C
【详解】A. 将碳酸氢钙溶液与过量的澄清石灰水混合,反应生成碳酸钙和水,反应的离子
方程式为: +Ca2++OH-=CaCO ↓+H O,选项A正确;
3 2
B. 将少量NO 通入NaOH溶液,反应生成硝酸钠、亚硝酸钠和水,反应的离子方程式为:
2
2NO +2OH-= + +H O,选项B正确;
2 2
C. 将少量SO 通入NaClO溶液,反应生成硫酸钠和盐酸,反应的离子方程式为:
2
SO +H O+3ClO-= +2HClO+Cl-,选项C不正确;
2 2
D. 向氨水中滴入少量硝酸银溶液,反应生成氢氧化二氨合银,反应的离子方程式为:Ag+
+2NH·H O= +2H O,选项D正确;
3 2 2
答案选C。
22.(2022·湖北·统考高考真题)下列各组离子在给定溶液中能大量共存的是
A.在 氨水中:
B.在 氯化钠溶液中:
C.在 醋酸溶液中:
D.在 硝酸银溶液中:
【答案】C
【详解】A.氨水显碱性,会与 反应,不能大量共存,A项错误;
B. 会发生氧化还原反应,不能大量共存,B项错误;
C.醋酸显酸性,在醋酸溶液中 均不会发生反应,能大量共存,C项
正确;D.硝酸银中的银离子会与氯离子反应生成沉淀,不能大量共存,D项错误;
答案选C。
23.(2021·重庆·统考高考真题)25°时, 下列各组离子在指定溶液中一定能大量共存的是
A.1.0 mol·L-1氯化钡溶液中: Mg2+、K+、Br-、
B.1.0 mol·L-1硫酸中: A13+、 Na+、Cl-、
C.pH=1l 的氨水中: Fe2+、 Na+、 、ClO-
D.pH=1的硝酸中: Fe3+、K+、I-、
【答案】B
【详解】A.Ba2+与 生成BaSO,不能大量共存,A项错误;
4
B.该条件下各离子之间不发生反应,可以大量共存,B项正确;
C. Fe2+会与氨水反应生成Fe(OH) 沉淀,不能大量共存,C项错误;
2
D.硝酸是强氧化剂会与具有还原性的I-发生氧化还原反应,不能大量共存,D项错误;
答案选B。
24.(2021·全国·统考高考真题)下列过程中的化学反应,相应的离子方程式正确的是
A.用碳酸钠溶液处理水垢中 的硫酸钙:
B.过量铁粉加入稀硝酸中:
C.硫酸铝溶液中滴加少量氢氧化钾溶液:
D.氯化铜溶液中通入硫化氢:
【答案】A
【详解】A.硫酸钙微溶,用碳酸钠溶液处理水垢中的硫酸钙转化为难溶的碳酸钙,离子方
程式为: ,故A正确;
B.过量的铁粉与稀硝酸反应生成硝酸亚铁、一氧化氮和水,离子方程式应为:3Fe+8H+
+2N =3Fe2++2NO↑+4HO,故B错误;
2
C.硫酸铝溶液与少量氢氧化钾溶液反应生成氢氧化铝沉淀和硫酸钾,离子方程式应为:
Al3++3OH-=Al(OH) ↓,故C错误;
3
D.硫化氢为弱电解质,书写离子方程式时不能拆,离子方程式应为:Cu2+
+H S=CuS↓+2H+,故D错误;
2
答案选A。
25.(2021·湖北·统考高考真题)对于下列实验,不能正确描述其反应的离子方程式是
A.向氢氧化钡溶液中加入盐酸:H++OH-=H O
2
B.向硝酸银溶液中滴加少量碘化钾溶液:Ag++I-=AgI↓C.向烧碱溶液中加入一小段铝片:2Al+2OH-+6H O=2[Al(OH) ]-+3H ↑
2 4 2
D.向次氯酸钙溶液中通入少量二氧化碳气体:ClO-+CO +H O=HClO+HCO
2 2
【答案】D
【分析】此题考查离子方程式的书写。
【详解】A.化学方程式为 ,强酸,强碱,可溶性盐拆开,
离子方程式 ,A项正确;
B.化学方程式为 ,钾盐,硝酸盐要拆开,离子方程式为
,B项正确;
C.化学方程式为 ,离子方程式
,C项正确;
D.向次氯酸钙溶液中通入少量 气体,发生反应生成 和
,D项错误;
故选D。