文档内容
第 04 讲 化学反应的方向、化学反应的调控
01 模拟基础练
【题型一】化学反应的方向
【题型二】化学反应的调控
02 重难创新练
03 真题实战练
题型一 化学反应的方向
1.对于化学反应能否自发进行,下列说法中错误的是
A.非自发过程在一定条件下可能变成自发过程
B.若△H>0,△S<0,任何温度下都不能自发进行
C.若△H<0,△S>0,任何温度下都能自发进行
D.需要加热才能够进行的过程肯定不是自发过程
5.下列说法中正确的是
A.自发反应速率一定快 B.非自发反应也可能发生
C.自发反应实际可能没有发生 D.自发反应的限度一定大
3.(2024·江苏南通·模拟预测)NH 快速消除烟气中的 的反应原理为
3
。反应装置示意图如图所示。下列关于该
反应的说法不正确的是
A.该反应
B.选择高效催化剂可降低反应的焓变
C.选择高效催化剂可提高 的转化率
D.每消耗1molNH ,转移电子的数目约为
3
4.(2024·黑龙江绥化·模拟预测)一种综合处理含 尾气的工艺流程如图所示。下列叙述错误的是A.“吸收”过程中发生反应的离子方程式为
B.“吸收”和“氧化”两步反应均为熵减的反应
C. 分子和 固体所含的化学键类型相同
D.该流程中可以循环使用的物质为
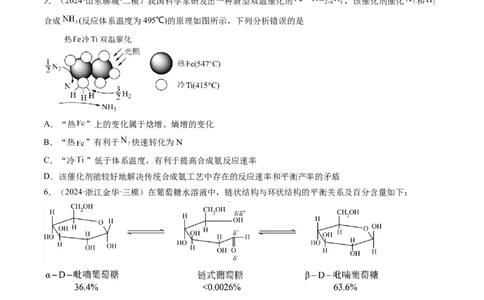
5.(2024·山东聊城·二模)我国科学家研发出一种新型双温催化剂 ,该催化剂催化 和
合成 (反应体系温度为495℃)的原理如图所示,下列分析错误的是
A.“热 ”上的变化属于焓增、熵增的变化
B.“热 ”有利于 快速转化为N
C.“冷 ”低于体系温度,有利于提高合成氨反应速率
D.该催化剂能较好地解决传统合成氨工艺中存在的反应速率和平衡产率的矛盾
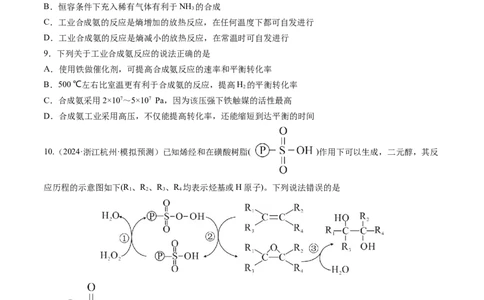
6.(2024·浙江金华·三模)在葡萄糖水溶液中,链状结构与环状结构的平衡关系及百分含量如下:
下列说法不正确的是
A.链状葡萄糖成环是-OH与-CHO发生加成反应的结果
B.链状葡萄糖成环反应的 ,
C.链状葡萄糖成环后,分子中多了一个手性碳原子
D.水溶液中, 吡喃葡萄糖比 吡喃葡萄糖稳定
7.(2024·湖北·一模)CaCN 可以作为固态氮肥,并改善土壤酸性,通过 反应制
2
备。下列说法错误的是A.该反应为熵增过程
B.该反应实现了氮的固定
C.该反应需在无水条件下进行
D. 的电子式为
题型二 化学反应的调控
8.下列有关合成氨工业的说法正确的是
A.N 的量越多,H 的转化率越大,因此,充入的N 越多越有利于NH 的合成
2 2 2 3
B.恒容条件下充入稀有气体有利于NH 的合成
3
C.工业合成氨的反应是熵增加的放热反应,在任何温度下都可自发进行
D.工业合成氨的反应是熵减小的放热反应,在常温时可自发进行
9.下列关于工业合成氨反应的说法正确的是
A.使用铁做催化剂,可提高合成氨反应的速率和平衡转化率
B.500 ℃左右比室温更有利于合成氨的反应,提高H 的平衡转化率
2
C.合成氨采用2×107~5×107 Pa,因为该压强下铁触媒的活性最高
D.合成氨工业采用高压,不仅能提高转化率,还能缩短到达平衡的时间
10.(2024·浙江杭州·模拟预测)已知烯经和在磺酸树脂( )作用下可以生成,二元醇,其反
应历程的示意图如下(R 、R 、R 、R 均表示烃基或H原子)。下列说法错误的是
1 2 3 4
A. 是该反应催化剂
B.整个过程的总反
C.操作时温度不能过高或过低
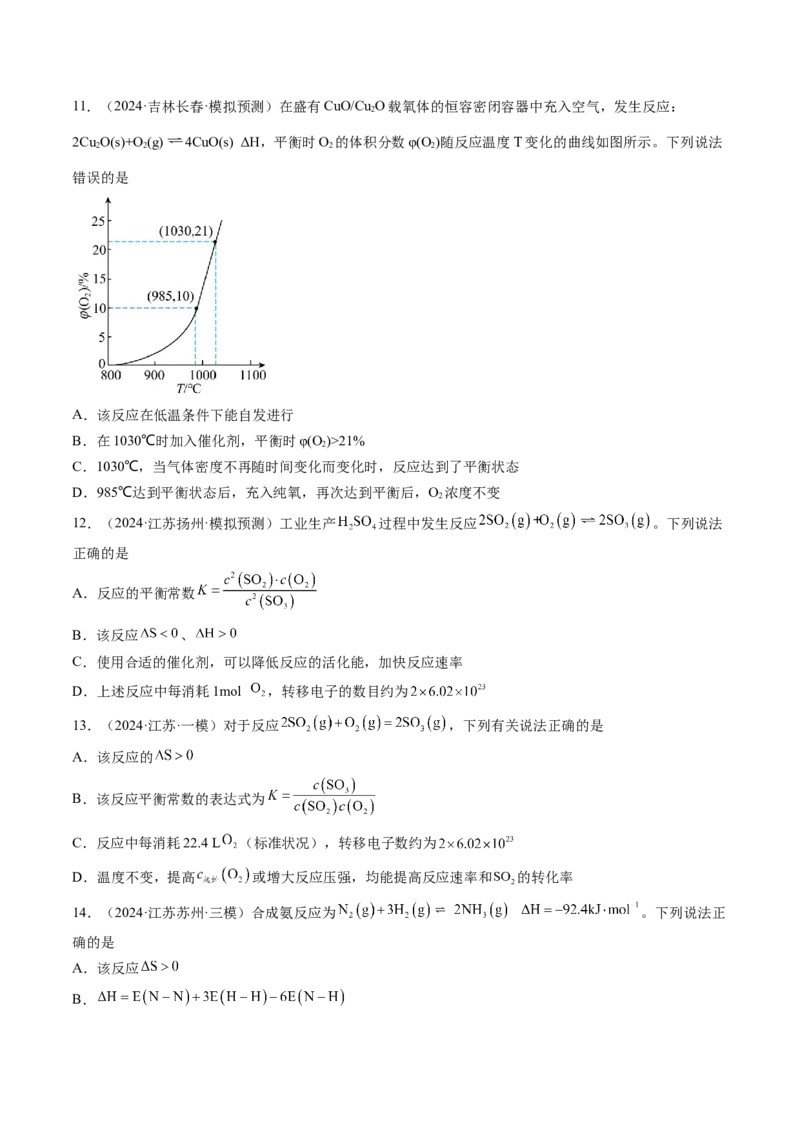
D.过程中反应的原子利用率为100%11.(2024·吉林长春·模拟预测)在盛有CuO/Cu O载氧体的恒容密闭容器中充入空气,发生反应:
2
2Cu O(s)+O (g) 4CuO(s) ΔH,平衡时O 的体积分数φ(O)随反应温度T变化的曲线如图所示。下列说法
2 2 2 2
错误的是
A.该反应在低温条件下能自发进行
B.在1030℃时加入催化剂,平衡时φ(O)>21%
2
C.1030℃,当气体密度不再随时间变化而变化时,反应达到了平衡状态
D.985℃达到平衡状态后,充入纯氧,再次达到平衡后,O 浓度不变
2
12.(2024·江苏扬州·模拟预测)工业生产 过程中发生反应 。下列说法
正确的是
A.反应的平衡常数
B.该反应 、
C.使用合适的催化剂,可以降低反应的活化能,加快反应速率
D.上述反应中每消耗1mol ,转移电子的数目约为
13.(2024·江苏·一模)对于反应 ,下列有关说法正确的是
A.该反应的
B.该反应平衡常数的表达式为
C.反应中每消耗22.4 L (标准状况),转移电子数约为
D.温度不变,提高 或增大反应压强,均能提高反应速率和 的转化率
14.(2024·江苏苏州·三模)合成氨反应为 。下列说法正
确的是
A.该反应
B.C.反应中每消耗 转移 电子
D.实际生产中以低温、高压、高活性催化剂的条件来提高氨气产率
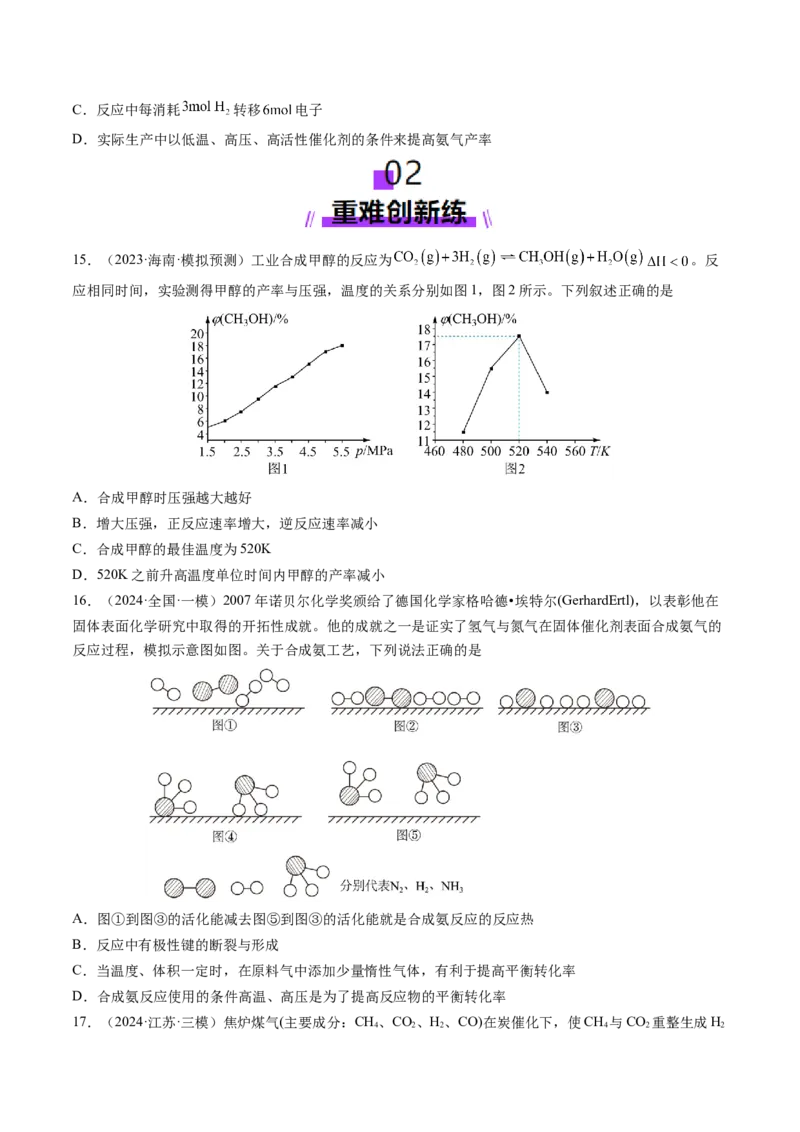
15.(2023·海南·模拟预测)工业合成甲醇的反应为 。反
应相同时间,实验测得甲醇的产率与压强,温度的关系分别如图1,图2所示。下列叙述正确的是
A.合成甲醇时压强越大越好
B.增大压强,正反应速率增大,逆反应速率减小
C.合成甲醇的最佳温度为520K
D.520K之前升高温度单位时间内甲醇的产率减小
16.(2024·全国·一模)2007年诺贝尔化学奖颁给了德国化学家格哈德•埃特尔(GerhardErtl),以表彰他在
固体表面化学研究中取得的开拓性成就。他的成就之一是证实了氢气与氮气在固体催化剂表面合成氨气的
反应过程,模拟示意图如图。关于合成氨工艺,下列说法正确的是
A.图①到图③的活化能减去图⑤到图③的活化能就是合成氨反应的反应热
B.反应中有极性键的断裂与形成
C.当温度、体积一定时,在原料气中添加少量惰性气体,有利于提高平衡转化率
D.合成氨反应使用的条件高温、高压是为了提高反应物的平衡转化率
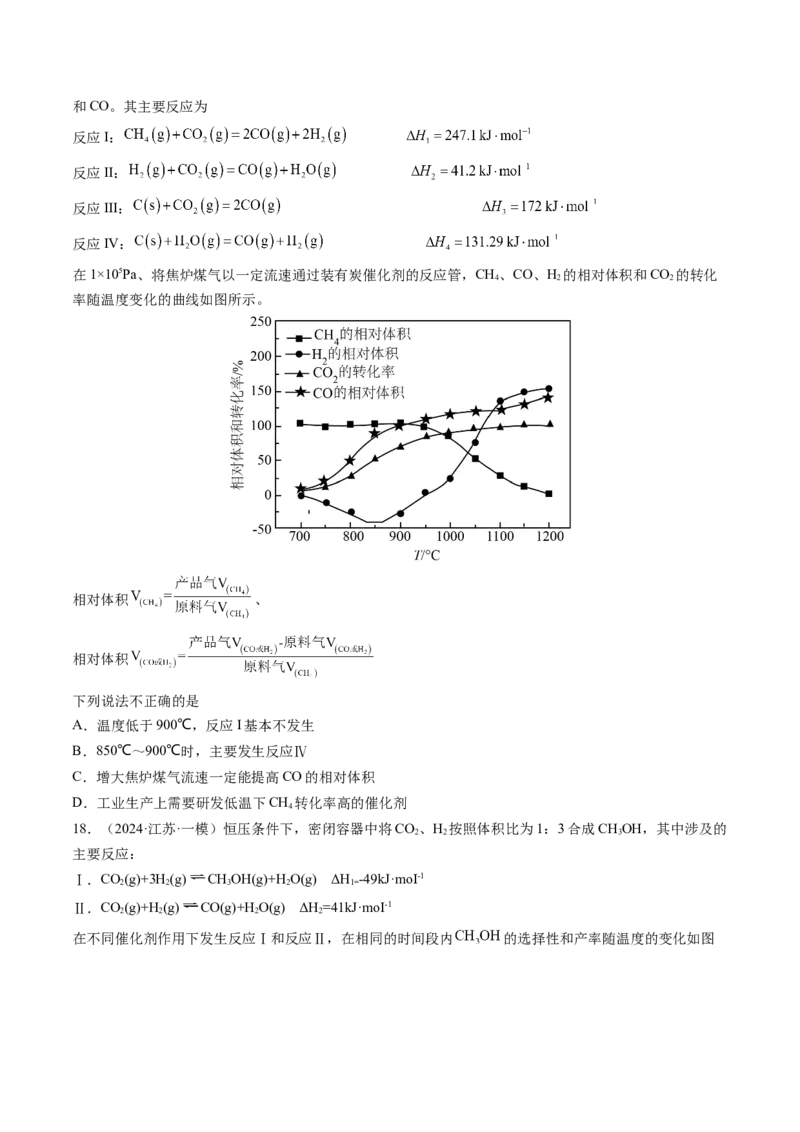
17.(2024·江苏·三模)焦炉煤气(主要成分:CH、CO、H、CO)在炭催化下,使CH 与CO 重整生成H
4 2 2 4 2 2和CO。其主要反应为
反应I:
反应II:
反应III:
反应IV:
在1×105Pa、将焦炉煤气以一定流速通过装有炭催化剂的反应管,CH、CO、H 的相对体积和CO 的转化
4 2 2
率随温度变化的曲线如图所示。
相对体积 、
相对体积
下列说法不正确的是
A.温度低于900℃,反应I基本不发生
B.850℃~900℃时,主要发生反应Ⅳ
C.增大焦炉煤气流速一定能提高CO的相对体积
D.工业生产上需要研发低温下CH 转化率高的催化剂
4
18.(2024·江苏·一模)恒压条件下,密闭容器中将CO、H 按照体积比为1:3合成CHOH,其中涉及的
2 2 3
主要反应:
Ⅰ.CO(g)+3H(g) CHOH(g)+H O(g) ΔH -49kJ·moI-1
2 2 3 2 1=
Ⅱ.CO(g)+H(g) CO(g)+HO(g) ΔH=41kJ·moI-1
2 2 2 2
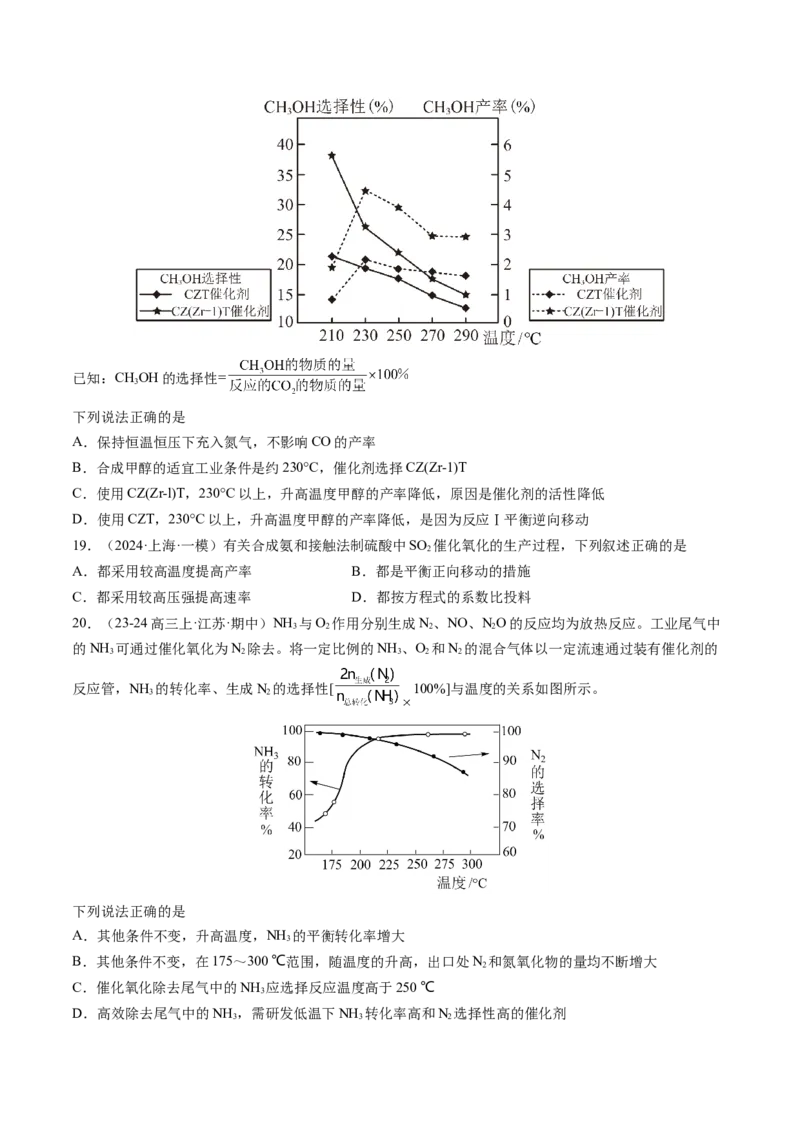
在不同催化剂作用下发生反应Ⅰ和反应Ⅱ,在相同的时间段内 的选择性和产率随温度的变化如图已知:CHOH的选择性=
3
下列说法正确的是
A.保持恒温恒压下充入氮气,不影响CO的产率
B.合成甲醇的适宜工业条件是约230°C,催化剂选择CZ(Zr-1)T
C.使用CZ(Zr-l)T,230°C以上,升高温度甲醇的产率降低,原因是催化剂的活性降低
D.使用CZT,230°C以上,升高温度甲醇的产率降低,是因为反应Ⅰ平衡逆向移动
19.(2024·上海·一模)有关合成氨和接触法制硫酸中SO 催化氧化的生产过程,下列叙述正确的是
2
A.都采用较高温度提高产率 B.都是平衡正向移动的措施
C.都采用较高压强提高速率 D.都按方程式的系数比投料
20.(23-24高三上·江苏·期中)NH 与O 作用分别生成N、NO、NO的反应均为放热反应。工业尾气中
3 2 2 2
的NH 可通过催化氧化为N 除去。将一定比例的NH 、O 和N 的混合气体以一定流速通过装有催化剂的
3 2 3 2 2
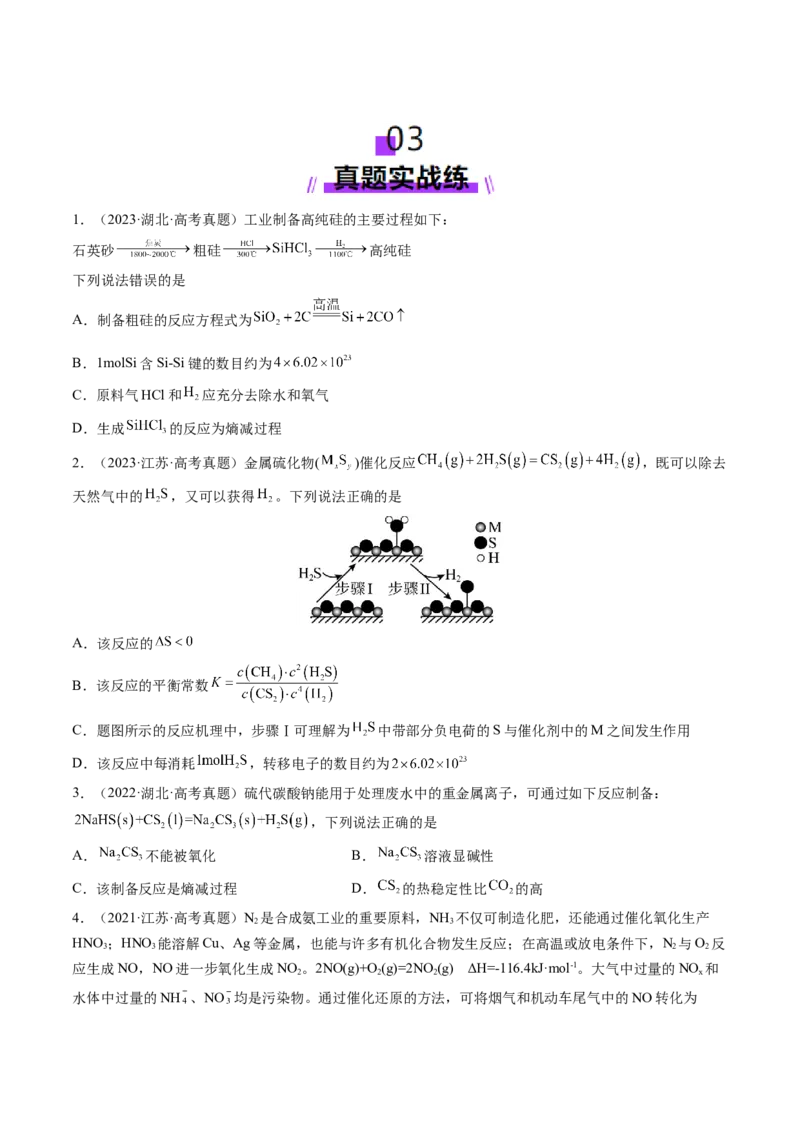
反应管,NH 的转化率、生成N 的选择性[ 100%]与温度的关系如图所示。
3 2
下列说法正确的是
A.其他条件不变,升高温度,NH 的平衡转化率增大
3
B.其他条件不变,在175~300 ℃范围,随温度的升高,出口处N 和氮氧化物的量均不断增大
2
C.催化氧化除去尾气中的NH 应选择反应温度高于250 ℃
3
D.高效除去尾气中的NH ,需研发低温下NH 转化率高和N 选择性高的催化剂
3 3 21.(2023·湖北·高考真题)工业制备高纯硅的主要过程如下:
石英砂 粗硅 高纯硅
下列说法错误的是
A.制备粗硅的反应方程式为
B.1molSi含Si-Si键的数目约为
C.原料气HCl和 应充分去除水和氧气
D.生成 的反应为熵减过程
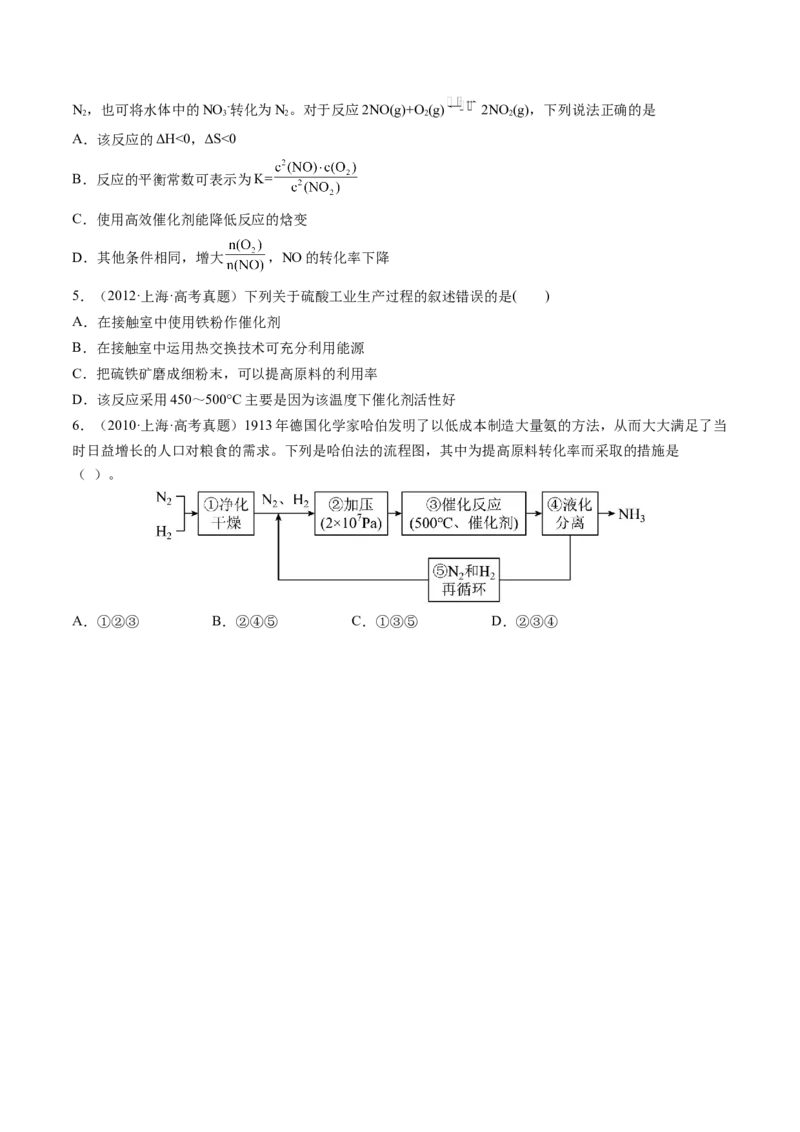
2.(2023·江苏·高考真题)金属硫化物( )催化反应 ,既可以除去
天然气中的 ,又可以获得 。下列说法正确的是
A.该反应的
B.该反应的平衡常数
C.题图所示的反应机理中,步骤Ⅰ可理解为 中带部分负电荷的S与催化剂中的M之间发生作用
D.该反应中每消耗 ,转移电子的数目约为
3.(2022·湖北·高考真题)硫代碳酸钠能用于处理废水中的重金属离子,可通过如下反应制备:
,下列说法正确的是
A. 不能被氧化 B. 溶液显碱性
C.该制备反应是熵减过程 D. 的热稳定性比 的高
4.(2021·江苏·高考真题)N 是合成氨工业的重要原料,NH 不仅可制造化肥,还能通过催化氧化生产
2 3
HNO;HNO 能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件下,N 与O 反
3 3 2 2
应生成NO,NO进一步氧化生成NO 。2NO(g)+O (g)=2NO (g) ΔH=-116.4kJ·mol-1。大气中过量的NO 和
2 2 2 x
水体中过量的NH 、NO 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N,也可将水体中的NO -转化为N。对于反应2NO(g)+O (g) 2NO (g),下列说法正确的是
2 3 2 2 2
A.该反应的ΔH<0,ΔS<0
B.反应的平衡常数可表示为K=
C.使用高效催化剂能降低反应的焓变
D.其他条件相同,增大 ,NO的转化率下降
5.(2012·上海·高考真题)下列关于硫酸工业生产过程的叙述错误的是( )
A.在接触室中使用铁粉作催化剂
B.在接触室中运用热交换技术可充分利用能源
C.把硫铁矿磨成细粉末,可以提高原料的利用率
D.该反应采用450~500°C主要是因为该温度下催化剂活性好
6.(2010·上海·高考真题)1913年德国化学家哈伯发明了以低成本制造大量氨的方法,从而大大满足了当
时日益增长的人口对粮食的需求。下列是哈伯法的流程图,其中为提高原料转化率而采取的措施是
( )。
A.①②③ B.②④⑤ C.①③⑤ D.②③④