文档内容
第 04 讲 碳、硅及无机非金属材料
目录
01
考情透视·目标导航
02 知识导图·思维引航....................................................................................................
03考点突破·考法探究.....................................................................................................
考点一 碳、硅及其化合物.....................................................
知识点1 碳及其重要化合物...................................................
知识点2 硅及其重要化合物...................................................
考向1 碳及其化合物的性质与应用..............................................
考向2 二氧化碳的综合利用...................................................
考向3 硅及其化合物的性质与应用.............................................
考向4 硅的工业制法........................................................
考点二 硅酸盐、新型无机非金属材料...........................................
知识点1 硅酸盐...........................................................
知识点2 传统无机非金属材料.................................................
知识点3 新型无机非金属材料.................................................
考向1 硅酸盐材料..........................................................
考向2 新型无机非金属材料...................................................
04真题练习·命题洞见.....................................................................................................考点要
考题统计 考情分析
求
2023浙江1月7题,2分;2022江苏卷7
题,3分;2022福建卷1题,4分;2021 本讲知识的特点是繁杂,涉及的化学反
碳及其化合
山东卷1题,2分;2021湖北卷1题,3 应多,物质间的转化关系多样。注意 Si、
物
分;2021全国乙卷1题,6分;2021海南 SiO 在现代科技中的应用经常以选择题形式
2
卷1题,2分 出现,随着新能源、新材料、新工艺的发展
应用,对碳硅及其化合物性质和应用的考查
2024浙江1月7题,3分;2023湖北卷3 有逐渐增多的趋势,已成为高考考查的热
题,3分;2023辽宁卷3题,3分;202山 点。预计高考命题仍然会以生活、生产、实
硅及其化合
东卷18题,12分;2022广东卷3题,2 际应用为背景,突出C、Si及其重要化合物
物
分;2022江苏卷6题,3分;2022浙江1 的性质及应用,题型延续选择题、填空题、
月10题,2分;2021辽宁卷1题,3分 综合推断题及实验探究题的形式,结合能
源、环保等,以新材料、新工艺为载体,考
查碳、硅及其化合物的晶体结构、性质及应
2023浙江6月1题,2分;2023湖南卷1
用,以检测考生理论联系实际、运用化学理
无机非金属 题,3分;2022河北卷1题,3分;2022
论解决实际问题的能力和将化学成果应用于
材料 广东卷3题,2分;2021重庆卷1题,3
生产、生活的意识。
分
复习目标:
1.了解C、Si元素单质及其重要化合物的制备方法,掌握其主要性质及应用。
2.了解C、Si元素单质及其重要化合物对环境的影响。
3.通过从材料组成和性质的角度对生活中常见的无机非金属材料进行分析,并能科学合理地使
用。考点一 碳、硅及其氧化物
知识点1 碳及其重要化合物
1.碳单质
(1)存在形式:有金刚石、石墨、无定形碳、足球烯,它们互为__________________。
(2)主要化学性质——还原性
可燃性 2C+O(不足)=====2CO、C+O(足量)=====CO
2 2 2
CuO:__________________________ (冶炼金属);
与氧化物反应 SiO:______________________________ (制取粗硅);
2
HO: ________________________ (制取水煤气)
2
浓HSO :__________________________________________;
2 4
与强氧化性酸反应 浓HNO:__________________________________________。
3
________________________________________________2.CO、CO 的性质对比
2
CO CO
2
______无味气体,密度 ______无味气体,密度比空气大,可
物理性质
比空气小,难溶于水 溶于水(溶解度小)
毒性 有毒(易结合______) 无毒(温室效应)
还原性 可燃性,还原氧化铁 无(灭火)
氧化性 ①与炽热炭反应,②Mg在CO 中燃烧
2
与水反应 无 CO+HO HCO
化学 2 2 2 3
与碱反应
性质 无 ____________===CaCO ↓+HO
3 2
(石灰水)
相互转化
灭火、制汽水、植物肥料、化工原料
用途 燃料、冶炼金属
等
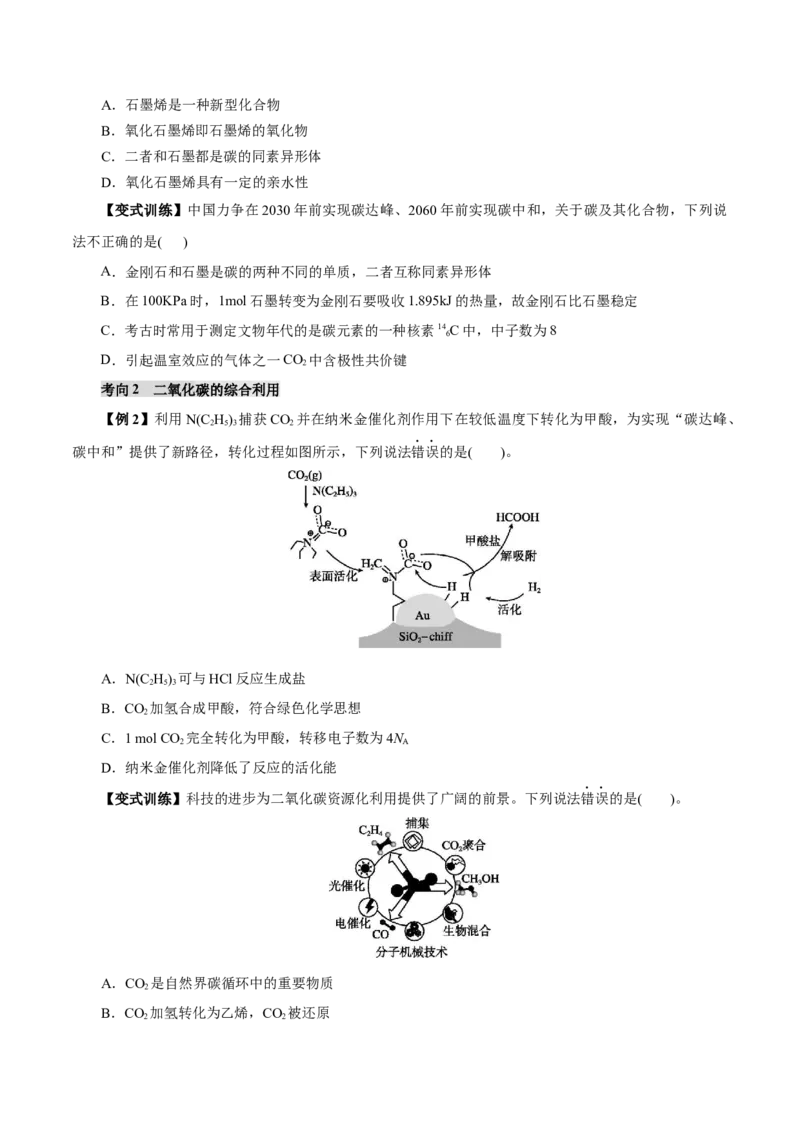
知识点2 硅及其重要化合物
1.硅单质
2.二氧化硅3.硅酸
【名师点晴】
熟记下列方程式:
1.用SiO 制取粗硅的反应:SiO+2C=====Si+2CO↑。
2 2
2.Si和NaOH溶液的反应:Si+2NaOH+HO===Na SiO+2H↑。
2 2 3 2
3.SiO 和NaOH溶液的反应:SiO+2NaOH===Na SiO+HO。
2 2 2 3 2
4.SiO 和氢氟酸的反应:SiO+4HF===SiF ↑+2HO。
2 2 4 2
5.向NaSiO 溶液中通入少量CO 气体:NaSiO+CO+HO===Na CO+HSiO↓。
2 3 2 2 3 2 2 2 3 2 3
考向1 碳及其化合物的性质与应用
【例1】新材料的新秀——石墨烯和氧化石墨烯已成为物理、化学、材料科学研究的国际热点课题。
其结构模型如图所示。
下列有关说法正确的是( )A.石墨烯是一种新型化合物
B.氧化石墨烯即石墨烯的氧化物
C.二者和石墨都是碳的同素异形体
D.氧化石墨烯具有一定的亲水性
【变式训练】中国力争在2030年前实现碳达峰、2060年前实现碳中和,关于碳及其化合物,下列说
法不正确的是( )
A.金刚石和石墨是碳的两种不同的单质,二者互称同素异形体
B.在100KPa时,1mol石墨转变为金刚石要吸收1.895kJ的热量,故金刚石比石墨稳定
C.考古时常用于测定文物年代的是碳元素的一种核素14C中,中子数为8
6
D.引起温室效应的气体之一CO 中含极性共价键
2
考向2 二氧化碳的综合利用
【例2】利用N(C H) 捕获CO 并在纳米金催化剂作用下在较低温度下转化为甲酸,为实现“碳达峰、
2 5 3 2
碳中和”提供了新路径,转化过程如图所示,下列说法错误的是( )。
A.N(C H) 可与HCl反应生成盐
2 5 3
B.CO 加氢合成甲酸,符合绿色化学思想
2
C.1 mol CO 完全转化为甲酸,转移电子数为4N
2 A
D.纳米金催化剂降低了反应的活化能
【变式训练】科技的进步为二氧化碳资源化利用提供了广阔的前景。下列说法错误的是( )。
A.CO 是自然界碳循环中的重要物质
2
B.CO 加氢转化为乙烯,CO 被还原
2 2C.CO 电催化时,在阳极转化为燃料
2
D.CO 与环氧丙烷可合成可降解塑料
2
考向3 硅及其化合物的性质与应用
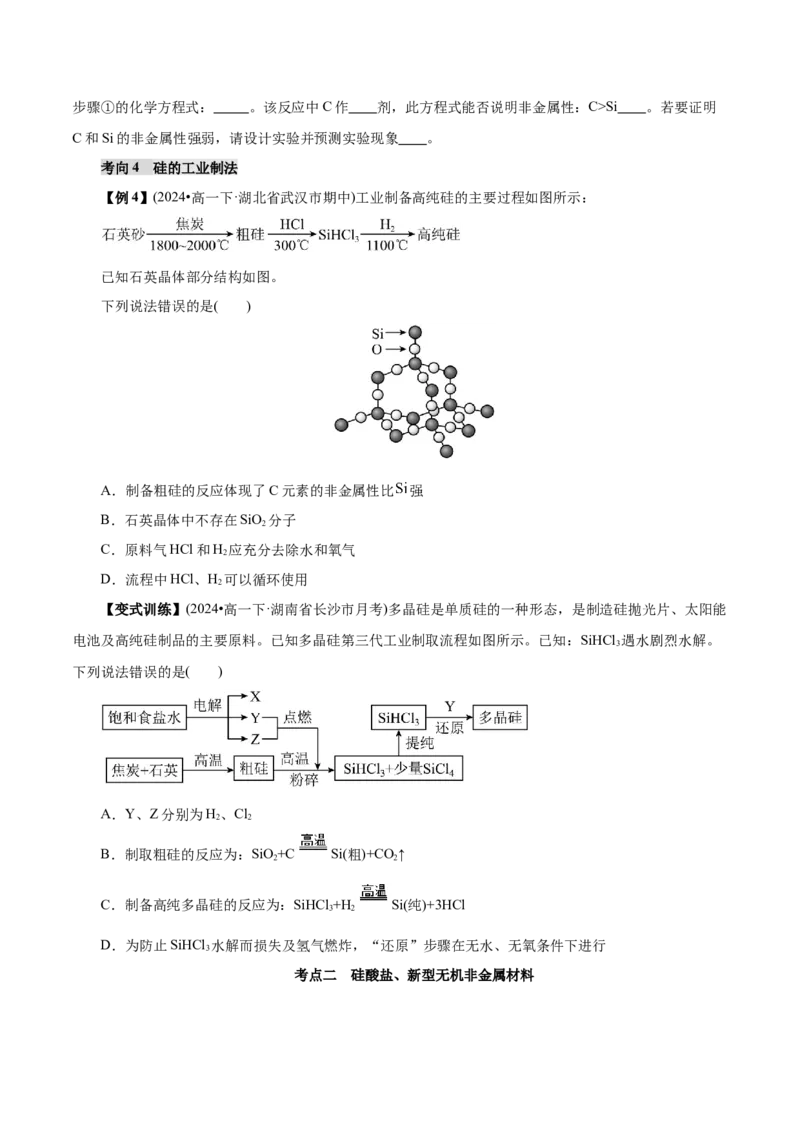
【例3】(2024•河南省许昌市检测)二氧化硅又称硅石,是制备硅及其化合物的重要原料,部分转化过
程如图所示。
回答下面问题:
(1)碳元素和硅元素都位于周期表的 族,非金属性较强的是 (填元素符号)。工业上制备
粗硅的反应:SiO+2C Si+2CO↑,该反应能否比较碳和硅元素的非金属性强弱 (填“是”或
2
“否”)。
(2)NaOH溶液需要盛放在有橡胶塞的试剂瓶中,原因 (用化学方程式表示,下同),利用HF溶
液可以在玻璃表面上写字作画,原因是 。制玻璃的原材料是石英(SiO)、纯碱(Na CO)和大理石
2 2 3
(CaCO),写出制玻璃时发生反应的化学方程式 、 。SiC是一种新型无机非金属材料,半导
3
体领域未来代替硅基芯片的一种新型原材料,SiC属于 (填“离子”戒“共价”)化合物。
【变式训练】(2024•·陕西省安康市高新中学质检)硅是无机非金属材料的主角,硅的氧化物和硅酸盐约
占地壳质量的90%以上。
(1)可用于制作计算机芯片和太阳能电池的是 (填化学式,下同),光导纤维的主要成分是
。
(2)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为 。
(3)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反
应的离子方程式: 。
(4)高纯度单晶硅可以按下列方法制备:SiO Si(粗) SiiHCl Si(纯)。写出
2 3步骤①的化学方程式: 。该反应中C作 剂,此方程式能否说明非金属性:C>Si 。若要证明
C和Si的非金属性强弱,请设计实验并预测实验现象 。
考向4 硅的工业制法
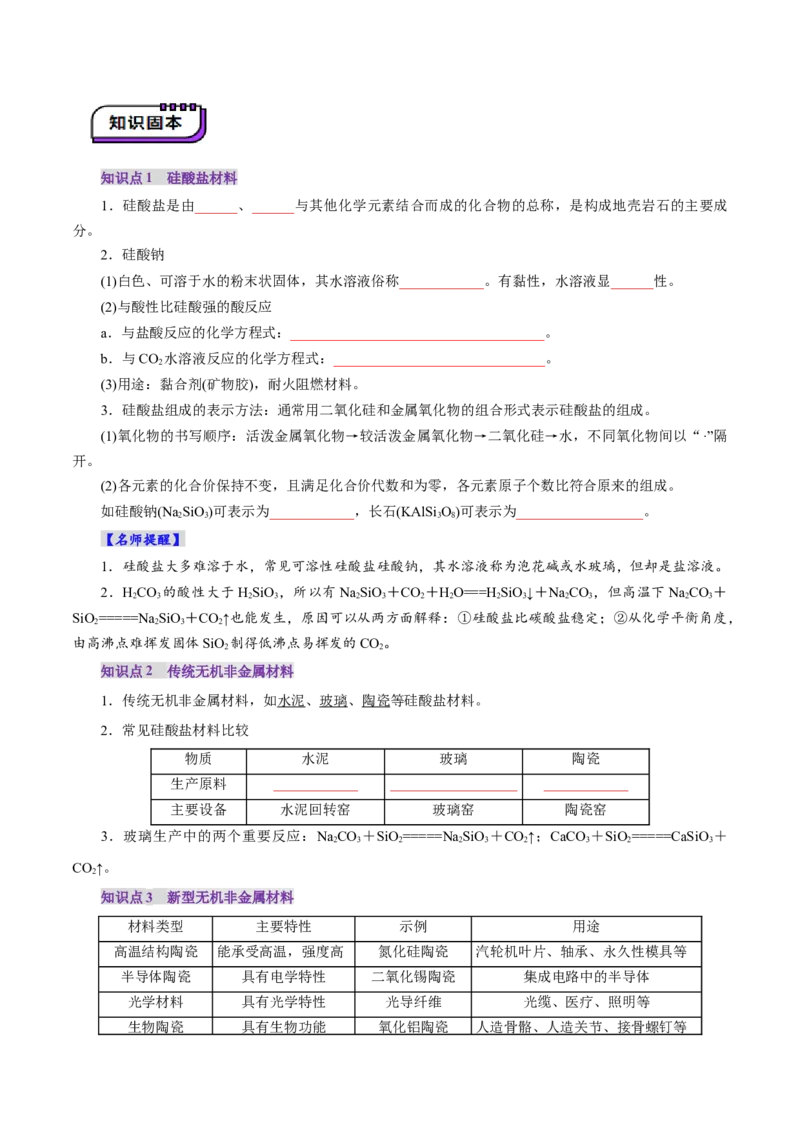
【例4】(2024•高一下·湖北省武汉市期中)工业制备高纯硅的主要过程如图所示:
已知石英晶体部分结构如图。
下列说法错误的是( )
A.制备粗硅的反应体现了C元素的非金属性比 强
B.石英晶体中不存在SiO 分子
2
C.原料气HCl和H 应充分去除水和氧气
2
D.流程中HCl、H 可以循环使用
2
【变式训练】(2024•高一下·湖南省长沙市月考)多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能
电池及高纯硅制品的主要原料。已知多晶硅第三代工业制取流程如图所示。已知:SiHCl 遇水剧烈水解。
3
下列说法错误的是( )
A.Y、Z分别为H、Cl
2 2
B.制取粗硅的反应为:SiO+C Si(粗)+CO ↑
2 2
C.制备高纯多晶硅的反应为:SiHCl +H Si(纯)+3HCl
3 2
D.为防止SiHCl 水解而损失及氢气燃炸,“还原”步骤在无水、无氧条件下进行
3
考点二 硅酸盐、新型无机非金属材料知识点1 硅酸盐材料
1.硅酸盐是由______、______与其他化学元素结合而成的化合物的总称,是构成地壳岩石的主要成
分。
2.硅酸钠
(1)白色、可溶于水的粉末状固体,其水溶液俗称____________。有黏性,水溶液显______性。
(2)与酸性比硅酸强的酸反应
a.与盐酸反应的化学方程式:____________________________________。
b.与CO 水溶液反应的化学方程式:______________________________。
2
(3)用途:黏合剂(矿物胶),耐火阻燃材料。
3.硅酸盐组成的表示方法:通常用二氧化硅和金属氧化物的组合形式表示硅酸盐的组成。
(1)氧化物的书写顺序:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水,不同氧化物间以“·”隔
开。
(2)各元素的化合价保持不变,且满足化合价代数和为零,各元素原子个数比符合原来的组成。
如硅酸钠(Na SiO)可表示为____________,长石(KAlSi O)可表示为__________________。
2 3 3 8
【名师提醒】
1.硅酸盐大多难溶于水,常见可溶性硅酸盐硅酸钠,其水溶液称为泡花碱或水玻璃,但却是盐溶液。
2.HCO 的酸性大于HSiO ,所以有NaSiO +CO +HO===H SiO↓+NaCO ,但高温下NaCO +
2 3 2 3 2 3 2 2 2 3 2 3 2 3
SiO=====NaSiO +CO↑也能发生,原因可以从两方面解释:①硅酸盐比碳酸盐稳定;②从化学平衡角度,
2 2 3 2
由高沸点难挥发固体SiO 制得低沸点易挥发的CO。
2 2
知识点2 传统无机非金属材料
1.传统无机非金属材料,如水泥、玻璃、陶瓷等硅酸盐材料。
2.常见硅酸盐材料比较
物质 水泥 玻璃 陶瓷
生产原料 ____________ __________________ ____________
主要设备 水泥回转窑 玻璃窑 陶瓷窑
3.玻璃生产中的两个重要反应:NaCO +SiO=====NaSiO +CO↑;CaCO +SiO=====CaSiO +
2 3 2 2 3 2 3 2 3
CO↑。
2
知识点3 新型无机非金属材料
材料类型 主要特性 示例 用途
高温结构陶瓷 能承受高温,强度高 氮化硅陶瓷 汽轮机叶片、轴承、永久性模具等
半导体陶瓷 具有电学特性 二氧化锡陶瓷 集成电路中的半导体
光学材料 具有光学特性 光导纤维 光缆、医疗、照明等
生物陶瓷 具有生物功能 氧化铝陶瓷 人造骨骼、人造关节、接骨螺钉等【易错提醒】
水泥、玻璃与陶瓷是三大传统无机非金属材料;碳化硅、氮化硅等是新型无机非金属材料。
考向1 硅酸盐
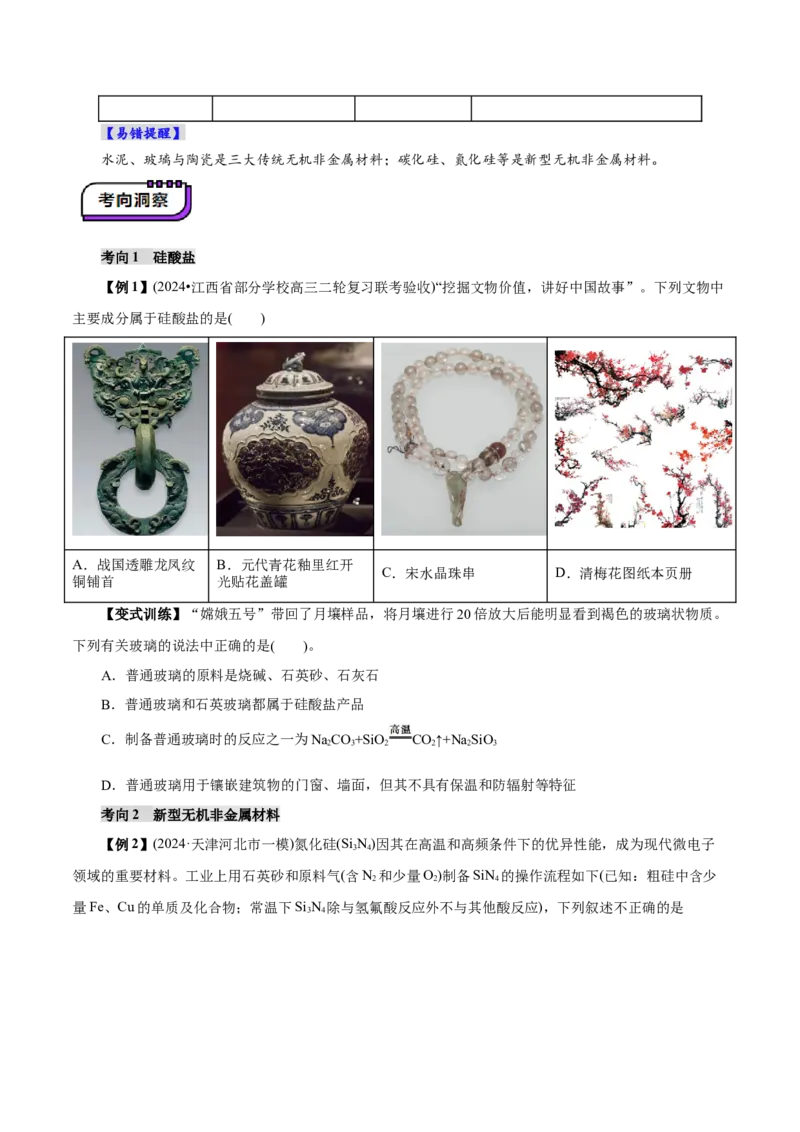
【例1】(2024•江西省部分学校高三二轮复习联考验收)“挖掘文物价值,讲好中国故事”。下列文物中
主要成分属于硅酸盐的是( )
A.战国透雕龙凤纹 B.元代青花釉里红开
C.宋水晶珠串 D.清梅花图纸本页册
铜铺首 光贴花盖罐
【变式训练】“嫦娥五号”带回了月壤样品,将月壤进行20倍放大后能明显看到褐色的玻璃状物质。
下列有关玻璃的说法中正确的是( )。
A.普通玻璃的原料是烧碱、石英砂、石灰石
B.普通玻璃和石英玻璃都属于硅酸盐产品
C.制备普通玻璃时的反应之一为NaCO+SiO CO↑+Na SiO
2 3 2 2 2 3
D.普通玻璃用于镶嵌建筑物的门窗、墙面,但其不具有保温和防辐射等特征
考向2 新型无机非金属材料
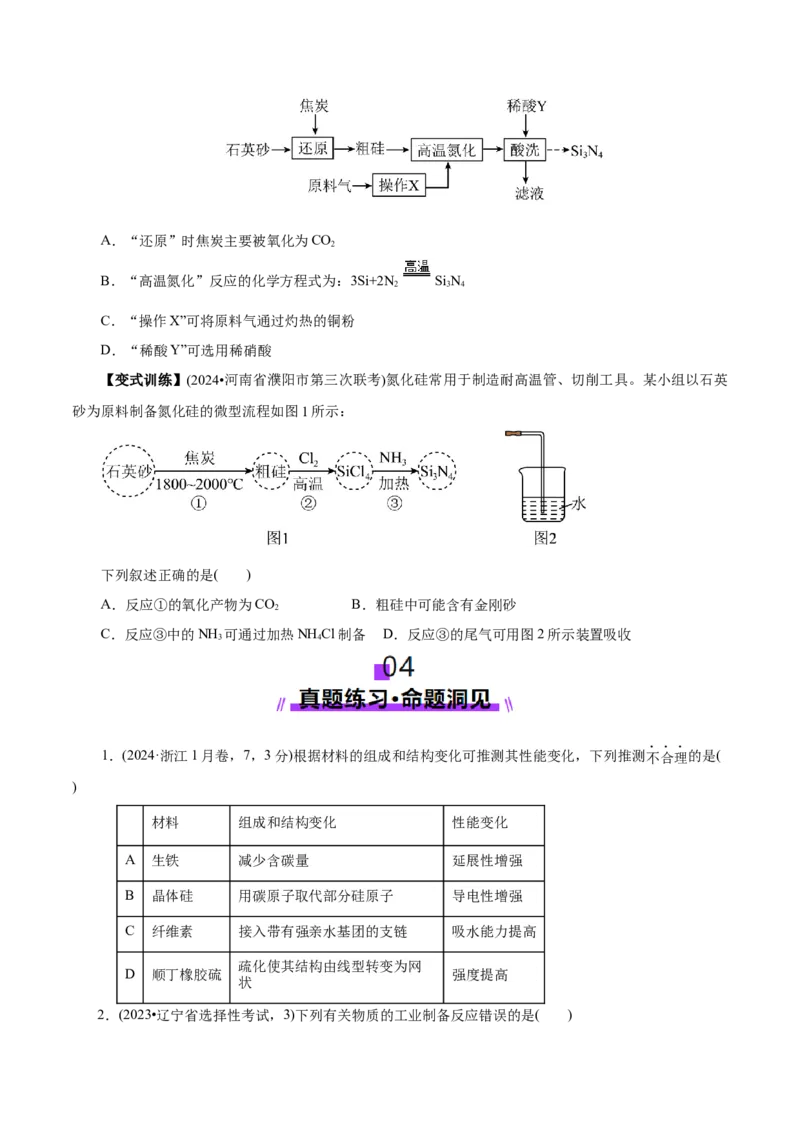
【例2】(2024·天津河北市一模)氮化硅(Si N)因其在高温和高频条件下的优异性能,成为现代微电子
3 4
领域的重要材料。工业上用石英砂和原料气(含N 和少量O)制备SiN 的操作流程如下(已知:粗硅中含少
2 2 4
量Fe、Cu的单质及化合物;常温下Si N 除与氢氟酸反应外不与其他酸反应),下列叙述不正确的是
3 4A.“还原”时焦炭主要被氧化为CO
2
B.“高温氮化”反应的化学方程式为:3Si+2N Si N
2 3 4
C.“操作X”可将原料气通过灼热的铜粉
D.“稀酸Y”可选用稀硝酸
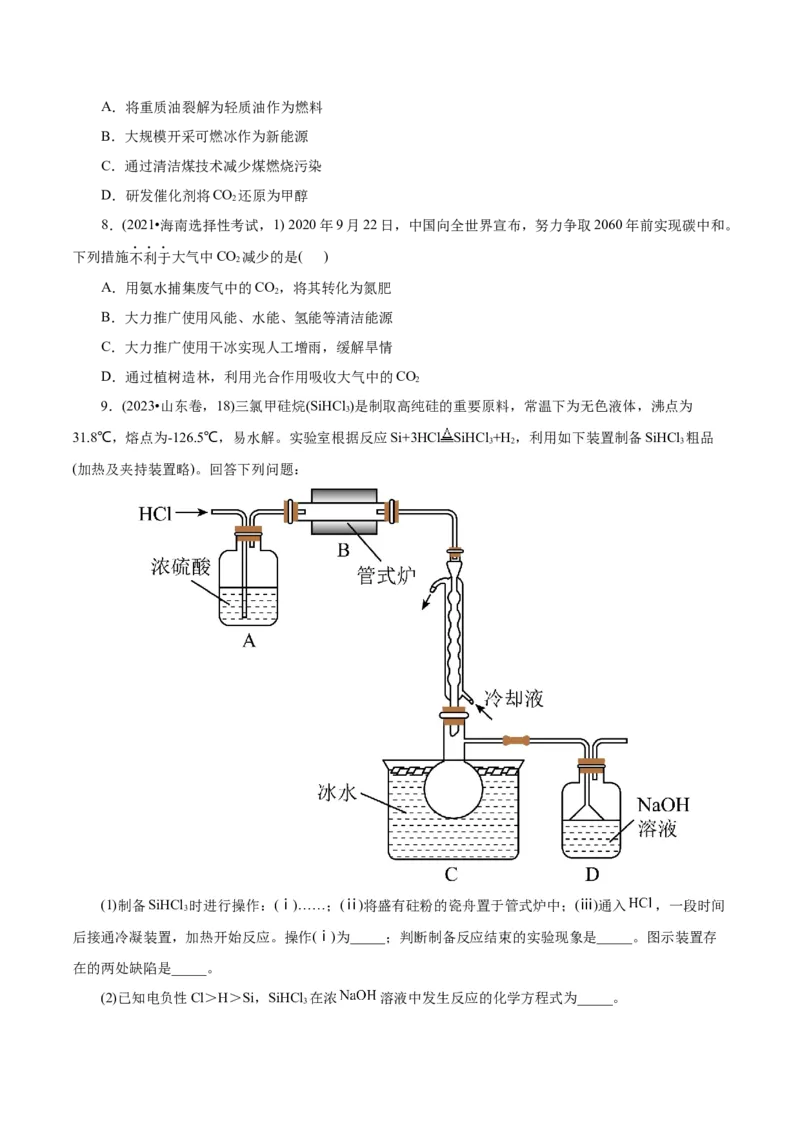
【变式训练】(2024•河南省濮阳市第三次联考)氮化硅常用于制造耐高温管、切削工具。某小组以石英
砂为原料制备氮化硅的微型流程如图1所示:
下列叙述正确的是( )
A.反应①的氧化产物为CO B.粗硅中可能含有金刚砂
2
C.反应③中的NH 可通过加热NH Cl制备 D.反应③的尾气可用图2所示装置吸收
3 4
1.(2024·浙江1月卷,7,3分)根据材料的组成和结构变化可推测其性能变化,下列推测不合理的是(
)
材料 组成和结构变化 性能变化
A 生铁 减少含碳量 延展性增强
B 晶体硅 用碳原子取代部分硅原子 导电性增强
C 纤维素 接入带有强亲水基团的支链 吸水能力提高
疏化使其结构由线型转变为网
D 顺丁橡胶硫 强度提高
状
2.(2023•辽宁省选择性考试,3)下列有关物质的工业制备反应错误的是( )A.合成氨:N+3H 2NH B.制HCl:H+Cl 2HCl
2 2 3 2 2
C.制粗硅:SiO+2C Si+2CO D.冶炼镁:2MgO(熔融) 2Mg+O↑
2 2
3.(2022•江苏卷,6)周期表中ⅣA族元素及其化合物应用广泛,甲烷具有较大的燃烧热(890.3 kJ·mol-
l),是常见燃料;Si、Ge是重要的半导体材料,硅晶体表面SiO 能与氢氟酸(HF,弱酸)反应生成HSiF
2 2 6
(H SiF 在水中完全电离为H+和SiF2-);1885年德国化学家将硫化锗(GeS )与H 共热制得了门捷列夫预言的
2 6 6 2 2
类硅—锗;下列化学反应表示正确的是( )
A.SiO 与HF溶液反应:SiO+6HF=2H++SiF 2-+2H O
2 2 6 2
B.高温下H 还原GeS :GeS +2H =Ge+2H S
2 2 2 2 2
C.铅蓄电池放电时的正极反应:Pb+SO2--2e-=PbSO
4 4
D.甲烷的燃烧:CH(g)+2O(g)==CO (g)+2HO(g) ΔH =890.3kJ·mol−1
4 2 2 2 2
4.(2022•河北省选择性考试,1)定窑是宋代五大名窑之一,其生产的白瓷闻名于世。下列说法正确的
是( )
A.传统陶瓷是典型的绝缘材料 B.陶瓷主要成分为SiO 和MgO
2
C.陶瓷烧制的过程为物理变化 D.白瓷的白色是因铁含量较高
5.(2022•河北省选择性考试,1)定窑是宋代五大名窑之一,其生产的白瓷闻名于世。下列说法正确的
是( )
A.传统陶瓷是典型的绝缘材料 B.陶瓷主要成分为SiO 和MgO
2
C.陶瓷烧制的过程为物理变化 D.白瓷的白色是因铁含量较高
6.(2022•广东选择性考试,3)广东一直是我国对外交流的重要窗口,馆藏文物是其历史见证。下列文
物主要由硅酸盐制成的是( )
文物
A.南宋鎏金饰
选项 B.蒜头纹银盒 C.广彩瓷咖啡杯 D.铜镀金钟座
品
7.(2021•全国乙卷,1)我国提出争取在2030年前实现碳达峰,2060年实现碳中和,这对于改善环境,
实现绿色发展至关重要。碳中和是指CO 的排放总量和减少总量相当。下列措施中能促进碳中和最直接有
2
效的是( )A.将重质油裂解为轻质油作为燃料
B.大规模开采可燃冰作为新能源
C.通过清洁煤技术减少煤燃烧污染
D.研发催化剂将CO 还原为甲醇
2
8.(2021•海南选择性考试,1) 2020年9月22日,中国向全世界宣布,努力争取2060年前实现碳中和。
下列措施不利于大气中CO 减少的是( )
2
A.用氨水捕集废气中的CO,将其转化为氮肥
2
B.大力推广使用风能、水能、氢能等清洁能源
C.大力推广使用干冰实现人工增雨,缓解旱情
D.通过植树造林,利用光合作用吸收大气中的CO
2
9.(2023•山东卷,18)三氯甲硅烷(SiHCl )是制取高纯硅的重要原料,常温下为无色液体,沸点为
3
31.8℃,熔点为-126.5℃,易水解。实验室根据反应Si+3HCl SiHCl +H ,利用如下装置制备SiHCl 粗品
3 2 3
(加热及夹持装置略)。回答下列问题:
(1)制备SiHCl 时进行操作:(ⅰ)……;(ⅱ)将盛有砫粉的瓷舟置于管式炉中;(ⅲ)通入 ,一段时间
3
后接通冷凝装置,加热开始反应。操作(ⅰ)为_____;判断制备反应结束的实验现象是_____。图示装置存
在的两处缺陷是_____。
(2)已知电负性Cl>H>Si,SiHCl 在浓 溶液中发生反应的化学方程式为_____。
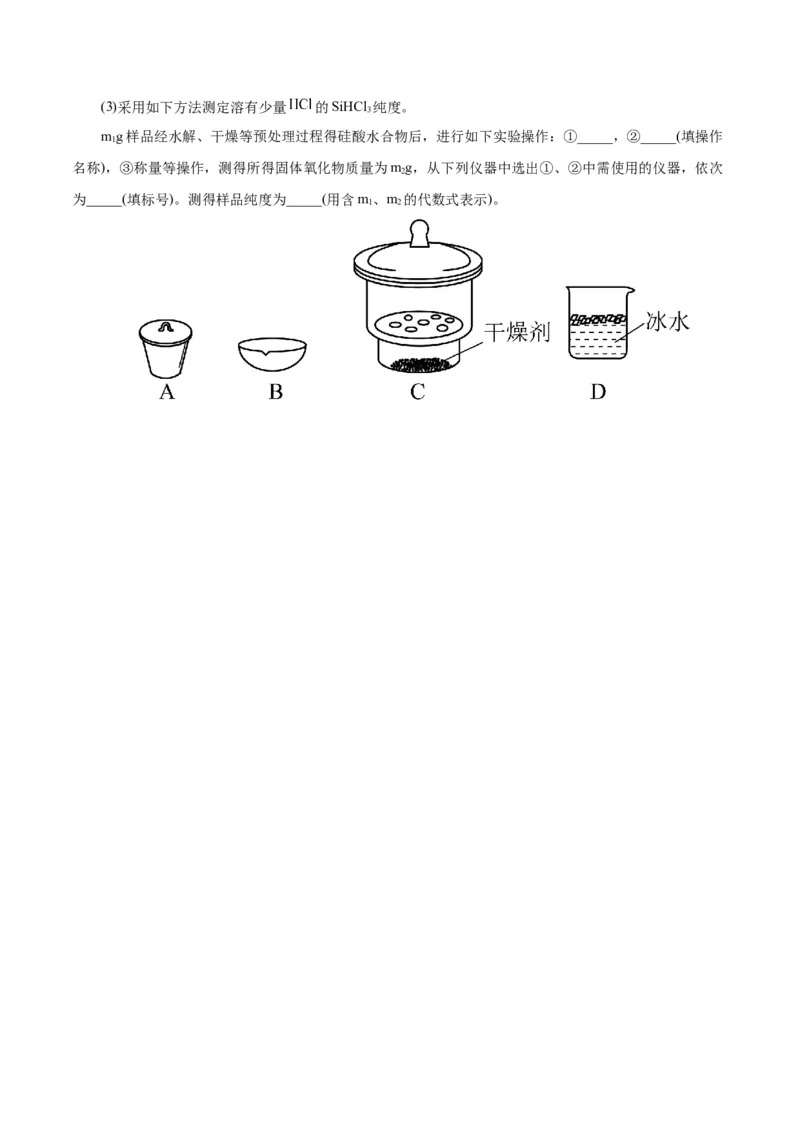
3(3)采用如下方法测定溶有少量 的SiHCl 纯度。
3
mg样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①_____,②_____(填操作
1
名称),③称量等操作,测得所得固体氧化物质量为mg,从下列仪器中选出①、②中需使用的仪器,依次
2
为_____(填标号)。测得样品纯度为_____(用含m、m 的代数式表示)。
1 2