文档内容
第 05 讲 工业流程解题策略
目录
01 模拟基础练
【题型一】以制备物质简单流程为背景
【题型二】以资源开发利用为背景
【题型三】以物质分离提纯为背景
【题型四】制备物质综合工艺流程
【题型五】化学原理运用工艺流程
02 重难创新练
03 真题实战练
题型一 以制备物质简单流程为背景
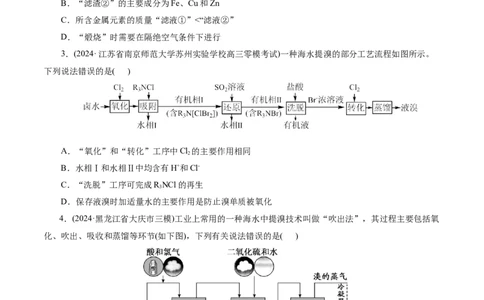
1.(2024·北京市朝阳区高三质量检测)实验小组同学制备KClO 并探究其性质,过程如下:
3
下列说法不正确的是( )
A.可用饱和NaOH溶液净化氯气
B.生成KClO 的离子方程式为3Cl+6OH- ClO -+5Cl-+3H O
3 2 3 2
C.推测若取无色溶液a于试管中,滴加稀HSO 后再加入少量CCl ,下层液体变紫色
2 4 4
D.上述实验说明碱性条件下氧化性:Cl>KClO ,酸性条件下氧化性:Cl”或“<”)
2 sp
K (Ag S)。
sp 2
②在HSO 溶液中,银锰精矿中的FeS 和氧化锰矿中的 发生反应,则浸锰液中主要的金属阳离
2 4 2
子有 。
(2) “浸银”时,使用过量FeCl、HCl和CaCl 的混合液作为浸出剂,将Ag S中的银以[AgCl]-形式浸出。
3 2 2 2
①将“浸银”反应的离子方程式补充完整: 。
Fe3++Ag S+ +2[AgCl]- +S
2 2
②结合平衡移动原理,解释浸出剂中Cl-、+的作用: 。
(3) “沉银”过程中需要过量的铁粉作为还原剂。
①该步反应的离子方程式有 。
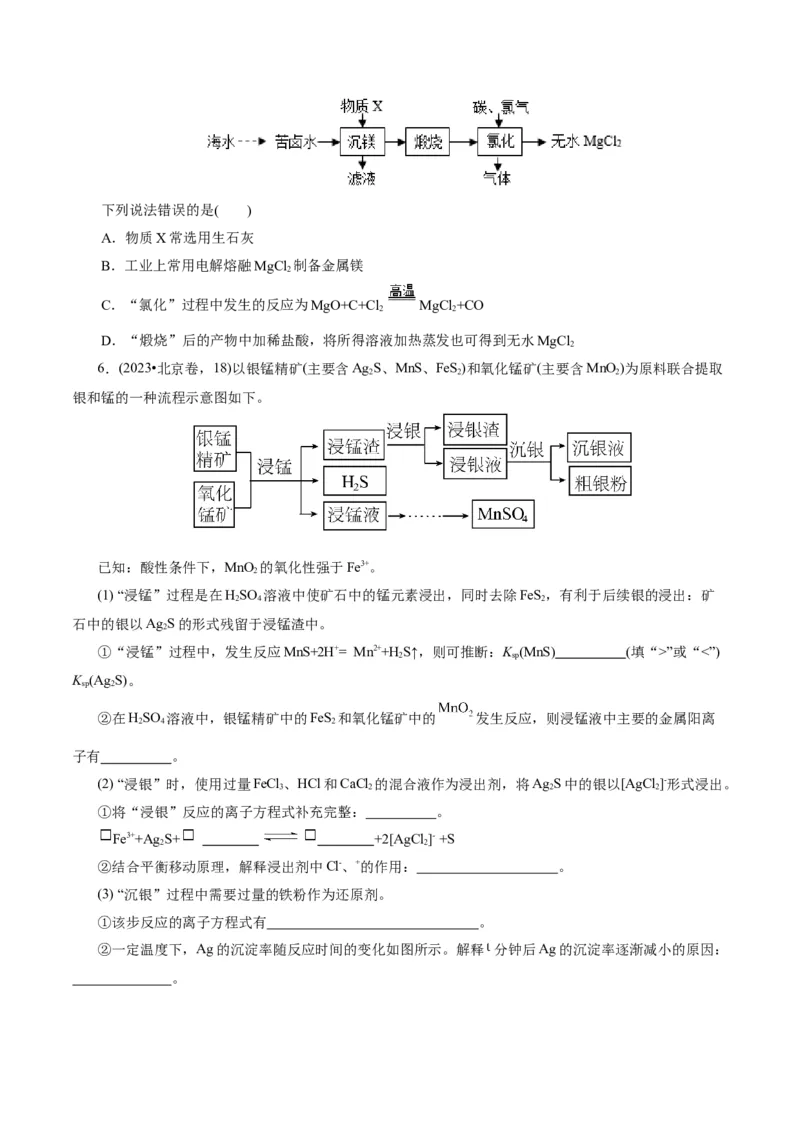
②一定温度下,Ag的沉淀率随反应时间的变化如图所示。解释 分钟后Ag的沉淀率逐渐减小的原因:
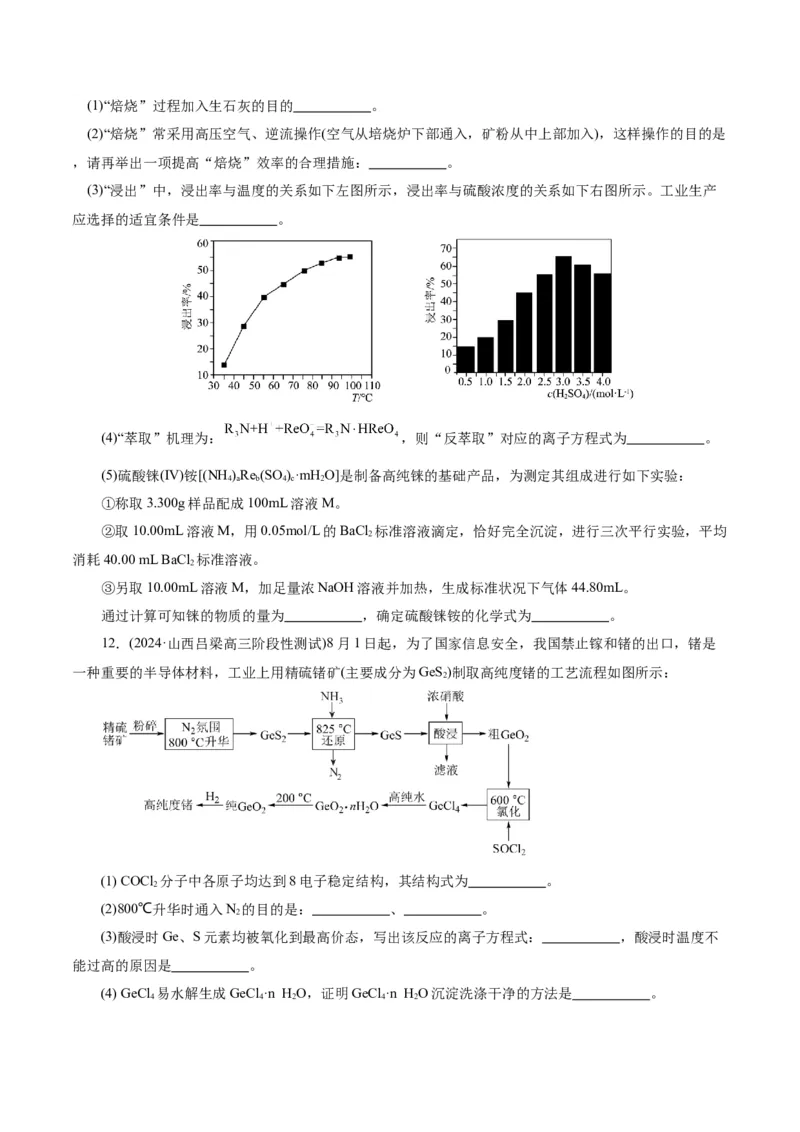
。(4)结合“浸锰”过程,从两种矿石中各物质利用的角度,分析联合提取银和锰的优势: 。
7.(2023•山东卷,17)盐湖卤水(主要含Na+、Mg2+、Li+、Cl-、SO 2-和硼酸根等)是锂盐的重要来源。一
4
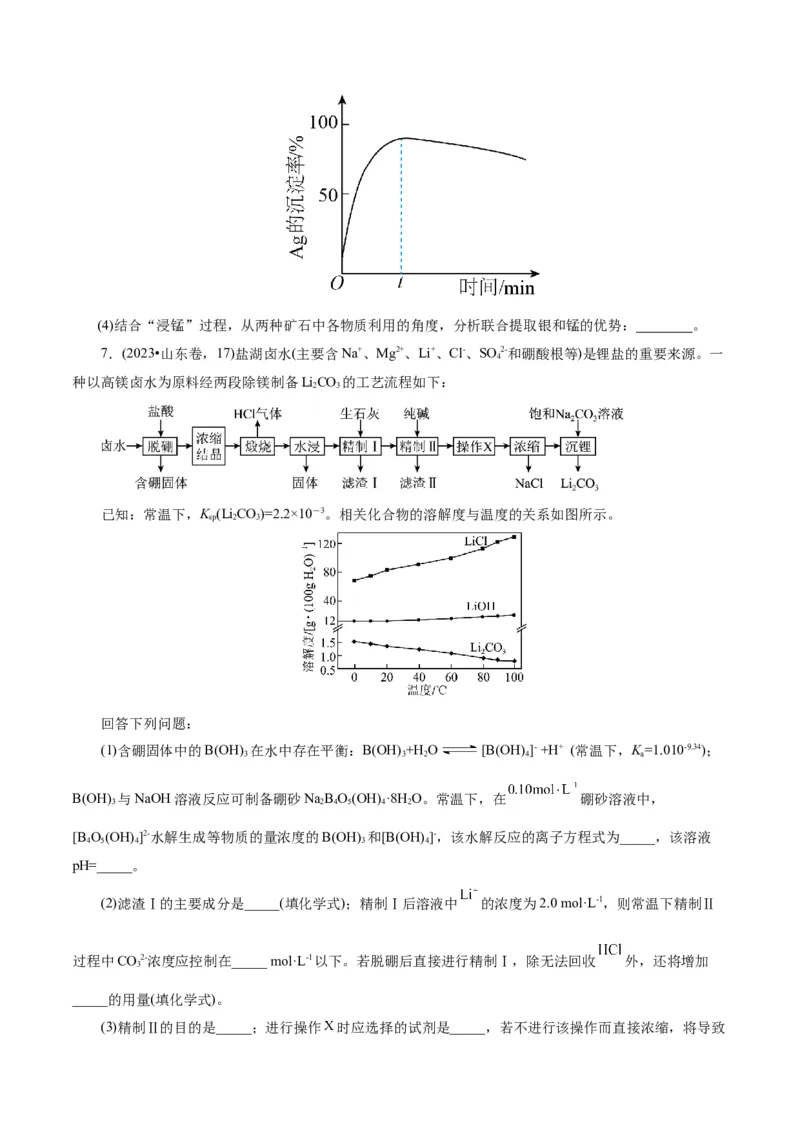
种以高镁卤水为原料经两段除镁制备LiCO 的工艺流程如下:
2 3
已知:常温下,K (LiCO)=2.2×10-3。相关化合物的溶解度与温度的关系如图所示。
sp 2 3
回答下列问题:
(1)含硼固体中的B(OH) 在水中存在平衡:B(OH) +H O [B(OH) ]- +H+ (常温下,K=1.010-9.34);
3 3 2 4 a
B(OH) 与NaOH溶液反应可制备硼砂NaB O(OH) ·8H O。常温下,在 硼砂溶液中,
3 2 4 5 4 2
[B O(OH) ]2-水解生成等物质的量浓度的B(OH) 和[B(OH) ]-,该水解反应的离子方程式为_____,该溶液
4 5 4 3 4
pH=_____。
(2)滤渣Ⅰ的主要成分是_____(填化学式);精制Ⅰ后溶液中 的浓度为2.0 mol·L-1,则常温下精制Ⅱ
过程中CO2-浓度应控制在_____ mol·L-1以下。若脱硼后直接进行精制Ⅰ,除无法回收 外,还将增加
3
_____的用量(填化学式)。
(3)精制Ⅱ的目的是_____;进行操作 时应选择的试剂是_____,若不进行该操作而直接浓缩,将导致_____。
8.(2023•湖南卷,17)超纯Ga(CH ) 是制备第三代半导体的支撑源材料之一,近年来,我国科技工作
3 3
者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯Ga(CH ) 方面取得了显著成果,工
3 3
业上以粗镓为原料,制备超纯Ga(CH ) 的工艺流程如下:
3 3
已知:①金属Ga的化学性质和 相似,Ga的熔点为29.8℃;
②EtO (乙醚)和NR (三正辛胺)在上述流程中可作为配体;
2 3
③相关物质的沸点:
物质 Ga(CH ) EtO CHI NR
3 3 2 3 3
沸点/℃ 55.7 34.6 42.4 365.8
回答下列问题:
(1)晶体Ga(CH ) 的晶体类型是_______;
3 3
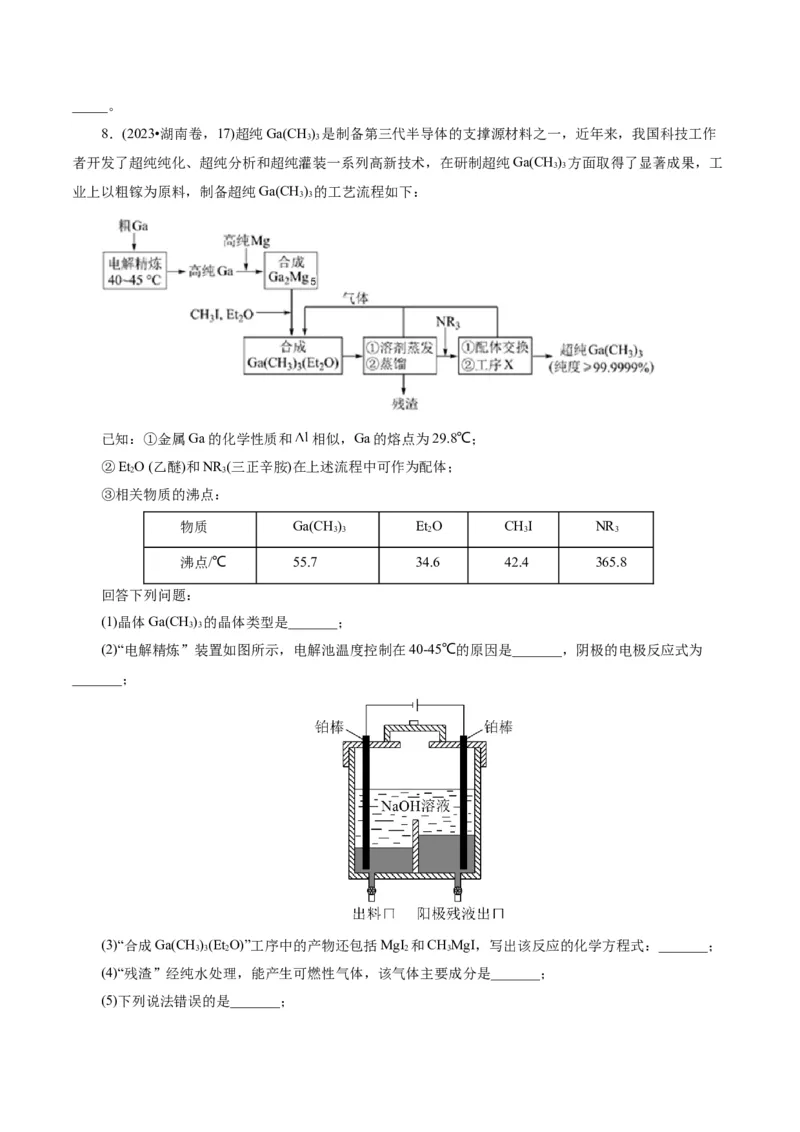
(2)“电解精炼”装置如图所示,电解池温度控制在40-45℃的原因是_______,阴极的电极反应式为
_______;
(3)“合成Ga(CH )(Et O)”工序中的产物还包括MgI 和CHMgI,写出该反应的化学方程式:_______;
3 3 2 2 3
(4)“残渣”经纯水处理,能产生可燃性气体,该气体主要成分是_______;
(5)下列说法错误的是_______;A.流程中EtO得到了循环利用
2
B.流程中,“合成GaMg”至“工序X”需在无水无氧的条件下进行
2 5
C.“工序X”的作用是解配Ga(CH )(NR ),并蒸出Ga(CH )
3 3 3 3 3
D.用核磁共振氢谱不能区分Ga(CH ) 和CHI
3 3 3
(6)直接分解Ga(CH )(Et O)不能制备超纯Ga(CH ),而本流程采用“配体交换”工艺制备超纯
3 3 2 3 3
Ga(CH ) 的理由是_______;
3 3
(7)比较分子中的C-Ga-C键角大小:Ga(CH )_______ Ga(CH )(Et O) (填“>”“<”或“=”),其原因是
3 3 3 3 2
_______。
9.(2023•全国乙卷,27)LiMn O 作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO ,含
2 4 3
有少量Si、Fe、Ni、Al等元素)制备LiMn O 的流程如下:
2 4
已知:K [Fe(OH) ]=2.8×10-39,K [Al(OH) ]=1.3×10-33,K [Ni(OH) ]=5.5×10-16。
sp 3 sp 3 sp 2
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为_______。为提高溶矿速率,可采取的措施_______(举1例)。
(2)加入少量MnO 的作用是_______。不宜使用HO 替代MnO ,原因是_______。
2 2 2 2
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=_______mol·L-1;用石灰乳调节至pH≈7,除去
的金属离子是_______。
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有_______。
(5)在电解槽中,发生电解反应的离子方程式为_______。随着电解反应进行,为保持电解液成分稳定,
应不断_______。电解废液可在反应器中循环利用。
(6)缎烧窑中,生成LiMn O 反应的化学方程式是_______。
2 4
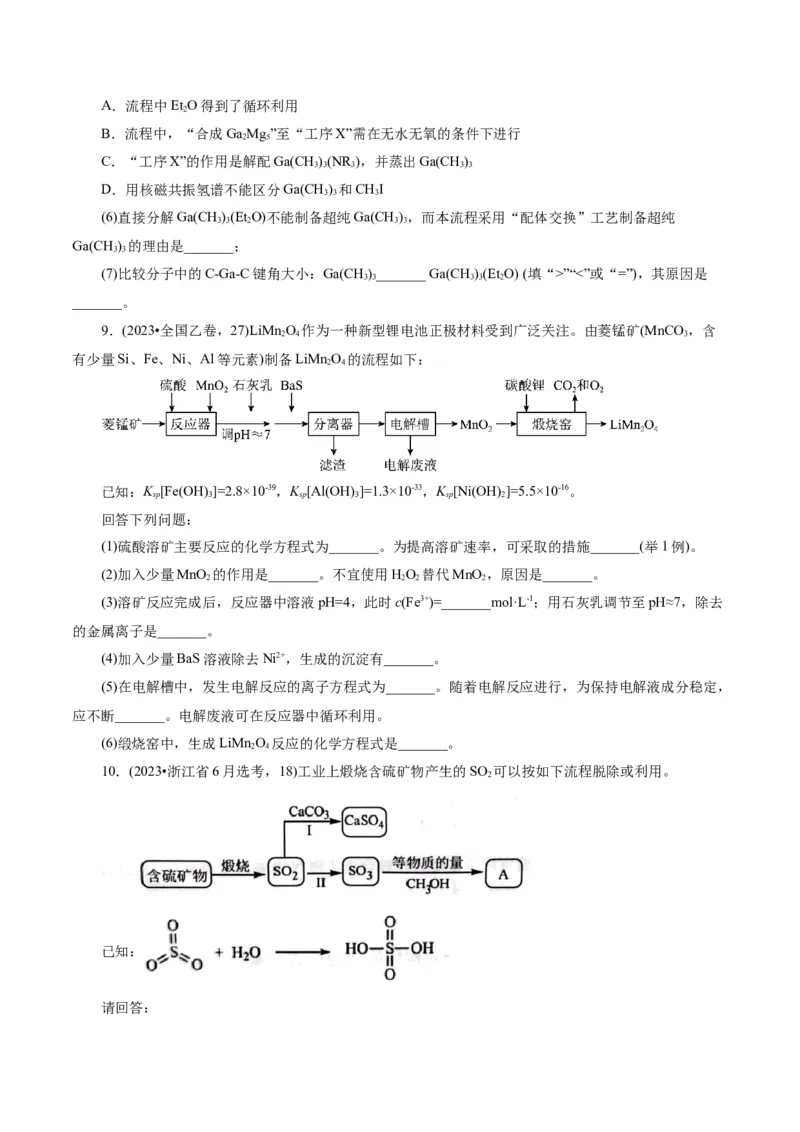
10.(2023•浙江省6月选考,18)工业上煅烧含硫矿物产生的SO 可以按如下流程脱除或利用。
2
已知:
请回答:(1)富氧煅烧燃煤产生的低浓度的SO 可以在炉内添加CaCO 通过途径Ⅰ脱除,写出反应方程式
2 3
___________。
(2)煅烧含硫量高的矿物得到高浓度的SO ,通过途径Ⅱ最终转化为化合物A。
2
①下列说法正确的是___________。
A.燃煤中的有机硫主要呈正价 B.化合物A具有酸性
C.化合物A是一种无机酸酯 D.工业上途径Ⅱ产生的SO 也可用浓HSO 吸收
3 2 4
②一定压强下,化合物A的沸点低于硫酸的原因是___________。
(3)设计实验验证化合物A中含有S元素_____;写出实验过程中涉及的反应方程式____。
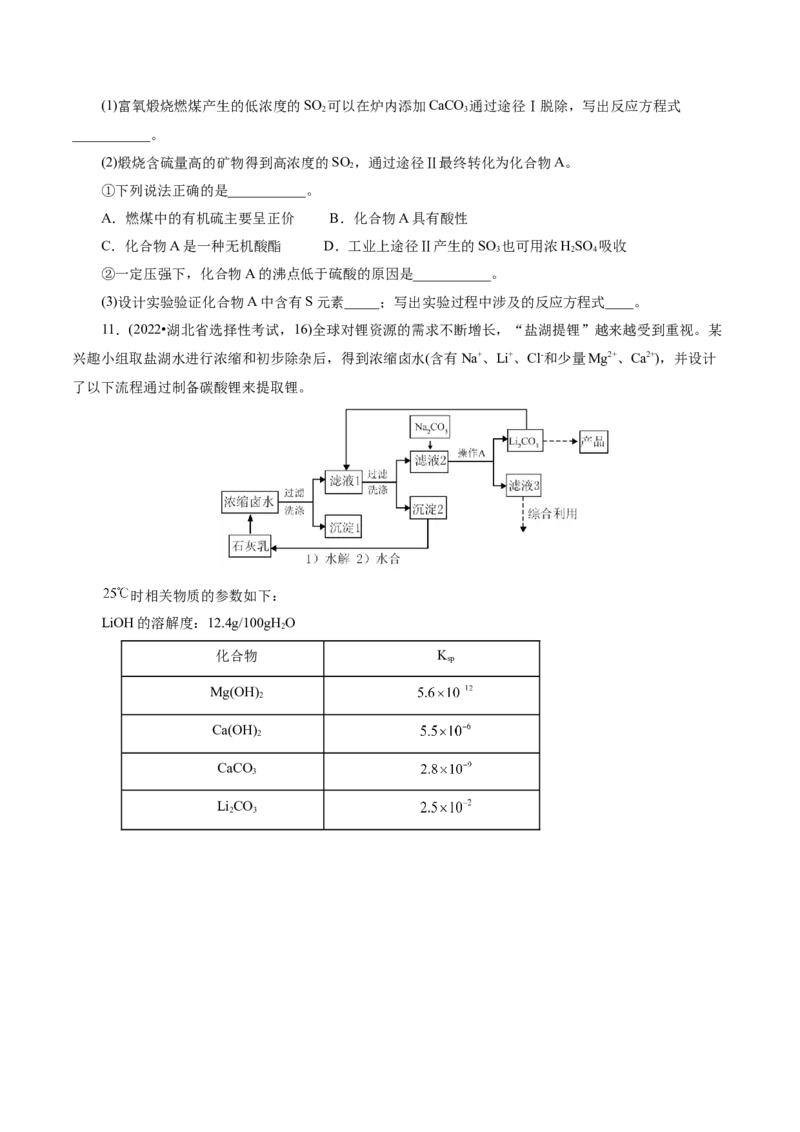
11.(2022•湖北省选择性考试,16)全球对锂资源的需求不断增长,“盐湖提锂”越来越受到重视。某
兴趣小组取盐湖水进行浓缩和初步除杂后,得到浓缩卤水(含有Na+、Li+、Cl-和少量Mg2+、Ca2+),并设计
了以下流程通过制备碳酸锂来提取锂。
时相关物质的参数如下:
LiOH的溶解度:12.4g/100gH O
2
化合物 K
sp
Mg(OH)
2
Ca(OH)
2
CaCO
3
LiCO
2 3回答下列问题:
(1)“沉淀1”为___________。
(2)向“滤液1”中加入适量固体LiCO 的目的是___________。
2 3
(3)为提高LiCO 的析出量和纯度,“操作A”依次为___________、___________、洗涤。
2 3
(4)有同学建议用“侯氏制碱法”的原理制备LiCO。查阅资料后,发现文献对常温下的LiCO 有不同
2 3 2 3
的描述:①是白色固体;②尚未从溶液中分离出来。为探究LiHCO 的性质,将饱和 溶液与饱和
3
NaHCO 溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述
3
现象说明,在该实验条件下LiHCO ___________(填“稳定”或“不稳定”),有关反应的离子方程式为
3
___________。
(5)他们结合(4)的探究结果,拟将原流程中向“滤液2”加入NaCO 改为通入CO。这一改动能否达到
2 3 2
相同的效果,作出你的判断并给出理由___________。
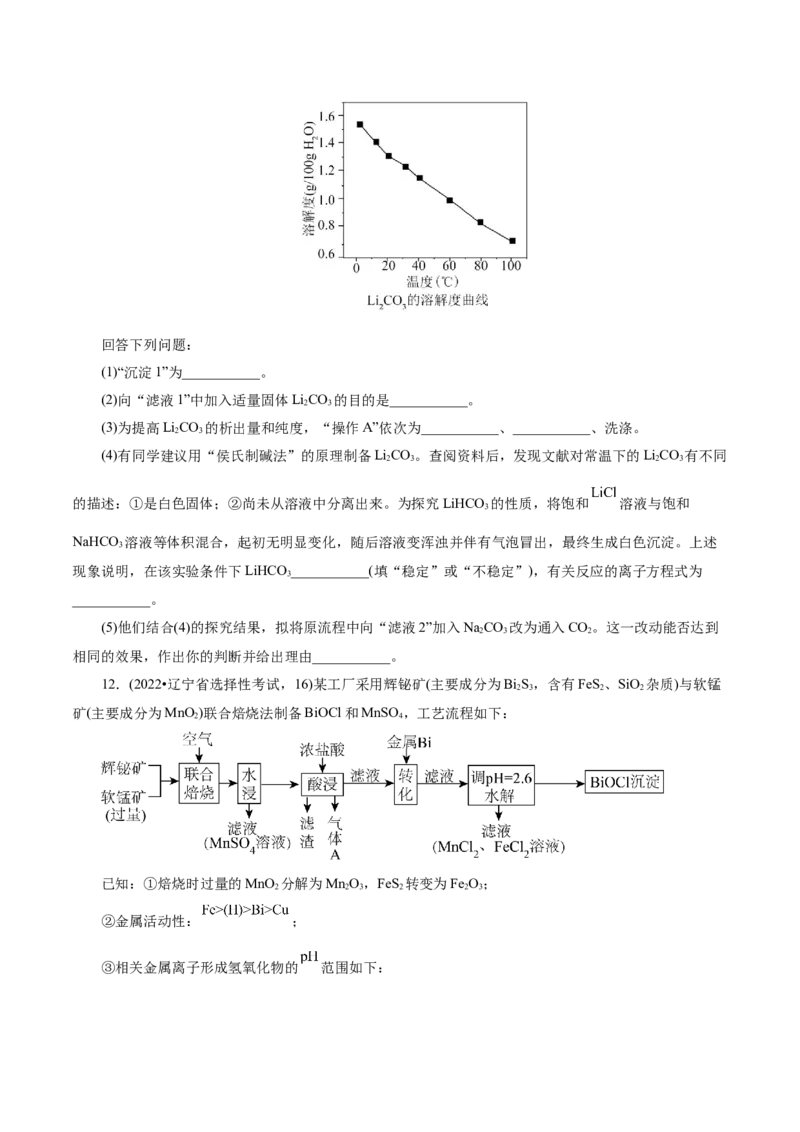
12.(2022•辽宁省选择性考试,16)某工厂采用辉铋矿(主要成分为BiS,含有FeS、SiO 杂质)与软锰
2 3 2 2
矿(主要成分为MnO )联合焙烧法制备BiOCl和MnSO ,工艺流程如下:
2 4
已知:①焙烧时过量的MnO 分解为MnO,FeS 转变为Fe O;
2 2 3 2 2 3
②金属活动性: ;
③相关金属离子形成氢氧化物的 范围如下:开始沉淀pH 完全沉淀pH
Fe2+ 6.5 8.3
Fe3+ 1.6 2.8
Mn2+ 8.1 10.1
回答下列问题:
(1)为提高焙烧效率,可采取的措施为___________。
a.进一步粉碎矿石
b.鼓入适当过量的空气
c.降低焙烧温度
(2) Bi S 在空气中单独焙烧生成BiO,反应的化学方程式为___________。
2 3 2 3
(3)“酸浸”中过量浓盐酸的作用为:①充分浸出Bi3+和Mn2+;②___________。
(4)滤渣的主要成分为___________(填化学式)。
(5)生成气体A的离子方程式为___________。
(6)加入金属 的目的是___________。
13.(2022•江苏卷,15)实验室以二氧化铈(CeO)废渣为原料制备Cl-含量少的Ce (CO),其部分实验过
2 2 3 3
程如下:
(1)“酸浸”时CeO 与HO 反应生成Ce3+并放出O,该反应的离子方程式为_______。
2 2 2 2
(2)pH约为7的CeCl 溶液与NH HCO 溶液反应可生成Ce (CO) 沉淀,该沉淀中 含量与加料方式有
3 4 3 2 3 3
关。得到含Cl-量较少的Ce (CO) 的加料方式为_______(填序号)。
2 3 3
A.将NH HCO 溶液滴加到CeCl 溶液中
4 3 3
B.将CeCl 溶液滴加到NH HCO 溶液中
3 4 3
(3)通过中和、萃取、反萃取、沉淀等过程,可制备 含量少的Ce (CO)。已知Ce3+能被有机萃取剂
2 3 3
(简称HA)萃取,其萃取原理可表示为
Ce3+ (水层)+3HA(有机层) Ce(A) (有机层)+3H+(水层)
3
①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是_______。
②反萃取的目的是将有机层Ce3+转移到水层。使Ce3+尽可能多地发生上述转移,应选择的实验条件或
采取的实验操作有_______(填两项)。③与“反萃取”得到的水溶液比较,过滤Ce (CO) 溶液的滤液中,物质的量减小的离子有_______(填
2 3 3
化学式)。
(4)实验中需要测定溶液中Ce3+的含量。已知水溶液中 可用准确浓度的(NH )Fe(SO ) 溶液滴定。
4 2 4 2
以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为 。
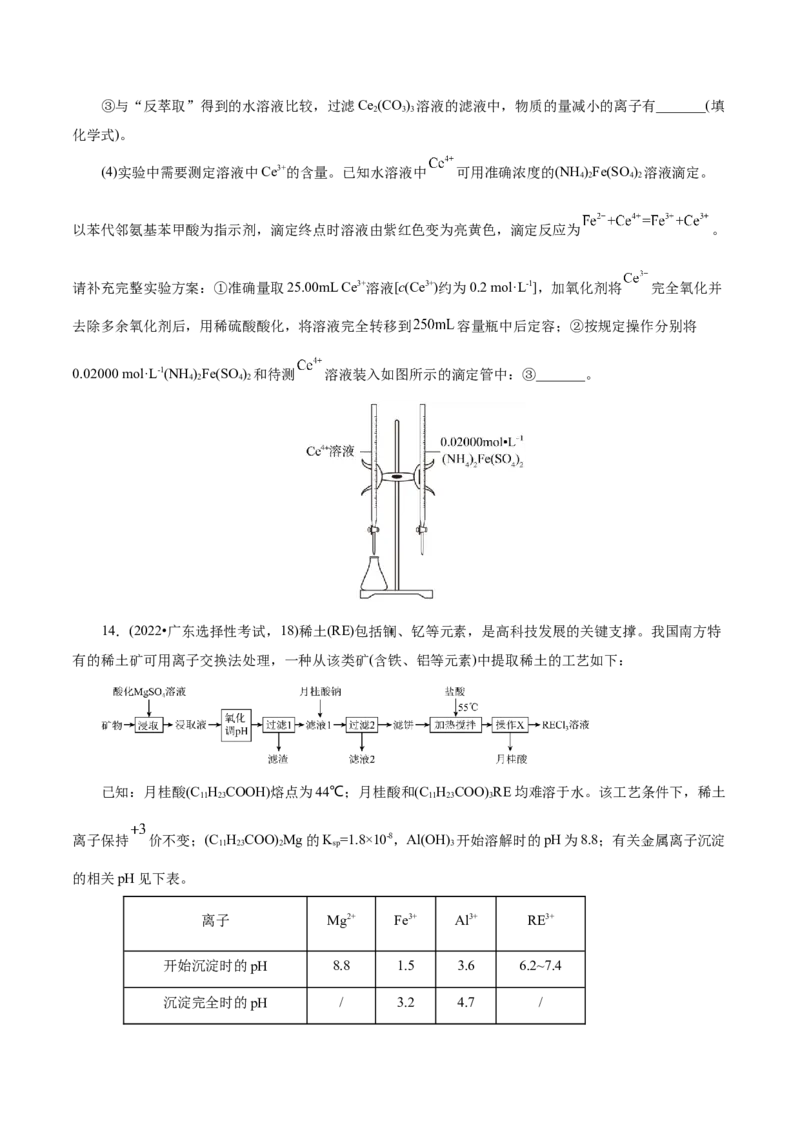
请补充完整实验方案:①准确量取25.00mL Ce3+溶液[c(Ce3+)约为0.2 mol·L-1],加氧化剂将 完全氧化并
去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到 容量瓶中后定容;②按规定操作分别将
0.02000 mol·L-1(NH )Fe(SO ) 和待测 溶液装入如图所示的滴定管中:③_______。
4 2 4 2
14.(2022•广东选择性考试,18)稀土(RE)包括镧、钇等元素,是高科技发展的关键支撑。我国南方特
有的稀土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
已知:月桂酸(C H COOH)熔点为44℃;月桂酸和(C H COO) RE均难溶于水。该工艺条件下,稀土
11 23 11 23 3
离子保持 价不变;(C H COO) Mg的K =1.8×10-8,Al(OH) 开始溶解时的pH为8.8;有关金属离子沉淀
11 23 2 sp 3
的相关pH见下表。
离子 Mg2+ Fe3+ Al3+ RE3+
开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4
沉淀完全时的pH / 3.2 4.7 /(1)“氧化调pH”中,化合价有变化的金属离子是_______。
(2)“过滤1”前,用NaOH溶液调pH至_______的范围内,该过程中 发生反应的离子方程式为
_______。
(3)“过滤2”后,滤饼中检测不到 元素,滤液2中Mg2+浓度为2.7g·Lˉ1。为尽可能多地提取RE3+,可
提高月桂酸钠的加入量,但应确保“过滤2”前的溶液中c(C H COO―)低于_______ mol·L-1 (保留两位有效
11 23
数字)。
(4)①“加热搅拌”有利于加快RE3+溶出、提高产率,其原因是_______。
②“操作X”的过程为:先_______,再固液分离。
(5)该工艺中,可再生循环利用的物质有_______(写化学式)。
(6)稀土元素钇(Y)可用于制备高活性的合金类催化剂Pt Y。
3
①还原YCl 和PtCl 熔融盐制备Pt Y时,生成1molPt Y转移_______ mol电子。
3 4 3 3
②Pt Y/C用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化O 的还原,发生的电极反应为
3 2
_______。
15.(2022•河北省选择性考试,15)以焙烧黄铁矿FeS(杂质为石英等)产生的红渣为原料制备铵铁蓝
2
Fe(NH )Fe(CN) 颜料。工艺流程如下:
4 6
回答下列问题:
(1)红渣的主要成分为_______(填化学式),滤渣①的主要成分为_______(填化学式)。
(2)黄铁矿研细的目的是_______。
(3)还原工序中,不生成S单质的反应的化学方程式为_______。
(4)工序①的名称为_______,所得母液循环使用。
(5)沉铁工序产生的白色沉淀Fe(NH )Fe(CN) 中 的化合价为_______,氧化工序发生反应的离子方程
4 2 6
式为_______。
(6)若用还原工序得到的滤液制备Fe O·x H O和(NH )SO ,所加试剂为_______和_______(填化学式,
2 3 2 4 2 4
不引入杂质)。