文档内容
第二章 化学物质及其变化
第06讲 氧化还原反应(精练)
完卷时间:50分钟
可能用到的相对原子质量:N 14 O 16 Mg 24 Mn 55 Cu 64 Zn 65
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2021·浙江高考真题)关于反应8NH+6NO=7N+12HO,下列说法正确的是
3 2 2 2
A.NH 中H元素被氧化
3
B.NO 在反应过程中失去电子
2
C.还原剂与氧化剂的物质的量之比为3:4
D.氧化产物与还原产物的质量之比为4:3
2.(2021·江苏常州市·高三二模)燃煤和工业生产中产生的 过量排放会形成酸雨。 是重要的
化工原料,可作漂白剂。在接触法制硫酸的工业中, 发生的反应为:
。下列关于 的说法正确的是
A. 分子呈直线形,是非极性分子
B. 的水溶液能导电, 是电解质
C. 和 反应,每生成1mol S,转移的电子数为2mol
D.用石灰石浆液吸收烟气中的 ,可减少酸雨的形成,最终转化为石膏
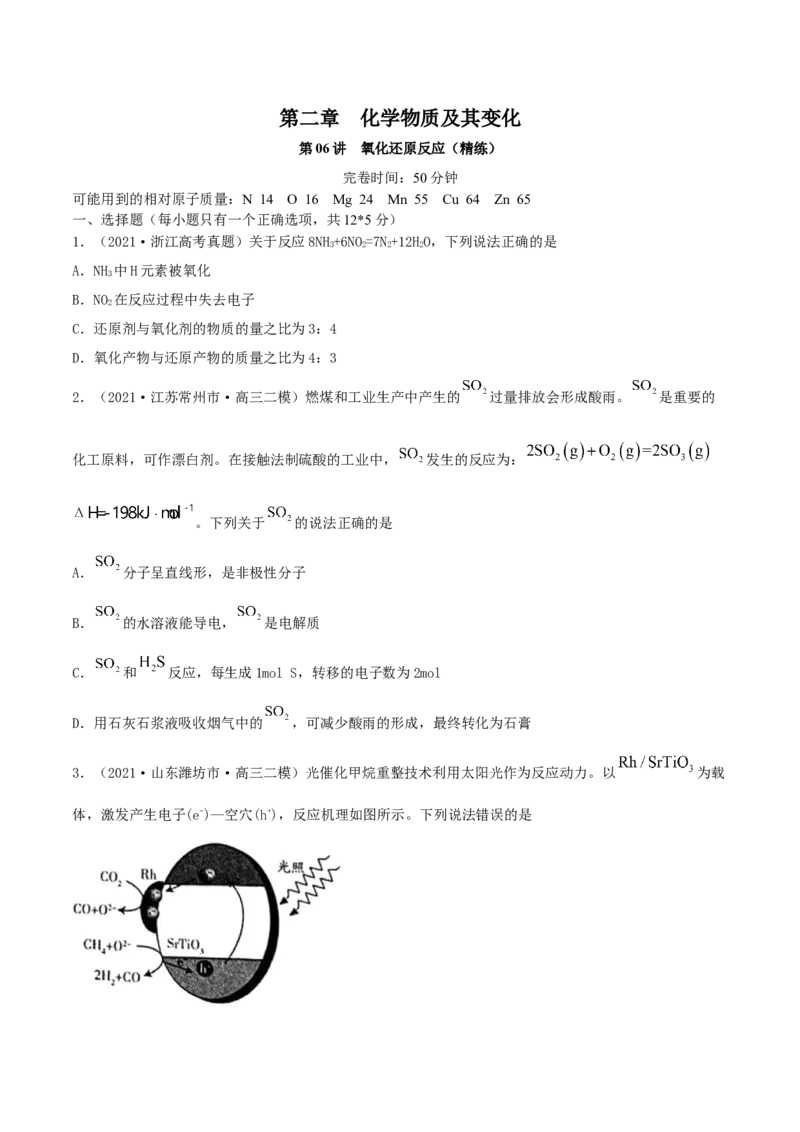
3.(2021·山东潍坊市·高三二模)光催化甲烷重整技术利用太阳光作为反应动力。以 为载
体,激发产生电子(e-)—空穴(h+),反应机理如图所示。下列说法错误的是A.该催化重整过程中,C原子的成键数目不变
B. 在 上发生还原反应
C.在 表面,每生成 ,向空穴转移电子数为
D.该反应可表示为
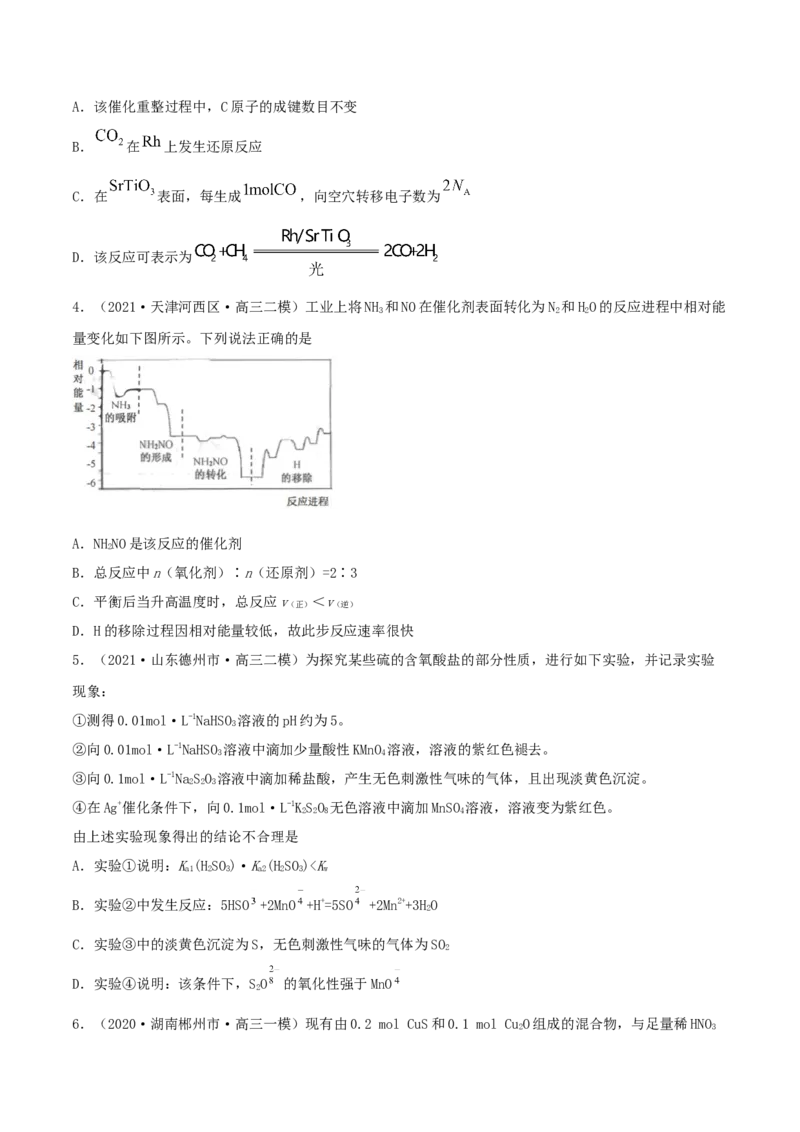
4.(2021·天津河西区·高三二模)工业上将NH 和NO在催化剂表面转化为N 和HO的反应进程中相对能
3 2 2
量变化如下图所示。下列说法正确的是
A.NHNO是该反应的催化剂
2
B.总反应中n(氧化剂)∶n(还原剂)=2∶3
C.平衡后当升高温度时,总反应v <v
(正) (逆)
D.H的移除过程因相对能量较低,故此步反应速率很快
5.(2021·山东德州市·高三二模)为探究某些硫的含氧酸盐的部分性质,进行如下实验,并记录实验
现象:
①测得0.01mol·L-1NaHSO 溶液的pH约为5。
3
②向0.01mol·L-1NaHSO 溶液中滴加少量酸性KMnO 溶液,溶液的紫红色褪去。
3 4
③向0.1mol·L-1NaSO 溶液中滴加稀盐酸,产生无色刺激性气味的气体,且出现淡黄色沉淀。
2 2 3
④在Ag+催化条件下,向0.1mol·L-1KSO 无色溶液中滴加MnSO 溶液,溶液变为紫红色。
2 2 8 4
由上述实验现象得出的结论不合理是
A.实验①说明:K(HSO)·K(HSO)HIO
3 3
d.氯化钠、碘化钠与浓硫酸共热,分别生成氯化氢、单质碘
(5)检验亚硫酸钠固体是否氧化变质的方法是___________。
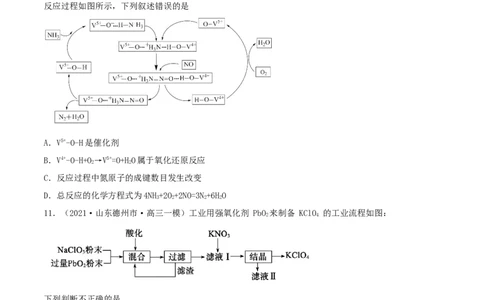
14.(2021·陕西安康市·高三一模)(14分)SO 在生产、生活中具有重要的作用,据所学知识回答相
2
关问题。
(1) SO 通入NaCO 溶液中有CO 生成,说明HSO 具有___________(填“酸性”、“氧化性”、“还原性”
2 2 3 2 2 3
或“漂白性”,下同),SO 通入品红溶液中,品红溶液褪色,说明SO 具有___________。
2 2
(2)已知SO 通入FeCl 溶液会发生反应,还原产物为___________(填化学式,下同),氧化产物为
2 3
___________。
(3)向含锌粉的悬浊液中通入SO 可制备ZnSO
2 2 4。
①该反应的化学方程式为___________,若反应中有0.1mol电子转移,则生成ZnSO___________g。
2 4
②向反应后的溶液中加入过量盐酸,溶液出现黄色浑浊,且有刺激性气体产生,反应的化学方程式为
___________。(4)已知室温下,ZnSO 微溶于水,Zn(HSO) 易溶于水。ZnO水悬浊液常用于吸收烟气中的SO。向ZnO水悬
3 3 2 2
浊液中缓慢匀速通入SO,在开始吸收的40min内,SO 吸收率、溶液pH的变化如图。0~20min内,溶液pH
2 2
几乎不变的原因是___________,SO 吸收率在30min后迅速降低,其原因是___________。
2
15.(2021·北京丰台区·高三一模)(12分)锰广泛存在于自然界中,工业可用软锰矿(主要成分是
MnO)制备锰。
2
资料:①MnCO 难溶于水,可溶于稀酸。
3
②在Mn2+催化下,SO 在水溶液中被氧化成HSO。
2 2 4
I.制备
(1)写出铝热法还原MnO 制备锰的化学方程式_______。
2
(2)工业上制备锰时,会产生大量废水和锰渣。锰渣煅烧会产生含高浓度SO 的烟气,可用以下方法处理。
2
处理方法一:
①用软锰矿进行脱硫可生成硫酸锰,从而达到资源的循环使用。写出一定条件下利用MnO 进行脱硫的化学
2
方程式_______。
②研究表明,用Fe2+/Fe3+可强化脱硫效果,其过程如下所示:
过程I:……
过程II :2Fe3++SO+2HO=2Fe2++ +4H+
2 2
过程I的离子方程式是_______。
处理方法二:
③用MnCO 进行脱硫,可提高脱硫率。结合化学用语解释原因:_______。
3
II.废水中锰含量的测定(3)取1 mL废水置于20 mL磷酸介质中,加入HClO ,将溶液中的Mn2+氧化为Mn3+,用c mol/L (NH)
4 4 2
Fe(SO) 溶液进行滴定,达到滴定终点时,滴定管刻度由VmL变为V mL,废水中锰的含量为____ g/mL。
4 2 0 1