文档内容
第 06 讲 离子共存、离子的检验与推断
(模拟精练+真题演练)
1.(2023·广东汕头·统考一模)离子鉴别能让我们感受微观世界的神奇。下列在透明溶液中能大量共存的
离子组是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
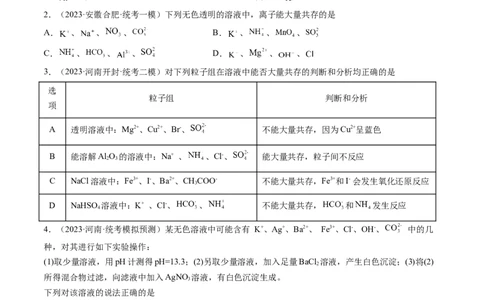
2.(2023·安徽合肥·统考一模)下列无色透明的溶液中,离子能大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
3.(2023·河南开封·统考二模)对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
选
粒子组 判断和分析
项
A 透明溶液中:Mg2+、Cu2+、Br-、 不能大量共存,因为Cu2+呈蓝色
B 能溶解Al O 的溶液中:Na+ 、 、Cl-、 能大量共存,粒子间不反应
2 3
C NaCl溶液中:Fe3+、I-、Ba2+、CHCOO- 不能大量共存,Fe3+和I- 会发生氧化还原反应
3
D NaHSO 溶液中:K+ 、Cl-、 、 不能大量共存, 和 发生反应
4
4.(2023·河南·统考模拟预测)某无色溶液中可能含有 K+、Ag+、Ba2+、 Fe3+、Cl-、OH-、 中的几
种,对其进行如下实验操作:
(1)取少量溶液,用pH计测得pH=13.3;(2)另取少量溶液,加入足量BaCl 溶液,产生白色沉淀;(3)将(2)
2
所得混合物过滤,向滤液中加入AgNO 溶液,有白色沉淀生成。
3
下列对该溶液的说法正确的是
A.要确定是否含有K+,需做焰色反应实验
B.一定含有K+、OH-、
C.含有Ag+、Ba2+、Fe3+三种离子中的一种
D.原溶液中一定含有Cl-
5.(2023·河北·模拟预测)某无色透明溶液,可能含有下列离子: 、 、 、 、 、 、
,现做实验如下:
①取少量原溶液滴加石蕊试液呈红色;②取少量原溶液,加入过量的NaOH溶液,有白色沉淀生成;③取
少量原溶液,加入过量氯化钡溶液,有白色沉淀生成,静置分层;取静置后的上层清液,加入硝酸银溶液,有不溶于稀硝酸的白色沉淀生成。
下列说法错误的是
A.溶液中一定存在的离子是 、 、
B.溶液中一定不存在的离子是 、 、
C.②中生成白色沉淀的离子方程式为
D.根据③现象可知原溶液中一定含有
6.(2023·重庆九龙坡·统考二模)加入下列物质后,不会影响溶液中 、 、 、 、 大量
共存的是
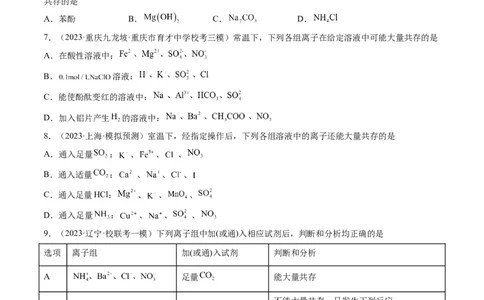
A.苯酚 B. C. D.
7.(2023·重庆九龙坡·重庆市育才中学校考三模)常温下,下列各组离子在给定溶液中可能大量共存的是
A.在酸性溶液中:
B. 溶液:
C.能使酚酞变红的溶液中:
D.加入铝片产生 的溶液中:
8.(2023·上海·模拟预测)室温下,经指定操作后,下列各组溶液中的离子还能大量共存的是
A.通入足量 : 、 、 、
B.通入适量 : 、 、 、
C.通入足量HCl: 、 、 、
D.通入足量 : 、 、 、
9.(2023·辽宁·校联考一模)下列离子组中加(或通)入相应试剂后,判断和分析均正确的是
选项 离子组 加(或通)入试剂 判断和分析
A 足量 能大量共存
不能大量共存,只发生下列反应
B 足量 溶液
不能大量共存,因 和 之间会发生
C 足量 溶液
完全双水解生成 气体和 沉淀
不能大量共存,只发生下列氧化还原反应
D 少量
10.(2022·上海静安·统考二模)某强酸性溶液中可能存在Al3+、Fe2+、NH 、Ba2+、Cl-、CO 、SO 、NO 中的若干种。为确定溶液的组成进行了如下实验:
ⅰ. 取100mL原溶液,加入足量Ba(NO ) 溶液,有白色沉淀a和无色气体b生成,过滤得滤液c。
3 2
ⅱ. 往滤液c中加入足量的NaOH溶液并加热,可得气体d和沉淀e,过滤得滤液f。
ⅲ. 取滤液f,通入少量的CO,有白色沉淀g生成。
2
下列有关判断正确的是
A.试液中一定没有Ba2+、CO 、NO 、Cl-
B.试液中一定有Fe2+、NH 、SO
C.气体b和气体d在一定条件下能反应生成盐
D.沉淀g一定含有Al(OH) ,可能含有BaCO
3 3
11.(2023·湖南邵阳·统考三模)常温下,下列各组离子在指定溶液中一定能大量共存的是
A.0.1mol•L-1AlCl 溶液中:H+、Na+、K+、SO
3
B.0.1mol•L-1FeCl 溶液中:H+、Al3+、SO 、NO
2
C.能使紫色石蕊试液变蓝的溶液中:Ag+、Fe3+、Br-、SO
D.由水电离产生的c(H+)=10-12mol•L-1的溶液中:NH 、SO 、HCO 、Cl-
12.(2022·山东威海·校考模拟预测)某溶液可能含有Cl-、SO 、CO 、NH 、Fe3+、Al3+和K+。取该溶
液100mL,加入过量NaOH溶液,加热,得到0.02mol气体(已知:NH +OH-=NH↑+H O),同时产生2.14g
3 2
红褐色沉淀;向上述滤液中加足量BaCl 溶液,得到4.66g不溶于盐酸的白色沉淀。由此可知原溶液中
2
A.至少存在4种离子
B.Cl-一定存在,且c(Cl-)≥0.4mol/L
C.SO 、NH 、Fe3+一定存在,Cl-可能不存在
D.CO 、Al3+一定不存在,K+可能存在
13.(2022·浙江·模拟预测)结晶水合物X由4种元素组成。某兴趣小组按如下流程进行实验:
请回答:
(1)组成X的元素除H、O外还有 ___________,X的化学式为 ___________。(2)溶液D中属于盐的成分是 ___________ ( 用化学式表示);若溶液C中滴入少量氨水,则首先参与反应
的微粒是_____
(3)请写出E →F化学方程式___________。
(4)设计实验方案确定溶液H中的阴离子___________。
14.(2022·广东惠州·一模)为检验溶液中是否含有Cl-,某同学采用向溶液中先加HNO,再加AgNO,
3 3
若有白色沉淀生成,则证明有Cl-。对此结论,有人提出了质疑,溶液中可能有SO ,设计了如下探究性
实验。
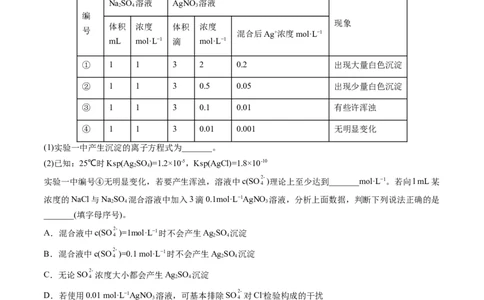
实验一:向NaSO 溶液中滴加AgNO 溶液
2 4 3
NaSO 溶液 AgNO 溶液
2 4 3
编
现象
体积 浓度 体积 浓度
号
混合后Ag+浓度mol·L−1
mL mol·L−1 滴 mol·L−1
① 1 1 3 2 0.2 出现大量白色沉淀
② 1 1 3 0.5 0.05 出现少量白色沉淀
③ 1 1 3 0.1 0.01 有些许浑浊
④ 1 1 3 0.01 0.001 无明显变化
(1)实验一中产生沉淀的离子方程式为_______。
(2)已知:25℃时Ksp(Ag SO )=1.2×10-5,Ksp(AgCl)=1.8×10-10
2 4
实验一中编号④无明显变化,若要产生浑浊,溶液中c(SO )理论上至少达到_______mol·L−1。若向l mL某
浓度的NaCl与NaSO 混合溶液中加入3滴0.1mol·L−1AgNO 溶液,分析上面数据,判断下列说法正确的是
2 4 3
_______(填字母序号)。
A.混合液中c(SO )=1mol·L−1时不会产生Ag SO 沉淀
2 4
B.混合液中c(SO )=0.1 mol·L−1时不会产生Ag SO 沉淀
2 4
C.无论SO 浓度大小都会产生Ag SO 沉淀
2 4
D.若使用0.01 mol·L−1AgNO 溶液,可基本排除SO 对Cl-检验构成的干扰
3
(3)将实验一编号③中的理论计算结果与现象对照,发现理论上大部分Ag+应该形成沉淀,这与“有些许浑
浊”的现象相矛盾。为探究真相,在实验一的基础上继续设计了以下实验。
实验二:
编号 AgNO 浓度/mol·L−1 现象 滴加硝酸后的现象
3
滴加稀硝酸,沉淀大量溶解;改加浓硝酸,
① 2 出现大量白色沉淀
沉淀较快消失
② 0.5 出现少量白色沉淀 滴加稀硝酸,沉淀基本消失对于Ag SO 溶于硝酸的原因提出了如下假设,请完成假设二。
2 4
假设一:NO 对Ag SO 溶解起作用。
2 4
假设二:_______。
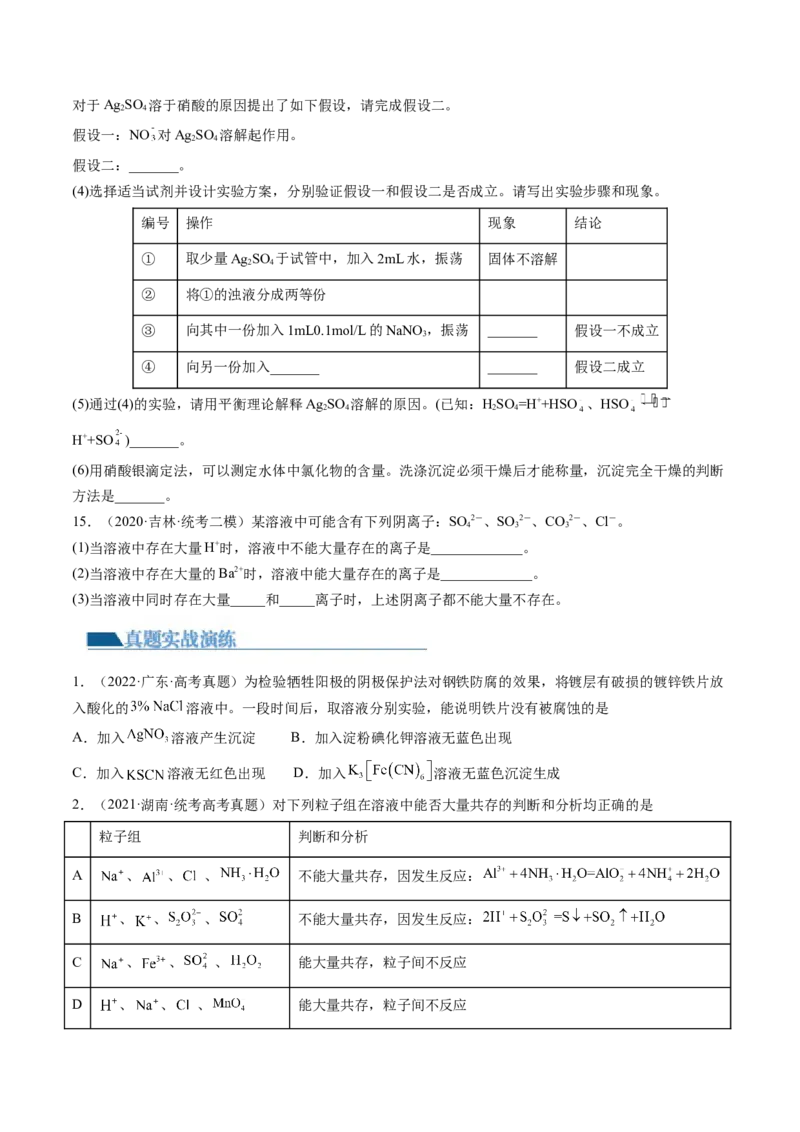
(4)选择适当试剂并设计实验方案,分别验证假设一和假设二是否成立。请写出实验步骤和现象。
编号 操作 现象 结论
① 取少量Ag SO 于试管中,加入2mL水,振荡 固体不溶解
2 4
② 将①的浊液分成两等份
③ 向其中一份加入1mL0.1mol/L的NaNO ,振荡 _______ 假设一不成立
3
④ 向另一份加入_______ _______ 假设二成立
(5)通过(4)的实验,请用平衡理论解释Ag SO 溶解的原因。(已知:HSO =H++HSO 、HSO
2 4 2 4
H++SO )_______。
(6)用硝酸银滴定法,可以测定水体中氯化物的含量。洗涤沉淀必须干燥后才能称量,沉淀完全干燥的判断
方法是_______。
15.(2020·吉林·统考二模)某溶液中可能含有下列阴离子:SO 2-、SO 2-、CO2-、Cl-。
4 3 3
(1)当溶液中存在大量H+时,溶液中不能大量存在的离子是_____________。
(2)当溶液中存在大量的Ba2+时,溶液中能大量存在的离子是_____________。
(3)当溶液中同时存在大量_____和_____离子时,上述阴离子都不能大量不存在。
1.(2022·广东·高考真题)为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁片放
入酸化的 溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是
A.加入 溶液产生沉淀 B.加入淀粉碘化钾溶液无蓝色出现
C.加入 溶液无红色出现 D.加入 溶液无蓝色沉淀生成
2.(2021·湖南·统考高考真题)对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
粒子组 判断和分析
A 、 、 、 不能大量共存,因发生反应:
B 、 、 、 不能大量共存,因发生反应:
C 、 、 、 能大量共存,粒子间不反应
D 、 、 、 能大量共存,粒子间不反应3.(2021·重庆·统考高考真题)25°时, 下列各组离子在指定溶液中一定能大量共存的是
A.1.0 mol·L-1氯化钡溶液中: Mg2+、K+、Br-、
B.1.0 mol·L-1硫酸中: A13+、 Na+、Cl-、
C.pH=1l 的氨水中: Fe2+、 Na+、 、ClO-
D.pH=1的硝酸中: Fe3+、K+、I-、
4.(2022·湖北·统考高考真题)下列各组离子在给定溶液中能大量共存的是
A.在 氨水中:
B.在 氯化钠溶液中:
C.在 醋酸溶液中:
D.在 硝酸银溶液中:
5.(2020·浙江·高考真题)黄色固体X,可能含有漂白粉、 、 、 、 之中的几种
或全部。将X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的是
A.X中含 ,可能含有
B.X中含有漂白粉和
C.X中含有 ,Y中含有
D.用 酸化溶液Z,若有黄绿色气体放出,说明X中含有