文档内容
第 10 讲 氯及其化合物
【学科核心素养】
1.宏观辨识与微观探析:能从氯原子的结构理解Cl 的性质,形成“结构决定性质”的观念。
2
2.科学探究与创新意识:能和同学交流实验探究的成果,提出进一步探究或改进氯及其化合物的制备
及性质实验的设想,培养勇于质疑和批判的创新精神。认识科学探究是进行科学发现、创造和应用的科学
实践活动;能从问题和假设出发,依据探究目的,设计探究方案,获得卤素单质的提取方法。
3.科学态度与社会责任:认识氯及其化合物对环境的影响,形成绿色环保的意识。关注与化学有关的
社会热点问题。了解环境保护与资源开发的关系.具有绿色化学观念。勇于承担责任,权衡利弊,积极参与
化学问题的社会决策。
【知识点解读】
知识点一 氯及其化合物的性质和应用
一、氯气的性质
1.氯气的物理性质
颜色 气味 毒性 密度 特性
黄绿色 刺激性气味 有毒 比空气重 易液化
【特别提醒】实验室里闻有毒气体及未知气体气味的方法是:用手在瓶口轻轻扇动,仅使极少量气体
飘进鼻孔。
2.从氯的原子结构认识氯气的化学性质——氧化性
依据氯气的氧化性完成下列方程式:
(1)与金属反应
①Fe:2Fe+3Cl=====2FeCl ,棕红色烟。
2 3
②Cu:Cu+Cl=====CuCl ,棕黄色烟。
2 2
(2)与非金属反应
H:H+Cl=====2HCl,苍白色火焰;
2 2 2
H 和Cl 的混合气体光照时会发生爆炸。
2 2
(3)与还原性无机化合物反应:
①与碘化钾溶液反应:Cl+2KI===2KCl+I。
2 2
②与SO 水溶液反应:Cl+SO +2HO===H SO +2HCl。
2 2 2 2 2 4③与FeCl 溶液反应:Cl+2FeCl ===2FeCl 。
2 2 2 3
3.从化合价的角度认识Cl 的化学性质——歧化反应
2
氯气与水或碱反应,氯元素的化合价既有升高又有降低,因而氯气既表现氧化性又表现还原性。
(1)与水反应
化学方程式:Cl+HO HCl+HClO,
2 2
离子方程式:Cl+HO H++Cl-+HClO。
2 2
(2)与碱反应
①与烧碱反应:Cl+2NaOH===NaCl+NaClO+HO。
2 2
②制取漂白粉:2Cl+2Ca(OH) ===CaCl +Ca(ClO) +2HO。
2 2 2 2 2
4.从平衡的角度理解氯水的成分和性质
氯气能溶于水(1∶2),氯气的水溶液称为氯水,溶于水的氯气只有少量与水反应。
(1)氯水中存在三种平衡关系:
①Cl+HO HCl+HClO
2 2
②HClO H++ClO-
③HO H++OH-
2
(2)氯水性质的多重性
新制氯水的多种成分决定了它具有多重性质,在不同的化学反应中,氯水中参与反应的微粒不同。
【易错警示】氯水的组成及性质在应用中的常见误区
(1)氯水中因HClO见光分解,随着HClO的消耗,最后成为盐酸,故久置氯水酸性增加,无漂白性。
因此,氯水要现用现配。(2)制取氯水的反应为Cl+HO HCl+HClO,反应中Cl 既是氧化剂,又是还原剂,且1 mol Cl
2 2 2 2
参加反应,转移电子数为N 。
A
(3)Cl 尽管有较强的氧化性,但没有漂白性,氯水具有漂白性是因为Cl 与水反应生成了强氧化性的
2 2
HClO。
(4)ClO-与Fe2+、I-、S2-、HS-、SO等在水中因发生氧化还原反应而不能大量共存。
二、次氯酸和次氯酸盐的性质
1.次氯酸
(1)不稳定性
次氯酸分解反应的化学方程式为2HClO=====2HCl+O↑。
2
(2)强氧化性
①能将有色物质氧化为无色物质,作漂白剂。
②杀菌、消毒。
(3)弱酸性
向NaClO溶液中通入少量CO,离子方程式为
2
ClO-+CO+HO===HCO+HClO。
2 2
2.次氯酸盐
(1)“84”消毒液
有效成分为NaClO,它与洁厕灵(主要成分盐酸)混合立即会产生氯气,其离子方程式是ClO-+Cl-+
2H+===Cl ↑+HO。
2 2
(2)漂白粉
①成分:漂白粉的主要成分是CaCl 和Ca(ClO) ,其中有效成分是Ca(ClO) 。
2 2 2
②漂白原理:在潮湿的空气中能吸收CO,化学方程式为Ca(ClO) +CO+HO===2HClO+CaCO ↓。
2 2 2 2 3
【特别提醒】
①向Ca(ClO) 溶液中通入少量CO,发生的反应为Ca2++2ClO-+CO+HO===CaCO↓+2HClO。
2 2 2 2 3
②向Ca(ClO) 溶液中通入SO ,生成的是CaSO 而不是CaSO。
2 2 4 3
③次氯酸盐(ClO-)无论是在酸性、碱性还是中性条件下,均具有强氧化性,均能氧化I-、Fe2+、SO、
S2-等还原性离子。
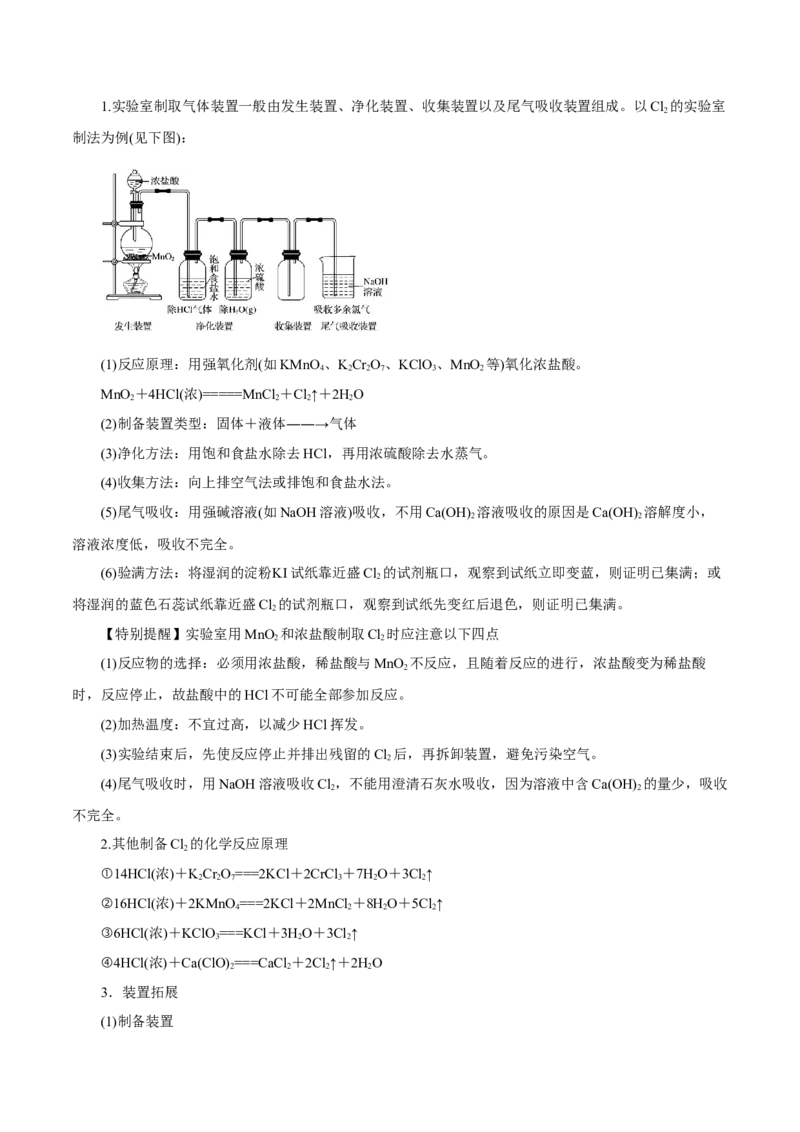
三、氯气的实验室制法1.实验室制取气体装置一般由发生装置、净化装置、收集装置以及尾气吸收装置组成。以Cl 的实验室
2
制法为例(见下图):
(1)反应原理:用强氧化剂(如KMnO 、KCr O、KClO、MnO 等)氧化浓盐酸。
4 2 2 7 3 2
MnO +4HCl(浓)=====MnCl +Cl↑+2HO
2 2 2 2
(2)制备装置类型:固体+液体――→气体
(3)净化方法:用饱和食盐水除去HCl,再用浓硫酸除去水蒸气。
(4)收集方法:向上排空气法或排饱和食盐水法。
(5)尾气吸收:用强碱溶液(如NaOH溶液)吸收,不用Ca(OH) 溶液吸收的原因是Ca(OH) 溶解度小,
2 2
溶液浓度低,吸收不完全。
(6)验满方法:将湿润的淀粉KI试纸靠近盛Cl 的试剂瓶口,观察到试纸立即变蓝,则证明已集满;或
2
将湿润的蓝色石蕊试纸靠近盛Cl 的试剂瓶口,观察到试纸先变红后退色,则证明已集满。
2
【特别提醒】实验室用MnO 和浓盐酸制取Cl 时应注意以下四点
2 2
(1)反应物的选择:必须用浓盐酸,稀盐酸与MnO 不反应,且随着反应的进行,浓盐酸变为稀盐酸
2
时,反应停止,故盐酸中的HCl不可能全部参加反应。
(2)加热温度:不宜过高,以减少HCl挥发。
(3)实验结束后,先使反应停止并排出残留的Cl 后,再拆卸装置,避免污染空气。
2
(4)尾气吸收时,用NaOH溶液吸收Cl,不能用澄清石灰水吸收,因为溶液中含Ca(OH) 的量少,吸收
2 2
不完全。
2.其他制备Cl 的化学反应原理
2
①14HCl(浓)+KCr O===2KCl+2CrCl +7HO+3Cl↑
2 2 7 3 2 2
②16HCl(浓)+2KMnO ===2KCl+2MnCl +8HO+5Cl↑
4 2 2 2
③6HCl(浓)+KClO===KCl+3HO+3Cl↑
3 2 2
④4HCl(浓)+Ca(ClO) ===CaCl +2Cl↑+2HO
2 2 2 2
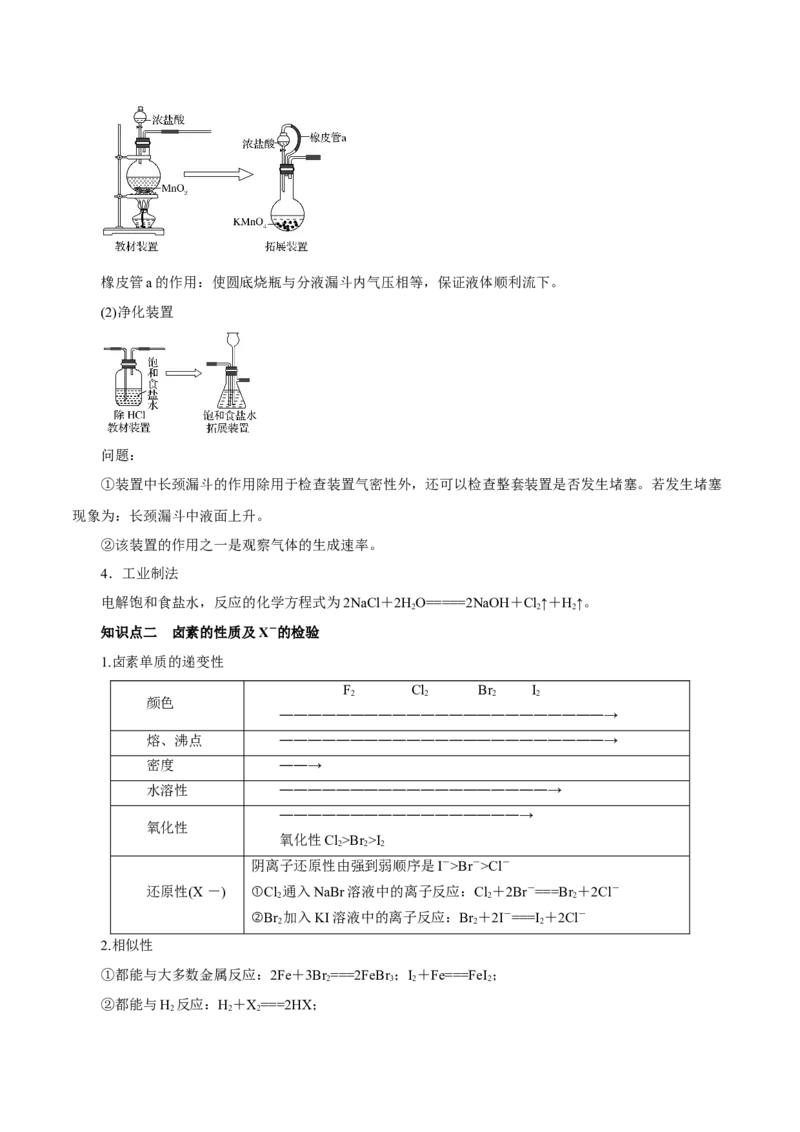
3.装置拓展
(1)制备装置橡皮管a的作用:使圆底烧瓶与分液漏斗内气压相等,保证液体顺利流下。
(2)净化装置
问题:
①装置中长颈漏斗的作用除用于检查装置气密性外,还可以检查整套装置是否发生堵塞。若发生堵塞
现象为:长颈漏斗中液面上升。
②该装置的作用之一是观察气体的生成速率。
4.工业制法
电解饱和食盐水,反应的化学方程式为2NaCl+2HO=====2NaOH+Cl↑+H↑。
2 2 2
知识点二 卤素的性质及X-的检验
1.卤素单质的递变性
F Cl Br I
2 2 2 2
颜色
―――――――――――――――――――――――→
熔、沸点 ―――――――――――――――――――――――→
密度 ――→
水溶性 ―――――――――――――――――――→
―――――――――――――――――→
氧化性
氧化性Cl>Br >I
2 2 2
阴离子还原性由强到弱顺序是I->Br->Cl-
还原性(X -) ①Cl 通入NaBr溶液中的离子反应:Cl+2Br-===Br +2Cl-
2 2 2
②Br 加入KI溶液中的离子反应:Br +2I-===I +2Cl-
2 2 2
2.相似性
①都能与大多数金属反应:2Fe+3Br ===2FeBr ;I+Fe===FeI ;
2 3 2 2
②都能与H 反应:H+X===2HX;
2 2 2③都能与HO反应:X+HO HX+HXO(F 例外);
2 2 2 2
④都能与碱液反应:X+2NaOH===NaX+NaXO+HO(F 例外)。
2 2 2
3.性质的特殊性
①无正价,非金属性最强,F-的还原性最弱
氟 ②2F +2HO===4HF+O,与H 反应在暗处即爆炸
2 2 2 2
③氢氟酸是弱酸,能腐蚀玻璃,故应保存在塑料瓶中
①Br 常温下是深红棕色液体,是唯一的液态非金属单质
2
②Br 易溶于有机溶剂
溴 2
③液态Br 有剧毒,易挥发,故盛溴的试剂瓶中加水,进行水封,保存液溴不能
2
用橡胶塞
①淀粉遇I 变色
2
②I 加热时易升华
2
碘 ③I 易溶于有机溶剂
2
④I 易与NaSO 反应:I+2SO===2I-+SO,此反应常用于滴定法(以淀粉为指
2 2 2 3 2 2 4
示剂)来定量测定碘的含量
【特别提醒】
①F 能与水反应放出O,故F 不能从其他卤化物的水溶液中将卤素单质置换出来。
2 2 2
②氯、溴单质的氧化性较强,能与一些还原性离子反应,如Br 与SO、Fe2+反应的离子方程式分别为
2
SO+Br +HO===SO+2Br-+2H+、2Fe2++Br ===2Fe3++2Br-。
2 2 2
4.卤素单质溶于水或有机溶剂所呈现的颜色
单质 水 CCl 汽油(或苯) 酒精
4
Cl 淡黄→黄绿 黄绿 黄绿 黄绿
2
Br 黄→橙 橙→橙红 橙→橙红 橙→橙红
2
I 深黄→褐 紫→深紫 淡紫→紫红 淡紫→紫红
2
5.卤族化合物的相似性和递变性
(1)卤素化合物的性质
化合物 性质 备注
稳定性:HF>HCl>HBr>HI
HF几乎没有还原性;HF为弱酸,
氢化物 还原性:HFFe2+>Br-,通入Cl 后,I-先被氧化,其次是Fe2+,最后是Br-,当通入2 mol
2
Cl 时,2 mol的I-消耗1 mol Cl ,剩余的1 mol Cl 再与2 mol Fe2+反应,即溶液中发生的离子反应可表示
2 2 2
为2Fe2++2I-+2Cl===2Fe3++I+4Cl-,故A正确;根据还原性强弱可知,DE段应为Br-的物质的量的
2 2
变化情况,故B错误;由消耗Cl 的量可知,I-的物质的量为2 mol,Fe2+的物质的量为4 mol,Br-的物质
2
的量为6 mol,n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3,故C错误;因还原性:I->Fe2+>Br-,B点时I-完全反应,溶液
中含有Fe2+、Cl-和Br-,故D错误。
高频考点六 海水资源的开发
例6.(2021·湖南高考)一种工业制备无水氯化镁的工艺流程如下:
下列说法错误的是A.物质X常选用生石灰
B.工业上常用电解熔融MgCl 制备金属镁
2
C.“氯化”过程中发生的反应为
D.“煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水MgCl
2
【答案】D
【分析】海水经一系列处理得到苦卤水,苦卤水中含Mg2+,苦卤水中加物质X使Mg2+转化为
Mg(OH) ,过滤除去滤液,煅烧Mg(OH) 得MgO,MgO和C、Cl 经“氯化”得无水MgCl 。
2 2 2 2
【解析】物质X的作用是使Mg2+转化为Mg(OH) ,工业上常采用CaO,发生CaO+H O=Ca(OH) ,
2 2 2
Ca(OH) +Mg2+=Mg(OH) +Ca2+,A正确;Mg是较活泼金属,工业上常用电解熔融MgCl 制备金属镁,B正
2 2 2
确;由图可知“氯化”过程反应物为MgO、氯气、C,生成物之一为MgCl ,C在高温下能将二氧化碳还
2
原为CO,则“气体”为CO,反应方程式为 ,C正确;“煅烧”后得到MgO,
MgO和盐酸反应得到MgCl 溶液,由于MgCl 在溶液中水解为氢氧化镁和HCl,将所得溶液加热蒸发HCl
2 2
会逸出,MgCl 水解平衡正向移动,得到氢氧化镁,得不到无水MgCl ,D错误;故选D。
2 2
【举一反三】海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下
列有关说法正确的是( )
A.制取NaHCO 的反应是利用其溶解度小于NaCl和NH Cl
3 4
B.①粗盐提纯中除去杂质离子Mg2+、Ca2+、SO时,必须先除Ca2+后除SO
C.在③④⑤步骤中,溴元素均被氧化
D.工业上通过电解饱和MgCl 溶液制取金属镁
2
【答案】A
【解析】制取NaHCO 的反应是利用其溶解度比较小,A项正确;先用过量的氯化钡除去SO,再用碳
3
酸钠除去Ca2+及Ba2+,所以应先除SO后除Ca2+,B项错误;第③⑤步骤中,溴元素被氧化,第④步骤
中,发生反应Br +SO +2HO===2HBr+HSO ,溴元素被还原,C项错误;电解饱和MgCl 溶液制得的
2 2 2 2 4 2
是Mg(OH) 、Cl 和H,工业上通过电解熔融状态的MgCl 制取金属镁,D项错误。
2 2 2 2
【变式探究】根据下图海水综合利用的工艺流程图,判断下列说法正确的是( )已知:MgCl ·6H O受热生成Mg(OH)Cl和HCl气体等。
2 2
A.过程①的粗盐提纯是物理过程,过程②通过氧化还原反应可产生两种单质
B.在过程③中将MgCl ·6H O灼烧即可制得无水MgCl
2 2 2
C.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题
D.在过程④⑥反应中每氧化0.2 mol Br-需要消耗2.24 L Cl
2
【答案】C
【解析】过程①中除去Mg2+、CO和SO需要用化学方法,A错误;根据已知信息可知,B错误;过
程⑤发生的反应为SO +2HO+Br ===H SO +2HBr,溶液呈强酸性,C正确;每氧化0.2 mol Br-需要消
2 2 2 2 4
耗0.1 mol Cl ,但不一定是2.24 L,D错误。
2