文档内容
第12讲 氮及其化合物
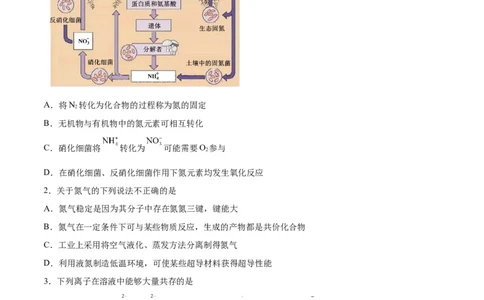
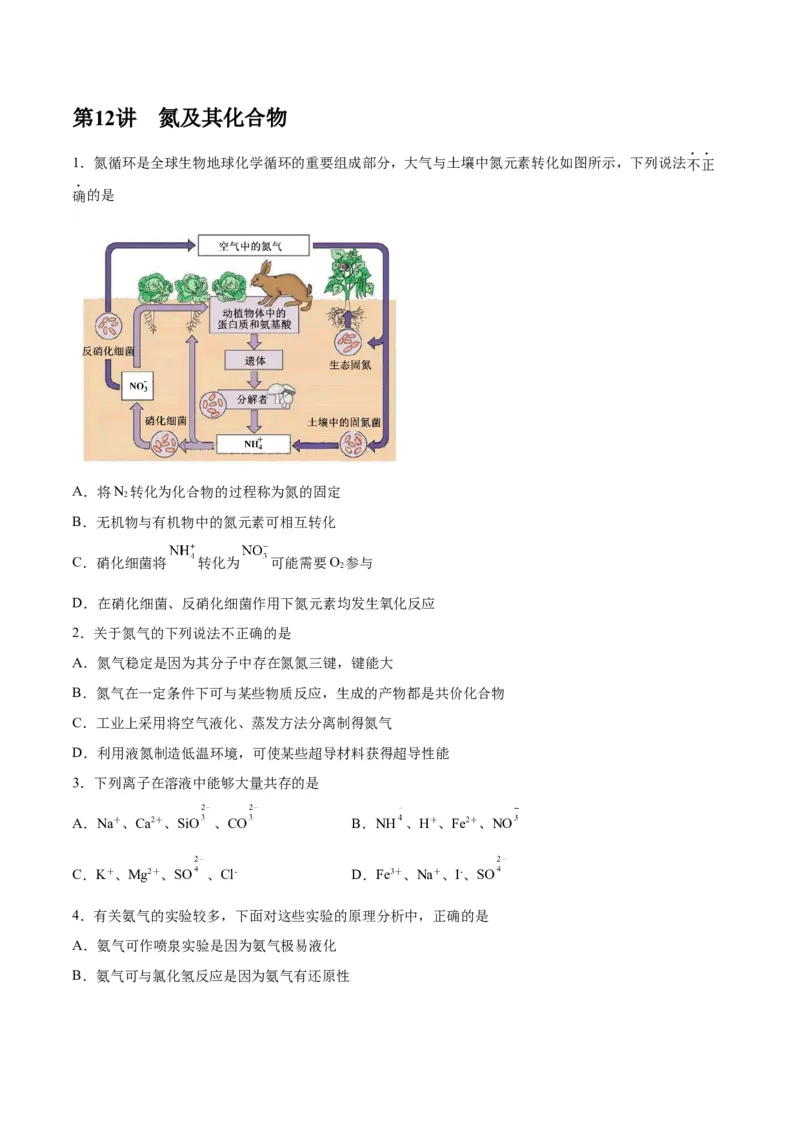
1.氮循环是全球生物地球化学循环的重要组成部分,大气与土壤中氮元素转化如图所示,下列说法不正
确的是
A.将N 转化为化合物的过程称为氮的固定
2
B.无机物与有机物中的氮元素可相互转化
C.硝化细菌将 转化为 可能需要O 参与
2
D.在硝化细菌、反硝化细菌作用下氮元素均发生氧化反应
2.关于氮气的下列说法不正确的是
A.氮气稳定是因为其分子中存在氮氮三键,键能大
B.氮气在一定条件下可与某些物质反应,生成的产物都是共价化合物
C.工业上采用将空气液化、蒸发方法分离制得氮气
D.利用液氮制造低温环境,可使某些超导材料获得超导性能
3.下列离子在溶液中能够大量共存的是
A.Na+、Ca2+、SiO 、CO B.NH 、H+、Fe2+、NO
C.K+、Mg2+、SO 、Cl- D.Fe3+、Na+、I-、SO
4.有关氨气的实验较多,下面对这些实验的原理分析中,正确的是
A.氨气可作喷泉实验是因为氨气极易液化
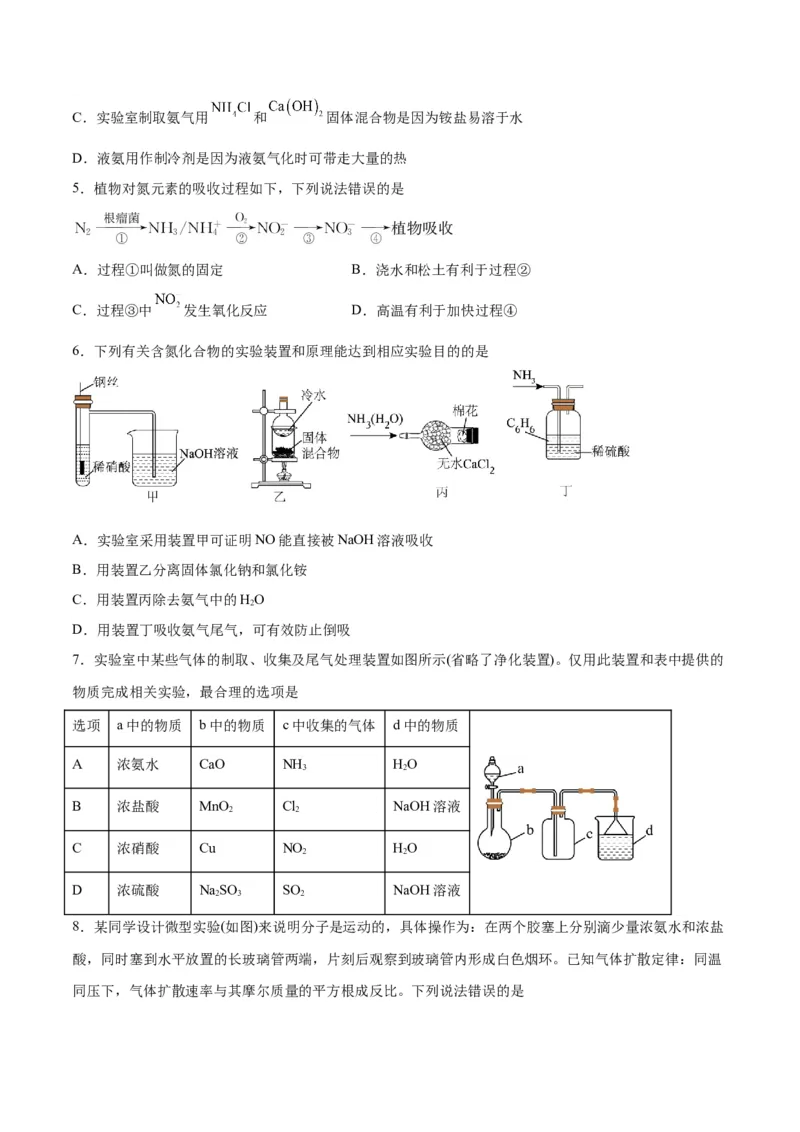
B.氨气可与氯化氢反应是因为氨气有还原性C.实验室制取氨气用 和 固体混合物是因为铵盐易溶于水
D.液氨用作制冷剂是因为液氨气化时可带走大量的热
5.植物对氮元素的吸收过程如下,下列说法错误的是
A.过程①叫做氮的固定 B.浇水和松土有利于过程②
C.过程③中 发生氧化反应 D.高温有利于加快过程④
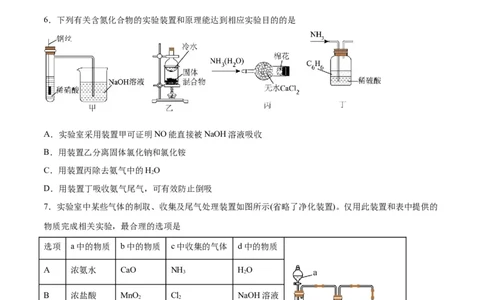
6.下列有关含氮化合物的实验装置和原理能达到相应实验目的的是
A.实验室采用装置甲可证明NO能直接被NaOH溶液吸收
B.用装置乙分离固体氯化钠和氯化铵
C.用装置丙除去氨气中的HO
2
D.用装置丁吸收氨气尾气,可有效防止倒吸
7.实验室中某些气体的制取、收集及尾气处理装置如图所示(省略了净化装置)。仅用此装置和表中提供的
物质完成相关实验,最合理的选项是
选项 a中的物质 b中的物质 c中收集的气体 d中的物质
A 浓氨水 CaO NH HO
3 2
B 浓盐酸 MnO Cl NaOH溶液
2 2
C 浓硝酸 Cu NO HO
2 2
D 浓硫酸 NaSO SO NaOH溶液
2 3 2
8.某同学设计微型实验(如图)来说明分子是运动的,具体操作为:在两个胶塞上分别滴少量浓氨水和浓盐
酸,同时塞到水平放置的长玻璃管两端,片刻后观察到玻璃管内形成白色烟环。已知气体扩散定律:同温
同压下,气体扩散速率与其摩尔质量的平方根成反比。下列说法错误的是A.白烟主要成份为 B. 的电子式为:
C. 中只含有离子键 D.该现象说明 的扩散速率比 快
9.如图所示,向一定量的铁粉中加入一定体积12 mol·L-1的浓硝酸并加热,待反应结束后,下列微粒在体
系中一定存在的是
① ②Fe2+ ③Fe3+ ④NO ⑤NO
2
A.①④ B.①⑤ C.②④⑤ D.①②③⑤
10.如图所示的装置,烧瓶中充满干燥气体a,打开弹簧夹c,将滴管中的液体b挤入烧瓶内,烧杯中的液
体d呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是
a(干燥气体) b(液体)
A 水
B 饱和 溶液
C NO 水
D NaOH溶液
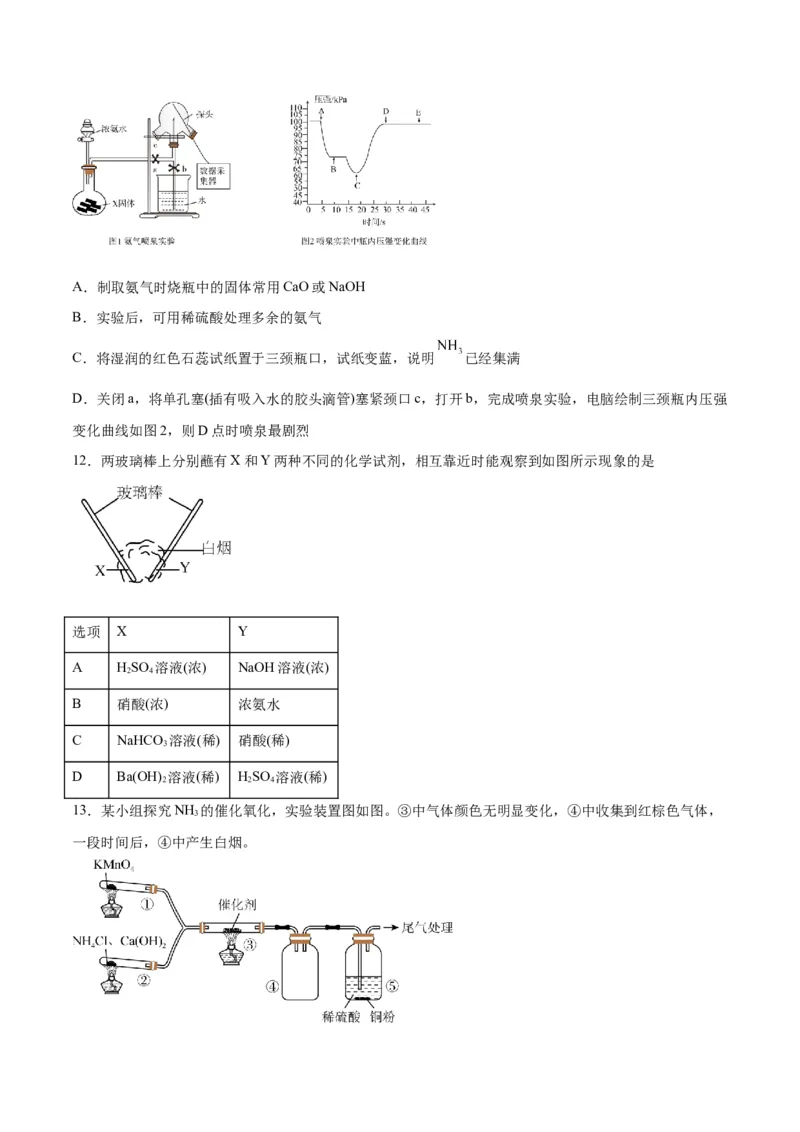
11.现用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理。下列说法错误的是A.制取氨气时烧瓶中的固体常用CaO或NaOH
B.实验后,可用稀硫酸处理多余的氨气
C.将湿润的红色石蕊试纸置于三颈瓶口,试纸变蓝,说明 已经集满
D.关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧颈口c,打开b,完成喷泉实验,电脑绘制三颈瓶内压强
变化曲线如图2,则D点时喷泉最剧烈
12.两玻璃棒上分别蘸有X和Y两种不同的化学试剂,相互靠近时能观察到如图所示现象的是
选项 X Y
A HSO 溶液(浓) NaOH溶液(浓)
2 4
B 硝酸(浓) 浓氨水
C NaHCO 溶液(稀) 硝酸(稀)
3
D Ba(OH) 溶液(稀) HSO 溶液(稀)
2 2 4
13.某小组探究NH 的催化氧化,实验装置图如图。③中气体颜色无明显变化,④中收集到红棕色气体,
3
一段时间后,④中产生白烟。下列分析不正确的是
A.若②中只加入NH Cl不可以实现上述现象
4
B.③、④中现象说明③中的反应是4NH +5O 4NO+6H O
3 2 2
C.④中白烟的主要成分是NH Cl
4
D.一段时间后,⑤中溶液可能变蓝
14.用排空气法收集气体X并将试管倒立在水中,实验如图所示。下列说法不正确的是
A.若X为NO ,剩余气体为NO,试管中溶液pH<7
2
B.若X为Cl,试管中溶液可使石蕊褪色
2
C.取反应后试管中溶液,滴入品红溶液褪色,X可能为SO
2
D.若X为NH ,试管中溶液在空气中露置后pH下降,说明氨水有挥发性
3
15. 是一种重要的化工原料,可以制备一系列物质(见图)。下列说法正确的是
A.流程中涉及的反应全是氧化还原反应
B.可以用排空气法收集NO
C. 和 在一定条件下可发生氧化还原反应
D.饱和食盐水中先通入 后通入 制取
16.柴油发动机在工作过程中会产生氮的氧化物,在尾气处理环节,加入尿素 可有效减少氮氧化物的排放,相关反应如下: ,下列说法不正确的是
A.该反应中氧化产物和还原产物物质的量之比为2∶5
B.常温下NO遇空气会变成红棕色
C.该反应每消耗1molNO转移2mol电子
D.氮气和氧气在高温条件下发生反应是汽车尾气中氮氧化物的主要成因
17.部分含氮物质的价~类二维关系如图,下列有关说法正确的是
A.将充满物质c的试管倒置于水槽中,水可充满试管
B.图中氧化物均为酸性氧化物
C.工业上可用a为原料合成d
D.常温下d的溶液与单质铝反应可生成b或c
18.氨是一种重要的化工原料,根据下图转化判断下列有关表述正确的是
A.浓硝酸见光易分解且易挥发,应用棕色试剂瓶盛放且用胶塞密封
B.戊与丁反应时,氧化剂与还原剂的物质的量之比为1∶2
C.实验室中可以采取加热甲物质的方法制取氨气
D.向饱和NaCl溶液中依次通入过量的 和 ,然后过滤可制得乙
19.某透明溶液中可能含有①Na+、② 、③Fe2+、④OH-、⑤ 、⑥ 中的几种离子依次进行下列实验:
Ⅰ.用红色的石蕊试纸检测原溶液,试纸未变蓝色;
Ⅱ.取少许原溶液于试管中,加入2滴酸性高酸钾溶液,溶液呈紫色;
Ⅲ.取100mL原溶液加入足量的浓氢氧化钠溶液并加热,收集到标准状况下气体的体积为0.56L;
Ⅳ.取50mL原溶液加入足量的Ba(NO ) 溶液和稀硝酸,产生2.33g沉淀。下列说法错误的是
3 2
A.原溶液中一定不存在OH-
B.原溶液中一定不存在Fe2+,可能存在
C.原溶液中NH 的浓度为0.25mol•L-1
D.原溶液中一定含有Na+、NH 、
20.现有一定量Cu和CuO的混合物,向其中加入0.6L2.0 稀硝酸,混合物完全溶解,同时生成
4.48L(标准状况)NO。向所得溶液中加入一定体积1.0 NaOH溶液,恰好使 沉淀完全,沉淀经
洗涤、充分灼烧后得32.0g固体(忽略溶液的体积变化)。下列说法不正确的是
A.该混合物中铜单质的质量为19.2g
B.与该混合物反应消耗的 的量为1.0mol
C.加入NaOH溶液的体积是800mL
D. 沉淀完全后,溶液中 为0.625
21.某小组同学探究铜和浓硝酸的反应,进行如下实验:
实验1:分别取 浓硝酸与不同质量的铜粉充分反应,铜粉完全溶解,溶液颜色如下表:
编号 ① ② ③ ④ ⑤
铜粉质量/g 0.1 0.2 0.3 0.4 0.5
溶液颜色 绿色 草绿色 蓝绿色偏绿 蓝绿色偏蓝 蓝色
(1)写出铜和浓硝酸反应的离子方程式: 。
(2)小组同学认为溶液显绿色的可能原因是:
猜想1:硝酸铜浓度较高,溶液呈绿色;猜想2: 溶解在混合溶液中,溶液呈绿色。
依据实验1中的现象,判断猜想1是否合理,并说明理由: 。
(3)取⑤中溶液, (填操作和现象),证实猜想2成立。
小组同学进行如下实验也证实了猜想2成立。
实验2:向①中溶液以相同流速分别通入 和空气,观察现象。
通入气体 氮气 空气
液面上方出现明显的红棕色气体 液面上方出现明显的红棕色气体
现象
后溶液变为蓝色 后溶液变为蓝色
(4)结合上述实验现象,下列推测合理的是 (填字母序号)。
a.①中溶液通入 时, 被缓慢氧化为
b.①中溶液里某还原性微粒与绿色有关,通入空气时较快被氧化
c.空气小的 溶于水显酸性,促进了溶液变蓝色
d.加热溶液①后,可能观察到溶液变蓝的现象
(5)小组同学继续探究实验2中现象的差异,并查阅文献:
ⅰ.“可溶性铜盐中溶解亚硝酸 ”可能是实验①中溶液显绿色的主要原因
ⅱ. 在溶液中存在
反应l: (慢)
反应2: (快)
解释实验2中“通入氮气变蓝慢,通入空气变蓝快”的原因 。
小组同学为确认亚硝酸参与了形成绿色溶液的过程,继续进行实验。
实验3:取3份等体积的①中绿色溶液,分别加入不同物质,观察现象。
加入物
固体 3滴30% 溶液 3滴水
质
现象 溶液绿色变深 溶液迅速变为蓝色 溶液颜色几乎不变
(6)实验中加入的固体物质是 (填化学式)。加入 后溶液迅速变蓝可能的原因是(用化学方程式表示): , , 。
22.用如图方法回收废旧CPU中的单质Au(金),Ag和Cu。
已知:①浓硝酸不能单独将Au溶解。②HAuCl =H++AuCl
4
(1)酸溶后经 操作,将混合物分离。
(2)浓、稀HNO 均可作酸溶试剂。溶解等量的Cu消耗HNO 的物质的量不同,写出消耗HNO 物质的量少
3 3 3
的反应的化学方程式: 。
(3)HNO-NaCl与王水[V(浓硝酸):V(浓盐酸)=1:3溶金原理相同。
3
①将溶金反应的化学方程式补充完整:
Au+ NaCl+ HNO=HAuCl + + + NaNO
3 4 3
②关于溶金的下列说法正确的是 。
A.用到了HNO 的氧化性
3
B.王水中浓盐酸的主要作用是增强溶液的酸性
C.用浓盐酸与NaNO 也可使Au溶解
3
(4)若用Zn粉将溶液中的1molHAuCl 完全还原,则参加反应的Zn的物质的量是 mol。
4
(5)用适当浓度的盐酸、NaCl溶液、氨水与铁粉,可按照如图方法从酸溶后的的溶液中回收Cu和Ag(图中
标注的试剂和物质均不同)。
试剂1是 ,物质2是 。