文档内容
第六章 化学反应与能量
第17讲 化学能与热能(精练)
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
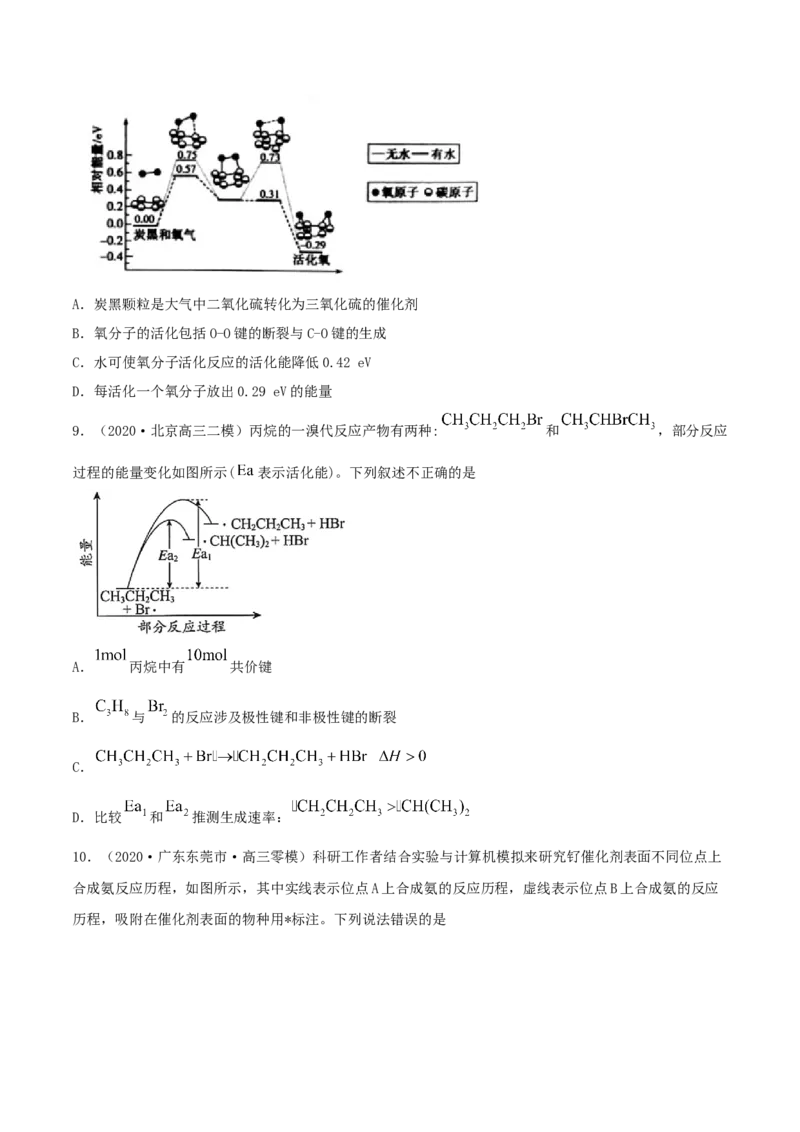
1.(2021·北京高三二模)依据图示关系,下列说法不正确的是
A.反应①是吸热反应
B.△H=△H+△H
3 1 2
C.反应③是一个熵增的反应
D.数据表明:VO(s)的能量比VO(s)低,更稳定
2 5 2 4
2.(2021·上海高三一模)反应2HO(l) 2HO(l)+O(g)能量变化如图所示,下列说法正确的是
2 2 ⇌ 2 2
A.因为是分解反应,所以该反应吸热
B.由途径a变成b改变了反应的热效应
C.1 mol HO(l)的能量高于1 mol HO(l)的能量
2 2 2
D.该反应说明HO(l)比HO(l)稳定
2 2 2
3.(2020·河南省驻马店市高三期末)“太阳能燃料”国际会议于2019年10月在我国武汉举行,旨在交流
和探讨太阳能光催化分解水制氢、太阳能光催化二氧化碳转化为燃料等问题。下列说法错误的是( )
A.太阳能燃料属于一次能源
B.直接电催化CO 制取燃料时,燃料是阴极产物
2
C.用光催化分解水产生的H 是理想的绿色能源
2
D.研发和利用太阳能燃料,有利于经济的可持续发展4.(2021·四川成都市·高三一模)已知正丁烷、异丁烷燃烧的热化学方程式分别为:CHCHCHCH(g)
3 2 2 3
+6.5O(g)→4CO(g)+5HO(l)△H=-2878kJ·mol-1,(CH)CHCH(g)+6.5O(g)→4CO(g)+5HO(l)△H=-
2 2 2 3 2 3 2 2 2
2869kJ·mol-1,下列说法正确的是
A.正丁烷分子储存的能量大于异丁烷分子 B.正丁烷的稳定性大于异丁烷
C.异丁烷转化为正丁烷的过程是一个放热过程 D.异丁烷和正丁烷属于同系物
5.(2021·湖南长沙市·长沙一中高三月考)如图所示为 破坏臭氧层的过程,下列说法不正确的
是( )
A.过程Ⅰ中断裂极性键 键
B.过程Ⅱ可用方程式表示为
C.过程Ⅲ中 是吸热过程
D.上述过程说明 中的氯原子是破坏臭氧层的催化剂
6.(2021·浙江嘉兴市·高三其他模拟)研究发现,一定条件下,Pt单原子催化反应CO(g)+3H(g)
2 2
CHOH(g)+HO(g)的历程如图所示,其中吸附在催化剂表面上的物种用“*”表示,“TS”表示过渡
3 2
态。下列说法不正确的是A.该反应的∆H<0
B.经历TS1CO 共价键发生了断裂,且生成了羧基
2
C.六个过渡态中对反应速率影响最大的是TS3
D.要提高该反应的选择性,可以选择合适的催化剂
7.(2020·安徽省怀宁县第二中学高三月考)图分别表示红磷、白磷燃烧时的能量变化,下列说法中正
确的是
A.白磷比红磷稳定
B.白磷燃烧产物比红磷燃烧产物稳定
C.1mol白磷转变为红磷放出2244.7kJ的热量
D.红磷燃烧的热化学方程式:4P(s)+5O
2
(g)=P
4
O
10
(s)△H=-2954kJ⋅mol−1
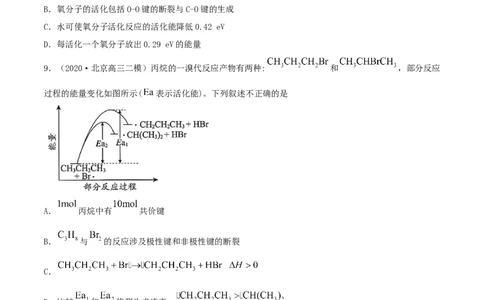
8.(2020·山东滨州市·高三二模)炭黑是雾霾中的重要颗粒物之一,研究发现它可以活化氧分子生成
活化氧,活化氧可以快速氧化二氧化硫。活化过程的能量变化模拟计算结果如图所示,下列说法错误的是A.炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
B.氧分子的活化包括O-O键的断裂与C-O键的生成
C.水可使氧分子活化反应的活化能降低0.42 eV
D.每活化一个氧分子放出0.29 eV的能量
9.(2020·北京高三二模)丙烷的一溴代反应产物有两种: 和 ,部分反应
过程的能量变化如图所示( 表示活化能)。下列叙述不正确的是
A. 丙烷中有 共价键
B. 与 的反应涉及极性键和非极性键的断裂
C.
D.比较 和 推测生成速率:
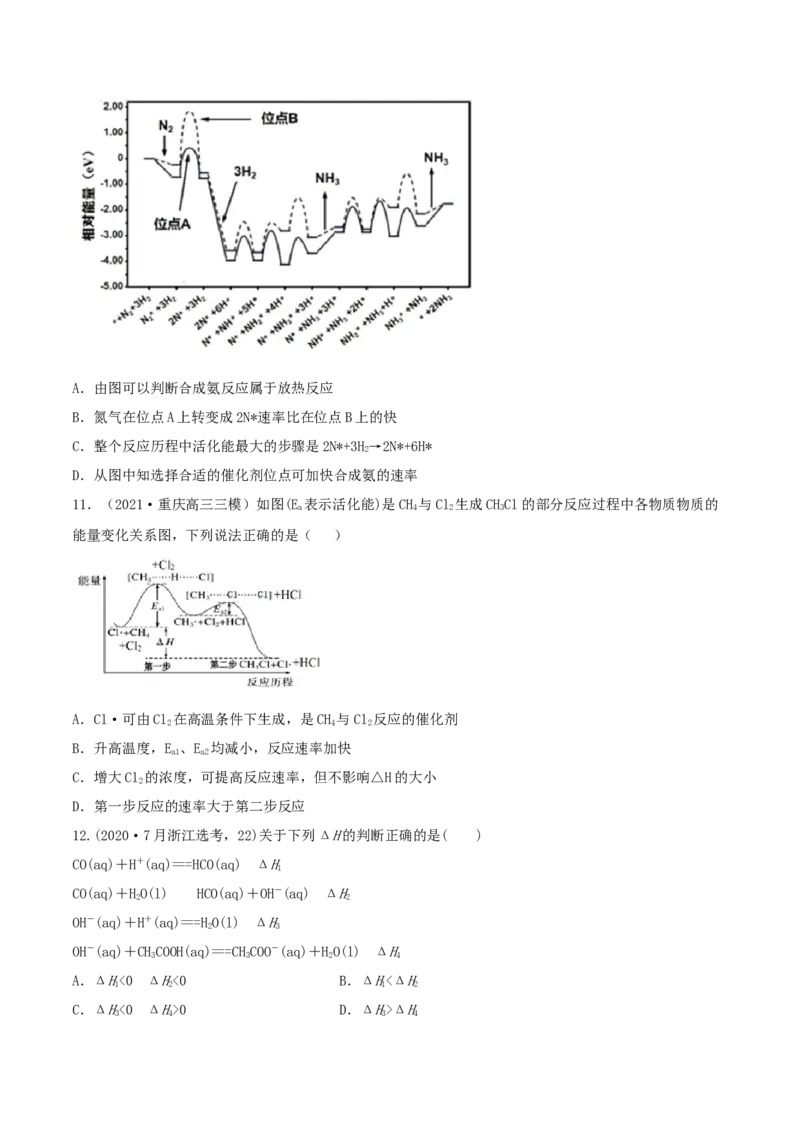
10.(2020·广东东莞市·高三零模)科研工作者结合实验与计算机模拟来研究钌催化剂表面不同位点上
合成氨反应历程,如图所示,其中实线表示位点A上合成氨的反应历程,虚线表示位点B上合成氨的反应
历程,吸附在催化剂表面的物种用*标注。下列说法错误的是A.由图可以判断合成氨反应属于放热反应
B.氮气在位点A上转变成2N*速率比在位点B上的快
C.整个反应历程中活化能最大的步骤是2N*+3H→2N*+6H*
2
D.从图中知选择合适的催化剂位点可加快合成氨的速率
11.(2021·重庆高三三模)如图(E 表示活化能)是CH 与Cl 生成CHCl的部分反应过程中各物质物质的
a 4 2 3
能量变化关系图,下列说法正确的是( )
A.Cl·可由Cl 在高温条件下生成,是CH 与Cl 反应的催化剂
2 4 2
B.升高温度,E 、E 均减小,反应速率加快
a1 a2
C.增大Cl 的浓度,可提高反应速率,但不影响△H的大小
2
D.第一步反应的速率大于第二步反应
12.(2020·7月浙江选考,22)关于下列ΔH的判断正确的是( )
CO(aq)+H+(aq)===HCO(aq) ΔH
1
CO(aq)+HO(l)HCO(aq)+OH-(aq) ΔH
2 2
OH-(aq)+H+(aq)===HO(l) ΔH
2 3
OH-(aq)+CHCOOH(aq)===CHCOO-(aq)+HO(l) ΔH
3 3 2 4
A.ΔH<0 ΔH<0 B.ΔH<ΔH
1 2 1 2
C.ΔH<0 ΔH>0 D.ΔH>ΔH
3 4 3 4二、主观题(共3小题,共40分)
13.(16分)(Ⅰ)丙烷是一种优良的燃料。试回答下列问题:
(1)已知丙烷完全燃烧生成CO 和1 mol HO(l)放出553.75kJ的热量,写出表示丙烷标准燃烧热的热化学
2 2
方程式:_____________。
(2)二甲醚(CHOCH)是一种新型燃料,应用前景广阔。1 mol 二甲醚完全燃烧生成CO 和液态水放出1 455
3 3 2
kJ的热量。若1 mol丙烷和二甲醚的混合气体完全燃烧生成CO 和液态水共放出1 645 kJ的热量,则混合
2
气体中,丙烷和二甲醚的物质的量之比为________。
(Ⅱ)CH、H、C都是优质的能源物质,它们燃烧的热化学方程式为:
4 2
①CH(g)+2O(g)=CO(g)+2HO(l) ΔH=-890.3 kJ·mol-1
4 2 2 2
②2H(g)+O(g)=2HO(l) ΔH=-571.6 kJ·mol-1
2 2 2
③C(s)+O(g)=CO(g) ΔH=-393.5 kJ·mol-1
2 2
(1)在深海中存在一种甲烷细菌,它们依靠酶使甲烷与O 作用产生的能量存活,甲烷细菌使1 mol甲烷生
2
成CO 气体与液态水,放出的能量____________(填“>”“<”或“=”)890.3 kJ。
2
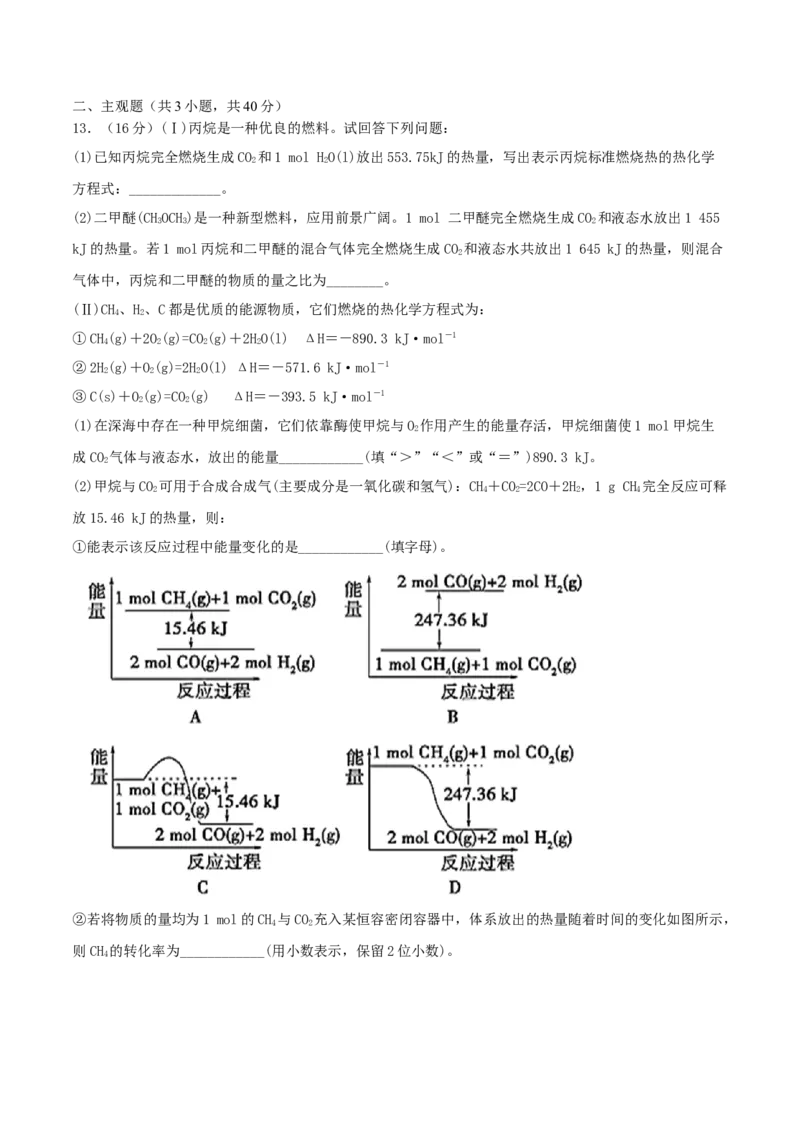
(2)甲烷与CO 可用于合成合成气(主要成分是一氧化碳和氢气):CH+CO=2CO+2H,1 g CH 完全反应可释
2 4 2 2 4
放15.46 kJ的热量,则:
①能表示该反应过程中能量变化的是____________(填字母)。
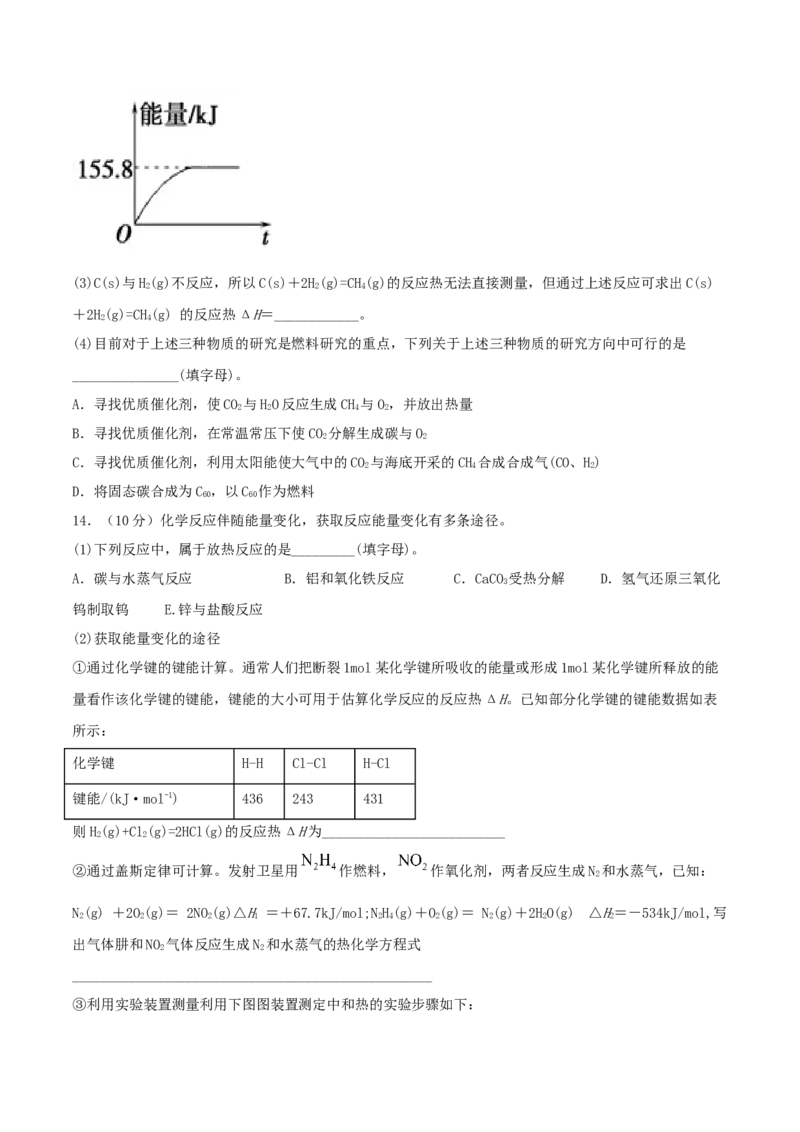
②若将物质的量均为1 mol的CH 与CO 充入某恒容密闭容器中,体系放出的热量随着时间的变化如图所示,
4 2
则CH 的转化率为____________(用小数表示,保留2位小数)。
4(3)C(s)与H(g)不反应,所以C(s)+2H(g)=CH(g)的反应热无法直接测量,但通过上述反应可求出C(s)
2 2 4
+2H(g)=CH(g) 的反应热ΔH=____________。
2 4
(4)目前对于上述三种物质的研究是燃料研究的重点,下列关于上述三种物质的研究方向中可行的是
_______________(填字母)。
A.寻找优质催化剂,使CO 与HO反应生成CH 与O,并放出热量
2 2 4 2
B.寻找优质催化剂,在常温常压下使CO 分解生成碳与O
2 2
C.寻找优质催化剂,利用太阳能使大气中的CO 与海底开采的CH 合成合成气(CO、H)
2 4 2
D.将固态碳合成为C ,以C 作为燃料
60 60
14.(10分)化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于放热反应的是_________(填字母)。
A.碳与水蒸气反应 B.铝和氧化铁反应 C.CaCO 受热分解 D.氢气还原三氧化
3
钨制取钨 E.锌与盐酸反应
(2)获取能量变化的途径
①通过化学键的键能计算。通常人们把断裂1mol某化学键所吸收的能量或形成1mol某化学键所释放的能
量看作该化学键的键能,键能的大小可用于估算化学反应的反应热ΔH。已知部分化学键的键能数据如表
所示:
化学键 H-H Cl-Cl H-Cl
键能/(kJ·mol-1) 436 243 431
则H(g)+Cl(g)=2HCl(g)的反应热ΔH为__________________________
2 2
②通过盖斯定律可计算。发射卫星用 作燃料, 作氧化剂,两者反应生成N 和水蒸气,已知:
2
N(g) +2O(g)= 2NO(g)△H =+67.7kJ/mol;NH(g)+O(g)= N(g)+2HO(g) △H=-534kJ/mol,写
2 2 2 1 2 4 2 2 2 2
出气体肼和NO 气体反应生成N 和水蒸气的热化学方程式
2 2
___________________________________________________
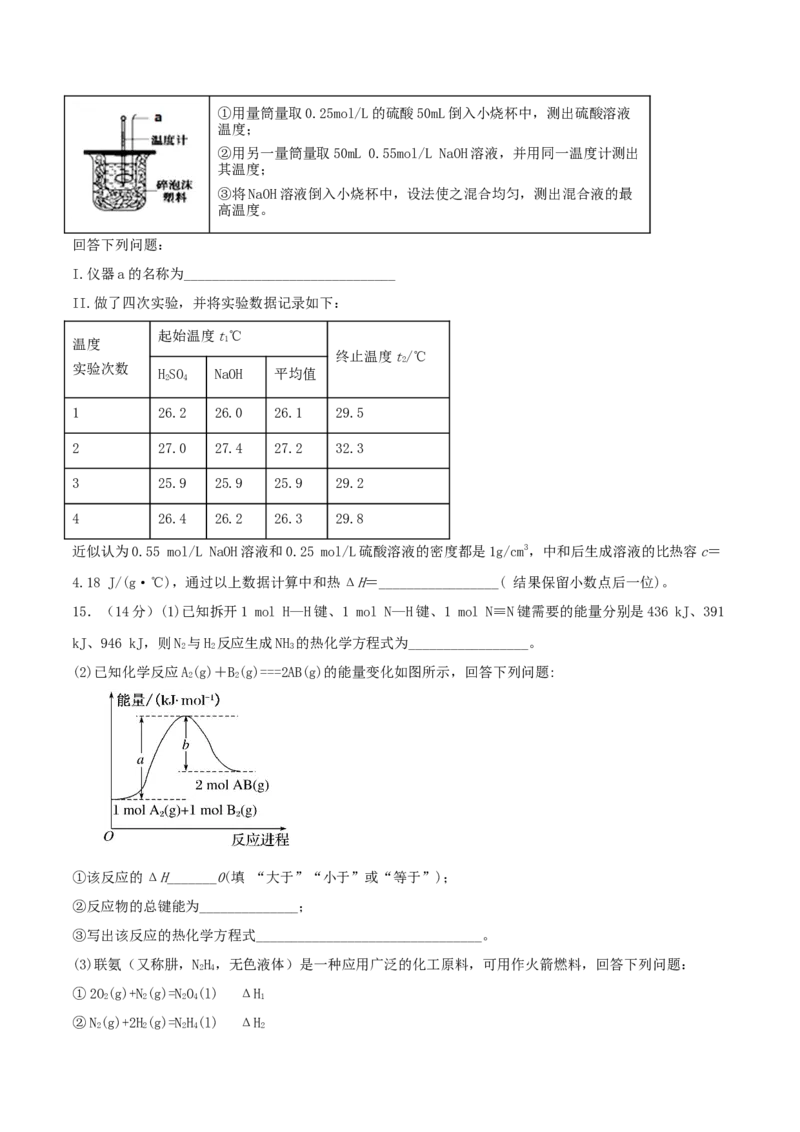
③利用实验装置测量利用下图图装置测定中和热的实验步骤如下:①用量筒量取0.25mol/L的硫酸50mL倒入小烧杯中,测出硫酸溶液
温度;
②用另一量筒量取50mL 0.55mol/L NaOH溶液,并用同一温度计测出
其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液的最
高温度。
回答下列问题:
I.仪器a的名称为______________________________
II.做了四次实验,并将实验数据记录如下:
起始温度t℃
温度 1
终止温度t/℃
2
实验次数
HSO NaOH 平均值
2 4
1 26.2 26.0 26.1 29.5
2 27.0 27.4 27.2 32.3
3 25.9 25.9 25.9 29.2
4 26.4 26.2 26.3 29.8
近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=
4.18 J/(g·℃),通过以上数据计算中和热ΔH=_________________( 结果保留小数点后一位)。
15.(14分)(1)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键需要的能量分别是436 kJ、391
kJ、946 kJ,则N 与H 反应生成NH 的热化学方程式为_________________。
2 2 3
(2)已知化学反应A(g)+B(g)===2AB(g)的能量变化如图所示,回答下列问题:
2 2
①该反应的ΔH_______0(填 “大于”“小于”或“等于”);
②反应物的总键能为______________;
③写出该反应的热化学方程式________________________________。
(3)联氨(又称肼,NH,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
2 4
①2O(g)+N(g)=NO(l) ΔH
2 2 2 4 1
②N(g)+2H(g)=NH(l) ΔH
2 2 2 4 2③O(g)+2H(g)=2HO(g) ΔH
2 2 2 3
④2NH(l) + NO(l)= 3N(g)+ 4HO(g) ΔH =-1048.9kJ/mol
2 4 2 4 2 2 4
写出联氨的结构式_______________,上述反应热效应之间的关系式为ΔH=__________,联氨和NO 可作
4 2 4
为火箭推进剂的主要原因为_______________________________。