文档内容
第 19 讲 化学平衡
【化学学科素养】
变化观念与平衡思想:知道化学变化需要一定的条件,并遵循一定规律;认识化学变化有一定限度,
是可以调控的。能多角度、动态地分析化学反应,运用化学反应原理解决实际问题。
证据推理与模型认知:建立观点、结论和证据之间的逻辑关系;知道可以通过分析、推理等方法认识
化学平衡的特征及其影响因素,建立模型。能运用模型解释化学现象,揭示现象的本质和规律。
【必备知识解读】
一、化学平衡状态
1.化学平衡研究的对象——可逆反应
2.化学平衡状态
(1)概念
一定条件下的可逆反应,当反应进行到一定程度时,正反应速率和逆反应速率相等,反应物的浓度和
生成物的浓度不再改变,我们称为“化学平衡状态”,简称化学平衡。
(2)建立过程
在一定条件下,把某一可逆反应的反应物加入固定容积的密闭容器中。反应过程如下:
以上过程可用如图表示:
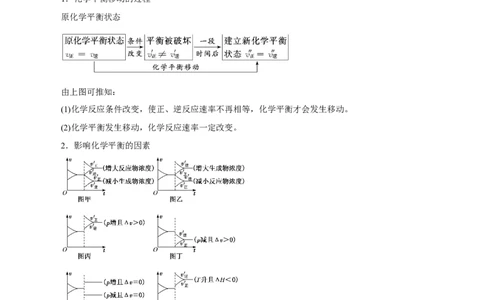
(3)平衡特点二、化学平衡移动
1.化学平衡移动的过程
原化学平衡状态
由上图可推知:
(1)化学反应条件改变,使正、逆反应速率不再相等,化学平衡才会发生移动。
(2)化学平衡发生移动,化学反应速率一定改变。
2.影响化学平衡的因素
(1)若其他条件不变,改变下列条件对化学平衡的影响
改变的条件(其他条件不变) 化学平衡移动的方向
浓度 增大反应物浓度或减小 向正反应方向移动,如图甲生成物浓度
减小反应物浓度或增大
向逆反应方向移动,如图乙
生成物浓度
增大压强 向气体分子总数减小的方向移动,如图丙
反应前后气
压强(对有
体体积改变
减小压强 向气体分子总数增大的方向移动,如图丁
气体参加
的反应) 反应前后气
改变压强 平衡不移动,如图戊
体体积不变
温度 升高温度 向吸热反应方向移动,如图己
降低温度 向放热反应方向移动,如图庚
催化剂 同等程度改变v 、v ,平衡不移动,如图辛
正 逆
【特别提醒】
压强对化学平衡的影响主要看改变压强能否引起反应物和生成物的浓度变化,只有引起物质的浓度变
化才会造成平衡移动,否则压强对平衡无影响。
(2)浓度的“决定性”作用
①恒温、恒容条件
原平衡体系――→体系总压强增大―→体系中各组分的浓度不变―→平衡不移动。
②恒温、恒压条件
原平衡体系――→容器容积增大,各反应气体的
3.化学平衡移动与化学反应速率的关系
v >v 平衡向正反应方向移动
正 逆
v =v 反应达到平衡状态,不发生平衡移动
正 逆
v <v 平衡向逆反应方向移动
正 逆
4.勒夏特列原理
如果改变影响化学平衡的条件之一(如温度、压强、以及参加反应的化学物质的浓度),平衡将向着能
够减弱这种改变的方向移动。
【特别提醒】
①由“化学平衡”可知:勒夏特列原理的适用对象是可逆过程。
②由“减弱”可知:只能减弱改变,而不能消除改变。
三、化学图像
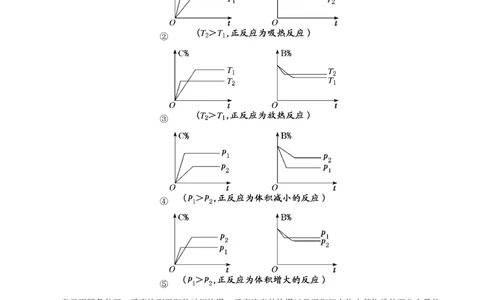
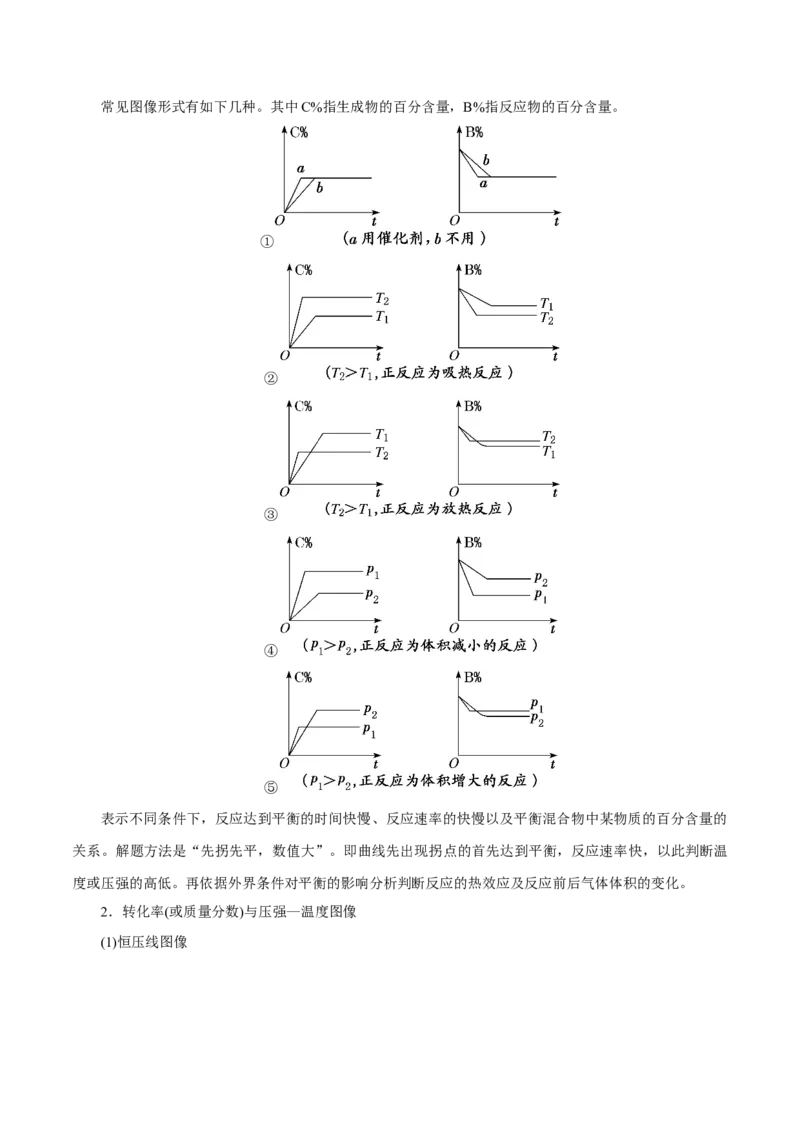
1.含量—时间—温度(压强)图像常见图像形式有如下几种。其中C%指生成物的百分含量,B%指反应物的百分含量。
①
②
③
④
⑤
表示不同条件下,反应达到平衡的时间快慢、反应速率的快慢以及平衡混合物中某物质的百分含量的
关系。解题方法是“先拐先平,数值大”。即曲线先出现拐点的首先达到平衡,反应速率快,以此判断温
度或压强的高低。再依据外界条件对平衡的影响分析判断反应的热效应及反应前后气体体积的变化。
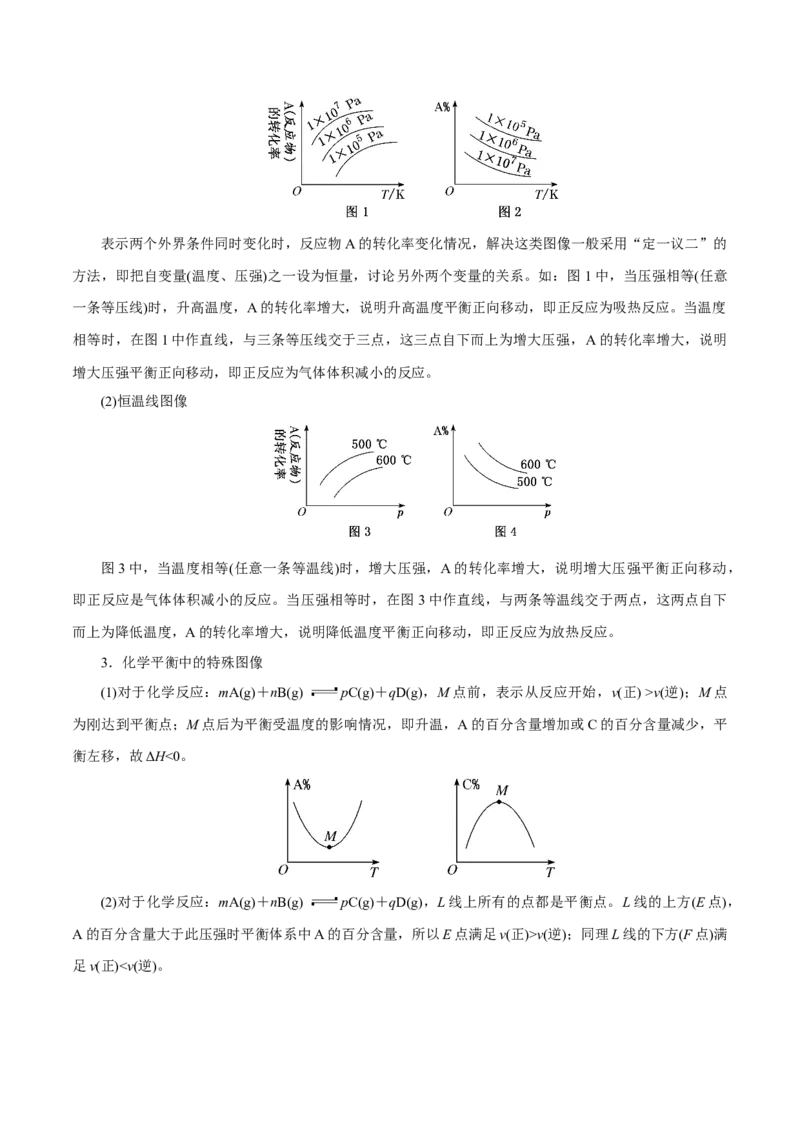
2.转化率(或质量分数)与压强—温度图像
(1)恒压线图像表示两个外界条件同时变化时,反应物A的转化率变化情况,解决这类图像一般采用“定一议二”的
方法,即把自变量(温度、压强)之一设为恒量,讨论另外两个变量的关系。如:图1中,当压强相等(任意
一条等压线)时,升高温度,A的转化率增大,说明升高温度平衡正向移动,即正反应为吸热反应。当温度
相等时,在图1中作直线,与三条等压线交于三点,这三点自下而上为增大压强,A的转化率增大,说明
增大压强平衡正向移动,即正反应为气体体积减小的反应。
(2)恒温线图像
图3中,当温度相等(任意一条等温线)时,增大压强,A的转化率增大,说明增大压强平衡正向移动,
即正反应是气体体积减小的反应。当压强相等时,在图3中作直线,与两条等温线交于两点,这两点自下
而上为降低温度,A的转化率增大,说明降低温度平衡正向移动,即正反应为放热反应。
3.化学平衡中的特殊图像
(1)对于化学反应:mA(g)+nB(g) pC(g)+qD(g),M点前,表示从反应开始,v(正) >v(逆);M点
为刚达到平衡点;M点后为平衡受温度的影响情况,即升温,A的百分含量增加或C的百分含量减少,平
衡左移,故ΔH<0。
(2)对于化学反应:mA(g)+nB(g) pC(g)+qD(g),L线上所有的点都是平衡点。L线的上方(E点),
A的百分含量大于此压强时平衡体系中A的百分含量,所以E点满足v(正)>v(逆);同理L线的下方(F点)满
足v(正) v ,平衡向正反应方向移动,但是因为温度不变,故平衡常数不变,A不正
正 逆
确;催化剂不影响化学平衡状态,因此,加入催化剂不影响平衡时CHCHOH(g)的浓度,B不正确;恒容
3 2
下,充入一定量的HO(g),HO(g)的浓度增大,平衡向正反应方向移动,C正确;恒容下,充入一定量的
2 2
CH=CH (g),平衡向正反应方向移动,但是CH=CH (g)的平衡转化率减小,D不正确;综上所述,本题
2 2 2 2
选C。
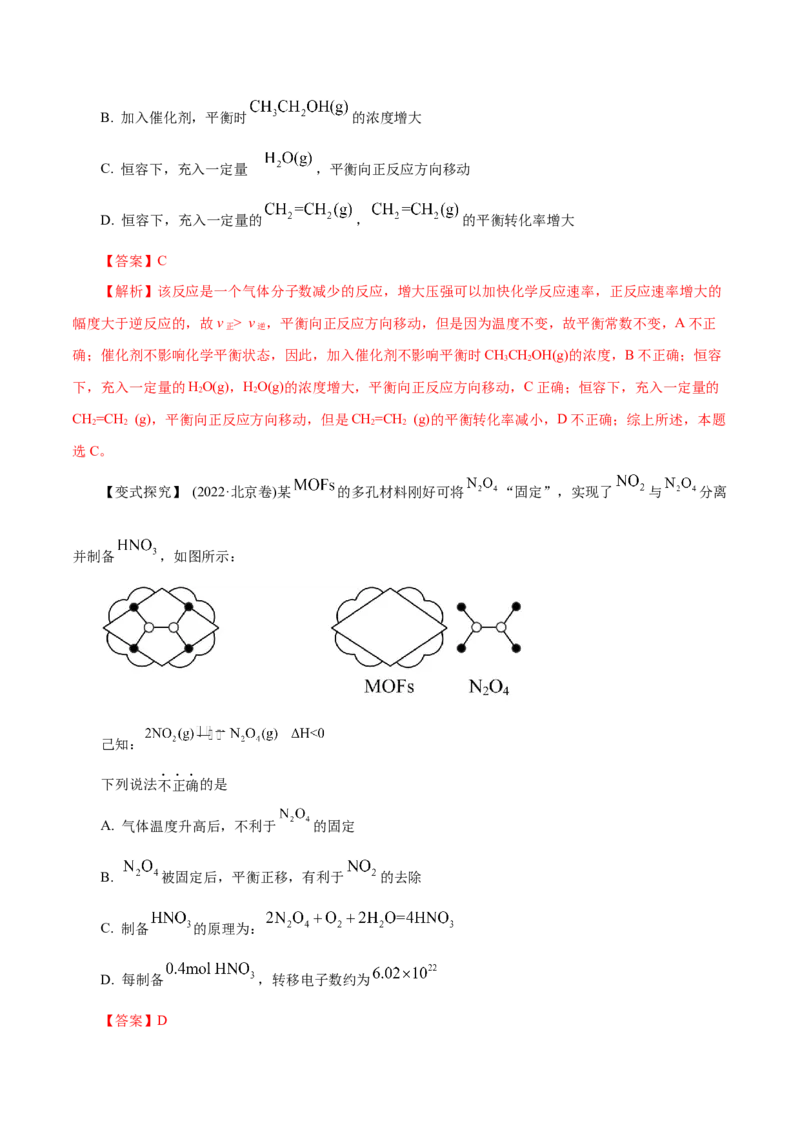
【变式探究】 (2022·北京卷)某 的多孔材料刚好可将 “固定”,实现了 与 分离
并制备 ,如图所示:
己知:
下列说法不正确的是
A. 气体温度升高后,不利于 的固定
B. 被固定后,平衡正移,有利于 的去除
C. 制备 的原理为:
D. 每制备 ,转移电子数约为
【答案】D【解析】二氧化氮转化为四氧化二氮的反应为放热反应,升高温度,平衡向逆反应方向移动,四氧化
二氮的浓度减小,所以气体温度升高后,不利于四氧化二氮的固定,故A正确;四氧化二氮被固定后,四
氧化二氮的浓度减小,二氧化氮转化为四氧化二氮的平衡向正反应方向移动,二氧化氮的浓度减小,所以
四氧化二氮被固定后,有利于二氧化氮的去除,故B正确;由题意可知,被固定后的四氧化二氮与氧气和
水反应生成硝酸,反应的化学方程式为 ,故C正确;四氧化二氮转化为硝
酸时,生成1mol硝酸,反应转移1mol电子,则每制备0.4mol硝酸,转移电子数约为
0.4mol×6.02×1023=2.408×1023,故D错误;故选D。
【变式探究】(2022·浙江卷)关于反应 ,达
到平衡后,下列说法不正确的是
A.升高温度,氯水中的 减小
B.氯水中加入少量醋酸钠固体,上述平衡正向移动, 增大
C.取氯水稀释, 增大
D.取两份氯水,分别滴加 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以证
在
明上述反应存 限度
【答案】D
【解析】HClO受热易分解,升高温度,HClO分解,平衡正向移动,c(HClO)减小,A正确;氯水中
加入少量醋酸钠固体,醋酸根离子和氢离子结合生成醋酸分子,氢离子浓度减小,平衡正向移动,
c(HClO)增大,B正确;氯水稀释,平衡正向移动,而c(HClO)和c(Cl-)均减小,但HClO本身也存在电离平
衡HClO⇌H++ClO-,稀释促进了HClO的电离,使c(HClO)减少更多,因此 增大,C正确;氯水中
加硝酸银产生白色沉淀,证明溶液中有氯离子,氯水中加淀粉碘化钾溶液,溶液变蓝,证明生成了碘单
质,溶液中有强氧化性的物质,而氯气和次氯酸都有强氧化性,不能证明反应物和生成物共存,即不能证
明上述反应存在限度,D错误;故选D。
【方法技巧】化学平衡移动题的解题流程【变式探究】温度为T℃时,向某密闭容器中分别加入足量活性炭和1 mol ,发生反应:
,并达到平衡。下列说法正确的是
A.使用催化剂,可以改变该反应的 和活化能
B.粉碎活性炭固体,正反应速率增大,平衡正向移动
C.降低压强,平衡正向移动,平衡常数K增大
D.恒压下,充入稀有气体,利于提高 的转化率
【答案】D【解析】A.使用催化剂,可降低反应的活化能,但不改变该反应的 ,故A错误;
B.粉碎活性炭固体,可增大反应物间的接触面积,从而加快反应速率,但对平衡无影响,故B错误;C.
平衡常数K为温度函数,不受压强影响,故C错误;D.恒压下,充入稀有气体,容器体积增大,平衡相
气体分子数增大的正向进行,从而利于提高二氧化氮的转化率,故D正确;故选D。
高频考点四 化学平衡移动原理在化工生产中的应用
【例4】硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发展水平的一种标志。目
前硫酸的重要生产方法是“接触法”,有关接触氧化反应2SO +O 2SO 的说法不正确的是
2 2 3
A.该反应为可逆反应,故在一定条件下二氧化硫和氧气不可能全部转化为三氧化硫
B.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为0
C.一定条件下,向某密闭容器中加入2molSO 和1molO ,则从反应开始到达平衡的过程中,正反应
2 2
速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等
D.在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题
【答案】B
【解析】A.可逆反应是在一定条件下不能进行彻底的反应,正反应和逆反应同时进行,该反应为可
逆反应,故在一定条件下SO 和O 不可能全部转化为SO ,选项A正确;B.达到平衡后,正反应速率和
2 2 3
逆反应速率相同,是动态平衡,速率不能为0,选项B错误;C.一定条件下,向某密闭容器中加入2molSO 和1molO ,则从反应开始到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时
2 2
刻,正、逆反应速率相等达到平衡,选项C正确;D.反应是放热反应,但为了反应速率需要一定温度,
催化剂活性最大,常压下,二氧化硫的转化率已经很高,改变压强对转化率影响不大,在利用上述反应生
产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题,选项D正确;答案选B。
【变式探究】有催化剂的合成塔中发生的反应为
, 。298K下合成氨反应的平衡常数K=4.1×106,下列说法错误的是
A.合成氨反应在298K时进行得比较完全
B.合成氨反应在298K时反应速率较快
C.仅从K的值无法得知该反应的平衡转化率
D.改变温度,K的值也会变化
【答案】B
【解析】A.一般K 就认为反应进行得较完全,298K下合成氨反应的平衡常数K=4.1×106 ,
因此合成氨反应在298K时进行得比较完全,A正确;
B.K较大,不能说明速率较快,B错误;
C.没有具体反应数据,仅从K的值无法得知该反应的平衡转化率,C正确;
D.K只和温度有关,改变温度,K的值也会变化 ,D正确;
故选B。
【方法技巧】化工生产适宜条件选择的一般原则
条件 原则
从化学反应速率分析 既不能过快,又不能太慢
既要注意外界条件对速率和平衡影响的一致性,又要
从化学平衡移动分析
注意二者影响的矛盾性
增加易得廉价原料,提高难得高价原料的利用率,从
从原料的利用率分析
而降低生产成本
从实际生产能力分析 如设备承受高温、高压能力等
从催化剂的使用活性分析 注意催化剂的活性对温度的限制
【变式探究】一定温度下,在某密闭容器中的 和 发生下列反应,并达到平衡状态:
。下列说法正确的是A.升高温度,
B.加入 ,平衡正向移动,平衡常数增大
C.使用合适的催化剂,可提高 的平衡转化率
D.压缩容器的容积,平衡时 的物质的量增大
【答案】D
【解析】A.该反应的正反应为放热反应,升高温度,正、逆反应速率都加快,但正反应速率加快的
倍数小于逆反应速率加快的倍数,即v <v ,平衡逆向移动,A项错误;
正 逆
B.加入CO(g),平衡正向移动,平衡常数与浓度无关,平衡常数不变,B项错误;
2
C.使用合适的催化剂,能加快反应速率,缩短达到平衡的时间,但不能使平衡发生移动,不能提高
CO 的平衡转化率,C项错误;
2
D.该反应的正反应气体体积减小,压缩容器的容积,增大压强,平衡正向移动,平衡时CHOH(g)的
3
物质的量增大,D项正确;
答案选D。
高频考点五 化学平衡移动原理的应用
【例5】(2023·北京卷第4题)下列事实能用平衡移动原理解释的是
A. H O 溶液中加入少量MnO 固体,促进HO 分解
2 2 2 2 2
B. 密闭烧瓶内的NO 和NO 的混合气体,受热后颜色加深
2 2 4
C. 铁钢放入浓HNO 中,待不再变化后,加热能产生大量红棕色气体
3
D. 锌片与稀HSO 反应过程中,加入少量CuSO 固体,促进H 的产生
2 4 4 2
【答案】B
【解析】MnO 会催化 HO 分解,与平衡移动无关,A项错误;NO 转化为NO 的反应是放热反应,
2 2 2 2 2 4
升温平衡逆向移动,NO 浓度增大,混合气体颜色加深,B项正确;铁在浓硝酸中钝化,加热会使表面的
2
氧化膜溶解,铁与浓硝酸反应生成大量红棕色气体,与平衡移动无关,C项错误;加入硫酸铜以后,锌置
换出铜,构成原电池,从而使反应速率加快,与平衡移动无关,D项错误;故选B。
【变式探究】下列有关化学平衡的说法错误的是
A.对于恒温密闭容器中进行的反应 N(g)+3H(g) 2NH (g),若 N 的体积分数保持不变,则一定
2 2 3 2
说明 反应已达到平衡状态B.一定温度下, 将 4.0g CaCO 固体置于 1L 恒容密闭容器中充分反应达到平衡后,
3
c(CO )=0.0125mol/L, 若保持温度不变,将容器体积扩大至 2L,达到新平衡后 c(CO)=0.0125mol/L
2 2
C.反应: CH(g)+HO(g) CO(g)+3H(g) ∆H>0,在其它条件不变的情况下, 升高温度、增大水蒸
4 2 2
气的浓度均能提高 CH 的平衡转化率
4
D.一定温度下, 恒容密闭容器中充入一定量 NO 发生反应:2NO NO 达到平衡后,再向容器中
2 2 2 4
充入一定量的 NO 并达到新的平衡, 则 NO 体积分数先增大后减小,但比原平衡小
2 2
【答案】D
【解析】A.平衡时,各物质的物质的量、物质的量浓度、百分含量及气体的体积分数都不变,所以
若N 的体积分数保持不变,则一定说明反应已达到平衡状态,故A正确;
2
B. 该反应的K=c(CO),温度不变,K不变,则c(CO)不变,故B正确;
2 2
C.该反应是一个反应前后气体体积增大的吸热反应,升高温度、增大水蒸气浓度都使平衡正向移
动,甲烷的转化率提高,故C正确;
D.恒温恒容条件下,达到平衡后,再向容器中充入一定量的 NO 并达到新的平衡, 则 NO 体积
2 2
分数先增大后减小,因为平衡正向移动,比原平衡大,故D错误;
答案选D。
【变式探究】下列事实不能用平衡移动原理解释的是
A.由 、 、 组成的平衡体系通过缩小体积加压后颜色变深
B.重铬酸钾溶液中存在: ,若滴加少量 溶液,溶
液由橙色变黄色
C.实验室用排饱和食盐水的方法收集
D.开启啤酒瓶后,马上泛起大量泡沫
【答案】A
【解析】A.加压平衡 不移动,但容器体积减小, 浓度增大,颜色加深,故
该事实不能用平衡移动原理解释,选项A符合题意;
B.重铬酸钾溶液中存在: ,若滴加少量 溶液,氢离子浓度减小,平衡正向移动, 减小,溶液由橙色变黄色,能用平衡移动原理解释,选项B不
符合题意;
C.饱和食盐水中氯离子浓度大,平衡 逆向移动,故氯气在饱和食盐水
中溶解度小,可用排饱和食盐水的方法收集 ,能用平衡移动原理解释,选项C不符合题意;
D.开启啤酒瓶后,马上泛起大量泡沫,原因是压强减小,碳酸分解向正反应方向移动,能用勒夏特
列原理解释,选项D不符合题意;答案选A。