文档内容
第十九讲 原子结构 化学键
【基础巩固】
1.(2022·武汉部分学校质检)下列对化学用语的描述错误的是( )
A.甲烷的结构式: B.磷原子的结构示意图:
C.U和U互为同位素 D.NaCl的电子式:
2.(2023·银川模拟)下列关于C 、H、O、N等微粒的叙述错误的是( )
60 3
A.碳、氢、氧、氮元素中各含有不同核素 B.H 与H 化学性质相同,互为同位素
3 2
C.C 与N中都含有共价键 D.KO 属于含有共价键的离子化合物
60 2
3.(2023·浙江·模拟预测)下列有关化学用语表示正确的是
A.中子数为10的氟原子:
B.Fe的原子结构示意图:
C.SO 分子的空间结构模型:
2
D.基态N原子的轨道表示式:
4.(2023·成都模拟)在宾馆、办公楼等公共场所,常使用一种电离式烟雾报警器,其主体是一个放有
镅-241(Am)放射源的电离室。Am原子核内中子数与核外电子数之差是( )
A.241 B.146 C.95 D.51
5.我国科研人员提出了由CO 和CH 转化为高附加值产品CHCOOH的催化反应历程。该历程示意图如下。
2 4 3
下列说法不正确的是( )
A.生成CHCOOH的总反应的原子利用率为100% B.CH→CHCOOH过程中,有C—H发生断裂
3 4 3
C.①→②放出能量并形成了C—C D.该催化剂可有效提高反应物的平衡转化率6.(2023·吉林·统考二模)下列化学用语表示错误的是
A.次氯酸的电子式: B.丙烷的球棍模型:
C.钠原子的原子结构示意图: D.原子核内有10个中子的氧原子:
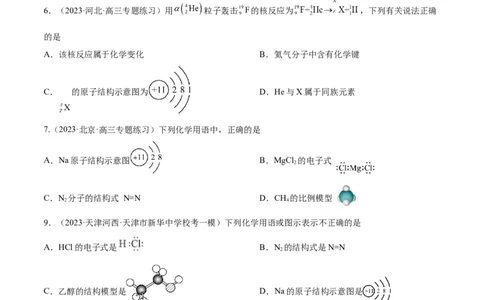
6.(2023·河北·高三专题练习)用 粒子轰击 的核反应为 ,下列有关说法正确
的是
A.该核反应属于化学变化 B.氦气分子中含有化学键
C. 的原子结构示意图为 D.He与X属于同族元素
7.(2023·北京·高三专题练习)下列化学用语中,正确的是
A.Na原子结构示意图 B.MgCl 的电子式
2
C.N 分子的结构式 N=N D.CH 的比例模型
2 4
9.(2023·天津河西·天津市新华中学校考一模)下列化学用语或图示表示不正确的是
A.HCl的电子式是 B.N 的结构式是N=N
2
C.乙醇的结构模型是 D.Na的原子结构示意图是
10.(2023·山东泰安·统考二模)下列有关化学用语正确的是
A. (碘酸碘)中碘的化合价为 、
B.用电子式表示氧化钠的形成过程:C.HF分子间的氢键:
D.砷原子结构示意图:
11.现有a~h 8种短周期元素,它们在元素周期表中的位置如图,据此回答下列问题:
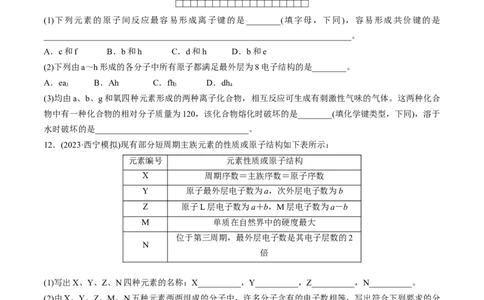
(1)下列元素的原子间反应最容易形成离子键的是________(填字母,下同),容易形成共价键的是
________________________________________________________________________。
A.c和f B.b和h C.d和h D.b和e
(2)下列由a~h形成的各分子中所有原子都满足最外层为8电子结构的是________。
A.ea B.Ah C.fh D.dh
3 3 4
(3)均由a、b、g和氧四种元素形成的两种离子化合物,相互反应可生成有刺激性气味的气体。这两种化合
物中有一种化合物的相对分子质量为120,该化合物熔化时破坏的是________(填化学键类型,下同),溶于
水时破坏的是____________________________________。
12.(2023·西宁模拟)现有部分短周期主族元素的性质或原子结构如下表所示:
元素编号 元素性质或原子结构
X 周期序数=主族序数=原子序数
Y 原子最外层电子数为a,次外层电子数为b
Z 原子L层电子数为a+b,M层电子数为a-b
M 单质在自然界中的硬度最大
位于第三周期,最外层电子数是其电子层数的2
N
倍
(1)写出X、Y、Z、N四种元素的名称:X__________,Y__________,Z__________,N__________。
(2)由X、Y、Z、M、N五种元素两两组成的分子中,许多分子含有的电子数相等,写出符合下列要求的分
子式:
①含10个电子且呈正四面体结构的分子:_________________________________________;
②含14个电子的双原子分子:___________________________________________________;
③含16个电子且能使溴水褪色的分子:___________________________________________;
④含18个电子且常温下呈液态的分子:___________________________________________。
【拔高练习】
1.“珍珠项链靠线穿,芝麻成球靠糖粘;微观粒子聚一起,全靠一种超魔力”,这种超魔力实际就是化
学键。下列关于化学键的说法错误的是( )A.CO和O 反应生成具有极性共价键的CO
2 2
B. 既含极性键,又含非极性键
C.只含H、N、O三种元素的化合物,可能形成含有共价键的离子化合物,也可能形成共价化合物
D.含有离子键的物质不可能是单质
2.(2023·西安模拟)月球上的每百吨He聚变所释放出的能量相当于目前人类一年消耗的能量,地球上氦元
素主要以He的形式存在。已知一个12C原子的质量为a g,一个He原子的质量为b g,N 为阿伏加德罗常
A
数。下列说法正确的是( )
A.He比He多一个中子 B.氦元素的近似相对原子质量为3.5
C.He的相对原子质量为 D.He的摩尔质量为bN
A
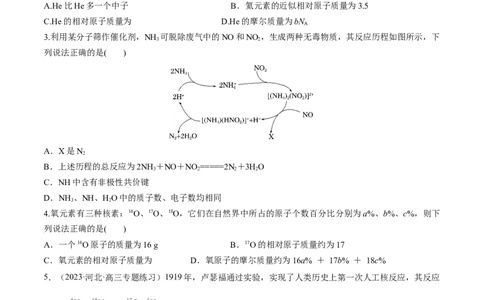
3.利用某分子筛作催化剂,NH 可脱除废气中的NO和NO ,生成两种无毒物质,其反应历程如图所示,下
3 2
列说法正确的是( )
A.X是N
2
B.上述历程的总反应为2NH +NO+NO =====2N+3HO
3 2 2 2
C.NH中含有非极性共价键
D.NH 、NH、HO中的质子数、电子数均相同
3 2
4.氧元素有三种核素:16O、17O、18O,它们在自然界中所占的原子个数百分比分别为a%、b%、c%,则下
列说法正确的是( )
A.一个16O原子的质量为16 g B.17O的相对原子质量约为17
C.氧元素的相对原子质量为 D.氧原子的摩尔质量约为16a% + 17b% + 18c%
5.(2023·河北·高三专题练习)1919年,卢瑟福通过实验,实现了人类历史上第一次人工核反应,其反应
原理为 。下列说法正确的是
A. 和 互为同位素, 和 互为同素异形体
B. 的原子结构示意图为
C. 的核外电子共有7种运动状态D.一个 原子中含有一个质子、一个中子和一个电子
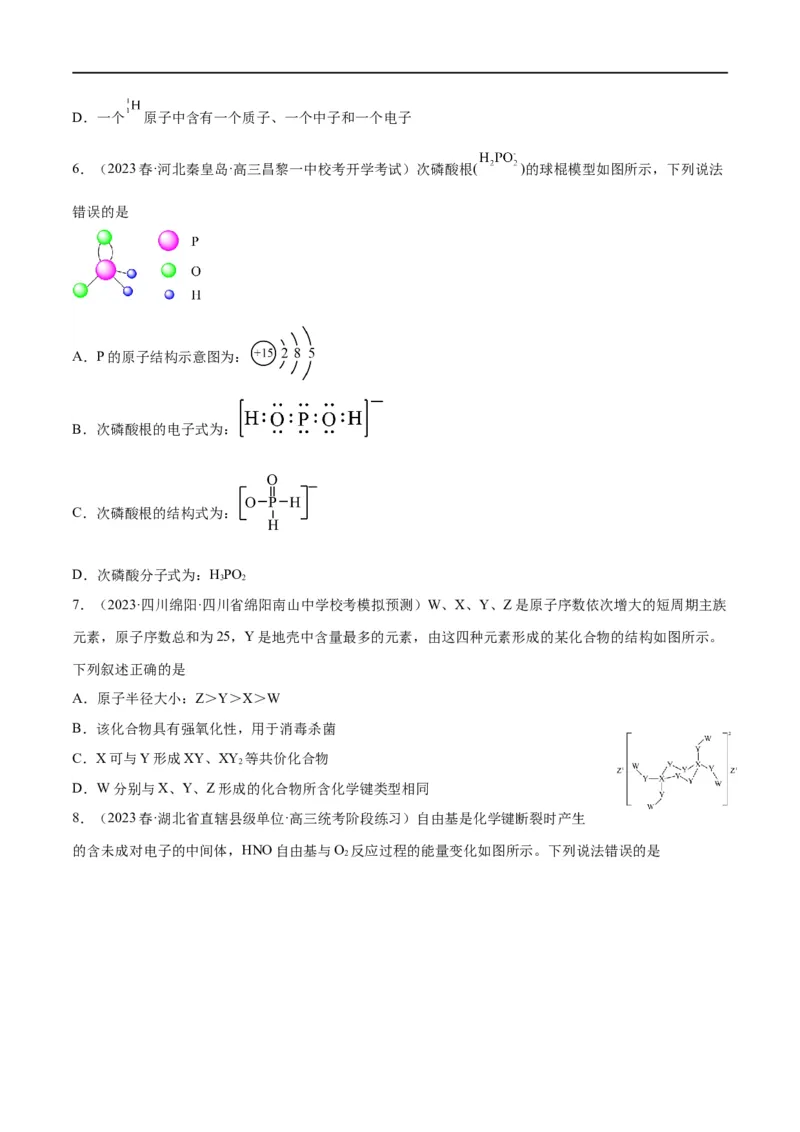
6.(2023春·河北秦皇岛·高三昌黎一中校考开学考试)次磷酸根( )的球棍模型如图所示,下列说法
错误的是
A.P的原子结构示意图为:
B.次磷酸根的电子式为:
C.次磷酸根的结构式为:
D.次磷酸分子式为:HPO
3 2
7.(2023·四川绵阳·四川省绵阳南山中学校考模拟预测)W、X、Y、Z是原子序数依次增大的短周期主族
元素,原子序数总和为25,Y是地壳中含量最多的元素,由这四种元素形成的某化合物的结构如图所示。
下列叙述正确的是
A.原子半径大小:Z>Y>X>W
B.该化合物具有强氧化性,用于消毒杀菌
C.X可与Y形成XY、XY 等共价化合物
2
D.W分别与X、Y、Z形成的化合物所含化学键类型相同
8.(2023春·湖北省直辖县级单位·高三统考阶段练习)自由基是化学键断裂时产生
的含未成对电子的中间体,HNO自由基与O 反应过程的能量变化如图所示。下列说法错误的是
2A.该历程中生成产物P 的能垒的最大值为186.19kJ•mol-1
2
B.产物P 的键能总和大于产物P 的键能总和
1 2
C.生成产物P 的反应的快慢取决于中间产物Z的生成速率
1
D.其他条件不变,适当升高温度有利于中间产物Z转化为产物P
2
9.(2023·全国·高三专题练习)2021 年 5 月 15 日,我国“天问一号”探测器成功着陆于火星,在火星
上首次留下中国人的印记。经科学家们研究发现,火星气体及岩石中含有原子序数依次增大的短周期主族
元素 X、Y、Z、W、Q,其中 X 与Q 同主族,XZ 是造成温室效应的重要气体,Y 的基态原子核外的
2
单电子数是同周期中元素最多的,W 基态原子的第一电离能比同周期的相邻原子都要小,下列说法正确的
是
A.原子半径:W>Q>Z>Y>X
B.简单氢化物的沸点:X>Y>Z
C.X 和 Q 分别与 Z 形成的二元化合物所含化学键类型和晶体类型完全相同
D.Y 与 W 形成的化合物能与 NaOH 溶液反应产生使湿润的红色石蕊试纸变蓝的气体
10.(2023秋·山西晋中·高三祁县中学校考阶段练习)光催化剂的催化原理为:催化剂在光照下产生电子
和空穴 ,催化剂表面的物种分别与电子和空穴发生还原反应和氧化反应。 光催化甲醇
分别转化为乙二醇 和甲醛 的原理如图所示,两种途径均有 产生。下
列说法不正确的是A. 和 均为反应的中间体 B. 从催化剂表面脱附需吸收能量
C.途径1中产生 的原理为 D.途径1和途径2中 断裂的化学键相同
11.A、B、C、D、E为短周期主族元素,且原子序数依次增大,质子数之和为39,B、C同周期,A、D
同主族,A、C常温下能形成两种液态化合物AC和AC ,E元素的周期数与主族序数相等。请用化学用
2 2 2
语回答下列问题:
(1)B元素在元素周期表中的位置为____________;由A、C、D三种元素组成的化合物中含有的化学键为
___________________________________________________________________。
(2)写出BC 的电子式:___________________________________________________________。
2
(3)元素E的单质与元素D的最高价氧化物对应的水化物反应的离子方程式:____________。
(4)常温下,AC与元素D的单质反应后,所得溶液的pH________(填“<”“=”或“>”)7。
2
(5)元素D的单质在一定条件下能与元素A的单质化合生成一种化合物DA,灼烧该化合物时,火焰呈
________色, DA能与水反应放出氢气,若将1 mol DA和1 mol E单质混合加入足量的水中,充分反应后
生成的气体在标准状况下的体积是________L。
12.下表是元素周期表的一部分,针对表中的①~⑨九种元素,填写下列空白:
族
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
周期
2 ① ② ③
3 ④ ⑤ ⑥ ⑦ ⑧
4 ⑨
Ⅰ.(1)在最高价氧化物对应的水化物中,酸性最强的化合物的化学式是________,碱性最强的化合物的电子
式是____________。
(2)用电子式表示元素④与⑥形成化合物的过程:__________________________________________________,
该化合物属于________(填“共价”或“离子”)化合物。
(3)表示①与⑦形成的化合物的电子式:___________________________________________。
(4)判断④⑤⑥原子半径的大小顺序:____________________________________________
(用元素符号或化学式表示,下同),比较③和⑥的气态氢化物的稳定性:_____________。
Ⅱ.A、B、C、D、F是由上表中的元素构成的五种物质,且焰色试验均为黄色,A、B、C、D与盐酸反应
均生成E,此外B还生成一种可燃气体。而C、D还生成一种无色无味气体H,该气体能使澄清石灰水变
浑浊。D和A可反应生成C,F和H也可反应生成C和另一种无色无味气体。请回答下列问题:
(1)写出A、E的化学式:A____________,E_______________________________。
(2)常温常压下制取100 mL纯净的H,将其通入装有F粉末的两通玻璃管中。
①反应的化学方程式为______________________________________________。
②若反应后收集的气体体积为65 mL,则反应消耗H的体积是________mL。