文档内容
[复习目标] 1.了解有机物中碳的成键特征、同分异构现象。2.掌握常见有机反应类型。3.了
解甲烷、乙烯、苯、乙醇、乙酸的结构和主要性质及重要应用。4.了解糖类、油脂、蛋白质
的组成和主要性质及重要应用。5.了解常见高分子材料的合成及重要应用。
考点一 有机物的结构与同分异构现象
1.某有机物的结构为 ,回答下列问题。
(1)最多有________个碳原子在同一条直线上。
(2)最多有________个碳原子在同一平面上。
(3)最多有________个原子在同一平面上。
2.回答下列问题。
(1)丁基有________种。
(2)丁醇、戊醛、戊酸分别有_______、_______、________种。
(3) 有________种。
(4)—C H、—C H 分别取代苯环上两个氢原子所得同分异构体有________种。
3 7 4 9
(5)写出CHCHCH 二氯代物的种类:_____________________________________。
3 2 3
(6)若—X、—Y、—Z分别取代苯环上的三个氢原子,所得同分异构体有________种。
近几年高考中频频涉及有机物分子的结构、碳原子的成键特征及同分异构体数目的判断,题
目难度一般较小。复习时要注意以下几点:
1.识记教材中典型有机物的分子结构特征、球棍模型、空间填充模型,会“拆分”比对结
构模板,“合成”确定共线、共面原子数目。(1)明确三类结构模板
结构 正四面体形 平面形 直线形
乙烯分子中所有原子(6个)共平
甲烷分子为正四面
面,键角为120°;苯分子中所有 乙炔分子中所有
体结构,最多有 3
模板 原子(12 个)共平面,键角为 原子(4 个)共直
个原子共平面,键
120°;甲醛分子是三角形结构, 线,键角为180°
角为109°28′
4个原子共平面,键角约为120°
(2)对照模板定共线、共面原子数目
需要结合相关的几何知识进行分析,如不共线的任意三点可确定一个平面;若一条直线与某
平面有两个交点时,则这条直线上的所有点都在该平面内;同时要注意问题中的限定性词语
(如最多、至少)。
(3)“还原”氢原子,根据规律直接判断
如果题中给出有机物的结构是键线式结构,首先“还原”氢原子,避免忽略饱和碳原子,然
后根据规律进行判断:
①结构中出现1个饱和碳原子,则分子中所有原子不可能共面;
②结构中出现1个碳碳双键,则分子中至少有6个原子共面;
③结构中出现1个碳碳三键,则分子中至少有4个原子共线;
④结构中出现1个苯环,则分子中至少有12个原子共面。
2.学会用等效氢法判断一元取代物的种类
在有机物分子中,位置等同的氢原子叫等效氢,有多少种等效氢,其一元取代物就有多少种。
等效氢的判断方法:
(1)同一个碳原子上的氢原子是等效的。
如 分子中—CH 上的3个氢原子是等效的。
3
(2)同一分子中处于轴对称位置或镜面对称位置上的氢原子是等效的。
如 分子中,在苯环所在的平面内有两条互相垂直的对称轴,故该分子有两
类等效氢。
角度一 选项中同分异构体的判断
1.正误判断,正确的打“√”,错误的打“×”
(1)戊二烯与环戊烷互为同分异构体( )(2021·全国甲卷,10D)
(2)乙烷、丙烷和丁烷都没有同分异构体( )(2017·海南,8B)
(3)淀粉和纤维素互为同分异构体( )(2017·全国卷Ⅲ,8B)
(4)乙苯的同分异构体共有3种( )(2016·海南,12B)
(5)C HCl有3种同分异构体( )(2016·全国卷Ⅰ,9C)
4 9(6)乙酸和甲酸甲酯互为同分异构体( )(2016·全国卷Ⅲ,8D)
角度二 常见物质同分异构体的判断
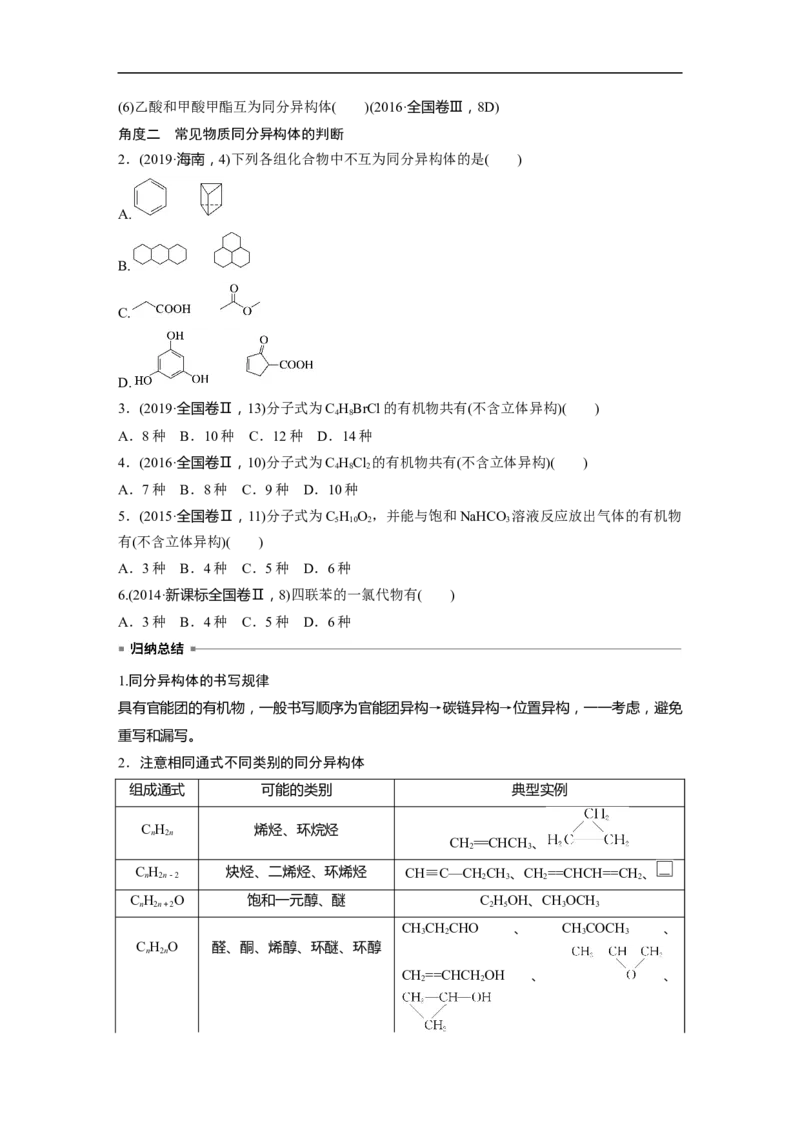
2.(2019·海南,4)下列各组化合物中不互为同分异构体的是( )
A.
B.
C.
D.
3.(2019·全国卷Ⅱ,13)分子式为C HBrCl的有机物共有(不含立体异构)( )
4 8
A.8种 B.10种 C.12种 D.14种
4.(2016·全国卷Ⅱ,10)分子式为C HCl 的有机物共有(不含立体异构)( )
4 8 2
A.7种 B.8种 C.9种 D.10种
5.(2015·全国卷Ⅱ,11)分子式为C H O ,并能与饱和NaHCO 溶液反应放出气体的有机物
5 10 2 3
有(不含立体异构)( )
A.3种 B.4种 C.5种 D.6种
6.(2014·新课标全国卷Ⅱ,8)四联苯的一氯代物有( )
A.3种 B.4种 C.5种 D.6种
1.同分异构体的书写规律
具有官能团的有机物,一般书写顺序为官能团异构→碳链异构→位置异构,一一考虑,避免
重写和漏写。
2.注意相同通式不同类别的同分异构体
组成通式 可能的类别 典型实例
C H 烯烃、环烷烃
n 2n
CH==CHCH 、
2 3
C n H 2n-2 炔烃、二烯烃、环烯烃 CH≡C—CH 2 CH 3 、CH 2 ==CHCH==CH 2 、
C H O 饱和一元醇、醚 C HOH、CHOCH
n 2n+2 2 5 3 3
CHCHCHO 、 CHCOCH 、
3 2 3 3
C H O 醛、酮、烯醇、环醚、环醇
n 2n
CH==CHCH OH 、 、
2 2CHCHCOOH、HCOOCH CH、
3 2 2 3
C H O 羧酸、酯、羟基醛、羟基酮
n 2n 2
HO-CHCH-CHO、
2 2
、 、
C H O 酚、芳香醇、芳香醚
n 2n-6
考向一 有机物的共线与共面
1.某有机物的分子结构如图: ,该分子中最多可以有
多少个原子共平面( )
A.19 B.20 C.21 D.22
2.下列关于有机物的分子结构的叙述正确的是( )
A.CH—CH==CH—C≡C—CF 分子中6个碳原子都在同一平面上
3 3
B.有机物 最多可能有11个碳原子共面
C.2-苯基丙烯( )分子中所有原子都能共面
D.CH—C≡C—CH==CH 分子中最多有4个碳原子共面
3 2
考向二 同分异构体
3.(2022·重庆市名校联盟高二下学期联考)分子式为 C H O 且分子结构中含有基团
5 10 2
的有机物(不含立体异构)共有( )
A.13种 B.14种
C.15种 D.16种
4.(2022·西安中学模拟预测)分子式为C H O ,与乳酸( )互为同系物的有机
5 10 3
物有( )
A.9种 B.10种
C.11种 D.12种
5.均三甲苯在电子工业中被用作硅酮感光片的显影剂,其结构简式如图。均三甲苯的二氯
代物(不考虑立体异构)有( )A.4种 B.5种 C.6种 D.7种
6.有机物 有多种同分异构体,其中属于酯且苯环上有2个取代基的同分
异构体共有( )
A.3种 B.4种 C.5种 D.6种
考点二 有机物的性质、反应类型及应用
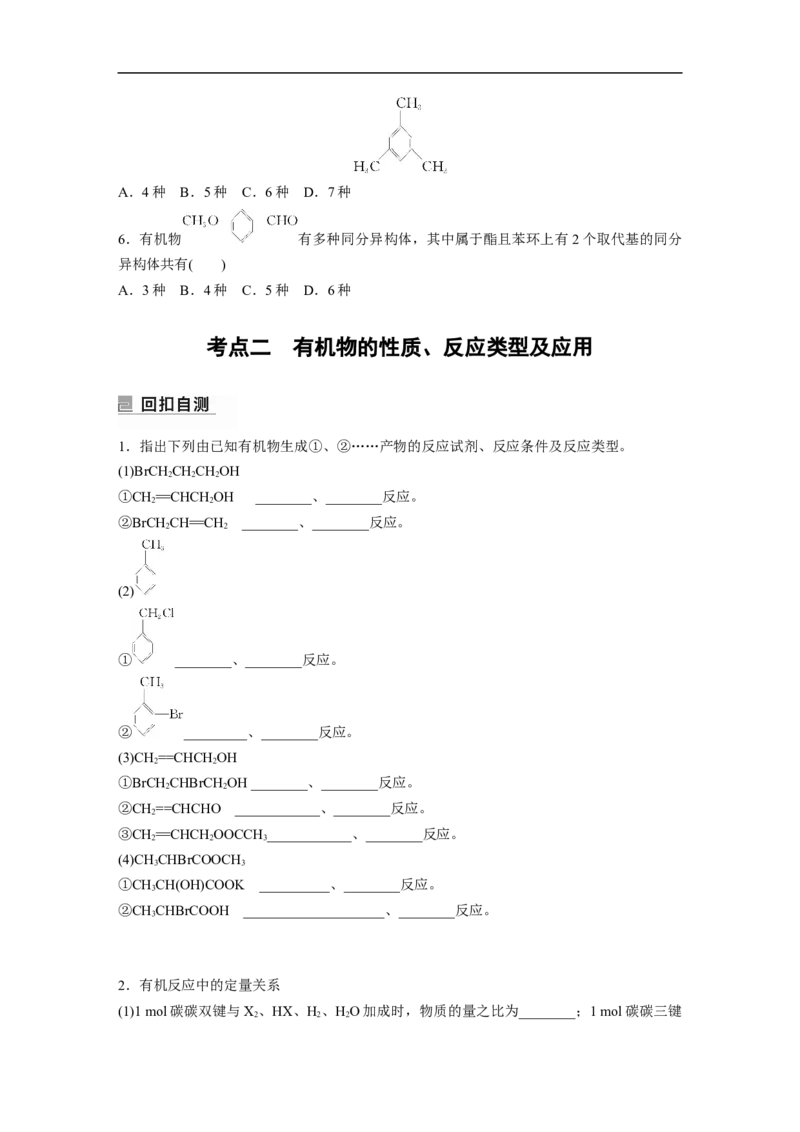
1.指出下列由已知有机物生成①、②……产物的反应试剂、反应条件及反应类型。
(1)BrCH CHCHOH
2 2 2
①CH==CHCH OH ________、________反应。
2 2
②BrCHCH==CH ________、________反应。
2 2
(2)
① ________、________反应。
② _________、________反应。
(3)CH ==CHCH OH
2 2
①BrCHCHBrCH OH ________、________反应。
2 2
②CH==CHCHO ____________、________反应。
2
③CH==CHCH OOCCH ____________、________反应。
2 2 3
(4)CH CHBrCOOCH
3 3
①CHCH(OH)COOK __________、________反应。
3
②CHCHBrCOOH ____________________、________反应。
3
2.有机反应中的定量关系
(1)1 mol碳碳双键与X 、HX、H 、HO加成时,物质的量之比为________;1 mol碳碳三键
2 2 2与X 、HX、H 发生彻底的加成反应时,物质的量之比为________;1 mol苯环与氢气完全
2 2
加成时,物质的量之比为________。
(2)醇与金属钠反应生成氢气时,2 mol —OH~________ H 。
2
(3)1 mol —COOH、—OH(酚羟基)分别与NaOH反应的物质的量之比均为________。
(4)1 mol —COO—与 NaOH 反应的物质的量之比为________;1 mol 与
NaOH反应的物质的量之比为________。
1.有机物的重要物理性质
(1)常温、常压下,分子中碳原子个数不多于4的烃是气体,烃的密度都比水小。
(2)烃、卤代烃、酯类物质均不溶于水,低级的醇、酸与水互溶。
(3)随分子中碳原子数目的增多,各类有机物的同系物熔、沸点升高,同分异构体的支链越
多,熔、沸点越低。
2.有机物的结构特点及主要化学性质
物质 结构特点 主要化学性质
甲烷 只有C—H,正四面体分子 在光照条件下与X 发生取代反应
2
可与X 、H 、HO、HX加成;能被
2 2 2
乙烯 酸性KMnO 溶液或酸性KCr O 溶液
烃 平面分子,官能团为 4 2 2 7
氧化;能发生加聚反应
在催化剂存在下:与X 、HNO 发生
2 3
苯 平面分子,碳碳键性质相同
取代反应;与H 发生加成反应
2
与活泼金属发生置换反应;被催化氧
烃的衍 乙醇 官能团为—OH
化生成醛、酸;与羧酸发生酯化反应
生物
乙酸 官能团为—COOH 具有酸的通性;能与醇发生酯化反应
3.基本营养物质的性质突破
(1)糖类性质巧突破
①葡萄糖分子含有羟基、醛基两种官能团,因此它具有醇、醛两类物质的化学性质,利用此
规律就能轻松掌握葡萄糖的化学性质。
②单糖、二糖、多糖的核心知识可用如下网络图表示出来。
+HO――→ +
C12H22O11 2 C6H12O6 C6H12O6
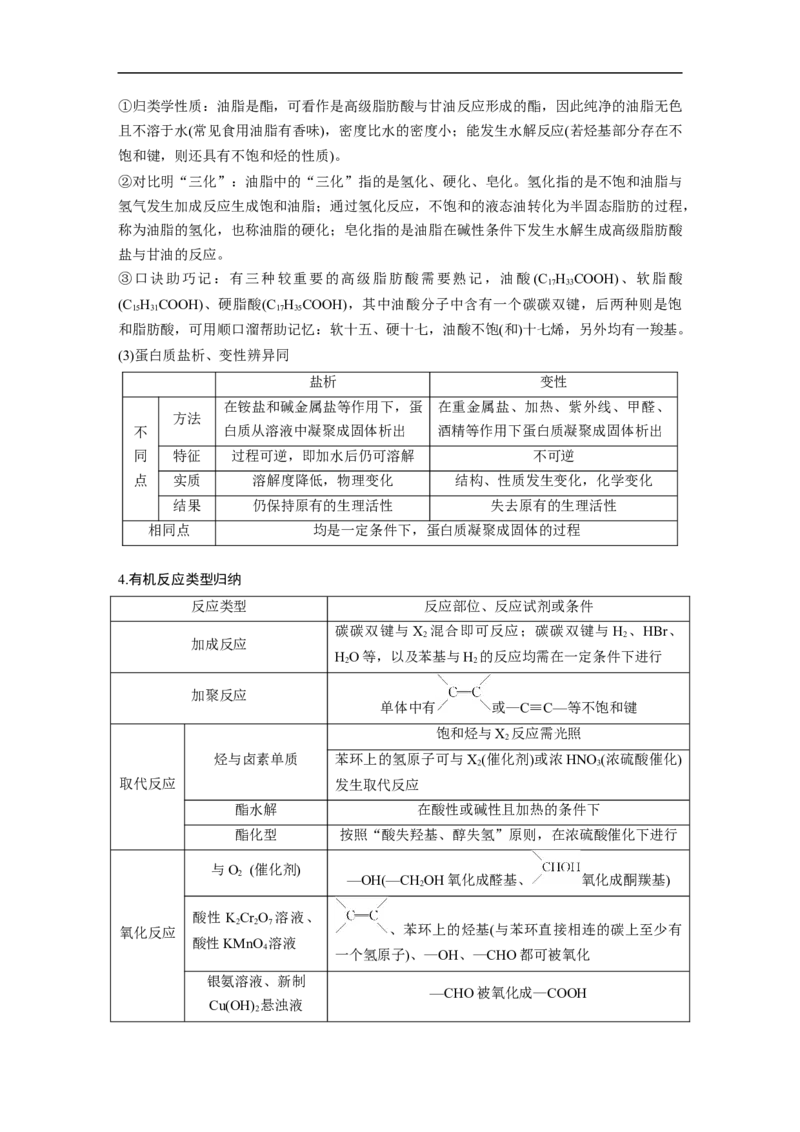
(2)油脂性质轻松学①归类学性质:油脂是酯,可看作是高级脂肪酸与甘油反应形成的酯,因此纯净的油脂无色
且不溶于水(常见食用油脂有香味),密度比水的密度小;能发生水解反应(若烃基部分存在不
饱和键,则还具有不饱和烃的性质)。
②对比明“三化”:油脂中的“三化”指的是氢化、硬化、皂化。氢化指的是不饱和油脂与
氢气发生加成反应生成饱和油脂;通过氢化反应,不饱和的液态油转化为半固态脂肪的过程,
称为油脂的氢化,也称油脂的硬化;皂化指的是油脂在碱性条件下发生水解生成高级脂肪酸
盐与甘油的反应。
③口诀助巧记:有三种较重要的高级脂肪酸需要熟记,油酸(C H COOH)、软脂酸
17 33
(C H COOH)、硬脂酸(C H COOH),其中油酸分子中含有一个碳碳双键,后两种则是饱
15 31 17 35
和脂肪酸,可用顺口溜帮助记忆:软十五、硬十七,油酸不饱(和)十七烯,另外均有一羧基。
(3)蛋白质盐析、变性辨异同
盐析 变性
在铵盐和碱金属盐等作用下,蛋 在重金属盐、加热、紫外线、甲醛、
方法
不 白质从溶液中凝聚成固体析出 酒精等作用下蛋白质凝聚成固体析出
同 特征 过程可逆,即加水后仍可溶解 不可逆
点 实质 溶解度降低,物理变化 结构、性质发生变化,化学变化
结果 仍保持原有的生理活性 失去原有的生理活性
相同点 均是一定条件下,蛋白质凝聚成固体的过程
4.有机反应类型归纳
反应类型 反应部位、反应试剂或条件
碳碳双键与X 混合即可反应;碳碳双键与H 、HBr、
2 2
加成反应
HO等,以及苯基与H 的反应均需在一定条件下进行
2 2
加聚反应
单体中有 或—C≡C—等不饱和键
饱和烃与X 反应需光照
2
烃与卤素单质 苯环上的氢原子可与X(催化剂)或浓HNO(浓硫酸催化)
2 3
取代反应 发生取代反应
酯水解 在酸性或碱性且加热的条件下
酯化型 按照“酸失羟基、醇失氢”原则,在浓硫酸催化下进行
与O (催化剂)
2 —OH(—CHOH氧化成醛基、 氧化成酮羰基)
2
酸性 KCr O 溶液、
2 2 7
氧化反应 、苯环上的烃基(与苯环直接相连的碳上至少有
酸性KMnO 溶液
4
一个氢原子)、—OH、—CHO都可被氧化
银氨溶液、新制
—CHO被氧化成—COOH
Cu(OH) 悬浊液
2燃烧型 多数有机物能燃烧,完全燃烧生成CO 和HO
2 2
烯烃、炔烃、苯及其同系物或部分芳香族化合物和H 的
2
得氢型
还原反应 加成反应
去氧型 R—NO ――→R—NH
2 2
置换反应 羟基、羧基可与活泼金属反应生成H
2
5.化学“三馏”把握准
(1)蒸馏是将液态物质加热到沸腾变为蒸气,又将蒸气冷却为液态这两个过程的联合操作。
用这一操作可分离、除杂、提纯物质。
(2)对于沸点比较接近的多种液态物质组成的混合物,用蒸馏方法难以单一蒸出分离,这就
要借助于分馏。
分馏和蒸馏一样,也是利用混合物中各物质的沸点不同,严格控制温度,进行分离或提纯的
操作。但分馏要安装一个分馏柱(工业装置为分馏塔)。混合物的蒸气进入分馏柱时,由于柱
外空气的冷却,蒸气中高沸点的组分被冷凝回流入烧瓶中,故上升的蒸气中含沸点低的组分
的相对量较多,从而达到分离、提纯的目的。
(3)干馏是把固态有机物(煤炭)放入密闭的容器中,隔绝空气加强热使之分解的过程,工业上
炼焦就属于干馏。干馏属于化学变化,蒸馏与分馏属于物理变化。
特别提醒
1.有机反应条件与反应类型的关系
(1)在NaOH的水溶液中加热发生水解反应,可能是酯的水解反应或卤代烃的水解反应。
(2)在NaOH的醇溶液中加热,发生卤代烃的消去反应。
(3)在浓HSO 和加热条件下,可能发生醇的消去反应、酯化反应或硝化反应等。
2 4
(4)与溴水或溴的CCl 溶液反应,可能发生的是烯烃、炔烃的加成反应。
4
(5)与H 在催化剂作用下发生反应,则发生的是烯烃、炔烃、芳香烃或醛的加成反应或还原
2
反应。
2.辨别材料,分析纤维
(1)棉花、羊毛、蚕丝、天然橡胶属于天然有机高分子材料,塑料、合成纤维、合成橡胶属
于合成有机高分子材料,高分子分离膜属于新型有机高分子材料。
(2)纤维分为天然纤维和化学纤维,棉、麻、丝、毛属于天然纤维,人造棉、人造丝、锦纶、
腈纶属于化学纤维,其中人造棉、人造丝又属于人造纤维,而锦纶、腈纶属于合成纤维。
3.糖类水解产物判断
若二糖或多糖是在稀硫酸作用下水解的,则先向冷却后的水解液中加入足量的 NaOH溶液,
中和稀硫酸,然后再加入银氨溶液(或新制的氢氧化铜悬浊液),水浴加热(或加热),观察现
象,作出判断。角度一 有机物结构、性质的判断
1.(2020·全国卷Ⅰ,7)国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙醚、75%乙醇、
含氯消毒剂、过氧乙酸(CHCOOOH)、氯仿等均可有效灭活病毒。对于上述化学药品,下列
3
说法错误的是( )
A.CHCHOH能与水互溶
3 2
B.NaClO通过氧化灭活病毒
C.过氧乙酸相对分子质量为76
D.氯仿的化学名称是四氯化碳
2.(2019·全国卷Ⅲ,8)下列化合物的分子中,所有原子可能共平面的是( )
A.甲苯 B.乙烷
C.丙炔 D.1,3-丁二烯
角度二 有机物官能团性质的判断
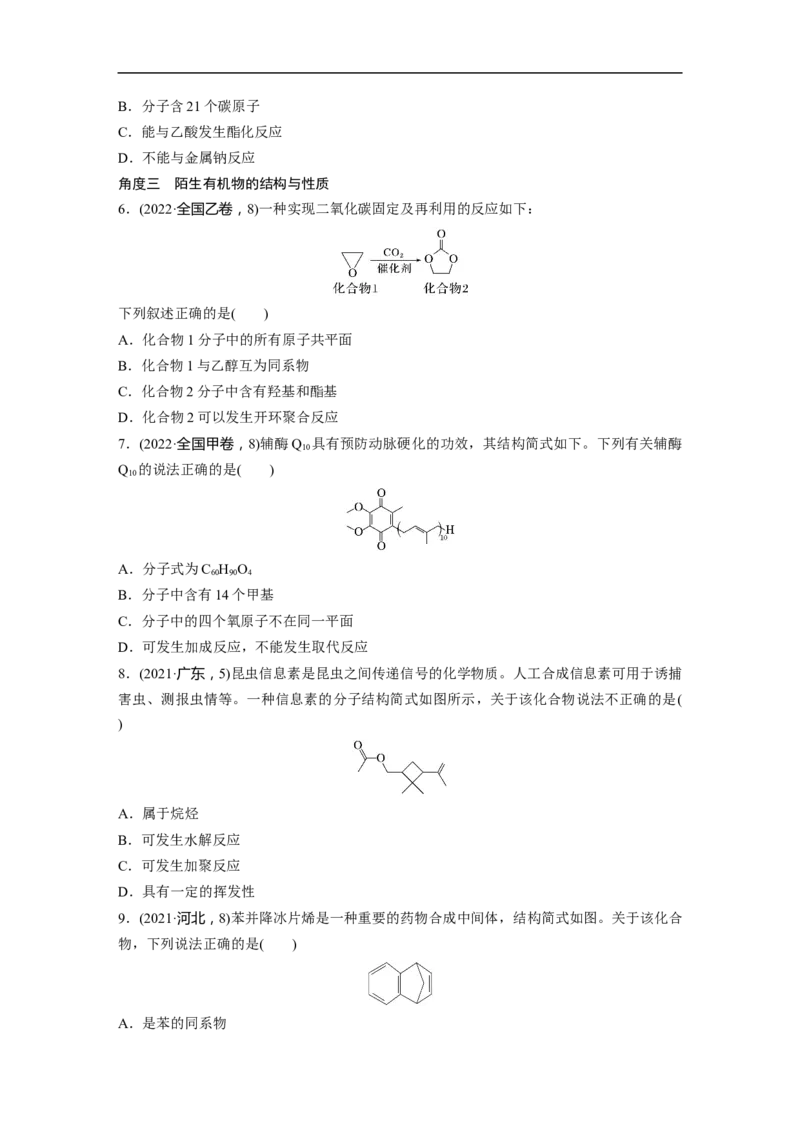
3.(2021·全国乙卷,10)一种活性物质的结构简式为 ,下列有关该
物质的叙述正确的是( )
A.能发生取代反应,不能发生加成反应
B.既是乙醇的同系物也是乙酸的同系物
C.与 互为同分异构体
D.1 mol该物质与碳酸钠反应得44 g CO
2
4.(2020·全国卷Ⅰ,8)紫花前胡醇 可从中药材当归和白芷中提取得到,
能提高人体免疫力。有关该化合物,下列叙述错误的是( )
A.分子式为C H O
14 14 4
B.不能使酸性重铬酸钾溶液变色
C.能够发生水解反应
D.能够发生消去反应生成双键
5.(2020·全国卷Ⅲ,8)金丝桃苷是从中药材中提取的一种具有抗病毒作用的黄酮类化合物,
结构简式如下:
下列关于金丝桃苷的叙述,错误的是( )
A.可与氢气发生加成反应B.分子含21个碳原子
C.能与乙酸发生酯化反应
D.不能与金属钠反应
角度三 陌生有机物的结构与性质
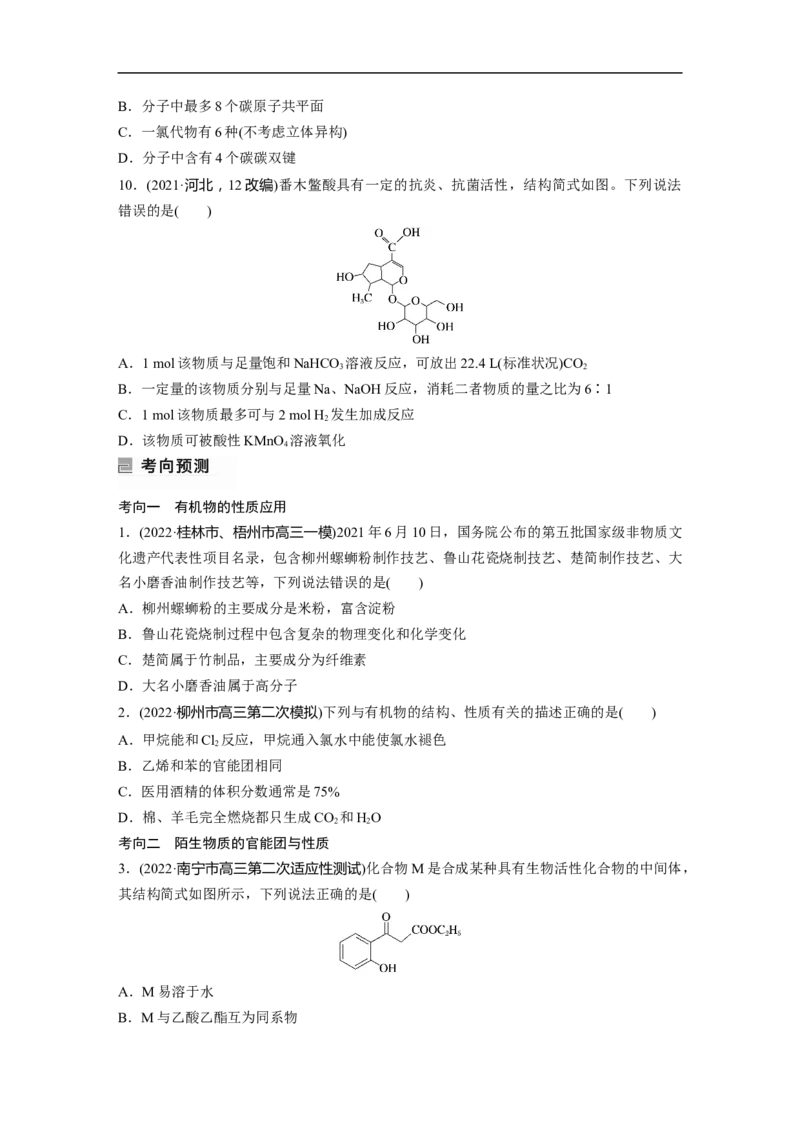
6.(2022·全国乙卷,8)一种实现二氧化碳固定及再利用的反应如下:
下列叙述正确的是( )
A.化合物1分子中的所有原子共平面
B.化合物1与乙醇互为同系物
C.化合物2分子中含有羟基和酯基
D.化合物2可以发生开环聚合反应
7.(2022·全国甲卷,8)辅酶Q 具有预防动脉硬化的功效,其结构简式如下。下列有关辅酶
10
Q 的说法正确的是( )
10
A.分子式为C H O
60 90 4
B.分子中含有14个甲基
C.分子中的四个氧原子不在同一平面
D.可发生加成反应,不能发生取代反应
8.(2021·广东,5)昆虫信息素是昆虫之间传递信号的化学物质。人工合成信息素可用于诱捕
害虫、测报虫情等。一种信息素的分子结构简式如图所示,关于该化合物说法不正确的是(
)
A.属于烷烃
B.可发生水解反应
C.可发生加聚反应
D.具有一定的挥发性
9.(2021·河北,8)苯并降冰片烯是一种重要的药物合成中间体,结构简式如图。关于该化合
物,下列说法正确的是( )
A.是苯的同系物B.分子中最多8个碳原子共平面
C.一氯代物有6种(不考虑立体异构)
D.分子中含有4个碳碳双键
10.(2021·河北,12改编)番木鳖酸具有一定的抗炎、抗菌活性,结构简式如图。下列说法
错误的是( )
A.1 mol该物质与足量饱和NaHCO 溶液反应,可放出22.4 L(标准状况)CO
3 2
B.一定量的该物质分别与足量Na、NaOH反应,消耗二者物质的量之比为6∶1
C.1 mol该物质最多可与2 mol H 发生加成反应
2
D.该物质可被酸性KMnO 溶液氧化
4
考向一 有机物的性质应用
1.(2022·桂林市、梧州市高三一模)2021年6月10日,国务院公布的第五批国家级非物质文
化遗产代表性项目名录,包含柳州螺蛳粉制作技艺、鲁山花瓷烧制技艺、楚简制作技艺、大
名小磨香油制作技艺等,下列说法错误的是( )
A.柳州螺蛳粉的主要成分是米粉,富含淀粉
B.鲁山花瓷烧制过程中包含复杂的物理变化和化学变化
C.楚简属于竹制品,主要成分为纤维素
D.大名小磨香油属于高分子
2.(2022·柳州市高三第二次模拟)下列与有机物的结构、性质有关的描述正确的是( )
A.甲烷能和Cl 反应,甲烷通入氯水中能使氯水褪色
2
B.乙烯和苯的官能团相同
C.医用酒精的体积分数通常是75%
D.棉、羊毛完全燃烧都只生成CO 和HO
2 2
考向二 陌生物质的官能团与性质
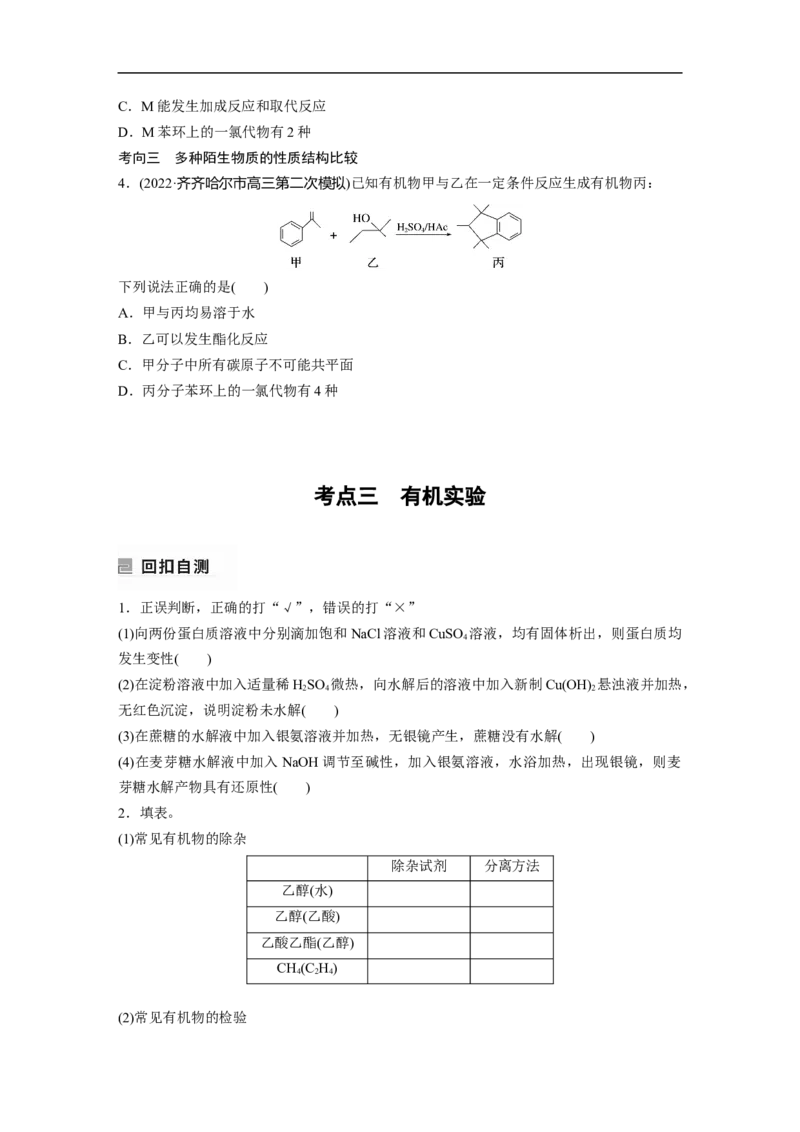
3.(2022·南宁市高三第二次适应性测试)化合物M是合成某种具有生物活性化合物的中间体,
其结构简式如图所示,下列说法正确的是( )
A.M易溶于水
B.M与乙酸乙酯互为同系物C.M能发生加成反应和取代反应
D.M苯环上的一氯代物有2种
考向三 多种陌生物质的性质结构比较
4.(2022·齐齐哈尔市高三第二次模拟)已知有机物甲与乙在一定条件反应生成有机物丙:
下列说法正确的是( )
A.甲与丙均易溶于水
B.乙可以发生酯化反应
C.甲分子中所有碳原子不可能共平面
D.丙分子苯环上的一氯代物有4种
考点三 有机实验
1.正误判断,正确的打“√”,错误的打“×”
(1)向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO 溶液,均有固体析出,则蛋白质均
4
发生变性( )
(2)在淀粉溶液中加入适量稀HSO 微热,向水解后的溶液中加入新制Cu(OH) 悬浊液并加热,
2 4 2
无红色沉淀,说明淀粉未水解( )
(3)在蔗糖的水解液中加入银氨溶液并加热,无银镜产生,蔗糖没有水解( )
(4)在麦芽糖水解液中加入NaOH调节至碱性,加入银氨溶液,水浴加热,出现银镜,则麦
芽糖水解产物具有还原性( )
2.填表。
(1)常见有机物的除杂
除杂试剂 分离方法
乙醇(水)
乙醇(乙酸)
乙酸乙酯(乙醇)
CH(C H)
4 2 4
(2)常见有机物的检验试剂、用品或方法 现象
乙醛 新制Cu(OH) 悬浊液(或银氨溶液) 有红色沉淀生成(或有银镜出现)
2
淀粉
蛋白质
3.回答下列问题。
(1)在溴苯的制备实验中,若锥形瓶中有淡黄色沉淀生成,能不能证明该反应中一定有HBr
生成?为什么?
________________________________________________________________________________
________________________________________________________________________________
(2)在硝基苯的制备实验中,水浴加热有什么优点?
________________________________________________________________________________
________________________________________________________________________________
(3)在乙醇和乙酸的酯化反应中,怎样加入试剂和碎瓷片?
________________________________________________________________________________
________________________________________________________________________________
(4)在乙醇和乙酸的酯化反应中,若乙酸中的氧为18O,在什么物质中含有18O?
________________________________________________________________________________
________________________________________________________________________________
1.常见的三个物质制备实验比较
制取物质 仪器 除杂及收集 注意事项
①催化剂为 ;
② 长 导 管 的 作 用 :
含有溴、FeBr 等,用
3
;
溴苯 ______溶液处理后分
③右侧导管 (填“能”或
液,然后
“不能”)伸入溶液中;
④右侧锥形瓶中有
可能含有未反应完的 ①导管1的作用: ;
、 、 ,用 ②仪器2为 ;
硝基苯 溶液中和酸,分液, ③用 控制温度为 50~60
然后用 的方法除 ℃;
去苯 ④浓硫酸的作用: 和
含有乙酸、乙醇,先
①浓硫酸的作用: 和
乙酸乙酯 用 __________ 处 理 ;
后,再______ ② 的作用:溶解乙醇、中和乙酸、降低乙酸乙酯的
;
③右边导管 (填“能”或“不
能”)伸入溶液中
2.有机物鉴别和分离提纯的方法
(1)常见有机物鉴别的方法
①物理法
如用水或溴水鉴别乙醇、苯和CCl 。
4
②化学法
如用新制的Cu(OH) 检验醛基;用碘水检验淀粉;用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯;
2
用点燃法、溴水或酸性KMnO 溶液鉴别甲烷和乙烯。
4
(2)常见有机物分离提纯的方法
①洗气法
如通过盛有溴水的洗气瓶除去气态烷烃中混有的气态烯烃。
②分液法
如用饱和碳酸钠溶液除去乙酸乙酯中的乙酸和乙醇。
③蒸馏法
如乙酸和乙醇的分离,加CaO,蒸出乙醇,再加稀硫酸,蒸出乙酸。
1.(2021·山东,7)某同学进行蔗糖水解实验,并检验产物中的醛基,操作如下:向试管Ⅰ中
加入1 mL 20%蔗糖溶液,加入3滴稀硫酸,水浴加热5分钟。打开盛有10% NaOH溶液的
试剂瓶,将玻璃瓶塞倒放,取1 mL溶液加入试管Ⅱ,盖紧瓶塞;向试管Ⅱ中加入5滴2%
CuSO 溶液。将试管Ⅱ中反应液加入试管Ⅰ,用酒精灯加热试管Ⅰ并观察现象。实验中存在
4
的错误有几处( )
A.1 B.2 C.3 D.4
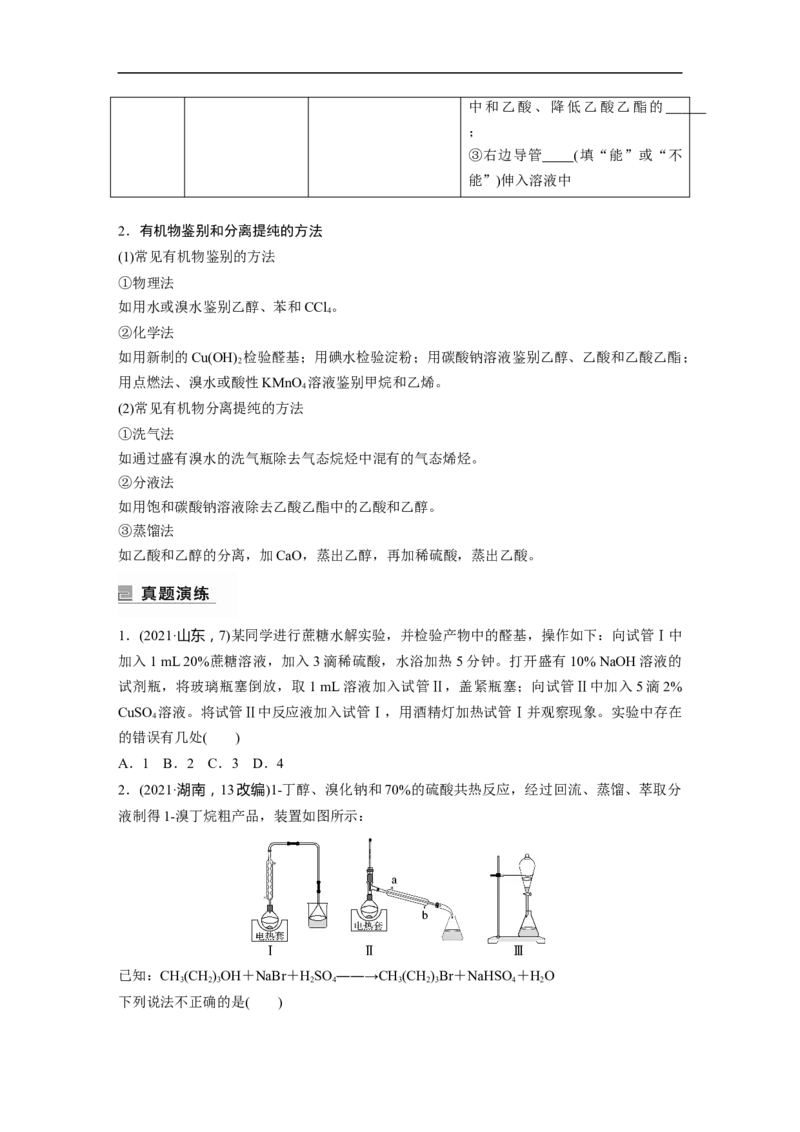
2.(2021·湖南,13改编)1-丁醇、溴化钠和70%的硫酸共热反应,经过回流、蒸馏、萃取分
液制得1-溴丁烷粗产品,装置如图所示:
已知:CH(CH)OH+NaBr+HSO ――→CH(CH)Br+NaHSO+HO
3 2 3 2 4 3 2 3 4 2
下列说法不正确的是( )A.装置Ⅰ中回流的目的是为了减少物质的挥发,提高产率
B.装置Ⅱ中b为进水口,a为出水口
C.用装置Ⅲ萃取分液时,将分层的液体依次从下口放出
D.经装置Ⅲ得到的粗产品干燥后,使用装置Ⅱ再次蒸馏,可得到更纯的产品
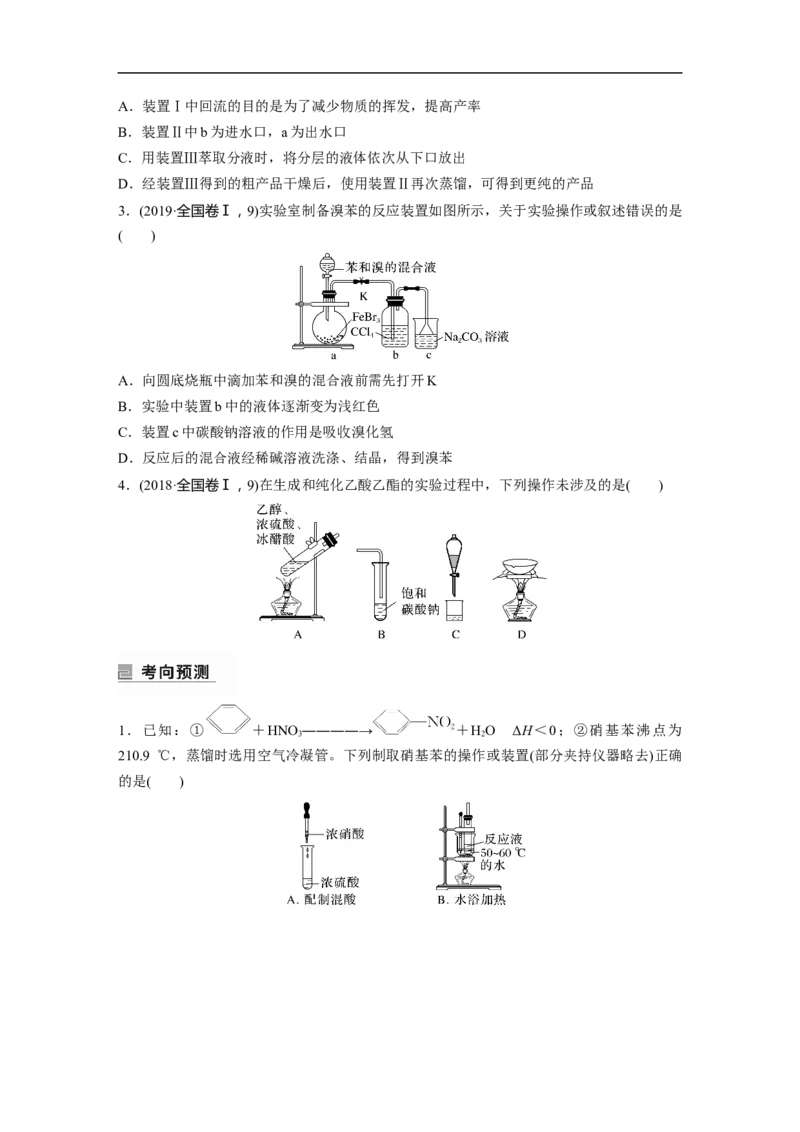
3.(2019·全国卷Ⅰ,9)实验室制备溴苯的反应装置如图所示,关于实验操作或叙述错误的是
( )
A.向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B.实验中装置b中的液体逐渐变为浅红色
C.装置c中碳酸钠溶液的作用是吸收溴化氢
D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
4.(2018·全国卷Ⅰ,9)在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是( )
1.已知:① +HNO――――→ +HO ΔH<0;②硝基苯沸点为
3 2
210.9 ℃,蒸馏时选用空气冷凝管。下列制取硝基苯的操作或装置(部分夹持仪器略去)正确
的是( )2.实验室常用氯气和苯在氯化铁为催化剂的条件下制备氯苯,其装置如图所示(省略夹持装
置)。
下列说法错误的是( )
A.装置e中盛放的是浓硫酸,是为了干燥氯气
B.本实验可以用浓盐酸和二氧化锰来制备氯气
C.反应结束后需通入一段时间空气,再拆解装置
D.反应后的混合液分别用水、碱溶液、水依次洗涤,干燥,蒸馏,可得到氯苯
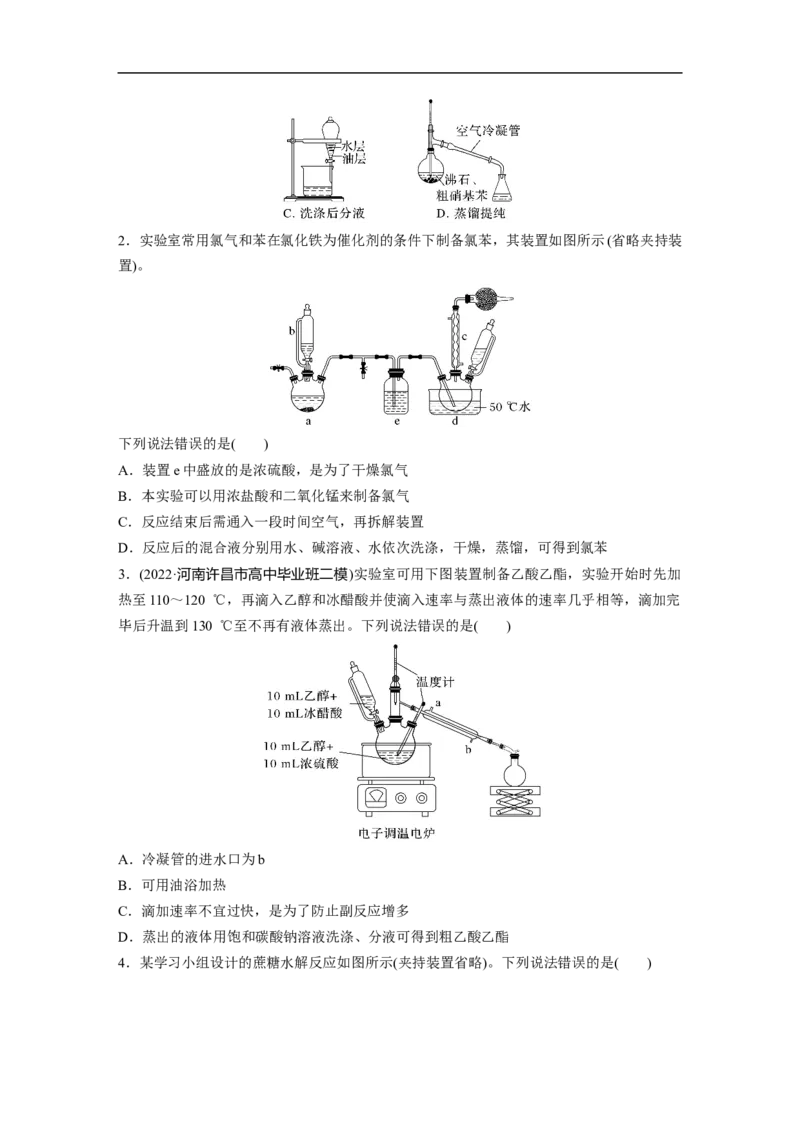
3.(2022·河南许昌市高中毕业班二模)实验室可用下图装置制备乙酸乙酯,实验开始时先加
热至110~120 ℃,再滴入乙醇和冰醋酸并使滴入速率与蒸出液体的速率几乎相等,滴加完
毕后升温到130 ℃至不再有液体蒸出。下列说法错误的是( )
A.冷凝管的进水口为b
B.可用油浴加热
C.滴加速率不宜过快,是为了防止副反应增多
D.蒸出的液体用饱和碳酸钠溶液洗涤、分液可得到粗乙酸乙酯
4.某学习小组设计的蔗糖水解反应如图所示(夹持装置省略)。下列说法错误的是( )A.稀硫酸和热水浴都能加快蔗糖水解速率
B.滴加NaOH溶液的目的是调节溶液的pH至碱性
C.加热至沸腾后试管内生成黑色沉淀
D.实验现象证明蔗糖水解有还原性物质生成