文档内容
第 20 讲 化学平衡常数及转化率的计算
1.下列反应的焓变和熵变与图示过程相符的是
A.2Na(g)+Cl(g)=2NaCl(s)
2
B.N
2
(g)+3H
2
(g)⇌2NH
3
(g)
C.2N
2
O
5
(g)⇌4NO
2
(g)+O
2
(g)
D.Zn(s)+HSO (aq)=ZnSO (aq)+H(g)
2 4 4 2
【答案】C
【解析】打开可乐瓶时,产生大量气泡,在由溶液到逸出气体过程中,溶解是放热,则逸出是吸热,则
ΔH>0,气体增多,则ΔS>0。
A.2Na(g)+Cl(g)=2NaCl(s),该反应是化合反应,ΔH<0,气体减少,ΔS<0,A不符合题意;
2
B.N
2
(g)+3H
2
(g) ⇌2NH
3
(g),该反应是化合反应,ΔH<0,气体减少,ΔS<0,B不符合题意;
C.2N 2 O 5 (g) ⇌ 4NO 2 (g)+O 2 (g),该反应是分解反应,ΔH>0,气体增多,ΔS>0,C符合题意;
D.Zn(s)+HSO (aq)=ZnSO(aq)+H(g),该反应是放热反应,ΔH<0,气体增多,ΔS>0,D不符合题
2 4 4 2
意;
故选C。
2.已知“凡气体分子总数增加的反应都是熵增大的反应”。下列反应在任何温度下都不自发进行的是
A.2O(g)=3O(g) ΔH<0
3 2
B.2CO(g)=2C(s)+O(g) ΔH>0
2
C.N(g)+3H(g)=2NH (g) ΔH<0
2 2 3
D.CaCO (s)=CaO(s)+CO(g) ΔH>0
3 2
【答案】B
【解析】A.该反应ΔH<0,ΔS>0,任何温度下都能自发进行,A不符合题意;
B.该反应ΔH>0,ΔS<0,任何温度都不能自发进行,B符合题意;
C.该反应ΔH<0,ΔS<0,低温条件下能自发进行,C不符合题意;
D.该反应ΔH>0,ΔS>0,高温条件下能自发进行,D不符合题意;
故选B。3.对于反应SO
2
(g)+Cl
2
(g)⇌SO
2
Cl
2
(g) ΔH=akJ⋅mol-1(a<0),下列说法正确的是
A.该反应在任意条件下均能自发进行
B.反应SO
2
(g)+Cl
2
(g)⇌SO
2
Cl
2
(l)的焓变ΔH0,△S<0
B.由公式△G=△H-T△S可知,该反应△G=985.29kJ/mol
C.金刚石比石墨稳定
D.相同条件下,1mol金刚石与1mol氧气的能量总和小于1molCO 气体的能量
2
【答案】A
【解析】A.在相同条件下,等物质的量的C(石墨)和C(金刚石)燃烧分别放出热量为393.51、395.40,说
明C(金刚石)具有更多能量,所以C(石墨)→C(金刚石)为吸热反应,△H>0;△S= S(金刚石)- S(石墨)=-3.3
J/(K·mol)<0,故A正确;
B.△G=△H-T△S=1.89 kJ/mol-298K×(-3.3 J/(K·mol))=2.8734kJ/mol,故B错误;
C.C(金刚石)具有更多能量,能量越高物质越不稳定,所以石墨更稳定,故C错误;
D.金刚石燃烧与氧气反应生成二氧化碳和水,为放热反应,说明反应物总能量大于生成物总能量,故D错误;故选A。
5.下列几个过程中,属于熵减的变化是
A.干冰的升华 B.NaCl溶于水
C.NH (g)+HCl(g) = NH Cl(s) D.2Na+2HO(l) = 2NaOH+H ↑
3 4 2 2
【答案】C
【解析】A.固态干冰变成气态二氧化碳,混乱程度增大,熵增加,A不符合题意;
B.NaCl溶于水,晶体电离成自由移动的阴阳离子,混乱程度增大,熵增加,B不符合题意;
C.NH (g)+HCl(g) = NH Cl(s),气体分子数减小,混乱程度减小,熵减小,C符合题意;
3 4
D.钠与水反应生成氢气,气体分子数增加,混乱程度增大,熵增加,D不符合题意。 故选C。
6.工业合成氨的反应为:N(g)+3H(g) 2NH (g)在298 K时,ΔH=-92.4 kJ·mol-1,ΔS=-198.2 J·mol
2 2 3
-1·K-1,特定条件下的速率可表示为v=kc(N )c1.5(H )c-1(NH ),其中k为反应速率常数,下列叙述正确的
2 2 3
是
A.该反应在298 K时不能正向自发进行
B.升高温度、增大压强有利于化学平衡向生成氨的方向移动
C.反应体系的三种物质中,H(g)的浓度对反应速率影响最大
2
D.反应达到一定转化率时将NH 从混合气中分离出去会降低反应速率
3
【答案】C
【解析】A.由题给数据可知,反应ΔH-TΔS=(—92.2kJ/mol)—298K×(—0.1982kJ/(K·mol) ≈—33.14kJ/mol<
0,所以反应能自发进行,,故A错误;
B.该反应为气体体积减小的反应,增大压强平衡正向移动,但该反应为放热反应,升高温度,平衡向逆
反应方向移动,故B错误;
C.由速率公式可知,反应速率与氮气和氢气的浓度成正比关系,与氨气的浓度成反比关系,所以幂指数
最大的氢气浓度对反应速率影响最大,故C正确;
D.由速率公式可知,反应速率与氨气的浓度成反比关系,所以反应达到一定转化率时将氨气从混合气中
分离出去会增大反应速率,故D错误;故选C。
7.在容积不变的密闭容器中发生反应:CO(g)+HO(g ) CO(g)+H(g) ΔH<0,830℃时反应的平衡常
2 2 2
数是1.0,下列说法正确的是
A.容器内的压强不变时,说明反应达到平衡状态
B.若平衡时移走CO,化学反应速率加快
2
C.830℃时,充入0.1molCO和0.3molHO保持温度不变,CO平衡转化率为75%
2
D.1000℃时,K<1,某时刻CO、H、CO和HO的浓度均为0.05mol•L-1,此时平衡向正反应方向移动
2 2 2【答案】C
【解析】A.一定温度下容积不变时,体系压强与物质的量成正比。该反应气体分子总数始终不变、故压
强也始终不变,则当体系压强不随时间变化时不能说明反应达到平衡状态,A错误;
B.若平衡时移走CO,则减少了产物浓度,化学反应速率减小,B错误;
2
C. , ,得
x=0.075mol,则CO平衡转化率为75%,C正确;
D.1000℃时,K<1。某时刻CO、H、CO和HO的浓度均为0.05mol·L-1,Q= =1>K,则
2 2 2 c
此时平衡向逆反应方向移动,D错误;故选C。
8.向一定温度下的2L密闭容器中通入 发生反应: 。 的物质的
量 随时间(t)变化的曲线如图所示(图中的X、Y两条线代表有、无催化剂),下列叙述正确的是
A.Y线表示无催化剂
B.c点时的
C.X线上a点时 的转化率为75%
D.X线前 内的平均反应速率可表示为
【答案】B
【解析】A.该图像表示的是 的物质的量 随时间(t)变化的曲线,曲线Y先达到拐点,说明反
应先达到化学平衡,速率较快,有催化剂催化,故A错误;B.c点 不再变化,说明该反应达到平衡状态,此时 ,故B正确;
C.到达a点时, 的物质的量转化量为0.1mol,则转化率 ,故C
错误;
D.X线前 内的平均反应速率可表示为 ,则
,故D错误;答案选B。
9.氨是一种重要的化工原料,可用于制备硝酸等工业。工业合成氮反应:
。实验室用加热 和 固体混合物的
方法制取少量氨气。下列有关合成氨反应的说法正确的是
A.反应的 (E表示键能)
B.反应每消耗 放出的热量为
C.使用催化剂可提高达平衡状态时 的转化率
D.将 与 置于密闭容器中充分反应,可生成
【答案】A
【解析】A.反应的ΔH=反应物的键能总和-生成物的键总和= ,故
A正确;
B.由题干信息可知,每消耗3mol H,即6g H 放出92.4 kJ的热量,由消耗 放出的热量为
2 2
,故B错误;
C.催化剂对化学平衡无影响,故使用催化剂不能提高达平衡状态时 的转化率,故C错误;
D.该反应为可逆反应,反应物不可能完全反应,将 与 置于密闭容器中充分反应,生成的物质的量小于2mol,故D错误;故选A。
10.一定条件下,密闭容器中发生反应,反应过程中各物质的物质的量的变化如图所示。下列说法不正确
的是
A.15 min时,反应处于化学平衡状态
B.15~20 min,正逆反应速率相等
C.达到平衡时,X的转化率为20%
D.反应的化学方程式为X +Y Z
【答案】D
【解析】A.由图可知,15min时,各物质的物质的量保持不变,处于化学平衡状态,故A正确;
B.反应达到平衡状态时,同一物质的正逆反应速率相等,15~20min时该反应达到平衡状态,则15~
20min时正逆反应速率相等,故B正确;
C.达到平衡时,X减少0.20mol-0.16mol=0.04mol,X的转化率 ×100%=20%,故C正确;
D.开始至平衡时,X减少0.20mol-0.16mol=0.04mol,Y减少0.10mol-0.08mol=0.02mol,Z增加
0.04mol-0=0.04mol,物质的量的变化量之比等于化学计量数之比,则反应的化学方程式为2X+Y⇌2Z,故
D错误;故选D。
11.把2.5molA和2.5molB混合,装入容积为2L的密闭容器里,发生如下反应:3A(g)+B(g)⇌xC(g)
+2D(g),经5s反应达平衡,在此5s内C的平均反应速率为0.2mol·L-1·s-1,同时生成1molD,下列叙述错误
的是
A.x=4
B.达到平衡时容器内气体的压强与起始时的压强比为6:5
C.达到平衡时B的转化率为50%
D.通过控制反应条件可以改变该可逆反应的限度【答案】C
【分析】根据5s内C的平均反应速率为0.2mol·L-1·s-1可知,反应后C的物质的量为
0.2mol/(L·s)×5s×2L=2mol,生成1molD,根据方程式系数之比等于变化量之比可得
x:2=2:1,解得x=4,根据题意可得:
【解析】A.根据分析可知,x=4,A正确;
B.根据阿伏伽德罗定律,其它条件相同时,压强之比等于物质的量之比,反应达到平衡状态时,相同条
件下容器内气体的压强与起始时压强比为(1+2+2+1):(2.5+2.5)=6:5,B正确;
C.反应达到平衡状态时B的转化率为 ×100%=20%,C错误;
D.化学反应限度受外界条件影响,D正确;
故选C。
12.合成氨实现了人工固氮,提高了粮食产量。工业合成氨的反应原理为 ,下列
说法不正确的是
A.可通过改变反应条件使 全部转化 B.升高温度能加快反应速率
C.反应达到限度时 的转化率最高 D.可通过控制反应条件提高 的产量
【答案】A
【解析】A.该反应是可逆反应,氮气不可能完全转化,A错误;
B.升高温度,活化分子百分数增大,反应速率加快,B正确;
C.反应达到限度时也即达到了平衡,此时 的转化率最高,C正确;
D.可通过改变温度或压强让平衡正向移动,从而提高氨气的产量,D正确;
故选A。
13.在密闭容器中发生反应 ,若反应达到平衡后,保持温度不变,将气
体压缩到原来的 体积,再次达到平衡时,Z的浓度是原平衡的1.8倍,下列叙述中正确的是
A.平衡向逆反应方向移动 B.C.X的转化率增大 D.W的体积分数增大
【答案】A
【解析】A.若平衡不移动,Z的浓度为原来的2倍而现在Z的浓度时原平衡的1.8倍,说明平衡逆向移
动,A正确;
B.压缩体积,相当于增大压强,平衡逆向移动,说明逆反应向着体积减小的方向进行,则 ,B
错误;
C.平衡逆向移动,反应物的转化率降低,C错误;
D.平衡逆向移动,W的体积分数减小,D错误; 故选A。
14.一定温度下,向容积为 的恒容密闭容器中加入等物质的量的 和 ,发生反应
。测得不同反应时间容器内 的物质的量如表;
时间(min) 0 10 20 30 40
1 0.75 0.65 0.6 0.6
下列说法正确的是
A.反应达到化学平衡状态时, 的转化率为0.6
B. 内HI的平均反应速率为
C.容器内压强不再改变,说明反应已达到平衡
D. 后,再充入 ,正反应速率增大,逆反应速率减小
【答案】B
【解析】A.起始氢气和碘等物质的量都是1mol,平衡时氢气剩余0.6mol,反应了0.4mol,碘也反应了
0.4mol,转化率为0.4,故A错误;
B.0到20min,氢气反应了0.35mol,氢气的反应速率为 ,HI系数是H 的2
2
倍,速率也是H 的2倍,HI的速率是 ,故B正确;
2
C.该反应是前后系数相等的反应,压强始终不变,压强不再改变,不能说明达到平衡状态,故C错误;
D.增大反应物浓度,正逆反应速率均增大,逆反应速率也随之增大,故D错误;
答案选B。15.工业上利用硫(S)与 为原料制备 ,在500℃以上发生反应:
。在2L密闭容器中充入1mol 和4mol ,发生上述反应,测得平衡体系中硫
蒸气的体积分数和温度的关系如表所示:
温度/℃ 560 580 600 620 640 660
0.286 0.333 0.378 0.420 0.462 0.500
下列说法错误的是
A.在580℃达到平衡时, 的转化率为70%
B.该反应660℃的平衡常数
C.上述反应的正反应为吸热反应
D.起始充入1mol 和2mol ,620℃平衡时
【答案】C
【解析】A.根据反应列三段式:
,解得 ,则 ,A项正确;
B.660℃时, ,解得 ,平衡时 , ,
, , 、 、 、
,故 ,B项正确;
C.由表中数据可知,随着温度的升高硫蒸气的体积分数升高,说明温度升高,反应平衡逆向移动,则正
反应为放热反应,C项错误;D.在恒温恒容条件下,在2L容器中充入1mol 和2mol 等效于充入1mol 和4mol S,D项正
确。
答案为:、C。
16.在一定温度下,在密闭容器中投入X(g)和Y(g),发生反应生成Z(g)。测得各物质浓度与时间关系如图
所示(提示:净反应速率等于正、逆反应速率之差)。下列说法错误的是
A.a点:正反应速率小于逆反应速率
B.b点:净反应速率等于零
C.上述可逆反应中X、Y、Z的化学计量数之比为3∶1∶2
D.该可逆反应在该反应条件下达到最大限度时,Y的平衡转化率为40%
【答案】A
【解析】A.a点未达到平衡,正反应速率大于逆反应速率,A项错误;
B.b点达到平衡,正,逆反应速率相等,净反应速率等于0,B项正确;
C.根据速率之比等于化学计量数之比知,X,Y,Z的化学计量数之比为0.6:0.2:0.4=3:1:2,C项正
确;
D.达到平衡时Y消耗0.2mol/L,Y的转化率为40%,D项正确;
答案选A。
17. 和 反应生成的碳基硫(COS)用于粮食熏蒸,能防止某些昆虫、线虫和真菌的危害。
,下列说法错误的是
A.已知该反应在加热条件下能自发进行,则其
B.上述反应的平衡常数
C.上述反应中消耗 ,生成标准状况下D.实际应用中,通过增加 的量来提高 转化率,能有效减少碳排放
【答案】D
【解析】A.已知该反应在加热条件下能自发进行,所以ΔG=ΔH−TΔS<0 ,因为△H > 0,所以△S > 0,A
正确;
B.由反应方程式,结合平衡常数含义可知,上述反应的平衡常数 ,B正确;
C.由反应方程式,每消耗 时,生成1molCOS,标况下体积为22.4L,C正确;
D.减少碳排放是指减少二氧化碳的生成,D错误;故选D。
18.在3个体积均为2.0L的恒容密闭容器中,反应 ,分别在一定
温度下达到化学平衡状态。下列说法不正确的是
起始时物质的量 平衡时物质的量
容
温度/K
器
Ⅰ 977 0.28 0.56 0 0.4
Ⅱ 977 0.56 0.56 0 x
Ⅲ 1250 0 0 0.56 y
A.977K,该反应的化学平衡常数值为1
B.达到平衡时,向容器Ⅰ中增加C的量,平衡不移动
C.达到平衡时,容器Ⅱ中 的转化率比容器Ⅰ中的小
D.达到平衡时,容器Ⅲ中的CO的转化率大于28.6%
【答案】D
【分析】容器Ⅰ中,起始投入CO 的物质的量为0.28mol、C为0.56mol,平衡时生成CO的物质的量为
2
0.4mol,则可建立如下三段式:977K,该反应的化学平衡常数值为 =1;
【解析】A.由分析可知,977K,该反应的化学平衡常数值为1,A正确;
B.达到平衡时,向容器Ⅰ中增加C的量,反应物和生成物的浓度都不发生改变,则平衡不移动,B正
确;
C.容器Ⅱ 与容器Ⅰ相比,容器Ⅱ相当于容器Ⅰ加压,使气体物质的浓度变为原来的二倍,则平衡逆向移
动,CO 的转化率减小,所以容器Ⅱ 中CO 的转化率比容器Ⅰ中的小,C正确;
2 2
D.容器Ⅲ 中,若温度为977K,则与容器Ⅰ中平衡等效,达到平衡时,容器Ⅰ中CO 的转化率为
2
≈71.4%,则CO的转化率为28.6%,现升高容器Ⅲ 的温度至1250K,平衡正向移动,CO的转化率减小,
则容器Ⅲ中CO的转化率小于28.6%,D不正确;故选D。
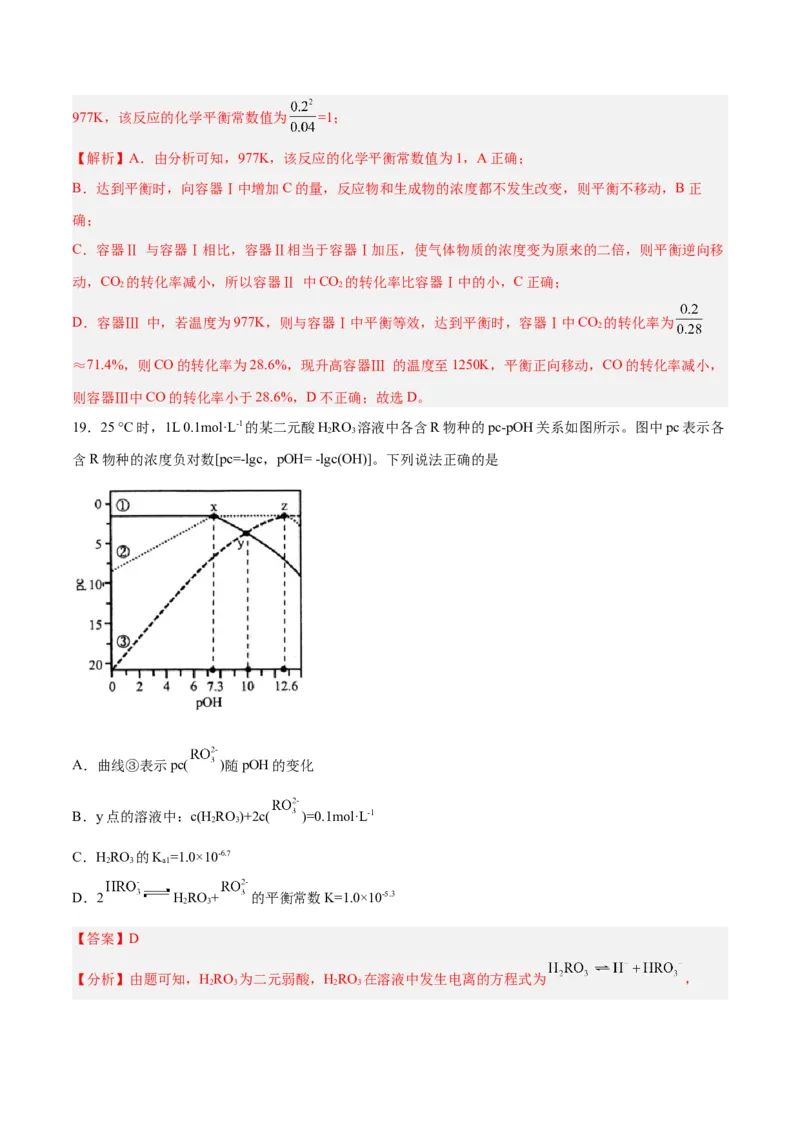
19.25 °C时,1L 0.1mol·L-1的某二元酸HRO 溶液中各含R物种的pc-pOH关系如图所示。图中pc表示各
2 3
含R物种的浓度负对数[pc=-lgc,pOH= -lgc(OH)]。下列说法正确的是
A.曲线③表示pc( )随pOH的变化
B.y点的溶液中:c(HRO)+2c( )=0.1mol·L-1
2 3
C.HRO 的K =1.0×10-6.7
2 3 a1
D.2 HRO+ 的平衡常数K=1.0×10-5.3
2 3
【答案】D
【分析】由题可知,HRO 为二元弱酸,HRO 在溶液中发生电离的方程式为 ,
2 3 2 3,pOH=-lgc(OH-),pc=-lgc,则pOH值越大,溶液的碱性越弱,pc值越大,粒子的浓
度越小,pOH=0时,溶液的碱性最强,此时对于HRO 溶液,各粒子浓度关系为
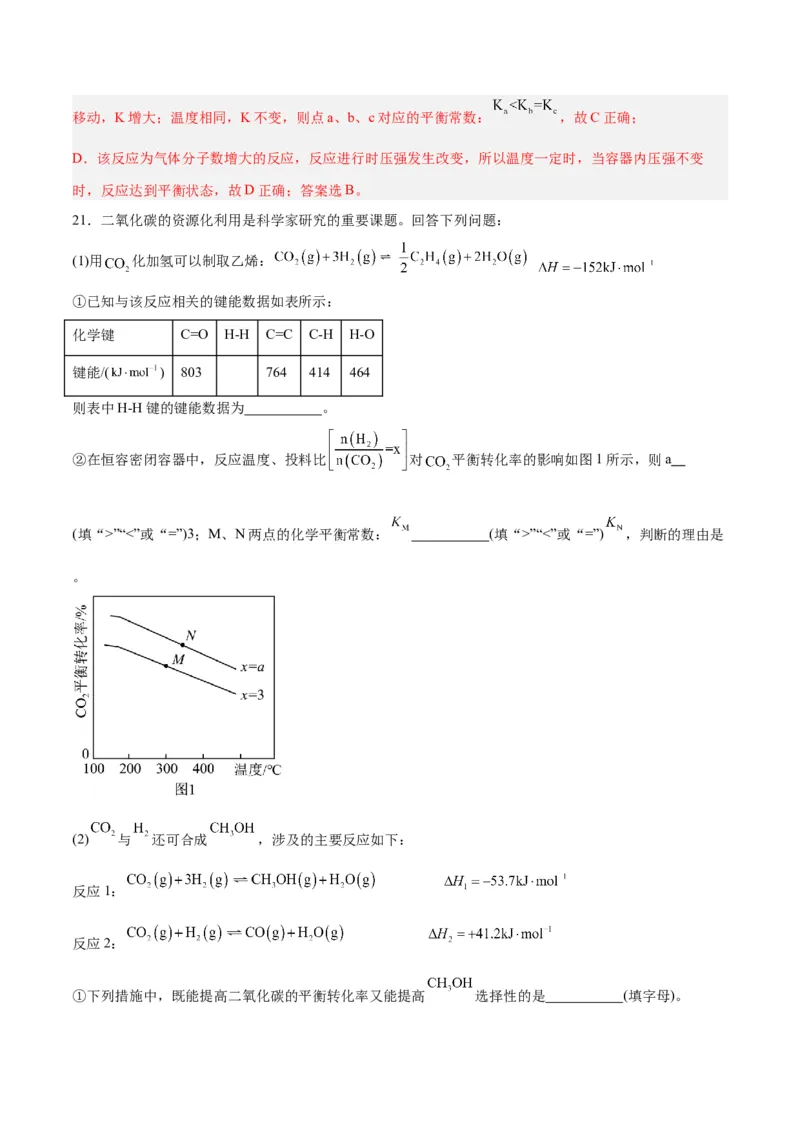
2 3
c(HRO)”“<”或“=”)3;M、N两点的化学平衡常数: (填“>”“<”或“=”) ,判断的理由是
。
(2) 与 还可合成 ,涉及的主要反应如下:
反应1:
反应2:
①下列措施中,既能提高二氧化碳的平衡转化率又能提高 选择性的是 (填字母)。A.加压 B.降温 C.及时移走甲醇
D.使用合适的催化剂
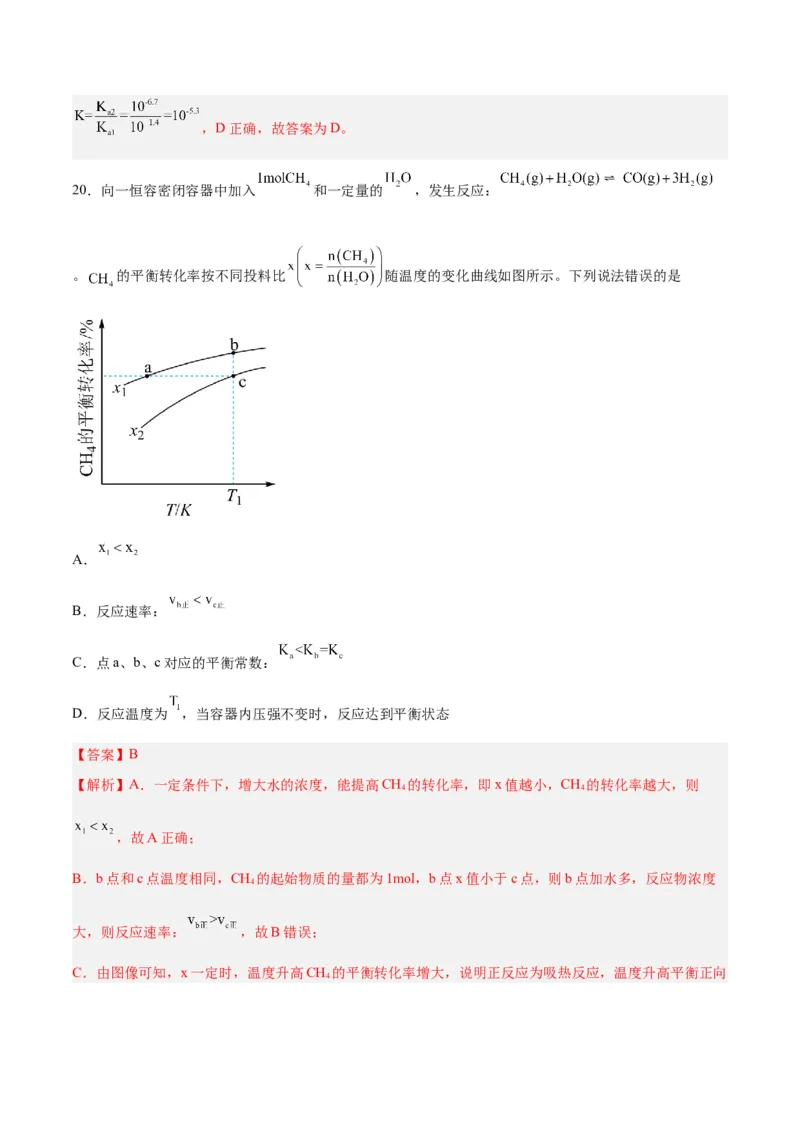
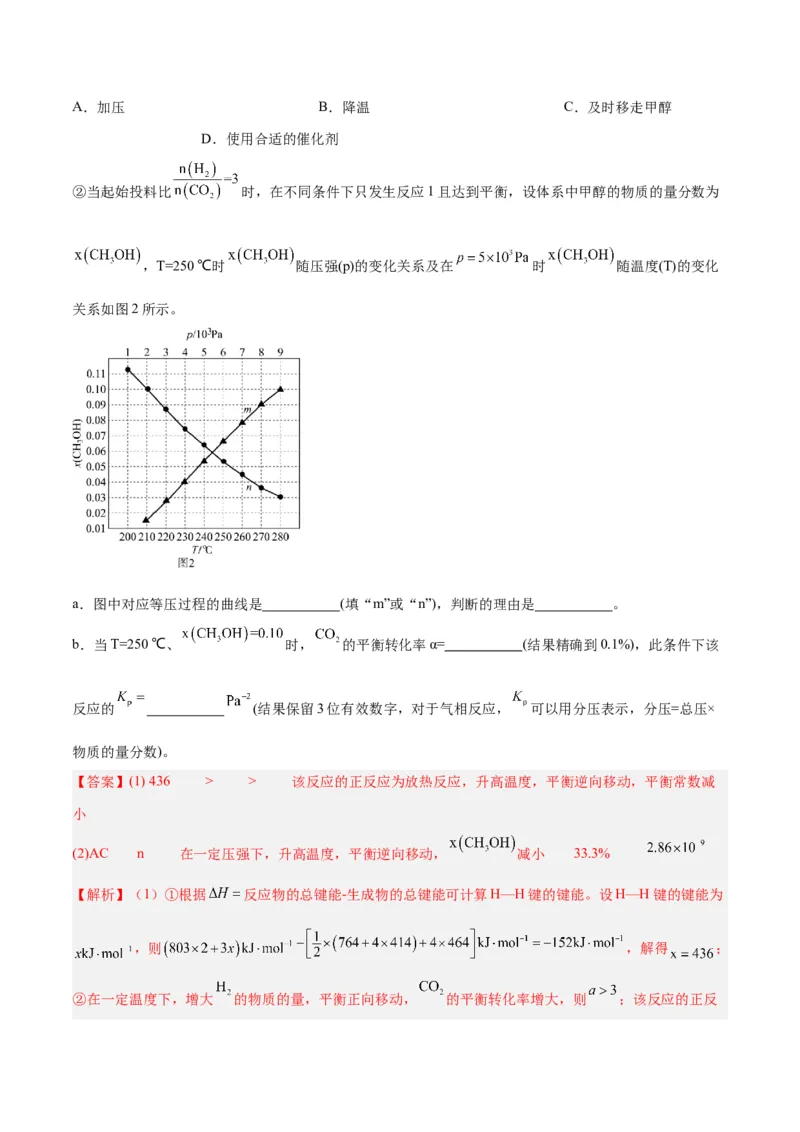
②当起始投料比 时,在不同条件下只发生反应1且达到平衡,设体系中甲醇的物质的量分数为
,T=250 ℃时 随压强(p)的变化关系及在 时 随温度(T)的变化
关系如图2所示。
a.图中对应等压过程的曲线是 (填“m”或“n”),判断的理由是 。
b.当T=250 ℃、 时, 的平衡转化率α= (结果精确到0.1%),此条件下该
反应的 (结果保留3位有效数字,对于气相反应, 可以用分压表示,分压=总压×
物质的量分数)。
【答案】(1) 436 > > 该反应的正反应为放热反应,升高温度,平衡逆向移动,平衡常数减
小
(2)AC n 在一定压强下,升高温度,平衡逆向移动, 减小 33.3%
【解析】(1)①根据 反应物的总键能-生成物的总键能可计算H—H键的键能。设H—H键的键能为
,则 ,解得 ;
②在一定温度下,增大 的物质的量,平衡正向移动, 的平衡转化率增大,则 ;该反应的正反应为放热反应,升高温度,平衡逆向移动,平衡常数减小,温度越高,平衡常数越小,M点的温度比N点
的低,所以M、N两点的化学平衡常数 。
(2)①加压时反应2平衡不移动,反应1向右移动,故该措施既能提高二氧化碳的平衡转化率又能提高
的选择性,选A;
降温时反应1向右移动,反应2向左移动,故甲醇的选择性提高,但二氧化碳的平衡转化率不一定提高,
故不选B;
及时移走甲醇,反应1向右移动,反应2不移动,该措施既能提高二氧化碳的平衡转化率又能提高
的选择性,故选C;
使用合适的催化剂,可以提高甲醇的选择性,但不能提高二氧化碳的平衡转化率,故不选D;
选A、C;
②a.反应1是 的反应,在一定压强下,升高温度,平衡逆向移动, 减小,故题图中对应
等压过程的曲线是n。
b.当 、 时,设起始时 的物质的量为1 mol,则 的物质的量为3 mol,平
衡时消耗 的物质的量为x mol,列“三段式”:
则 ,解得 , 的平衡转化率 。平衡时 、 、
、 的物质的量分数分别为0.20、0.60、0.10、0.10;根据题图可知平衡时压强
,则该反应的平衡常数。
22.碳热还原法是一种在一定温度下以无机碳为还原剂进行氧化还原反应的方法,在冶金行业有着广泛的
应用。回答下列问题:
(1)氧化铝碳热还原过程发生了如下反应:
反应初始温度
反应初始温度
反应初始温度
① (用含 的代数式表示)。
②根据以上信息分析,在相同系统压力下, 时, 与C反应优先生成的含铝化合物为
(填化学式)。
(2)科学家在氧化铝碳热还原法研究中加入无水氯化铝作氯化剂,一定条件下,氧化铝先转化为 和
, 和 再转化为低价氯化铝 ,低价氯化铝进入低温区歧化得到铝。忽略中间产物,
写出由氧化铝直接获得 的化学方程式: 。
(3)三氯化铝固体在一定温度与压强下升华,可能生成三氯化铝气体[ 反应ⅰ],也可能
生成六氯化二铝气体[ 反应ⅱ],实验结果如图所示:①在 , 条件下,氯化铝升华得到 (填 或 )。
②气态氯化铝是具有配位键的化合物,分子中原子间成键关系如图所示,请将图中你认为是配位键的斜线
上加上箭头 。
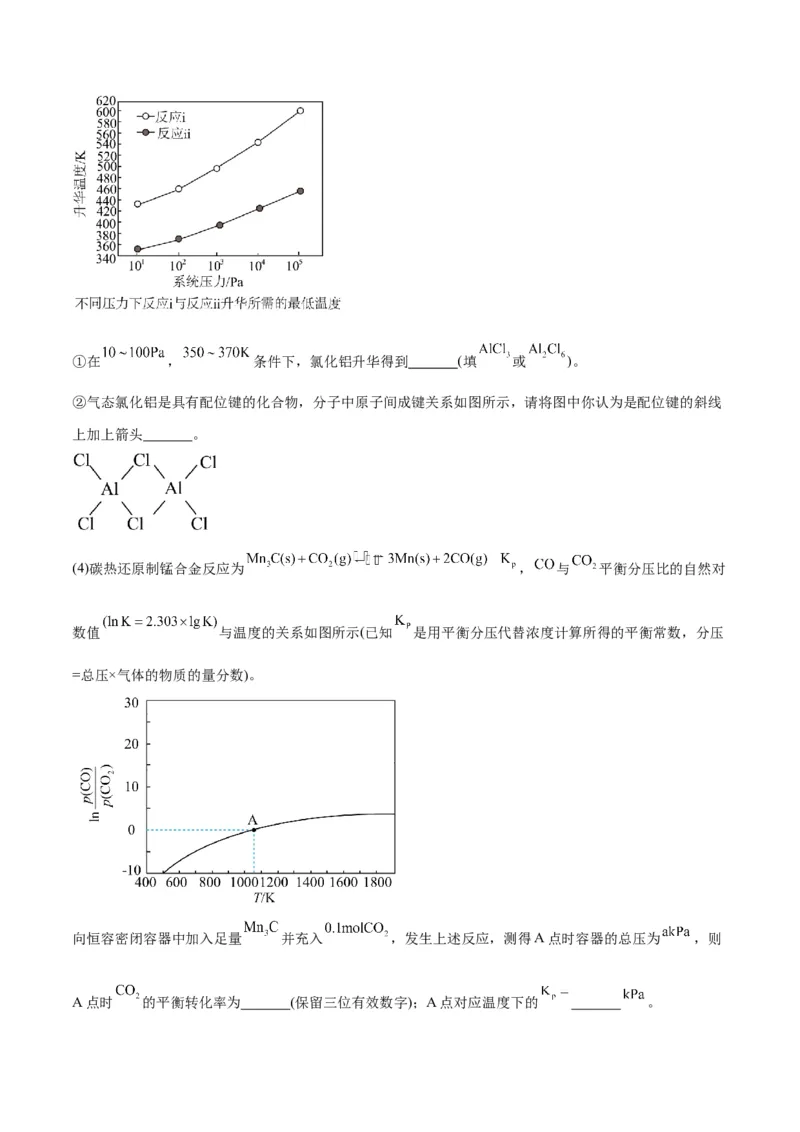
(4)碳热还原制锰合金反应为 , 与 平衡分压比的自然对
数值 与温度的关系如图所示(已知 是用平衡分压代替浓度计算所得的平衡常数,分压
=总压×气体的物质的量分数)。
向恒容密闭容器中加入足量 并充入 ,发生上述反应,测得A点时容器的总压为 ,则
A点时 的平衡转化率为 (保留三位有效数字);A点对应温度下的 。【答案】(1)
(2)
(3)
(4)33.3% 0.5a
【解析】(1)根据盖斯定律可知反应③=反应①-反应②,则 ;由题中信息可知 时,
未到达反应①的初始温度,但高于反应②的初始温度,则先发生反应②生成 ;
(2)由氧化铝直接获得 的化学方程式: ;
(3) 的摩尔质量大于 ,则 熔沸点高于 ,其生化温度高于 ; 中Al提高
空轨道,Cl提供孤对电子形成配位键, 的结构可表示为: ;
(4)结合题中信息列三段式:
A点ln =0,则 =1,说明 ,即平衡时,0.1-x=2x,x= mol, 的平衡转
化率为 ;平衡时n(总)= mol,则A点对应温度下K= =0.5akPa。
p